Доброкачественная миоклоническая эпилепсия младенчества у кого было
Добрый день, просьба помочь разобраться в ситуации. Очень хотелось бы получить комментарий доктора Василий Юрьевича (drwn). Краткая история:
У нас мальчик - 4,5 мес. (род. 10.07.15).
Роды были обычными - плановое кесарево, по апгар 8 из 8. Беременность проходила нормально, за исключением временного повышения АСТ и АЛТ в середине беременности и с 7-8 месяца был зуд беременных (при этом была повышена только щелочная фосфатаза). При рождении образовалась небольшая субэпендимальная киста 4 мм в левой каудо-таламической вырезке (сказали это нормально у кесарят). Прививку делали только БЦЖ в роддоме. Малыш стал развиваться хорошо.
Месяц назад (где то в 3-3,5 мес.) заметили что сын плохо спит ночью - может по часу спать, просыпаться, потом опять засыпать (до этого спал и по 2-3 часа). Было ощущение, что ему что то мешает. Думали на колики.
18.11.15 начали делать ему общеукрепляющий массаж (до этого делали месяц назад - все ок) - не по показаниям, а просто ради доп. пользы. Возможно дальнейшее было спровоцировано массажем.
21-22 ноября 15 года вечером заметили, что сын непроизвольно в состоянии покоя стал делать движения, как в рефлексе Моро (см. видео). Дико перепугались. До этого рефлекс был только при испуге (и то нам его показывал невропатолог), а тут он сам по себе и несколько раз (в сериеи 1-10 приступов, по 5-7 серий в день). Массаж отменили (7 курсов из 10 сделали).
25.11.15 Посетили невролога, которая сделала повторное узи (киста уменьшилась до 3,5 мм), обследовала ребенка (заболеваний нервной системы нет, психомоторное развитие соответствует возрасту) и направила к неврологу-эпелептологу и на ЭЭГ. Сказала, что малыш хорошо развит.
25.11.15 Сделали ЭЭГ (правда малышу было постоянно неудобно, он капризничал после того как ему надели шапочку, даже потом остались сильные раздражения где были контакты, потом сказали, что хорошие детские шапочки для ЭЭГ были на сервисном обслуживании в тот день) - результат: "В ЭЭГ выявляются выраженные диффузные общемозговые изменения биоэлектрической активности в виде дизритмии, признаков раздражения стволовых структур, политопной эпилептиформной активности, сопровождающейся клиническими проявлениями.". Малыш несколько раз проявил судороги при ЭЭГ, но не всегда они отображались одновременно с разрядом. Доктор написал: "Изредка сразу за разрядом клинически отмечаются движения в виде вдрагивания, разведения рук".
26.11.15 Пошли к неврологу-эпелиптологу (сказали, что лучший в городе - к.м.н) - результат: по ЭЭГ она не видит эпи-активности, нужно пересдать (через 3 нед.). Мы честно говоря пропылесосив весь интернет подумали на синдром Веста, но врач сказала, что должна быть гипсаритмия, которой у нас по ЭЭГ нет. Так же должны быть инфантильные спазмы (которые якобы невозможно ни с чем перепутать и от них нельзя отвлечь/переключить ребенка во время приступа). У нас же малыш проявил спазмы при ней и она сказала, что это точно не они (и вообще это не имеет отношения к эпилепсии). Так же сказала, что у нас чудный малыш и он отлично развит по возрасту. На наш вопрос, что до проявления спазмов бывает, что младенцы развиваются нормально, она сказала, что такое практически невозможно и были бы по нему уже заметны проявления повреждений. Поставила диагноз "Доброкачественный миоклонус младенчества, психомоторное развитие соответствует возрасту." И что ничего нам принимать не нужно, но может быть только витамин Б-6.
На следующий день (27.11.15) вызвали на дом невролога, которая работает с ДЦП-шными детками: она нас несколько раз предупредила, что ее квалификация не имеет отношения к эпилепсиям, но она может определить при осмотре какая часть мозга может быть поражена/раздражена. Далее после 3-х признаков она сказала, что видит раздражение ствола и возможно это спазм сосудов/артерий ствола мозга. Признаки такие: 1) у нас есть пятно аиста/родимое на затылке (а оно появляется либо при стоячем положении плода при беременности, либо при травме-растяжении если плод лежал нормально вниз головой как в нашем случае); 2) с 2,5-3-х месяцев у нас хорошее такое слюноотделение, хотя сейчас поуменьшилось (что так же возникает из за раздражения ствола, хотя нам все говорили, что это нормально и часто бывает - зубы, не умеет глотать, так работают слюнные железы, скоро будут зубы и т.п.) и 3) заметила тонус пронаторов предплечий (больше на одной руке, вторая чуть чуть). Сказала, что можно попить Стугерон (снять спазмы задних мозговых артерий), но на последнем УЗИ первый врач "схалявила" (хотим его повторить) и не описала скорость кровотока в них на первом было 0,68, что не совсем нормально (норма 61). Но в целом сказала, что ребенок развит хорошо.
Хотим попросить местных врачей и специалистов оценить наше состояние по результатам в прикрепленных документах. Стоит ли нам волноваться? Какие действия еще предпринять, что бы не опоздать с лечением (если оно нужно). Судороги у нас вызывают сильную озабоченность (постоянно переживаем). Эпелиптолог сказала, что они могут спадать до 2-х лет - мы честно говоря не представляем как это будет влиять на качество жизни нашего малыша. Хотим их купировать (врач говорит, что принятие препаратов повлияет на развитие). Специалист по ДЦП сказала, что видела 2 раза такие случаи и что они прошли к году. Мы конечно будем следить за развитием малыша, но что можно еще предпринять кроме повторного ЭЭГ и посещения другого хорошего эпелиптолога? есть смысл пить Стугерон или он может навредить? Всем заранее спасибо за ответы.
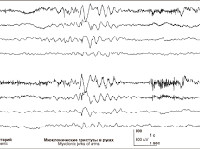
Одна из форм идиопатической эпилепсии, для которой характерны генерализованные миоклонические припадки в раннем детском возрасте. Причины развития недуга до конца не изучены. Заболевание является генетически детерминированным и передается полигенным типом наследования. У новорожденных наблюдаются приступы мышечных сокращений рук, шеи и головы на протяжении нескольких секунд. Обычно, болезнь не влияет общее самочувствие, физическое и психологическое развитие. Для установления и подтверждения диагноза, врач анализирует симптомы, исследует историю болезни и назначает дополнительные обследования. Как правило, выполняют полиграфическую видеоэлектроэнцефалографию, нейросонографию, компьютерную и магнитно-резонансную томографию. Терапевтическая тактика может включать прием вальпроатов, бензодиазепинов либо производных сукцинимида. Заболевание встречается очень редко, известно всего лишь 100-130 случаев.
Причины доброкачественной миоклонической эпилепсии младенчества
Болезнь является генетически детерминированным и передается полигенным типом наследования. Так как недуг встречается очень редко, причины его образования до конца не изучены, и дефектные гены не выявлены. Обычно, в семейном анамнезе малыша присутствуют случаи эпилепсии или фебрильных припадков. Генерализованные миоклонические припадки могут быть спровоцированы звуковыми, тактильными и ритмичными световыми раздражителями.
Симптомы доброкачественной миоклонической эпилепсии младенчества
Болезнь дебютирует в период от полугода до трех лет. Изредка припадки возникают в пятилетнем возрасте. Как правило, физическое и психологическое развитие ребенка не нарушено, до проявления первого припадка. У пятой части младенцев судорожные приступы могут обнаруживаться сразу после рождения. Обычно, заболевание не влияет на общее самочувствие и неврологический статус пациента. В основном, у новорожденных наблюдаются приступы мышечных сокращений рук, шеи и головы на протяжении нескольких секунд. При этом выраженность симптоматики может отличатся даже у одного больного, иногда отмечаются малозаметные подпрыгивания, а иногда – видимые фибрилляции. За один день у пациента может быть 2-3 припадка. Во время засыпания судороги могут усиливаться, а в фазе медленного сна – исчезать. Кроме того, в некоторых случаях во время приступов голова ребенка наклоняется вперед, наблюдаются отводящие и приводящие движения, сгибаются руки, а иногда – плавно вращаются глазные яблоки.
Для рефлекторного типа недуга характерно появления приступа на фоне раздражительного воздействия: звука, света, прикосновений. При спонтанном типе припадки возникают сами по себе. У пациентов с тяжелой формой заболевания отмечаются генерализованные судороги, потеря равновесия, внезапное выпадение предмета из рук, изредка – расстройства сознания. В некоторых случаях возможны нарушения дыхания из-за вовлеченности в процесс межреберных мышц, передней брюшной стенки и диафрагмы. Обычно, по мере роста ребенка выраженность симптоматики нарастает, однако, по достижению старшего возраста – полностью исчезает.
Диагностика доброкачественной миоклонической эпилепсии младенчества
Для установления и подтверждения диагноза, врач анализирует симптомы, исследует историю болезни и назначает дополнительные обследования. Как правило, выполняют полиграфическую видеоэлектроэнцефалографию, нейросонографию, компьютерную и магнитно-резонансную томографию. Если клинические симптомы наблюдаются на протяжении продолжительного периода, специалисты проводят оценку уровня психомоторного развития. Заболевание отличают от криптогенных детских судорог, доброкачественного неэпилептического миоклонуса, синдрома Леннокса-Гасто.
Лечение доброкачественной миоклонической эпилепсии младенчества
Госпитализация необходима лишь при тяжелой форме болезни. Обычно, врачи назначают противоэпилептические средства. Препаратом выбора первой линии являются вальпроаты (Натрия вальпроат). Если же они неэффективны, выписывают бензодиазепины (Нитразепам) либо производные сукцинимида (Этосуксимид). В некоторых случаях медикаментозная терапия не показана, и приступы исчезают самостоятельно.
Профилактика доброкачественной миоклонической эпилепсии младенчества
Специфические меры профилактики не разработаны, поскольку причины заболевания до конца не изучены.
Доброкачественная миоклоническая эпилепсия младенчества (ДМЭМ) – зависящая от возраста форма идиопатической эпилепсии, которая характеризуется генерализованными миоклоническими припадками. Этиология детально не изучена. Патология проявляется мышечными сокращениями верхних конечностей, шеи и головы длительностью в 1-3 сек. с частотою 2-3 раза в день. Общее состояние ребенка и его психофизическое развитие нарушается редко. Диагностика направлена на определение спайк- или полиспайк-волн на ЭЭГ. Основное лечение – медикаментозная монотерапия. Препараты выбора – вальпроаты, при их неэффективности используются бензодиазепины или производные сукцинимида.

Общие сведения
Доброкачественная миоклоническая эпилепсия младенчества (ДМЭМ) – редкая форма эпилепсии в педиатрии. Характерна только для определенной возрастной категории. Впервые заболевание выделено как отдельная нозологическая форма в 1981 году Дарве и Биором. Патология составляет менее 1% от всех форм эпилепсий и порядка 2% от ее идиопатических генерализованных форм. На данный момент в литературе описано около 100-130 случаев данного заболевания. ДМЭМ наблюдается у детей от 6 месяцев до 3 лет, в редких случаях возникает в возрасте до 5 лет. Представители мужского пола болеют в 1,5-2 раза чаще. Патология, как правило, хорошо поддается лечению и полностью купируется в старшем возрасте (в основном – после 6 лет). Осложнения в виде отставания в психомоторном развитии возникают редко и только при отсутствии терапии.

Доброкачественная миоклоническая эпилепсия младенчества
Причины ДМЭМ
Доброкачественная миоклоническая эпилепсия младенчества относится к числу генетически детерминированных заболеваний, передающихся по полигенному типу наследования. Является малоисследованной патологией, поскольку встречается довольно редко. ДМЭМ входит в группу идиопатических генерализованных эпилепсий, однако связи с другими нозологиями из этой группы не установлено. На данный момент неизвестно, мутация каких генов приводит к развитию ДМЭМ.
При сборе семейного анамнеза выясняется, что родители 40% больных страдают или страдали эпилепсией либо фебрильными припадками. Патогенетически развитие миоклонических атак обусловлено возникновением разряда быстрых генерализованных спайк-волн (СВ) или полиспайк-волн (ПСВ). Их частота составляет 3 Гц или более, а длительность – 1-3 сек. Волны формируются в лобных или теменных участках коры головного мозга. Сами атаки могут быть спонтанными или возникающими на фоне определенных (звуковых, тактильных или ритмичных световых) раздражителей.
Симптомы ДМЭМ
ДМЭМ диагностируется в возрасте от 6 месяцев до 3 лет. Развитие ребенка до появления первых миоклонических припадков проходит нормально. Примерно у 20% детей проявляются редкие судороги при рождении или в неонатальном периоде. Общее состояние пациента страдает редко, нарушения неврологического статуса не выявляются. Первые миоклонические атаки поражают верхние конечности, шею и голову, редко – ноги. Они могут иметь разную интенсивность, в том числе – у одного и того же ребенка во время разных эпизодов. Выраженность колеблется от еле заметных подергиваний до видимых фибрилляций.
Частота припадков составляет 2-3 раза в сутки с разными временными интервалами. Длинных серий атак не наблюдается. Возможна провокация атаки громким звуком, тактильной или ритмичной световой стимуляцией. После каждого эпизода может наблюдаться рефрактерный период длительностью от 20 до 120 сек. В этом временном промежутке даже интенсивная стимуляция не вызывает новый приступ. При этом часто наблюдается мышечная атония. Для заболевания характерно усиление миоклонических приступов при засыпании (дремоте) и их исчезновение в фазе медленного сна.
При тяжелых формах возможна генерализация судорог, сопровождающаяся потерей равновесия, внезапным выпадением предметов из рук, редко – расстройствами сознания. В процесс иногда вовлекаются межреберные мышцы, передняя брюшная стенка и диафрагма, из-за чего нарушается дыхание и может выслушиваться экспираторный шум. Для ДМЭМ характерно увеличение интенсивности клинических проявлений до определенного возраста и их последующее полное исчезновение. При длительном течении заболевания возможно отставание в психомоторном развитии. Трансформация в другие формы приступов, в том числе в абсансы, не происходит даже на фоне отсутствия специфического лечения.
Диагностика ДМЭМ
Диагностика доброкачественной миоклонической эпилепсии младенчества заключается в сборе анамнестических данных и проведении инструментальных методов исследования. Физикальное обследование ребенка в интериктальный период неинформативно. Лабораторные тесты каких-либо отклонений от возрастной нормы не выявляют. Наибольшую диагностическую ценность имеет повторная полиграфическая видеоэлектроэнцефалография (видео-ЭЭГ), которая позволяет обнаружить спайк-волны и доказать наличие миоклонических приступов. При необходимости проводится провокационная проба с ритмической световой или тактильной стимуляцией.
Вне приступов (а изредка – во время них) данные ЭЭГ остаются в пределах нормы, спонтанные спайк-волны возникают редко. Во время медленного сна возможно усиление разрядов в коре головного мозга при сохранении их нормальной структуры, возникновение быстрых ритмов или формальных изменений. В быструю фазу (REM-сон) могут фиксироваться генерализованные разряды спайк-волн. С целью исключения органической патологии могут назначаться нейросонография, компьютерная и магнитно-резонансная томография. При наличии клинической симптоматики на протяжении длительного периода проводится оценка психомоторного развития.
Дифференциальная диагностика ДМЭМ осуществляется с криптогенными детскими судорогами, доброкачественным неэпилептическим миоклонусом, синдромом Леннокса-Гасто и миоклонически-астатической эпилепсией раннего детского возраста.
Лечение ДМЭМ
Лечение ДМЭМ, как правило, проводится в амбулаторных условиях, исключением являются частые и тяжелые миоклонические атаки, требующие постоянного наблюдения. Показана медикаментозная терапия при помощи противоэпилептических средств. Первую линию составляют препараты из группы вальпроатов (натрия вальпроат). Важную роль играет подержание стабильной концентрации действующего вещества в крови. Нерегулярное введение назначенных средств провоцирует новые приступы и формирование резистентности к дальнейшей терапии данным медикаментом. При недостаточной эффективности вальпроатов показаны препараты из группы бензодиазепинов (нитразепам) или производных сукцинимида (этосуксимид). Терапевтический курс предполагает лечение на протяжении 3-4 лет с момента возникновения первых припадков.
При выраженной чувствительности к ритмичным световым раздражителям длительность курса увеличивается. При минимальной активности приступов или их исключительно рефлекторном характере лечение может проводиться в сокращенные сроки или не назначаться вовсе. При рецидиве миоклонических атак в старшем возрасте после пройденного лечения рекомендован упрощенный вариант аналогичного терапевтического курса. Обязательным моментом является психологическая поддержка семьи, непосредственно влияющая на эффективность лечения и направленная на исключение триггеров для ребенка.
Специфической профилактики для доброкачественной миоклонической эпилепсии младенчества не разработано. Прогноз в большинстве случаев благоприятный, заболевание, как правило, заканчивается полным выздоровлением ребенка. Миоклонические атаки, возникающие на фоне звуковой или тактильной стимуляции, прогностически более благоприятны, чем спонтанные. Переход в другие формы эпилепсии нехарактерен. Острый период, при котором наблюдаются выраженные припадки, в среднем длится менее 12 месяцев. Более чем у 53% детей в возрасте 6 лет все симптомы ДМЭМ полностью исчезают. Примерно у 14% в дальнейшем наблюдаются задержка психического развития или нарушения в поведении, из-за чего пациенты вынуждены получать образование в специализированных учебных заведениях. Частота осложнений напрямую зависит от своевременности диагностики, эффективности проводимого лечения и психологического климата в семье, в первую очередь – взаимоотношений между ребенком и матерью.
Эпилепсия — общее название группы хронических пароксизмальных болезней головного мозга, проявляющихся повторными судорожными или другими (бессудорожными) стереотипными припадками, сопровождающихся разнообразными (патологическими) изменениями личности и сн
Часть 3. Начало статьи читайте в № 6, 8, 2014 год
Существует немало форм эпилепсии, встречающихся исключительно в детском или подростковом возрасте. Именно зависимость от возраста многих разновидностей эпилепсии является главным отличительным признаком эпилептологии детского возраста [1–4].
Хотя продолжительность неонатального периода невелика, целый ряд эпилептических синдромов свойственен именно для новорожденных детей [3–5].
Доброкачественные семейные приступы (судороги) новорожденных
Доброкачественная неонатальная эпилепсия (с аутосомно-доминатным типом наследования) трех типов, проявляющаяся в первые 7 дней жизни (начиная с трех суток). В семейном анамнезе обязательно фигурируют указания на наличие в прошлом судорог у членов семьи пациента (в неонатальном периоде). Связь припадков с уточненными врожденными нарушениями метаболизма не установлена. Доброкачественные семейные неонатальные приступы манифестируют в виде фокальных и мультифокальных или генерализованных тонико-клонических (судорожных) припадков. Указанные припадки характеризуются малой продолжительность (1–2 мин) и значительной частотой (20–30 эпизодов за сутки). Впоследствии, по прошествии от 1 до 3 недель, приступы самопроизвольно спонтанно купируются.
Эта эпилепсия с дебютом в раннем неонатальном периоде имеет также другое название (доброкачественные идиопатические неонатальные судороги). Болезнь впервые описана в конце 1970-х гг. Судорожные приступы развиваются у доношенных новорожденных детей, не имевших до этого признаков патологии со стороны ЦНС. Дебют приступов происходит к концу 1-й недели жизни (в 80–90% случаев — между 4-м и 6-м днями), а их пик приходится на 5-й день жизни (отсюда и название). Описываемые приступы обычно имеют вид мультифокальных клонических судорог, которым нередко сопутствуют апноэ. В большинстве случаев доброкачественные идиопатические неонатальные судороги длятся не более 24 ч (они всегда прекращаются по прошествии 15 дней после дебюта). В 80% случаев за время судорожного периода у новорожденных отмечается развитие эпилептического статуса [3–5].
Ранняя миоклоническая (эпилептическая) энцефалопатия
Витамин В6-зависимая эпилепсия
Cравнительно редкое наследственное заболевание, характеризующееся фармакорезистентными судорогами. Относится к группе метаболически обусловленных эпилепсий. Развивается у новорожденных, матери которых длительно получали пиридоксин во время беременности, а также при специфическом наследственном дефекте метаболизма (с повышенной потребностью в витамине В6). Известны случаи дебюта пиридоксинзависимых судорог у детей старше 1 мес и даже на втором году жизни. Между приступами судорог дети остаются беспокойными, реагируют мышечными подергиваниями на внешние раздражения. Болезнь не поддается обычному противосудорожному лечению, но назначение витамина В6 в высоких дозах (25 мг/кг/сут) быстро приводит к нормализации состояния [3–5].
Злокачественные мигрирующие парциальные судороги (приступы) младенческого возраста
Чрезвычайно редко встречающийся эпилептический синдром, описанный G. Coppola и соавт. (1995). К настоящему времени сообщается всего о примерно 50 случаях болезни, зарегистрированных в различных странах мира. Злокачественные мигрирующие парциальные судороги в 50% случаев наблюдаются в первые дни жизни; остальные 50% приходятся на возраст 1–3 мес. При дебюте приступы носят фокальный клонический характер, а по прошествии нескольких недель они становятся мультифокальными, причем исключительно частыми и фармакорезистентными к терапии антиэпилептическими препаратами. При ЭЭГ-исследовании у детей выявляется выраженная многоочаговая эпилептическая активность; метаболических нарушений не обнаруживается, а МРТ-признаки патологических изменений отсутствуют. Паталогоанатомическое исследование позволило выявить в гиппокампе признаки нейрональной потери [1, 3, 5, 8].
По достижении 1-месячного возраста число разновидностей эпилептических синдромов, специфичных для первого года жизни ребенка, практически не уступает таковому, свойственному периоду новорожденности.
Инфантильные спазмы (синдром Веста)
Тяжелая миоклонус-эпилепсия младенческого возраста (синдром Драве)
Болезнь, описанная C. Dravet (1978, 1992), дебютирует на первом году жизни (между 2-м и 9-м мес), что нередко происходит вслед за развитием фебрильного эпизода, вскоре после вакцинации или перенесения инфекции. Синдром Драве характеризуется появлением генерализованных или односторонних клонических судорог (обычно на фоне гипертермии или лихорадки), что происходит на фоне предшествующего нормального психомоторного развития ребенка на протяжении первого года жизни. Постепенно (по прошествии нескольких недель или месяцев) у ребенка развиваются афебрильные миоклонические и парциальные (фокальные) припадки. Прогрессивное нарастание частоты миоклоний (изолированных или серийных) предшествует появлению у пациентов генерализованных припадков. У детей выявляются умеренные мозжечковые и пирамидные знаки, связанные с дефицитарностью грубой моторики и атаксией походки. Нарушения психомоторного развития впоследствии отмечаются у детей примерно до 4-летнего возраста. Нередко при синдроме Драве у детей развивается эпилептический статус (судорожный или миоклонический). Данные ЭЭГ на протяжении первого года жизни обычно остаются в пределах нормы, хотя у отдельных пациентов встречаются спонтанные фотоиндуцированные пик-волновые разряды. Впоследствии иктальные ЭЭГ-исследования при синдроме Драве характеризуются наличием миоклонических или клонических припадков (генерализованная пик-волновая или полипик-волновая активность). Генерализованные разряды усиливаются в состоянии релаксации; одновременно отмечаются фокальные и мультифокальные пики и острые волны. Традиционные и новые антиэпилептические препараты обычно не предотвращают рецидива приступов при синдроме Драве. Прогноз по интеллектуальному развитию при синдроме Драве всегда неблагоприятен [3–5, 8].
Идиопатические доброкачественные парциальные эпилепсии младенчества
Для детей раннего возраста (от 12 до 36 месяцев), в первую очередь, характерны cиндром Доозе, синдром Леннокса–Гасто, доброкачественная миоклонуc-эпилепсия младенческого возраста, синдром гемиконвульсий-гемиплегии, идиопатическая парциальная эпилепсия младенчества, абсансная эпилепсия раннего детства, электрический эпилептический статус медленно-волнового сна, ранний и поздний детский нейрональный липофусциноз (типы I и II).
Миоклоническая астатическая эпилепсия раннего детского возраста (cиндром Доозе)
Синдром Леннокса–Гасто, или миокинетическая эпилепсия раннего детства с медленными пик-волнами
Группа гетерогенной патологии с эпилептическими приступами (атоническими, тоническими, атипичными абсансами), интеллектуальной дефицитарностью и характерным ЭЭГ-паттерном. Как и при синдроме Веста, при синдроме Леннокса–Гасто выделяют симптоматический и криптогенный варианты болезни. Ранние формы дебютируют примерно с 2-летнего возраста. До 30% случаев представляют собой результат трансформации из синдрома Веста. Клинически синдром Леннокса–Гасто характеризуется миоклонически-астатическими припадками, салаамовыми судорогами (молниеносными кивательными), атипичными абсансами, тоническими приступами (чаще во сне). Могут встречаться генерализованные тонико-клонические, миоклонические и фокальные (парциальные) приступы. Для детей типична серийность припадков с изменениями сознания (ступор) и постепенным переходом в эпилептический статус. Помимо эпилептических приступов, в неврологическом статусе могут отмечаться церебральные парезы/параличи, а также атонически-астатические нарушения (до 40% пациентов). У детей происходит снижение интеллекта (различной степени), наблюдаются выраженные нарушения когнитивных функций. По ЭЭГ-данным типичны изменения фоновой активности в виде медленных пик-волн
В. М. Студеникин, доктор медицинских наук, профессор, академик РАЕ

Доброкачественная миоклоническая эпилепсия младенчества (ДМЭМ) – зависящая от возраста форма идиопатической эпилепсии, которая характеризуется генерализованными миоклоническими припадками. Этиология детально не изучена. Патология проявляется мышечными сокращениями верхних конечностей, шеи и головы длительностью в 1-3 сек. с частотою 2-3 раза в день. Общее состояние ребенка и его психофизическое развитие нарушается редко. Диагностика направлена на определение спайк- или полиспайк-волн на ЭЭГ. Основное лечение – медикаментозная монотерапия. Препараты выбора – вальпроаты, при их неэффективности используются бензодиазепины или производные сукцинимида.

- Причины ДМЭМ
- Симптомы ДМЭМ
- Диагностика ДМЭМ
- Лечение ДМЭМ
- Прогноз и профилактика ДМЭМ
- Цены на лечение
Общие сведения
Доброкачественная миоклоническая эпилепсия младенчества (ДМЭМ) – редкая форма эпилепсии в педиатрии. Характерна только для определенной возрастной категории. Впервые заболевание выделено как отдельная нозологическая форма в 1981 году Дарве и Биором. Патология составляет менее 1% от всех форм эпилепсий и порядка 2% от ее идиопатических генерализованных форм. На данный момент в литературе описано около 100-130 случаев данного заболевания. ДМЭМ наблюдается у детей от 6 месяцев до 3 лет, в редких случаях возникает в возрасте до 5 лет. Представители мужского пола болеют в 1,5-2 раза чаще. Патология, как правило, хорошо поддается лечению и полностью купируется в старшем возрасте (в основном – после 6 лет). Осложнения в виде отставания в психомоторном развитии возникают редко и только при отсутствии терапии.

Причины ДМЭМ
Доброкачественная миоклоническая эпилепсия младенчества относится к числу генетически детерминированных заболеваний, передающихся по полигенному типу наследования. Является малоисследованной патологией, поскольку встречается довольно редко. ДМЭМ входит в группу идиопатических генерализованных эпилепсий, однако связи с другими нозологиями из этой группы не установлено. На данный момент неизвестно, мутация каких генов приводит к развитию ДМЭМ.
При сборе семейного анамнеза выясняется, что родители 40% больных страдают или страдали эпилепсией либо фебрильными припадками. Патогенетически развитие миоклонических атак обусловлено возникновением разряда быстрых генерализованных спайк-волн (СВ) или полиспайк-волн (ПСВ). Их частота составляет 3 Гц или более, а длительность – 1-3 сек. Волны формируются в лобных или теменных участках коры головного мозга. Сами атаки могут быть спонтанными или возникающими на фоне определенных (звуковых, тактильных или ритмичных световых) раздражителей.
Симптомы ДМЭМ
ДМЭМ диагностируется в возрасте от 6 месяцев до 3 лет. Развитие ребенка до появления первых миоклонических припадков проходит нормально. Примерно у 20% детей проявляются редкие судороги при рождении или в неонатальном периоде. Общее состояние пациента страдает редко, нарушения неврологического статуса не выявляются. Первые миоклонические атаки поражают верхние конечности, шею и голову, редко – ноги. Они могут иметь разную интенсивность, в том числе – у одного и того же ребенка во время разных эпизодов. Выраженность колеблется от еле заметных подергиваний до видимых фибрилляций.
Частота припадков составляет 2-3 раза в сутки с разными временными интервалами. Длинных серий атак не наблюдается. Возможна провокация атаки громким звуком, тактильной или ритмичной световой стимуляцией. После каждого эпизода может наблюдаться рефрактерный период длительностью от 20 до 120 сек. В этом временном промежутке даже интенсивная стимуляция не вызывает новый приступ. При этом часто наблюдается мышечная атония. Для заболевания характерно усиление миоклонических приступов при засыпании (дремоте) и их исчезновение в фазе медленного сна.
При тяжелых формах возможна генерализация судорог, сопровождающаяся потерей равновесия, внезапным выпадением предметов из рук, редко – расстройствами сознания. В процесс иногда вовлекаются межреберные мышцы, передняя брюшная стенка и диафрагма, из-за чего нарушается дыхание и может выслушиваться экспираторный шум. Для ДМЭМ характерно увеличение интенсивности клинических проявлений до определенного возраста и их последующее полное исчезновение. При длительном течении заболевания возможно отставание в психомоторном развитии. Трансформация в другие формы приступов, в том числе в абсансы, не происходит даже на фоне отсутствия специфического лечения.
Диагностика ДМЭМ
Диагностика доброкачественной миоклонической эпилепсии младенчества заключается в сборе анамнестических данных и проведении инструментальных методов исследования. Физикальное обследование ребенка в интериктальный период неинформативно. Лабораторные тесты каких-либо отклонений от возрастной нормы не выявляют. Наибольшую диагностическую ценность имеет повторная полиграфическая видеоэлектроэнцефалография (видео-ЭЭГ), которая позволяет обнаружить спайк-волны и доказать наличие миоклонических приступов. При необходимости проводится провокационная проба с ритмической световой или тактильной стимуляцией.
Вне приступов (а изредка – во время них) данные ЭЭГ остаются в пределах нормы, спонтанные спайк-волны возникают редко. Во время медленного сна возможно усиление разрядов в коре головного мозга при сохранении их нормальной структуры, возникновение быстрых ритмов или формальных изменений. В быструю фазу (REM-сон) могут фиксироваться генерализованные разряды спайк-волн. С целью исключения органической патологии могут назначаться нейросонография, компьютерная и магнитно-резонансная томография. При наличии клинической симптоматики на протяжении длительного периода проводится оценка психомоторного развития.
Дифференциальная диагностика ДМЭМ осуществляется с криптогенными детскими судорогами, доброкачественным неэпилептическим миоклонусом, синдромом Леннокса-Гасто и миоклонически-астатической эпилепсией раннего детского возраста.
Лечение ДМЭМ
Лечение ДМЭМ, как правило, проводится в амбулаторных условиях, исключением являются частые и тяжелые миоклонические атаки, требующие постоянного наблюдения. Показана медикаментозная терапия при помощи противоэпилептических средств. Первую линию составляют препараты из группы вальпроатов (натрия вальпроат). Важную роль играет подержание стабильной концентрации действующего вещества в крови. Нерегулярное введение назначенных средств провоцирует новые приступы и формирование резистентности к дальнейшей терапии данным медикаментом. При недостаточной эффективности вальпроатов показаны препараты из группы бензодиазепинов (нитразепам) или производных сукцинимида (этосуксимид). Терапевтический курс предполагает лечение на протяжении 3-4 лет с момента возникновения первых припадков.
При выраженной чувствительности к ритмичным световым раздражителям длительность курса увеличивается. При минимальной активности приступов или их исключительно рефлекторном характере лечение может проводиться в сокращенные сроки или не назначаться вовсе. При рецидиве миоклонических атак в старшем возрасте после пройденного лечения рекомендован упрощенный вариант аналогичного терапевтического курса. Обязательным моментом является психологическая поддержка семьи, непосредственно влияющая на эффективность лечения и направленная на исключение триггеров для ребенка.
Специфической профилактики для доброкачественной миоклонической эпилепсии младенчества не разработано. Прогноз в большинстве случаев благоприятный, заболевание, как правило, заканчивается полным выздоровлением ребенка. Миоклонические атаки, возникающие на фоне звуковой или тактильной стимуляции, прогностически более благоприятны, чем спонтанные. Переход в другие формы эпилепсии нехарактерен. Острый период, при котором наблюдаются выраженные припадки, в среднем длится менее 12 месяцев. Более чем у 53% детей в возрасте 6 лет все симптомы ДМЭМ полностью исчезают. Примерно у 14% в дальнейшем наблюдаются задержка психического развития или нарушения в поведении, из-за чего пациенты вынуждены получать образование в специализированных учебных заведениях. Частота осложнений напрямую зависит от своевременности диагностики, эффективности проводимого лечения и психологического климата в семье, в первую очередь – взаимоотношений между ребенком и матерью.
Читайте также:


