Эпилептическая энцефалопатия синдром леннокса гасто
Синдром Леннокса-Гасто — отдельная форма эпилепсии детского возраста, характеризующаяся наличием полиморфных пароксизмов (миоклонических, атонических, тонических и абсансов) и задержкой нейро-психического развития. Может иметь криптогенный характер или выступать синдромом других патологических состояний (церебральных аномалий, генетических обменных заболеваний, перинатальной патологии). Синдром Леннокса-Гасто диагностируется по типичной вариативной картине эпиприступов и характерному паттерну электроэнцефалограммы. Дополнительно проводится МРТ и КТ головного мозга. Антиконвульсантная терапия синдрома малоэффективна, проводится поиск альтернативных методов лечения. Прогноз вариабельный, но в большинстве случаев неблагоприятный.
- Причины синдрома Леннокса-Гасто
- Симптомы синдром Леннокса-Гасто
- Диагностика синдрома Леннокса-Гасто
- Лечение синдрома Леннокса-Гасто
- Прогноз синдрома Леннокса-Гасто
- Цены на лечение
Общие сведения
Синдром Леннокса-Гасто (СЛГ) — вариант эпилепсии детского возраста, для которого характерно сочетание атонических, миоклонических, тонических эпиприступов и атипичных абсансов, медленный островолновой паттерн ЭЭГ. В 1950 г. СЛГ был выделен в качестве отдельного эпилептического синдрома, а в 1964-1966 гг. неврологическое сообщество признала его самостоятельной нозологической формой. Синдром Леннокса-Гасто по различным данным составляет от 3% до 10% всех случаев детской эпилепсии. Его распространенность колеблется в пределах 1-2,8 случаев на 10 тыс. Несколько чаще встречается у мальчиков. Типичный возраст начала заболевания от 2 до 5 лет, реже — 6-8 лет. Сегодня СЛГ является тяжелым заболеванием с прогрессирующим течением, эффективное лечение которого пока является предметом надежд многих специалистов в области детской неврологии и эпилептологии.

Причины синдрома Леннокса-Гасто
Синдром Леннокса-Гасто относится к заболеваниям, этиологические факторы которых пока точно не установлены. Известно, что во многих случаях синдром носит симптоматический характер и формируется на фоне генетической патологии, последствий различных неблагоприятных факторов, действующих в перинатальном периоде и на 1-ом году жизни. Однако в большинстве случаев морфологический субстрат заболевания остается не выявленным. К этиофакторам, способным спровоцировать развитие СЛГ, относят гипоксию плода, внутриутробные инфекции (краснуху, цитомегалию, герпес, токсоплазмоз), родовые травмы новорожденных (в первую очередь внутричерепные), недоношенность, асфиксию новорожденных, тяжелые инфекционные заболевания постнатального периода (менингит, энцефалит), аномалии развития головного мозга (гидроцефалию, кортикальную дисплазию, гипоплазию мозолистого тела и др.), метаболические нарушения с поражением ЦНС, отдельные генетические заболевания (например, туберозный склероз).
В 25-40% случаев синдром Леннокса-Гасто возникает у детей с отягощенным по эпилепсии семейным анамнезом. Кроме того, существует гипотеза об этиологической роли иммунных нарушений, в т. ч. возникающих вследствие вакцинации. Примерно в 30% случаев СЛГ является следствием эволюции синдрома Веста. Когда синдром Леннокса-Гасто манифестирует на фоне полного благополучия в здоровье ребенка и отсутствия в его анамнезе вышеперечисленных факторов, говорят о криптогенной (не имеющей вероятной причины) форме заболевания. Криптогенный вариант СЛГ встречается в 10-20% случаев и отличается более благоприятным течением.
Симптомы синдром Леннокса-Гасто
Симптоматический синдром Леннокса-Гасто, как правило, дебютирует на фоне уже имеющегося отставания в умственном и психическом развитии. При криптогенной форме развитие ребенка на момент манифестации синдрома соответствует норме. СЛГ отличается большой вариативностью приступов, их различной продолжительностью и частотой.
Миоклонические пароксизмы представляют собой локальные мышечные подергивания. Чаще охватывают мышцы-сгибатели проксимальных отделов рук, при распространении на нижние конечности происходит падение. Характеризуются симметричным серийным возникновением в обеих конечностях и стереотипностью. Нуждаются в дифференцировке с миоклониями при клещевом энцефалите и токсических поражениях ЦНС; миоклонусом неэпилептического характера, для которого типичны нерегулярные асимметричные миоклонии, возникающие в ответ на различные сенсорные раздражители (звук, свет, прикосновение) и не сопровождающиеся изменениями ЭЭГ.
Тонические пароксизмы СЛГ часто возникают в период сна и отличаются своей кратковременностью (средняя длительность 10 сек.). Сопровождаются отключением сознания. Могут иметь генерализованный характер или проявляться в виде тонического напряжения отдельных мышечных групп (заднешейных, спинных, мышц брюшного пресса, плечевого пояса и пр.). Тонические пароксизмы сопровождаются тахикардией, цианозом лица, слезотечением, апноэ, гиперсаливацией. Минимальные локальные пароксизмы тонического характера иногда с трудом можно отдифференцировать от зевоты или потягивания.
Задержка психомоторного развития (ЗПР) отмечается почти во всех случаях СЛГ. Ее выраженность зависит от формы синдрома (криптогенная или симптоматическая), характера фоновой патологии ЦНС, тяжести и частоты эпилептических пароксизмов. Как правило, на первый план выходят проблемы с обучением владению новыми навыками и с усвоением новой информации. Зачастую наблюдается агрессивность, гиперактивность, эмоциональная нестабильность, характерные для аутизма особенности характера. Около 50% подростков, имеющих синдром Леннокса-Гасто, не владеют навыками самообслуживания. Еще 25% социально и эмоционально дезадаптированы по причине выраженной олигофрении. Особенности поведения и характера не дают возможность нормально адаптироваться в социуме даже тем пациентам, у которых олигофрения имеет легкую степень выраженности. Нормальная социальная адаптация наблюдается лишь в 15% случаев.
Диагностика синдрома Леннокса-Гасто
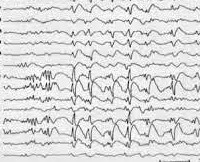
Синдром Леннокса-Гасто устанавливается на основании типичной клинической картины, состоящей из полиморфных эпиприступов и симптомов отставания нейро-психического развития. Учитывается также возраст начала пароксизмов и семейный эпилептический анамнез. Большую диагностическую роль играет электроэнцефалография. Межприступная (интериктальная) ЭЭГ в бодрствующем состоянии регистрирует плохую структурированность и замедленность основного ритма. ЭЭГ-паттерн имеет картину гипсаритмии с большим количеством спайков различной амплитуды. Наиболее высокие пики регистрируются в лобной области. ЭЭГ-паттерн в период приступов зависит от их формы.
Методы нейровизуализации (МРТ и КТ головного мозга) выявляют преимущественно неспецифичные патологические изменения: внутреннюю гидроцефалию, атрофию подкорковых областей и корковых структур преимущественно лобной зоны, гипоплазию лобных долей. Попытки проанализировать при помощи ПЭТ головного мозга степень утилизации глюкозы церебральными тканями дали противоречивые сведенья: в одних случаях были выявлены зоны гиперметаболизма, в других — гипометаболизма; у части пациентов метаболизм глюкозы был в пределах нормы.
По причине большой вариативности пароксизмов, синдром Леннокса-Гасто следует дифференцировать с целым рядом других форм эпилепсии, дебютирующих в детском возрасте: с миоклонической эпилепсией, доброкачественной роландической эпилепсией, синдромом Веста, детской абсансной эпилепсией, дисметаболической эпилепсией при болезни Гоше, Краббе, Ниманна-Пика и др.
Лечение синдрома Леннокса-Гасто
Терапия проводится противоэпилептическими средствами. Применяются вальпроевая к-та, этосуксимид, карбамазепин, ламотриджин и др. В большинстве случаев проводится комбинированное лечение одним из указанных фармпрепаратов и вальпроатом натрия. Однако до 90% случаев синдрома Леннокса-Гасто являются резистентными к антиконвульсантной терапии. В связи с этим основной целью лечения является уменьшение числа эпиприступов и улучшение качества жизни ребенка и его семьи в межпароксизмальный период.
Неврологами и эпилептологами ведется поиск новых способов терапии. Доказанной является положительная роль кетогенной диеты, заключающейся в резком ограничении употребления углеводов и повышении содержания жиров в пище. Рядом клиницистов отмечен положительный эффект лечения синдрома Леннокса-Гасто большими дозировками иммуноглобулина. Наблюдалась эффективность применения АКТГ и глюкокортикоидов. В случаях, когда синдром Леннокса-Гасто сопровождается частыми и тяжелыми эпипароксизмами с падением и угрозой травматизации ребенка, совместно с нейрохирургом может быть рассмотрен вопрос о проведении хирургической операции рассечения мозолистого тела — каллозотомии. Подобное вмешательство не избавляет пациентов от приступов, но существенно уменьшает их интенсивность.
К новым способам лечения относится имплантация стимулятора блуждающего нерва и RNS-стимулятора. В первом случае прибор устанавливается подкожно в область ключицы, а его электрод проводят к проходящему в шее блуждающему нерву. По данным проведенных в США и Европе исследований, в 60% случаев данное устройство позволяет снизить количество эпиприступов. Во втором случае прибор вшивается под кожу головы, а его электроды имплантируются в зону эпилептогенного очага. С их помощью, подобно ЭЭГ, устройство постоянно регистрирует электрическую активность мозга. При получении сигналов, свидетельствующих о начинающемся пароксизме, прибор генерирует ответные импульсы, обеспечивающие супрессию эпилептической активности.
Синдром Леннокса-Гасто имеет в основном неблагоприятный прогноз. До 10% случаев заканчивается гибелью детей в течение первого десятилетия жизни. Летальные исходы связаны преимущественно с тяжелой травматизацией во время эпиприступов с падением. Прогностически неблагоприятными критериями считаются: манифестация синдрома в более раннем возрасте, начало судорог на фоне ЗПР, предшествующий синдром Веста, высокая частота и интенсивность пароксизмов. Невозможность медикаментозного купирования эпиприступов приводит к прогрессирующей ЗПР. Практически у всех пациентов наблюдается выраженная в различной степени умственная отсталость, половина больных не способны к самообслуживанию.
Этиология. Синдром Леннокса – Гасто (СЛГ) относится к генерализованным криптогенным или симптоматическим формам эпилепсии. Генетические факторы играют малую роль в возникновении заболевания. Вместе с тем, при классическом (криптогенном) варианте СЛГ структурные изменения в мозге также не определяются. По Проекту классификации 2001 года СЛГ относится к группе эпилептических энцефалопатий детского возраста.
Диагностические критерии. Частота встречаемости синдрома Леннокса-Гасто (СЛГ) составляет около 3% от всех форм эпилепсии в педиатрической практике. История описания синдрома связана с именами Gibbs (1939), Lennox (1945) и Gastaut & Dravet (1966). СЛГ дебютирует в детском возрасте, проявляясь полиморфными приступами, специфическими изменениями ЭЭГ, выраженными когнитивными нарушениями и резистентностью к терапии с высокой частотой инвалидизации. Наиболее точные критерии СЛГ были представлены Beaumanoir & Dravet (1992).
- Эпилептические приступы: преимущественно, аксиальные тонические, атонические и атипичные абсансы.
- Данные ЭЭГ: диффузные медленные комплексы острая – медленная волна в бодрствовании, а также пробеги быстрой активности во сне.
- Статус: задержка психического развития и нарушения поведения.
Заболевание дебютирует в возрасте от 2 до 8 лет. Пик начала приходится на дошкольный возраст: 3-5 лет. При симптоматической форме отмечается более ранний дебют, чем при криптогенной. Примерно в 20% случаев СЛГ трансформируется из синдрома Веста. Фебрильные судороги предшествуют развитию синдрома в 10% случаев.
Семиология приступов при СЛГ крайне разнообразна. Следующие виды приступов составляют клиническую картину синдрома Леннокса – Гасто.
Тонические приступы - облигатный клинический симптом СЛГ. Наиболее характерны тонические аксиальные приступы с вовлечением мускулатуры туловища, поясов конечностей, шеи, лица. Проявляются в виде двухсторонних спазмов с внезапным кивком; наклоном туловища; приподниманием, разведением и вытягиванием вперед рук. Обычно они непродолжительны (от 10 до 30 сек), сопровождаются выключением сознания и чаще возникают в медленную фазу сна.
Эпилептический статус констатируется у 75% больных СЛГ, достигая максимума у пациентов с выраженным снижением интеллекта. Обычно возникает в утренние часы, после пробуждения пациентов. Продолжительность его варьирует от десятков минут до нескольких часов, реже - суток. Проявляется в двух основных формах: статус спутанного сознания и статус тонических приступов [Beaumanoir и соавт., 1988]. Клинически характеризуется снижением двигательной (до ступора) и психической активности, гипомимией, мышечной гипотонией, слюнотечением; сознание флюктуирует. Эпилептический статус свидетельствует о неблагоприятном течении заболевания и может представлять непосредственную угрозу для жизни пациентов. Важно, что парентеральное введение бензодиазепинов (диазепам), может привести к нарастанию тонических спазмов и дыхательных нарушений. Большинство авторов рекомендуют применение кортикостероидных гормонов для купирования статуса при СЛГ.
Полиморфизм приступов – отличительная черта СЛГ. Практически во всех случаях у пациентов отмечается более, чем 1 тип приступов и в большинстве случаев – более 2-х типов. Наиболее типичны комбинации из 3-х основных типов приступов: тонических аксиальных, атипичных абсансов и падений в сочетании с эпилептическим статусом. Приступы имеют тенденцию к учащению в период после пробуждения пациентов, а также при снижении уровня бодрствования (например, в случае назначения барбитуратов, нейролептиков или транквилизаторов).
ЭЭГ изменения при СЛГ характеризуются 3 основными признаками:
- замедление основной активности фоновой записи;
- наличие пробегов генерализованной быстрой активности с частотой около 20 Гц, чаще во сне;
- появление высокоамплитудной генерализованной активности острая – медленная волна с частотой 2,5 Гц и менее.
Характер изменений при нейровизуализации зависит от формы заболевания. При криптогенном варианте локальные структурные нарушения отсутствуют. Вместе с тем, у большинства пациентов по данным КТ и МРТ выявляется диффузная атрофия головного мозга. В симптоматических случаях обнаруживаются очаговые поражения коры головного мозга. При этом, однако, возникают сложности дифференциальной диагностики с симптоматическими фокальными формами эпилепсии.
Дифференцировать СЛГ следует с широким спектром различных форм эпилепсии (прежде всего, с криптогенной лобной эпилепсией с псевдогенерализованными приступами), а также с рядом наследственно – дегенеративных заболеваний. При дифференциальной диагностике следует использовать все клинико – электро – анатомические характеристики СЛГ, а также данные анамнеза об особенностях течения заболевания. Кардинальным звеном в диагностике СЛГ является сочетание тонических аксиальных приступов с пробегами быстрых ритмов на ЭЭГ.
Тяжелую инвалидизацию при СЛГ приходится констатировать практически в 100% случаев. До 65% больных не способны жить самостоятельно.
Терапия. Один из важных диагностических критериев синдрома Леннокса-Гасто (СЛГ) – терапевтическая резистентность. Все методы лечения больных СЛГ систематизированы нами следующим образом.
- I. Антиэпилептические препараты.
- Базовые: топирамат и вальпроаты.
- Дополнительные: леветирацетам, сукцинимиды, ламотриджин, карбамазепин, бензодиазепины, гидантоины.
- II. Другие препараты.
- Стероидные гормоны.
- Иммуноглобулины.
- Тиреотропин - релизинг гормон.
- III. Немедикаментозные методы.
- Кетогенная диета.
- Стимуляция блуждающего нерва.
- Оперативное вмешательство (передняя каллозотомия или кортикальные резекции).
Препараты второго выбора - вальпроаты. Назначается конвульсофин с постепенным увеличением до 900-2500 мг/сут (40-80) мг/кг/сут и выше до максимально переносимой дозы. Вальпроаты особенно эффективны при криптогенных формах с преобладанием атипичных абсансов и миоклонических приступов. Недостаток вальпроатов – слабое воздействие на тонические приступы.
При недостаточном эффекте монотерапии (большинство случаев) рекомендован переход на комбинацию препаратов. Базовые комбинации: топамакс + конвульсофин, конвульсофин + суксилеп, конвульсофин или топамакс + ламиктал. Суксилеп назначается в дозе 500–1000 мг/сут (20-35 мг/кг/сут) в 2-3 приема; он эффективен при атипичных абсансах. Ламиктал применяется, начиная с 12,5 мг/сут, наращивая дозу по 12,5 мг 1 раз в нед. Средние дозировки препарата – 75-200 мг/сут (3-7 мг/кг/сут) в 2 приема.
Наиболее частая комбинация при резистентных приступах у больных СЛГ: топамакс + конвульсофин + суксилеп (или фризиум). Другие методы лечения (стероидные гормоны, иммуноглобулины, вагус – стимуляция, кетогенная диета) показали слабую эффективность при СЛГ.
Механизм действия - ограничение разрядов нейронов, связанное с блокирующим действием на натриевые каналы (регулирование активности натриевых каналов за счет увеличение длительности их неактивного состояния), и стабилизация мембран нейронов. Препарат выпускается в таблетках, содержащих 100, 200 или 400 мг действующего вещества.
У пациентов старше 4 лет с массой тела менее 30 кг, не принимающих вальпроевую кислоту, начальная доза составляет 200 мг в сутки, титрация дозы – увеличение на 200 мг в сутки раз в 2 дня до терапевтической дозы 1000 мг в сутки. У пациентов с массой тела менее 30 кг, одновременно принимающих вальпроевую кислоту (вальпроат увеличивает клиренс руфинамида), рекомендуемая терапевтическая доза составляет 600 мг в сутки.
У пациентов с массой тела более 30 кг, включая взрослых, начальная доза составляет 400 мг в сутки, титрация – по 400 мг раз в 2 дня, терапевтическая доза варьирует от 1800 до 2400 и 3200 мг в сутки (максимальная суточная терапевтическая доза). [Инструкция по применению]
При расчете на кг веса тела стартовая доза руфинамида составляет 10 мг/кг/сут с повышением дозы на 10 мг/кг/сут каждые 2 дня до терапевтической дозы 45 мг/кг/сут (в два приема) (Wier H. A. и соавт., 2011).
Руфинамид рекомендовано принимать 2 раза в сутки с 12-часовым интервалом. [Инструкция по применению].
Руфинамид также характеризуется достаточно хорошей переносимостью. Наиболее распространенные побочные эффекты руфинамида: сонливость, усталость, головокружение, диплопия, тошнота и атаксия; сонливость, раздражительность, рвота и потеря аппетита. По мнению Coppola G и соавт. (2014), руфинамид, по-видимому, имеет более благоприятный профиль когнитивных ПЭ по сравнению с другими АЭП, применяющимися в лечении СЛГ.
По данным Montouris GD и соавт. (2014), в настоящее время в мире официально зарегистрировано 5 АЭП для лечения СЛГ: фелбамат, ламотриджин, топирамат, руфинамид и клобазам, и еще несколько АЭП применяются off-label с определенными показаниями и ограничениями.
Таблица. Данные клинических исследований АЭП, одобренных FDA для лечения СЛГ (Montouris CD, 2014)

Синдром Леннокса-Гасто — это редкая и тяжёлая форма эпилепсии, симптомы которой начинают проявляться в раннем детстве. Приступы характеризуются разнообразием эпилептических припадков.
Этот тип эпилепсии очень трудно поддаётся терапии, однако медицина разрабатывает всё новые и новые методики для успешного лечения этого заболевания.
Дебют болезни обычно приходится на возраст от двух до восьми лет, иногда чуть позднее. Таким деткам тяжело учиться, в первую очередь это связано с задержкой общего развития — они начинают довольно поздно самостоятельно садиться, ползать, ходить.
Задержка в развитии может быть умеренной или же выражаться в тяжёлой степени, наряду с этим наблюдаются когнитивные расстройства.
Физиологическое и психическое развитие каждого ребёнка индивидуально, поэтому сложно предугадать, как будет вести себя малыш с этим синдромом.
В то время, как у большинства больных обнаруживаются частые приступы эпилептических припадков и другие различные нарушения, в некоторых случаях адекватное лечение даёт достаточно хорошие результаты и снижение числа приступов.
Впервые детская миоклоническая эпилепсия был выделена в качестве отдельного синдрома в 50-х гг. прошлого столетия, а уже через десять лет неврологическое сообщество признало его самостоятельной нозологической формой.
Это заболевание по разным данным составляет от 3% до 10% всех случаев эпилепсии у детей. Распространённость патологии равна одному-двум случаям на 10 тысяч человек. Чаще встречается у мальчиков, чем у девочек.

Патогенез нарушения
Хотя первые симптомы возникают у детей в возрасте от двух до восьми лет, выделяют отдельную фокус-группу больных, у которых 
заболевание проявляется в 4-6-летнем возрасте.
В некоторых случаях болезнь трансформируется из синдрома Веста, диагноз которого ставят деткам до года. Тогда синдром будет развиваться по одному из сценариев:
- инфантильные спазмы синдрома Веста сменяются тоническими приступами, пропуская скрытую форму и переходят в синдром Леннокса-Гасто;
- детские спазмы синдрома Веста проходят, отмечается улучшение психомоторного развития.
Комплекс провоцирующих факторов
На сегодняшний день конкретные причины, провоцирующие этот вид эпилепсии не известны. К факторам риска можно отнести:
- кислородное голодание плода в пренатальном периоде;
- поражения головного мозга ребёнка в пренатальный и натальный период — преждевременные роды, физиологическое недоразвитие;
- инфекционные поражения мозга вследствие краснухи, энцефалита, менингита;
- кортикальная дисплазия — нарушение строения коры головного мозга;
- туберозный склероз — доброкачественные опухоли во множестве тканей и органов.
- идиопатический фактор — болезнь развивается по неизвестным причинам;
- генетическая предрасположенность.
Характеристика припадков
Дети с синдромом Леннокса-Гасто подвергаются частым приступам эпилептических припадков в тяжёлой форме. Клиническая картина болезни выглядит следующим образом:
У многих детей с болезнью Леннокса-Гасто присутствует умственное недоразвитие, и как следствие — трудности в обучении, а также когнитивные (поведенческие) расстройства, например, отсутствие чувства самосохранения, демонстративность, импульсивность.
Диагностика болезни
Диагноз заболевания ставится на основе проведения таких мероприятий:
- Сбор анамнеза — в каком возрасте появились первые симптомы, как проходили роды, имелись ли в семье больные эпилепсией, как протекало умственное и физическое развитие ребёнка.
- Неврологическое обследование — беседа с ребёнком, использование специальных тестов и шкал для выявления задержки в умственном развитии.
- Электроэнцефалография — анализ электрической активности в головном мозге. У больных обнаруживаются диффузные медленные острые волны. Процедура проводится в течение целого дня в состоянии бодрствования и покоя, что позволяет отследить частоту приступов.
- МРТ и КТ — послойное обследование строения мозга с целью обнаружения повреждения его структур.
Лечение заболевания Леннокса-Гасто предполагает использование нескольких методов.
Медикаментозная терапия
Цель терапии — снижение частоты приступов. Препараты подбираются индивидуально с учётом минимального возникновения побочных эффектов.
Назначаются следующие противосудорожные препараты:
- Клобазам;
![]()
- Руфинамид;
- Дивальпроат натрия;
- Ламотриджин;
- Топирамат;
- Депакин;
- Карбамазепин;
Зачастую применение одного средства не даёт нужных результатов. Препараты назначаются комплексно, и приём строго контролируется лечащим врачом.
Хирургическое лечение
В случае отсутствия положительного эффекта после проведения медикаментозной терапии, проводится хирургическое лечение с использованием различных методов:
- Имплантация стимулятора блуждающего нерва. Выполняется посредством вшивания в области ключицы специального устройства с электродом, передающим электрические импульсы на блуждающий нерв. Этот метод позволяет снизить количество
![]()
припадков. Как показывает практика, более чем у половины пациентов благодаря этому методу частота приступов заметно снижается. - Имплантация RNS-стимулятора под кожу головы, который генерирует электроды в область мозга. Электроды непрерывно фиксируют электрическую активность мозга, и в момент начала приступа стимулятор подаёт электрические импульсы, которые подавляют эпилептический очаг.
- Каллозотомия — рассечение мозолистого тела, которое представляет собой пучок нервов, соединяющий между собой полушария мозга и передающий эпилептические импульсы из одной части мозга в другую. После проведённой операции приступы не пропадают совсем, но становятся менее интенсивны, т. к. импульсы не генерируются из одного полушария в другое. Обычно такое лечение применяется в случаях неконтролируемых эпилептических припадков.
Особенности питания
Очень часто наряду с другими терапевтическими методами применяется кетогенная диета. Она представляет собой снижение потребления углеводов и увеличение потребления жиров.
Кроме этого, рекомендуются продукты с низким гликемическим индексом, т. е. те, которые снижают уровень сахара в крови. К ним относятся: фрукты, овощи, бобовые, цельнозерновые продукты, обезжиренное молоко.
Во время такой диеты врач должен контролировать возможность уменьшения доз принимаемых препаратов.
Осложнения и прогноз

Заболевание в большинстве случаев имеет неблагоприятный прогноз. Около 10% больных умирают в возрасте десяти лет, это связано с тяжёлыми травмами во время приступов.
Практически у всех больных детей наблюдается умственная отсталость в той или иной степени, половина больных не способны к самообслуживанию.
Также к осложнениям можно отнести:
- устойчивость припадков в связи с резистентностью к лечению;
- сохранность умственного дефекта, который не исчезает;
- расстройство социальной и трудовой адаптации.
Предупредить возникновение данного заболевания невозможно. Основными профилактическими мерами в данном случае можно считать:
- Поддержание высокого качества жизни — здоровый образ жизни, полноценный восьмичасовой сон, правильное питание, избегание влияния стрессовых факторов.
- Квалифицированное лечение на протяжении всей жизни. Ни в коем случае нельзя самостоятельно менять схему лечения или прерывать его.

Синдром Леннокса-Гасто, или миоклонически-астатическая эпилепсия– эпилептическая энцефалопатия, которой болеют только дети.СЛГ сопровождается атипичными абсансами, тоническими, атоническими или астатическими судорогами, задержкой умственного развития и медленными спайками и волнами на электроэнцефалограмме.
Причины синдрома Леннокса-Гасто (СЛГ)
Смертность от СЛГ равна 3% в случаях, когда средний период наблюдения за детьми составлял 8,5 лет, а когда этот период продлевали в среднем до 9,7 лет, от болезни умирали приблизительно 7 человек из 100. Однако смерть наступала чаще из-за несчастных случаев, случившихся во время эпилептического припадка.
Начало заболевания можно заметить по эпизодам внезапных падений, которые случаются у маленьких детей. В школьном возрасте признаками заболевания служат продолжающиеся приступы падения вместе с нарушениями в поведении. Эти симптомы позже сочетаются с участившимися судорогами, эпизодами эпилептического статуса, прогрессивными нарушениями интеллекта и нарушением личности. Дети с синдромом Леннокса-Гастов 6 лет, как правило, переносят большую или меньшую задержку умственного развития.

По мере взросления ребёнка меняется тип судорог – приступы падения в основном сменяются парциальными, сложными парциальными или вторично-генерализованными припадками. В подростковом возрасте наиболее распространены сложные парциальные эпилептические припадки.
Считается, что видимую причину болезни обнаружить невозможно, однако чаще всего причинами заболевания являются аномальное развитие мозга, его генетические заболевания (например, метаболические заболевания с поражением центральной нервной системы или туберозный склероз), перинатальные травмы нервной системы, в том числе асфиксия, преждевременные роды или низкий вес при рождении, а также тяжёлые инфекции ЦНС – энцефалит, менингит, краснуха и токсоплазмоз.
Как правило, СЛГ поражает детей в возрасте 2-8 лет, и врачи выделяют фокус-группу – дети 4-6 лет. В редких случаях синдром Вест, диагностируемый у младенцев до 1 года, трансформируется в СЛД, причём заболевание протекает по одному из 2-х вариантов:
- Синдром Веста с инфантильными спазмами плавно переходит в тонические приступы. Латентный период отсутствует, болезнь перетекает в СЛГ.
- Детские спазмы, характерные для синдрома Веста, исчезают, психомоторное развитие ребёнка улучшается, что также заметно на ЭЭГ. Но по прошествии некоторого времени (этот период у каждого больного – свой), наступают неожиданные приступы падений и атипичные абсансы. ЭЭГ выявляет рост диффузионной пик-волновой активности.

Тонические, миоклонические и атонические (негативный миоклонус) пароксизмы вызывают приступы неожиданных падений. В это время некоторые больные находятся в сознании, у других оно на миг отключается. Судорог не наблюдается; дети после падения тут же встают на ноги. Тем не менее, повторяющиеся приступы могут стать причиной тяжёлых травм и даже инвалидности.
Тонические приступы бывают аксиальными, проксимальными и тотальными; реже –симметричными или чётко латерализованными. Во время приступа неожиданно сгибаются шея и туловище, руки поднимаются вверх, а ноги разгибаются. Мышцы лица сокращаются, глаза непроизвольно вращаются. Наступают гиперемия лица и апноэ. Такие приступы случаются как в дневное, так и в ночное время.
Большая часть больных СЛГ страдают пирамидной недостаточностью, координаторными нарушениями, у них наблюдается небольшое снижение интеллекта. Последний признак можно заметить в раннем возрасте во время симптоматических форм, а в криптогенных формах он развивается только после приступа.
Врачебный прогноз у заболевших синдромом Леннокса-Гасто тяжёл. Только 10-20% заболевших находятся под медикаментозным наблюдением. Болезнь без тяжёлых патологий структуры головного мозга с миоклоническими приступами легче всего поддаётся лечению. Частые тонические приступы и сильное снижение интеллекта требует более долгого и сложного лечения. Однако лечение СЛГ возможно и необходимо – это единственный путь к выздоровлению.

Специальность: Невролог, Эпилептолог, Врач функциональной диагностики Стаж 15 лет / Врач первой категории.
Читайте также:




