Метипред для лечения эпилепсии
Этиология. Предположительно идиопатическая форма эпилепсии. В 5% случаев роландическая эпилепсия может трансформироваться в синдром псевдо-Леннокса (СПЛ). Данная форма эпилепсии признана большинством детских эпилептологов, но пока еще не введена ни в одну международную классификацию.
Диагностические критерии. Заболевание впервые было описано Aicardi & Chevrie в 1982 году. СПЛ дебютирует в дошкольном возрасте, преимущественно, от 1,5 до 6 лет. Для СПЛ характерен полиморфизм приступов:
- фокальные моторные,
- атонические (негативный миоклонус),
- атипичные абсансы,
- вторично - генерализованные тонико – клонические,
- миоклонические (активный миоклонус),
- эпилептический статус.
Основной вид приступов - короткие фокальные моторные в виде фаринго – оральных, гемифациальных или фацио - брахиальных пароксизмов с нарушением речи, гиперсаливацией, возникающие при засыпании или пробуждении. Этот тип приступов характерен для роландической эпилепсии и наблюдается обычно в дебюте заболевания. Далее частота приступов катастрофически нарастает; присоединяются атонические пароксизмы и атипичные абсансы. Фокальные атонические приступы (негативный миоклонус) проявляются в виде пассивных кивков, наклонов туловища, ступенчатых приседаний, и наконец, мгновенных падений без судорог. Частота данных приступов достигает нескольких десятков в сутки, нарастая в период после пробуждения пациентов. Вторично - генерализованные судорожные приступы (обычно ассоциированные со сном) и миоклонические пароксизмы (активный миоклонус) встречаются у 1/3 больных СПЛ.
При неадекватном лечении нередко возникает эпилептический статус атипичных абсансов или фаринго – оральных приступов со снижением двигательной (ступор) и психической активности, анартрией, гиперсаливацией, атоническими феноменами (кивки, наклоны). Статус чаще наступает в утреннее время (после пробуждения) и может продолжаться часами.
Неврологическое обследование нередко выявляет динамическую атаксию, интенционный тремор, дисметрию, брадикинезию, скандированную речь. Выраженность данных симптомов флюктуирует, нарастая в период учащения приступов. Во время активного периода заболевания у всех пациентов констатируются выраженные когнитивные и речевые расстройства, резко затрудняющие их обучение [Hahn, 2000].
ЭЭГ при СПЛ характеризуется сочетанием региональной и диффузной эпилептиформной активности. Основной ЭЭГ паттерн – высокоамплитудная эпилептиформная активность острая – медленная волна (идентичная по морфологии доброкачественным эпилептиформным паттернам детства), возникающая, преимущественно, в передне - центральных отведениях и имеющая высокий индекс представленности. Характерно усиление эпилептиформной активности в медленном сне с появлением продолженной диффузной активности, возникающей в результате феномена вторичной билатеральной синхронизации. Результаты, полученные при нейровизуализации, неспецифичны. Возможно появление умеренной кортикальной и субкортикальной атрофии. Локальные нарушения, как правило, отсутствуют.
Определение инвалидности при СПЛ следует проводить с осторожностью и решать индивидуально. Во время активного периода заболевания пациенты обычно не способны посещать массовую школу ввиду высокой частоты приступов и выраженных когнитивных нарушений. После 10 лет активность заболевания уменьшается, однако, у ряда больных когнитивные и речевые расстройства остаются, что существенно снижает их способность к обучению и социальную адаптацию.
Терапия. Стартовое лечение начинается с производных вальпроевой кислоты. Назначается конвульсофин в дозе 900-2000 мг/сут (30-70 мг/кг/сут) в 2-3 приема. Вальпроаты особенно эффективны при миоклонических, генерализованных судорожных приступах и атипичных абсансах.
Препарат второго выбора – топирамат. Топамакс назначается с постепенным увеличением дозы до 75-200 мг/сут (3-7 мг/кг/сут) в 2 приема. Он эффективен при фокальных моторных, генерализованных судорожных и атонических приступах. В единичных случаях высокие дозы препарата могут приводить к парадоксальному учащению приступов.
Препарат третьего выбора – леветирацетам. Кеппра назначается с постепенной титрацией дозы до 750-2500 мг/сут (30-60 мг/кг/сут) в 2 приема. Препарат эффективен при фокальных моторных, генерализованных судорожных и миоклонических приступах. Hoppen и соавт. (2003) показали высокую эффективность кеппры в средней дозе 50 мг/кг/сут у больных синдромом псевдо-Леннокса в комбинации с вальпроатами.
При неэффективности монотерапии следует переходить к комбинированному лечению. Оптимальные комбинации в лечении СПЛ: вальпроаты + сукцинимиды, вальпроаты + топирамат, вальпроаты + леветирацетам, а также указанные препараты в комбинации с бензодиазепинами. Присоединять суксилеп к базовым АЭП рекомендуется сразу после неэффективности монотерапии. Суксилеп назначается в дозе 500-1000 мг/сут (20-35 мг/кг/сут) в 3 приема. Такая комбинация особенно эффективна в отношении псевдогенерализованных приступов (атонические, миоклонические, атипичные абсансы) и продолженной диффузной эпилептиформной активности на ЭЭГ.
Следующая комбинация – вальпроаты, топирамат или леветирацетам + бензодиазепины. Назначается фризиум в дозе 10-30 мг/сут (0,5-1,0 мг/кг/сут) в 2-3 приема. Нередко добавление фризиума приводит к резкому урежению приступов и улучшению когнитивных функций. Однако обычно этот эффект кратковременный. Фризиум рекомендуется в период учащения приступов, а также при развитии эпилептического статуса фокальных моторных приступов или атипичных абсансов.
Применение препаратов карбамазепина и барбитуратов не рекомендуется ввиду возможности учащения приступов.
При отсутствии эффективности от АЭП назначаются стероидные гормоны (синактен - депо, преднизолон, метипред, дексаметазон). Синактен – депо назначается, начиная с 0,1 мг внутримышечно 1 раз в сутки с постепенным наращиванием по 0,1 мг 1 раз в 2-5 дней до дозы 1,0 мг в сутки. Продолжительность терапии - 1-2 мес. с постепенным снижением. Средняя доза преднизолона – 2 мг/кг/сут перорально однократно утром. Возможно применение дексаметазона по схеме: дексаметазон в дозе 2 мг/кг/сут перорально в течение 1 нед., затем 1 мг/кг/сут еще 2 нед., затем переход на альтернирующий метод терапии – 1 поддерживающая доза (например, 0,5 мг/кг/сут) раз в 2-3 дня в течение 3-6 мес.
Прогноз при СПЛ следует проводить с осторожностью. Во время активного периода заболевания приступы обычно резистентны к проводимой терапии. В связи с этим, необходимы высокие дозы препаратов, нередко с включением бензодиазепинов и гормонов. После 9-и летнего возраста частота приступов постепенно снижается; после 11 лет постепенно блокируется эпилептиформная активность; и к началу пубертатного периода пациенты достигают полной электро – клинической ремиссии [Мухин К.Ю. и соавт., 2001; Fejerman и соавт., 2000]. Выраженность когнитивных нарушений также уменьшается с возрастом. Однако у ряда больных когнитивные и речевые расстройства остаются, не смотря на прекращение приступов, что существенно снижает их способность к обучению и социальную адаптацию.
Основные принципы лечения эпилептических припадков
В.А. Карлов
Кафедра неврологии и нейрохирургии ММСИ
C реди неврологических заболеваний мозга эпилепсия занимает третье место. Однако это не только неврологическая проблема. С эпилепсией также имеют дело педиатры, психиатры, нейрохирурги. Уже это показывает клиническую значимость проблемы эпилепсии.
Не только частота эпилепсии (около 1% популяции) определяет ее важность, но и ряд других значимых факторов: преимущественное начало в детском возрасте, прогредиентность течения большинства ее форм, неблагоприятное влияние припадков на мозг, частота изменений психики, потенциальная опасность припадков для больных и окружающих и т.д.
Другим не менее существенным аспектом эпилепсии следует считать социальный. Жизнь больного с припадками делится на два периода - до и после диагноза "эпилепсия" [1], ибо диагноз "эпилепсия" обладает ярко выраженной негативной социальной значимостью. У больных эпилепсией много проблем, касающихся работы, вождения машины, климата в семье, потомства и т.д.
Особую остроту представляет эпилепсия у женщин - проблема беременности, риск рождения больного ребенка, влияние антиэпилептических препаратов на организм матери и плода и т.д.
Эпилептические разряды, даже субклинические, оказывают отрицательное действие на внимание, когнитивные функции, темп работы и др. Хронический прием антиэпилептических препаратов (АЭП), в свою очередь, неблагоприятно воздействует на печень, кровь, желудочно-кишечный тракт, обмен веществ и в особенности на нервную систему, вызывая седацию или, наоборот, возбуждение (последнее - чаще у детей), снижение внимания, памяти и т.д. Таким образом, очевиден и не менее важен второй аспект проблемы эпилепсии - социальный. Это делает понятным участие социологов, психологов, реабилитологов в разработке проблемы эпилепсии.
Наконец, есть еще и третий аспект - нейрофизиологический. Эпилептическое возбуждение является "меченым", оно имеет патогномоничный эклектрографический коррелят и поэтому может быть хорошо прослежено при регистрации электроэнцефалограммы.
Вследствие этого эпилепсия в течение нескольких последних десятилетий была и продолжает оставаться моделью для изучения функциональной организации головного мозга человека [2, 3].
Терапевтический аспект проблемы - один из важнейших и труднейших. За последние десятилетия в клиническую практику введены десятки новых АЭП. Конечно, это существенно расширило возможности медикаментозной терапии эпилепсии, однако и породило ряд новых проблем, главная из них - лекарственное взаимодействие: индукция или, наоборот, ингибирование одного препарата другим, стимулирующий, аддитивный, позитивный и негативный эффекты взаимодействия.
Крупным вкладом в проблему эпилепсии явилось внедрение в клиническую практику методов определения уровня АЭП в сыворотке крови.
В целом стратегия лечения эпилепсии за последние годы не изменилась: раннее начало, комплексность, непрерывность, длительность, преемственность. Однако тактика претерпела определенные изменения. Главным все же остается максимальная индивидуализация терапии.
Лечебный аспект тесно связан с диагностическим. При обращении больного с первым припадком следует прежде всего решить, о каком припадке идет речь - эпилептическом или неэпилептическом. Проблема дифференциального диагноза эпилептических припадков с неэпилептическими, в особенности демонстративными (так называемыми псевдоприпадками), а иногда и другими (пароксизмальные формы мышечной дистонии прежде всего), весьма непроста.
В наиболее крупных клиниках мира применяют видео- и электроэнцефалотелемониторирование.
Рассмотрим тактику терапии отдельных форм эпилепсии и эпилептических припадков.
Фебрильные судороги, аффект-респираторные приступы, парасомнии следует рассматривать как факторы риска по эпилепсии. Они могут требовать назначения АЭП при наличии нескольких других факторов риска.
Если установлено, что припадок эпилептический, необходимо исключить текущий церебральный процесс (опухоль мозга, абсцесс и т.д.). Для этого надо, помимо врачебного осмотра больного, включая неврологический статус и электроэнцефалографию (ЭЭГ), провести эхоэнцефалоскопию и компьютерную (а при необходимости и магнитнорезонансную томографию головы). Если текущий церебральный процесс исключен, следующим этапом в диагностико-терапевтическом алгоритме должно быть принятие решения о целесообразности начала медикаментозной антиэпилептической терапии. Это также может представить немалые трудности. Недаром в Международной лиге борьбы с эпилепсией есть специальный комитет по первому эпилептическому припадку. К сожалению, он не выработал однозначных рекомендаций [4]. На основании нашего опыта мы можем рекомендовать двухступенчатость подхода: вначале следует выяснить, был ли первый эпилептический припадок спонтанным или спровоцированным. При таких факторах провокации, как высокая температура (фебрильные судороги у детей), депривация сна, алкоголизация, просмотр телевизионных передач, следует не спешить с назначением АЭП, а сделать все для предупреждения факторов провокации. Так, при лихорадочных заболеваниях у детей необходимо назначать жаропонижающие средства. При "телевизионном" припадке роль телевизионного воздействия легко подтверждается энцефалографией: под влиянием ритмических световых мельканий в ЭЭГ регулярно возникает эпилептическая активность. В этих случаях следует рекомендовать смотреть телевизор с расстояния не менее 3 м, либо пользоваться телевизором с небольшим экраном (менее 25 см по диагонали). Абсолютно надежно действует просмотр телевизионных программ одним глазом, для чего практично применение очков с ширмой на одной из линз [5].
При провокации приступа депривацией сна больной должен категорически соблюдать режим сна - бодрствования, исключить недосыпание, запрещается работа в ночную смену. Больному надо состоять под наблюдением, необходим также динамический электроэнцефалографический контроль.
Следует подчеркнуть, что наличие эпилептических разрядов в ЭЭГ у больного с отсутствием эпилептических припадков не может рассматриваться как повод для начала антиэпилептического лечения, так как, во-первых, диагноз эпилепсии является клиническим (у многих больных с эпилептическими припадками в ЭЭГ нет эпилептических проявлений) и, во-вторых, справедлив афоризм: "лечить надо больного, а не энцефалограмму". Наличие эпилептической активности в ЭЭГ у лиц без припадков следует рассматривать как фактор риска эпилепсии . Эти лица нуждаются в динамическом наблюдении.
Второй ступенью в алгоритме действия врача в тех случаях, когда диагностирован первый неспровоцированный эпилептический припадок , должно быть решение о выжидательной тактике, либо начале антиэпилептической медикаментозной терапии. Как уже было сказано, определенных рекомендаций на этот счет нет.
Авторы в своей практике руководствуются учетом факторов риска эпилепсии. Основными факторами риска являются: отягощенный перинатальный анамнез, органические поражения мозга в постнатальном периоде (черепно-мозговая травма, менингит и т.д.), пароксизмальные состояния в детстве (фебрильные припадки, аффект-респираторные судороги, ночные страхи и кошмары), задержка развития, наличие очаговой неврологической симптоматики, эпилептическая активность в ЭЭГ.
При нескольких факторах риска противоэпилептическое лечение надо начинать немедленно. Для более точного определения степени риска нами с помощью компьютерной обработки большого количества данных разработаны специальные таблицы, в которых дано количественное определение (удельный вес) различным значимым анамнестическим, клиническим и электроэнцефалографическим признакам, суммирование которых позволяет вывести "индекс эпилептичности", т.е. определить степень риска эпилепсии. Риск III степени является показанием к назначению медикаментозного антиэпилептического лечения [6].
В случае, когда решение о начале лечения принято, дальнейший шаг зависит от типа припадка и формы эпилепсии. Если определить их оказалось невозможным, средством первой очереди выбора являются соли вальпроевой кислоты, которые могут быть применены практически без риска неблагоприятного воздействия на те или иные виды припадков и в то же время потенциально высокоэффективны при идиопатической эпилепсии с абсансами и/или генерализованными судорожными припадками, обладают значительной эффективностью при парциальных припадках.
Обычно применяется натриевая соль вальпроевой кислоты - депакин, конвулекс, апилепсин, ацедипрол и др. или кальциевая соль (конвульсарт). Дозы на 1 кг массы тела в сутки значительно варьируют - от 15 до 50 мг. Иногда наблюдаются побочные действия: увеличение массы тела, желудочно-кишечные расстройства.
Если удалось определить тип припадка и форму эпилепсии, производится выбор адекватного АЭП.
Так, при генерализованных бессудорожных припадках - абсансах (приступы кратковременного - секунды - отключения сознания с прерыванием действия, иногда элементарным автоматизмом - перебирание руками, бормотание и т.д.) с наличием характерного ЭЭГ патерна - генерализованных синхронных симметричных разрядов комплексов пик-волн 3 Гц-средством первой очереди выбора является вальпроат, второй - сукцинимиды: этосуксимид, пикнолепсин, суксилеп. Дозы на 1 кг массы тела составляют 15-40 мг в сутки.
Основные побочные явления со стороны желудочно-кишечного тракта: боли в подложечной области, тошнота, реже рвота и др.
При генерализованных судорожных припадках у больных с идиопатической эпилепсией средством первой очереди выбора является вальпроат (депакин), второй - карбамазепин (тегретол, финлепсин), хотя есть сведения, что эффективность карбамазепина может превышать таковую вальпроата [7].
Дозы карбамазепина - 10-20 мг на 1 кг массы тела в сутки. Основные неблагоприятные явления: головокружение, атаксия (неустойчивость при ходьбе), нистагм и др., которые значительно менее выражены при применении ретардных форм (финлепсин-ретард 200 мг, 400 мг, тегретол 200 мг, 400 мг). При непереносимости или неэффективности этих препаратов средствами следующей очереди выбора могут быть фенитоин и барбитураты: фенобарбитал, майсолин (гексамидин, примидон).
Фенитоин (дифенин, дилантин) применяют в дозе 5-6 мг на 1кг массы тела в сутки. Основные неблагоприятные явления схожи с таковыми у карбамазепина. Кроме того, фенитоин часто вызывает гиперплазию и кровоточивость десен.
Фенобарбитал (за рубежом - фенобарбитон и метилфенабарбитал) применяется в дозах 1,5 - 3 мг на 1 кг в сутки.
Несмотря на то, что при генерализованных припадках, идиопатической эпилепсии фенобарбитал оттеснен на 3-4-й план, он остается средством первой очереди выбора при младенческих судорогах и эпилептическом статусе, связанном с внезапным прекращением приема фенобарбитала. Кроме того, его широкое применение связано с низкой стоимостью.
При симптоматической эпилепсии (известна этиология, подтверждается наличие очагового поражения мозга) или криптогенной (имеется очаговость, но этиология органического поражения неизвестна), парциальных припадках - простых (без изменения сознания), сложных (с изменением сознания) и вторично генерализованных припадках (с присоединением генерализованных судорог) средством первой очереди выбора является карбамазепин (тегретол, финлепсин).
Однако, возможно, эффективность карбамазепина не превышает таковой вальпроата натрия и дифенина.
Как правило, трудную терапевтическую задачу представляют миоклонические формы эпилепсии , при которых миоклонии (быстрые подергивания мышц) являются одним из главных проявлений заболевания: доброкачественная и тяжелая миоклоническая эпилепсия раннедетского возраста, эпилепсия с миоклоническими абсансами, миоклонически-астатическая эпилепсия, ювенильная абсансная эпилепсия, миоклонус-эпилепсия.
Средством первой очереди выбора признан вальпроат (депакин), может быть эффективен клоназепам (дозы: 0,1 - 0,15 мг на 1 кг в сутки), антелепсин, иногда другие АЭП или их комбинации (см. далее). Напротив, карбамазепин при этих формах эпилепсии противопоказан.
В настоящее время общепризнанной тактикой лечения эпилептических припадков является монотерапия, т.е. лечение одним препаратом . При отсутствии должного эффекта от препарата первой очереди выбора переходят к препарату следующей очереди выбора. И лишь при безуспешности этих попыток назначают комбинацию из двух, иногда трех АЭП.
Однако это вряд ли правильно для некоторых форм эпилепсии, которые относятся главным образом к специфическим детским формам. Так, при детском спазме (синдром Уэста), характеризующемся началом в 0,5 - 1,5 года и своеобразными приступами так называемых пропульсивных припадков (саламовы судороги): наиболее типичны кивки с подбрасыванием рук в сочетании с характерными изменениями ЭЭГ (гипоаритмия - медленная сноподобная активность), необходимо сразу же одновременно назначать глюкокортикоиды или АКТГ и АЭП. Чаще применяют синтетический аналог АКТГ - синактен-депо внутримышечно по 1 мг на год жизни ребенка (первые инъекции - 0,1 - 0,2 - 0,3 мг) с интервалами в 2, 3, 5 и 10 дней. Дозы АКТГ - 20 - 60 Ед в сутки, преднизолона - от 2 до 10 мг на 1 кг в сутки.
Из АЭП предпочтительнее вальпроат (депакин) или нитразепам. В резистентных случаях может помочь внутривенное введение иммуноглобулина по 0,4 мг на 1 кг в сутки [8].
Следующей формой эпилепсии, при которой оправдана стартовая полипрагмазия, является миоклонически-астатическая эпилепсия у детей раннего возраста, при которой миоклонические подергивания наиболее часто сочетаются с падением ребенка, иногда абсансами или тоническими приступами.
Средством первой очереди выбора является вальпроат (депакин). В большинстве случаев, однако, требуется его сочетание с этосуксимидом, а при наличии и генерализованных судорожных припадков - с барбитуратами, лучше - примидоном. При статусе абсансов добавляется АКТГ.
Крайне труден для лечения синдром Леннокса-Гасто (возраст дебюта - 26 лет). Характерна триада припадков: судорожных тонических, атипичных абсансов (сочетание выключения сознания с миоклониями век, периооральной мускулатуры и генерализованными синхронными разрядами пик-волн 1,5 - 2,5 в 1с в ЭЭГ и внезапных падений, а также задержка психического развития).
Применяется сочетание вальпроата, карбамазепина и бензодиазепинов (нитразепам, клоназепам, клобазам). Более трех препаратов одновременно также, как и максимальные дозы, назначать нельзя.
Полипрагмазии требуют и некоторые другие миоклонические формы эпилепсии, в частности эпилепсия с миоклоническими абсансами. Назначается комбинация вальпроата (депакина) и этосуксимида. У некоторых больных действенна комбинация вальпроата с барбитуратами (фенобарбитал, примидон) или банзодиазепинами (нитразепам, диазепам и др.).
Среди новых АЭП наиболее перспективны вигабатрин, ламотриджин, окскарбазепин, тиагабин, фелбамат, топирамин [9].
Наибольшее применение уже нашли окскарбазепин, вигабитрин, ламотриджин.
Основной действующий метаболит окскарбазепина отличается от соответствующего метаболита карбамазепина меньшей токсичностью, и поэтому препарат лучше переносится.
Вигабатрин (сабрил) имеет ГАМК-подобную структуру, но отличается иным способом действия, оказывая противоэпилептическое влияние путем необратимого подавления ГАМК-трансаминазы, тем самым повышая содержание ГАМК в ЦНС. Вигабатрин практически не подвергается в организме биотрансформации. Это имеет два важных последствия для клиники: 1) отсутствие гепатотоксичности; 2) при совместном применении с другими АЭП вигабатрин не оказывает существенного влияния на их содержание в плазме крови.
Дозы: 20 - 50 мг на 1 кг в сутки. Препарат назначают при парциальных и вторично генерализованных припадках.
В последнее время показана его эффективность в отношении наиболее трудно курабельных эпилептических приступов падения, в частности при синдроме Леннокса-Гасто .
Ламотриджин (ламиктал) относится к препаратам с иным типом действия, чем у других АЭП. Он не усиливает ГАМК-опосредованное торможение, но оказывает подавляющее влияние на возбудительные трансмиттеры (глютамат) или ингибирует соответствующие рецепторы.
Препарат также наиболее эффективен при сложных парциальных и вторично генерализованных припадках, а также эпилептических приступах падения у детей (при синдроме Леннокса-Гасто прежде всего). Дозы: 5-8 мг на 1 кг в сутки. При одновременном использовании с другими АЭП ламотриджин незначительно укорачивает период полужизни энзиминдуцирующих препаратов (фенобарбитал, карбамазепин, фенитоин, примидон), но период полужизни самого ламотриджина существенно удлиняется вальпроатом, что требует снижения доз ламотриджина, так как это чревато явлениями интоксикации.
Следует еще раз подчеркнуть, что добиться результатов при назначении АЭП, адекватных форме эпилепсии и типу припадков, можно только при применении должных дозировок, корригируемых контролем уровня препарата в крови.
Начинать лечение надо с малых доз, которые повышают постепенно.
Ниже приведена таблица доз и терапевтического уровня в крови основных АЭП.
Дозы и терапевтические уровни в сыворотке крови основных АЭП
Некоторые заболевания могут протекать с определенной устойчивостью к лекарствам, т. е. не реагировать на введение препаратов. В таких случаях, как правило, прибегают к использованию глюкокортикоидов. Одним из таких препаратов является "Метипред". Для чего назначают данное лекарство и что оно из себя представляет?
Что это за препарат?
"Метипред" относится к группе синтетических глюкокортикостероидов, т. е. является искусственно синтезированным аналогом гормонов. Он обладает противовоспалительной активностью, оказывает противоаллергическое действие, снимает отек, несколько понижает активность иммунитета, восстанавливает метаболические нарушения.
Механизм его действия основан на реакции со специфическими рецепторами, расположенными во многих тканях. За счет связи с ними образуются специальные белки, которые отвечают за регуляцию большинства жизненно важных процессов.
Лекарство оказывает воздействие на все виды обменных процессов в организме.
Так как препарат относится к группе глюкокортикостероидов, его назначают только в определенных случаях, когда базисные средства, показанные для лечения данного заболевания, становятся неэффективными.
В каких же случаях можно использовать "Метипред"? Для чего назначают его при том или ином заболевании?
Показания к назначению
Какие же заболевания требуют для своего излечения назначения гормональных препаратов? При каких недугах показан "Метипред"? Для чего прописывают это лекарство?
В первую очередь назначение данного лекарства обязательно при системных заболеваниях соединительной ткани. В качестве таковых выступают: системная склеродермия, системная красная волчанка, все васкулиты, дерматомиозит. В данных случаях гормон способствует уменьшению воспалительного процесса, восстановлению обмена в пораженных тканях.
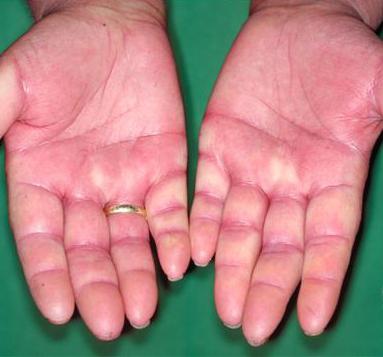
В ревматологии также широко используют "Метипред". Показания к применению – острые воспалительные заболевания суставов: артриты подагрической и псориатической этиологии, остеоартроз, бурситы, синовиты, болезнь Бехтерева. Основной эффект препарата при данных заболеваниях – противовоспалительный и анальгезирующий.
Можно использовать "Метипред" при бронхиальной астме и различных хронических аллергических заболеваниях.
Дозирование препарата
В каких же дозах показано использование "Метипреда"? Следует помнить, что при назначении данного лекарства, как и других гормонов, нужно учитывать циркадные ритмы организма, а также функцию коры надпочечников. Доза для каждого пациента подбирается индивидуально.
Суточное количество гормона лучше всего принимать утром (обычно советуют пить всю дозу в промежутке от 6 до 8 часов утра, либо же делить ее на два приема – в 8 и 12 часов). Подобное дозирование наблюдается у всех гормональных препаратов. Не является исключением и "Метипред".
Таблетки принимаются непосредственно во время еды или после нее. У детей доза определяется согласно возрасту и массе тела.
Норма препарата составляет от 4 до 50 мг в сутки. Более высокая доза (до 1 г) показана пациентам с системными заболеваниями соединительной ткани крайней степени тяжести. Особое внимание следует уделить назначению препарата перед трансплантацией органа реципиенту или при экстракорпоральном оплодотворении.
Побочные эффекты
При грамотном дозировании препарата и соблюдении всех предписаний врача при его приеме побочные эффекты практически никогда не развиваются. Однако следует помнить о том, что при нарушении условий приема могут развиться достаточно тяжелые состояния. К чему же может привести использование данного лекарства?

"Метипред" в первую очередь оказывает негативное воздействие на эндокринную систему. Может наблюдаться снижение толерантности к глюкозе, развитие синдрома Иценко-Кушинга, задержка полового развития (при назначении детям).
Пищеварительная система может реагировать на введение препарата развитием тошноты и рвоты, изменением стула, панкреатитом, язвой, вплоть до кровотечения и перфорации стенки желудка.
Влияние "Метипреда" на сердечно-сосудистую систему проявляется в виде аритмий, брадикардии, ухудшения состояния организма при сердечной недостаточности.
Со стороны нервной системы чаще всего наблюдается делириеподобное состояние, развитие психозов, паранойи, бессонницы и головокружения.
Противопоказания
Когда же не стоит использовать данное лекарство? "Метипред" можно использовать только на протяжении короткого промежутка времени. При более длительном приеме список противопоказаний значительно расширяется.
С осторожностью используют лекарство при таких заболеваниях пищеварительного тракта, как язвы, гастриты, неспецифический язвенный колит, перенесенные операции на ЖКТ.

Многие инфекционные заболевания также входят в перечень относительных противопоказаний, поскольку неизвестно, как организм отреагирует на введение гормонального препарата. Другим условием, запрещающим использование гормонов, является их иммуносупрессивное действие.
Не стоит использовать препарат при сахарном диабете, ожирении.
Дети и беременные относятся к категории с абсолютными противопоказаниями к использованию "Метипреда". Назначать его можно только лишь в случае, когда имеется значительная угроза жизни.
Взаимодействие с другими лекарствами
Как известно, многие препараты могут усиливать, ослаблять или нейтрализовать действие другого лекарства. Как же реагирует "Метипред" при параллельном назначении других препаратов?
Использование данного лекарства с индукторами печеночных ферментов приводит к уменьшению концентрации действующего вещества в крови (усиливается его метаболизм).
Если назначать лекарство "Метипред" с диуретиками, значительно возрастает риск развития сердечной недостаточности и гипокалиемии.
Пульс-терапия "Метипредом" при одновременном назначении сердечных гликозидов на порядок увеличивает риск развития желудочковой экстрасистолии.
Не стоит использовать вместе метилпреднизолон и антикоагулянты, так как ухудшается лечебный эффект последних.
Прием препарата с алкоголем и нестероидными средствами приводит к увеличению риска развития язв ЖКТ.
" Метипред" снижает эффективность вводимого инсулина и гипотензивных препаратов.
Указания к использованию
В каких же лекарственных формах может существовать "Метипред"? Для чего назначают каждую из них? Давайте рассмотрим эти вопросы подробнее.
"Метипред" (таблетки) прописывают при нетяжелых формах заболеваний, а также при отсутствии противопоказаний к пероральному приему.
Лиофилизат – специальная форма препарата, представляющая собой порошок для разведения и внутривенного введения. Применяют преимущественно при тяжелых формах заболеваний, а также при оказании экстренной помощи.

Полученный раствор рекомендуется использовать сразу. Если необходимо хранить его некоторое время, то это следует делать при температуре от 15 до 20 градусов. При более низких показателях можно держать приготовленный препарат не более суток.
С целью безопасности здоровья пациента рекомендуется параллельно использовать антациды (для защиты слизистой оболочки).
Перед использованием лекарства обязательно следует проконсультироваться с лечащим врачом относительно дозы препарата и частоты его приема.
"Метипред" в лечении бесплодия
В гинекологии, как и в других областях медицины, также используют "Метипред". Для чего назначают данное лекарство?
Основное использование препарата – подавление иммунитета при экстракорпоральном оплодотворении.
ЭКО – процедура, суть которой заключается в выделении у женщины яйцеклетки, оплодотворении ее в пробирке мужским сперматозоидом и внедрении получившейся зиготы в матку.

"Метипред" при ЭКО показан для некоторого подавления иммунитета. Его рекомендуют применять несколько дней после переноса зиготы в полость матки. Это делается для того, чтобы исключить возможность отторжения организмом “инородного объекта”.
При благоприятном исходе происходит имплантация зародыша в слизистую матки, образование плаценты и внутриутробный рост зародыша.
"Метипред" при ЭКО показан всем женщинам. При наличии противопоказаний к его использованию лучше отказаться от экстракорпорального оплодотворения.
Некоторые заболевания женской половой системы могут потребовать назначения гормонов. "Метипред" в гинекологии изредка применяют для лечения лейкоплакии и некоторых воспалительных процессов.
Лечение системных заболеваний
При данных состояниях, как правило, прибегают к так называемой пульс-терапии. Суть данного метода лечения заключается в следующем: на протяжении краткого периода времени (обычно 1-2 суток) пациенту вводится довольно большая доза препарата, а затем в течение нескольких недель (в зависимости от тяжести и типа заболевания) – поддерживающая доза лекарства.
Например, при лечении системных васкулитов, данная схема выглядит следующим образом: препарат "Метипред" сначала вводится в дозе до 1000 мг, после чего пациент переводится на поддерживающую терапию (80-100 мг).
Такая схема получила свое распространение благодаря высокой эффективности.
Введение большой дозы способствует "стрессу" заболевания и развитию так называемого сбоя метаболизма. При этом пораженному организму проще восстановить нормальные реакции, чем без такого сильного воздействия. Также за счет большой дозы удается ингибировать большинство иммунных клеток.
Пульс-терапия может дополняться цитостатиками для достижения более выраженного иммуносупрессивного эффекта.
Важность использования препарата
Данное лекарство невозможно просто купить в аптеке. Только лечащий врач может выдать рецепт на "Метипред". Показания к применению должны быть вескими (например, системные воспалительные заболевания). Только в данном случае провизор сможет выдать необходимый вам препарат.
Другой особенностью лекарства является то, что при его длительном использовании возможно привыкание или появление абстинентного синдрома.
Он развивается в том случае, когда длительно и в больших дозах назначался "Метипред". Параллельно наблюдается угнетение собственных гормонов, вырабатываемых в надпочечниках. В данном случае не следует сразу же отменять препарат. Рекомендуется на протяжении длительного времени постепенно снижать дозу. Только при таких условиях нормальный синтез гормонов сможет восстановиться.
Читайте также:


