Вариабельность ритма при эпилепсии

активность мв-креатинфосфокиназы сыворотки крови
спектральные параметры вариабельности ритма сердца: общая мощность спектра
нарушение сердечной деятельности
дети младшего школьного возраста
1. Воронина Л.П. Биохимические и генетические маркеры эндотелиальной дисфункции / Л.П. Воронина, И.В. Нуржанова, О.С. Полунина, Т.А. Уклистая, Е.А. Полунина, Т.В. Прокофьева // Монография. – Астрахань, 2010. – 147 с.
2. Горст В.Р. Адаптационный потенциал системы кровообращения /Н.А. Горст, В.Р. Горст, М.В. Горст, Е.Г. Львова, М.Ж. Амреева //Естественные науки. Журнал фундаментальных и прикладных исследований. – Астрахань: Из-во АГПУ. – 2002. — №4. – С. 53 — 55.
3. Доронина Т.Н. Состояние спектральных параметров ритма сердца у детей младшего школьного возраста/ Т. Н. Доронина, О.В. Степанов, Н. С. Черкасов, Е. В. Сосиновская// Вестник ВолгГМУ.-2015.-№3(55).-С.44-46.
5. Котлукова Н.П. Современные представления о некоторых механизмах формирования легочной гипертензии и миокардиальной дисфункции при врожденных пороках сердца у детей первого года жизни/ Н. П. Котлукова, Е. В. Неудахин, О.И. Артеменко, О.А. Кисленко, И.Г. Морено//Российский вестник перинатологии и педиатрии.-2012.-№4(1).-С.19-25.
Несмотря на успехи в исследовании больных эпилепсией, остаются актуальными проблемы, касающиеся состояния кардиоваскулярной системы при этой неврологической патологии. Известно, что патологические изменения в коре головного мозга, подкорковых образований и вегетативных центрах при эпилепсии могут вызывать нарушения сердечной деятельности. Эти расстройства на фоне эпиприпадков проявляются изменениями артериального давления, нарушениями ритма.
Принято считать, что в понятие нарушения сердечной деятельности (СД) входят изменения ритма и проводимости сердца, миокардиальная и клапанная дисфункции, хроническая сердечная недостаточность, легочная гипертензия и их сочетания [5].
Патогенетические механизмы этих нарушений остаются мало изученными. Существует мнение, что даже в межприступном периоде эпилепсии нарушается энергообеспеченность мозга и сердца. В связи с этим используются биохимические показатели и инструментальные методы исследования.
Определение активности МВ фракции креатинфосфокиназы сыворотки крови является важным критерием оценки нарушений, происходящих в миокарде [1,4], так как изоформа МВ креатинфосфокиназы преобладает в кардиомицитах и может считаться специфическим маркером повреждения сердечной мышцы.
Известно, что сердечный ритм отражает фундаментальные соотношения в функционировании кардиоваскулярной системы, являясь основным маркером функционирования вегетативной обеспеченности. Вариабельность ритма сердца (ВРС) — неинвазивный, стандартизированный метод количественной оценки естественных изменений интервалов времени между сердечными сокращениями (длительность кардиоциклов) нормального синусового ритма сердца. Считается, что снижение показателей ВРС свидетельствует о нарушении вегетативного контроля сердечной деятельности и является неблагоприятным фактором для прогноза заболевания. Исследование основных спектральных параметров вариабельности ритма сердца (ВРС) позволяет оценивать не только состояние вегетативной нервной системы, но и энергообеспеченность организма [2,6].
В связи с этим в современных условиях актуальным является изучение взаимосвязи основных параметров вариабельности ритма сердца и активности миокардиальной фракции креатинфосфокиназы.
Цель: установить взаимосвязь основных параметров вариабельности ритма сердца с уровнем активности МВ-креатинфосфокиназы у детей с нарушением сердечной деятельности при эпилепсии.
Материалы и методы исследования
Результаты исследования и их обсуждение
Нами проанализированы анамненстические данные у наблюдаемых детей. Из анамнеза установлено, что в первые часы жизни после рождения у исследуемой группы диагностировались синдром угнетения ЦНС в 4 (6,9%) случаях, кардиореспираторные расстройства – в 6 (10,3%), судорожный синдром – в 7 (8%), повышение нервно-рефлекторной возбудимости – в 11 (19%).
Дебют эпилепсии определялся в возрасте до 1 года у 9,5% случаев, в 1-3 года у 43,5% , 4-7 лет – у 18,5%, в 8-11 лет – у 28,5% больных. Приступы протекали от простых парциальных, кратковременных в любое время суток (с частотой 1 раз в 2-5 месяцев) до частых (1-3 раза в месяц) первично и вторично-генерализованного характера.
На основании данных опроса и анализа медицинской документации выявлено, что у родителей детей с эпилепсией имеется отягощенная наследственная предрасположенность по сердечно-сосудистой патологии в 12 (20,7%) случаях, по эпилепсии — в 9 (15,5%) семьях.
Наблюдения проводились за детьми в межприступном периоде. Отмечались чаще всего жалобы на утомляемость – 36 (62%) больных, боль в сердце различного характера – 23(39,6%), сердцебиение при эмоциональной и физической нагрузках – 19(32,6%), кратковременное головокружение –15(25%), реже на ощущение нехватки воздуха при эмоциональной или физической нагрузке-7(12%) пациентов.
Границы относительной сердечной тупости у наблюдаемых детей были в пределах возрастной нормы. Аускультативно обнаружены: дыхательная аритмия – у 32(55%), тахикардия – у 23 (39 %), брадикардия – у 13(22%), приглушенность тонов сердца – у 19(32,6%), негрубый систолический шум на верхушке и реже в V точке – у 17(29%), единичные экстрасистолы – у 11(19%) пациентов.
При анализе ЭКГ исследования установлены нарушения процессов реполяризации — в 40(68%) случаях, умеренно выраженная синусовая тахикардия — у 14(24%), синусовая брадикардия — у 12(20,7%), неполная блокада правой ножки пучка Гиса у 8(13,8%), нарушение внутрижелудочковой проводимости — у 5(8,6%) детей. Наджелудочковая и желудочковая экстра-систолия отмечалась нечасто — в 4(6,9%) случаях.
Выявленные нарушения ритма на электрокардиограммах сопоставлены с данными холтеровского мониторирования ЭКГ. При этом количество экстрасистол (желудочковых и наджелудочковых) колеблется от 3000 до 5500 в сутки, с преобладанием их в дневное время.
Оценка сердечной деятельности основывались на общепринятых критериях. Это позволило выделить две подгруппы: с нарушением СД 37(63,8%) и без таковых -21(36,2%).
В подгруппе без нарушений сердечной деятельности оказались дети с симптоматической (височная 12(32,4%), лобная 2(5,4%)) и идиопатическими генерализованными формами эпилепсии – 13(35,1%). Длительность заболевания составила 1 — 2,5 года, дебют заболевания отмечался в возрасте 6-10 лет в виде простых парциальных, кратковременных приступов, в любое время суток с частотой 1-2 раз в 6 месяцев при фокальной эпилепсии и тонико-клонических приступов с частотой припадков 1-2 раза в год или реже при идиопатических формах эпилепсии. У этих пациентов клинико-анамнестические данные и показатели МВ-КФК, ЭКГ, ВРС существенно не отличались от здоровых детей.
В подгруппе с нарушением сердечной деятельности оказались дети с фокальными (лобная – 4(10%), височная – 21(56,6%) и генерализованными 12(32,4%) формами эпилепсии. Длительность заболевания 3-5 лет и более, дебют заболевания в возрасте от 1 до 3 лет. В большинстве случаев течение эпилепсии имело волнообразный характер с учащением приступов на фоне снижения дозы препарата, ОРВИ, обострения соматической патологии или в связи с другими причинами. При объективном обследовании выявлены: приглушенность тонов сердца – у 10 (47,6%), дыхательная аритмия – у 7(33%), брадиаритмии — у 4 (19,4%), тахиаритмия — у 3 (14,3%), негрубый систолический шум в V точке, а также явления экстрасистолии – у 4(19,4%) детей.
По результатам ЭКГ установлено: синусовая брадиаритмия — в 5(13,5%) случаях, синусовая тахиаритмия – в 6(16,2%), изменение метаболизма в миокарде – в 4(10,8%), неполная блокада правой ножки пучка Гиса – в 3(8,1%), нарушение внутрижелудочковой проводимости – в 3(8,1%), желудочковая экстрасистолия – в 2(5,4%), инверсия зубца Т в грудных отведениях, регистрируемая более чем в трех отведениях – в 10(27%), депрессия сегмента ST — в 4(10,8%) случаях.
При оценке биохимических показателей установлено значительное увеличение содержания МВ-КФК–0,54 [0,45-0,60] мккат/л в сыворотке крови по сравнению с предыдущей группой, (р Источник
Обычно, когда говорят об эпилепсии, ее диагностике и предсказании очередного приступа, подразумевают измерение электрической активности головного мозга. Однако есть работы, которые связывают это заболевание с активностью сердца, что упрощает диагностику. Группа японских исследователей нашла способ его предсказать за несколько минут до того, как он произойдёт. Этого времени должно хватить для того, чтобы успеть принять меры. Работа опубликована в журнале IEEE Transactions in Biomedical Engineering.
Обычно около семидесяти процентов пациентов с эпилепсией могут существовать без приступов благодаря современным противоэпилептическим препаратам. Однако остальные тридцать процентов живут в постоянной опасности. Ведь очередной припадок может настигнуть внезапно в то время, когда рядом не окажется никого, кто бы мог оказать помощь.
Схема работы сенсора
На основе этой работы учёные предлагают запустить в производство комплекс для постоянной носки. В нём сенсор кардиограммы снимает ЭКГ, передаёт данные на мобильный телефон в режиме онлайн по Bluetooth, а специальная программа анализирует их в режиме реального времени и подаёт сигнал тревоги перед приступом.
Ученым же из Университета Кейс Вестерн Резерв удалось установить связь между эпилепсией и изменениями сердечного ритма, причем диагностировать эпилепсию и установить риск SUDEP (внезапной неожиданной смерти при эпилепсии, SUDEP — sudden unexpected death in epilepsy) можно по ЭКГ в отсутствие приступа. Исследование опубликовано в Journal of Neurophysiology.
Вверху: ЭКГ контрольной группы, внизу: ЭКГ эпилептиков.
Учёные отобрали для исследования 91 ребенка и подростка с генерализованной эпилепсией и 25 неврологически нормальных детей. У всех снималась кардиограмма во сне, во время медленноволнового сна. Ни у кого из эпилептиков в это время не наблюдался приступ.
Медикам удалось увидеть, что дыхательная синусовая аритмия — ускорение сердечного ритма во время вдоха и замедление во время выдоха — более выражена у пациентов с эпилепсией и вообще, в среднем, у эпилептиков сердечная мышца сокращается реже. Разницы в артериальном давлении в обеих группах не было никакой.
Оказалось, что пилотное исследование, проведенное неврологами, позволяет ещё и диагностировать эпилепсию на ранних стадиях — до припадков. У нескольких детей из неврологически здоровой группы кардиограмма показывала только что открытые признаки эпилепсии. И, как оказалось, позже у этих детей действительно начались припадки.
Авторы делают оговорку, что им удалось найти диагностически важную корреляцию, но пока не знают, где причина, а где — следствие.
— говорит Роберто Фернандес Галан, доцент кафедры электротехники и компьютерных наук в Кейт Вестерн Резерв и старший автор исследования.
Кафедра невропатологии и нейрохирургии и кафедра функциональной диагностики Иркутского государственного института усовершенствования врачей
В настоящее время абсолютно достоверным методом диагностики цереброгенных аритмий сердца по праву считается синхронная амбулаторная регистрация ЭЭГ и ЭКГ [15, 23]. Особую ценность этот метод имеет при дифференциации цереброгенного и кардиогенного генеза приступов утраты сознания [8, 11].
Мы использовали синхронную регистрацию ЭЭГ и ЭКГ, ограниченную по времени (обычно 15-30 мин), при обследовании 20 больных ПГЭ и 24 больных ПЭ в состоянии покоя и при проведении функциональных проб (гипервентиляция в течение 3 мин, высокочастотная и низкочастотная фотостимуляция ).
За время регистрации нарушения ритма в виде предсердных и желудочковых экстрасистол отмечались у 11 (45,8%) больных ПЭ и 2 (10%) больных ПГЭ. У 9 (37,5%) больных ПЭ и 1 (5%) больного ПГЭ преждевременные сердечные сокращения имели характер изолированных спонтанных нарушений, а у 2 (8,3%) больных ПЭ и 1 (5%) больного ПГЭ были отчетливо связаны с пароксизмальными разрядами на ЭЭГ (см. рисунок), за которыми они следовали с некоторой задержкой (2-3 с). Эта задержка, по нашему мнению, была обусловлена временем, необходимым для возбуждения под влиянием пароксизмальной активности полисинаптических надсегментарных вегетативных центров, и временем распространения импульса от этих центров до эффекторных органов (в данном случае сердца). Н.А. Белоконь и соавт. [2] отметили, что у 46% детей с хронической непароксизмальной тахикардией возвратного типа возникновению гетеротопной активности на ЭКГ также предшествовали пароксизмальные разряды на ЭЭГ, и расценили это как отражение дисфункции диэнцефально-стволовых структур мозга.
Как показал спектральный анализ ЭЭГ до и после преждевременных сердечных сокращений, у больных со спонтанной экстрасистолией в период, предшествующий экстрасистоле, как правило, определялись разной степени выраженности изменения спектрального состава ЭЭГ в виде смещения максимума мощности спектра в сторону низких (3-7 Гц) или высоких (14-16 Гц) частот.
Таким образом, полученные данные свидетельствуют о непосредственной связи нарушений сердечного ритма у больных эпилепсией с пейсмекерной активностью систем лимбико-ретикулярного комплекса и пароксизмальными событиями.
Модулирующее влияние вегетативной нервной системы в развитии, поддержании и прекращении многих аритмий сердца подтверждено многими исследованиями. В то же время конкретные механизмы этого влияния на развитие и течение аритмий очень сложны и далеко не полностью изучены [12].
Из вышесказанного следует, что дисфункция надсегментарных вегетативных центров с чрезмерной активацией церебральных эрготропных систем, сопровождающаяся увеличением мощности спектра сердечного ритма в диапазоне VLF и перемещением его на первые позиции относительно диапазонов LF и HF, может считаться одним из значимых факторов аритмогенеза при эпилепсии. Напротив, сохранность паттерна регуляции вегетативного тонуса, близкого к нормальному с максимумом мощности спектра в диапазонах HF и LF, является относительно благоприятным фактором для возможного развития нарушений ритма и проводимости сердца.
Полученные результаты свидетельствуют также о том, что в возникновении различий доминирующих нарушений сердечного ритма у больных ПГЭ и ПЭ значительную роль могут играть имеющиеся у них различия в вегетативной регуляции деятельности сердца. Так, отмечаемая у больных ПГЭ склонность к тахикардии и тахиаритмии может рассматриваться как результат преимущественной активации симпатической нервной системы, а характерные для больных ПЭ нарушения проводимости по типу блокад - как проявление повышенной активности парасимпатической нервной системы.
Таким образом, основываясь на результатах нашего исследования, можно сделать вывод, что нарушения ритма и проводимости сердца являются одним из характерных и патогномоничных для эпилепсии симптомов, существующих у больных постоянно, а не только в момент эпилептического приступа.
Тесная взаимосвязь сердечных аритмий и эпилепсии обусловлена сложным комплексом патофизиологических механизмов, среди которых ведущая роль принадлежит дисфункции надсегментарных вегетативных центров с преимущественной активацией симпатического или парасимпатического отдела вегетативной нервной системы. В числе значимых аритмогенных факторов, существенно влияющих на частоту и выраженность аритмий у больных эпилепсией, следует назвать, во-первых, наличие у них органических изменений головного мозга, во-вторых, частоту эпилептических припадков, в-третьих, дисфункцию надсегментарных вегетативных центров с активацией церебральных эрготропных систем. Усиление влияния какого-либо одного или сочетание двух либо всех трех перечисленных факторов обусловливает увеличение частоты и выраженности аритмий у больных эпилепсией.
В заключение следует подчеркнуть, что диагностика цереброгенных аритмий сердца представляет достаточно сложную задачу и требует активного использования современных инструментальных методов, таких как компьютерная эхоэнцефалография, холтеровский мониторинг ЭКГ и синхронная регистрация ЭЭГ и ЭКГ.
Журнал неврологии и психиатрии N 9-2000, стр.16-20
1. Антюфьев В.Ф., Гузовский Е.В., Мякотных В.С. Кардиология 1992; 4: 17-20.
2. Белоконь Н.А., Школьникова М.А., Белозеров Ю.М. и др. Кардио-логия 1990; 6: 67-79.
3. Дабровски Б. Суточное мониторирование ЭКГ. М 1998; 164- 194.
4. Карлов В.А. Эпилепсия. М 1990.
5. Кушаковский М.С. Аритмии сердца. М 1998.
6. Либис Р.А., Прокопьев А.Б., Коц Я.И. Кардиология 1998; 3: 49- 51.
7. Соловьева А.Д., Данилов А.Б., Хаспекова Н.Б. Вегетативные расстройства. М 1998; 44-85.
8. Beauregard L., Fabiszewski R., Black C.H. et al. Am J Cardiol 1991; 68: 1067-1072.
9. Blumhardt L.D., Smith P.E., Owen L. Lancet 1986; 1: 1051-1056.
10. Howell S.J., Blumhardt L.D. J Neurol Neurosurg Psychiat 1989; 52: 795-798.
11. Jallon P. Rev Neurol (Paris) 1997; 153: 173-184. 12. Jurkovicova O., Cagan E. Vnitr Lek 1991; 37: 501-506.
13. Keller C., Williams A. J Neurosci Nurs 1993; 25: 349-355.
14. Linzer M., Yang E.H., Estes N.A. 3rd et al. Ann Intern Med 1997; 126: 989-996.
15. Massetani R., Strata G., Galli R. et al. Epilepsia 1997; 38: 363-369.
16. Natelson B.H., Chang Q. Neurol Clin 1993; 11: 293-308.
17. Natelson B.H., Suarez R.V., Terrence C.F. et al. Arch Neurol 1998; 55: 857-860.
18. Oppenheimer S.M., Wilson J.X., Guiraudon C. et al. Brain Res 1991; 550: 115-121.
19. Oppenheimer S.M., Kedem G., Martin W.M. Clin Auton Res 1996; 6: 131-140.
20. Persinger M.A., Psych C. Int J Biometeorol 1995; 38: 180-187.
21. Ptacek L. J. Neuromuscul Disord 1997; 7: 250-255.
22. Steffensen I.E., Nielsen H.V., Laursen L.C. et al. Ugeskr Laeger 1992; 154: 870-871.
23. Wilder Smith E., Wilder Smith A. Schweiz Med Wochenschr 1995; 125: 2237-2243.

Почти 50 лет назад исследователи наблюдали вегетативные реакции на стимуляцию мозга у больных , перенесших эпилептический судоржный припадок при местной анестезии. Различные кортикальные и подкорковые регионы стимуляции вызывали целый ряд вегетативных изменений, это заставляло предположить, что эпилептические очаги могут также дифференцированно влиять на вегетативную активность. Соответственно, фокальные разряды в височной и лобной коре могут приводить к автономным нарушениям, влияющим на артериальное давление и сердечный ритм, дыхание и потливость. Исследования на животных показали, что даже минимальная эпилептогенная активность (одиночные спайки) может изменять нейронные разряды, направляющиеся к сердечной мышце и вызывать аритмии. Также следует отметить, что пациенты с эпилепсией, по сравнению со здоровыми людьми, проявляют межвидовые автономные аномалии (при электродермальной активности и вариабельности сердечного ритма, ВСР). В частности, пациенты с эпилепсией, по сравнению со здоровыми лицами, имеют значительно более высокую амплитуду и латентность симпатической кожной реакции и демонстрируют последовательное снижение ВСР (показатель парасимпатического тонуса вагуса). Внезапная неожиданная смерть, связанная с эпилепсией (SUDEP), может быть ключевым следствием связанной с эпилепсией вегетативной дисфункции.
Большинство генетических причин эпилепсии обусловлены мутациями в генах, кодирующих ионные каналы, что приводит к измененной нейронной функции в центральной нервной системе. Они также могут влиять на метаболические функции, и эти же самые мутации, скорее всего, влияют на функцию вегетативной нервной системы. Синдром Туретта (Tourette Syndrome )- это нейропсихиатрическое расстройство развития, характеризующееся непроизвольными двигательными и звуковыми симптомами.
Есть много свидетельств, что приступы эпилепсии у пациентов часто связаны с колебаниями эмоциональных, психических и физиологических состояний, встречающихся в повседневной жизни больных и что тревога является общим триггером приступов. И , действительно , из всех непосредственных причин судорог наиболее важными являются фобии, волнение и тревога.
Увеличение количества и интенсивности тиков у пациентов с синдромом Туретта при обсуждении чувствительных тем или во время состояний физического возбуждения, связанных со значительным эмоциональным нарушением, наблюдалось у пациентов , страдающих этим заболеванием. Вероятно, здесь также существует взаимодействие с аффективной нестабильностью и связанными с этим проблемами поведения , поскольку при синдроме Туретта распространены сопутствующие нейропсихиатрические синдромы, такие как синдром дефицита внимания с гиперактивностью (СДВГ), ADHD) , расстройство аутистического спектра (ASD), аффективное расстройство и обсессивно-компульсивное расстройство (OCD).
Эпилептологи идентифицировали два типа нейронов , окружающих эпилептический фокус: нейроны первой группы, являются высокоэпилептонными и постоянно участвуют в нейронных кластерах. Этот класс нейронов показывает отсутствие затухания разрядов нейронной активности во время состояния операнта (повышенное внимание). Окружающими их нейронами являются нейроны второй группы, которые содержат как эпилептогенные, так и неэпилептогенные нейроны. Интересно, что оперантное обусловлевание может уменьшить разряд одной клетки в нейронах 2-й группы.
Обычно, когда говорят об эпилепсии, ее диагностике и предсказании очередного приступа, подразумевают измерение электрической активности головного мозга. Однако есть работы, которые связывают это заболевание с активностью сердца, что упрощает диагностику. Группа японских исследователей нашла способ его предсказать за несколько минут до того, как он произойдёт. Этого времени должно хватить для того, чтобы успеть принять меры. Работа опубликована в журнале IEEE Transactions in Biomedical Engineering.

Обычно около семидесяти процентов пациентов с эпилепсией могут существовать без приступов благодаря современным противоэпилептическим препаратам. Однако остальные тридцать процентов живут в постоянной опасности. Ведь очередной припадок может настигнуть внезапно в то время, когда рядом не окажется никого, кто бы мог оказать помощь.
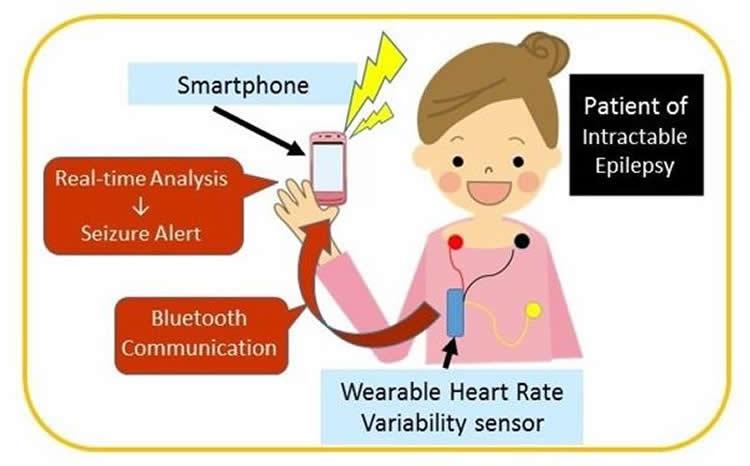
Схема работы сенсора
На основе этой работы учёные предлагают запустить в производство комплекс для постоянной носки. В нём сенсор кардиограммы снимает ЭКГ, передаёт данные на мобильный телефон в режиме онлайн по Bluetooth, а специальная программа анализирует их в режиме реального времени и подаёт сигнал тревоги перед приступом.
Ученым же из Университета Кейс Вестерн Резерв удалось установить связь между эпилепсией и изменениями сердечного ритма, причем диагностировать эпилепсию и установить риск SUDEP (внезапной неожиданной смерти при эпилепсии, SUDEP — sudden unexpected death in epilepsy) можно по ЭКГ в отсутствие приступа. Исследование опубликовано в Journal of Neurophysiology.
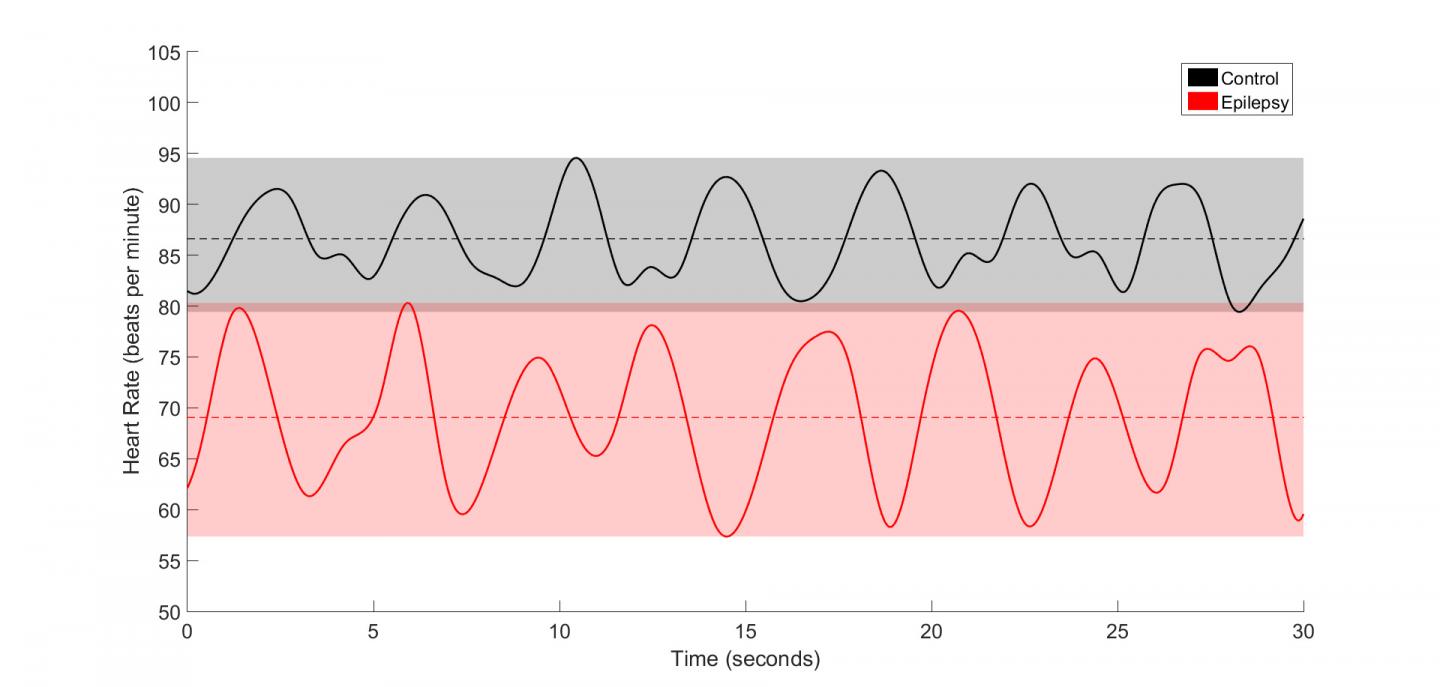
Вверху: ЭКГ контрольной группы, внизу: ЭКГ эпилептиков.
Учёные отобрали для исследования 91 ребенка и подростка с генерализованной эпилепсией и 25 неврологически нормальных детей. У всех снималась кардиограмма во сне, во время медленноволнового сна. Ни у кого из эпилептиков в это время не наблюдался приступ.
Медикам удалось увидеть, что дыхательная синусовая аритмия — ускорение сердечного ритма во время вдоха и замедление во время выдоха — более выражена у пациентов с эпилепсией и вообще, в среднем, у эпилептиков сердечная мышца сокращается реже. Разницы в артериальном давлении в обеих группах не было никакой.
Оказалось, что пилотное исследование, проведенное неврологами, позволяет ещё и диагностировать эпилепсию на ранних стадиях — до припадков. У нескольких детей из неврологически здоровой группы кардиограмма показывала только что открытые признаки эпилепсии. И, как оказалось, позже у этих детей действительно начались припадки.
Авторы делают оговорку, что им удалось найти диагностически важную корреляцию, но пока не знают, где причина, а где — следствие.
— говорит Роберто Фернандес Галан, доцент кафедры электротехники и компьютерных наук в Кейт Вестерн Резерв и старший автор исследования.
Анализ вариабельности сердечного ритма является комплексным показателем, который позволяет оценить функциональные взаимоотношения между сердечно-сосудистой и нейро-гуморальной системами. В первую очередь методику используют для оценки функциональных возможностей здоровых людей. Изучение ВСР широко применяется для обследования спортсменов и космонавтов. Тем не менее этот способ хорошо показал себя в ранней диагностике функциональных нарушений сердечно-сосудистой системы. Еще одними преимуществами данного средства являются его простота (в отличие от холтер-ЭКГ) и дешевизна.
Почему появляется вариабельность ритма и что это такое
Простыми словами, вариабельность сердечного ритма — это изменения интервалов между систолами, которые появляются вследствие влияния внешних и внутренних факторов. Этот показатель измеряется путем изучения длительности периодов сокращений сердца в течение определенного промежутка времени. Обычно для этого используют данные электрокардиографии, а именно расстояния между зубцами R (т. е. самые высокие пики на ЭКГ).

Помимо измерения интервалов R-R, также применяется исследование N-N — промежутков между нормальными сокращениями. Это особенно важно при наличии у пациента аритмии.
Известно, что человек является открытой системой. Т. е. любые изменения внешней или внутренней среды отражаются на функционировании органов и клеток. Это и выступает основой вариабельности — изменчивости показателей жизнедеятельности под влиянием тех или иных факторов.
Сердце в этом плане — весьма чуткий орган. Его работа очень сильно зависит от общего состояния человека, в особенности от нервной и эндокринной систем.
Улавливая изменения в работе организма, нервная система соответствующим образом регулирует деятельность сердца. Симпатический отдел повышает частоту сердцебиений, увеличивает силу сокращений миокарда. В свою очередь блуждающий нерв действует обратным путем — снижает упомянутые показатели.
Таким образом, анализ ВСР позволяет выявить изменения сердечной деятельности и, следовательно, нарушения в работе регулирующих систем.
Методы диагностики
Несмотря на простоту методики, ее обычно применяют в условиях стационара. Это связано с тем, что нужен строгий контроль за нагрузкой на организм. Только в этом случае можно сделать точные выводы о состоянии сердца и его реакции на различные стимулы.
Существует несколько способов диагностики вариабельности.
В зависимости от длительности регистрации:
- кратковременные — до 5 минут (используются при массовых или поликлинических обследованиях);
- средней продолжительности — до 2 часов (при функциональных пробах);
- многочасовые и суточные записи (применяются в ходе операций и в отделениях реанимации).
Чаще всего используют пятиминутные записи.
В зависимости от целей выделяют:
- параллельные исследования (как средство медицинского контроля, например, во время операции);
- специализированные (применяются для обследования всего организма в функциональной диагностике).
Что касается собственно способов анализа, тут также есть немалый арсенал.
- Статистические методы — непосредственные измерения промежутков R-R и N-N, затем определяют такие значения, как стандартное отклонение интервалов или коэффициент вариации.
- Геометрические методы (вариационная пульсометрия) заключаются в вычислении вероятностных характеристик полученных данных и построении графических гистограмм.
- Кореляционная ритмография заключается в графическом отображении последовательности кардиоинтервалов. При этом становятся хорошо заметны выпадения или, наоборот, дополнительные сокращения сердца.
- Спектральные методы позволяют определить разночастотные показатели сердечного ритма. Благодаря этому становится возможным изучение воздействия регулирующих органов. Однако следует помнить, что наличие аритмий может значительно искажать результаты этого анализа.
Дальнейшая тактика действий
Важно помнить, что значения изменчивости сердечного ритма зависят не только от состояния здоровья, но и от многих других факторов:
- пол (у женщин обычно выше);
- возраст (у пожилых людей некоторые параметры проводящей системы сердца снижены);
- вес (ожирение способствует понижению вариабельности);
- занятия спортом (тренированный человек обладает большими резервами изменчивости);
- эмоциональное состояние (ухудшает показатели).
Также на ВСР негативно влияют нарушения сна, питания, прием некоторых медикаментов и загрязненная окружающая среда. В общем, все то, что нарушает работу организма, особенно его регуляторных систем.
Вариабельность ритма резко снижена при некоторых острых патологиях:
- ишемическая болезнь сердца (в том числе инфаркт миокарда);
- артериальная гипертензия;
- острые нарушения мозгового кровообращения (инсульты);
- болезнь Паркинсона.
В меньшей степени показатель снижается при хронических болезнях:
- синдром перетренированости;
- хроническая сердечная недостаточность в начальной степени;
- рассеянный склероз;
- ортостатическая гипертензия;
- метаболические кардиомиопатии (при сахарном диабете, инфекционных и аутоиммунных заболеваниях);
- расстройства адаптации.
Перспективным может быть использование данной методики в отношении плода и новорожденных для оценки риска синдрома внезапной смерти.
Выводы
Исследование вариабельности сердечного ритма — это простой и надежный способ изучения состояния важнейших систем органов.
Дешевизна методики позволяет использовать её для проведения массовых скрининговых обследований с целью выявления скрытых патологий на ранних стадиях. Широкое применение в спорте и космонавтике подчеркивает профилактическую сущность данного средства, что соответствует современным веяниям в медицине.
Если у вас обнаружено нарушение данного показателя, это еще не говорит о необходимости лечения. Попробуйте такие простые средства коррекции, как спорт и отдых. Вместе с тем вариабельность сердечного ритма может быть резко снижена при некоторых острых патологиях, вроде инфаркта миокарда или инсульта.
Для подготовки материала использовались следующие источники информации.
Читайте также:


