Амплитуда пд нерва что это
- Все (14)
Вообще, безусловно, хорошо, если невролог может сам работать с электронейромиографом и знает не только биофизические аспекты процедуры, но и умеет оценивать полученные результаты. Однако, тема электронейромиографии достаточно обширна, по ней имеется ряд руководств, как отечественных, так и зарубежных, поэтому данная тема не претендует на полноту раскрытия материала. При рассмотрении отдельных заболеваний, где это необходимо, будут указываться наиболее типичные изменения по ЭНМГ.
В основе электронейромиографии (ЭНМГ) лежит применение электрической стимуляции нерва с последующим анализом параметров, регистрируемых с иннервируемой мышцы или с самого нерва. Это комплекс исследований для оценки работы мышц и качества передачи нервных импульсов по периферическим нервам и проводящим путям головного и спинного мозга. Метод применим для исследования любого доступного периферического нерва, но в практике чаще исследуют срединный, локтевой, большеберцовый, малоберцовый, седалищный, лицевой, межреберные нервы, поскольку топография других нервов затрудняет стимуляцию их в двух точках, что является неизменным условием для проведения процедуры. Достаточно эффективный и безопасный метод для установки места повреждения (сдавления, травмы и др.) периферического нерва.

Различают две разновидности электронейромиографии:
- спонтанная ЭНМГ – регистрируется активность мышц и нервных волокон в состоянии покоя или при возбуждении
- вызванная ЭНМГ – регистрируется потенциал, который возникает при воздействии на мышцу электрическим током.
Для регистрации используются различные электроды, которые могут быть накожными и инвазивными (игольчатыми). Для понимания сути процесса можно сравнить метод с работой электрика при выявления обрыва в электрической цепи - между парой электродов должен идти ток определённых характеристик. Если ток не идёт - цепь (нерв в нашем случае) оборвана. если сигнал искажен или замедлен - по оценке характеристик можно понять, что не так с цепью и даже получить ответ на вопрос "почему?". Оцениваются следующие показатели:
- параметры вызванных потенциалов (ВП) мышцы и нерва (латентный период, форма, амплитуда и длительность ВП);
- число функционирующих двигательных единиц (ДЕ);
- скорость проведения импульса (СПИ) по двигательным и чувствительным волокнам периферических нервов;
- производится подсчет мотосенсорного и краниокаудального коэффициентов, коэффициентов асимметрии и отклонения от нормы.
Исследование спонтанной активности мышц помогает нам оценить состояние самих мышц и состояние двигательных нервных клеток спинного мозга (миопатия, полимиозит, болезнь мотонейрона, миелопатия и др).
Исследование нервно-мышечной передачи с помощью электромиографии дает информацию о проблемах перехода нервного импульса с периферического нерва непосредственно к мышце-исполнителю (помогает в диагностике миастении и миастенических синдромов).
Исследование двигательных и чувствительных нервов выполняется с использованием электрической или магнитной стимуляции. Оценивается множество параметров, в том числе скорость проведения импульсов по нервам, наличие и местоположение блоков проведения и др. Исследование ценно для диагностики и оценки эффективности лечения полинейропатии, полиневрита, других болезней и травм нервов.
Вызванные зрительные, слуховые и соматосенсорные потенциалы – способ исследования проводящий путей, соединяющих органы чувств с нервной системой. Используются для диагностики рассеянного склероза, патологии слуховых, зрительных нервов и ряда других заболеваний с помощью электромиографии.
М-ответ — вызванный потенциал мышцы, являющийся суммарным синхронным разрядом двигательных единиц мышцы в ответ на электрическое раздражение нерва. Обычно М-ответ регистрируется с помощью накожных отводящих электродов, которые более объективно, чем игольчатые, отражают суммарную активность мышцы. Пластины электродов помещают поперечно расположению волокон. При изучении М-ответа обращают внимание на интенсивность порогового раздражения, форму вызванного потенциала, его амплитуду и длительность. Форма М-ответа зависит от ряда факторов. При биполярном отведении М-ответ имеет негативную и позитивную фазы соответственно прохождению волны возбуждения над обеими электродными пластинками.
Потенциал действия (ПД) нерва обусловлен электрической активностью волокон периферических нервов в ответ на электрическое раздражение нервного ствола. ПД нерва является суммарным потенциалом действия, складывающимся из потенциалов отдельных нервных волокон разного диаметра и степени миелинизации. ПД афферентных волокон регистрируется кольцевыми пальцевыми электродами при стимуляции ствола нерва или, наоборот, со ствола нерва при стимуляции концевых его ответвлений. ПД эфферентных волокон можно регистрировать при избирательной стимуляции двигательных волокон нерва, изолированно от чувствительных волокон. В клинической практике исследование ПД двигательных волокон обычно не проводится в связи с его малой амплитудой, поэтому, говоря о ПД нерва, имеют в виду ПД чувствительных волокон. При изучении ПД нерва обращают внимание на интенсивность порогового раздражения, форму и амплитуду вызванного потенциала.
Уменьшение числа функционирующих ДЕ наблюдается при поражении центрального и периферического двигательных нейронов. При миодистрофии уменьшение количества ДЕ менее значительно.
Изучение вызванных потенциалов мышц, полученных повторной стимуляцией нерва, направлено прежде всего на выявление нарушенийнервно-мышечной синаптической передачи и патологической нервно-мышечной утомляемости. О наличии нервно-мышечного утомления судят по снижению амплитуды М-ответа при повторной электрической стимуляции нерва.
Методика определения СПИ (скорости проведения импульса) по периферическим нервам основана на сопоставлении латентных периодов ВП при электрическом раздражении двух точек нерва, находящихся на некотором расстоянии друг от друга.
Поражение периферического нервного ствола сопровождается наиболее четкими ЭНМГ-изменениями:
- выраженным снижением скорости проведения импульсов по чувствительному и двигательному нервам,
- уменьшением амплитуды потенциала действия пораженного нерва и мышечного ответа (М-ответа) иннервируемых мышц.
При сегментарном поражении спинного мозга, в основном его передних рогов наблюдаются:
- относительно нормальные величины скорости проведения импульсов по чувствительному и двигательному нервам верхних и нижних конечностей,
- значительное повышение амплитуды потенциала действия нервов верхних и в меньшей степени нижних конечностей,
- резкое снижение амплитуды максимального мышечного ответа мышц кистей и стоп
- повышение амплитуды минимальных (пороговых) мышечных ответов,
- резкое падение числа функционирующих двигательных единиц в мышцах верхних и нижних конечностей.
Дифференциально-диагностическим отличием поражения передних рогов спинного мозга от поражения нерва являются диссоциированное снижение амплитуды максимальных мышечных ответов и падение числа функционирующих двигательных единиц при нормальных или повышенных величинах скорости проведения импульсов и амплитуд вызванных биопотенциалов нерва.
Электронейромиография находит все более широкое применение в клинике нервных болезней. Метод наиболее информативен в диагностике заболеваний, сопровождающихся поражением периферических нервов (мононевриты, полиневриты, невральная амиотрофия, полиневропатии при эндокринных и коллагеновых заболеваниях, при которых наблюдается снижение СПИ по двигательным и чувствительным волокнам периферических нервов, снижение амплитуд вызванных потенциалов мышцы и нерва). Электронейромиография нашла применение при изучении супрасегментарных пирамидных и экстрапирамидных поражений. Портативные электромиографы позволяют проводить лечебно-диагностические манипуляции в любом месте и в любое время, существенно облегчают поиск глубоких мышц, например - для топического введения ботулинического токсина с целью коррекции дистонии (в лечении писчего спазма, например).
Потенциал действия нервной клетки
- Потенциал действия нервной клетки
- Ионные механизмы потенциала действия
- Проведение возбуждения по нервным волокнам
- Законы проведения возбуждения
- Типы нервных волокон и их функции
- Все страницы
Проведение ПД по мембране можно сравнить с поджиганием пороховой дорожки: вспыхнувший порох немедленно воспламеняет впереди лежащие частицы, и пламя движется вперёд до конца дорожки.
Продолжительность потенциала действия нервной клетки измеряется единицами миллисекунд (мс).
Потенциалы действия, зарегистрированные двумя электродами, один из которых находится внутри клетки, а другой — в окружающем растворе, представлены на рис. 5-3 и 5-7.
Рис. 5–3. Изменения мембранного потенциала и потенциал действия. Вертикальная стрелка в нижней части рисунка — момент появления раздражающего стимула, на отметке –80 мВ — исходный уровень МП.
Между моментом нанесения раздражения и первым проявлением ПД имеется задержка — латентный период. Латентный период соответствует времени, когда ПД движется по мембране нервной клетки от места раздражения до отводящего электрода. Под действием раздражающего стимула происходит нарастающая деполяризация мембраны — локальный ответ. При достижении критического уровня деполяризации, который в среднем составляет —55 мВ, начинается фаза деполяризации. В эту фазу уровень МП падает до нуля и даже приобретает положительное значение (овершут), а затем возвращается к исходному уровню (фазареполяризации). Фазы деполяризации, овершута и реполяризации образуют спайк (пик) ПД. Длительность спайка составляет 1—2 мс. После спайка наблюдается замедление скорости спада потенциала — (раза следовой деполяризации. После достижения исходного уровня покоя нередко наблюдается фаза следовой гиперполяризации. Эти следовые потенциалы могут длиться десятки и сотни миллисекунд.
В основе изменений мембранного потенциала (МП), происходящих в течение потенциала действия (ПД), лежат ионные механизмы. На рис. 5—7 представлены суммарные ионные токи, протекающие через мембрану нервной клетки в ходе потенциала действия.
Рис. 5-7. Потенциал действия и ионные токи нервной клетки [5|. По оси ординат отложены значения МП (мВ), по оси абсцисс — время (мс)
Локальный потенциал. Раздражение клетки приводит к открытию части Na+-каналов и появлению локального (нераспространяющегося) потенциала.
Фаза деполяризации. При достижении критического уровня деполяризации мембраны (соответствует порогу активации потен-циалозависимых Na+-каналов) начинается лавинообразный процесс открытия большого количества Na+-каналов. В фазу деполяризации происходит массивный вход в клетку ионов Na+ по концентрационному и электрохимическому градиентам.
Овершут. Деполяризация мембраны приводит к реверсии МП (МП становится положительным). В фазу овершута Na+-ток начинает стремительно спадать, что связано с инактивацией потенциало-зависимых Na+-каналов (время открытого состояния –– доли миллисекунды) и исчезновением электрохимического градиента Na+.
Фаза реполяризации. Помимо инактивации Na+-каналов, развитию реполяризации способствует открытие потенциалозависимых K+-каналов. Этот процесс происходит медленнее, чем открытие Na+-каналов, но K+-каналы остаются открытыми более продолжительное время. Выход К+ наружу способствует полному завершению фазы реполяризации.
Следовые потенциалы связаны с длительными изменениями кинетических свойств К+-каналов. Восстановление исходного уровня МП приводит Na+- и K+-каналы в состояние покоя.
В ходе развития ПД происходят изменения возбудимости мембраны нервной клетки.
Абсолютно рефрактерный период. Во время фазы деполяризации и большей части фазы реполяризации ПД клетка находится в абсолютно рефрактерном периоде, в течение которого даже сверхпороговое раздражение не способно вызвать ПД. Этот феномен связан с инактивацией большинства Na+-каналов.
Относительно рефрактерный период. В конце фазы реполяризации, а также во время следовой гиперполяризации клетка способна генерировать ПД только в ответ на сверхпороговые раздражители. Это связано со значительным реполяризующим действием выходящих калиевых токов.
Наличие рефрактерности ограничивает частоту генерации ПД. Физиологическое значение рефрактерности заключается в создании условий для своевременного и полного осуществления восстановительных процессов в нервной клетке. Феномен рефрактерности лежит в основе понятия о функциональной подвижности, или лабильности (Н.Е. Введенский [1] ).
Лабильность — максимально возможная частота генерации ПД для данного типа возбудимой клетки. Лабильность большинства нейронов составляет приблизительно 400 ПД/с, а у интернейронов спинного мозга доходит до 1000 ПД/с.
В нормальных условиях рефрактерность предохраняет нервные клетки от излишне частой генерации ПД. Мутации, гипоксия, механические травмы и другие патологические воздействия приводят к значительным изменениям возбудимости нейронов. Такие нейроны или группы нейронов являются потенциальными источниками возникновения пароксизмальных состояний ЦНС, эпилептических припадков и других неврологических расстройств.
Нервные волокна — аксоны нервных клеток, окружённые оболочкой из олигодендроглиоцитов в ЦНС и шванновских [2] клеток в периферических нервах. Нервные волокна подразделяют на 2 типа — безмиелиновые и миелиновые. Основная функция нервных волокон — проведение ПД. Скорость проведения в миелиновых и безмиелиновых волокнах различна (рис. 5–8) и существенно зависит от диаметра нервных волокон.
Рис. 5–8. Скорость проведения возбуждения в миелиновых и безмиелиновых нервных волокнах разного диаметра [4]. Скорость проведения пропорциональна диаметру нервного волокна и в миелиновых волокнах выше, чем в безмиелиновых.
Безмиелиновые нервные волокна (рис. 5–9А). В покое мембрана аксона (осевого цилиндра) поляризована — положительно заряжена снаружи и отрицательно внутри. При ПД полярность изменяется, и наружная поверхность мембраны приобретает отрицательный заряд. Из-за разности потенциалов между возбуждённым и невозбуждёнными сегментами возникают локальные токи, деполяризующие соседний участок мембраны. Теперь этот участок становится возбуждённым и деполяризует следующий участок мембраны.
Рис. 5–9. Проведение возбуждения в нервных волокнах [7]. А — безмиелиновое волокно (электротоническое проведение), Б — миелиновое волокно (скачкообразное проведение). Миелин, полностью окружая аксон в межузловых промежутках, выступает в роли электрического изолятора, а межклеточная жидкость в перехватах Ранвье [3] — проводник.
Появление так называемых рефрактерных каналов (рефрактерное состояние мембраны после прохождения ПД) предупреждает распространение возбуждения в обратном направлении.
Скорость проведения возбуждения по безмиелиновому нервному волокну в основном составляет 0,5–2 м/с и зависит от диаметра волокна: чем больше диаметр, тем выше скорость проведения ПД (см. рис. 5–8).
Миелиновое нервное волокно (рис. 5–9Б) состоит из осевого цилиндра (аксона), вокруг которого шванновские клетки образуют миелин за счёт концентрического наслаивания собственной плазматической мембраны. Миелин прерывается через регулярные промежутки (от 0,2 до 2 мм) концентрической щелью шириной около 1 мкм, это узлы, или перехваты Ранвье. Таким образом, межузловые сегменты аксона, расположенные между соседними перехватами Ранвье, содержат миелин — электрический изолятор, не позволяющий проходить через него локальным токам, поэтому ПД возникают только в перехватах Ранвье. Другими словами, ПД перемещается вдоль нервного волокна скачками, от одного перехвата Ранвье к другому перехвату (скачкообразное проведение).
Плотность потенциалозависимых Na+?каналов аксолеммы в перехватах Ранвье — до 2000 на 1 мкм2 (в перикарионе — 50–70, в начальном сегменте аксона — 2000, в межузловых сегментах Na+?каналы практически отсутствуют). В силу высокой плотности Na+?каналов перехваты Ранвье характеризуются высокой возбудимостью, а локальные токи достаточно велики для возбуждения соседнего перехвата.
Локальные токи текут от перехвата к перехвату (через внеклеточную жидкость кнаружи от миелина и через аксоплазму внутри аксона) с минимальными потерями.
Энергозатраты нервного волокна на проведение ПД относительно невелики, поскольку возбуждаются только перехваты Ранвье, площадь которых составляет менее 1% общей поверхности мембраны аксона. Поэтому даже после длительных ритмических пачек ПД трансмембранный градиент концентраций ионов практически не изменяется.
В физиологических условиях ПД движутся в одном направлении от места раздражения (ортодромное проведение). ПД, проходящий по нервному волокну, возбуждает следующий, но не предыдущий участок мембраны. Это связано с рефрактерностью предыдущего участка после возбуждения. Проведение в противоположном направлении (антидромное проведение) возможно при травматическом поражении нервных волокон и в редких случаях (аксон–рефлекс).
Нарушение миелинизации нервных волокон приводит к нарушениям проводимости (демиелинизирующие заболевания). При разрушении миелиновой оболочки происходит резкое снижение скорости и надёжности проведения возбуждения по нервам. Наиболее распространённым среди демиелинизирующих заболеваний является множественный склероз, проявляющийся различными параличами и потерей чувствительности.
Бездекрементное проведение возбуждения. Амплитуда ПД в различных участках нерва одинакова, то есть проведение возбуждения по нервному волокну осуществляется без затухания (бездекрементно). Таким образом, кодирование информации осуществляется не за счёт изменения амплитуды ПД, а путём изменения их частоты и распределения во времени.
Изолированное проведение возбуждения. Нервные стволы обычно образованы большим количеством нервных волокон, однако ПД, идущие по каждому из них, не передаются на соседние. Эта особенность нервных волокон обусловлена:
- наличием оболочек, окружающих отдельные нервные волокна и их пучки (в результате образуется барьер, предупреждающий переход возбуждения с волокна на волокно);
- сопротивлением межклеточной жидкости (жидкость, находящаяся между волокнами, имеет гораздо меньшее сопротивление току, чем мембрана аксонов; поэтому ток шунтируется по межволоконным пространствам и не доходит до соседних волокон).
Физиологическая и анатомическая целостность. Необходимым условием проведения возбуждения является не только его анатомическая целостность, но и нормальное функционирование мембраны нервного волокна (физиологическая целостность). В клинике широко применяют различные ЛС, нарушающие физиологическую целостность нервных волокон. Так, эффекты местных анестетиков (новокаин, лидокаин, и др.) основаны на блокаде потенциалозависимых Na+?каналов. Нарушение физиологической целостности чувствительных нервных волокон вызывает анестезию (потерю чувствительности).
При регистрации электрической активности нервного ствола Джозеф Эрлангер и Герберт Гассер в 1937 г. обнаружили составной характер тока действия нервного ствола. На основании полученных данных (диаметр, скорость проведения, функция) разработана классификация (табл. 5—1), в соответствии с которой нервные волокна подразделены на группы А, В и С с дальнейшими градациями ( ? , ? , и т.д.).
Орлов Р.С., Ноздрачёв А.Д. Нормальная физиология : Учебник. - М.: ГЭОТАР-Медиа, 2009. 688 с. - Глава 5. Физиология нейронов. - Потенциал действия. С. 73-78.
[2] Шванн Теодор (Schwann T.), немецкий гистолог и физиолог (1810–1882); вместе с М. Шульце создал клеточную теорию (1839 г.); в 1836 г. открыл пепсин, в 1838 г. опубликовал первую работу по строению миелиновой оболочки.
[3] Ранвье Луи (Ranvier L.), французский патолог (1835–1922). Занимался изучением нервной ткани с применением азотнокислого серебра и хлорного золота. Его именем названы безмиелиновые участки (узловые перехваты) миелинового нервного волокна.
Нервный ствол, или нерв, представляет собой пучок множества нервных волокон, покрытых у позвоночных общими эпителиальной и соединительнотканной оболочками.
Обычно нерв включает в себя волокна различного типа и разного диаметра. Например, седалищный нерв лягушки содержит двигательные волокна (аксоны мотонейронов), чувствительные (аксоны чувствительных клеток) и автономные (аксоны нейронов симпатических ганглиев). Моторные и наиболее толстые чувствительные волокна этого нерва миелинизированы, симпатические — не имеют миелиновой оболочки, покрыты одним слоем шванновских клеток.
Все эти волокна в покое обладают поляризованной поверхностной мембраной[Б47] . Немецкий физиолог Эмиль Дю Буа-Реймон [Б48] показал, что если нерв перерезать и соединить его поврежденную и продольную поверхность с регистрирующим устройством, то отводится потенциал повреждения, или потенциал покоя (ПП)[Б49] . [++512+с374].
Рис. 210041815. Закон силы раздражения в приложении к составной возбудимой структуре (нерву, мышце)..
Почему это происходит? Нервные волокна имеют разный порог раздражения. Когда фиксируется минимальный порог раздражения? Когда возбудились волокна имеющие наименьшие пороги раздражения. При увеличении силы стимула всё большее количество волокон вовлекается в реакцию возбуждения. При достижении максимального порога преодолеваются пороги раздражения всех волокон.
При раздражении нервного стола естественно должно быть воздействие электрическим током через наружные (внеклеточные) электроды. При этом нужно учитывать ветвление тока в нерве, шунтирование тока в межклеточных щелях (рис. 210041846).
Рис. 210041846. Ветвление тока в ткани при раздражении через наружные (внеклеточные) электроды (схема). Волокна обведены толстой линией, между ними – межклеточные щели[Мф53] . Объяснение в тексте.
Классификация нервных волокон по Эрлангеру-Гассеру
В 1939 г. американские[Мф54] физиологи Джозеф Эрлангер [Б55] и Герберт С.Гассер [Б56] [Б57] зарегистрировали токи действия от целого нервного ствола седалищного нерва лягушки на разных расстояниях от стимулирующего электрода (рис. 210041905).[Б58]
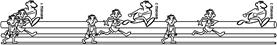
Было установлено, что регистрируемый суммарный потенциал имеет ряд пиков, которые были обозначены буквами латинского алфавита A, B, C (рис. , I). Пик A имел дополнительные пики, помеченные греческими буквами α, β, γ, δ (рис. , II). [Б59] В 1944 г. работа Дж.Эрлангера и Г.С.Гассера была оценена присуждением Нобелевской премии[Б60] .
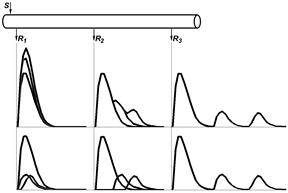
Нервы у позвоночных состоят из трех основных групп волокон (А, В и С), различающихся по степени миелизации, диаметру волокна, длительности пика ПД (скорости развития ПД), электровозбудимости, его компенсации и скорости проведения (все эти показатели в ряду А — В — С падают).
Группа А включает наиболее толстые хорошо миелинизированные моторные и чувствительные волокна; группа В — слабомиелинизированные, преганглионарные волокна автономной нервной системы; группа С - немиелинизированные, постганглионарные (симпатические) волокна.
В группе А в ряду a, b, g, d названные показатели тоже падают. Соотношения свойств этих групп волокон демонстрируются в табл. .
Необходимо заметить, что указанные соотношения порогов электрического раздражения групп волокон не отражают точного соотношения электровозбудимости их мембран. Относительно высокие пороги тонких волокон при их раздражении в нервном стволе определяются в основном тем обстоятельством, что тонкие волокна по сравнению с толстыми обладают более высоким входным сопротивлением. В них входит такая малая часть раздражающего тока, что при пороговой силе для Аa-волокон она совершенно недостаточна для создания на мембране более тонких волокон сколько-нибудь существенной деполяризации. По этой же причине (высокое RI) отводимые от ствола (внеклеточно) ПД тонких волокон предстают значительно меньшими, чем ПД толстых волокон.

Рис. . Составные части потенциала действия смешанного нерва.
I – при относительно медленной скорости записи.
II – при относительно высокой скорости записи.
Объяснение в тексте. По оси абсцисс – время, по оси ординат амплитуда составного потенциала в мВ.
Суммарная электрическая активность нерва создается его волокнами, каждое из которых генерирует свой стандартный по амплитуде и временным параметрам ПД, распространяющийся в обе стороны от точки, к которой приложено раздражение. Суммарный электрический сигнал нерва зависит от числа активных волокон, синхронности их активности, способа отведения и других обстоятельств.
При дальнейшем увеличении силы стимула этот ПД несколько удлиняется во времени. Все изменения амплитуды и длительности пика ПД нерва при усилении стимула определяются ростом числа активных волокон, подключением к низкопороговым и быстрым А(альфа)-волокнам более высокопороговых медленных бета-, гамма-, дельта-волокон группы А, затем В- и, наконец, С-группы.
| Группы волокон (по Эрлангеру и Гассеру) | Диаметр, мкм | Скорость проведения, м/с |
| Aa | 13 - 22 | 70 - 120 |
| Ab | 8 -13 | 40 - 70 |
| Ag | 4 - 8 | 15 – 40 |
| Ad | 1 – 4 | 5 – 15 |
| B | 1 - 3 | 3 – 14 |
| C | 0,5 – 1,0 | 0,5 - 2 |
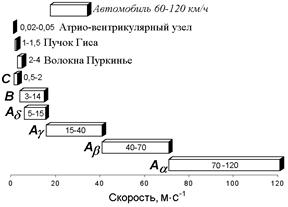
Таблица . Классификация нервных волокон по Дж.Эрлангеру и Х.Гассеру
| Группы волокон (по Эрлангеру и Гассеру) | Диаметр, мкм | Пороги электрического раздраженния (относительно Aa) | Длительность пика ПД 1 | Отрицательный следовой потенциал (ОСП) | Положительный следовой потенциал [Б61] | Скорость проведения, м/с | |
| Длительность, мс | Амплитуда СП, % к амплитуде ПД | Длительность, мс | Амплитуда СП, % к амплитуде ПД | ||||
| Aa | 13 - 22 | 1,0 | 0,4 | 15 – 20 | 40 - 60 | 0,2 | 70 - 120 |
| Ab | 8 -13 | 40 - 70 | |||||
| Ag | 4 - 8 | 15 – 40 | |||||
| Ad | 1 – 4 | 5 – 15 | |||||
| B | 1 - 3 | 11,7 | 1,2 | ОСП нет | 100 – 300 | 3 – 14 | |
| C | 0,5 – 1,0 | 100,0 | 2,0 | 50 – 60 | 300 - 1000 | 0,5 - 2 |
1 Приблизительно ту же величину имеют и абсолютные рефрактерные фазы
| | | следующая лекция ==> | |
| Сальтаторное проведение потенциалов действия | | | Законы проведения возбуждения в нервных волокнах и нервах |
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Электромиография (ЭМГ) — это метод исследования нервно-мышечной системы посредством регистрации электрических потенциалов мышц. Во многих зарубежных странах (США, Бельгия, Великобритания и др.) обучение электромиографии является обязательной составляющей частью образовательной подготовки врачей-реабилитологов; реабилитолог обязан уметь проводить электромиографическое обследование и анализировать полученные результаты. В нашей стране электромиографическое обследование осуществляется врачами функциональной диагностики. Тем не менее, врач-реабилитолог должен иметь представления о возможностях этого метода и его значения для реабилитационной практики. Ниже будут изложены лишь самые общие основы метода. Более подробные сведения о методе электромиографии можно подчерпнуть в специальных руководствах (Бадалян Л.О., Скворцов И А. Клиническая электромиография. — М.: Медицина, 1986; Гехт Б.М. Теоретическая и клиническая электромиография. — Л.:Наука, 1990; Зенков Л.Р., Ронкин М.А. Функциональная диагностика нервных болезней. — М.:Медицина, 1991; Aminoff М. Electromyography in clinical practic. - Addison-Wesley, 1978).
Основным функциональным элементом мышцы является мышечное волокно. При передаче возбуждения с нервного волокна на мышечное в последнем возникают сложные биохимические и электрофизиологические процессы, результатом которых являются электрические разряды. Эти быстрые потенциалы продолжительностью до 5 мс и средней амплитудой 50—100 мкВ, соответствующие возбуждению одной мышечной фибриллы, называются потенциалами фибрилляций (рис. 2.46 а).
Потенциалы фибрилляций (ПФ) могут возникать не только в ответ на нервный импульс, но и спонтанно. Но в норме ПФ практически не регистрируются, так как каждое нервное волокно одновременно иннервирует не одно, но группу мышечных волокон, и поэтому при возбуждении нерва на ЭМГ регистрируются суммарные разряды многих мышечных волокон. Группа мышечных волокон, иннервируемых одним мотонейроном и, соответственно, одним двигательным аксоном, называется двигательной единицей (ДЕ). Суммарный разряд мышечных волокон, составляющих ДЕ, называется потенциалом действия двигательной единицы (рис. 2.46 б). Поскольку возбуждение отдельных волокон происходит не абсолютно синхронно, потенциал действия двигательной единицы (ПД ДЕ) превышает ПФ по амплитуде (до 200— 2000 мкВ) и длительности (до 10 мс), в норме он чаще трехфазный, но может быть и полифазным. Характеристики ПД ДЕ зависят от числа и плотности расположения мышечных волокон в зоне отводящей поверхности игольчатого электрода, синхронности поступления нервных импульсов к отдельным мышечным волокнам, диаметра мышечного волокна. ПФ и ПДЦЕ — основные элементарные феномены ЭМГ, подлежащие анализу. С помощью специальных приборов — электромиографов — производится усиление и запись потенциалов действия возбудимых элементов мышцы, т. е. регистрируется электромиограмма.
В зависимости от метода регистрации биопотенциалов различают глобальную, или поверхностную, и локальную, или игольчатую, ЭМГ ис. 2.47. Типы ЭМГ по Ю.С.Юсевич: а — I тип, б — тип; в — III тип, г— IV тип.
Глобальная, или поверхностная, ЭМГ нашла наиболее широкое применение в отечественных медицинских учреждениях, поскольку этот метод наиболее прост в исполнении, безболезненен и бескровен; за рубежом к диагностической ценности поверхностной ЭМГ в настоящее время относятся достаточно скептически [Aminoff М., 1978]. Биопотенциалы мышц отводятся накожными металлическими электродами. Поверхностная ЭМГ представляет собой суммарную интерференционную) активность большой группы ДЕ, расположенных вблизи электрода. Оценка глобальной ЭМГ сводится к общей характеристике кривой, определению суммарной электрической активности мышц, максимальной амплитуде колебаний и отнесению ЭМГ к тому или иному классу. В отечественной диагностической практике наиболее широко используют методические приемы и способы анализа поверхностной ЭМГ, выработанные Ю.С.Юсевич [1958]. Автор выделяет четыре типа ЭМГ (рис. 2.47). I тип — интерференционная кривая, представляющая собой высокочастотную (до 50—100 кол/с) полиморфную активность, возникающую при произвольном сокращении мышцы. Снижение амплитуды интерференционной ЭМГ наблюдается при первично мышечных и при аксональных поражениях. II тип — редкая (до 20—40 кол/с) ритмическая активность, характерная для поражения передних рогов спинного мозга. III тип — усиление частых колебаний в покое, группировка их в ритмические разряды, появление вспышек колебаний на фоне ЭМГ произвольного мышечного сокращения; этот тип характерен для различного рода супраспинальных расстройств. Тип IV ЭМГ — полное биоэлектрическое молчание в покое, при тоническом напряжении или попытке к произвольному сокращению; характеризует полный паралич мышцы [Юсевич Ю.С., 1958].
Амплитуда интерференционной ЭМГ может быть использована (при стандартизации условий отведения) для оценки величины усилия, развиваемого мышцей, поэтому в реабилитационной практике поверхностную ЭМГ можно использовать для объективизации динамики мышечной силы в процессе лечения.
Игольчатая ЭМГ— это метод регистрации электрических потенциалов мышц с помощью вводимых в мышцу игольчатых электродов. К преимуществу метода относится возможность регистрировать электрическую активность ограниченного числа мышечных волокон в пределах одной или нескольких ДЕ, что дает возможность точнее и раньше диагностировать уровень и характер поражения нервно-мышечного аппарата. Нормальная ЭМГ характеризуется отсутствием электрической активности в мышце, находящейся в состоянии покоя и расслабления. При слабом сокращении или синергическом напряжении мышцы на ЭМГ вначале регистрируются потенциалы отдельных ДЕ, которые по мере нарастания силы мышечного сокращения сливаются в сплошную высокочастотную активность. К патологическим феноменам, обнаруживаемым при отведении ЭМГ игольчатыми электродами, относят следующие:
Спонтанная активность, регистрируемая в мышце при отсутствии произвольного сокращения или искусственной стимуляции (т.е. в покое), а именно: потенциалы фибрилляции (разряды одиночных мышечных волокон), потенциалы фасцикуляций (изолированные разряды ДЕ), положительные острые волны (ПОВ), миотонические разряды. Происхождение ПФ связывают с тем, что лишенные нормальной иннервации мышечные волокна вследствие патологического повышения их возбудимости приобретают способность к спонтанным разрядам [Зенков J1.P., 1995]. Появление ПФ, таким образом, свидетельствует лишь о лишении мышечного волокна контакта с иннервирующим его аксоном двигательного нерва, но не об уровне поражения (ПФ могут наблюдаться при денервации, длительном нарушении нервно-мышечной передачи либо при механическом разъединении мышечного волокна от той его части, которая находится в контакте с нервом). Потенциалы фасцикуляций (Пфас) возникают при поражении передних рогов спинного мозга, когда некоторые, еще не дегенерировавшие и сохранившие функциональную активность, мотонейроны приобретают способность к спонтанным разрядам. Амплитуда и длительность Пфас варьирует в широких пределах и полностью совпадают с динамикой амплитуды и длительности ПД ДЕ в данной мышце (рис. 2.46 в). ПОВ (рис. 2.46 г) — это колебания потенциалов характерной формы: быстрое позитивное отклонение потенциала, за которым следует медленное возвращение потенциала в сторону негативности. ПОВ имеют амплитуду от 20 до 4000мкВ, длительность от 2 до 100 мс и обычно регистрируются в виде разрядов частотой от 0,1 до 200 в секунду; служат свидетельством денервации мышечных волокон [Гсхт Б.М., 1990]. Миотонические разряды — высокочастотные разряды двухфазных ПД и ПОВ, вызываемые шевелением иглы или движением; характерны для миотонии.
Изменения ЭМГ при активном сокращении мышцы, проявляющиеся в изменении структуры ПД ДЕ в связи с уменьшением либо, наоборот, увеличением числа мышечных волокон в составе данной двигательной единицы. Б.М.Гехт [1982] выделяет 5 стадий этих изменений. 1 и 2 стадии отражают постепенное уменьшение числа функционируюших мышечных волокон в ДЕ и характеризуются увеличением (соответственно умеренным и значительным) количества ПД ДЕ малой длительности. Последующие стадии отражают процесс компенсаторного восстановления нервного контроля над мышечными волокнами: происходит либо синхронизации активности близлежащих ДЕ, либо реин нервации мышечных волокон сохранными мотонейронами с образованием гигантских ДЕ; в результате на ЭМГ наряду с ПД ДЕ малой длительности начинают регистрироваться укрупненные ПД ДЕ (3-я стадия), в 4-ю стадию число ПД ДЕ увеличенной длительности нарастает при исчезновении ПД ДЕ малой длительности, а 5-я стадия характеризуется преобладанием укрупненных и нередко гигантских ПД ДЕ.
Изменения ЭМГ не являются нозологически специфичными и могут возникать при поражении периферического мотонейрона на любом уровне, однако существуют некоторые особенности ЭМГ в зависимости от уровня поражения. Так, при первично мышечном поражении (мышечная дистрофия, миозит) при сохранности нормального числа активных ДЕ наблюдается диффузное уменьшение числа мышечных волокон, входящих в состав каждой ДЕ; вследствие этого на ЭМГ при активном сокращении мыщцы отмечается уменьшение амплитуды ПД ДЕ, его укорочение и увеличение числа полифазных ПД ДЕ. В покое могут регистрироваться фибрилляции. Для поражения мотонейрона на уровне передних рогов спинного мозга характерно появление в покое фасцикуляций, а при активном сокращении регистрируется разреженная интерференционная кривая с отдельными высокоамплитудными разрядами большой длительности. При поражении аксона двигательного нерва особенно характерна стадийность изменений ЭМГ. В острую стадию при полном поражении нерва отмечается биоэлектрическое молчание, ПД ДЕ не регистрируются. Через 4—20 дней появляются ПФ, еще через 10—15 дней — ПОВ (выявление ПОВ свидетельствует о более давнем и более тяжелом патологическом процессе). Далее ЭМГ может служить важным тестом в обнаружении наличия либо отсутствия процессов реиннервации мышцы.
(1) В случае полного перерыва нерва и отсутствия реиннервации за счет соседних нервных элементов ЭМГ характеризуется отсутствием ПД ДЕ, невозможностью получить вызванный ответ мышцы при стимуляции соответствующего нерва, наличием ПОВ (могут прослеживаться в течение 3 и более лет после полного перерыва нерва) и ПФ (на протяжении 16—17 месяцев). Наличие ПФ может служить признаком относительной сохранности мышцы, в то время как исчезновение фибрилляций при отсутствии признаков реиннервации свидетельствует о полном перерождении мышцы.
(2) В случае восстановления иннервации на ЭМГ вначале появляются ПД ДЕ малой амплитуды и длительности, затем наблюдается постепенное укрупнение их. ПФ по мере восстановления иннервации исчезают, ПОВ могут не возникать. Снижение выраженности ПФ и отсутствие ПОВ являются хорошим прогностическим признаком, свидетельствующим об обратимости поражения аксона и о возможности быстрого и полного восстановления функции нерва.
Кроме того, игольчатая ЭМГ позволяет определить топографический уровень поражения периферических нервных проводников благодаря тестированию ключевых мышц — т. е. тех мышц, которые наиболее достоверно отражают функциональное состояние отдельных корешков или периферических нервов. Обычно исследуется несколько мышц, иннервируемых одним корешком (или периферическим нервом), и одна или две мышцы, не иннервируемые им. В каждом конкретном случае задача решается подбором соответствующих ключевых мышц [Бадалян Л.О., 1986]. При исследовании функции корешков обязательно тестируются мышцы, иннервируемые несколькими периферическими нервами, что исключает ошибку в топической диагностике.
При проксимальном уровне поражения игольчатая ЭМГ позволяет провести дифференциальную диагностику между повреждением корешков и сплетения, что нередко может определять дальнейшую тактику лечения больного. Для этого исследуются паравертебральные мышцы, имеющих моносегментарную корешковую иннервацию без значительных анатомических вариаций. Наиболее удобной для этих исследований считается многораздельная мышца. Уровень поражения корешка может считаться установленным, если одновременно с поражением паравертебральных мышц на соответствующем уровне выявляется патология в иннервируемых данным корешком мышцах конечностей (сегментарная денервация). При поражении сплетения, в отличии от поражения корешков, не отмечаются денервационные изменения в паравертебральных мышцах. Обнаруживаются денервационные изменения в мышцах, иннервируемых двумя или несколькими корешками (мультисегментарная денервация).
Основой метода является регистрация активности нервов и мышц в ответ на электрическое раздражение. Стимуляцию производят в двигательных точках нервов и мышц накожньми электродами, для стимуляции используют импульсный ток интенсивностью до 150 В и длительностью импульсов 0,1 — 1 мс. Вызванную активность отводят также с помощью поверхностных электродов. Исследуется ряд показателей, характеризующих возбудимость мышц, мото-нейронов и их аксонов, чувствительных волокон периферических нервов: М-ответ (суммарный потенциал действия, возникающий в мышце при одиночном электрическом раздражении ее двигательного нерва), F-волна (ответ мышцы на антидромное возбуждение спинальных мотонейронов), Н-волна (суммарный потенциал действия мышцы в ответ на раздражение идущих от мышц афферентных волокон — моносинаптический рефлекторный ответ), потенциалы действия нервов в ответ на электрическую стимуляцию (активность нервного волокна или нервного ствола в ответ на электрическое раздражение, нанесенное на другом участке нерва) и скорость проведения возбуждения (СПВ) по нервам. Последний показатель в практике работы реабилитологов анализируется наиболее часто. Для определения СПВ по двигательному нерву накладывают два стимулирующих электрода и один регистрирующий, причем один из стимулирующих электродов располагают на проксимальном участке нерва, второй — на дистальном. Регистрирующий электрод накладывают на ин нервируемую этим нервом мышцу. Используется супрамаксимальная стимуляция, на 50% превышающая силу тока, вызывающую максимальный ответ. Измеряют латентное время ответа из проксимальной, затем из дистальной точек стимуляции, определяют расстояние между точками стимуляции и находят СПВ, равную отношению расстояния между точками стимуляции (в метрах) к разности латентных времен (в сек). Средние значения СПВ для моторных волокон срединного и локтевого нервов колеблются от 50 до 70 м/с, для малои больше-берцового нервов — от 40 до 60 м/с [Гехт Б.М., 1990]. Снижение СПВ (до 40—30 м/с и ниже) наблюдается при демиелинизирующих поражениях нервов. Деструкция аксонов не так сильно сказывается на снижении СПВ.
При исследовании нервно-мышечной передачи проводят декремент-тест, или определение величины декремента (уменьшения) М-ответа при повторной стимуляции нерва, иннервирующего данную мышцу (в случаях, когда мышца недоступна для непрямой стимуляции, регистрируют электромиографическую кривую утомления соответствующей мышцы).
Стимуляционная электромиография помогает дифференцировать поражение мышцы, нейромышечного синапса, периферического нерва, сплетения, корешка и переднего рога спинного мозга.
При преимущественном поражении синаптических образований (миастения), а также при первично мышечных заболеваниях без сопутствующего поражения периферических нервов СПВ по двигательным нервам остается в пределах нормальных величин. Также не меняется скорость проведения по нервам при поражении периферического мотонейрона на переднероговом уровне и уровне корешков. Амплитуда М-ответа при этом нередко бывает снижена (в норме находится в пределах 5— 300 мВ), что сочетается с увеличением его длительности и изменением формы.
Поражение стволов сплетения (в отличие от поражения дистальных отрезков периферических нервов) сопровождается изменением СПВ в первую очередь на проксимальном и лишь затем — дистальном участке соответствующих нервных стволов. В клинической практике хорошо зарекомендовали себя такие расчетные показатели, как проксимально-дистальный градиент скоростей проведения возбуждения и отношение амплитуд максимальных моторных ответов при стимуляции нерва в дистальной (А1) и проксимальной (А2) точках. Проксимально-дистальный фадиент СПВ, или отношение СПВ по проксимальному и дистальному участкам нервов в норме составляет 1,09—1,1; отношение амплитуд максимальных М-ответов, полученных при стимуляции в дистальной и проксимальной точках у здорового человека близко к 1,0. Снижение этих показателей может свидетельствовать о поражении нервных проводников на уровне сплетения. Определить поражение проксимальной части нервного ствола или спинномозгового корешка можно также путем сравнения латентного периода F- и М-ответов. Так (на примере верхней конечности), отсутствие F-волны при регистрации с короткой мышцы, отводящей большой палец, или с мышцы, отводящей мизинец, или отсутствие F-волны в сочетании с замедлением проводимости между спинным мозгом и локтем при сохранении нормальной проводимости между локтем и запястьем указывает на проксимальную локализацию поражения. По степени выраженности обнаруженных изменений на различных нервных стволах конечности можно косвенно судить о преимущественном поражении тех или иных корешков или стволов сплетения.
При поражениях стволов периферических нервов в большей степени, как правило, страдает дистальный участок нерва, поэтому проксимально-дистальный градиент СПВ оказывается выше нормальных значений.
Необходимо отметить, что степень и выраженность изменений СПВ при нейропатиях и нейронопатиях часто не соответствуют клиническому состоянию больного (при выраженной клинике СПВ может быть снижена незначительно, и наоборот — при низких величинах СПВ — хорошее состояние больного) [Гехт Б.М., Ильина Н.А., 1982|. Целесообразнее ориентироваться на динамику показателей ЭМГ индивидуального больного в процессе его лечения.
Резюмируя вышеизложенное, реабилитологу можно рекомендовать следующую тактику при выборе метода исследования: для осуществления эк-спресс-оценки динамики восстановления двигательных функций можно использовать поверхностную ЭМГ; для целей дифференциальной диагностики характера заболевания и уровня повреждения нервных проводников используются игольчатая ЭМГ и стимуляционная ЭМГ. При этом при локальных либо дистальных повреждениях нервных структур, когда имеется возможность произвести стимуляцию нерва проксимальнее и дистальнее уровня поражения и оценить биоэлектрическую реакцию нервов и мышц на стимуляцию, рекомендуется начинать исследование с проведения стимуляционной ЭМГ. При проксимальных поражениях предпочтительнее начинать электрофизиологическое обследование с игольчатой ЭМГ, не забывая при этом путем тестирования паравертебральных мышц уточнить уровень поражения (корешки или сплетение?).
Читайте также:


