Анатомия и физиология цнс с позиции анестезиологии и реаниматологии
Дли выбора адекватного метода анестезии и проведения последующей интенсивной терапии нейроанестезиолог должен понимать риски, связанные с хирургическим лечением, знать, какие функциональные изменения происходят в нервной системе, и иметь представление о механизме действия лекарственных веществ.
ЦНС состоит из головного и спинного мозга, окруженных костными структурами— черепом и позвоночным столбом.
Головной мозг. Головной мозг состоит из ствола мозга (моста и продолговатого мозга), мозжечка, среднего мозга и переднего мозга.
Ствол. Ствол мозга участвует в передаче информации между отделами головного и спинного мозга и включает следующие важные структуры:
• центры регуляции дыхания и кровообращения
• восходящие и нисходящие проводящие пути
• бульварные ядра черепных нервов и ретикулярную формацию, которая связана с сознанием.
Повреждения или компрессия ствола, вызванные увеличением внутричерепного давления, вызывают нарушение функций жизненно важных центров, что быстро приводит к летальному исходу.
Мозжечок. Мозжечок расположен в задней черепной ямке под наметом мозжечка. Он состоит из двух полушарий, соединенных посередине червем и функционально связан со стволом и средним мозгом. Мозжечок отвечает за регуляцию позы и движений. Поражения мозжечка проявляются неврологической симптоматикой на противоположенной половине тела.
Средний мозг. Средний мозг соединяет ствол мозга и мозжечок с гипоталамусом и полушариями мозга. Таламус содержит ядра основных чувствительных проводящих путей.
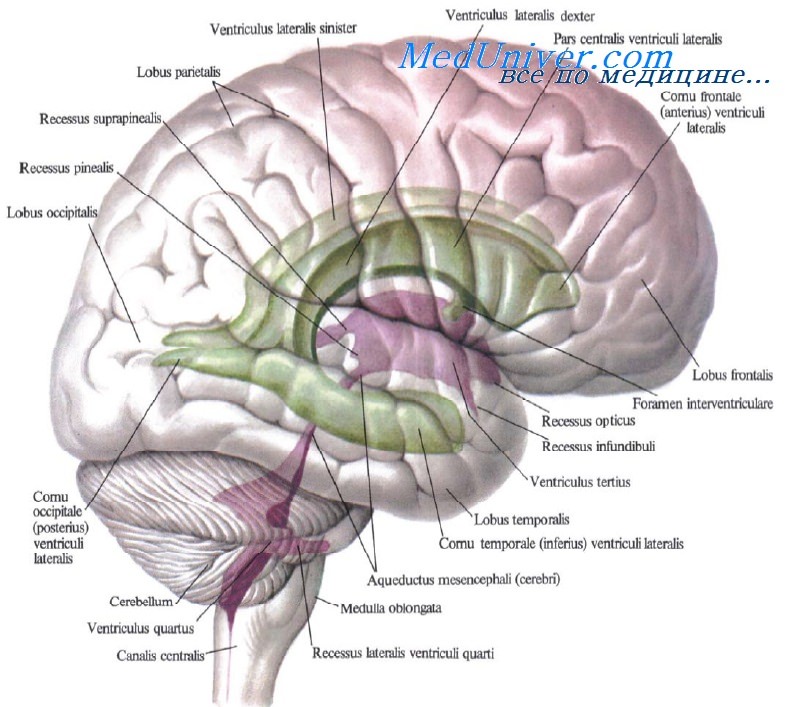
Передний мозг. Передний мозг включает диэнцефалон и два больших полушария.
Диэнцефалон — центральная часть переднего мозга, состоящая из таламуса и гипоталамуса.
• Гипоталамус координирует вегетативную и эндокринную регуляцию.
• Гипофиз находится под гипоталамусом. Опухоли гипофиза могут вызывать симптомы новообразования, сркение полей зрения при сдавлении зрительного перекреста или проявляться эндокринными нарушениями.
В состав больших полушарий входят кора, базальныс ганглии и боковые желудочки. Поверхность коры образует складки, или извилины, разделенные между собой посредством расщелин, или борозд. Центральная борозда отделяет главную двигательную извилину (кпереди) от главной чувствительной (кзади). Каждое полушарие разделено на четыре области или доли: лобную, теменную, затылочную и височную.
• Лобная доля состоит из моторной коры и зон, связанных с интеллектом и поведением.
• Теменная доля состоит из чувствительной коры.
• Височная доля связана со слуховой чувствительностью и интеграцией других видов чувствительности.
• Затылочная доля включает зрительную кору.
• Медиальные структуры коры включают лимбическую систему, которая связана с эмоциями и поведением.
Повреждение коры больших полушарий проявляется двигательными или чувствительными нарушениями на противоположной стороне тела. Между базальными ганглиями и таламусом расположена внутренняя капсула, в которой проходят нисходящие двигательные пути от коры больших полушарий.
Спинной мозг. Спинной мозг имеет длину около 45 см. Он начинается от большого затылочного отверстия и заканчивается мозговым конусом на уровне первого или второго поясничного позвонка. На уровне каждого позвонка от спинного мозга с каждой стороны отходят парные передние (двигательные) и задние (чувствительные) корешки. Корешки объединяются на уровне каждого межпозвоночного отверстия и формируют смешанные спинномозговые нервы. Спинной мозг состоит из:
• центрального канала — пространства, которое при некоторых заболеваниях может содержать ликвор
• окружающего центральный канал серого вещества, формирующего передние и задние рога:
• передних рогов серого вещества, содержащих тела двигательных нейронов и задних рогов, где находятся синапсы периферических чувствительных нейронов
• белого вещества, состоящего из восходящих и нисходящих трактов, формирующих передние, задние и латеральные канатики.
Определение и общий план строения ЦНС
Центральная нервная система (сокращенно ЦНС) является основной частью нервной системы человеческого организма, состоящей из комплексов нейронов (нервных клеток) и их отростков (аксонов, дендритов), представленной головным и мозгом, выполняющей рефлекторные функции и осуществляющей высшую нервную деятельность.
Одной из актуальных проблем современной медицины является вопрос защиты мозга от пагубного воздействия общего наркоза во время проведения хирургических вмешательств, ведь использование общей анестезии воздействует как в целом на весь организм, так и непосредственно на головной и спинной мозг, которые по сути и являются целью воздействия при наркозе.
Как можно заметить из определения ЦНС, она состоит из двух отделов:
- головной мозг с его оболочками;
- спинной мозг с его оболочками.
Особенности строения и физиологии ЦНС с позиции анестезиологии
Основные моменты анатомии и физиологии ЦНС, имеющие значение для анестезиолога-реаниматолога:
- Курсовая работа Анатомия и физиология центральной нервной системы с позиции анестезиологии и реаниматологии 410 руб.
- Реферат Анатомия и физиология центральной нервной системы с позиции анестезиологии и реаниматологии 240 руб.
- Контрольная работа Анатомия и физиология центральной нервной системы с позиции анестезиологии и реаниматологии 190 руб.
- Центральная нервная система является единой структурой, в которой различают две части: головной мозг и спинной мозг.
- И головной, и спинной мозг имеют защиту в виде трех мозговых оболочек (мягкой, паутинной и твердой).
- ЦНС состоит из множества миллионов нервных клеток (нейронов), отростки которых образуют проводящие пути, окруженные нейроглией.
- В центральной нервной системе присутствуют два типа ткани, выполняющие различные функции, это белое и серое вещество.
- В головном мозге основная часть серого вещества расположена снаружи, которое в данном случае называется корой, а внутри находится белое вещество. В спинном же мозге белое и серое вещество расположены в противоположном порядке.
- Серое вещество в основном представлено самими нервными клетками (то есть их телами) и выполняет функции различных анализаторов и жизненно важных центров.
- Белое вещество представлено волокнами (отростками) нервных клеток и выполняет функции проводящих путей.
- В головном мозге различают три основных отдела: большой мозг, мозжечок и ствол.
- Полушария большого мозга занимают основную часть черепной коробки.
- Мозжечок располагается между стволом и полушариями мозга, кзади и снизу от ствола.
- Мозговой ствол в свою очередь представлен промежуточным мозгом, средним мозгом, мостом и продолговатым мозгом.
- Спинной мозг представляет собой продолговатую, почти цилиндрическую структуру ЦНС, которая расположена внутри позвоночного канала. Он соединяется непосредственно с продолговатым мозгом, являющимся отделом ствола головного мозга.
- Твердая оболочка представлена плотной белесоватой соединительной тканью, которая расположена кнаружи от других оболочек. Ее наружная поверхность непосредственно прилегает к костям черепа, для которых она выполняет роль надкостницы. Такая особенность твердой оболочки характерна только для головного мозга. Твердая оболочка содержит артерии и вены, а также в черепной коробке образует ряд вместилищ (синусов), которые собирают кровь от мозга. Основные пути оттока из синусов крови – это внутренние яремные вены.
- Пространство, расположенное между твердой мозговой оболочкой и костями черепа и позвоночника, носит название эпидурального.
- Строение паутинной оболочки одинаково, как для спинного, так и для головного мозга, она отделена капиллярной щелью от твердой оболочки, которая называется субдуральным пространством, в котором имеется небольшое количество жидкости.
- Мягкая оболочка непосредственно покрывает мозг и тесно прилежит к нему, она богата кровеносными сосудами и сосудистыми сплетениями. Между мягкой и паутинной мозговыми оболочками располагается субарахноидальное пространство, которое также называется подпаутинным.
- Подпаутинные пространства головного и спинного мозга являются замкнутыми и, как и мозговые желудочки, заполнены цереброспинальной жидкостью, являющейся внутренней средой, которая необходима для нормального функционирования центральной нервной системы. Отток церебральной жидкости из данных пространств осуществляется посредством фильтрации в венозную, а также отчасти в лимфатическую, систему.
- У взрослого человека общее количество цереброспинальной жидкости составляет около 130-150 мл, из которых на центральный канал спинного мозга приходится около 20-30 мл.
- Фиксация спинного мозга в субарахноидальном пространстве обеспечивается пересекающими в различных плоскостях это пространство тяжами и связками.
- Наибольшее значение в этом плане представляют три связки: одна продольная и две боковые.
- Часть субарахноидального пространства в области конского хвоста является местом, где скапливается наибольшее количество цереброспинальной жидкости. Поэтому с точки зрения спинномозговой анестезии она представляет наибольший интерес.
- Ретикулярная формация располагается в сером веществе спинного мозга между его латеральными и дорсальными рогами, также захватывая частично и белое вещество. В головном мозге ретикулярная формация находится в связи со многими его головного мозга, в частности с корой. Механизм действия многих анестетических препаратов связан с оказанием тормозного воздействия на ретикулярную формацию.
- Во время проведения спинномозговой и эпидуральной анестезии обязательно учитываются также анатомические особенности позвоночника, неодинаковая в различных отделах форма позвонков и его физиологические изгибы.
- Целостность позвоночника обеспечивается благодаря связкам, скрепляющим между собой позвонки (двум продольным, надостистой, межостистой и желтой).
- Во время проведения пункции центрального канала спинного мозга необходимо учитывать, что положение остистых отростков неодинаково в различных отделах позвоночника. В шейном отделе, у двух верхних грудных и нижних поясничных позвонков остистые отростки расположены почти горизонтально и их уровень полностью совпадает с уровнем соответствующих позвонков.
- У остальных позвонков остистые отростки направлены вниз и черепицеобразно накладываются друг на друга таким образом, что их верхушки располагаются на уровне тел нижележащих позвонков.
- В положении максимального сгибания вперед туловища и шеи остистые отростки несколько отодвигаются друг от друга, что улучшает при пункции доступ к позвоночному каналу.
- При эпидуральной анестезии препарат вводится в эпидуральное пространство спинного мозга, также оно называется перидуральным или экстрадуральным и располагается между надкостницей позвонков и твердой мозговой оболочкой. В нем содержится жировая ткань и сеть сосудов. Это пространство, в отличие от центрального канала спинного мозга, не имеет сообщения с черепномозговой полостью через большое затылочное отверстие. Поэтому введение в него анестетиков не сопровождается развитием центрального паралича. Раствор лекарства при введении в эпидуральное пространство далее распространяется вниз и вверх по клетчатке позвоночного канала, а затем проникает в паравертебральное пространство через боковые отверстия.
- При пункции эпидурального пространства иглой проходится надостистая, межостистая и желтая связки.
- Если продвигать иглу глубже, то после желтой связки она проходит твердую, а затем и паутинную мозговые оболочки и попадает в подпаутинное пространство. Основным ориентиром его достижения является наличие спинномозговой жидкости. Введение анестетика в подпаутинное пространство спинного мозга называется спинномозговой анестезией.
Задай вопрос специалистам и получи
ответ уже через 15 минут!
Презентация была опубликована 6 лет назад пользователемГлеб Анджиевский
Презентация на тему: " Анатомия и физиология основных органов и систем с позиции анестезиологии и реаниматологии Микрюков Сергей Ростиславович 2014 г." — Транскрипт:
1 Анатомия и физиология основных органов и систем с позиции анестезиологии и реаниматологии Микрюков Сергей Ростиславович 2014 г.
2 Сердечно - сосудистая система Система, обеспечивающая циркуляцию крови в организме, Доставку кислорода к тканям, Доставку метаболитов к тканям, Удаление продуктов метаболизма из тканей ( СО 2)
3 Основные структурные разделы ССС Сердце Артериальная часть Микроциркуляторное русло Венозная часть Система регуляции ( ауторегуляция, гуморальная регуляция, нервно - рефлекторная регуляция )
5 Проводящая система сердца
6 Параметры работы ССС Сократимость миокарда - УО, СВ, СИ Преднагрузка – ДЗЛА, дДЛА, ЦВД. КДО Постнагрузка - ОПСС
7 Функциональная роль печени обезвреживание различных чужеродных веществ в частности аллергенов, ядов и токсинов, путём превращения их в безвредные, менее токсичные или легче удаляемые из организма соединения ; обезвреживание и удаление из организма избытков гормонов, медиаторов, витаминов, а также токсичных промежуточных и конечных продуктов обмена веществ, например аммиака, фенола, этанола, ацетона и кетоновых кислот ; участие в процессах пищеварения, а именно обеспечение энергетических потребностей организма глюкозой, и конвертация различных источников энергии ( свободных жирных кислот, аминокислот, глицерина, молочной кислоты и др.) в глюкозу ( так называемый глюконеогенез ); пополнение и хранение быстро мобилизуемых энергетических резервов в виде депо гликогена и регуляция углеводного обмена ; пополнение и хранение депо некоторых витаминов ( особенно велики в печени запасы жирорастворимых витаминов А, D, водорастворимого витамина B 12 ), а также депо катионов ряда микроэлементов металлов, в частности катионов железа, меди и кобальта. Также печень непосредственно участвует в метаболизме витаминов А, В, С, D, E, К, РР и фолиевой кислоты ; синтез холестерина и его эфиров, липидов и фосфолипидов, липопротеидов и регуляция липидного обмена ; синтез желчных кислот и билирубина, продукция и секреция желчи ; также служит депо для довольно значительного объёма крови, который может быть выброшен в общее сосудистое русло при кровопотере или шоке за счёт сужения сосудов, кровоснабжающих печень ; синтез гормонов и ферментов, которые активно участвуют в преобразовании пищи в 12- перстной кишке и прочих отделах тонкого кишечника ;
8 Печеночная недостаточность Интоксикация Коагулопатия
9 Функциональная роль почек Выделительная функция Регуляция КОС, ВЭО Участие в эритропоэзе Вырабатывают БАВ ( простогландины, ренин ) Дезинтоксикация
11 Роль гормонов в поддержании гомеостаза Тиреоидные гормоны увеличивают скорость большинства химических реакций в клетках Адренокортикотропный гормон ( АКТГ ) содержание ионов натрия Паратиреоидный гормон содержание ионов кальция и фосфатов Инсулин - обмен глюкозы
12 Нервная система ЦНС Периферическая нервная система
15 Перичерическая НС Соматическая Вегетативная - симпатическая - парасимпатическая - метасимпатическая
18 Нейромедиаторы ГАМК, глицин, глутамат, аспартат Дофамин, адреналин, норадреналин Серотонин, гистамин Ацетилхолин, АТФ, окситоцин, таурин И др. …
19 Адренореактивные и холинореактивные системы Система биохимических событии, развивающихся в результате воздействия медиатора и обеспечивающая осуществление нервного воздействия на функции иннервируемой клетки, называется реактивной системой А 1, А 2, В 1, В 2,… адренорецепторы М, Н, холинорецепторы
20 Система органов дыхания Доставка кислорода (O2) Выделение углекислого газа (CO2)
21 Этапы газообмена Внешнее дыхание ( доставка газа из окружающей среды к альвеолам ) Транспорт газов через альвеолокапиллярную мембрану Циркуляция О 2 и СО 2 с током крови Тканевое дыхание ( доставка О 2 внутрь клетки, окисление метаболитов до образования СО 2, вывод СО 2 из клетки в кровь )
24 Параметры системы дыхания, оценка газообмена Внешнее дыхание : ЧД (f), ДО (Vt), биомеханика вдоха ( С, R) SO2 (SpO2, SaO2, SvO2) pO2 (paO2, pvO2) pCO2 (PaCO2, PvCO2) EtCO2
25 Гипоксия Повышение ЧД Цианоз Потливость Тахикардия Повышение АД SO2 снижается (SpO2
45 mm Hg" title="Гиперкапния Тахипноэ Тахикардия Повышение АД EtCO2 > 45 mm Hg" > 26 Гиперкапния Тахипноэ Тахикардия Повышение АД EtCO2 > 45 mm Hg 45 mm Hg"> 45 mm Hg"> 45 mm Hg" title="Гиперкапния Тахипноэ Тахикардия Повышение АД EtCO2 > 45 mm Hg">
Для анестезиологического обеспечения нейрохирургических операций необходимо знание физиологии ЦНС. Многие анестетики оказывают значительное воздействие (как нежелательное, так и благоприятное) на метаболизм мозга, мозговой кровоток, образование и всасывание цереброспинальной жидкости, объем внутричерепного содержимого и внутричерепное давление. В настоящей главе обсуждаются важные для анестезиологической практики нейрофизиологические концепции, а также влияние анестетиков и различных вспомогательных средств на ЦНС. И хотя речь пойдет в основном о головном мозге, почти все изложенное можно отнести и к спинному мозгу.
Физиология ЦНС
Метаболизм мозга
В покое мозг потребляет до 20 % получаемого организмом человека кислорода. Главный потребитель энергии в мозге — это фермент АТФ-аза, поддерживающий электрическую активность нейронов. Метаболизм в мозге обычно оценивают по потреблению кислорода мозгом, или CMRO2 (CMR — cerebral metabolic rate), которое у взрослых составляет в среднем 3-3,5 мл/100 г/мин (50 мл/мин). CMRO2 максимально в сером веществе коры больших полушарий и прямо пропорционально биоэлектрической активности коры. Потребность мозга в кислороде по сравнению с таковой у других органов чрезвычайно велика, а запасов кислорода в нем нет. Если кровь не поступает в мозг в течение 10 с, напряжение кислорода падает ниже 30 мм рт. ст. и человек теряет сознание. Если мозговой кровоток не восстанавливается в течение 3-8 мин, то запасы АТФ истощаются и возникает необратимое повреждение нейронов. Наиболее чувствительны к гипоксии нейроны гиппокампа pi мозжечка.
Нейроны обеспечиваются энергией преимущественно за счет утилизации глюкозы. В среднем по-
требление глюкозы мозгом равно 5 мг/100 г/мин. В ЕЩС почти вся глюкоза (> 90 % ) подвергается аэробному распаду, поэтому потребление кислорода и потребление глюкозы изменяются параллельно. При голодании главным источником энергии для мозга становятся кетоновые тела — ацетоаце-тат и |3-гидроксибутират. Хотя мозг способен поглощать из крови молочную кислоту, ее метаболизм не играет значительной роли в энергетическом обеспечении. Не меньше чем гипоксия, опасна для мозга острая устойчивая гипогликемия. Исследования выявили парадоксальное явление: при тотальной ишемии мозга гипергликемия способствует внутриклеточному ацидозу и усугубляет повреждение нейронов. Влияние гипергликемии на очаговую ишемию не исследовано.
Мозговой кровоток
Мозговой кровоток (MK) зависит от интенсивности метаболизма. Мозговой кровоток чаще всего изучают с помощью изотопных методов исследований (обычно измеряют у
изл У чение изотопа ксенона [ 153 Xe]). После в/в инъекции изотопа датчики, установленные по окружности головы, регистрируют темп изменения радиоактивности, который пропорционален величине MK. Новейшей методикой исследования MK является позитрон-ная эмиссионная томография (ПЭТ); в сочетании с применением короткоживущих изотопов 11 C и 15 O ПЭТ позволяет измерить потребление мозгом глюкозы и кислорода соответственно. ПЭТ подтвердила полученные другими методами данные, что регионарный мозговой кровоток (рМК) изменяется прямо пропорционально интенсивности метаболизма и варьируется от 10 до 300 мл/100 г/ мин. Например, при движениях в конечности быстро возрастает рМК в соответствующем участке двигательной коры. Аналогичным образом активизация зрения приводит к увеличению рМК в зрительной коре затылочных долей мозга.
Хотя MK равен в среднем 50 мл/100 г/мин, в сером веществе головного мозга он достигает

80 мл/100 г/мин, в белом веществе — 20 мл/100 г/мин. MK у взрослых в среднем составляет 750 мл/мин, что соответствует 15-20 % от сердечного выброса. При MK ниже 20-25 мл/100 г/мин возникает повреждение мозга, что на ЭЭГ проявляется замедлением ритма. MK в пределах 15-20 мл/100 г/мин сответствует изоэлектрической линии на ЭЭГ, а при уменьшении MK до 10 мл/100 г/мин наступает необратимое повреждение мозга.
Регуляция мозгового кровообращения
Вопросы для самоподготовки по специальности
1.Система непрерывного медицинского образования в РФ. Формы повышения квалификации специалистов со средним медицинским образованием. Аттестация и сертификация средних медицинских работников.
- Современное состояние сестринского дела в РФ. Стратегия развития сестринского дела в РФ. Программа развития сестринского дела в РФ на 2010-2020 годы.
- Философия сестринского дела. Роль этического Кодекса в работе специалистов со средним медицинским образованием.
- Основы общей психологии. Психология успешного взаимодействия медицинской сестры с пациентом и его родственниками. Психологический комфорт пациента.
- Система управления качеством сестринской помощи.
- Технологии простых медицинских услуг.
- Современные технологии в работе медицинской сестры-анестезиста.
- Инфекционный контроль и инфекционная безопасность. Санитарно-
противоэпидемический режим в ЛПУ. Дезинфекция и стерилизация изделий медицинского назначения. Сбор, хранение, утилизация медицинских отходов. Профилактика ВИЧ-инфекции.
Неотложная доврачебная помощь при травмах и травматическом шоке, кровотечениях и геморрагическом шоке. Неотложная доврачебная помощь при неотложных состояниях и острых заболеваниях (острая коронарная, сердечная, сосудистая, дыхательная недостаточность, гипертонический криз, судорожный синдром, острые аллергические реакции).
- Организация анестезиологической службы в РФ. Организация работы РАО. Функциональные обязанность и права медицинской сестры-анестезиста.
- Анатомия и физиология центральной нервной системы, системы кровообращения, дыхания пищеварения, печени и почек с позиций анестезиологии и реаниматологии. Водно-электролитный обмен в норме и патологии, кислотно-основное равновесие, формы их нарушений.
- Клиническая фармакология основных препаратов, используемых в анестезиологии и реаниматологии.
- Аппаратура и инструментарий, используемые в анестезиологии и реаниматологии.
- Мониторинг безопасности в операционной.
- Оснащение рабочего места анестезиолога в операционной, перевязочной, отделении реанимации и интенсивной терапии.
- Подготовка пациентов к наркозу и операции.
- Ингаляционный наркоз. Показания, противопоказания, основные лекарственные средства, особенности их действия. Масочный наркоз.
- Эндотрахеальный наркоз. Показания, противопоказания, основные лекарственные средства, особенности их действия, возможные осложнения и роль медицинской сестры-анестезиста в их профилактике.
- Неингаляционный наркоз. Показания, противопоказания, основные лекарственные средства, особенности их действия, возможные осложнения и роль медицинской сестры-анестезиста в их профилактике.
- Многокомпонентная общая анестезия.
- Клиника наркоза.
- Осложнения анестезии. Профилактика и лечение осложнений.
- Особенности анестезиологического обеспечения операций.
- Региональная анестезия в анестезиологическом обеспечении.
- Современный сосудистый доступ.
- Инфузионная терапия.
- Основы клинической трансфузиологии.
- Гемотрансфузионная терапия.
- Современные кровозамещающие препараты.
- Терминальные состояния.
- Сердечно-легочная реанимация. Особенности сердечно-легочной реанимации в отделении реанимации и интенсивной терапии.
- Острая дыхательная недостаточность: причины, клинические проявления, неотложная помощь и интенсивная терапия. Тактика медицинской сестры-анестезистки.
- Острая сердечная недостаточность: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
43.Острая сосудистая недостаточность: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
47.Сепсис и септический шок: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Анафилактический шок: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Комы: классификация, причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Принципы организации интенсивного наблюдения, лечения и ухода в послеоперационном периоде.
- Острая почечная недостаточность: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Острая печеночная недостаточность: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Острые отравления: причины возникновения, клинические проявления, осложнения, принципы лечения, организация наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Современные методы эфферентной терапии.
- Реанимационные мероприятия при утоплении, электротравме, механической асфиксии.
- Современные принципы энтерального питания в интенсивной терапии.
- Анатомо-физиологические особенности системы кровообращения, центральной нервной системы, органов дыхания, пищеварения, печени и почек у детей с позиций анестезиологии и реаниматологии.
- Особенности анестезии и реанимации у детей.
- Острые отравления у детей: причины возникновения, особенности клинических проявлений, осложнения, принципы лечения, особенности организации наблюдения и ухода в отделении реанимации и интенсивной терапии.
- Особенности реанимации и интенсивной терапии в акушерстве.
- Особенности реанимации и интенсивной терапии в гинекологии.
- Виды, формы и методы реабилитации, организация мероприятий по реабилитации пациентов.
- Организация делопроизводства и учетно-отчетной деятельности структурного подразделения; основные виды медицинской документации.
ФИЗИОЛОГИЯ КРОВООБРАЩЕНИЯ
Функциональные отделы системы кровообращения.
В клинико-физиологическом аспекте систему кровообращения целесообразно рассматривать состоящей из следующих функциональных отделов:
2) сосуды-буферы, или артерии (некоторые авторы называют их иначе сосуды “котла”, подразумевая под ними аорту и крупные артерии) - выполняют
преимущественно пассивную транспортную функцию между насосом и системой микроциркуляции;
3) сосуды-емкости, или вены, также выполняющие транспортную функцию возврата крови к сердцу. Это более активная, чем артерии, часть системы кровообращения, поскольку вены способны изменять свой объем в десятки раз, активно участвуя в регуляции венозного возврата и ОЦК;
4) сосуды-сопротивления - артериолы и венулы, включая сфинктеры, регулирующие кровоток через капилляры и являющиеся главным физиологическим средством распределения сердечного выброса по органам и тканям, в связи с чем их также называют сосудами распределения;
5) сосуды обмена - капилляры, присоединяющие систему кровообращения к общей системе циркуляции биологических жидкостей организма;
6) сосуды-шунты - артерио-венозные анастомозы, регулирующие периферическое сопротивление при спазме артериол, сокращающем кровоток через капилляры.
Три первые функциональные части кровообращения (сердечный насос, сосуды-буферы и сосуды-емкости) образуют систему макроциркуляции - хорошо зримую и потому кажущуюся самой главной в кровообращении организма. Но на самом деле в клинико-физиологическом аспекте гораздо важнее знать о состоянии системы микроциркуляции, состоящей из трех последних разделов схемы (сосуды-сопротивления, сосуды обмена и шунты).
Система микроциркуляции важнее для изучения патофизиологии кровообращения потому, что она поражается при критическом состоянии любой этиологии, тогда как система макроциркуляции - при первичной патологии самих органов кровообращения, а при критических состояниях она страдает вторично из-за поражения системы микроциркуляции.
Главная функциональная цель системы макроциркуляции - обеспечить движение и транспорт крови. Задача микроциркуляции - присоединить систему кровообращения к общей системе циркуляции биологических жидкостей организма и распределить сердечный выброс между разными органами соответственно их потребности.
Элементы систем макро- и микроциркуляции.
СЕРДЦЕ. Ни один из известных механике насосов не работает так долго, как сердце. Этот маленький орган, весящий приблизительно 300 г, снабжает кровью “среднего человека” весом 70 кг в течение 70 лет. У человека в покое каждый желудочек сердца выбрасывает 5-5,5 литров крови в час, таким образом производительность обоих желудочков за 70 лет составляет приблизительно 400 млн. литров, даже если человек находится в состоянии покоя. По существу сердце состоит из двух насосов - правого сердца (предсердие и желудочек) и левого сердца (предсердие и желудочек). Во время систолы левое сердце выбрасывает 70-80 мл крови за одно сокращение в аорту, а кровь, поступающая из полых вен, нагнетается правым желудочком в легочный круг. Во время тяжелой физической нагрузки сердце может нагнетать 25 л в час и даже более в результате увеличения частоты и силы сокращений.
Некоторые из этих изменений обусловлены нервными воздействиями на волокна сердечной мышцы, а некоторые являются простым физическим следствием воздействия “растягивающей” силы венозного возврата на диастолическое растяжение, таким образом, на сократительную силу волокон сердечной мышцы; каждый насос должен быть наполнен, чтобы он мог работать. Кровь в сердце поступает под давлением, лишь незначительно превышающем нулевой уровень, во время диастолы. Сокращение и связанное с ним смещение желудочков сердца вниз приводят к пассивному расширению предсердий и оказывают некоторое присасывающее действие на кровь в центральных венах, что увеличивает эффективность сил, обеспечивающих наполнение вен (“заправка насоса”).
ОБЩАЯ ОРГАНИЗАЦИЯ СОСУДОВ. Во время систолы внутрижелудочковое давление повышается от уровня, близкого к нулю, до 120 мм рт. ст. в левом желудочке и до 25 мм рт. ст. в правом. В результате этого систолическое давление в аорте повышается до 120 мм рт. ст., а в легочной артерии до 25 мм рт. ст. По окончании фазы сокращения миокард расслабляется, и внутрижелудочковое давление круто падает почти до нуля, полулунные клапаны захлопываются, отделяя аорту и легочную артерию от желудочков.
Благодаря эластичности больших артерий и сопротивлению току крови в периферических сосудах АД колеблется в значительно меньшей степени, чем давление в желудочках, в результате чего диастолическое давление составляет
приблизительно 80 мм рт. ст. в системном сосудистом ложе (большом круге кровообращения). Поэтому фазовое изменение давления в левом желудочке - от 120 до 0 мм рт. ст. - превращается в артериальное пульсовое давление, равное (120 - 80) - 40 мм рт. ст. В малом круге эти показатели равны приблизительно 25/10 мм рт. ст., так что пульсовое давление составляет 15 мм рт. ст. Таким образом, оба желудочка соответственно обеспечивают энергией кровообращения в обоих кругах кровообращения градиент давления, который приводит в движение кровь.
Аналогия с законом Ома дает возможность понять факторы, которые в этом участвуют: L = Е/Р (ом), где Е - градиент давления, приводящий в движение кровь, равен средней разнице между давлением в артериальном и венозном отделах каждого круга; Р - общее сопротивление, оказываемое сосудами системного и легочного круга. наибольшая часть которого приходится на долю артериол. Приток крови к каждому кругу (L) определяется частным от деления градиента давления на региональное сопротивление кровотоку.
Дифференциация сосудов
СОСУДЫ-БУФЕРЫ (ИЛИ СОСУДЫ “КОТЛА”) - они оказывают незначительное сопротивление току крови и поэтому смягчают пульсирующий систолический выброс желудочка. Выброс левого желудочка растягивает аорту и ее крупные ветви. После захлопывания аортальных клапанов эластичная аорта и ее ветви сокращаются, поддерживая этим градиент давления и делая поступление крови на периферию более равномерным. Старение эластических
элементов артериальной стенки является причиной высокого пульсового давления в результате снижения функции сосудов - буферов.
ПРЕКАПИЛЛЯРНЫЕ СОСУДЫ СОПРОТИВЛЕНИЯ - это в основном мелкие артерии и артериолы, на долю которых приходится большая часть сопротивления кровотоку. Снабжение кровью любого участка, а также гидростатическое давление в капиллярах этого участка определяются главным образом изменениями радиуса этих сосудов. Прекапиллярным сосудам сопротивления свойственна высокая степень внутреннего (миогенного) базального тонуса, который постоянно изменяется под влиянием местных физических и химических факторов. Изменения базального миогенного тонуса в результате таких местных воздействий является почти единственным механизмом приспособления регионарного сопротивления сосудов, снабжающих кровью сердце и головной мозг. В других местах сосуды сопротивления регионарных цепей находятся также под влиянием симпатических нервов. Влияние этой иннервации в состоянии равновесия в покое относительно незначительно, но при стрессовых обстоятельствах оно может стать выраженным.
ПРЕКАПИЛЛЯРНЫЕ СФИНКТЕРЫ. Эти сосуды, хотя они и являются частью прекапиллярных сосудов сопротивления, определяет в основном площадь обменной поверхности капилляров, изменяя число капилляров, перфузируемых в каждый определенный момент. Они находятся главным образом под местным контролем, т.е. под контролем внутренней
миогенной активности, непрерывно изменяющиеся под влиянием местных сосудорасширяющих метаболитов.
КАПИЛЛЯРНЫЕ ОБМЕННЫЕ СОСУДЫ. Эти сосуды - ключевой пункт сердечно-сосудистой системы - представляют собой трубочки, состоящие из одного слоя эндотелиальных клеток. Растворенные вещества проходят через их стенку в обоих направлениях. Сами капилляры не оказывают активного влияния ни на скорость кровотока, ни на чрезвычайно важные обменные механизмы диффузии и фильтрации-абсорбции.
ПОСТКАПИЛЛЯРНЫЕ СОСУДЫ СОПРОТИВЛЕНИЯ. Венулы и мелкие вены не играют большой роли в общем сопротивлении сосудов. Тем не менее они имеют большое значение, т. к. от соотношения между прекапиллярным и посткапиллярным давлением зависит гидростатическое давление в самих капиллярах, а от него в свою очередь зависит транспорт жидкой фазы между кровью и межтканевой жидкостью. Таким образом, изменения градиента пре- и посткапиллярного сопротивления оказывает влияние на ток крови, а изменения соотношения между пре- и посткапиллярным сопротивлением влияют на объем крови.
СОСУДЫ-ЁМКОСТИ. Эти сосуды, т.е. все венозное ложе, играют незначительную роль в создании на емкость сосудистого русла изменением своей конфигурации и диаметра просвета. МОК зависит от венозного возврата, в соответствии с этим изменения емкости венозного русла, вызываемые в основном активностью внешних сосудосуживающих симпатических волокон,
могут оказывать глубокое влияние на наполнение сердечного насоса. Венозный отдел можно считать своего рода “форкамерой” насоса.
СОСУДЫ-ШУНТЫ. В большинстве цепей эти сосуды являются скорее исключением. Они осуществляют прямые связи между мелкими артериями и венами в обход капиллярного ложа. Поэтому они не выполняют обменной функции и локализуются в изобилии в участках кожи (пальцы рук, ног, уха и т.д.), выполняющих в основном терморегуляторную функцию. Их тонус находится в большой зависимости от влияния симпатических сосудосуживающих нервов.
МАССООБМЕН В КАПИЛЛЯРОНЕ. Конечной функциональной ячейкой системы микроциркуляции является капиллярон, состоящий из артериолы, венулы, капилляров и артериовенозного анастомоза (шунта). Основные законы гемодинамики капиллярона можно сформулировать следующим образом:
1) регуляция кровотока через капиллярон осуществляется в сооответствии с местными потребностями путем изменения тонуса сосудов-сопротивлений;
2) анатомическое строение капиллярона соответствует общему назначению системы микроциркуляции, но детали структуры его приспособлены к функциональным задачам данного органа и специфичны именно для него;
3) реологические свойства крови и связанный с ними транскапиллярный массообмен зависят от скорости кровотока.
Местной тканевой регуляцией кровоток может быть направлен через капилляры или через атериовенозные шунты. От такого распределения зависит собственный метаболизм организма, в котором рапсположен капиллярон. Сокращение артериол увеличивает ОПС и ухудшает кровоток в капилляроне. Сокращение венул задерживает повышенный объем крови в нем.
Существуют два биофизических механизма, регулирующих массобмен в капилляроне: изменение тонуса мышечных сосудов и изменение проницаемости капиллярной стенки.
Регуляция мышечного тонуса осуществляется нейрогенным путем (быстрый процесс), а также через местные метаболиты и биологически активные вещества (медленный процесс). Регуляция массообмена через капиллярную стенку может быть описана уравнением Старлинга для полупроницаемых мембран:
lу = Кф х ((Рс - Рт) - л (Пс - Пт)),
где 1у - объем жидкости, движущейся через капиллярную стенку; Кф - коэффициент фильтрации: Рс - внутрикапиллярное давление: Рт - интерстициальное давление: л - коэффициент отражения макромолекул: Пс - онкотическое давление крови: Пт - онкотическое давление интерстициальной жидкости.
Условия критического состояния могут воздействовать на все эти параметры микроциркуляции многочисленными факторами. Например, гипоксия, респираторный и метаболический ацидоз могут влиять на них непосредственно или через определенные вещества. Нервные окончания альфа- и бета-адренергических систем также могут стимулировать естественными медиаторами или метаболитами и экзогенными веществами. Накопление кислых продуктов вызывает вазодилятацию с увеличением кровотока через капиллярон, благодаря чему ацидоз снижается, т.к. избыток кислых продуктов удаляется.
Реологические свойства крови.
Кровь - суспензия клеток и частиц, взвешенных в коллоидах плазмы. Это типично неньютоновская жидкость, вязкость которой, в отличие от ньютоновской, в различных частях системы кровообращения различается в сотни раз, в зависимости от изменения скорости кровотока.
Для вязкостных свойств крови имеет значение белковый состав плазмы. Так, альбумины снижают вязкость и способность клеток к агрегации, тогда как глобулины действуют противоположно. Особенно активен в повышении вязкости и наклонности клеток к агрегации фибриноген, уровень которого меняется при любых стрессовых состояниях. Гиперлипидемия и гиперхолестеринемия также способствует нарушению реологических свойств крови.
Гематокрит - один из важных показателей, связанных с вязкостью крови. Чем выше гематокрит, тем больше вязкость крови и хуже ее реологоческие свойства. Геморрагия, гемодилюция и, наоборот, плазмопотеря и дегидратация значительно отражаются на реологических свойствах крови. Поэтому, например, управляемая гемодилюция является важным средством профилактики реологических расстройств при оперативных вмешательствах. При гипотермии вязкость крови возрастает в полтора раза по сравнению с таковой при 37 о С, но если снизить гематокрит с 40% до 20% , то при таком перепаде температур вязкость не изменяется. Гиперкапния повышает вязкость крови. При снижении рН крови на 0,5 и высоком гематокрите вязкость крови увеличивается втрое.
Расстройства реологических свойств крови
Основной феномен реологических расстройств крови - агрегация эритроцитов, совпадающая с повышением вязкости. Чем медленнее поток крови, тем более вероятно развитие этого феномена. Так называемые ложные агрегаты (“монетные столбики”) носят физиологический характер и распадаются на здоровые клетки при изменении условий. Истинные агрегаты, возникающие при патологии, не распадаются, порождая явление сладжа (в переводе с английского как “отстой”). Клетки в агрегатах покрываются белковой пленкой, склеивающей их в глыбки неправильной формы.
Главным образом, вызывающим агрегацию и сладж, является нарушение гемодинамики - замедление кровотока, встречающееся при всех критических состояниях - травматическом шоке, геморрагии, клинической смерти, кардиогенном шоке и т. д. Очень часто гемодинамические расстройства сочетаются и с гиперглобулинемией при таких тяжелых состояниях, как перитонит, острая кишечная непроходимость, острый панкреатит, синдром длительного сдавления, ожоги. Усиливают агрегацию состояния жировой, амниотической и воздушной эмболии, повреждение эритроцитов при искусственном кровообращении, гемолиз, септический шок и т. д., т.е. все критические состояния.
Можно сказать, что основной причиной нарушения кровотока в капилляроне является изменение реологических свойств крови, которые в свою очередь зависят главным образом от скорости кровотока. Поэтому нарушения кровотока при всех критических состояниях проходят четыре этапа.
I этап - спазм сосудов-сопротивлений и изменение реологических свойств крови. Стрессорные факторы (гипоксия, страх, боль, травма и т.д.) ведут к гиперкатехолемии, вызывающей первичный спазм артериол для централизации кровотока при кровопотере или снижении сердечного выброса любой этиологии (инфаркт миокарда, гиповолемия при перитоните, острой кишечной непроходимости, ожогах и т.д.).
Сужение артериол сокращает скорость кровотока в капилляроне, что меняет реологические свойства крови и ведет к агрегации клеток и сладжу. С
этого начинается II этап нарушения микроциркуляции, на котором возникают следующие явления:
1. Возникает ишемия тканей, что ведет к увеличению концентрации кислых метаболитов, активных полипептидов. Однако явление сладжа характерно тем, что происходит расслоение потоков, а вытекающая из капиллярона плазма может уносить в общую циркуляцию кислые метаболиты и агрессивные метаболиты. Таким образом, функциональная способность органа, где нарушилась микроциркуляция, резко снижается.
2. На агрегатах эритроцитов оседает фибрин, вследствие чего возникают условия для развития ДВС-синдрома.
3. Агрегаты эритроцитов, обволакиваемые веществами плазмы, скапливаются в капилляроне и выключаются из кровотока - возникает секвестрация крови.
Секвестрация отличается от депонирования тем, что в “депо” физико-химические свойства крови не нарушены, и выброшенная из депо кровь включается в кровоток вполне физиологически пригодной. Секвестированная кровь же должна пройти легочный фильтр, прежде чем снова будет соответствовать физиологическим параметрам.
Если кровь секвестируется в большом количестве капилляронов, то соответственно уменьшается ее объем. Поэтому гиповолемия возникает при любом критическом состоянии, даже при тех, которые не сопровождаются первичной крово- и плазмопотерей.
III этап реологических расстройств - генерализованное поражение системы микроциркуляции. Раньше других органов страдают печень, почки, гипофиз. Мозг и миокард страдают в последнюю очередь. После того как секвестрация крови уже снизила минутный объем крови, гиповолемия с помощью дополнительного артериолоспазма, направленного на централизацию кровотока, включает в патологический процесс новые системы микроциркуляции - объем секвестированной крови растет, вследствие чего ОЦК падает.
IV этап - тотальное поражение кровообращения, нарушение метаболизма, расстройство деятельности метаболических систем.
Подводя итог вышеизложенному, можно выделить при всяком нарушении кровотока 4 этапа: нарушение реологических свойств крови, секвестрация крови, гиповолемия, генерализованное поражение микроциркуляции и метаболизма.
Причем в танатогенезе терминального состояния не имеет существенного значения, что же было первичным: уменьшение ОЦК вследствие кровопотери или уменьшение сердечного выброса из-за правожелудочковой недостаточности (острый инфаркт миокарда, например). При возникновении вышеописанного порочного круга результат гемодинамических нарушений оказывается в принципе одинаковым.
Простейшими критериями расстройств микроциркуляции могут служить: уменьшение диуреза до 0,5 мл/час на 1 кГ массы тела и менее, разница между накожной и ректальной температурой более 2° С.
Читайте также:


