Что такое токсоплазмозный менингоэнцефалит
- Что такое Токсоплазмозный энцефалит
- Что провоцирует Токсоплазмозный энцефалит
- Патогенез (что происходит?) во время Токсоплазмозного энцефалита
- Симптомы Токсоплазмозного энцефалита
- Диагностика Токсоплазмозного энцефалита
- Лечение Токсоплазмозного энцефалита
- Профилактика Токсоплазмозного энцефалита
- К каким докторам следует обращаться если у Вас Токсоплазмозный энцефалит
Что такое Токсоплазмозный энцефалит
Возбудитель - Toxoplasma gondii относится к простейшим. Тип Protozoa. Подтип Sporozoa (обычно образуют споры; реснички, жгутики или псевдоподии отсутствуют). Класс Telosporea (имеется фаза полового размножения). Подкласс Coccidea (трофозоиты располагаются внутриклеточно, имеют "верхушечный комплекс"). Отряд Eucoccideia (жизненный цикл включает чередование бесполого - шизогония и полового размножения - спорогония). Подотряд Eimeriina (половая стадия в эпителии кишки у позвоночных животных; один хозяин или чередование двух хозяев; спорозоиты находятся в "споре"). Вид Toxoplasma gondii. Существует в трех основных формах: трофозоиты (эндозоиты), цисты и ооцисты. Трофозоиты имеют размеры 4-7 мкм в длину и 2-4 мкм в ширину, по форме напоминают полумесяц, хорошо окрашиваются по Романовскому. Они размножаются внутриклеточно во всех клетках млекопитающих за исключением безъядерных (эритроциты) и обнаруживаются в тканях в острой стадии инфекции. Скопление трофозоитов внутри одной клетки называют псевдоцистой. На трофозоиты активно воздействуют различные химиопрепараты (хлоридин, сульфаниламиды, макролиды и др.), они нестойки вне клетки и во внешней среде, быстро погибают при высушивании, прогревании, под влиянием дезинфицирующих средств.
Цисты формируются в организме хозяина, имеют собственную плотную оболочку. Размеры их до 100 мкм, внутри содержится 3000-5000 паразитов и более. Через плотную оболочку цист не проникают ни антитела, ни лекарственные препараты. Они очень устойчивы к различным воздействиям и в организме хозяина сохраняются десятки лет. Большая часть их локализуется в скелетных мышцах, миокарде, центральной нервной системе.
Ооцисты представляют собой образования овальной формы диаметром 10-12 мкм. Они формируются в слизистой оболочке тонкой кишки некоторых представителей семейства кошачьих и выделяются с испражнениями. Сроки появления ооцист в испражнениях кошки зависят от характера инфицирования и составляют от 3 до 24 дней. Экскреции продолжаются от 7 до 20 дней, за сутки с испражнениями может выделяться до 10 млн ооцист. Споруляция в выделенных фекалиях происходит через 2-3 дня (при температуре 24°С); она не реализуется при температуре ниже 4°С и выше 37°С. Ооцисты при благоприятных условиях сохраняются во внешней среде до 1 года и более. Именно они играют основную роль в передаче инфекции.
Культивируются токсоплазмы путем заражения лабораторных животных (белые мыши, морские свинки, кролики, хомяки), в развивающихся куриных эмбрионах, а также в культуре тканей. Имеются различные штаммы токсоплазм, некоторые из них отличаются высокой вирулентностью (штамм RH) и быстро приводят к гибели лабораторных животных, другие - маловирулентные (авирулентные) обычно не вызывают заметных клинических проявлений болезни.
Воротами инфекции чаще служат органы пищеварения, хотя известны случаи внутрилабораторных заражений высоковирулентными штаммами токсоплазм при повреждении кожи (пипеткой или шприцем с культурой токсоплазм). Внедрение возбудителя происходит в нижних отделах тонкой кишки, затем с током лимфы токсоплазмы достигают регионарных (мезентериальных) лимфатических узлов. Здесь развиваются воспалительные изменения с формированием инфекционных гранулем, напоминающих по клеточному составу туберкулезные или бруцеллезные гранулемы. Мезентериальные лимфатические узлы значительно увеличиваются. Затем токсоплазмы попадают в кровь, разносятся по всему организму и фиксируются в различных органах и тканях (печень, селезенка, лимфатические узлы, нервная система, глаза, миокард, скелетные мышцы). В этих органах образуются скопления паразитов в виде цист, которые могут сохраняться в организме десятки лет и даже пожизненно. В местах фиксации возникают воспалительные очаги, а в некоторых органах (нервная система, скелетные мышцы) - очажки некроза, в которых затем откладываются соли кальция и образуются кальцинаты.
В результате жизнедеятельности паразита и выделения антигенов и аллергенов наступает аллергическая перестройка организма (по типу реакций гиперчувствительности замедленного типа) и вырабатываются антитела, которые выявляются в различных иммунных реакциях (РСК, реакция с красителем Сэбина-Фельдмана, РПГА, ИФА и др.). В развитии иммунитета большое значение имеют как клеточные, так и гуморальные факторы. Наличие антител предохраняет от нового заражения даже высоковирулентными штаммами токсоплазм и обусловливает бессимптомное (латентное) течение токсоплазмоза у большинства инфицированных лиц. При ослаблении защитных сил организма и снижении напряженности иммунитета может наступить обострение заболевания (переход латентной формы в манифестную).
Обострение хронического токсоплазмоза, как правило, провоцируется интеркуррентными заболеваниями (грипп, ОРЗ, пневмонии и др.) и может наблюдаться иногда спустя длительное время (до 10-20 лет) после инфицирования. Описаны обострения с развитием тяжелого токсоплазмозного энцефалита после лечения лиц с латентным токсоплазмозом цитостатиками и иммунодепрессантами. В последние годы важное значение приобрела проблема генерализации латентного токсоплазмоза у ВИЧ-инфицированных. В этих случаях токсоплазмоз приобретает острое злокачественное течение с развитием некротического локализованного или диффузного менингоэнцефалита, в процесс вовлекаются глаза и многие органы (сердце, печень, легкие). На фоне развернутой картины СПИДа наслоившееся обострение (генерализация токсоплазмоза) может приводить к гибели больных.
Основная роль в развитии токсоплазмоза у лиц с иммуносупрессией отводится нарушениям продукции цитокинов. Показано, что при развитии токсоплазмоза на фоне ВИЧ-инфекции резко снижается как концентрация сывороточного гамма-интерферона, так и его способность активировать макрофаги. К факторам защиты относят интерлейкин-12, ФНО-, CD-8+, к факторам, способствующим генерализации заболевания - интрелейкины-4, -6, -10.
В патогенезе манифестных форм хронического токсоплазмоза основную роль играет развитие реакций гиперчувствительности замедленного типа к антигенам токсоплазм и продуктам их жизнедеятельности.
Токсоплазмозный энцефалит служит основной причиной заболеваемости и смертности у больных со СПИДом. Заболеваемость токсоплазмозным энцефалитом среди больных этой категории, имеющих антитела к токсоплазмам, колебалась от 6 до 12%. На основании этого полагают, что имелось приблизительно 170 случаев токсоплазмозного энцефалита среди 7000 больных СПИДом, о которых сообщалось в 1984 г., а развитие еще 150 случаев ожидается среди 7000 больных, которые должны заболеть СПИДом по прогнозу на 1985 г.
Частота случаев токсоплазмозного энцефалита у больных со СПИДом и энцефалитом, как сообщалось, колебалась от 25 до 80%. Диагноз токсоплазменного энцефалита следует иметь в виду у лиц с заболеванием центральной нервной системы, не относящихся к группе риска по СПИДу, так как гетеросексуальная передача вируса лейкоза Т-клеток человека (HTLV III) приводит к развитию СПИДа у лиц, не относящихся к типичным группам повышенного риска.
К внешним признакам и симптомам токсоплазменного энцефалита у больных со СПИДом относят озноб, лихорадку, головную боль, припадки, депрессию и неврологические нарушения; эти проявления могут возникать в сочетании с хориоретинитом. У большинства больных со СПИДом и токсоплазмозным энцефалитом в сыворотке отсутствуют специфические антитела, указывающие на наличие острого токсоплазмоза. Демонстрация повышения титра антител к токсоплазмам в спинномозговой жидкости, но не в сыворотке свидетельствует о токсоплазмозном энцефалите у больных со СПИДом.
В спинномозговой жидкости выявляют плеоцитоз, повышение содержания белка и гипогликорахию; в препаратах из центрифугата спинномозговой жидкости могут быть обнаружены тахизоиты. При исследовании спинномозговой жидкости (или тканей мозга) на наличие вирусов методами культивирования необходимо тщательно контролировать клеточные культуры с целью обнаружения токсоплазм, также способных вызывать формирование бляшек или обширные цитопатические эффекты. Клеточные культуры могут быть окрашены красителем Гимзы.
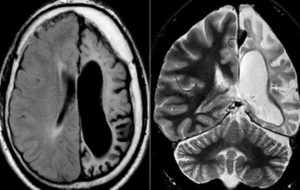
При компьютерной томографии головного мозга наблюдаются признаки диффузного энцефалита и/или одного или нескольких очагов объемного поражения. Внутривенное введение контрастного вещества может выявить кольцевидные, узелковые, мишеневидные поражения в коре или белом веществе, при этом отмечается тенденция к локализации этих поражений глубоко в пределах базальных ганглиев. В начальной фазе инфекционного процесса отклонения от нормы на сканограммах головного мозга выявляются не всегда; иногда первые признаки нарушений впервые могут появиться спустя несколько недель после заражения.
Исследования с задержкой в 1 ч с двойной дозой контрастного вещества помогают выявить поражения, неразличимые на простых сканограммах. При возможности следует произвести биопсию пораженных участков головного мозга, обнаруженных на сканограммах, так как дифференциальная диагностика этих поражений включает энцефалиты, вызываемые грибками родов Candida и Aspergillus, микобактериями и Cryptococcus neoformans, равно как и многоочаговую лейкоэнцефалопатию и лимфому.
При стандартных методах окраски токсоплазмы обнаруживаются только в 50% биоптатов головного мозга от больных с токсоплазмозным энцефалитом. Однако при использовании специфических иммуногистологических методов окрашивания тахизоиты, цисты и/или антигены токсоплазм обнаруживают в биоптатах, полученных от большинства зараженных больных.
Если у больных СПИДом появляются неврологические признаки или симптомы, а на сканограмме головного мозга очаговых изменений не выявляется, однако отмечается положительный тест Сейбина-Фельдмана или высокий уровень IgG в реакции непрямой флюоресценции антител (НФА), целесообразно проведение пробного лечения токсоплазмозного энцефалита. Если при компьютерной томографии на сканограммах выявляются очаговые нарушения, антитела к токсоплазмам, а проведение биопсии затруднено локализацией очагов поражения или клиническим состоянием больного, следует начать предварительное лечение токсоплазмоза.
В подобных случаях положительный эффект от проводимого лечения, наблюдающийся в течение первых 7- 10 дней, подтверждает диагноз токсоплазмозного энцефалита. Если лечение осуществляли с применением кортикостероидов, признаки улучшения, выявленные рентгенографическими методами, не обеспечивают надежного свидетельства в пользу терапевтического эффекта.
При установлении диагноза энцефалита больной должен быть госпитализирован в специализированное (инфекционное) или неврологическое отделение. Назначают строгий постельный режим. Больной нуждается в постоянном наблюдении.
На догоспитальном этапе показано применение дегидратационных средств (лазикс, диакарб).
При выраженных менингеальных и энцефалитических симптомах (сильная головная боль, боль в мышцах, токсикоз, рвота, очаговые симптомы) вводят изотонический раствор натрия хлорида, раствор Рингера-Локка. Одновременно подкожно или внутримышечно вводят витамины группы В, аскорбиновую кислоту (не менее 1,5 г в сутки).
Если стандартная схема лечения с применением хлоридина (по 25 мг в сутки), трисульфапиримидина (по 6 - 8 г) или сульфадизина неэффективна, суточную дозу хлоридина следует увеличить до 50 мг. В случае развития у больного неблагоприятной реакции на сульфаниламидный препарат рекомендуется использовать только пириметамин в дозе 50 мг в сутки. Необходимо применять фолиевую кислоту в дозе до 15 мг в сутки, особенно когда отмечается депрессия костного мозга в результате воздействия хлоридина. Однако если депрессия костного мозга у больных со СПИДом обусловлена иммунными механизмами, профилактический прием фолиевой кислоты не устраняет лейкопению.
Меры по профилактике инвазии включают вмешательство в цикл передачи, и их соблюдение особенно важно для больных с иммунодефицитом и серонегативных беременных женщин. Очень важно, чтобы больные из групп риска знали о том, как можно избежать заражения цистами (плохая кулинарная обработка мяса) и спорулированными ооцистами (при контактах с домашними кошками).
Для уничтожения цист мясо следует прогревать до 60°С или замораживать при - 20°С. (Бытовые морозильные камеры не способны создавать и поддерживать такую температуру.) После приготовления пищи из сырого мяса руки следует тщательно мыть; необходимо также мыть фрукты и овощи, которые могут быть загрязнены ооцистами. Обработка продуктов сухим жаром (66°С) или кипящей водой делает ооцисты неинфективными. Следует избегать контактов с экскрементами кошек.
Данных, позволяющих дать четкие рекомендации относительно использования цельной крови, переливания лейкоцитов или трансплантации органов в случае обнаружения у донора антител против токсоплазм нет. Вместе с тем не следует использовать кровь или продукты крови, полученные от лиц с наличием антител против токсоплазм, для переливания больным с иммуносупрессией, а органы для трансплантации серонегативным реципиентам следует брать от лиц с отрицательными серологическим реакциями на токсоплазмоз.
Токсоплазменный энцефалит – угрожающее жизни заболевание, которое регистрируют преимущественно у ВИЧ-инфицированных или больных СПИДом лиц.
Патогенез заболевания
Заболевание провоцирует Toxoplasma gondii, относящаяся к простейшим. Микроорганизм проникает в тело человека через желудочно-кишечный тракт, однако существует вероятность заражения через поврежденную кожу.
Из тонкого отдела кишечника токсоплазма попадает в лимфатическую систему, внедряясь в регионарные узлы, провоцируя гранулематозное воспаление.
Из увеличенных лимфатических узлов возбудитель проникает в кровь, распространяясь по организму и образуя в органах и тканях своеобразные скопления (цисты).
В местах агломерации развиваются воспалительные процессы, в том числе с последующей кальцинацией.
Паразит выделяет антигены, в ответ на которые, иммунная система синтезирует антитела. Эти антитела препятствуют новому инфицированию. Они подавляют, но, как правило, не уничтожают инфекцию, которая уже закрепилась в организме, что обуславливает ее латентное течение. В таком состоянии паразит может существовать в теле человека десятки лет и никогда не проявляться.
Обострение возникает в связи с развитием другого инфекционного недуга на фоне хронического токсоплазмоза (пневмония, грипп, простуда) или в результате применения препаратов, подавляющих иммунитет.
В особую группу риска попадают ВИЧ-инфицированные люди, у которых обострение токсоплазмозной инфекции ведет к развитию менингоэнцефалита с вовлечением в процесс внутренних органов. Таким пациентам, болезнь грозит серьезными осложнениями, вплоть до летального исхода.
У людей с поражениями иммунной системы нарушается синтез цитокинов, что позволяет возбудителю активироваться. Токсоплазмоз, который развивается при наличии ВИЧ-инфекции, способствует снижению концентрации гамма-интерферона в плазме крови и подавляет активацию макрофагов.
В таких условиях простейшие бесконтрольно размножаются, что приводит к манифестации болезни.
Симптомы токсоплазмозного энцефалита
Данная патология широко распространена среди людей, больных СПИДом. Для большинства заболевших токсоплазмозный энцефалит заканчивается летально. Среди больных СПИДом, у которых зарегистрирован энцефалит, в 25- 80% случаев он обусловлен наличием токсоплазмы.
Первыми признаками заболевания выступает лихорадка, которая сопровождается помрачением сознания, психическими и неврологическими нарушениями. В некоторых случаях лихорадка отсутствует, а патология проявляется эпилептическим приступом без другой характерной симптоматики.
Больные жалуются на головную боль на фоне повышения температуры до субфебрильных или фебрильных показателей. Позднее появляются неврологические и поведенческие нарушения, депрессивные состояния.
Менингеальные симптомы проявляются:
- интенсивной головной болью;
- общей слабостью;
- ригидностью мышц затылка;
- тошнотой и рвотными позывами;
- симптомами Бехтерева, Кернинга, Брудзинского.
У некоторых больных токсоплазмозный менингоэнцефалит протекает в атипичной форме, что затрудняет постановку диагноза.
Диагностика токсоплазмозного энцефалита
Диагностика должна быть комплексной. Лечащий врач собирает анамнез больного, проводит осмотр и направляет пациента на дополнительные обследования и анализы.
Для выявления признаков инфекции проводят пункцию спинномозгового канала и исследуют ликвор. При наличии возбудителя обнаруживают повышенное количество лейкоцитов, белка и пониженное содержание сахара в спинномозговой жидкости. Посев на питательные среды и последующее исследование микроорганизмов под микроскопом выявляет токсоплазму. В некоторых случаях паразита удается выявить в центрифугате ликвора.

Проводят исследование головного мозга при помощи компьютерной томографии или магнитно-резонансной томографии. Энцефалит токсоплазмозной этиологии проявляется признаками диффузного воспаления тканей мозга с очагами поражения. В некоторых случаях очаги могут отсутствовать. Исследование с контрастным веществом выявляет в тканях головного мозга дефекты в форме узелков или колец, преимущественно в области базальных ганглиев.
На ранних этапах заболевания структурные изменения в мозге могут отсутствовать, но спустя несколько недель они будут отчетливо видны на снимках. При первых клинических проявлениях болезни целесообразно проводить исследование с задержкой и увеличенной дозой контраста, что позволяет выявить минимальные дефекты.
Желательно взять биопсию из пораженных участков, чтобы дифференцировать болезнь от воспалительных процессов, провоцируемых патогенными грибами и микобактериями, а также от новообразований. Биоптат направляют на гистологическое исследование, проводят окраску срезов. Стандартное окрашивание позволяет выявить возбудителя в половине случаев. Для увеличения достоверности метода используют иммуногистологические методики, выявляющие не только простейших и цисты, но и антигены.
Серологические исследования плазмы крови выявляют высокие титры иммуноглобулина G в НФА, а реакция Сейбина-Фельдмана дает положительный результат. Это позволяет своевременно начать лечение токсоплазмоза при отсутствии явных структурных изменений на КТ или МРТ снимках.
Если все проведенные исследования дают сомнительный результат, однако токсоплазмозный энцефалит не был исключен, то назначают пробное лечение и следят за динамикой состояния пациента.
Токсоплазмозный менингоэнцефалит: лечение заболевания
Лечение проводится в условиях стационара неврологического отделения. Больной должен соблюдать постельный режим, а терапия осуществляется под постоянным наблюдением специалистов. Для предотвращения отека мозга используют мочегонные средства, выводящие лишнюю жидкость из организма.
Энцефалические и менингеальные симптомы устраняют при помощи инфузионного введения физиологического раствора и раствора Рингера, витамина С и витаминов В.
Для борьбы с токсоплазмой используют следующие схемы:
- Внутрь 1-1,5 г сульфадиазина четыре раза в сутки, в сочетании с 0,05 г пириметамина два раза в сутки. Препараты необходимо принимать в вышеуказанных дозах в течение трех дней, после чего дозировку сокращают в два раза. Дополнительно следует принимать по 0,045 г фолината кальция один раз в семь дней.
- Внутривенно 0,6 г Клиндамицина четыре раза в сутки, и внутрь 0,05 г пириметамина два раза в сутки. Через три дня дозировку уменьшают в два раза + 0,045 г фолината кальция один раз в семь дней.
- Внутрь суспензию Атовакона по 1,5 г и Пириметамин по 0,05 г по два раза в сутки. После трех дней лечения дозу снижают в два раза. Фолинат кальция по 0,045 г один раз в семь дней.
Учитывая сложность лечения менингоэнцефалита, курс рассчитан на 4-6 недель. Как правило, при своевременно начатой терапии, улучшения наступают спустя несколько суток после применения противомикробных препаратов. Параллельно с этиотропной терапией проводят симптоматическое лечение противовоспалительными, обезболивающими, противосудорожными препаратами.
Профилактика заболевания
Профилактика заключается в недопущении инфицирования токсоплазмозом, особенно людей с ВИЧ-инфекцией и беременных женщин, своевременной диагностике и лечении несложной формы заболевания.
Токсоплазма попадает в организм человека после контакта с домашними животными, или при употреблении в пищу недостаточно обработанных продуктов животного происхождения.
- Людям с иммунодефицитом желательно отказаться от общения с питомцами, либо строго соблюдать правила гигиены. Чистку кошачьего туалета следует осуществлять в резиновых перчатках.
- Важно избегать употребления в пищу мяса, не прошедшего полноценную термическую обработку.
- ВИЧ-инфицированным с обнаруженными антителами к токсоплазме назначают профилактическое лечение сульфаметоксазолом или Дапсоном.
- Больным, перенесшим токсоплазмозный энцефалит надо пожизненное поддерживающее лечение. Без постоянного приема антибактериальных препаратов у подавляющего большинства больных случаются рецидивы.
При необходимости гемотрансфузии ВИЧ-инфицированным пациентам, надо использовать донорскую кровь без антител к токсоплазмам.

Общие сведения
Патогенез
Развитие болезни провоцируют вирусы (вирус клещевого энцефалита, вирус Западного Нила) бактерии (Neisseria meningitidis, Listeria monocytogenes, Treponema pallidum, Rickettsia prowazekii), простейшие (Toxoplasma gondii, Trypanosoma brucei, Naegleria fowleri (неглерия Фоулера)).
После того, как возбудитель внедряется в организм, в тканях мозга развивается воспалительный процесс. Его характер зависит от типа инфекционного агента. В процессе развития болезни развиваются периваскулярные воспалительные инфильтраты, вследствие чего ухудшается церебральное кровообращение. Далее происходит ишемия, активизируется выработка ликвора, и это приводит к повышению внутричерепного давления. Происходит раздражение оболочек мозга, развивается менингеальный синдром.
В процессе воспаления церебрального вещества образуются разнообразные воспалительные фокусы. Так как функции нейронов, расположенных в очагах воспаления, нарушаются, формируется очаговая симптоматика. Происходит массовая гибель нервных клеток, возникает стойкий неврологический дефицит.
Классификация
В современной медицине менингоэнцефалиты классифицируют согласно с несколькими разными критериями.
С точки зрения этиологии болезни выделяют такие ее типы:
- Вирусный – его развитие провоцируют вирусы гриппа, кори, герпеса, энтеровирусы, цитомегаловируси др. Отличается серозным характером изменений.
- Бактериальный – его провоцируют пневмо-, стрепто-, менингококки, клебсиелла, гемофильная палочка. Для этого типа характерен гнойный характер изменений.
- Протозойный – редкий тип заболевания, который провоцируют токсоплазмы, амебы и другие простейшие.
- Грибковый – в основном развивается у людей с нарушенными функциями иммунной системы. Иногда диагностируется у людей с ВИЧ/СПИД.
С учетом типа воспалительного процесса используется следующая классификация заболевания:
- Гнойный – в процессе развития воспалительного процесса происходит образование гноя, что приводит к помутнению ликвора. Отмечается преобладание лейкоцитов.
- Серозный – в процессе развития воспаления образуется серозное отделяемое. Цереброспинальная жидкость при этом прозрачная, преобладают лимфоциты.
- Геморрагический – для этого типа характерно нарушение проницаемости стенок мозговых сосудов. Как следствие, происходят петехиальные кровоизлияния в тканях.
С учетом особенностей протекания клинического процесса применяется такая классификация:
- Молниеносный – развивается очень быстро, на протяжении нескольких часов. В большинстве случаев такая форма заболевания завершается летально.
- Острый – в этом случае симптомы нарастают уже медленнее. Их развитие отмечается на протяжении 1-2 суток.
- Подострый – процесс развивается постепенно, ухудшение состояния больного занимает период от 1 суток до 1 недели.
- Хронический – воспаление может продолжаться долго, от нескольких месяцев до нескольких лет. Периодически возникают обострения и ремиссии. Острый и подострый типы болезни могут постепенно перерасти в хроническую форму.
В свою очередь, острый менингоэнцефалит может быть первичным и вторичным.
- Первичный – эта форма развивается непосредственно в головном мозге вследствие воздействия разнообразных возбудителей.
- Вторичный – является осложнением другой болезни ввиду ослабления иммунитета.
Также выделяют несколько типов болезни в зависимости от возбудителя:
- Туберкулезный – развивается на фоне заболевания туберкулезомлегких или вследствие контакта с людьми, болеющими открытой формой туберкулеза. Лечение этого недуга проводится в специализированном стационаре специалистами-фтизиатрами.
- Герпетический – болезнь угрожает серьезными последствиями. В процессе развития отмечаются выраженные мозговые и токсические симптомы, нарастающий отек мозга, отмирание нейронов. Этот тип болезни может встречаться у новорожденных, так как заражение часто происходит в процессе родов, или еще до рождения – через плаценту. Однако эта форма поражает и взрослых людей.
- Гнойный менингоэнцефалит – этот тип воспалительного процесса вызывают стрептококки групп В или D, гемофильная или кишечная палочки и др. Чаще всего такая форма болезни поражает людей с иммунодефицитом, а также тех, кто недавно перенес травмы головы или операции в этой области. Патогенные микроорганизмы, провоцирующие развитие этой формы болезни, активнее размножаются, если в организме есть очаги хронической инфекции. Как правило, протекает остро, но возможно и молниеносное, а также хроническое течение.
- Гриппозный геморрагический – развивается после перенесенного гриппа. В таком случае у человека быстро поднимается температура тела, отмечается помутнение сознания, больной может впасть в кому.
- Менингоэнцефалит двуволновой вирусный – болезнь переносят иксодовые клещи, которые заражают животных, а люди, в свою очередь, инфицируются, потребляя зараженное молоко. Развивается, как правило, весной и летом, когда повышается активность клещей. Протекает тяжело. Болезнь начинается с головной боли, повышения температуры, рвоты. Через несколько дней состояние больного улучшается, но спустя еще десять дней начинается вторая стадия болезни, когда нарушается работа мозговых центров.
- Токсоплазмозный – эту форму провоцируют простейшие. В процессе развития болезни поражаются внутренние органы, нервная система, отмечается нарушение координации и боли в мышцах.
- Вакцинальный — проявляется через 1-2 недели после вакцинации.
- Гуммозный – проявляется при третичном сифилисе.
- Орнитозный — серозно-геморрагическая форма, развивающаяся при тяжелом протекании орнитоза.
- Паротитный – спровоцированный вирусом паротита.
- Ревматический – развивается на фоне ревматизма.
- Цитомегалический – поражает новорожденных и грудничков при цитомегалии.
- Амебный – редкая форма. Заражение может произойти в пресноводном водоеме. Его вызывает одноклеточный организм неглерия Фоулера. Неглериоз протекает стремительно и поражает нервную систему.
- Бруцеллезный – происходит поражение мягких тканей оболочек мозга, где образуются бруцеллезные гранулемы. Тяжело поддается лечению, вызывает паралич и нарушения психики.
Причины
Основной причиной развития этого заболевания является инфекция. Нейротропные возбудители проникают в церебральные структуры, либо инфекционный процесс распространяется из очагов, расположенных поблизости, или вследствие общих инфекционных болезней.
Инфицирование возможно вследствие таких явлений:
- Когда возбудитель попадает в носоглотку. Человек заражается воздушно-капельным путем, алиментарным способами. В полость черепа инфекция попадает гематогенным путем.
- Когда человека кусает насекомое. Заражение происходит трансмиссивным путем. Насекомое переносит возбудитель, который во время укуса попадает в кровь и с ней – в церебральные ткани.
- Когда в организме развиваются инфекционные процессы. Если человек болеет сифилисом, туберкулезом, или же у него развиваются гнойные процессы (отит, гайморит и др.), может произойти гематогенное распространение бактериальной инфекции. Иногда менингоэнцефалит у детей и взрослых развивается после перенесенного ОРВИ. Болезнь может стать осложнением энцефалита, менингита, ветрянки, краснухи, кори.
- После того, как произошла черепно-мозговая травма. Если травма у детей или взрослых открытая, существует вероятность инфицирования контактным путем. Как свидетельствует статистика, посттравматический менингоэнцефалит диагностируется примерно у 1-3,5% людей с ЧМТ.
- После того, как была проведена вакцинация. Если иммунитет ослаблен, и при этом была введена живая вакцина, может развиваться инфекционный процесс. Возбудители проникают через гематоэнцефалический барьер.
Однако важно понимать, что далеко не всегда после попадания в организм инфекционных агентов развивается эта грозная болезнь. Ее проявлению способствуют следующие факторы:
- ослабленный организм;
- незрелая иммунная система;
- иммунодефицит;
- аутоиммунные реакции;
- массивное инфекционное поражение.
Симптомы воспаления головного мозга
В процессе развития менингоэнцефалита, являющегося очень тяжелым заболеванием, развиваются общие септические симптомы. Симптомы воспаления коры головного мозга и его оболочек могут быть следующими:
- резко поднимается температура тела, начинается озноб;
- ощущаются позывы к рвоте;
- сильно болит голова;
- отсутствует аппетит;
- ухудшается слух;
- отмечается светобоязнь, повышенная чувствительность к звукам;
- могут развиваться судороги;
- наблюдается ригидность затылочных мышц;
- повышается давление;
- отмечается заторможенность.
Если происходит воспаление коры или оболочек мозга, отмечаются и специфические симптомы тканей мозга:
- нарушается координация;
- иногда возникают высыпания на коже;
- поражаются нервы черепа;
- развивается анизорефлексия.
Симптомы воспаления сосудов головного мозга и его коры у детей проявляется аналогично. Вместе с резким подъемом температуры тела отмечаются признаки интоксикации организма: сильная головная боль, тошнота и рвота. Острое воспаление сосудов и коры влияет на нервную систему и провоцирует развитие повышенной чувствительности к внешним раздражителям, проявление общего беспокойства.
Следует учесть, что клиническая картина болезни развивается очень быстро, и признаки этого заболевания начинают проявляться уже в первые-вторые сутки. В это время отмечается напряженность мышц затылка и спины, и этот симптом наиболее заметен у маленьких детей.
Важно учесть, что при проявлении ряда признаков неотложную помощь нужно вызывать сразу же. Насторожить должны такие признаки:
- судороги;
- потеря сознания;
- дезориентация;
- парезы;
- глазодвигательные расстройства.
Если течение менингоэнцефалита осложненное, развиваются такие проявления:
- редкое и неритмичное сердцебиение;
- расстройства речи и глотания;
- поверхностное и частое дыхание;
- состояние комы (при молниеносном течении).
При развитии отека головного мозга вероятен летальный исход.
Анализы и диагностика
Для установления диагноза врач, прежде всего, оценивает состояние больного, проводит осмотр и опрос пациента и его близких. Специалисту важно определить, не перенес ли больной недавно инфекционную болезнь, ЧМТ, укус клеща, не проводилась ли вакцинация. После этого он назначает необходимые исследования. Очень важно, чтобы при проявлении угрожающих симптомов, описанных выше, больной был сразу же доставлен в стационар.
В процессе установления диагноза могут быть назначены такие исследования:
- Неврологический осмотр – в его ходе определяется наличие менингиальных симптомов, проводится оценка общего состояния больного.
- Лабораторные исследования – оценивается картина выраженных изменений в анализе крови (лейкоцитоз, ускоренная СОЭ). Для определения возбудителя проводят посев крови на стерильность, практикуется метод полимеразной цепной реакции.
- Люмбальная пункция – дает возможность оценить спинномозговую жидкость. Если воспаление гнойное, она будет мутной, если серозное – прозрачная, если геморрагическое – с примесями крови. Для определения возбудителя жидкость исследуют микроскопически, проводят ее посев, ПЦР-диагностику.
- МРТ, КТ головного мозга – позволяют выявить уплотнение и утолщение оболочек мозга, диффузные изменения церебральных тканей. Иногда удается визуализировать очаги воспаления.
- Стереотаксическая биопсия мозга – применяют в сложных случаях для подтверждения менингоэнцефалита паразитарного происхождения и исключения опухоли.
Важно дифференцировать менингоэнцефалит от обширных инсультов, опухолей мозга, токсических поражений ЦНС, прогрессирующих дегенеративных заболеваний.
Лечение воспаления головного мозга
Так как менингоэнцефалит у взрослых и детей протекает тяжело, его лечение необходимо проводить в стационаре. Терапия болезни у взрослых и детей должна быть комплексной, ее назначают в зависимости от причины, спровоцировавшей менингоэнцефалит.
Проводится антибактериальное лечение, прием сульфаниламидных и противогрибковых средств, проводят иммунокорригирующее и дезинтоксикационное лечение. Также назначают витаминные комплексы и лекарства для улучшения реологических свойств крови, рекомендуют высококалорийное питание.
Читайте также:


