Электрическая активность нервных клеток
Информативная деятельность нервных клеток связана с их электрической активностью и осуществляется на основе синаптического возбуждения, синаптического торможения и генерации нервных импульсов. Данные процессы базируются на специфических свойствах клеточной мембраны, разделяющей внутриклеточную и внеклеточную среду. Как та, так и другая среды содержат положительные ионы натрия, калия и других элементов.
Мембрана имеет толщину 5нм и состоит из двух молекулярных слоев, в которые встроены канальные белки, образующие шлюзы для ионов внутри и внеклеточной среды. Управление закрыванием или открыванием шлюзов осуществляется с помощью электрического, либо химического механизмов. Электрически управляемые белки (ЭУБ) расположены в основном на мембране аксона и частично сомы, а химически управляемые белки (ХУБ) расположены на мембранах дендритов и сомы. Кроме того, мембрана клетки пронизана белками, реализующими функцию ионного насоса (ИН).
Белки ИН постоянно выводят из клетки ионы натрия и вводят в нее ионы калия. Так, что вне клетки ионов натрия примерно в 10 раз больше, чем внутри нее, а ионов калия, наоборот, в клетке в 10 раз больше, чем вне ее. При таких концентрациях внутренний потенциал нейрона оказывается отрицательным и составляет – 70 мВ. В невозбужденном состоянии белки ионных насосов работают непрерывно при закрытых шлюзах. Потенциал покоя постоянен.
Если под влиянием внешних факторов внутренний потенциал повысится до некоторой пороговой величины, то расположенные у основания аксона (аксоном холмике) ЭУБ откроют свои шлюзы. Через них внутрь клетки начнут поступать в большом количестве положительные ионы натрия. Локальный внутренний потенциал аксона увеличивается и достигает положительных значений (+ 40 мВ). При таких значениях шлюзы положительных ионов натрия закрываются и открываются шлюзы положительных ионов калия. В локальной области увеличенного потенциала начинают уходить положительные ионы калия, потенциал снижается до исходной величины, шлюзы закрываются и ионный насос восстанавливает потенциал покоя.. Таким образом возникает электрический импульс, называемый спайком. Длительность импульса составляет примерно 3 мсек.
Возникнув в аксоном холмике, импульс вызывает последовательное открывание шлюзов следующего по ходу аксона участков мембраны, что приводит к его перемещению по мембране аксона вплоть до терминальных волокон (синаптических бляшек).
Нейрон получает сигналы (импульсы) от других нейронов через дендриты (приемники) и передает сигналы, сгенерированные телом клетки, вдоль аксона (передатчик), который в конце разветвляется на волокна На окончаниях этих волокон находятся синапсы .
Рис. 1Схема биологического нейрона.
Синапс является элементарной структурой и функциональным узлом между двумя нейронами (волокно аксона одного нейрона и дендрит другого). Когда импульс достигает синаптического окончания, высвобождаются определенные химические вещества, называемые нейротрансмиттерами (медиаторами). Молекулы медиатора диффундируют через щель и попадают на постсинаптическую мембрану дендрита или сомы следующего нейрона. Попав на мембрану медиатор открывает расположенные здесь каналы химически управляемых белков. Если синапс возбуждающий, то медиатор открывает каналы положительных ионов натрия, если тормозящий – калия. В первом случае ионы натрия поступают в клетку и возбуждают ее, смещая внутриклеточный потенциал в положительную область, во втором - ионы калия уходят из клетки и тормозят ее, смещая внутриклеточный потенциал в отрицательную область. Результативность синапса может настраиваться проходящими через него сигналами, так что синапсы могут обучаться в зависимости от активности процессов, в которых они участвуют. Эта зависимость от предыстории действует как память, которая, возможно, ответственна за память человека. В головном мозге человека 1 мм 3 формирует независимую локальную сеть, несущую определенную функциональную нагрузку.
ИСКУССТВЕННЫЕ НЕЙРОННЫЕ СЕТИ
Искусственная нейронная сеть – это набор нейронов, соединенных между собой. Как правило, активационная функция всех нейронов в сети фиксирована, а весв являются параметроами и могут изменяться. Некоторые входы нейронов помечены как внешние входы сети, а некоторые – как выходы – как выходы сети. Подавая любые числа на входы на выходе сети получаем какой-то набор чисел. пара Таким образом, работа нейронной сети состоит в преобразовании входного вектора Х в выходной вектор У, причем это преобразование задается весами сети
Например: алфавит русского языка содержит 33 буквы. Необходимо распознать буквы алфавита.
Дано: растровое черно-белое изображение букв размером 30х30 пикселов.
Задача для нейронной сети сформировать входной вектор из 900 двоичных символов, выходной вектор должен содержать 33 символа.
Он обладает группой синапсов – однонаправленных входных связей, соединенных с выходами других нейронов, а также имеет аксон – выходную связь данного нейрона, с которой сигнал (возбуждения или торможения) поступает на синапсы следующих нейронов. Общий вид нейрона приведен на рисунке 2.
Рис.2. Схема искусственного нейрона.
Каждый синапс характеризуется величиной синаптической связи или ее весом wi, который по физическому смыслу эквивалентен электрической проводимости.
Текущее состояние нейрона определяется, как взвешенная сумма его входов:
Выход нейрона есть функция его состояния y = F(s) , которая может быть различной:
Нелинейнаяфункция F называется активационной и может иметь различный вид, как показано на рисунке 3. Одной из наиболее распространенных является нелинейная функция с насыщением, так называемая логистическая функция или сигмоид (т.е. функция S-образного вида):
При уменьшении a сигмоид становится более пологим, в пределе при a=0 вырождаясь в горизонтальную линию на уровне 0.5, при увеличении a сигмоид приближается по внешнему виду к функции единичного скачка с порогом T в точке x=0. Из выражения для сигмоида очевидно, что выходное значение нейрона лежит в диапазоне [0,1]. Одно из ценных свойств сигмоидной функции – простое выражение для ее производной.
Следует отметить, что сигмоидная функция дифференцируема на всей оси абсцисс, что используется в некоторых алгоритмах обучения. Кроме того, она обладает свойством усиливать слабые сигналы лучше, чем большие, и предотвращает насыщение от больших сигналов, так как они соответствуют областям аргументов, где сигмоид имеет пологий наклон.
МакКалок и Питтс доказали, что при соответствующем образом подобранных весах совокупность параллельно функционирующих нейронов подобного типа способна выполнять универсальные вычисления. Здесь наблюдается определенная аналогия с биологическим нейроном - передачу сигнала и взаимосвязи имитируют аксоны и дендриты, веса связей соответствуют синапсам, а пороговая функция отражает активность сомы.
ИНС может рассматриваться как направленный граф со взвешенными связями в котором искусственные нейроны являются узлами. По архитектуре связей ИНС могут быть сгруппированы в два класса (рис. 2): сети прямого распространения, в которых графы не имеют петель, и рекуррентные сети, или сети с обратными связями.
86 миллиардов нейронов. Blue Brain Project – это вычислительная часть, а Human Brain – это больше фундаментальная часть, где работают над сбором научных данных о принципах работы мозга и созданием единой модели. Чтобы прикоснуться к этой науке и попробовать самим сделать нечто подобное, хотя и в значительно меньших масштабах, была написана эта заметка.
Но в них не рассматривались вопросы вычислительной нейробиологии, или по-другому вычислительной нейронауки, включающей в себя компьютерное моделирование электрической активности нейронов, поэтому я решил восполнить этот пробел.
Возбудить нейрон можно, например, воткнув в него микроэлектрод и подав ток внутрь нейрона, но в живом мозге возбуждение обычно происходит путем синаптического воздействия. Как уже было сказано, нейроны соединяются друг с другом с помощью синапсов, образующихся в местах контакта аксона одного нейрона с дендритами другого. Нейрон, от которого идет сигнал, называется пресинаптическим, а тот к которому идет сигнал – постсинаптическим. При возникновении импульса на пресинаптическом нейроне, он выделят в синаптическую щель нейротрансмиттеры, которые открывают натриевые каналы на постсинаптическом нейроне, а дальше происходит цепь описанных выше событий, приводящих к возбуждению. Кроме возбуждения нейроны могут и тормозить друг друга. В случае если пресинаптический нейрон тормозный, то он выделят в синаптическую щель тормозный нейротрансмиттер открывающий хлорные каналы, а так как снаружи хлора больше, то хлор течет внутрь нейрона из-за чего отрицательный заряд на внутренней стороне мембраны увеличивается (не забываем, что ионы хлора в отличии от натрия и калия заряжены отрицательно), вгоняя нейрон в ещё более неактивное состояние. В таком состоянии нейрон труднее возбудить.
Где a, b, c, d, k, Cm различные параметры нейрона. Vm — это разность потенциалов на внутренней и внешней стороне мембраны, а Um — вспомогательная переменная. I — это внешний постоянный приложенный ток. В данной модели наблюдаются такие характерные для нейронов свойства как: генерация спайка в ответ на одиночный импульса внешнего тока и генерация последовательности спайков с определённой частотой при подаче на нейрон постоянного внешнего тока. Isyn — сумма синаптических токов от всех нейронов, с которыми связан этот нейрон.
В случае если на пресинаптическом нейроне генерируется спайк, на постсинаптическом происходит скачок синапического тока, который экспоненциально затухает с характерным временем.
Итак, мы приступаем к самому интересному. Пора закодить на компьютере виртуальный кусок нервной ткани. Для этого будем численно решать систему дифференциальных уравнений, задающих динамику мембранного потенциала нейрона. Для интегрирования будем использовать метод Эйлера. Кодить будем на С++, рисовать с помощью скриптов написанных на Python с использованием библиотеки Matplolib, но у кого нет Питона могут рисовать с помощью Exel.
Нам понадобятся двумерные массивы Vms, Ums размерности Tsim*Nneur для хранения мембранных потенциалов и вспомогательных переменных каждого нейрона, в каждый момент времени, Tsim это время симуляции в отсчетах, а Nneur количество нейронов в сети.
Связи будем хранить в виде двух массивов pre_con и post_con размерности Ncon, где индексами является номера связей, а значениями являются индексы пресинаптических и постсинаптических нейронов. Ncon — число связей.
Так же нам понадобится массив для представления переменной, модулирующей экспоненциально затухающий постсинаптический ток каждого синапса, для этого создаем массив y размерности Ncon*Tsim.
Как уже было сказано, информация кодируется во временах возникновения импульсов, поэтому создаем массивы для сохранения времен их возникновения и индексов нейронов где они возникли. Далее их можно будет записать в файл, с целью визуализации.
Разбрасываем случайно связи и задаем веса.
Установка начальных условий для нейронов и случайное задание внешнего приложенного тока. Те нейроны для которых внешний ток превысит порог генерации спайков, будут генерировать спайки с постоянной частотой.
Основная часть программы с интегрированием модели Ижикевича.
Полный текст кода можно скачать тут. Код свободно компилируется и запускается хоть под виндой с Visual Studio 2010 Express Edition или MinGW, хоть под GNU/Linux c GCC. После завершения работы программа сохраняет растр активности, времена и индексы возникновения нервных импульсов, и осциллограммы среднего мембранного потенциала в файлах rastr.csv и oscill.csv, соответственно. Можно их прямо в Exelе и нарисовать. Либо с помощью прикрепленных мною питоновских скриптов, но для их работы нужна библиотека Matplotlib. Для тех у кого GNU/Linux установить из репозиториев пакет python-matplotlib не составит труда, пользователям же Windows придется вручную скачать отсюда последовательно пакеты numpy, scypy, pyparsing, python-dateutil и matplotlib.
Рисование растра активности — plot_rastr.py
Рисование среднего мембранного потенциала — plot_oscill.py
Вот что получается при моделировании 1 секунды активности 125 нейронов. Мы наблюдаем периодическую активность на частоте
- 3656
- 2,3
- 1
- 7
![]()
Олег Жуков
![]()
Анна Петренко![]()
Андрей Панов




Происхождение подхода
С середины ХХ века известно, что головной мозг потребляет значительную часть энергоресурсов всего организма: четверть всей глюкозы и ⅕ всего кислорода в случае высшего примата [1–5]. Это вдохновило Уильяма Леви и Роберта Бакстера из Массачусетского технологического института (США) на проведение теоретического анализа энергетической эффективности кодирования информации в биологических нейронных сетях (рис. 1) [6]. В основе исследования лежит следующая гипотеза. Поскольку энергопотребление мозга велико, ему выгодно иметь такие нейроны, которые работают наиболее эффективно — передают только полезную информацию и затрачивают при этом минимум энергии.
Это предположение оказалось справедливым: на простой модели нейронной сети авторы воспроизвели экспериментально измеренные значения некоторых параметров [6]. В частности, рассчитанная ими оптимальная частота генерации импульсов варьирует от 6 до 43 имп./с — почти так же, как и у нейронов основания гиппокампа. Их можно подразделить на две группы по частоте импульсации: медленные (
10 имп./с) и быстрые (
40 имп./с). При этом первая группа значительно превосходит по численности вторую [7]. Аналогичная картина наблюдается и в коре больших полушарий: медленных пирамидальных нейронов (
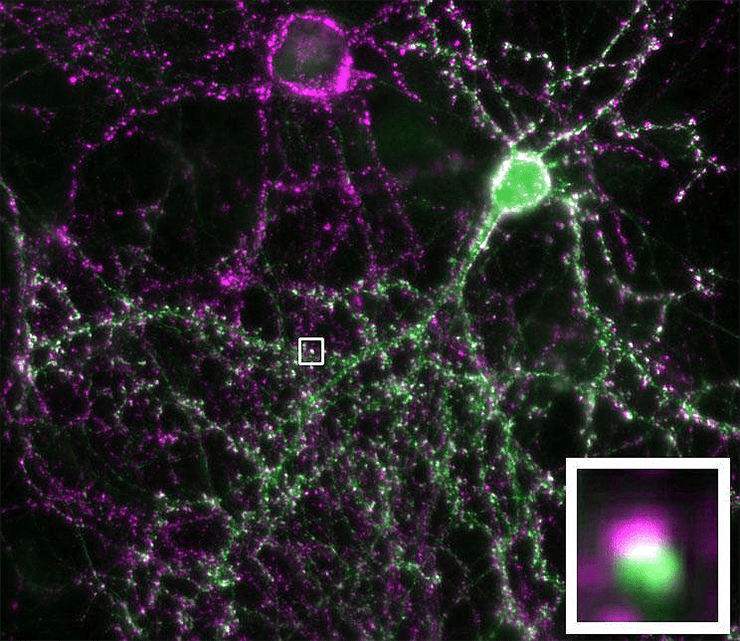
Нейроны центральной нервной системы разделяются на активирующие (образуют активирующие синапсы) и тормозящие (образуют тормозящие синапсы). Последние в значительной степени представлены интернейронами, или промежуточными нейронами. В коре больших полушарий и гиппокампе они ответственны за формирование гамма-ритмов мозга [15], которые обеспечивают слаженную, синхронную работу других нейронов. Это крайне важно для моторных функций, восприятия сенсорной информации, формирования памяти [9], [11].
За последнее время этот подход нашел множество подтверждений [10], [22], [24–26]. Он позволил по-новому взглянуть на устройство мозга на самых разных уровнях организации — от молекулярно-биофизического [20], [26] до органного [23]. Он помогает понять, каковы компромиссы между выполняемой функцией нейрона и ее энергетической ценой и в какой степени они выражены.
Положим, у нас есть модель нейрона, описывающая его электрофизиологические свойства: потенциал действия (ПД) и постсинаптические потенциалы (ПСП) (об этих терминах — ниже). Мы хотим понять, эффективно ли он работает, не тратит ли неоправданно много энергии. Для этого нужно вычислить значения параметров модели (например, плотность каналов в мембране, скорость их открывания и закрывания), при которых: (а) достигается максимум отношения полезной информации к энергозатратам и в то же время (б) сохраняются реалистичные характеристики передаваемых сигналов [6], [19].
Потенциал действия
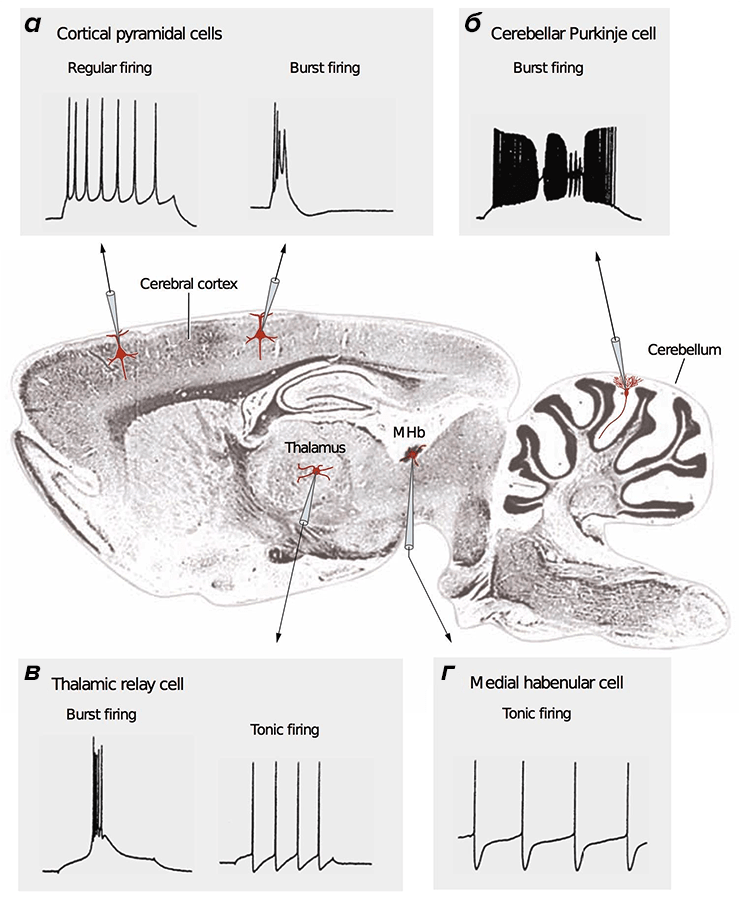
Рисунок 2. Разные типы нейронов генерируют различные сигналы. В центре — продольный срез мозга млекопитающего. Во вставках представлены разные типы сигналов, зарегистрированные методами электрофизиологии [15], [38]. а — Кортикальные (Cerebral cortex) пирамидальные нейроны могут передавать как низкочастотные сигналы (Regular firing), так и короткие взрывные, или пачечные, сигналы (Burst firing). б — Для клеток Пуркинье мозжечка (Cerebellum) характерна только пачечная активность на очень высокой частоте. в — Релейные нейроны таламуса (Thalamus) имеют два режима активности: пачечный и тонический (Tonic firing). г — Нейроны средней части поводка (MHb, Medial habenula) эпиталамуса генерируют тонические сигналы низкой частоты.
Большое разнообразие сигналов обусловлено огромным количеством комбинаций разных типов ионных каналов, синаптических контактов, а также морфологией нейронов [28], [29]. Поскольку в основе сигнальных процессов нейрона лежат ионные токи, стоит ожидать, что разные ПД требуют различных энергозатрат [20], [27], [30].
- Мембрана и ионы. Плазматическая мембрана нейрона поддерживает неравномерное распределение веществ между клеткой и внеклеточной средой (рис. 3б) [31–33]. В числе этих веществ есть и маленькие ионы, из которых для описания ПД важны К + и Nа + .
Ионов Na + внутри клетки мало, снаружи — много. Из-за этого они постоянно стремятся попасть в клетку. Напротив, ионов К + много внутри клетки, и они норовят из нее выйти. Самостоятельно ионы этого сделать не могут, потому что мембрана для них непроницаема. Для прохождения ионов через мембрану необходимо открывание специальных белков — ионных каналов мембраны.
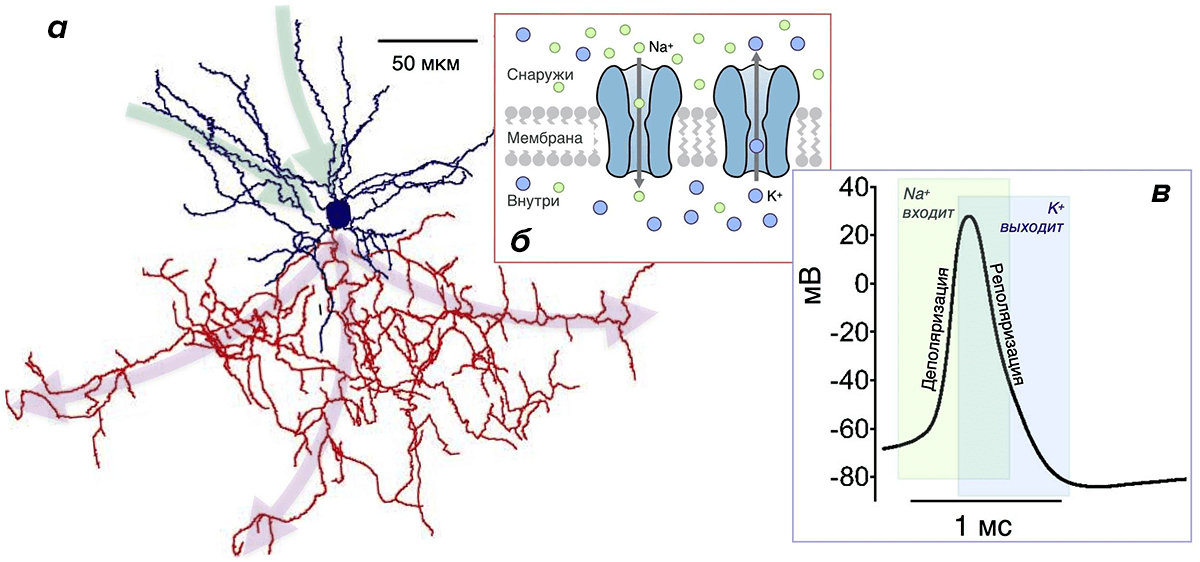
Рисунок 3. Нейрон, ионные каналы и потенциал действия. а — Реконструкция клетки-канделябра коры головного мозга крысы. Синим окрашены дендриты и тело нейрона (синее пятно в центре), красным — аксон (у многих типов нейронов аксон разветвлен намного больше, чем дендриты [8], [11], [35]). Зеленые и малиновые стрелки указывают направление потока информации: дендриты и тело нейрона принимают ее, аксон — отправляет ее к другим нейронам. б — Мембрана нейрона, как и любой другой клетки, содержит ионные каналы. Зеленые кружки — ионы Na + , синие — ионы К + . в — Изменение мембранного потенциала при генерации потенциала действия (ПД) нейроном Пуркинье. Зеленая область: Na-каналы открыты, в нейрон входят ионы Na + , происходит деполяризация. Синяя область: открыты К-каналы, К + выходит, происходит реполяризация. Перекрывание зеленой и синей областей соответствует периоду, когда происходит одновременный вход Na + и выход К + .
ПД — это относительно сильное по амплитуде скачкообразное изменение мембранного потенциала.
Анализ разных типов нейронов (рис. 4) показал, что нейроны беспозвоночных не очень энергоэффективны, а некоторые нейроны позвоночных почти совершенны [20]. По результатам этого исследования, наиболее энергоэффективными оказались интернейроны гиппокампа, участвующего в формировании памяти и эмоций, а также таламокортикальные релейные нейроны, несущие основной поток сенсорной информации от таламуса к коре больших полушарий.
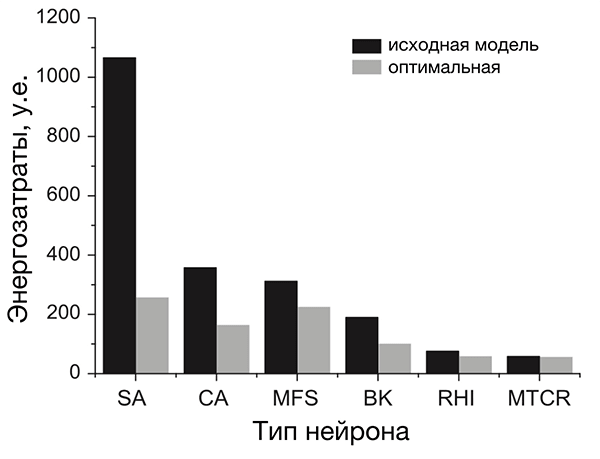
Рисунок 4. Разные нейроны эффективны по-разному. На рисунке представлено сравнение энергозатрат разных типов нейронов. Энергозатраты рассчитаны в моделях как с исходными (реальными) значениями параметров (черные столбцы), так и с оптимальными, при которых с одной стороны нейрон выполняет положенную ему функцию, с другой — затрачивает при этом минимум энергии (серые столбцы). Самыми эффективными из представленных оказались два типа нейронов позвоночных: интернейроны гиппокампа (rat hippocampal interneuron, RHI) и таламокортикальные нейроны (mouse thalamocortical relay cell, MTCR), так как для них энергозатраты в исходной модели наиболее близки к энергозатратам оптимизированной. Напротив, нейроны беспозвоночных менее эффективны. Условные обозначения: SA (squid axon) — гигантский аксон кальмара; CA (crab axon) — аксон краба; MFS (mouse fast spiking cortical interneuron) — быстрый кортикальный интернейрон мыши; BK (honeybee mushroom body Kenyon cell) — грибовидная клетка Кеньона пчелы.
Кстати, интернейроны гораздо более активны, чем большинство других нейронов мозга. В то же время они крайне важны для слаженной, синхронной работы нейронов, с которыми образуют небольшие локальные сети [9], [16]. Вероятно, высокая энергетическая эффективность ПД интернейронов является некой адаптацией к их высокой активности и роли в координации работы других нейронов [20].
Синапс
Передача сигнала от одного нейрона к другому происходит в специальном контакте между нейронами, в синапсе [12]. Мы рассмотрим только химические синапсы (есть еще электрические), поскольку они весьма распространены в нервной системе и важны для регуляции клеточного метаболизма, доставки питательных веществ [5].
Такие синапсы называются возбуждающими: они способствуют активации нейрона и генерации ПД. Существуют также и тормозящие синапсы. Они, наоборот, способствуют торможению и препятствуют генерации ПД. Часто на одном нейроне есть и те, и другие синапсы. Определенное соотношение между торможением и возбуждением важно для нормальной работы мозга, формирования мозговых ритмов, сопровождающих высшие когнитивные функции [49].
Что еще?
Энергетическая эффективность клеток мозга исследуется также и в отношении их морфологии [35], [52–54]. Исследования показывают, что ветвление дендритов и аксона не хаотично и тоже экономит энергию [52], [54]. Например, аксон ветвится так, чтобы суммарная длина пути, который проходит ПД, была наименьшей. В таком случае энергозатраты на проведение ПД вдоль аксона минимальны.
Снижение энергозатрат нейрона достигается также при определенном соотношении тормозящих и возбуждающих синапсов [55]. Это имеет прямое отношение, например, к ишемии (патологическому состоянию, вызванному нарушением кровотока в сосудах) головного мозга. При этой патологии, вероятнее всего, первыми выходят из строя наиболее метаболически активные нейроны [9], [16]. В коре они представлены ингибиторными интернейронами, образующими тормозящие синапсы на множестве других пирамидальных нейронов [9], [16], [49]. В результате гибели интернейронов, снижается торможение пирамидальных. Как следствие, возрастает общий уровень активности последних (чаще срабатывают активирующие синапсы, чаще генерируются ПД). За этим немедленно следует рост их энергопотребления, что в условиях ишемии может привести к гибели нейронов.
Еще раз обо всем
В конце ХХ века зародился подход к изучению мозга, в котором одновременно рассматривают две важные характеристики: сколько нейрон (или нейронная сеть, или синапс) кодирует и передает полезной информации и сколько энергии при этом тратит [6], [18], [19]. Их соотношение является своего рода критерием энергетической эффективности нейронов, нейронных сетей и синапсов.
Использование этого критерия в вычислительной нейробиологии дало существенный прирост к знаниям относительно роли некоторых явлений, процессов [6], [18–20], [26], [30], [43], [55]. В частности, малая вероятность выброса нейромедиатора в синапсе [18], [19], определенный баланс между торможением и возбуждением нейрона [55], выделение только определенного рода приходящей информации благодаря определенной комбинации рецепторов [50] — все это способствует экономии ценных энергетических ресурсов.
Более того, само по себе определение энергозатрат сигнальных процессов (например, генерация, проведение ПД, синаптическая передача) позволяет выяснить, какой из них пострадает в первую очередь при патологическом нарушении доставки питательных веществ [10], [25], [56]. Так как больше всего энергии требуется для работы синапсов, именно они первыми выйдут из строя при таких патологиях, как ишемия, болезни Альцгеймера и Хантингтона [19], [25]. Схожим образом определение энергозатрат разных типов нейронов помогает выяснить, какой из них погибнет раньше других в случае патологии. Например, при той же ишемии, в первую очередь выйдут из строя интернейроны коры [9], [16]. Эти же нейроны из-за интенсивного метаболизма — наиболее уязвимые клетки и при старении, болезни Альцгеймера и шизофрении [16].
В общем, подход к определению энергетически эффективных механизмов работы мозга является мощным направлением для развития и фундаментальной нейронауки, и ее медицинских аспектов [5], [14], [16], [20], [26], [55], [64].
Благодарности
Изучение активности нервных клеток, или нейронов, как целостных морфологических и функциональных единиц нервной системы, безусловно, остается базовым направлением в психофизиологии. Одним из показателей активности нейронов являются потенциалы действия – электрические импульсы длительностью несколько мс и амплитудой до нескольких мВ. Современные технические возможности позволяют регистрировать импульсную активность нейронов у животных в свободном поведении и, таким образом, сопоставлять эту активность с различными поведенческими показателями. В редких случаях в условиях нейрохирургических операций исследователям удается зарегистрировать импульсную активность нейронов у человека.
Рис. 2.1. А – принципиальная схема регистрации импульсной активности нейрона:
1 - нейрон (увеличен) и кончик отводящего электрода;
2 – микроманипулятор (в разрезе);
3 – микроэлектрод с отводящим проводом;
4 – индифферентный электрод;
6 – монитор и записывающее устройство
Б – пример записи импульсной активности нейрона (нейронограмма)
ЭЛЕКТРОЭНЦЕФАЛОГРАФИЯ
Среди методов электрофизиологического исследования ЦНС человека наибольшее распространение получила регистрация колебаний электрических потенциалов мозга с поверхности черепа – электроэнцефалограммы. В электроэнцефалограмме отражаются только низкочастотные биоэлектрические процессы длительностью от 10 мс до 10 мин. Предполагается, что электроэнцефалограмма (ЭЭГ) в каждый момент времени отражает суммарную электрическую активность клеток мозга. Но окончательно вопрос о происхождении ЭЭГ не решен.
ЭЭГ регистрируют с помощью наложенных на кожную поверхность головы (скальп) отводящих электродов, скоммутированных в единую цепь со специальной усилительной техникой. Увеличенные по амплитуде сигналы с выхода усилителей можно записать на магнитную ленту или в память компьютера для последующей статистической обработки. Для минимизации контактного сопротивления между электродом и скальпом на месте наложения электрода тщательно раздвигают волосы, кожу обезжиривают раствором спирта и между электродом и кожей кладут специальную электропроводную пасту. Для исключения электрохимических процессов на границе электрод–электролит (паста), приводящих к собственным электрическим потенциалам, поверхность электродов покрывают электропроводными неполяризующимися составами, например хлорированным серебром. В норме контактное сопротивление не должно превышать 3–5 кОм.
Как любые электрические потенциалы, ЭЭГ всегда измеряется между двумя точками. Существуют два способа регистрации ЭЭГ – биполярный и монополярный. При биполярном отведении регистрируется разность потенциалов между двумя активными электродами. Этот метод применяется в клинике для локализации патологического очага в мозге, но он не позволяет определить, какие колебания возникают под каждым из двух электродов и каковы их амплитудные характеристики. В психофизиологии общепринятым считается метод монополярного отведения. При монополярном методе отведения регистрируется разность потенциалов между различными точками на поверхности головы по отношению к какой-то одной индифферентной точке. В качестве индифферентной точки берут такой участок на голове или лице, на котором какие-либо электрические процессы минимальны и их можно принять за нуль: обычно это – мочка уха или сосцевидный отросток черепа. В этом случае с электрода, наложенного на скальп, регистрируются изменения потенциала с определенного участка мозга.
Рис. 2.2. Схема расположения электроэнцефалографических электродов на скальпе [Jasper, 1958]:
А– вид сверху; Б– вид сбоку справа; В– вид спереди; Г– вид сверху
Рис. 2.3. Основные ритмы электроэнцефалограммы:
1 – бета-ритм; 2 – альфа-ритм; 3 – тета-ритм; 4 – дельта-ритм
Однако описанные ритмы довольно редко встречаются в чистом виде в реальном психофизиологическом эксперименте; когда испытуемый вовлечен в определенный вид деятельности, его ЭЭГ представляет постоянно меняющуюся по амплитуде и частоте кривую. В настоящее время выпускаются самые разнообразные пакеты программ для анализа ЭЭГ на персональных компьютерах. Мы не будем здесь подробно останавливаться на методах анализа ЭЭГ, так как эта проблема требует специального обсуждения. Отметим лишь, что можно выделить два направления в анализе ЭЭГ у субъекта, выполняющего определенный вид деятельности. Одно из них – это сопоставление описанных ритмов ЭЭГ или ее частотного спектра, выявляющего выраженность альфа-, бета-, тетаили каппа-ритмов, с текущей деятельностью (решение задач, счет в уме, выполнение ассоциативных тестов, мысленное представление зрительных или слуховых ощущений, выполнение задач на объем кратковременной памяти и т.д.) [Труш, Кориневский, 1978; Ливанов, Хризман, 1978]. Сюда же можно отнести и выявление особенностей того или иного ритма ЭЭГ и их сопоставление с индивидуальной способностью выполнять определенный психологический тест, причем проведение этих исследований может быть разделено во времени [см., например, гл. 6; Психофизиол. закономерн., 1985 ]. В рамках другого направления ЭЭГ описывается на основе прямого сопоставления тех или иных ее компонентов с реально развивающимися этапами экспериментально контролируемой деятельности. Одним из примеров подобного подхода является сопоставление амплитудно-временных характеристик компонентов связанных с событием потенциалов (ССП) с выделяемыми характеристиками реализующегося в это время поведения (см. гл.16).
Важное значение в изучении активности мозга имеет сравнительный анализ биоэлектрических потенциалов, регистрируемых одновременно в разных областях мозга [Труш, Кориневский, 1978]. Так, в школе М.Н. Ливанова впервые был обнаружен феномен развития пространственной синхронизации потенциалов в диапазоне определенного ритма (чаще тета-ритма) при формировании поведенческого навыка у животных и у человека при различных психологических тестах [Ливанов, Хризман, 1978]. В настоящее время компьютерные программы просчитывают амплитуды ЭЭГ, ВП и ССП в каждом частотном диапазоне – альфа-, бета-, тетаи дельта-ритмов для каждого отведения. Цифровые данные в виде черно-белых или цветных шкал переносятся на соответствующие места отведений на черепе, что дает наглядное представление о том, в каких частях мозга и в какой степени выражена та или иная частота колебаний или тот или иной потенциал [Kaplan et al., 1994].
Артефакты (рис. 2.4). При записи ЭЭГ могут регистрироваться электрические процессы, не связанные с активностью мозга. Их называют артефактами. Все артефакты можно разделить на технические и биологические.
Следует лишь отметить, что и методы получения определенных феноменов в ЭЭГ, и методы анализа ЭЭГ определяются задачей исследования и методологией, которой придерживается тот или иной исследователь.
Рис. 2.4. Артефакты на электроэнцефалограмме:
1,2,3 - электродные артефакты; 4 – посторонние электрические помехи; 5 – артефакты, вызванные движением испытуемого; 6, 7 – мышечные потенциалы, вызванные напряжением мышц корпуса и сморщиванием лба соответственно; 8 – кожные потенциалы; 9 - моргание; 10- электрокардиограмма на фоне элетроэнцефалограммы; 11 – пульсовые волны [Егорова, 1973]
МАГНИТОЭНЦЕФАЛОГРАФИЯ
Активность мозга всегда представлена синхронной активностью большого количества нервных клеток, сопровождаемой слабыми электрическими токами, которые создают магнитные поля. Регистрация этих полей неконтактным способом позволяет получить так называемую магнитоэнцефалограмму (МЭГ). МЭГ регистрируют с помощью сверхпроводящего квантового интерференционного устройства – магнетометра. Предполагается, что если ЭЭГ больше связана с радиальными по отношению к поверхности коры головного мозга источниками тока (диполями), что имеет место на поверхности извилин, то МЭГ больше связана с тангенциально направленными источниками тока, имеющими место в корковых областях, образующих борозды (рис. 2.5). Если исходить из того, что площадь коры головного мозга в бороздах и на поверхности извилин приблизительно одинакова, то несомненно, что значимость магнитоэнцефалографии при изучении активности мозга сопоставима с электроэнцефалографией. Как следует из рис. 2.5, электрическое и магнитное поля взаимоперпендикулярны, поэтому при одновременной регистрации обоих полей можно получить взаимодополняющую информацию об исходном источнике генерации тех или иных потенциалов [Хари, Каукоранта, 1987]. МЭГ может быть представлена в виде профилей магнитных полей на поверхности черепа либо в виде кривой линии, отражающей частоту и амплитуду изменения магнитного поля в определенной точке скальпа. МЭГ дополняет информацию об активности мозга, получаемую с помощью электроэнцефалографии.
Читайте также:





