Гипоксически-ишемическая энцефалопатия у новорожденных пальчик шабалов
Полный текст:
- Аннотация
- Об авторах
- Список литературы
- Cited By
2. Зарубин А.А., Голуб И.Е., Федорова О.С., Мельников В.А., Богданова А.Д. Системная лечебная гипотермия в терапии тяжёлой асфиксии у новорождённых // Анестезиология и реаниматология. - 2016. - № 4. -С. 269-272
4. Иванов Д.О. Нарушения обмена глюкозы у новорождённых. - СПб.: Изд-во Н-Л, 2011. - 100 с
5. Иова А.С., Щугарева Л.М., Гармашов Ю.А. Пути повышения чувствительности шкалы комы Глазго у детей (педиатрическая шкала комы Глазго - Санкт-Петербург) // Матер. I Всерос. конф. по детской нейрохирургии. - М., 2003. - С. 134-135
6. Пальчик А.Б., Шабалов Н.П. Гипоксически-ишемическая энцефалопатия новорождённых. - М.: МЕДпресс-информ, 2009. - 253 с
7. Петренко Ю.В., Иванов Д.О., Курзина Е.А. Оценка органной недостаточности у новорождённых // Бюллетень Федерального Центра сердца, крови и эндокринологии им. В.А. Алмазова. - 2011. - № 2. - С. 43-50
8. Салмина А.Б., Окунева О.С., Таранушенко Т.Е., Фурсов А.А., Прокопенко С.В., Михуткина С.В., Малиновская Н.А., Тагаева Г.А. Роль нейронастроглиальных взаимодействий в дизрегуляции энергетического метаболизма при ишемическом перинатальном поражении головного мозга // Анналы клинической и экспериментальной неврологии. - 2008. - № 3. -С. 44-51
9. Abu-Shaweesh J.M. (2011). Respiratory disorders in preterm and term infants. In: Martin R.J., Fanaroff A.A., Walsh M.C. (eds.). Fanaroff and Martin's neonatal perinatal medicine: diseases of the fetus and infant, (2), 1141-1170.
10. Anderson P. (2012). Neuropeptide could be biomarker for stroke. J. Am. Coll. Cardiol., 60, 346-354.
11. Azzopardi D. (2014). TOBY study group. Predictive value of the amplitude integrated EEG in infants with hypoxic ischaemic encephalopathy: data from a randomized trial of therapeutic hypothermia. Arch. Dis. Child Fetal Neonatal Ed., 99, 80-82.
12. Azzopardi D., Strohm B., Marlow N. (2014). Effects of hypothermia for perinatalasphyxia on childhood outcomes. N. Engl. J. Med., 371, 140-149.
13. Barkovich A.J. (2005). Magnetic resonance techniques in the assessment of myelin and myelination. J. Inherit. Metab. Dis., 28, 311-343.
14. Chakkarapani E., Dingley J., Aquilina K., Osredkar D., Liu X., Thoresen M. (2013). Effects of xenon and hypothermia on cerebrovascular pressure reactivity in newborn global hypoxic-ischemic pig model. J. Cereb. Blood Flow Metab, 33, 1752-1760.
15. Cowan F.M., de Vries LS. (2005). The internal capsule in neonatal imaging. Semin. Fetal Neonatal Med., 10 (5), 461-474.
16. Da Silva S., Hennebert N., Denis R., Wayenberg J.-L. (2000). Clinical value of a single postnatal lactate measurement after intrapartum asphyxia. Acta Paediatr., 89 (3), 320-223.
17. De Vries L.S., Groenendaal F. (2010). Patterns of neonatal hypoxic-ischemic brain injury. Neuroradiology, 52 (6), 555-566.
18. Edwards A.D., Brocklehurst P., Gunn A.J., Halliday H., Juszczak E., Levene M. Strohm B., Thoresen M., Whitelaw A., Azzopardi D. (2010). Neurological outcomes at 18 months of age after moderate hypothermia for perinatal hypoxic ischaemic encephalopathy: synthesis and meta-analysis of trial data. Br. Med. J., 340, 363.
19. Elmandy H., El-Machad A.R., El-Bahrawy H., El-Gohary T., El-Barbary A., Aly H. (2010). Pediatrics. Human recombinant erythropoietin in asphyxia neonatorum: pilot trial. Pediatrics, 125 (5), 1135-1142.
20. Fan X., Kavelaars A., Heijnen C.J., Groenendaal F., van Bel F. (2010). Pharmacological neuroprotection after perinatal hypoxic-ischemic brain injury. Curr. Neurophar-macol, 8 (4), 324-334.
21. Field D., Juszczak E., Linsell L. (2013). Neonatal ECMO study of temperature (NEST): a randomized controlled trial. Pediatrics, 132, e1247-e1256.
22. Frymoyer A., Lee S., Bonifacio S.L., Meng L., Lucas S.S., Guglielmo B.J., Sun Y., Verotta D. (2013). Every 36-h gentamicin dosing in neonates with hypoxic-ischemic encephalopathy receiving hypothermia.J. Perinatol., 33, 778-782.
23. Gonzales-Portillo G.S., Reyes S., Aguirre D. (2014). Stem cell therapy for neonatal hypoxic-ischemic encephalopathy. Front. Neurol., 5, 147.
24. Hellstrom-Westas L., Rosén I., de Vries L.S., Greisen G. (2006). Amplitude-integrated EEG classification and interpretation in preterm and term infants. NeoReviews, 7 (2), 76-87.
25. Hill A., Volpe J.J. (1994). Neurologic disorders. In: Avery G.B, Fletcher M.A, MacDonald M.G. (eds.). Neonatology: Pathophysiology and management of the newborn. Philadelphia NY, 1117-1138.
26. Holmes G.L. (2005). Effects of seizures on brain development: lessons from the laboratory. Pediatr. Neurol., 33 (1), 1-11.
27. Huang B.Y., Castillo M. (2008). Hypoxic-ischemic brain injury: imaging findings from birth to adulthood. Radiographics, 28 (2), 417-439.
28. Jacobs S.E., Berg M., Hunt R. (2013). Cooling for newborns with hypoxic ischaemic encephalopathy. Cochrane Database Syst. Rev., 1, CD003311.
29. Jeanie L.Y., Cheong J.L., Coleman L., Hunt R.W., Lee K.J., Doyle L.W., Inder T.E., Jacobs S.E. (2012). Prognostic utility of magnetic resonance imaging in neonatal hypoxic-ischemic encephalopathy: substudy of a randomized trial. Arch. Pediatr. Adolesc. Med., 166, 634-640.
30. Jing L., Yue S. (2010). Clinical characteristics, diagnosis and management of respiratory distress syndrome in full-term neonates. Chin. Med. J., 123 (19), 2640-2644.
31. Kecskes Z., Healy G., Jensen A. (2005). Fluid restriction for term infants with hypoxic-ischaemic encephalopathy following perinatal asphyxia. Cochrane Database Syst. Rev., CD004337.
32. Liu J., Li J., Gu M. (2007). The correlation between myocardial function and cerebral hemodynamics in term infants with hypoxic-ischemic encephalopathy. J. Trop. Pediatr., 53 (1), 44-48.
33. Massaro A.N., Chang T., Kadom N., Tsuchida T., Scafidi J., Glass P., McCarter R., Baumgart S., Vezina G., Nelson K.B. (2012). Biomarkers of brain injury in neonatal encephalopathy treated with hypothermia. J. Pediatr., 161 (3). 434-440.
34. Murray D.M., Boylan G.B., Ryan C.A., Connolly S. (2009). Early EEG findings in hypoxic-ischemic encephalopathy predict outcomes at 2 years. Pediatrics, 124, 459-467.
35. Natarajan G., Shankaran S., Laptook A.R., Pappas A., Bann C.M., McDonald S.A., Das R., Higgins D., Hintz S.R., Vohr B.R. (2013). Apgar scores at 10 min and outcomes at 6-7 years following hypoxic-ischaemic encephalopathy. Arch. Dis. Child Fetal Neonatal Ed., 98, 473-479.
36. Perlman J.M. (2006). Intervention strategies for neonatal hypoxic-ischemic cerebral injury. Clin. Ther., 28 (9), 1353-1365.
37. Pin T.W., Eldridge B., Galea M.P. (2009). A review of developmental outcomes of term infants with post-asphyxia neonatal encephalopathy. Eur. J. Paediatr. Neurol., 13 (3), 224-234.
38. Pressler R.M., Boylan G.B., Morton M., Binniea C.D., Rennieb J.M. (2001). Early serial EEG in hypoxic ischaemic encephalopathy. Clin. Neurophys., 112, 31-37.
39. Rutherford M., Ramenghi L.A., Edwards A.D., Brocklehurst P., Halliday H., Levene M., Strohm B., Thoresen M., Whitelaw A.D. (2010). Assessment of brain tissue injury after moderate hypothermia in neonates with hypoxic-ischaemic encephalopathy: a nested substudy of a randomised controlled trial. Lancet Neurol., 9, 39-45.
40. Sabir H., Jary S., Tooley J., Liu X., Thoresen M. (2012). Increased inspired oxygen in the first hours of life is associated with adverse outcome in newborns treated for perinatal asphyxia with therapeutic hypothermia. J. Pediatr., 161 (3), 409-416.
41. Sarnat H.B., Sarnat M.S. (1976). Neonatal encephalopathy following fetal distress: A clinical and electro-encphalographic study. Arch. Neur., 33, 696-705.
42. Shah P. (2010). Hypothermia: a systematic review and meta-analysis of clinical trials. Seminars in Fetal and Neonatal Medicine, 15 (5), 238-246.
43. Shankaran S., Barnes P.D., Hintz S.R. (2012). Brain injury following trial of hypothermia for neonatal hypoxic-ischaemic encephalopathy. Arch. Dis. Child Fetal Neonatal Ed., 97, 398-404.
44. Shankaran S., Pappas A., McDonald S.A. (2011). Predictive value of an early amplitude integrated electroencephalogram and neurologic examination. Pediatrics, 128, 112-120.
45. Shankaran S., Pappas A., Scott A., McDonald S.A., Vohr B.R., Hintz S.R., Epi M.S., Yolton K., Gustafson K.E., Theresa M. (2012). Childhood outcomes after hypothermia for neonatal encephalopathy. N. Engl. J. Med., 36, 2085-2092.
46. Shellhaas R.A., Ng C.M., Dillon C.H., Barks J.D., Bhatt-Mehta V. (2013). Population pharmacokinetics of phenobarbital in infants with neonatal encephalopathy treated with therapeutic hypothermia. Pediatr. Crit. Care Med, 14, 194-202.
47. Thoresen M., Hellström-Westas L., Liu X., de Vries L.S. (2010). Effect of hypothermia onamplitude-integrated electroencephalogram in infants with asphyxia. Pediatrics, 126, 131-139.
48. Thoresen M., Tooley J., Liu X., Jary S., Fleming P., Luyt K., Jain A., Cairns P., Harding D., Sabir H. (2013). Time is brain: starting therapeutic hypothermia within three hours after birth improves motor outcome in asphyxiated newborns. Neonatology, 104, 228-233.
49. Traudt C.M., McPherson R.J., Bauer L.A. (2013). Concurrent erythropoietin and hypothermia treatment improve outcomes in a term nonhuman primate model of perinatal asphyxia. Dev. Neurosci., 35, 491-503.
50. Vohr B.R., Stephens B.E., McDonald S.A. (2013). Cerebral palsy and growth failure at 6 to 7 years. Pediatrics, 132, 905-914.

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Гипоксически-ишемическая энцефалопатия (ГИЭ) встречается примерно у 1-6 из 1000 живорожденных и является самой важной проблемой неонатальной неврологии (Levene et al., 1985, Volpe, 2001, Ferriero, 2004). Гипоксически-ишемическая энцефалопатия (ГИЭ) относится к серьезным состояниям, при котором 15-20% пострадавших детей умирает в течение неонатального периода, а у 25% развиваются стойкие неврологические последствия (Volpe, 2008). Более двадцати лет назад было отмечено завышенное значение перинатальной гипоксии в этиологии задержки умственного развития и церебрального паралича (Freeman и Nelson, 1988, Вах и Nelson, 1993).
Badawi et al. (1998) обнаружили, что многие новорожденные подвергались антенатальным факторам риска, таким как лечение материнского бесплодия или заболеваний щитовидной железы, тогда как другие имели и анте-, и интранатальные факторы риска. Хотя не исключается возможность наличия пренатальных факторов риска, вероятно повышающих чувствительность ребенка к проблемам родового периода, в проспективном исследовании результатов MPT Cowan et al. (2003) было отмечено, что у большинства новорожденных (n=351) с неонатальной энцефалопатией повреждение мозга возникало в момент рождения или незадолго до этого.
Патофизиология. Недостаточное поступление кислорода, вызывающее развитие гипоксической-ишемической энцефалопатии (ГИЭ), может возникнуть по двум механизмам: гипоксемия, т.е. ограниченный доступ кислорода в кровь; и ишемия, т.е. сниженная перфузия головного мозга. В большинстве случаев оба механизма связаны с асфиксией в виде гипоксии, сопровождающейся гиперкарбией (Altman et al., 1993). Обычно присутствующий при гипоксии ацидоз в значительной степени связан с повышенным образованием лактата. Преобразование глюкозы в молочную кислоту менее эффективно, чем окисление в цикле Кребса и митохондриальной системе транспорта электронов.
В результате окисления каждой молекулы глюкозы, переработанной в анаэробных условиях, образуется только две молекулы аденозина дифосфата (АДФ) по сравнению с 38 молекулами при аэробных условиях. Несмотря на значительное повышение скорости гликолиза и усиление мозгового кровотока из-за ацидоза и гиперкапнии (Laptook et al., 1988), потребности ткани мозга в кислороде не могут быть удовлетворены. Повышенная скорость гликолиза приводит к падению уровня глюкозы в мозге. Предупреждение этого состояния предварительным введением глюкозы повышает выработку АТФ и улучшает выживаемость (Vannucci и Yager, 1992). Однако избыточный уровень глюкозы в то же время приводит к повышенному образованию лактата, вредного для мозговой ткани взрослого, но, по-видимому, полезного для ЦНС новорожденного (Hattori и Wasterlain, 1990).
В итоге, в результате нехватки кислорода в клетках мозга снижается количество фосфокреатина и АТФ, конечных акцепторов электронов. Эти изменения были продемонстрированы у новорожденных с использованием фосфорной МРС (магнитно-резонансная спектроскопия) (Younkin et al., 1988, Laptook et al., 1989). Падение уровня высокоэнергетических соединений фосфата наблюдалось даже при стабилизации кардиопульмональной функции (Hope et al., 1984). В экспериментах на животных снижение уровня АТФ более чем на 30% происходило за 6 минут (Raichle, 1983). Также было отмечено накопление лактата, сохранявшееся в течение длительного периода времени (Groenendaal et al, 1994, Robertson et al., 1999).
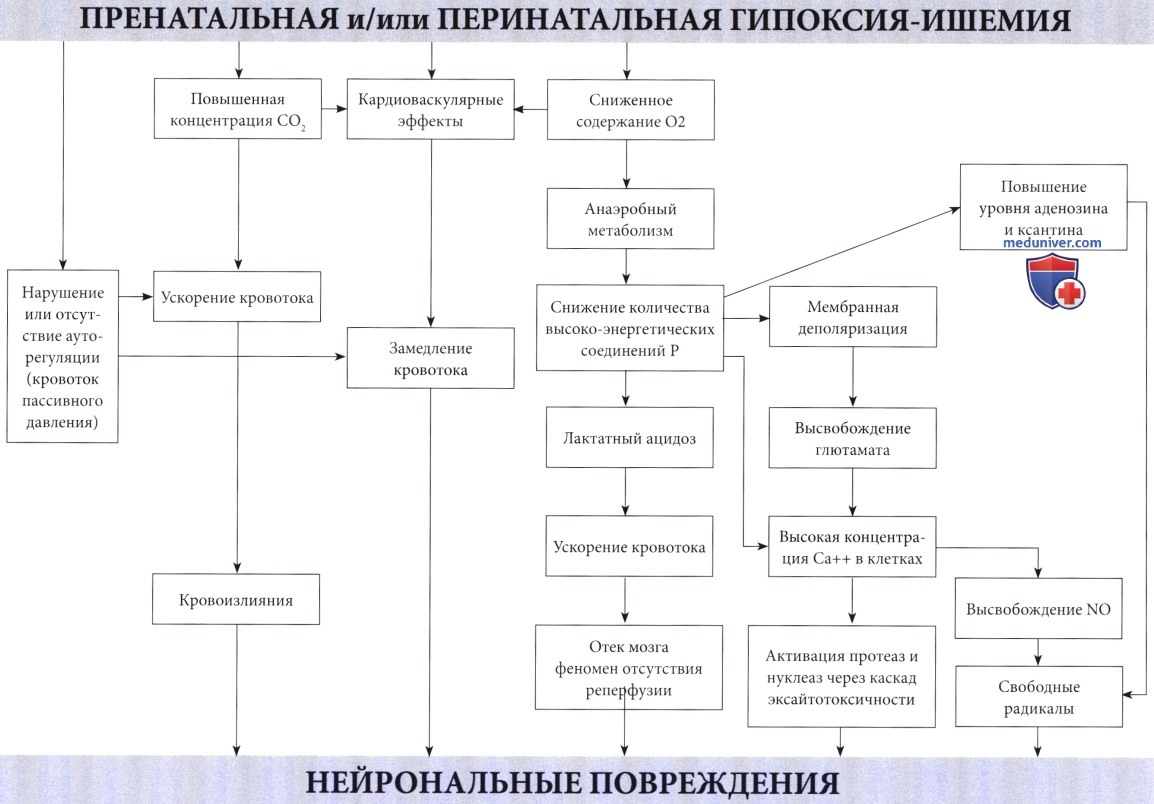
Механизм повреждения мозга при гипоксически-ишемической энцефалопатии.
Нейрональные повреждения являются следствием различных комбинаций кровоизлияний и некрозов.
Последние связаны с каскадом событий, инициированных высвобождением глютамата, приводящим к массивному входу кальция в клетки.
Образование оксида азота (NO), вероятно, также является важным фактором.
В действительности, нарушению мозговой функции предшествует сбой в энергетическом метаболизме (см. Volpe, 2001). При угрозе перебоев организм отвечает угнетением нейрональной активности по неопределенному механизму, но при длительной гипоксии этого недостаточно.
Однако мозг новорожденного чрезвычайно устойчив к гипоксии. При экспериментах на плодах обезьян потребовалось снижение сатурации кислорода на 90% в течение не менее 25 минут, чтобы вызвать повреждение ткани мозга. В результате, любой, достаточно тяжелый для повреждения мозга эпизод асфиксии вызывает нарушения и других органов, особенно сердца, и при таких условиях ишемия постоянна.
Ишемия оказывает влияние, подобное асфиксии (Painter, 1989). Процесс гликолиза ускоряется, но поглощению глюкозы препятствует нарушение кровотока, соответственно запасы высокоэнергетических фосфатов истощаются, и накапливается лактат.
Влияние гиперлактатемии многопланово. Первоначально оно благотворно, поскольку повышает приток крови к мозгу, но затем становится вредным, так как хотя бы отчасти влияет на отек мозга, который в свою очередь может сдавить капиллярное русло и вызвать ишемию (Myers, 1972). В то же время он нарушает ауторегуляцию церебрального кровообращения, приводя к мозговому кровотоку пассивного давления (Lou, 1988), что делает мозг более чувствительным к изменениям системного давления крови. Сочетание отека мозга и системной недостаточности кровообращения, вероятно, играет существенную роль в происхождении гипоксического повреждения ЦНС. Гипоксия обычно повышает долю сердечного выброса, предназначенную для головного мозга.
По мере усиления степени гипоксии наблюдается уменьшение сердечного выброса с последующей неспособностью поддерживать артериальное давление на необходимом уровне. Но показатели частоты сердечных сокращений и артериального давления остаются неизменными до тех пор, пока артериальная сатурация не снизится более, чем на 65%, а затем также линейно снижаются. Это снижение может поддерживаться на протяжении часов без развития энцефалопатии, если содержание кислорода в артериальной крови не упадет более, чем на 85% (Fenichel, 1997).
Механизм отека мозга и гипоксического повреждения у плодов до конца неясен. Levene et al. (1989) выявили хорошую корреляцию между высокой скоростью мозгового кровотока—предположительно отражающей церебральную гиперемию, которая, в свою очередь, может отвечать за повышение внутричерепного давления — и неблагоприятным течением. Lupton et al. (1988) показали, что отек в большей степени является следствием, чем причиной, нейрональных некрозов, объясняя, таким образом, ограниченную эффективность противоотечного лечения новорожденных с ГИЭ (Levene et al., 1987). Не было замечено различий в степени внутричерепной гипертензии у детей с ГИЭ в группе выживших и умерших (Goitein et al, 1983).
Последние данные подтверждают основную роль апоптоза в развитии гипоксически-ишемического повреждения мозга новорожденных, возможно, даже большую, чем некроз после повреждения. Во время неонатального поражения мозга токсичность возбуждающих медиаторов, оксидативный стресс и воспаление способствуют ускоренной гибели клеток, главным образом, посредством апоптоза или некроза, что зависит от области поражения и тяжести повреждения. В настоящее время известно, что ГИЭ состоит из двух последовательных стадий, с окончательным повреждением с отсрочкой на несколько часов во время второй из них, определяемой как вторичная недостаточность энергии. Тем не менее, профилактика возможна, как только появляется терапевтическое окно.
Механизмы повреждения и некроза клеток при гипоксии и ишемии не просто итог энергетической недостаточности. Это вторичные пусковые факторы каскада разрушительных событий при достижении критического уровня дефицита энергии. Такие события происходят в течение нескольких часов. Избыточная мембранная деполяризация и высвобождение возбуждающих аминокислотных нейротрансмиттеров, в первую очередь глютамата (Lipton и Rosenberg, 1994), приводит к массивному входу кальция через NMDA и АМРА мембранные рецепторы (Morley et al., 1994) и к накоплению кальция в цитозоле. Кальций, в свою очередь, активирует различные липазы, протеазы и нуклеазы с последующим разрушением основных клеточных белков. Свободные радикалы прямо или косвенно вызваны повышенным уровнем кальция в цитозоле (McCord, 1985) и оксида азота (Dawson et al., 1992), играющего главную роль в их образовании.
Этот каскад возбуждающих медиаторов в конечном счете приводит к повреждению мембраны, разрушению цитоскелета и, наконец, к дезинтеграции клетки.
Теоретически существует возможность предотвращения многих процессов, поэтому проводились исследования с различными средствами, в том числе блокаторами кальциевых каналов (Miller, 1993, Palmer и Vanucci, 1993); антагонистами возбуждающих аминокислот (Hattori et al., 1989), особенно магнезией (Marret et al., 1995, Nelson и Grether, 1995); ингибиторами синтеза оксида азота (Dawson et al., 1992); акцепторами свободных радикалов (Palmer и Vannucci, 1993) и веществами, подавляющими образование свободных радикалов типа аллопуринола (Palmer et al., 1990, van Bel et al., 1998, Benders et al., 2006).
Редактор: Искандер Милевски. Дата публикации: 25.11.2018
Настоящее руководство отражает многолетние многосторонние исследования авторов в области неонатальной неврологии, а также представляет обобщение научных достижений различных неонатологических и неврологических школ в этой области. Рассмотрены вопросы эпидемиологии, причины и механизмы развития гипоксических пораженийголовного мозга, представлены данные о морфологических изменениях в нервной системе новорожденного при гипоксии. Значительное место уделено клинической картинеи современным методам диагностики гипоксически-ишемической энцефалопатии, приведены результаты оригинальных исследований авторов. Лечение рассматриваемых состояний представлено с учетом современных требований к назначению и контролю медикаментозной терапии. Для неонатологов, педиатров, неврологов, врачей общей практики и студентов медицинских вузов. ISBN:978-5-98322-987-7
Издательство: "МЕДпресс-информ" (2013)
| Книга | Описание | Год | Цена | Тип книги |
|---|---|---|---|---|
| Токсические энцефалопатии новорожденных | Монография посвящена актуальной проблеме современных неонатологии и детской неврологии - токсическим энцефалопатиям новорожденных. В ней раскрыты общие закономерности развития токсического поражения… — МЕДпресс-информ, (формат: 84x108/32, 176 стр.) Подробнее. | 2013 | 430 | бумажная книга |
| Гипоксически-ишемическая энцефалопатия новорожденных | Настоящее руководство отражает многолетние многосторонние исследования авторов в области неонатальной неврологии, а также представляет обобщение научных достижений различных неонатологических и… — МЕДпресс-информ, (формат: 84x108/32, 288 стр.) Подробнее. | 2013 | 474 | бумажная книга |
| Гипоксически - ишемическая энцефалопатия новорожденных | Настоящее руководство отражает многолетние клинические и лабораторные исследования авторов в области неонатальной неврологии, а также представляет обобщение современных научных достижений различных… — Питер, (формат: 84x104/32, 224 стр.) Современная медицина Подробнее. | 2000 | 294 | бумажная книга |
Ройтберг, Григорий Ефимович — Григорий Ефимович Ройтберг (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Доктор медицинских наук (1990), профессор (1990), заведующий кафедрой семейной медицины… … Википедия
Простатический специфический антиген — ПСА в ткани нормальной предстательной железы (иммуногистохимия) Простатический специфический антиген (ПСА) опухолевый маркёр, определение которого проводится в сыворотке крови, применяющийся для диагностики … Википедия
Григорий Ефимович Ройтберг — (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Доктор медицинских наук (1990), профессор (1990), заведующий кафедрой семейной медицины Российского государственного… … Википедия
Григорий Ройтберг — Григорий Ефимович Ройтберг (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Доктор медицинских наук (1990), профессор (1990), заведующий кафедрой семейной медицины… … Википедия
Ройтберг — Ройтберг, Григорий Ефимович Григорий Ефимович Ройтберг (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Док … Википедия
Ройтберг, Григорий — Григорий Ефимович Ройтберг (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Доктор медицинских наук (1990), профессор (1990), заведующий кафедрой семейной медицины… … Википедия
Ройтберг Григорий Ефимович — Григорий Ефимович Ройтберг (род. 20 августа 1951, Сороки Молдавской ССР) российский учёный медик, кардиолог, организатор здравоохранения, предприниматель. Доктор медицинских наук (1990), профессор (1990), заведующий кафедрой семейной медицины… … Википедия
Сегменты лёгкого — Доли лёгких и бронхолёгочные сегменты (последние в … Википедия
Синдром беспокойных ног — МКБ 10 G25.825.8 МКБ 9 333.94333.94 OMIM … Википедия
Гемангиобластома — мозжечка МКБ 1 … Википедия
- Медицина
Описание книги
Для бесплатного просмотра предоставляются: аннотация, публикация, отзывы, а также файлы на скачивания.
- Медицина
Подробная статистика
Оценки по возрасту и полу

Ни одной рецензии нет








- ТОП-15 лучших книг 2020 года
- Что в имени тебе моем.
- Заразительное одиночество
- Все дороги ведут домой
- 75 ракурсов Победы. ТОП-ВОВ-75 от ведущих издательств
- Юмор всему голова
- ТОП-20 Новинки ведущих издательств
- Самоизоляция. Как провести время, чтобы оно не провело тебя. Советы от Book24 и Litres
- Вирусы. Пограничники жизни
- Вирус-вдохновитель
- Читаем первыми. ТОП-15 новейших книг 2020 года
- От классического до военного. Заведи свой роман
- детская литература
- Сказки и мифы
- Феминизм
- О любви
- юмор
- ветеринария
- Исторические книги
- 10 книг, которые помогут разобраться в медицине
- Нумизматика
- рисование
- Биографии
- Деньги
- F.A.Q.
- О проекте
- Пользовательское соглашение
- Помощь и контакты
- Все 0
- Друзья 0
- Похожие 0
Если у Вас возникли вопросы по работе сайта - напишите нам!



Для восстановления обратитесь к администратору
Уважаемые пользователи!
На нашем сайте происходят большие изменения: мы усиленно работаем над улучшением дизайна и логики сайта, а также пополняем базу новыми книгами.
Администрация сайта приносит свои глубочайшие извинения всем пользователям.
Часто после первого осмотра невропатолога в поликлинике или в роддоме малышу ставится диагноз перинатальная энцефалопатия. По различным источникам, ее имеет от 30 до 70% новорожденных. Какие же жалобы мамы заставляют врача поставить такой диагноз? Продолжительный плач и вообще плаксивость, частое сосание, срыгивания, вздрагивания или вскидывания рук и ног, плохой ночной (частые просыпания, беспокойный поверхностный сон) и дневной сон (мало спит днем), трудности с засыпанием (долгое укачивание на руках). При осмотре ребенка врач может заметить нарушения мышечного тонуса – гипертонус или гипотонус, дистонию. При нейросонографических исследованиях иногда видны затемненные или измененные участки мозга, иногда нет. Врач назначает средства, улучшающие мозговое кровообращение (пирацетам, ноотропил, кавинтон) и успокоительные (глицин, микстура с цитралью, валериана, иногда люминал или фенобарбитал), а так же рекомендует провести курсы массажа, купания в сборах успокаивающих трав. Это вы наверняка все знаете.
А теперь стоит сказать о другом подходе к проблеме.
Во-первых, это нарушение принципов неврологического осмотра:
а) нарушения стандартизации осмотра (наиболее частые из них: диагностика повышенной возбудимости у дрожащего и скованного ребенка в холодном помещении, а также при возбужденном состоянии или чрезмерных манипуляциях исследователя; диагностика угнетения центральной нервной системы у вялого ребенка при перегревании или в дремотном состоянии).
Например, в роддоме педиатр поставила ПЭП, так как ребенок часто громко плакал, но когда невропатолог пришел осмотреть ребенка, малыш крепко спал, и врач сказал, что тонус в норме, и он не видит никаких патологий. Через месяц в поликлинике осмотр производился, когда ребенок спал, проснулся и испугался, что его чужая тетка за руки-ноги дергает. Естественно, что он заплакал и напрягся. ПЭП подтвердили.
Так, у одного ребенка могут диагностировать то гипер, то гипотонус.
Но до 3-х лет — это абсолютно нормальное явление, потому что она только формируется!
Плохой ночной сон – когда ребенок часто просыпается. Но для грудного ребенка характерен преимущественно поверхностный неглубокий сон и сосание во время такого сна. С 3-4 месяцев у детей ночное сосание может становиться более активным, т.к. днем они начинают легко отвлекаться от груди и сосут относительно не долго. За счет активного ночного сосания они добирают необходимое количество молока.
Во–вторых, это отнесение к патологическим ряда адаптационных, проходящих явлений со стороны нервной системы новорожденного (например, вздрагивания или вскидывании рук и ног, дрожание подбородка при сильном плаче или испуге, постнатальная депрессия, физиологическая мышечная гипертония и т. д.).
В-третьих, плохая осведомленность в классификации Гипоксической Ишемической Энцефалопатии (в основном, в связи с иностранным происхождением исследований на эту тему) и недостаточная квалификация врача.
Например, месячному ребенку был поставлен диагноз Минимальная Мозговая Дисфункция, который должен ставиться после 2, а то и 5 лет, по разным источникам. Другому ребенку назначили пить настойку женьшеня, что недопустимо в его возрасте. Часто медикаментозные методы лечения приводят к еще большему ухудшению в поведении детей. Врачи знают о вреде различных лекарств для детей, но или просто не информируют родителей, или сознательно или неосознанно не обращают их внимание на побочные эффекты.
В исследовании петербургских ученых подробно описаны наиболее часто встречающиеся ошибки при проведении эхоэнцефалография, нейросонографии, допплерографии, аксиальной компьютерной и магнитно-резонансной томографии.
Причины ошибок различны и связаны с тем, что при интерпретации полученных данных используются параметры и нормы, разработанные для детей старшего возраста и взрослых, используется неадекватная оценка полученных данных и их абсолютизация, используются методы, имеющие при диагностике данного заболевания недостаточную информативность, используются также аппараты, имеющие неподходящие технические характеристики.
В-пятых, это непонимание врачами и родителями естественных потребностей новорожденного ребенка. Чаще всего ребенок сигнализирует об ошибках в уходе своим плачем. Ребенку нужен контакт с мамой постоянно сразу после рождения.
Общеизвестно, что сосание оказывает на ребенка своего рода седативное действие, не сравнимое по своей полезности ни с какими лекарствами. Содержание аминокислоты таурина в женском молоке, в отличие от коровьего, очень высоко. Таурин необходим для усвоения жиров, а также служит нейропередатчиком и нейромодулятором при развитии центральной нервной системы. Поскольку дети, в отличие от взрослых, не способны синтезировать таурин, считается, что его нужно рассматривать как аминокислоту, необходимую для маленького ребенка. Среди полиненасыщенных жирных кислот особенно важны арахидоновая и линоленовая кислоты, которые являются необходимыми компонентами для формирования головного мозга и сетчатки глаза ребенка. Их содержание в женском молоке почти в четыре раза выше, чем в коровьем (0,4 г и 0,1 г/100 мл соответственно). В женском молоке представлены нуклеотиды и многочисленные факторы роста. К последним относится, в частности, фактор роста нервной ткани (NGF). Именно поэтому ребенку очень важно находится на естественном вскармливании, если у вас были проблемы при родах или во время беременности, которые могли повлечь за собой гипоксию плода и травму его нервной системы.
Четкой общепринятой тактики ведения детей с синдромом повышенной нервно-рефлекторной возбудимости до настоящего времени не существует, многие специалисты относятся к данному состоянию как к пограничному, и советуют только наблюдать за такими детьми, воздерживаясь от лечения. В отечественной практике некоторые врачи продолжают применять детям с синдромом повышенной нервно-рефлекторной возбудимости достаточно серьезные препараты (фенобарбитал, диазепам, сонапакс и т.п.), назначение которых в большинстве случаев мало оправдано…
У гомеопатов есть хороший опыт лечения неврологических расстройств, и официальная медицина это подтверждает. Но общеизвестна высокая пластичность детского мозга, его способность компенсировать структурные дефекты. Так что можно никогда не узнать, помогла ли ребенку терапия или он сам справился с проблемами. Очень хорошо помогает массаж, и мамин, и профессиональный (но только если ребенок хорошо на него реагирует, не плачет, не перевозбуждается, не теряет в весе и не приостанавливает прибавку) Показана витаминотерапия, и, учитывая хорошую усвояемость витаминов из материнского молока, обратите на это внимание.
Что же заставляет направить ребенка к неврологу? Во-первых, сведения о том, как проходили беременность и роды. Насторожиться заставляют:
сильные проявления токсикоза (особенно позднего);
подозрения на внутриутробную инфекцию;
анемия матери (гемоглобин ниже 100 единиц);
слабость родовой деятельности, длительный безводный период, применение в родах медикаментозной стимуляции или акушерских щипцов;
обвитие пуповиной; слишком большой вес ребенка или, наоборот, признаки незрелости и недоношенности;
роды в ягодичном предлежании и т.п.
Словом, все, что может привести к гипоксии плода в родах, то есть к нехватке кислорода, почти неминуемо приводящей к временному нарушению деятельности центральной нервной системы (ЦНС). Нанести урон ее работе могут также вирусные инфекции у женщины в период закладки нервной системы плода, нарушенная экология жилища или места работы.
Прямой зависимости между уровнем и длительностью имевшего место кислородного голодания нет: иногда мозг ребенка переносит серьезный дефицит кислорода без большого для себя вреда, но случается, что небольшой дефицит приносит довольно ощутимый вред.
Кроме выяснения обстоятельств беременности и родов, существуют и определенные клинические признаки, настораживающие педиатра. Ребенок слишком вял или, что чаще, возбужден, много кричит, при крике у него дрожит подбородок, он часто срыгивает, реагирует на ухудшение погоды. Или ко всему этому у него вздувается животик, никак не налаживается стул — он с зеленью, частый или, напротив, имеется склонность к запорам.
Сопоставив все эти данные, убедившись, что малыша правильно кормят, врач-педиатр направляет такого ребенка к неврологу — специалисту, нацеленному на исследование состояния центральной и периферической нервной системы. Задача — выяснить, в какой степени имевшаяся в родах гипоксия оставила свой неприятный след.
Только без паники!
Тут часто начинается то, ради чего, собственно, и затевалась эта статья — родителей охватывает страх. Как, у нашего ребенка не все в порядке с головой?! Этот страх восходит к общей нашей ментальности, говорящей, что иметь отклонения в сфере нервной системы прежде всего стыдно.
Убеждаешь, говоришь о том, что эти отклонения скорее всего временны, что чем раньше мы поможем ребенку, тем быстрее он с ними справится… Большинство родителей, вняв уверениям педиатра, идут к неврологу и возвращаются с записью, которая гласит обычно следующее:
ПЭП (перинатальная энцефалопатия), восстановительный период, СПНРВ (синдром повышенной нервно-рефлекторной возбудимости).
То, что написано в скобочках, расшифровано автором статьи — к сожалению, неврологи не часто снисходят до пояснения непонятных аббревиатур. Они пишут для себя и для врача-педиатра, и обе стороны прекрасно понимают друг друга. Но не родители.
Насколько это страшно? Чаще всего с этим вопросом они бегут к педиатру, служащему в этот момент переводчиком с непонятного медицинского на бытовой язык.
И ведь действительно растут и вырастают. Но родители при этом не пытаются связать свое бездействие с выраженными проявлениями экссудативного диатеза у ребенка, явлениями дискинезии желудочно-кишечного тракта, со склонностью к запорам и даже с такими явными вещами, как отставание в развитии речи, расторможенность, непослушание.
А ведь многих из этих неприятностей можно было бы избежать, отнесись родители к проблеме так, как она того заслуживает — достаточно серьезно, но без избыточного драматизма. Названные диагнозы в карте ребенка — это не сигнал паники, а сигнал к действию! Есть сомнения в рекомендациях участкового детского невролога? Проконсультируйте ребенка у другого специалиста.
Что скрывается за непонятными словами?
Итак, ПЭП расшифровывается как перинатальная энцефалопатия. То есть у ребенка в родах имелись факторы, способные повредить головному мозгу. Что-то случилось, и надо разобраться, какие поломки в организме эта авария произвела.
Слова восстановительный период совершенно справедливо указывают на то, что нервная система и сама, без постороннего вмешательства, восстанавливается — дело только в темпах и качестве этого восстановления. А они не всегда удовлетворительны.
Что же касается труднопроизносимой аббревиатуры СПНРВ (синдром повышенной нервно-рефлекторной возбудимости), то она как раз и обозначает тот печальный факт, что ребенок плаксив, много срыгивает, легко возбуждается, трудно успокаивается. И ему надо помочь от этого избавиться.
На что обращают внимание неврологи при осмотре? Во-первых, на рефлексы и мышечный тонус. Равномерны ли рефлексы справа и слева? Нет ли спазмов мышц? И наоборот — не слишком ли слабо они сокращаются?
Затем проверяют, нет ли у ребенка признаков повышенного внутричерепного давления. Для этого через открытый родничок делают УЗИ (нейросонограмму) — смотрят, не расширены ли желудочки мозга. И в заключение исследуют поведение ребенка, соответствие его так называемого психомоторного и физического развития возрасту.
Диагноз поставлен. Что дальше?
Если дело ограничивается нарушением мышечного тонуса и возбуждением нервной системы, обычно невролог назначает массаж, легкие успокаивающие средства и препараты, улучшающие мозговое кровообращение.
Если невролог обнаружил у малыша явления повышения внутричерепного давления, которое обычно зависит от избыточной продукции спинномозговой жидкости, он назначает ему курс так называемой дегидратационной терапии (дегидратация — обезвоживание). С этой целью даются различные мочегонные средства. Для компенсации потери калия при усиленном мочеотделении назначают препараты, содержащие калий.
Не надо надеяться, что с ростом черепа эти явления пройдут сами собой — этого может и не случиться. Кстати, контроль за показателями внутричерепного давления нужно проводить и позже, в течение нескольких лет, что избавит вашего ребенка от головных болей и приступов так называемой вегето-сосудистой дистонии в дошкольном и школьном возрасте.
Но самое важное значение при формах ПЭП любой сложности имеют щадящие и безмедикаментозные способы восстановительного лечения: рефлексомассаж, специальные приемы лечебного массажа, элементы лечебной гимнастики, водолечение с проведением массажа и лечебной гимнастики в воде различной температуры и состава и др.
Рефлексомассаж (воздействие на активные точки) поначалу делается руками опытного массажиста, который потом передает родителям эстафету грамотного обращения с малышом. Не забывайте: младенцы быстро устают, все процедуры нужно проводить коротко, но часто, на высоте положительных эмоций.
После выныривания ребенок получает полноценный, грамотный вдох, что особенно важно для малышей, родившихся с помощью кесарева сечения, имевших гипоксию и т.д. Вода помогает и при проблемах с кишечными коликами — улучшается стул, уходят спастические болезненные явления.
А что с животом?
Часто у детей с перинатальной энцефалопатией имеются серьезные расстройства со стороны желудочно-кишечного тракта: запоры и поносы, вздутия живота, кишечные колики. Обычно все это начинается с дисбактериоза и, к сожалению, часто заканчивается различными кожными проявлениями — экссудативным диатезом или даже экземой.
Какая здесь связь? Самая простая. При гипоксии мозга в родах почти всегда страдает центр созревания иммунитета, расположенный в продолговатом мозгу. Вследствие этого кишечник заселяется той флорой, которая живет в родильных домах, особенно при позднем прикладывании к груди и раннем переходе на искусственное вскармливание. В результате у малыша очень рано возникает дисбактериоз: ведь вместо необходимых бифидобактерий его кишечник заполоняют стафилококки, кишечные палочки и т.д.
Как быть? Для достижения лучшего эффекта лечить не только кишечник, но и нервную систему. Только совместные усилия педиатра и невролога при самой активной помощи родителей могут дать нужный эффект.
А напоследок хочется напомнить, что малышу с неустойчивой нервной системой материнское тепло, нежные прикосновения, ласковый разговор, покой в доме — словом, все, что вызывает у него чувство защищенности, — нужны в еще большей степени, чем здоровому ребенку.
Как же при лечении энцефалопатии понять, что усилия врачей и родителей увенчались успехом? Ребенок стал спокойнее, перестал подолгу плакать, у него наладился сон. Он вовремя стал держать головку, сел, затем встал, сделал первый шаг. У него наладилось пищеварение, он хорошо прибавляет в весе, у него здоровая кожа. Это видно не только врачам, но и вам самим. Значит, вы помогли своему малышу преодолеть повреждения нервной системы.
И в заключение один пример того, что может сделать материнская любовь.
В середине 60-х годов в одном из роддомов на далеком Сахалине у молодой акушерки родилась дочь. Как это, к сожалению, часто бывает у медиков, роды были крайне тяжелыми, ребенок родился в глубокой асфиксии, долго не дышал, потом несколько недель находился практически в параличе.
Девочку кормили из пипетки, выхаживали, как могли. Честно говоря, врачи думали, что ребенок этот — не жилец. И только мать думала иначе. Она не отходила от малыша, прекрасно овладела массажем и упорно массировала с трудом оживающее тельце.
Через 18 лет автор этой статьи встретил в Ленинграде дочь и мать. Они приехали поступать в Ленинградский университет. Оказалось, что девочка с золотой медалью окончила школу на Сахалине. От нее трудно было отвести глаза — такая она была стройная и красивая. Потом она университет закончила, защитила кандидатскую диссертацию по биологии, стала ученым, вышла замуж, родила двоих прекрасных детей. Ничего этого могло и не быть, будь любовь матери менее самоотверженной и разумной.
Правила для всех
Изучите и покажите опытному педиатру выписку из роддома. Если в ней проставлены низкие баллы по шкале Апгар (6 и ниже), другие пометки (например, закричал после рождения не сразу, имелась кефалогематома, гипоксия, асфиксия, судорожный синдром и т.п.), не откладывайте консультацию у детского невролога.
Если вы планируете следующего ребенка, выясните все причины перинатальной энцефалопатии у первенца. И по возможности попытайтесь исправить ситуацию, если она связана с невнимательным отношением к своему здоровью во время беременности и в родах. Посещайте курсы по подготовке семейных пар к родам. Внимательно отнеситесь к выбору врачей и медицинского учреждения, где вы планируете рожать малыша.
Читайте также:



