Гипоксически ишемическое поражение цнс код
Рубрика МКБ-10: P91.6
Содержание
- 1 Определение и общие сведения
- 2 Этиология и патогенез
- 3 Клинические проявления
- 4 Гипоксически-ишемическая энцефалопатия новорожденного: Диагностика
- 5 Дифференциальный диагноз
- 6 Гипоксически-ишемическая энцефалопатия новорожденного: Лечение
- 7 Профилактика
- 8 Прочее
- 9 Источники (ссылки)
- 10 Дополнительная литература (рекомендуемая)
- 11 Действующие вещества
Гипоксически-ишемическая энцефалопатия
Синонимы: перинатальное гипоксическое поражение мозга, постасфиктическое поражение головного мозга.
Гипоксически-ишемическая энцефалопатия - синдром, характеризуемый наличием признаков острого повреждения головного мозга в результате недостаточного кровоснабжения головного мозга ребенка во время беременности матери, родов или в течение первого месяца его жизни.
Гипоксически-ишемическая энцефалопатия является наиболее распространенным поражением среди всей перинатальной патологии нервной системы.
Основными причинами перинатальной гипоксии-ишемии являются:
• внутриутробная гипоксия (нарушения маточно-плацентарного и/или фетоплацентарного кровотока);
• интра- и постнатальная асфиксия, РДС (Респираторный дистресс - синдром), повторяющиеся приступы апноэ, врожденная пневмония или аспирационный синдром;
• ВПС (врожденные пороки сердца), гемодинамически значимый ОАП (открытый артериальный проток), персистирование фетальных коммуникаций;
• постнатальные нарушения системной гемодинамики, приводящие к резкому падению системного АД и снижению церебральной перфузии.
Развивающийся мозг является гетерогенным образованием по степени зрелости (морфологической и функциональной) его тканевых и сосудистых компонентов. Особенности архитектоники и морфологии церебральных сосудов новорожденных лежат в основе специфических механизмов, обеспечивающих регуляцию интенсивности мозгового кровотока на региональном уровне в ответ на асфиксию.
В настоящее время показано, что у недоношенных новорожденных (при сроке гестации менее 35 нед) гипоксемия приводит к повышению кровотока в стволе головного мозга и перивентрикулярных областях белого вещества. У доношенных новорожденных при поддержании системного АД на нормальном уровне гипоксемия вызывает усиление кровотока во всех областях мозга, но более всего в области ствола, глубоких отделов больших полушарий и базальных ганглиев как структур, обеспечивающих жизненно важные функции и рефлекторно-двигательные реакции. Дефицит кровоснабжения мозга приводит к ишемическому поражению зон пограничного или коллатерального кровоснабжения бассейнов мозговых артерий, имеющих различное расположение в зависимости от гестационного возраста.
В этих условиях поступление обогащенной кислородом крови в участки, перенесшие ранее ишемическое воздействие, приводит к активации процессов свободнорадикального окисления, сопровождающегося накоплением токсичных продуктов и возбуждающих аминокислот (глутамат, N-метил-D-аспарагиновая кислота и др.). В итоге каскада патологических процессов, инициированных тканевой гипоксией-ишемией в очагах повреждения под действием цитокинов и ИЛ, развивается воспалительная реакция нейроглии, что обусловливает дальнейшее повреждение паренхимы мозга, длительность которого может варьировать от нескольких часов до нескольких недель.
Церебральная гипоксия - ишемия I степени (легкая)
Возбуждение ЦНС чаще возникает у доношенных новорожденных, угнетение - у недоношенных длительностью не более 5-7 сут.
Церебральная ишемия II степени (средней тяжести)
Возникают угнетение ЦНС, возбуждение или смена фаз церебральной активности (длительностью более 7 дней); неонатальные судороги редки. У недоношенных судороги чаще тонические или атипичные (судорожное апноэ, стереотипные спонтанные оральные автоматизмы, трепетание век, миоклонии глазных яблок, гребущие, плавающие движения рук, педалирующие движения ног). У доношенных - мультифокальные клонические судороги. Приступы обычно кратковременные, однократные, реже повторные. Внутричерепная гипертензия (транзиторная, чаще у доношенных новорожденных). Вегетативно-висцеральные нарушения.
Церебральная ишемия III степени (тяжелая)
Прогрессирующая потеря церебральной активности - свыше 10 дней (в первые 12 ч жизни глубокое угнетение или кома, в период с 12-24 ч кратковременное нарастание уровня бодрствования, с 24-72 ч - нарастание угнетения или кома). Повторные судороги (чаще мультифокальные клонические или тонические), возможен эпилептический статус. Дисфункция стволовых отделов мозга (нарушения ритма сердца и дыхания, зрачковых реакций, сосания и глотания, глазодвигательные расстройства). Поза разгибательная (декортикация или децеребрация). Вегетативновисцеральные нарушения. Прогрессирующая внутричерепная гипертензия (отек мозга).
Диагноз церебральной гипоксии-ишемии и степень ее тяжести устанавливаются на основании данных анамнеза о наличии внутриутробной гипоксии плода или интра-/постнатальной асфиксии у новорожденного, оценки по шкале Апгар, клинических неврологических симптомов и дополнительных методов исследования, включающих НСГ, КТ, ДГ, ЭЭГ. Также учитывают динамическое определение КОС, гематокрита, гемоглобина и газового состава крови. Широко используются результаты суточного мониторинга за такими показателями, как ЧСС, АД, температура тела, SO2, исследование лабораторных показателей в сыворотке (креатинина и билирубина) и плазме (глюкозы, калия, кальция, магния, натрия, остаточного азота) крови. При необходимости (по показаниям) проводится исследование цереброспинальной жидкости. При возможности контролируют содержание нейроспецифических белков, таких как нейроспецифическая енолаза, глиальный фибриллярный кислый белок, основной белок миелина и др.
Гипоксия у новорожденных детей способна приводить к серьезным нарушениям в работе головного мозга. Эта проблема стоит достаточно остро, так как практически каждый 10 младенец страдает от гипоксии в той или иной степени. Гипоксически-ишемическое поражение ЦНС является самым распространенным осложнением, которое развивается на фоне кислородного голодания новорожденного. Часто оно диагностируется у детей, которые появились на свет раньше срока.
Эффективные методы борьбы с гипоксией новорожденных до настоящего времени просто отсутствуют, хотя ученые не перестают работать в данном направлении. Более того, против осложнений, которые вызывает гипоксия, наука вовсе оказывается бессильна. Ни один лекарственный препарат не способен восстановить погибшие клетки головного мозга. Хотя, по уверениям ученых, такие средства уже появились и находятся на стадии клинических испытаний.
Центральная нервная система болезненно реагирует на нехватку кислорода. Когда речь идет о новорожденном ребенке и о ребенке, находящемся в утробе матери, вопрос кислородного голодания встает еще острее. Головной мозг малыша находится на стадии развития, поэтому ему требуется постоянное и бесперебойное питание. Негативным образом отразиться на состоянии ЦНС ребенка могут любые патогенные влияния, которые испытала на себе беременная женщина, либо которые были получены во время родов. Нервная ткань будет повреждена, что в будущем проявится неврологическими нарушениями.
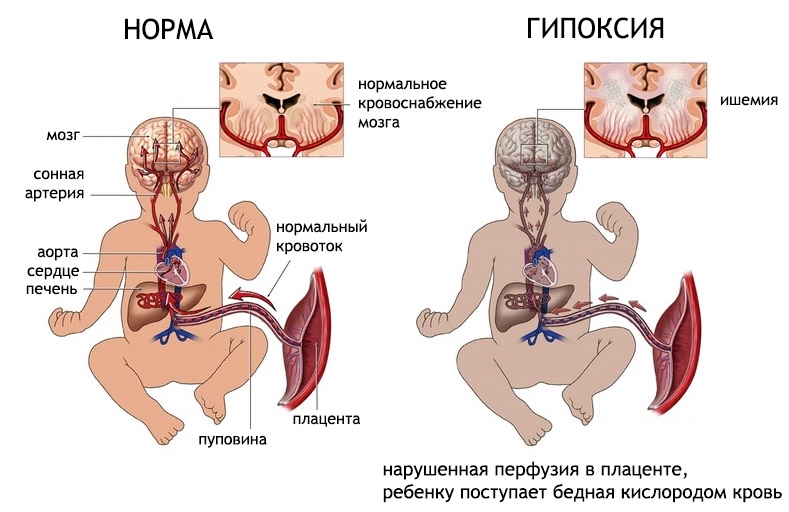
Степень гипоксии различается. Она может быть легкой и тяжелой, может длиться на протяжении нескольких минут или на протяжении нескольких дней и даже месяцев. Однако нарушения в работе головного мозга гипоксия спровоцирует обязательно.
Если при легком течении гипоксии эти нарушения не имеют ярко выраженной симптоматики и могут самостоятельно пройти через определенный промежуток времени, то при глубокой гипоксии изменения будут необратимыми. В этом случае головной мозг подвергается органическим поражениям, что может сделать ребенка инвалидом.
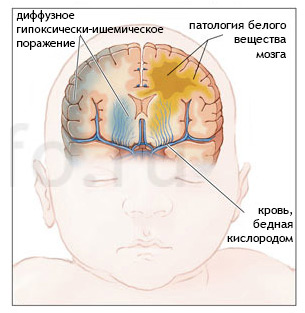
Гипоксия способна развиваться как во время внутриутробной жизни плода, так и во время родов, при условии, что они имеют патологическое течение. Кроме того, гипоксически-ишемические нарушения наблюдаются у детей, которые страдают от патологии органов дыхательной системы, при проблемах, связанных со свертываемостью крови, при резком снижении артериального давления и не только.
В медицинской терминологии используют два понятия. О гипоксически-ишемическом поражении ЦНС говорят в том случае, когда осложнения гипоксии имеют тяжелое течение. Также в данном контексте может быть применен термин гипоксически-ишемическая энцефалопатия. Его чаще всего употребляют, когда головной мозг поражен в легкой степени.
Хотя до настоящего момента времени не утихают споры по поводу того, может ли головной мозг восстанавливаться после перенесенной гипоксии, большинство врачей убеждены, что это возможно. Нервная система детей имеет на вооружении определенные механизмы, которые направлены на то, чтобы самостоятельно себя защищать. Более того, часть ученых настаивает, что головной мозг ребенка даже может регенерировать. Ведь не каждый новорожденный, который перенес глубокое кислородное голодание, становится инвалидом. Более того, далеко не у каждого из них в дальнейшем развиваются какие-либо неврологические нарушения.
Если гипоксия тяжелая, то в первую очередь будут повреждены самые незрелые зоны головного мозга, расположенные в его стволовой части, а также подкорковые узлы. Опасна не только острая, но и продолжительная гипоксия, которая может не сопровождаться выраженными симптомами. Такое кислородное голодание провоцирует диффузное поражение корковых структур мозга. При гипоксии, организм ребенка запускает определенный механизм, который перераспределяет кровоток таким образом, что большая его часть будет направлена именно на стволовую часть мозга. Поэтому при продолжительном кислородном голодании будет страдать преимущественно его серое вещество.
В связи с тем, что осложнения гипоксии могут быть фатальными, неврологи должны уделять самое пристальное внимание осмотру младенцев. Особенно это касается тех детей, которые перенесли гипоксию во время родов, независимо от степени ее тяжести. Следует исключить все адаптационные проявления организма (например, тремор) установить неврологический статус ребенка, обнаружить возможные нарушения в работе нервной системы. При выявлении гипоксических поражений за рубежом опираются на принцип стадийности патологии. В России применяют системный подход, ориентируясь на синдромы, которые могут указывать на развитие осложнений.
Почему возникают поражения ЦНС, стадии их развития
О перинатальном поражении ЦНС говорят в том случае, когда ребенок подвергся воздействию негативных факторов во время периода новорожденности, во время родов или во время нахождения в материнской утробе.
Причины, которые могут спровоцировать нарушения в функционировании нервной системы ребенка:
Нарушение кровотока в матке и плаценте. Тромбоз плаценты, задержка развития плода, кровотечение у беременной женщины.
Прием спиртных напитков во время беременности, курение и прохождение терапии некоторыми лекарственными средствами.
Сильные кровопотери во время родовой деятельности, обвитие пуповины вокруг шеи младенца. Гипотония или брадикардия у ребенка, родовая травма.
Пороки сердца, ДВС-синдром, патологии органов дыхательной системы, эпизоды остановки дыхания у младенца, появившегося на свет.
Нехватка кислорода в артериальной крови является фактором, который запускает нарушения обменных процессов в нервной ткани. В это же время начинают гибнуть отдельные нейроны, либо целые их группы. В таких условиях ткани головного мозга становятся максимально восприимчивыми к любым колебаниям артериального давления. Если в это время у ребенка развивается гипотония, то патологический процесс еще больше усугубляется.
Нарушения метаболических процессов в головном мозге провоцирует ацидоз его тканей, что влечет за собой отек мозга с повышением внутричерепного давления. Это вызывает массивную гибель клеток головного мозга.
Глубокая асфиксия сказывается на функционировании всех органов ребенка. Страдают почки, кишечник, печень. Гипоксия вызывает отмирание тканей этих органов.
Имеются различия в течение осложнений, вызванных кислородным голоданием у детей доношенных и у детей недоношенных. Так, если гипоксии подвергся ребенок, появившийся на свет в положенный срок, то поражена будет в большей степени кора головного мозга, его подкорковые структуры и ствол головного мозга. Если ребенок недоношенный, то у него, скорее всего, разовьется перивентрикулярная лейкомаляция, то есть участки некроза будут сконцентрированы в области боковых желудочков головного мозга.
Степень тяжести гипоксической энцефалопатии имеет прямую взаимосвязь с глубиной ишемического поражения головного мозга.
В связи с этим, различают:
Легкая или 1 степень тяжести. Неврологические нарушения преходящие, спустя 7 дней они будут полностью купированы.
Средняя или 2 степень тяжести. Гипоксически-ишемические нарушения сохраняются на протяжении более чем в одну неделю. При этом нервная система ребенка либо угнетена, либо гипервозбудима, наблюдаются судороги, внутричерепное давление повышено, но повышение не отличается стабильностью. Также появляются расстройства со стороны вегетативной нервной системы.
Тяжелая форма нарушений или 3 степень тяжести. В этом случае ребенок будет находиться либо в коме, либо в сопоре. У него наблюдаются судороги, имеется отек мозга, работа внутренних органов нарушена.
Симптомы гипоксически-ишемического поражения ЦНС
Если у ребенка поражена центральная нервная система, то врачи установят этот факт с первых минут его жизни. Симптомы напрямую зависит от того, какова степень тяжести состояния младенца.
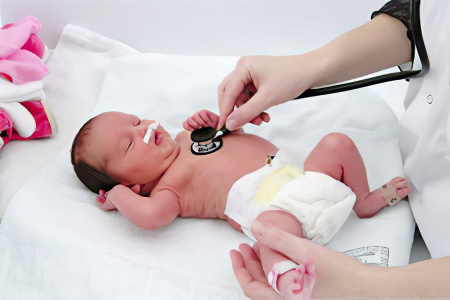
Если гипоксически-ишемическая энцефалопатия имеет легкое течение, то состояние ребенка будет стабильным. По шкале Апгар малыш получает 6-7 баллов. У него будет наблюдаться цианотичное окрашивание кожных покровов, мышечный тонус несколько снижен.
Со стороны нервной системы наблюдаются следующие симптомы:
Нервно-рефлекторная возбудимость повышена.
Сон нарушен, ребенок проявляет беспокойство.
Подбородок и конечности слегка подрагивают.
Ребенок часто срыгивает.
Возможно усиление, либо, напротив, снижение рефлексов.
Как правило, за последующие 7 дней после появления младенца на свет, все эти патологические симптомы будут купированы. Малыш становится спокойнее, начинает прибавлять в весе. Выраженные расстройства со стороны нервной системы отсутствуют.
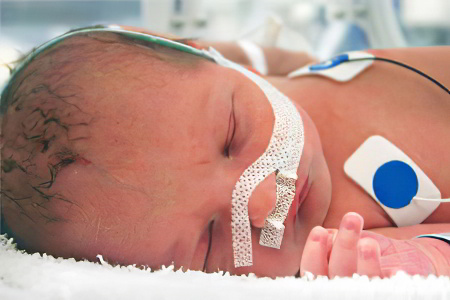
При второй степени гипоксического поражения головного мозга симптомы будут более интенсивными. Чаще всего младенцы со средней тяжестью течения гипоксически-ишемической энцефалопатии страдали от кислородного голодания еще находясь в утробе матери, а также подверглись неблагоприятным факторам во время родовой деятельности. По шкале Апгар такому ребенку выставляют отметку в 5 баллов, у него прослеживаются аритмии, выслушиваются глухие тона сердца.
Нарушения со стороны нервной системы следующие:
Рефлексы угнетены, это справедливо, в том числе, в отношении сосательного рефлекса.
Тонус мышц понижен, произвольные движения минимальны, либо отсутствуют вовсе.
Внутричерепное давление повышается.
Кожные покровы имеют синюшный окрас.
Наблюдаются вегетативные нарушения: возникают периодические остановки дыхания, пульс может ускоряться, часто диагностируется брадикардия. Кишечник сокращается слабо, терморегуляция нарушена.
Ребенок часто срыгивает, может страдать от запора или диареи, вес набирает медленно.
Чем выше внутричерепное давление ребенка, тем большее беспокойство он будет проявлять. Кожа имеет повышенную чувствительность, сон беспокоен. Подбородок и руки ребенка подрагивают, роднички выбухают. У малыша наблюдаются глазодвигательные расстройства, нистагм. Судороги также могут указывать на повышенное внутричерепное давление.
К 7 дню с момента появления ребенка на свет его состояние стабилизируется. Однако при этом он должен получать интенсивную терапию. Полностью к этому времени неврологическая симптоматика не проходит. Если патология прогрессирует, то усиливается угнетение мозговой активности, происходит падение мышечного тонуса. Ребенок может впасть в кому.
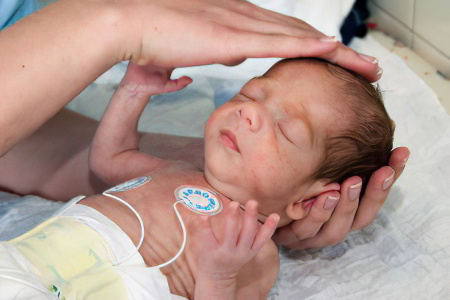
Если у ребенка диагностируется 3 степень гипоксически-ишемических поражений, то у женщины всегда наблюдается тяжелый гестоз второй половины беременности. Она страдает от повышенного артериального давления, у нее наблюдаются нарушения в работе почек, выраженные отеки.
На свет младенец появляется уже с симптомами перенесенного кислородного голодания, Задержка развития явно прослеживается. Если роды протекали с осложнениями, то имеющиеся нарушения будут лишь усугубляться.
Ребенок страдает от выраженного нарушения кровообращения, может не дышать, тонус мышц и рефлекторная активность часто отсутствуют. Если реанимационные мероприятия не будут проведены в экстренном порядке, то ребенок погибает.
В первые же часы после его появления на свет, наблюдается угнетение работы головного мозга, развивается кома. Рефлексы и двигательная активность у младенца отсутствуют, зрачки расширены, реакция на свет нулевая.
Отек головного мозга проявляется судорогами, возможна остановка дыхания и сердечной деятельности. Давление в легочной артерии повышается, фильтрация мочи ухудшается, артериальное давление падает, ткани кишечника начинают отмирать, печень перестает функционировать, развивается ДВС-синдром.
Постасфиксический синдром – это следствие тяжелой гипоксии новорожденного. Ребенок практически обездвижен, не плачет, не реагирует на болевой раздражитель, на прикосновения, кожа бледная, температура тела понижена. Младенец с трудом совершает глотательные и сосательные движения, поэтому кормить его самостоятельно женщина не может. Без интенсивной терапии ребенок погибнет. Прогноз неблагоприятный, о стабильности состояния нельзя сделать заключение ранее 10 дня с момента его рождения.
Последующее нарастание неврологического дефицита характеризует все формы гипоксически-ишемических нарушений. Дело в том, что нейроны, которые были повреждены в результате гипоксии, продолжают погибать.
Возможные варианты течения патологии:
Состояние ребенка быстро улучшается. Прогноз благоприятный.
Неврологические нарушения проходят к моменту выписки младенца из родильного дома. Прогноз благоприятный.
Неврологические нарушения продолжают прогрессировать. Прогноз неблагоприятный.
В течение первого месяца жизни ребенок становится инвалидом.
Неблагоприятное течение со скрытым нарастанием неврологических нарушений, которые развиваются на протяжении первого полугода жизни ребенка.
Энцефалопатия новорожденных делится на 3 периода:
Острый период, который длится на протяжении первого месяца. В это время наблюдаются максимальные расстройства нервной деятельности. Они могут быть слабовыраженными, либо доходить до комы.
Период восстановления, который может продолжаться на протяжении года. В это время у ребенка может появиться судорожный синдром, гидроцефалия, повышается нервно-рефлекторная возбудимость, происходит отставание в физическом и умственном развитии.
Отдаленный период, когда проявляют себя последствия перенесенной гипоксии. Одни симптомы могут исчезать, а другие появляются, например, у ребенка может наблюдаться задержка речевого развития.
Лечение
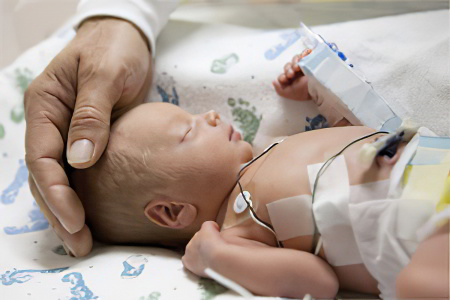
Чтобы выставить диагноз гипоксически-ишемическая энцефалопатия, требуется выявить характерные симптомы у младенца, изучить историю ведения беременной женщины. Также в диагностике патологического состояния оказывают помощь инструментальные методики обследования, среди которых:
Компьютерная томография и магнитно-резонансная томография головного мозга.
Допплерографическое исследование сосудов головного мозга.
Сложность в лечении гипоксически-ишемических осложнений заключается в том, что ни один лекарственный препарат не позволяет добиться восстановления однажды пораженных нервных тканей. Однако нормализовать в той или иной степени работу головного мозга все-таки можно.
В зависимости от превалирования конкретной симптоматики и от тяжести гипоксии, будет различаться терапевтическая схема.
Если гипоксия имеет среднюю или легкую степень тяжести, то ребенку показан прием диуретиков, ноотропных препаратов, лекарственных средств для устранения судорог. При условии, что гипоксия имеет тяжелое течение, пациенту в экстренном порядке проводят интенсивную терапию.
Когда у ребенка присутствуют симптомы легкой гипоксически-ишемической энцефалопатии, но при этом отсутствуют судороги, то врач может ограничиться только наблюдением за пациентом. Иногда при такой клинической картине может быть показан прием Диазепама, но на короткий промежуток времени. Это лекарственное средство способно тормозить развитие ребенка, поэтому его назначают только по строгим показаниям.
Пантогам и Фенибут оказывают комплексный ноотропный и тормозящий эффект на нервную систему ребенка. Нитразепам назначают для нормализации сна ребенка. Также с этой целью может быть использован Экстракт валерианы, мелисса, пустырник, мята. Седативным эффектом обладает массаж и водолечение.
Если гипоксия имеет тяжелое течение, то ребенку назначают противосудорожные препараты, мочегонные средства (Фуросемид, Маннитол, Диакарб) и Магния сульфат.
Ребенка экстренно реанимируют, если у него наблюдается задержка дыхания или остановка сердца. Показано подключение пациента к аппарату ИВЛ, введение кардиотонических препаратов, проведение инфузионной терапии.
Диуретики назначают в качестве основного лекарственного средства при гипертензионно-гидроцефальном синдроме. Предпочтение отдают препарату под названием Диакарб. Его можно использовать для лечения детей любого возраста. К оперативному вмешательству прибегают в том случае, когда консервативная терапия не приносит желаемого эффекта. С этой целью проводят шунтирующие операции с выводом ликвора в полость брюшины или в перикардиальную полость.
Для снятия судорог и уменьшения возбудимости нервной системы назначают такие препараты, как: Диазепам, Фенобарбитал, Клоназепам, Фенитоин. Если ребенок новорожденный то предпочтение следует отдать барбитуратам, а именно Фенобарбиталу. Если ребенок грудной, то ему назначают Карбамазепин.
Для снятия повышенного тонуса с мышц, используют Баклофен или Мидокалм. Если мышечный тонус, напротив, понижен, то ребенку назначают Дибазол и Галантамин. Физиотерапия оказывает подспорье в лечении осложнений, вызванных гипоксией. Для этого ребенка направляют на курсовой массаж, с ним занимаются лечебной гимнастикой. Хорошим эффектом обладает рефлексотерапия и водные процедуры.
Если у ребенка наблюдаются трудности в речевом развитии, что становится очевидным к концу первого года жизни, то ему показан прием Ноотропила и Энцефабола, витаминов группы В. Обязательно малыш должен плотно взаимодействовать с логопедом и дефектологом.
Назначение большого количества лекарственных средств не всегда является верной тактикой лечения детей, перенесших гипоксию с последующей энцефалопатией. Часто без нужды ребенку прописывают Диакарб, ноотропные препараты, витамины, Актовегин. Однако если энцефалопатия имеет легкое течение, эти лекарственные средства не принесут пользы, так как организм сможет восстановиться самостоятельно. Более того, они имеют возрастные противопоказания, поэтому необоснованное их использование может даже нанести вред.
Прогноз
Восстановление ребенка возможно, при этом наступает полноценное выздоровление. Однако нельзя исключать, что малыш останется инвалидом, если гипоксия имела тяжелое течение. Также возможно развитие незначительной мозговой дисфункции с малосимптомным течением патологии.
Последствиями гипоксически-ишемической энцефалопатии является эпилепсия, ДЦП, гидроцефалия, олигофрения. Последнее нарушение отличается стойкостью во времени, вылечить олигофрению невозможно.
Если ребенок незначительно отстает в развитии на протяжении первого года жизни, но при этом получает адекватное лечение, скорее всего, он догонит своих сверстников в недалеком будущем, и ничем не будет отличаться от здоровых детей.
Рубрика МКБ-10: P91.6
МКБ-10 / P00-P96 КЛАСС XVI Отдельные состояния, возникающие в перинатальном периоде / P90-P96 Другие нарушения, возникающие в перинатальном периоде / P91 Другие нарушения церебрального статуса у новорожденного
Гипоксически-ишемическая энцефалопатия
Синонимы: перинатальное гипоксическое поражение мозга, постасфиктическое поражение головного мозга.
Гипоксически-ишемическая энцефалопатия — синдром, характеризуемый наличием признаков острого повреждения головного мозга в результате недостаточного кровоснабжения головного мозга ребенка во время беременности матери, родов или в течение первого месяца его жизни.
Гипоксически-ишемическая энцефалопатия является наиболее распространенным поражением среди всей перинатальной патологии нервной системы.
Основными причинами перинатальной гипоксии-ишемии являются:
• внутриутробная гипоксия (нарушения маточно-плацентарного и/или фетоплацентарного кровотока);
• интра- и постнатальная асфиксия, РДС (Респираторный дистресс — синдром), повторяющиеся приступы апноэ, врожденная пневмония или аспирационный синдром;
• ВПС (врожденные пороки сердца), гемодинамически значимый ОАП (открытый артериальный проток), персистирование фетальных коммуникаций;
• постнатальные нарушения системной гемодинамики, приводящие к резкому падению системного АД и снижению церебральной перфузии.
Развивающийся мозг является гетерогенным образованием по степени зрелости (морфологической и функциональной) его тканевых и сосудистых компонентов. Особенности архитектоники и морфологии церебральных сосудов новорожденных лежат в основе специфических механизмов, обеспечивающих регуляцию интенсивности мозгового кровотока на региональном уровне в ответ на асфиксию.
В настоящее время показано, что у недоношенных новорожденных (при сроке гестации менее 35 нед) гипоксемия приводит к повышению кровотока в стволе головного мозга и перивентрикулярных областях белого вещества. У доношенных новорожденных при поддержании системного АД на нормальном уровне гипоксемия вызывает усиление кровотока во всех областях мозга, но более всего в области ствола, глубоких отделов больших полушарий и базальных ганглиев как структур, обеспечивающих жизненно важные функции и рефлекторно-двигательные реакции. Дефицит кровоснабжения мозга приводит к ишемическому поражению зон пограничного или коллатерального кровоснабжения бассейнов мозговых артерий, имеющих различное расположение в зависимости от гестационного возраста.
В этих условиях поступление обогащенной кислородом крови в участки, перенесшие ранее ишемическое воздействие, приводит к активации процессов свободнорадикального окисления, сопровождающегося накоплением токсичных продуктов и возбуждающих аминокислот (глутамат, N-метил-D-аспарагиновая кислота и др.). В итоге каскада патологических процессов, инициированных тканевой гипоксией-ишемией в очагах повреждения под действием цитокинов и ИЛ, развивается воспалительная реакция нейроглии, что обусловливает дальнейшее повреждение паренхимы мозга, длительность которого может варьировать от нескольких часов до нескольких недель.
Церебральная гипоксия — ишемия I степени (легкая)
Возбуждение ЦНС чаще возникает у доношенных новорожденных, угнетение — у недоношенных длительностью не более 5-7 сут.
Церебральная ишемия II степени (средней тяжести)
Возникают угнетение ЦНС, возбуждение или смена фаз церебральной активности (длительностью более 7 дней); неонатальные судороги редки. У недоношенных судороги чаще тонические или атипичные (судорожное апноэ, стереотипные спонтанные оральные автоматизмы, трепетание век, миоклонии глазных яблок, гребущие, плавающие движения рук, педалирующие движения ног). У доношенных — мультифокальные клонические судороги. Приступы обычно кратковременные, однократные, реже повторные. Внутричерепная гипертензия (транзиторная, чаще у доношенных новорожденных). Вегетативно-висцеральные нарушения.
Церебральная ишемия III степени (тяжелая)
Прогрессирующая потеря церебральной активности — свыше 10 дней (в первые 12 ч жизни глубокое угнетение или кома, в период с 12-24 ч кратковременное нарастание уровня бодрствования, с 24-72 ч — нарастание угнетения или кома). Повторные судороги (чаще мультифокальные клонические или тонические), возможен эпилептический статус. Дисфункция стволовых отделов мозга (нарушения ритма сердца и дыхания, зрачковых реакций, сосания и глотания, глазодвигательные расстройства). Поза разгибательная (декортикация или децеребрация). Вегетативновисцеральные нарушения. Прогрессирующая внутричерепная гипертензия (отек мозга).
Диагноз церебральной гипоксии-ишемии и степень ее тяжести устанавливаются на основании данных анамнеза о наличии внутриутробной гипоксии плода или интра-/постнатальной асфиксии у новорожденного, оценки по шкале Апгар, клинических неврологических симптомов и дополнительных методов исследования, включающих НСГ, КТ, ДГ, ЭЭГ. Также учитывают динамическое определение КОС, гематокрита, гемоглобина и газового состава крови. Широко используются результаты суточного мониторинга за такими показателями, как ЧСС, АД, температура тела, SO2, исследование лабораторных показателей в сыворотке (креатинина и билирубина) и плазме (глюкозы, калия, кальция, магния, натрия, остаточного азота) крови. При необходимости (по показаниям) проводится исследование цереброспинальной жидкости. При возможности контролируют содержание нейроспецифических белков, таких как нейроспецифическая енолаза, глиальный фибриллярный кислый белок, основной белок миелина и др.
Лечение и профилактика см. Другие внутричерепные (нетравматические) кровоизлияния у плода и новорожденного
Таблица 2 — Схема применения леветирацетама. Версия для печати Скачать или отправить файл.
Коды МКБ: G00-G99
Таблица 2 — Схема применения леветирацетама. Версия для печати Скачать или отправить файл. Союз педиатров России Клинические рекомендации. МКБ P Год утверждения частота пересмотра : пересмотр каждые 3 года Последствия перинатального поражения центральной нервной системы с эпилепсией — поражение головного мозга в определенный период его развития с последующим формированием хронической пароксизмальной болезни, проявляющейся повторными судорожными или бессудорожными стереотипными припадками.
Довольно часто заболевание является исходом перинатального поражения центральной нервной системы гипоксически-ишемического генеза Церебральная ишемия P Анатомо-морфологические изменения головного мозга при тяжелых перинатальных поражениях, гидроцефалии, детском церебральном параличе являются органическим субстратом для возникновения аномальной электрической активности мозга с формированием эпилептических пароксизмов.
Задержка психомоторного развития. Риск формирования симптоматической эпилепсии. Недоношеннность недель в анамнезе. Спастический тетрапарез. Симптоматическая фокальная эпилепсия. Инфантильные спазмы Синдром Веста G Недоношеннность 24 недели в анамнезе. Классификация последствий перинатальных поражений нервной системы у детей первого года жизни Российская ассоциация специалистов перинатальной медицины, г.
Таблица 1 — Классификация последствий перинатальных поражений нервной системы у детей первого года жизни Российская ассоциация специалистов перинатальной медицины, г.
Этиология и патогенетическая основа. Варианты клинического течения. Основные нозологические формы. Последствия перинатального поражения центральной нервной системы гипоксически-ишемического генеза Церебральная ишемия II-III степени. Внутричерепное нетравматическое кровоизлияние у плода и новорожденного II,.
III степени P Симптоматические эпилепсии и эпилептические синдромы раннего детского возраста. Риск формирования или сформированная эпилепсия раннего возраста G Неврологические отклонения не компенсированы к первому году жизни. Частыми причинами формирующейся эпилепсии являются тяжелые перинатальные поражения центральной нервной системы гипоксически-ишемического и травматического генеза, церебральная ишемия II, III степени, внутричерепное кровоизлияние II, III степени.
Гипоксия плода — неспецифическое проявление различных осложнений беременности и родов, прежде всего токсикозов беременных. Степень и выраженность токсикоза, его связь с экстрагенитальной патологией женщины особенно с болезнями сердечно-сосудистой системы определяют длительность и выраженность гипоксии плода, центральная нервная система которого наиболее чувствительна к кислородной недостаточности.
Антенатальная гипоксия приводит к замедлению роста капилляров головного мозга, увеличивает их проницаемость. Возрастают проницаемость клеточных мембран и метаболический ацидоз, развивается ишемия мозга с внутриклеточным ацидозом. Антенатальная гипоксия часто сочетается с интранатальной асфиксией. Гипоксия и асфиксия сопровождаются комплексом компенсаторно-приспособительных реакций, важнейшей из которых является усиление анаэробного гликолиза.
Воздействие гипоксии приводит к комплексу микроциркуляторных и метаболических расстройств, которые на тканевом уровне вызывают два основных повреждения: геморрагический инфаркт и развитие ишемии с последующей лейкомаляцией вещества мозга. Геморрагическому особенно и ишемическому поражению вещества мозга способствуют некоторые манипуляции в первые часа жизни ребенка: введение гиперосмолярных растворов, искусственная вентиляция легких ИВЛ и связанная с ней гипоперфузия мозга на фоне падения напряжения углекислого газа, недостаточная коррекция объема циркулирующей крови и др.
Наиболее часто геморрагический инфаркт и ишемия развиваются у плодов и новорожденных в области перивентрикулярных сплетений — субэпендимально в сочетании с поражением вещества мозга.
Кровоизлияние может происходить также в боковые желудочки мозга и в субарахноидальное пространство. Помимо описанных изменений, морфологическим субстратом гипоксии, как правило, является полнокровие мозга, его общий или локальный отек.
Нарушение гемодинамики макро- и микроциркуляции приводят к многовариантным метаболическим сдвигам нарушение кислотно-основного состояния и электролитного баланса, дестабилизация клеточных мембран, гипоксемия и тканевая гипоксия , а эти сдвиги в свою очередь усугубляют расстройства микроциркуляции.
У недоношенных детей повреждающее действие внутриутробной гипоксии потенцируется незрелостью сосудов головного мозга, дезадаптацией в интранатальном периоде. В последние годы расшифрованы тонкие механизмы патогенеза гипоксически-ишемических поражений мозга. Установлена роль выброса свободно-радикальных веществ и нарушений перекисного окисления липидов в повреждении мембран нервных клеток, роль блокады кальциевых каналов, страдания энергетических субклеточных структур — в первую очередь митохондрий.
Установлено, что повреждающее воздействие различных факторов может реализоваться как в форме быстрой гибели клетки нейрональный некроз , так и в форме отсроченной, замедленной гибели — апоптоз. Установлено, что пострадавшие нейроны через межнейронные связи могут обусловить каскады патологических реакций, которые так же необходимо купировать, что обусловливает необходимость своевременного лечения и реабилитации детей с перинатальной патологией [4, 16, 19, 20, 22].
Этиологические факторы эпилепсии включают также травмы и инфекционные заболевания, метаболические нарушения, генетическую предрасположенность.
Кроме того, эпилепсия нередко сопровождает врожденные пороки развития ЦНС гидроцефалия, порэнцефалия, микрогирия, агенезия мозолистого тела, другие виды дизгенезий головного мозга , например, при синдроме Айкарди. Установлена или предполагается генетическая природа многих форм эпилепсии. Существуют также гипотезы и исследования об участии иммунных, в том числе аутоиммунных, механизмов развития эпилепсии [27,28].
Основной патогенетический механизм эпилепсии — аномальное возбуждение и торможение нейрональных мембран и нейронов нейромедиаторами и распространение судорожной активности.
На клеточном уровне при этом заболевании происходят многочисленные изменения в функциях ионных каналов, регуляции рецепторов нейротрансмиттеров и метаболизма энергии, что приводит к развитию приступов. Под воздействием различных провоцирующих факторов нормальный уровень нейрональной активации трансформируется в синхронные разряды с формированием паттерна аномальной активации. Вид эпилептического приступа зависит от локализации и количества клеток ЦНС, задействованных в этом процессе. Повторные и непровоцируемые эпилептические приступы как правило сочетаются с выраженными анатомическими и патофизиологическими нарушениями, часто генетически детерминированы.
Эпилептический очаг — несколько аномально функционирующих нейронов, действующих патологически синхронно. Критерием эпилептизации нейрона является деполяризация мембраны уменьшение величины отрицательного заряда при поляризации.
Возникновение эпилептического приступа происходит при внутриклеточной пароксизмальной деполяризации, которая в интериктальном периоде сменяется глобальной деполяризацией [30,31]. Существуют также эпилепсии, обусловленные метаболическими нарушениями нарушение обмена креатина, метаболизма аминокислот, пурина и пиримидина, ГАМК. Витаминозависимые эпилепсии связаны с недостаточностью витамина В6, фолатов и других микроэлементов.
Простые парциальные приступы ППП , наиболее распространенные у детей раннего возраста, зависят от места локализации эпилептогенного очага, могут протекать с различными феноменами: моторными, соматосенсорными, вегетативными и др. При простых парциальных вегетативных приступах ППВП преобладают вегетативные симптомы, при этом эпилептогенный очаг локализуется в орбито-инсуло-темпоральной области.
Сложные парциальные приступы СПП протекают с изменением сознания, которое сложно зафиксировать у детей раннего возраста [27,30]. Жалобы и анамнез. При сборе анамнеза и жалоб следует учитывать:. Лабораторная диагностика. Сила рекомендаций — 1; достоверность доказательств — С. Комментарии : оценивается функция печени на фоне приема противоэпилептических препаратов. Комментарии : исследование проводится с целью выявления и дальнейшей коррекции лактатацидоза. Инструментальная диагностика. Комментарии : у пациентов с последствиями перинатального поражения центральной нервной системы с эпилепсией возможно выявление признаков внутричерепной гипертензии, врожденной атрофии зрительного нерва, характерных изменений для наследственных болезней обмена веществ.
Комментарии : проводится у пациентов с последствиями перинатального поражения центральной нервной системы с эпилепсией при подозрении на тугоухость [6]. Медико-генетическое консультирование. Иная диагностика. Консультации специалистов проводятся по показаниям. Дифференциальный диагноз проводится с эпилепсией, обусловленной токсико-метаболическими нарушениями функции ЦНС, перинатальными инфекционными заболеваниями, генетически детерминированными эпилепсиями.
Дифференциальный диагноз проводится с наследственными генетическими синдромами, митохондриальными заболеваниями, сопровождающимися эпилептическими приступами. Консервативное лечение. При эпилепсии требует длительного многолетнего приема препаратов, должно быть строго индивидуализированным и следует учитывать риск нежелательных лекарственных реакций. Для подбора адекватной противоэпилептической терапии необходимы данные о клинических особенностях приступа, динамике заболевания, механизме действия противоэпилептичеких препаратов.
Лечение начинают с назначения одного препарата, увеличивая его дозу до тех пор, пока приступы не прекратятся или не проявится токсическое действие препарата. Если назначенное средство не позволяет осуществлять контроль над приступами, его постепенно отменяют по мере назначения другого препарата и увеличения его дозы.
Масса тела, кг. Длительность лечения устанавливается индивидуально. Комментарии : антиспастическая терапия с целью снижения тонуса сосудов и снижения мышечного тонуса, улучшения произвольных активных движений. Хирургическое лечение. Нейрохирургическое лечение проводится по показаниям, возможна коррекция прогрессирующей гидроцефалии. В современной мировой литературе также сообщается об использовании следующих видов нейрохирургических операций при различных резистентных к лечению эпилептических синдромах: передняя темпоральная лобэктомия; ограниченная темпоральная резекция, а также экстратемпоральная неокортикальная резекция.
В России данные методы лечения не используются. Комплекс реабилитационных мероприятий разрабатывается индивидуально и включает физические факторы:. Комплексное восстановительное лечение пациента с последствиями перинатального поражения центральной нервной системы с эпилепсией должно начинаться в максимально ранние сроки, что в большинстве случаев позволяет предотвратить формирование стойкого неврологического дефицита, существенно снизить риск развития осложнений и степени инвалидизации больного [5,6,15,23,24, 26,27,30].
Исходы и прогноз последствий перинатального поражения центральной нервной системы с эпилепсией. Прогноз для жизни благоприятный, зависит от вида и тяжести эпилептических приступов, этиологии, своевременного начала терапии, наличия или отсутствия сопутствующих, в том числе неврологических заболеваний, определяется ответом на терапию противоэпилептическими препаратами.
Прогноз для здоровья — при формировании эпилепсии зависит от времени начала противоэпилептической терапии, реабилитации, этапности, преемственности между этапами, мультидисциплинарного подхода, повторных курсов реабилитации по показаниям, отсутствия фармакорезистентности к противоэпилептическим препаратам.
Адекватная реабилитация позволяет снизить тяжесть неврологического дефицита, социализировать ребенка в соответствии с его уровнем психического развития и моторных навыков.
Законодательная база Российской Федерации
Справочник кодов общероссийских классификаторов. КлассИнформ — все коды общероссийских классификаторов. Воспалительные болезни центральной нервной системы. Системные атрофии, поражающие преимущественно центральную нервную систему. Экстрапирамидные и другие двигательные нарушения.
Другие нарушения церебрального статуса у новорожденного (P91)
ДРУГИЕ НАРУШЕНИЯ НЕРВНОЙ СИСТЕМЫ (G90-G99)
ПОСМОТРИТЕ ВИДЕО ПО ТЕМЕ: МКБ 10 на телефоне
Читайте также:


