Интраоперационный нейромониторинг возвратного нерва

В настоящее время неуклонно растет число пациентов с хирургической патологией щитовидной и околощитовидных желез. Это связано как с широкой доступностью диагностических процедур, так и с сохранением йодной недостаточности во многих регионах России, приводящей к диффузным и узловым изменениям в ткани щитовидной железы.
В 2014 г. в России диагностировано около 10 тыс. впервые выявленных злокачественных опухолей щитовидной железы, с динамикой прироста выявленных случаев с 2004 г. по 2014 г. на 18,47%. Хирургические вмешательства до сих пор остаются основным методом лечения опухолей щитовидной железы.
Одним из осложнений этого раздела хирургии является парез, или паралич гортани. Основной причиной нарушения функции гортани является интраоперационное повреждение возвратного гортанного нерва (ВГН). Различают временный и постоянный, а также односторонний и двусторонний парезы. Частота временного пареза верхних гортанных нервов, по данным разных авторов, варьирует от 0,5 до 18%, постоянного – от 0,2 до 1%.
Повреждение нерва приводит к парезу мышц, суживающих, расширяющих, а также натягивающих голосовые складки. Парез гортани может проявляться симптомами от незаметной охриплости голоса до таких жизнеугрожающих состояний, как стридор и обструкция верхних дыхательных путей при двустороннем парезе, что может потребовать наложения трахеостомы и привести к инвалидизации пациента.
Вероятность развития пареза гортани возрастает при повторных операциях на щитовидной железе, злокачественных опухолях с распространением за пределы щитовидной железы, загрудинном расположении зоба, а также обратно коррелирует с количеством выполненных хирургом операций. При этом некоторые авторы указывают, что даже опытный хирург не застрахован от возникновения у пациента пареза гортани.
Со времен Н. В. Лежнева и F. Н. Lahey золотым стандартом в контроле повреждения ВГН является его визуализация. Показано снижение количества парезов в группе пациентов с визуальной идентификацией нерва. Важно отметить, что основным механизмом развития пареза гортани является натяжение ВГН – тракция. До 80% парезов гортани связаны с перерастяжением ВГН. Таким образом, только визуального контроля недостаточно для оценки функционального состояния нерва. Опубликованные данные показывают, что парезы ВГН подчас выявляются, даже если интраоперационно нерв был визуализирован.
Появление в арсенале хирургов и анестезиологов интраоперационного нейромониторинга (ИОНМ) ВГН позволяет контролировать сохранность нервных структур на протяжении всей операции, прогнозировать функцию ВГН в послеоперационном периоде, а также получать графическое отражение функции ВГН с соответствующей документацией.
Учитывая растущую актуальность применения ИОНМ, усиливается и необходимость информирования о некоторых особенностях его применения не только хирургов, но и анестезиологов. Неверный выбор миорелаксанта, его дозировки, кратности и времени введения, незнание тонкостей позиционирования эндотрахеальной трубки и ларингеального электрода могут сделать весь нейромониторинг (НМ) бесполезной дорогостоящей процедурой.
По мнению зарубежных авторов, для стабильной работы ИОНМ операционной бригаде необходимо провести не менее 100 операций с его использованием. Основная задача данного обзора состоит в описании методики ИОНМ при оперативных вмешательствах на щитовидной и околощитовидных железах с позиции врача анестезиолога-реаниматолога, а также демонстрации важности тесного взаимодействия хирурга и анестезиолога при его проведении.
Система ИОНМ состоит из трех основных компонентов: регистрирующий электрод в области голосовых складок на эндотрахеальной трубке (ЭТТ), стимулирующий зонд и регистрирующий блок. Основной принцип действия ИОНМ состоит в том, что хирург при касании зондом нерва получает характерный звук и графическое изображение на мониторе регистрирующего блока. Данная информация позволяет дать прогноз в отношении целостности и послеоперационного состояния ВГН.
Патофизиологически повреждение нерва может быть обусловлено следующими причинами: компрессия, деваскуляризация, пересечение или избыточная тракция во время выделения. Согласно последним исследованиям, именно тракционный механизм является ведущей причиной послеоперационных парезов. В многочисленных исследованиях показано, что до 70-80% парезов гортани связано с натяжением железы и повреждением ВГН в области бугорка Цукеркандля, когда нерв пересекает связку Берри.
В настоящее время выделяют два типа повреждения ВГН: сегментарный и глобальный. При сегментарном типе повреждения хирург может точно определить с помощью нейромонитора точку повреждения (выше нее идет сигнал, ниже сигнал отсутствует), при глобальном типе повреждения сигнала нет на всем протяжении нерва. Прогностически сегментарный тип повреждения хуже, при нем восстановление функции гортани происходит медленнее.
Одним из главных компонентов ИОНМ ВГН в хирургии щитовидной и околощитовидной желез является адекватный режим миорелаксации. Это обусловлено особенностями самого метода – необходимость получить нейромышечный ответ с голосовых складок при стимуляции нерва, что, естественно, невозможно в условиях полного нейромышечного блока (НМБ).
В этой ситуации крайне важна роль анестезиолога. С одной стороны, ему надо обеспечить безопасность пациента, атравматичную интубацию трахеи и комфортную работу хирурга, а с другой – полноценное функционирование системы НМ. В арсенале анестезиолога есть большой выбор миорелаксантов: недеполяризующие средней и короткой продолжительности и деполяризующий – сукцинилхолин.
Именно сукцинилхолин по своим фармакокинетическим свойствам наиболее хорошо соответствует требованиям для проведения НМ – быстрый эффект и короткая продолжительность действия. Но он обладает рядом побочных эффектов, обусловленных механизмом его действия. Их спектр – от минимальных до катастрофических, таких как мышечная боль, аритмии, высвобождение калия, злокачественная гипертермия. Несмотря на вышеперечисленное, сукцинилхолин остается весьма распространенным препаратом в анестезиологии.
Рекомендовано избегать его применения у пациентов с исходной гиперкалиемией, острым почечным повреждением, хронической болезнью почек, внутричерепной и внутриглазной гипертензией, принимающих статины и имеющих в анамнезе злокачественную гипертермию или предрасположенность к ней, аллергию на препарат и диагностированный дефицит активности псевдохолинэстеразы.
Существуют рекомендации, что при использовании ИОНМ вообще следует воздержаться от любых миоплегических агентов. Вместе с тем интубация без использования миорелаксантов может быть сопряжена с техническими трудностями. В исследовании Y. D. Han et al. (2015 г.) группа пациентов без применения миорелаксантов имела достоверно меньший балл по шкале Купера, нежели при использовании даже половинной дозы рокурония, не говоря уже о полной. Причем оптимальное соотношение легкости интубации по шкале Купера и качества НМ было в группе пациентов, получивших полную расчетную дозу рокурония.
Необходимо отметить, что в данном исследовании время от индукции анестезии и интубации до кожного разреза в среднем превышало 20 мин, а время до начала НМ и, соответственно, регистрации нейромышечного ответа на голосовых связках от ВГН или блуждающего нерва до резекции щитовидной железы – более 30 мин. В другом исследовании время от развития НМБ до начала НМ составляло в среднем 36 + 9 мин.
Это согласуется с данными производителя препаратов о прогнозируемой продолжительности действия рокурония в расчетной дозировке. Также не стоит забывать, что в большинстве случаев длительность НМБ под действием миорелаксантов основана на данных TOF-мониторинга (с мышцы, приводящей большой палец руки), в то время как при проведении ИОНМ ВГН нас интересует движение голосовых складок.
В работе F. Marusch et al. (2005 г.) показано, что сигнал с голосовых складок в ответ на стимуляцию ВГН был получен у всех пациентов, у которых по данным TOF-мониторинга степень релаксации находилась на отметке выше 90%. Таким образом, в мышцах гортани нейромышечная проводимость восстанавливается значительно быстрее, нежели в мышце, приводящей большой палец кисти.
Достаточно интересные данные представлены в небольшом исследовании I. С. Lu et al. (2013 г.) на свиньях: сукцинилхолин в дозе 1 мг/кг и рокуроний в дозе 0,3 мг/кг обеспечивают восстановление нервно-мышечной проводимости на 80% от исходного уровня через 19 и 16 мин соответственно, в то время как 0,6 мг/кг рокурония – через 29 мин. При этом возвращение к исходному уровню в первых двух группах произошло через 30 мин, а в третьей не произошло даже через 1 ч. У этой публикации имеется ряд недостатков, о которых упоминают и сами авторы: достаточно небольшая выборка и значительная вариабельность амплитуды электромиографии.
Опубликованы результаты работ об интраоперационном применении антагониста недеполяризующих миорелаксантов сугаммадекса для полной реверсии НМБ, вызванного рокуронием и векуронием, с целью обеспечения полноценного НМ. В дозе 16 мг/кг сугаммадекс позволяет полностью восстановить нейромышечную проводимость после введения расчетной дозировки аминостероидных миорелаксантов. Впрочем, использование столь дорогостоящего препарата исключительно для этих целей не всегда обосновано по соотношению стоимость – эффективность.
Не менее важным компонентом успешного НМ является правильное позиционирование ларингеального электрода. До интубации не рекомендовано использовать лидокаиновые гели и другие лубриканты, наносимые на поверхность ЭТТ. Размер ЭТТ должен быть таким, чтобы обеспечить максимальный контакт электрода с голосовыми складками, при этом желательно использовать ЭТТ наибольшего размера, допустимого у данного пациента. Глубина введения ЭТТ больше у мужчин, чем у женщин, и зависит от роста, но не от массы тела и возраста.
Установка ЭТТ может быть проведена как при обычной ларингоскопии, так и при использовании видеоларингоскопа, что позволит увидеть корректность нахождения ЭТТ не только анестезиологу, но и всей операционной бригаде. Имеет значение также поворот ЭТТ в руках анестезиолога в момент интубации. Доктора-правши при установке ЭТТ непреднамеренно поворачивают ее по часовой стрелке, что может привести к смещению электрода и неэффективности НМ. Чтобы этого избежать, можно делать отметку на трубке на 12 ч и при дислокации делать корректирующий поворот.
В хирургии щитовидной и околощитовидной желез для обеспечения максимальной визуализации операционного поля пациент находится в положении гиперэкстензии. Некоторые хирурги предпочитают подкладывать валик под плечи. Все эти манипуляции несут риск смещения ЭТТ, дислокации электрода и в итоге ведут к потере ответа с голосовых складок при стимуляции ВГН.
Смещение ЭТТ при разгибании шейного отдела позвоночника происходит в проксимальном направлении приблизительно на 6 мм. При гиперэкстензии шеи ЭТТ смещается проксимально в 90% случаев, причем в меньшей степени, если она не была зафиксирована до разгибания. Изменение положения трубки может произойти и во время операции, например, из-за ассистента, опирающегося на лицо пациента.
Фиксация трубки должна быть, с одной стороны, надежной, а с другой – легко снимаемой, для облегчения репозиции ЭТТ при ее смещении. Место узла должно соответствовать уровню губ, поскольку это препятствует смещению ЭТТ дистально. Подтверждение позиции электродов можно произвести с помощью назоларингоскопии фиброоптической техникой. Тем не менее в 10% случаев может потребоваться репозиция ЭТТ для достижения оптимального контакта электродов с голосовыми складками.
В международных рекомендациях по ИОНМ приводится три теста, при помощи которых можно проверить корректность положения ларингеальных электродов:
- респираторная вариабельность базовой линии: после интубации и окончания действия миоплегии, но до развития достаточной глубины анестезии на основе ингаляционных анестетиков (ИА) на экране нейромонитора появляется респираторная вариабельность базовой линии амплитудой от 30 до 70 мВ. Ее наличие подтверждает корректность позиционирования ЭТТ, но требует дополнительной седации пациента после обнаружения ввиду возможности появления выраженной мышечной активности (кашель) и, как следствие, смещения ЭТТ;
- повторная ларингоскопия или фиброоптическая бронхоскопия;
- TAP-test: хирург или анестезиолог пальцем надавливает на щитовидный или перстневидный хрящ для получения ответа с голосовых связок на механическое раздражение (впрочем, корректность данного теста подвергается сомнению).
Давно известно, что галогенсодержащие ИА удлиняют НМ Б как деполяризующего, так и недеполяризующего (в большей степени) типа, хотя механизм остается до конца неясным. Причем между различными препаратами наблюдается разница в степени усиления НМБ. ИА не только удлиняют НМБ, но и сами вызывают дозозависимую миорелаксацию поперечно-полосатой мускулатуры.
В исследовании Н. Wulf et al. изучали влияние ингаляций севофлурана, десфлурана и изофлурана на продолжительность НМБ, вызванного рокуронием, в сравнении с тотальной внутривенной анестезией (ТВВА): потребность в миорелаксанте в группах ИА была достоверно ниже, чем в группе ТВВА. Причем в группе изофлурана отмечалась меньшая выраженность потенцирования НМБ.
Также отмечено, что она может зависеть не только от анестетика, но и от типа недеполяризующего миорелаксанта – НМБ под действием аминостероидных препаратов пролонгируется в большей степени, нежели бензилизохинолиновых, и что данный эффект проявляется только при концентрации ИА от 1 МАК.
Для оценки влияния анестетиков и гипнотиков на НМБ при появлении гортанно-глоточных рефлексов у пациента во время манипуляций хирурга болюсно вводили пропофол или тиопентал, что никак не влияло на НМБ, но вызывало снижение артериального давления, причем в большей степени в группе пропофола. При сравнении влияния пропофола, севофлурана и изофлурана на потребность в инфузии мивакурия для достижения целевых значений НМБ показано, что галогенсодержащие ИА снижали дозировку релаксанта в течение анестезии.
С другой стороны, есть данные, что восстановление нейромышечной проводимости при применении севофлурана происходит быстрее в сравнении с пропофолом. Но при этом частота проявлений гортанно-глоточных рефлексов в группе севофлурана была ниже.
Наркотические анальгетики, используемые при общей анестезии, не только не пролонгируют НМБ, но, наоборот, могут повышать мышечный тонус и вызывать мышечную ригидность. Точный механизм не выяснен, но, вероятнее всего, это связано с воздействием на центральную нервную систему. Наиболее часто этот эффект проявляется при использовании высоких доз данных препаратов, хотя описаны случаи его проявления и при дозе, снижающей ноцицептивную стимуляцию при интубации трахеи. Адекватной профилактикой может быть использование как внутривенных гипнотиков (тиопентал, мидазолам, пропофол), так и собственно миорелаксантов.
Информация о влиянии анестетиков на НМБ достаточно противоречива. Использование ИА или ТВВА остается на усмотрение анестезиолога.
Резюмируя вышеизложенное, остается добавить, что ИОНМ ВГН – относительно новое и, безусловно, крайне важное и актуальное направление в анестезиологии и хирургии. Но, как уже указывалось, успешное функционирование НМ зависит от всей операционной бригады. Этого можно добиться только при полном взаимодействии и взаимопонимании хирурга и анестезиолога, а также их информированности об особенностях методики.
Казалось бы, незначительные мелочи могут сыграть решающую роль в качестве жизни пациента после операции. Несмотря на то что НМ ВГВ сравнительно новый метод, о нем написано достаточно много. Тем не менее многие аспекты применения НМ требуют дальнейшего рассмотрения и изучения.
М. А. Алексеев, В. А. Макарьин, О. В. Кулешов, А. А. Успенская,
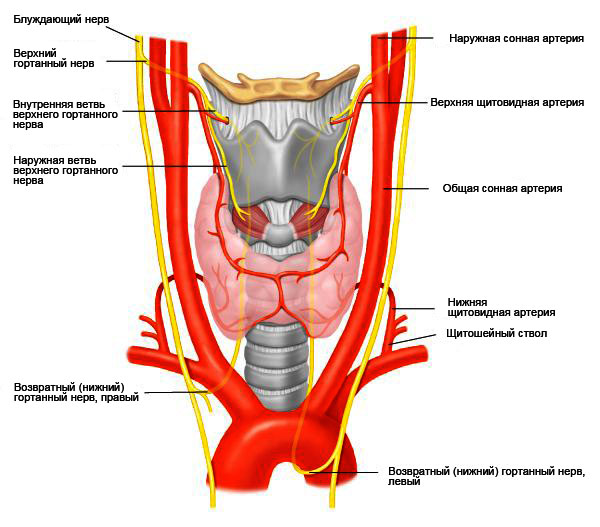
Анатомия гортанных нервов и щитовидной железы
Нервы имеют очень малую толщину - верхний гортанный нерв имеет диаметр около 1 мм, а нижний гортанный нерв (его еще называют возвратным гортанным нервом) - от 2 до 4 мм. При этом и место прохождения нервов, и их количество, и диаметр могут различаться у разных пациентов. Это создает дополнительные трудности при проведении операций.
 |
Функция верхнего гортанного нерва заключается в обеспечении натяжения голосовых связок, благодаря чему человек способен петь высокие ноты и длительно разговаривать. При повреждении верхнего гортанного нерва развивается голосовая утомляемость (после 5-10 минут разговора голос "срывается" и становится сиплым, слабым, что требует остановки разговора и отдыха в течение 10-15 минут). Также у пациентов с повреждением верхнего гортанного нерва изменяется тембр голоса - он становится более низким, исчезает возможность пения, особенно пропевания высоких нот. Для певцов потеря функции данного нерва может стать фатальной. Хорошо известна история всемирно знаменитой итальянской певицы Амелиты Галли-Курчи (Amelita Galli-Curci), обладательницы колоратурного сопрано, которая после операции на щитовидной железе в 1935 году вследствие повреждения верхнего гортанного нерва потеряла свой знаменитый тембр и была вынуждена оставить сцену навсегда.
Еще большее значение для человека имеет функция нижнего (возвратного) гортанного нерва, который обеспечивает подвижность голосовых связок. Для того, чтобы человек был способен произносить звуки, обе голосовые связки должны быть подвижны. При произнесении звуков голосовые связки смыкаются, при дыхании - расходятся в стороны. Если при операции повреждается один возвратный нерв, то голосовая складка с соответствующей стороны перестает двигаться, и голос нарушается - появляется осиплость, хрипота. Степень нарушения голосовой функции при одностороннем нарушении функции нерва может быть различной - от минимальных симптомов у одних пациентов до почти полной потери звучности голоса у других. Если же функция нервов нарушается с обеих сторон, то голос может полностью исчезнуть, но, что более важно, может появиться нарушение дыхания. В тяжелых случаях при двустороннем нарушении функции нервов может потребоваться установка трубки в трахею ("дыхательное горло") - трахеостомия, поскольку только таким образом можно обеспечить возможность дыхания.
Паралич голосовой складки после операции на щитовидной железе
Профилактика нарушения функции гортанных нервов - одна из основных задач хирурга при проведении операции. Для этого применяется ряд технологий - микроскопическая визуализация нерва с использованием бинокулярных луп, использование высокоточных электрокоагуляторов, клипирование сосудов титановыми клипсами вблизи нерва. Важнейшее значение имеет опыт хирурга - многочисленными зарубежными исследованиями показано, что минимальный риск нарушения функции гортанных нервов имеют хирурги, выполняющие не менее 100 операций на щитовидной железе в год в течение не менее 5 лет. Таким образом, создание специализированных отделений эндокринной хирургии - это не прихоть, это обязательный компонент обеспечения безопасности. В Северо-Западном центре эндокринологии и эндокринной хирургии каждый хирург выполняет от 200 до 700 операций в год. По количеству операций на щитовидной железе центр занимает 1-е место в мире, что обеспечивает высокую степень безопасности.
Исследования последних лет показали, что в значительной части случаев нарушение функции нерва может быть связано не с его повреждением (рассечением, электрокоагуляцией, перевязыванием лигатурой), а с натяжением нервного ствола во время операции. Повреждение нерва характерно для неопытных хирургов. При повреждении нерва вероятность восстановления его функции после операции близка к нулю. Опытный же врач практически никогда не повреждает нерв, поскольку четко ориентируется в его анатомии, включая возможные варианты. Вместе с тем, и у очень опытных врачей бывают случаи, когда в течение определенного времени пациент может испытывать проблемы с голосом. Чаще всего это связано с натяжением нерва во время операции. У опытного врача более 80% случаев нарушений голоса связано именно с манипуляциями рядом с нервом (смещением нерва, натяжением его). Обычно (более чем в 90% случаев) нарушение голоса, не связанное с повреждением нерва, проходит самостоятельно в течение ближайших 3х месяцев после операции. Однако, в некоторых случаях, и после операции у опытного врача голос у пациента может нарушиться навсегда.
В последние годы в области профилактики нарушений голоса после операции состоялась настоящая революция. Появилось новое поколение нейромониторов - аппаратов, позволяющих контролировать функцию голосовых складок во время операции. Нейромонитор позволяет возбуждать нерв электромагнитным полем и вызывать прохождение импульсов по нерву. Во время операции хирург имеет возможность оценивать параметры прохождения электрического сигнала по нерву и определять, где и в каком состоянии находится нерв. Появление методики интраоперационного нейромониторинга позволило резко снизить вероятность нарушения голоса при операции. Безусловно, можно с уверенностью говорить, что нейромониторинг - это лучшее, что появилось в области эндокринной хирургии в последние годы.
Методика переменного и постоянного нейромониторинга
Северо-Западный центр эндокринологии и эндокринной хирургии Клиники высоких медицинских технологий им. Н. И. Пирогова Санкт-Петербургского государственного университета располагает в настоящее время наибольшим в мире опытом использования интраоперационного нейромониторинга - более 5000 операций. В центре применяется оборудование ведущих мировых производителей - Inomed (Германия) и Medtronic (США). Применяются все виды мониторинга - постоянный и переменный мониторинг гортанных нервов, мониторинг добавочного и диафрагмального нервов.
Стоимость расходных материалов для проведения нейромониторинга не покрывается бюджетным финансированием. В связи с этим пациентам, желающим использовать при операции данную технологию, необходимо оплатить стоимость расходных материалов для мониторинга в размере 17000 рублей. Оплата производится в кассе отделения эндокринной хирургии при поступлении в клинику. Вложения в нейромониторинг с уверенностью можно считать оправданными, поскольку эти вложения обеспечивают безопасность.
- Домашняя
- Инновации
- Интраоперационный нейромониторинг
Интраоперационный нейромониторинг
ИННОВАЦИЯ В ХИРУРГИИ - НЕЙРОМОНИТОРИНГ ИНТРАОПЕРАЦИОННЫЙ
В настоящее время интраоперационный нейромониторинг (ИОНМ) при операциях на щитовидной и паращитовидной железе достаточно широко используется в дополнение к традиционной визуальной идентификации нерва

NIM-Response® 3.0
NIM® ЭМГ эндотрахеальная трубка
APS® электроды
Зачем нужен нейромониторинг?
Данные клинических исследований
Повреждение возвратного гортанного нерва (ВГН) является самым серьезным осложнением операций на щитовидной железе, при этом частота повреждения ВГН при таких вмешательствах недооценивается.2-7 По данным клинических исследований интраоперационный нейромониторинг (ИОНМ) позволяет сохранить целостность нерва и снизить риск осложнений при диссекции тканей шеи, в том числе при операциях на щитовидной железе.1-5,8-15
ИОНМ позволяет защитить не только ВГН, но и другие нервы, повреждение
которых возможно во время операции. Благодаря последним разработкам, системы нейромониторинга обладают высокой чувствительностью и заранее предупреждают о приближении к нерву, постоянно контролируют состояние блуждающего нерва и дают информацию в режиме реального времени.
АНАТОМИЧЕСКИЕ ВАРИАНТЫ ВГН
Согласно данным исследований, анатомическая вариабельность расположения нерва во многом определяет риск его повреждения. Описано более 25 анатомических вариантов ВГН, и потому в некоторых случаях визуальное определение нерва может оказаться трудным, даже для опытных хирургов. Вариант расположения нерва нельзя определить до операции. К тому же, факт визуального определения нерва еще не гарантирует отсутствия паралича в послеоперационном периоде.
Примерно у 70% пациентов имеется экстраларингеальная бифуркация ВГН, и риск поражения ветвей нерва в этом случае выше. У 1% пациентов имеется невозвратный гортанный нерв. ИОНМ помогает выявить бифуркацию ВГН и подтвердить локализацию двигательного компонента.3,4 ИОНМ также указывает на наличие невозвратного ГН.

Мониторинг ВГН при тиреоидектомии имеет следующие задачи
- определение локализации нерва;
- упрощение диссекции нерва;
- прогноз функции нерва в послеоперационном периоде.
БЛУЖДАЮЩИЙ НЕРВ И ВЕРХНИЙ ГОРТАННЫЙ НЕРВ
Стимуляция блуждающего нерва дает исходную информацию для оценки целостности нерва и последующего мониторинга, а также позволяет оценить правильность размещения ЭМГ-трубки.1,10,14 Наружная ветвь верхнего гортанного нерва пересекает верхние щитовидные артерии, в связи с чем существует опасность повреждения нерва при диссекции и наложении зажима, особенно при выраженной гипертрофии щитовидной железы. ИОНМ можно использовать для стимуляции верхнего гортанного нерва во время операций на щитовидной железе.
Ценный вспомогательный метод
ИОНМ не подменяет знания анатомии и топографии оперируемой области или хирургических навыков, однако как вспомогательное средство предоставляет следующие возможности:
Прямой и постоянный мониторинг помогают уменьшить риск осложнений операции и в целом улучшить исходы лечения.
THE NIM-RESPONSE® 3.0

Система NIM-Response® 3.0 создана с учетом 20-летнего опыта разработок в области нейромониторинга.
Применение системы NIM-Response® 3.0 позволяет предотвратить тяжелые осложнения после операции и способствует улучшению исходов лечения.
Особенности системы NIM 3.0
- Звуковые и визуальные сигналы о состоянии нерва
- Дружественный интерфейс и сенсорный экран
- Возможность мониторинга при биполярной коагуляции
- Специальное программное обеспечение для устранения артефактов
- Простота и удобство документации ЭМГ-активности
- Цветная маркировка электродов
- Удобная проверка рабочего состояния электродов
- Постоянный мониторинг ВГН нерва в реальном времени с помощью электрода APS
Мониторинг позволяет оценить целостность нерва во время операции.
NIM® 3.0
Уникальные особенности системы
ОДНОВРЕМЕННЫЙ МОНИТОРИНГ ПРИ БИПОЛЯРНОЙ КОАГУЛЯЦИИ
- Исключает необходимость заглушения/выключения мониторинга при биполярной коагуляции
- Высокая чувствительность мониторинга
ПРОГРАММНОЕ ОБЕСПЕЧЕНИЕ ДЛЯ ВЫЯВЛЕНИЯ АРТЕФАКТОВ
- Различает артефакты и сигналы ЭМГ
- Убирает информационный шум при операции, заглушая большинство артефактов
ПОСТОЯННЫЙ МОНИТОРИНГ С APS ЭЛЕКТРОДОМ (АПС, АВТОМАТИЧЕСКОЙ ПЕРИОДИЧЕСКОЙ СТИМУЛЯЦИЕЙ)
- Обеспечивает постоянный мониторинг ВГН нерва в реальном времени
- Позволяет немедленно выявлять изменение функции нерва
Система NIM 3.0 выявляет и гасит артефакт
(выделено желтым).

ПОСТОЯННЫЙ МОНИТОРИНГ С ПОМОЩЬЮ
APS ® электрода
APS ® электрод используется совместно с системой NIM® 3.0 и позволяет своевременно выявлять изменения состояния нерва. Электрод располагают в проекции блуждающего нерва и выполняют длительную стимуляцию на низкой мощности. Оценивают исходную функцию нерва и затем в режиме реального времени следят за изменением ответа на ЭМГ
Для чего нужен мониторинг с электродом APS ® ?
Функция
- Постоянная стимуляция блуждающего нерва на малой мощности с последовательным возбужением ВГН
- Запись ответа через ЭМГ эндотрахеальную трубку
- Отображение амплитуды и задержки ответа в реальном времени
- Возможность настройки предупреждающих сигналов для значимых изменений функции нерва
Преимущества

NIM® ЭМГ-трубки используются для интубации пациента и совместимы с системой ИОНМ. Биполярные контактные электроды из нержавеющей стали в составе ЭМГ-трубок позволяют контролировать состояние нервов в голосовых связках с обеих сторон, что снижает риск их повреждения.При использовании с системой NIM 3.0 ЭМГ-трубка позволяет визуализировать электроды, контактирующие с голосовыми связками и задней группой мышц. При изменении функции нерва система NIM 3.0 выдает звуковой и визуальный предупреждающие сигналы.Для совместного применения с системой NIM 3.0 используются только NIM ЭМГ-трубки.
Процедуры с применением NIM ® ЭМГ-трубок
ТИРЕОИДЕКТОМИЯ
ГЕМИТИРЕОИДЕКТОМИЯ
ПАРАТИРЕОИДЕКТОМИЯ
ДИССЕКЦИЯ ТКАНЕЙ ШЕИ
КРИКОФАРИНГЕАЛЬНАЯ МИОТОМИЯ
ЧАСТИЧНАЯ ЛАРИНГОТОМИЯ
НДАРТЕРЕКТОМИЯ НА СОННЫХ
АРТЕРИЯХБИОПСИЯ ТКАНЕЙ
ШЕИИССЕЧЕНИЕ ДИВЕРТИКУЛА
ЗЕНКЕРАСУБСТЕРНАЛЬНЫЙ ЗОБПЕРЕДНИЙ
ШЕЙНЫЙ СПОНДИЛОДЕ
Читайте также:


