Исследование зрительного нерва звпш

Современные исследования позволяют оценить работу нервной системы и поставить точный диагноз на основе ответа от коры головного мозга. Зрительные вызванные потенциалы – один из таких методов, дающих возможность понять, как головной мозг реагирует на различные зрительные стимулы. Важность исследования связана с тем, что объективно оценить работу органов зрения с помощью стандартного обследования может быть сложно. Не всегда понятно, какая часть зрительной системы задействована в развитии патологии.
Суть метода
Врач с помощью подачи специальных стимулов проверяет работоспособность зрения и регистрирует ответы, поступающие от коры головного мозга. На пациента надевают специальные очки, на которые подают вспышки и изображения. Или пациент сидится перед монитором, на котором видит разноцветные мигающие клетки – это называется шахматный паттерн.
Особенности исследования
Регистрация зрительных вызванных потенциалов – это классическое исследование при диагностике некоторых специфических заболеваний нервной системы. На данный момент регистрация ЗВП входит в список рекомендуемых процедур в рамках комплексной диагностики рассеянного склероза и других заболеваний, связанных с явлением демиелинизации.
Еще одно серьезное преимущество обследования – возможность оценить состояние зрения у детей (начиная с трехмесячного возраста). Благодаря тому, что процедура полностью безболезненная и не вызывает неприятных ощущений, дети легко переносят исследование. От ребенка требуется неподвижность, поэтому при обследовании новорожденных и грудных малышей требуется дождаться сна. Наибольшую эффективность метод ЗВП показывает при диагностике наследственных и врожденных аномалий, которые могут вызывать вопросы при проведении стандартного офтальмологического обследования.
- Диагностика демиелинизирующих заболеваний (в частности, рассеянного склероза).
- Диагностика врожденных аномалий зрения.
- Подозрение на болезнь зрительных нервов.
- Для оценки уровня функционального поражения зрительных нервов.
- Для дифференциации заболеваний, связанных с физическим поражением оптического аппарата от заболеваний, связанных с поражением нервного волокна.
- В рамках комплексной диагностики при опухолях мозга, невритах, нейроинфекциях.
- При атрофии зрительного нерва.
- Наличие нехарактерных для конкретного заболевания жалоб на работу органов зрения.
Как проходит процедура
Регистрация ЗВП относится к категории неинвазивных процедур. Это значит, что не потребуется проникновения в организм или повреждения кожных покровов. Поэтому беспокоиться не о чем.
Сначала специалист накладывает электроды в соответствии с выбранной схемой – обычно в районе мочек ушей и на голове. Затем начнется непосредственно исследование, в ходе которого нужно следовать инструкциям врача. Обычно пациента просят по очереди закрывать глаза с помощью специального приспособления – для каждого глаза проводится свое исследование. По окончании регистрации ЗВП врач производит с помощью специальной программы обработку полученных данных.
Для качественного лечения потребуется комплексная диагностика – поэтому ЗВП нередко сочетают с другими исследованиями вызванных потенциалов. Так, при поражении головного мозга целесообразно провести ряд других мероприятий для выяснения области и степени поражения.
Если есть возможность, после исследования необходимо получить консультацию профильного специалиста. Совместно с исследованием рекомендуются следующие диагностические офтальмологические процедуры:
- Периметрия – оценка полей зрения.
- Измерение внутриглазного давления – важно для исключения глаукомы.
- Осмотр сетчатки.
Только комплексный подход позволяет поставить правильный диагноз.

Содержание:
- 1 Современные методы исследования зрительного нерва при оптических нейропатиях различного генеза
- 1.1 Материал и методы
- 1.2 Результаты и обсуждение

Учреждение Российской академии медицинских наук НИИ глазных болезней РАМН, Москва
Оптические неглаукомные нейропатии — это группа гетерогенных заболеваний, характеризующихся острой или хронической прогрессирующей гибелью ганглиозных клеток сетчатки и их аксонов, что заканчивается утратой зрительных функций различной степени вследствие частичной или полной атрофии зрительного нерва.
Ранняя диагностика оптической нейропатии (ОН) имеет критическое значение для предотвращения или ограничения структурного повреждения зрительного нерва и необратимой потери функций глаза.
В выявлении ОН, несомненно, важное место занимают данные анамнеза, клинического осмотра и стандартного офтальмологического обследования Однако в сложных клинических ситуациях для раннего обнаружения признаков заболевания требуются современные чувствительные диагностические тесты, благодаря которым можно точно оценить функциональные и структурные нарушения зрительного нерва.
Изучение зрительных функций предполагает тщательное исследование поля зрения (ПЗ) с помощью автоматической статической периметрии, а также определение биоэлектрической активности сетчатки и зрительного нерва электрофизиологическими методами. Компьютерная статическая периметрия с применением пороговых программ исследования центрального и периферического поля зрения, выполненная на периметре Octopus 900, является, как принято считать, "золотым стандартом" для определения световой чувствительности. Исследование зрительных вызванных потенциалов (ЗВП) — объективный метод оценки повреждения зрительного пути, предоставляющий информацию о функциональном состоянии аксонов и миелиновой оболочки зрительного нерва.
Изучение структурных особенностей зрительного нерва с помощью оптической когерентной томографии (ОКТ) — относительно новая технология качественной и количественной оценки диска зрительного нерва, ретинального слоя нервных волокон.
Целью настоящей работы является комплексное изучение морфофункционального состояния зрительного нерва при ОН различного генеза.
↑ Материал и методы
Обследовано 132 пациента (188 глаз) в возрасте от 16 до 87 лет (медиана 48 лет) с установленным диагнозом ОН различного неглаукомного генеза, в том числе 23% глаз с неартериитной передней ишемической ОН, 10% с задней ишемической ОН, 22% с ОН воспалительного генеза (при демиелинизирующих заболеваниях, аутоиммунной, инфекционной, саркоидозной этиологии), 10% с компрессионной ОН при опухолях зрительного нерва, орбиты, хиазмально-селлярной области и основания передней черепной ямки, 12% с ОН при друзах диска зрительного нерва, 8% с травматической ОН, 7% с эндокринной нейроофтальмопатией, 6% с наследственной ОН Лебера, 2% с ОН токсического генеза. В 43% случаях (58 пациентов) ОН была двусторонней. Все пациенты не имели другой офтальмопатологии, влияющей на функции и структуры зрительного нерва.
Для определения специфичности морфофункциональных методов исследования зрительного нерва были обследованы 52 пациента (75 глаз) без патологии зрительного нерва.
Всем пациентам проводили традиционные офтальмологические функциональные исследования: определение максимальной остроты зрения, оценку цветового зрения по таблицам Рабкина, исследование зрачковых реакций с определением относительного афферентного зрачкового дефекта (ОАЗД), кинетическую периметрию с объектом III4e; биомикро- и офтальмоскопию.
Выполняли также углубленные функциональные исследования: компьютерную периметрию с применением статической неврологической N1-программы (периметр Octopus 900, "Interzeag AG", Швейцария), общую и мультифокальную электро-ретинографию (мф-ЭРГ), изучение ЗВП на вспышку и паттерн ("Тоmеу", ЕР-1000 Multifocal, Германия).
Исследование структуры диска зрительного нерва с определением средней толщины слоя нервных волокон сетчатки (СНВС) в перипапиллярной зоне (диаметр 3,4 мм) и отдельно в 4 квадрантах (верхний, нижний, назальный, темпоральный) выполняли с помощью ОКТ на ретинотомографе OCT Stratus 3000 ("Carl Zeiss").
Критерии определения показателей методов исследования с отклонениями от нормы
Статическая периметрия. Результаты считали анормальными при индексах периметрии MD (mean defect) — более 2 децибел и/или sLV (loss variance) — более 2,5 децибела. Все результаты статической периметрии, включенные в данное исследование, были достоверны, так как индекс RF (reliability factor), рассчитанный по ложноположительным и ложноотрицатель-ным ответам пациентов, во всех случаях был менее 15%.
ОКТ. Результаты считали анормальными, если средняя толщина СНВС или толщина СНВС в одном из квадрантов была значительно уменьшена или увеличена по сравнению с нормой, р

Атрофия зрительного нерва клинически представляет собой совокупность признаков: нарушения зрительных функций (понижение остроты зрения и развитие дефектов поля зрения) и побледнения диска зрительного нерва. Атрофия зрительного нерва характеризуется уменьшением диаметра зрительного нерва вследствие уменьшения числа аксонов.
Атрофия зрительного нерва занимает одно из ведущих мест в нозологической структуре, уступая лишь глаукоме и дегенеративной близорукости. Атрофией зрительного нерва принято считать полное или частичное разрушение его волокон с замещением их соединительной тканью.
По степени снижения зрительных функций атрофия может быть частичной или полной. Согласно данным исследований видно, что от частичной атрофии зрительного нерва страдают мужчины в 57,5%, а женщины в 42,5%. Чаще всего наблюдается двустороннее поражение (в 65% случаев).
Прогноз атрофии зрительного нерва всегда серьезный, но не безнадежный. В связи с тем, что патологические изменения обратимы, лечение частичной атрофии зрительного нерва является одним из важных направлений в офтальмологии. При адекватном и своевременном лечении этот факт позволяет добиться повышения зрительных функций даже при длительном существовании заболевания. Так же в последние годы увеличилось количество данной патологии сосудистого генеза, что связано с ростом общей сосудистой патологии - атеросклерозом, ишемической болезнью сердца.
- По этиологии
- наследственная: аутосомно-доминантная, аутосомно-рецессивная, митохондриальная;
- ненаследственная.
- По офтальмоскопической картине — первичная (простая); вторичная; глаукоматозная.
- По степени поражения (сохранности функций): начальная; частичная; неполная; полная.
- По топическому уровню поражения: нисходящая; восходящая.
- По степени прогрессирования: стационарная; прогрессирующая.
- По локализации процесса: односторонняя; двусторонняя.
Различают врожденную и приобретенную атрофию зрительного нерва. Приобретенная атрофия зрительного нерва развивается в результате повреждения волокон зрительного нерва (нисходящая атрофия) или клеток сетчатки (восходящая атрофия).
Врожденную, генетически обусловленную атрофию зрительного нерва разделяют на аутосомно-доминантную, сопровождающуюся асимметричным понижением остроты зрения от 0,8 до 0,1, и аутосомно-рецессивную, характеризующуюся noнижением остроты зрения нередко до практической слепоты уже в раннем детском возрасте.
К нисходящей приобретенной атрофии приводят процессы, повреждающие волокна зрительного нерва на различном уровне (орбита, зрительный канал, полость черепа). Природа повреждения различна: воспаление, травма, глаукома, токсическое повреждение, нарушение кровообращения в сосудах, питающих зрительный нерв, нарушение метаболизма, сдавление зрительных волокон объемным образованием в полости глазницы или в полости черепа, дегенеративный процесс, близорукость и т. д.).
Каждый этиологический фактор обусловливают атрофию зрительного нерва с определенными, типичными для нее офтальмоскопическими особенностями. Тем не менее имеются характеристики, общие для атрофии зрительного нерва любой природы: побледнение диска зрительного нерва и нарушение зрительных функций.
Этиологические факторы атрофии зрительного нерва сосудистого генеза разнообразны: это и патология сосудов, и острые сосудистые нейропатии (передняя ишемическая нейропатия, окклюзия центральной артерии и вены сетчатки и их ветвей), и следствие хронических сосудистых нейропатий (при общесоматической патологии). Атрофия зрительного нерва появляется в результате непроходимости центральной и периферических артерии сетчатки, питающих зрительный нерв.
Офтальмоскопически обнаруживается сужение сосудов сетчатки, побледнение части или всего диска зрительного нерва. Стойкое побледнение только височной половины бывает при поражении папилломакулярного пучка. Когда атрофия является следствием заболевания хиазмы или зрительных трактов, тогда имеются гемианопические типы дефектов поля зрения.
В зависимости от степени повреждения зрительных волокон, а следовательно, и от степени понижения зрительных функций и побледнения диска зрительного нерва различают начальную, или частичную, и полную атрофию зрительного нерва.
Жалобы: постепенное снижение остроты зрения (различной степени выраженности), изменение поля зрения (скотомы, концентрическое сужение, выпадение полей зрения), нарушение цветовосприятия.
Анамнез: наличие объёмных образований головного мозга, внутричерепной гипертензии, демиелинизирующего поражения ЦНС, поражения сонных артерий, системных заболеваний (в том числе васкулитов), интоксикаций (в том числе алкогольных), перенесенных неврита зрительного нерва или ишемической нейропатии, окклюзий сосудов сетчатки, прием лекарственных препаратов, обладающих нейротоксическим действием, в течение последнего года; травмы головы и шеи, сердечно-сосудистые заболевания, гипертоническая болезнь, острые и хронические нарушения мозгового кровообращения, атеросклероз, менингит или менинго-энцефалит, воспалительные и объемные процессы придаточных пазух, профузные кровотечения.
Физикальное обследование:
- наружный осмотр глазного яблока (ограничение подвижности глазного яблока, нистагм, экзофтальм, птоз верхнего века)
- исследование роговичного рефлекса – может быть снижен на стороне поражения
Лабораторные исследования
- биохимический анализ крови: холестерин крови, липопротеиды низкой плотности, липопротеиды высокой плотности, триглицериды; ·
- коагулограмма;
- ИФА на вирус простого герпеса, цитомегаловирус, токсоплазмоз, бруцеллез, туберкулез, ревмопробы (по показаниям, для исключения воспалительного процесса)
Инструментальные исследования
- визометрия: острота зрения может колебаться от 0,7 до практической слепоты. При поражении папилломакулярного пучка острота зрения значительно снижена; при незначительном поражении папилломакулярного пучка и вовлечении в процесс периферических нервных волокон ЗН острота зрения снижается незначительно; при поражении только периферических нервных волокон - не меняется. ·
- рефрактометрия: наличие аномалий рефракции позволит провести дифференциальный диагноз с амблиопией.
- тест Амслера - искажение линий, затуманивание рисунка (поражение папилломакулярного пучка). ·
- периметрия: центральная скотома (при поражении папилломакулярного пучка); различные формы сужения поля зрения (при поражении периферических волокон зрительного нерва); при поражении хиазмы - битемпоральную гемианопсию, при поражении зрительных трактов - гомонимная гемианопсия. При поражении интракраниальной части зрительного нерва гемианопсия возникает на одном глазу.
- Кинетическая периметрия на цвета – сужение поля зрения на зелёный и красный цвет, реже – на желтый и синий.
- Компьютерная периметрия - определение качества и количества скотом в поле зрения, в том числе и в 30 градусах от точки фиксации.
- исследование адаптации к темноте: нарушение темновой адаптации. · исследование цветового зрения: (таблицы Рабкина) - нарушение цветовосприятия (повышение цветовых порогов), чаще зелёно-красной части спектра, реже - жёлто-синей.
- тонометрия: возможно повышение ВГД (при глаукоматозной атрофии зрительного нерва).
- биомикроскопия: на стороне поражения - афферентный зрачковый дефект: снижение прямой зрачковой реакции на свет с сохранением содружественной реакции зрачка.
- офтальмоскопия:
- начальная атрофия ЗН – на фоне розовой окраски ДЗН появляется побледнение, которое в дальнейшем становится более интенсивным.
- частичная атрофия ЗН – побледнение височной половины ЗН, симптом Кестенбаума (уменьшение количества капилляров на ДЗН от 7 и меньше), артерии сужены,
- неполная атрофия ЗН – равномерное побледнение зрительного нерва, умеренно выражен симптом Кестенбаума (уменьшение количества капилляров на ДЗН), артерии сужены,
- полная атрофия ЗН – тотальное побледнение ЗН, сосуды сужены (артерии сужены больше, чем вены). Резко выражен симптом Кестенбаума (уменьшение количества капилляров на ДЗН – до 2-3 или капилляры могут отсутствовать).
При первичной атрофии ЗН границы ДЗН четкие, цвет его белый, серовато-белый, голубоватый или слегка зеленоватый. В бескрасном свете контуры остаются четкими, тогда как контуры ДЗН в норме становятся нечеткими. В красном свете при атрофии ДЗН - синего цвета. При вторичной атрофии ЗН границы ДЗН нечеткие, размытые, ДЗН серый или грязно-серый, сосудистая воронка заполнена соединительной или глиальной тканью (в отдаленный период границы ДЗН становятся четкими).
- оптическая когерентная томография ДЗН (по четырем сегментам – височному, верхнему, носовому и нижнему): снижение площади и объема нейроретинального пояска ДЗН, уменьшение толщины слоя нервных волокон диска зрительного нерва и в макуле.
- гейдельбергская ретинальная лазерная томография – уменьшение глубины головки зрительного нерва, площади и объема нейроретинального пояска, увеличение площади экскавации. При частичной атрофии зрительного нерва - диапазон глубины головки ЗН менее 0,52 мм, площадь ободка - менее 1,28 мм 2 , площадь экскавации - более 0,16 мм 2 .
- флюоресцентная ангиография глазного дна: гипофлюоресценция диска зрительного нерва, сужение артерий, отсутствие или уменьшение числа капилляров на ДЗН;
- электрофизиологические исследования (зрительные вызванные потенциалы) - снижение амплитуды ЗПВ и удлинение латентности. При поражении папилломакулярного и аксиального пучка ЗН электрическая чувствительность нормальная, при нарушении периферических волокон порог электрического фосфена резко повышен. Лабильность особенно резко снижается при аксиальных поражениях. В период прогрессирования атрофического процесса в ЗН существенно увеличивается ретино-кортикальное и кортикальное время;
- УЗДГ сосудов головы, шеи, глаза: снижение кровотока в глазничной, надблоковой артерии и интракраниальной части внутренней сонной артерии;
- МРТ сосудов головного мозга: очаги демиелинизации, интракраниальная патология (опухоли, абсцессы, кисты головного мозга, гематомы);
- МРТ орбиты: сдавление орбитальной части ЗН;
- Рентгенография орбиты по Ризе – нарушение целостности зрительного нерва.
Степень понижения остроты зрения и характер дефектов поля зрения определяются характером процесса, вызвавшего атрофию. Острота зрения может колебаться от 0,7 до практической слепоты.
Атрофия зрительного нерва при табесе развивается на обоих глазах, но степень поражения каждого глаза может быть далеко не одинаковой. Острота зрения падает постепенно, но т.к. процесс при табесе всегда прогрессирующий, то в конечном итоге наступает в разные сроки (от 2-3 недель до 2-3 лет) двусторонняя слепота. Наиболее частой формой изменения поля зрения при табетической атрофии является постепенно прогрессирующее сужение границ при отсутствии скотом в пределах сохранившихся участков. Редко при табесе наблюдаются битемпоральные скотомы, битемпоральное сужение границ поля зрения, а также центральные скотомы. Прогноз при табетической атрофии зрительного нерва всегда плохой.
Атрофия зрительного нерва может наблюдаться при деформациях и заболеваниях костей черепа. Такая атрофия наблюдается при башнеобразном черепе. Понижение зрения обычно развивается в раннем детском возрасте и редко после 7 лет. Слепота обоих глаз наблюдается редко, иногда наблюдается слепота одного глаза с резким понижением зрения на другом глазу. Со стороны поля зрения отмечается значительное сужение границ поля зрения по всем меридианам, скотом не бывает. Атрофию зрительного нерва при башнеобразном черепе большинство считают последствием застойных сосков, развивающихся на почве повышения внутричерепного давления. Из других деформаций черепа атрофию зрительных нервов вызывает dysostosis craniofacialis (болезнь Крузона, синдром Аперта, мраморная болезнь и др.).
Атрофия зрительного нерва может быть при отравлении хинином, плазмоцидом, папоротником при изгнании глистов, свинцом, сероуглеродом, при ботулизме, при отравлении метиловым спиртом. Метилалкогольная атрофия зрительного нерва встречается не так редко. После употребления метилового спирта через несколько часов появляется паралич аккомодации и расширение зрачков, возникает центральная скотома, резко снижается зрение. Затем зрение частично восстанавливается, но постепенно нарастает атрофия зрительного нерва и наступает необратимая слепота.
Атрофия зрительного нерва может быть врожденная и наследственная, при родовых или послеродовых повреждениях головы, длительной гипоксии и т.д.
Лечение атрофий зрительного нерва - очень сложная задача. Кроме патогенетической терапии применяется тканевая терапия, витаминотерапия, спинномозговая пункция в сочетании с осмотерапией, сосудорасширяющие средства, витаминами группы В, особенно В1 и В12. В настоящее время широко применяют магнито-, лазер- и электростимуляцию.
В лечении частичной атрофии зрительного нерва, как правило, используется фармакотерапия. Применение лекарственных препаратов дает возможность воздействовать на различные звенья патогенеза атрофии зрительного нерва. Но не стоит забывать о методах физиовоздействия и различных путях введения лекарственных средств. Вопрос об оптимизации путей введения лекарственных препаратов так же актуален в последние годы. Так, парентеральное (внутривенное) введение сосудорасширяющих препаратов может способствовать системному расширению сосудов, что, в некоторых случаях, может приводить к синдрому обкрадывания и ухудшать кровообращение в глазном яблоке. Общепризнанным считается факт большего терапевтического эффекта при местном применении препаратов. Однако при заболеваниях зрительного нерва местное применение лекарств сопряжено с определенными трудностями, вызванными существованием ряда тканевых барьеров. Создание терапевтической концентрации лекарственного препарата в патологическом очаге достигается более успешно при сочетании медикаментозной терапии и физиовоздействий.
Медикаментозное лечение (в зависимости от степени тяжести заболевания)
Консервативное (нейропротекторное) лечение направлено на усиление кровообращения и улучшение трофики зрительного нерва, стимулирование жизнедеятельных сохранившихся и/или находящихся в стадии апоптоза нервных волокон.
Медикаментозное лечение включает нейропротекторные препараты прямого (непосредственно защищают ретинальные ганглии и аксоны) и непрямого (снижают действие факторов, вызывающих гибель нервных клеток) действия.
- Ретинопротекторы: аскорбиновая кислота 5% 2 мл внутримышечно один раз в день 10 дней, с целью снижения проницаемости стенки сосудов и стабилизации мембран эндотелиоцитов
- Антиоксиданты: токоферола 100 МЕ 3 раза в сутки – 10 дней, с целью улучшения снабжения тканей кислородом, коллатерального кровообращения, укрепления сосудистой стенки
- Препараты, улучшающие обменные процессы (прямые нейропротекторы): ретиналамин для внутримышечного по 1,0 мл и/или парабульбарного введения 5 мг по 0,5 мл парабульбарно 1 раз в сутки 10 дней
- Перечень дополнительных лекарственных средств:
- винпоцетин – взрослым по 5-10 мг 3 раза в сутки в течение 2 месяцев. Оказывает сосудорасширяющее, антигипоксическое и антиагрегантное действие
- цианокобаламин 1 мл внутримышечно 1 раз в сутки 5/10 дней
Тауже применяют электростимуляцию – она направлена на восстановление функции нервных элементов, которые были работоспособны, но не проводили зрительную информацию; формирование очага стойкой возбудимости, что приводит к восстановлению активности нервных клеток и их связей, ранее слабо функционировавших; улучшение метаболических процессов и кровообращения, что способствует восстановлению миелиновой оболочки вокруг осевых цилиндров волокон ЗН и, соответственно, ведет к ускорению проведения потенциала действия и возрождению анализа зрительной информации.
Показания для консультации узких специалистов:
- консультация терапевта – для оценки общего состояния организма;
- консультация кардиолога – высокий уровень артериального давления - один из главных факторов риска развития окклюзий сосудов сетчатки и зрительного нерва;
- консультация невролога - для исключения демиелинизирующего заболевании ЦНС и уточнения топической зоны поражения зрительных путей;
- консультация нейрохирурга - при появлении у больного признаков внутричерепной гипертензии или симптомов, характерных для объёмного образования головного мозга;
- консультация ревматолога - при наличии симптомов, характерных для системных васкулитов;
- консультация сосудистого хирурга для решения вопроса о необходимости хирургического лечения при наличии признаков окклюзирующего процесса в системе внутренней сонной и глазничной артерии (появление у больного scotoma fugax);
- консультация эндокринолога – при наличии сахарного диабета/другой патологии эндокринной системы;
- консультация гематолога (при подозрении на заболевания крови);
- консультация инфекциониста (при подозрении на васкулит вирусной этиологии).
- консультация отоларинголога – при подозрении на воспаление или новообразование в гайморовой или лобной пазухе.
Индикаторы эффективности лечения:
- повышение электрической чувствительности зрительного нерва на 2-5% (по данным компьютерной периметрии),
- повышение амплитуды и/или снижение латентности на 5% (по данным ЗВП).
Зрительные вызванные потенциалы (ЗВП) регистрируются с затылочной области волосистой части головы. Они отражают процессы деполяризации в слое 4с стриарной коры (зона VI), вызываемые ретиногеникулярными афферентными импульсами. ЗВП являются проявлением активности, главным образом, центральной 5° зоны сетчатки, преимущественно нижней части поля зрения, и ПЗВП у детей можно использовать в качестве показателя функции макулярных проводящих путей. При аномальных ПЗВП необходимо при помощи ПЭРГ, мфЭРГ и/или получения изображения глазного дна исключить первичную макулярную дисфункцию.
При наличии диагностированной макулопатии или дегенеративной формы паттерна ПЭРГ/мфЭРГ, формы волн ПЗВП тем не менее могут быть информативными при оценке резидуальных функций макулярной и парамакулярной зон сетчатки. Перед монокулярным исследованием мы регистрируем ПЗВП при стимуляции с обоими открытыми глазами. Мы используем трансокципитальную схему установки электродов, широкопольную (30°) стимуляцию и, по возможности, стимуляцию половины поля зрения, что позволяет дифференцировать патологию зрительного нерва, хиазмы и полушарий.
а) Применение различных типов стимуляции: паттерн-реверсивная, паттерн-onset и стимуляция вспышкой. При паттерн-реверсивной стимуляции ЗВП имеют форму простой трехфазной волны, сохраняющейся в течение всей жизни и достигающей пикового положительного значения около 100 мс к возрасту семи месяцев, этот пик называется p100 (компоненты называются в зависимости от их полярности: р — положительные, п — отрицательные; цифрами обозначается латентность (интервал) от стимула до пика). Форма паттерн-реверсивного ЗВП при стимуляции всего поля зрения может становиться двугорбой (р-n-р),если центральная скотома уменьшает вклад макулярной области, как это наблюдается, например, при доминантной атрофии зрительного нерва. Двугорбая форма сигнала вызывается увеличением участия парамакулярных структур n105 и p135.
Стимуляции половины поля зрения помогает разделить макулярные и парамакулярные пики. Мы используем стимулы с клетками различных размеров, от 400' до 6,25', предъявляемые с частотой 3/с в возрасте старше шести недель.
Паттерн-onset стимуляция требует концентрации внимания, устойчива к движениям глаз, что позволяет применять этот метод при нистагме и с целью компенсации активного дефокуса. Сигнал имеет сложную форму, три компонента волны имеют пространственно разные источники: CI, положительный, примерно на 90 мс; СII, отрицательный, приблизительно на 110 мс; и СIII, резко положительный, примерно на 180-200 мс. Разные пики появляются в разном возрасте: первый положительный CI наиболее выражен в детстве и зависит от контрастности и освещенности. СII возникает в старшем детском возрасте и в большей степени зависит от контура. Эти изменения затрудняют использование паттерн-onset ЗВП для лонгитудинального мониторинга.
Стимуляция вспышкой — надежный метод, который может быть информативным и при закрытых веках. Одновременно записывается контрольная ЭРГ, тогда как ЗВП позволяют контролировать уровень стимуляции сетчатки. Мы применяем и паттерн-стимуляцию, и стимуляцию вспышкой, часто также и стимуляцию реверсивным паттерном и onset-стимуляцию, чтобы получить перекрывающие и дополняющие друг друга данные о функциональном состоянии зрительного пути, особенно о трансокципитальной асимметрии.
При записи ЗВП со стимуляцией вспышкой и реверсивным паттерном отмечается парадоксальная локализация. Например, при стимуляции левого полушария через правые половины поля зрения ответ регистрируется правым затылочным электродом. Это происходит вследствие расположения активированной области коры и вызвано широкопольной стимуляцией и расположением референтного электрода в среднефронтальной области. При регистрации паттерн-onset ЗВП таких феноменов не отмечается. При стимуляции правой половины поля зрения ответ регистрируется над левой затылочной долей, что соответствует анатомическому строению.
Сравнение трансокципитальных асимметрий ЗВП при паттерн-onset и паттерн-реверсивной стимуляции всего поля зрения иногда может оказаться информативным для выявления патологической природы трансокципитальной асимметрии ЗВП, особенно у детей с плоским или асимметричным черепом, у которых не удается выполнить стимуляцию половины поля зрения.
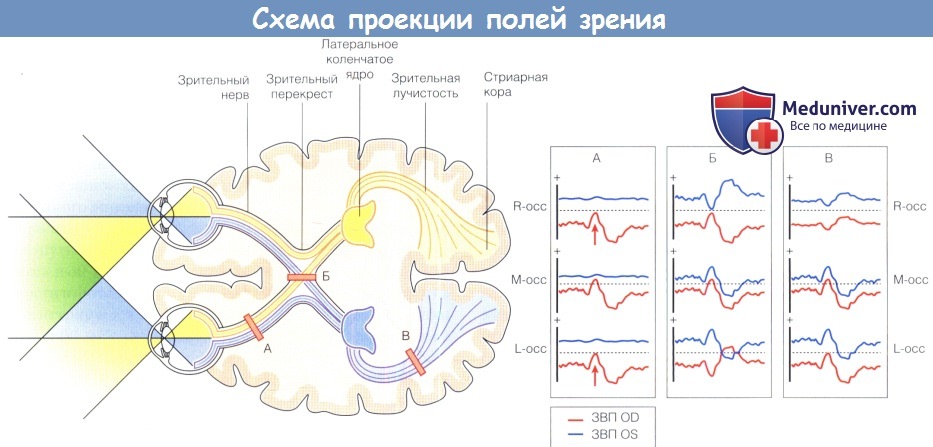
Схема проекции правой (обозначена синим) и левой (обозначена желтым) половин поля зрения обоих глаз (OD - правый глаз; OS — левый глаз).
Красными полосками, пересекающими проводящие пути, обозначены повреждения левого зрительного нерва (А), хиазмы (Б) и левой зрительной лучистости и затылочной коры (В).
Форма сигналов ЗВП, регистрируемых при этих повреждениях, при стимуляции правого глаза (красным) и левого глаза (синим) схематически показана напротив электродов правого (R-occ),
левого (L-occ) боковых и среднего (М-осс) затылочного каналов.
В столбце А показано снижение амплитуды ЗВП OS и симметричное распределение ЗВП OD при равенстве амплитуды сигналов боковых каналов (показана стрелками).
В столбце Б показана перекрестная асимметрия, трансокципитальное распределение сигнала при стимуляции одного глаза является зеркальным отражением сигнала, регистрируемого при стимуляции парного глаза,
т.е. ЗВП OD негативны (отклоняются книзу) на левом затылочном канале, тогда как ЗВП OS негативны на правом затылочном канале.
Это указывает на патологию хиазмы. В столбце В показано одинаковое для обоих глаз гомонимное распределение сигнала, который ослаблен на правом затылочном канале.
Такое гомонимное распределение или неперекрестная асимметрия указывает на патологию полушария.
Из-за парадоксальной латерализации такое распределение ЗВП при стимуляции вспышкой или реверсивным паттерном означает дисфункцию представительства правой половины поля зрения в левом полушарии.
б) Острота зрения и ЗВП. Очень привлекательной кажется идея найти простое числовое соотношение между ПЗВП и остротой зрения; к сожалению, дело обстоит не так просто. У здоровых детей можно оценивать остроту зрения по амплитуде ПЗВП, вызванными стимуляцией паттернами с постепенно уменьшающимся размерами элементов. При этом пороговая острота зрения определяется по наименьшему размеру элемента паттерна, вызывающего ЗВП выше уровня шума, или при экстраполяции точки нулевой амплитуды на графике амплитуда/пространственная частота. Хотя и существует некоторая корреляция между ПЗВП и определяемой поведенческими методами остротой зрения, не нужно искать прямой зависимости этих показателей у пациентов. Например, при атрофии зрительного нерва, сопровождающейся гибелью нейронов, ПЗВП будут значительно ослаблены или иметь дегенеративную форму, но, поскольку рецептивные поля немногих сохранившихся нейронов тесно расположены в центральной зоне поля зрения, разрешающая способность может оказаться неожиданно высокой, даже при выраженной бледности диска зрительного нерва.
В первые 12-18 месяцев жизни результаты оценки остроты зрения при помощи ЗВП превышают результаты визометрии поведенческими методами; в более старшем возрасте результаты поведенческих тестов превышают результаты определения остроты зрения при помощи ЗВП. Функция остроты зрения как интерпретации статических высококонтрастных изображений реализуется в высших ассоциативных зонах. При регистрации ЗВП не нужно удивляться разбросу показателей активности стриарной коры. Тем не менее, ПЗВП является информативным показателем функции макулярных проводящих путей и позволяют оценить качество зрения, которое в состоянии обеспечить ретиногеникулярные пути. Мы считаем, что реверсивные паттерн-ЗВП с размером клеток в 50' или мельче указывают на хороший уровень зрительных функций, с 100'-200' — средний, и 400' — на низкие зрительные функции.
Регистрация вспышечных ЗВП при отсутствии ПЗВП указывает на рудиментарные зрительные функции. ПЗВП характеризуются высокой повторяемостью результатов, они являются надежным методом длительного наблюдения и особенно информативны при сравнении функций двух глаз у младенцев.
При увеличении частоты стимуляции возникают индивидуальные транзиторные ПЗВП-сигналы, принимающие синусоидальную форму. Этот устойчивый ответ используется в методике ЗВП с циклически меняющимся масштабом паттерна (sweep VEP), когда пациенту предъявляются быстро меняющиеся паттерны с разными по размеру и контрастности элементами. Параметры амплитуды и фазы устойчивого ЗВП анализируются методом Фурье. Во время регистрации сигнала перед предъявлением более мелких паттернов имеется возможность определить пороги соотношения сигнал/шум — пошаговая визометрия с помощью ЗВП. Методика циклически меняющегося масштаба паттерна (sweep) позволяет быстро получить числовое значение (обычно в цикл/град.), соответствующее остроте зрения или контрастной чувствительности, но при этой методике теряется информация о форме сигнала и, часто, о трансокципитальном соотношении.
Скорость стимуляции сетчатки быстро сменяющимися паттернами превышает оптимальную для определения максимальной остроты зрения. Поскольку форма сигнала ЗВП является важным диагностическим показателем, в повседневной клинической практике мы предпочитаем выполнять ПЗВП.
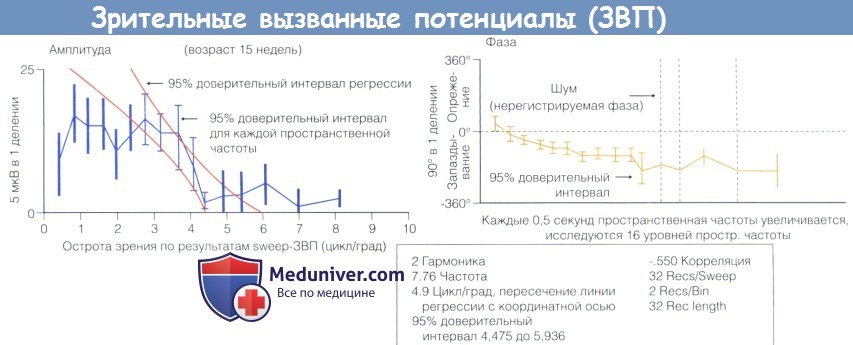
Зрительные вызванные потенциалы (ЗВП) с циклически меняющимся масштабом паттерна (sweep VEP).
Для получения квазисинусоидального ЗВП и анализа его частоты и фазы применяются стимуляции с высокой частотой смены стимулов.
На рисунке представлен диапазон пространственных частот. При увеличении пространственной частоты отмечается тенденция снижения амплитуды ЗВП.
Рассчитывается регрессия до базового уровня или до уровня шума, на основании этих расчетов оценивается острота зрения, в данном случае 4,9 цикл/град.
в) Технические факторы. Зрительные стимулы включают в себя транзиторные вспышки различной интенсивности, длительности, временной частоты, цветов, паттернов, и мультифокальные мозаики.
Зрительные стимуляторы:
1. Вспышка. Доступные на рынке стимуляторы-вспышки представлены ручными стробами, удобными при обследовании детей. Их можно перемещать при обследовании беспокойного ребенка, такие устройства позволяют напрямую контролировать положение глаз пациента. Ганцфельд-стимуляторы равномерно рассеивают свет по всей сетчатке, они сконструированы в виде стационарных аппаратов, представляющих собою полусферу с упором для подбородка, или небольших ручных LED осветителей, которые удерживаются вблизи глаза. Важной особенностью является наличие камеры для контроля раскрытия глаз и правильности стимуляции.
2. Паттерны. Стимулирующие паттерны генерируются компьютером и предъявляются с помощью электронно-лучевой трубки (ЭЛТ, cathode ray tube — CRT), в настоящее время больше не выпускаемых промышленностью, жидкокристаллического монитора (liquid crystal diode — LCD), плазменных панелей (plasma display panels — PDP) или проекционных систем. При применении CRT стимулы синхронизированы с растровой частотой генерации изображения. При частоте в 50 Гц наблюдается задержка в 20 мс между ПЗВП, записанными при взгляде в верхний левый и в нижний правый угол экрана. LCD экраны характеризуются возникновением в паттерне яркостных артефактов типа вспышки вследствие различного времени возникновения и исчезновения изображения. PDP лишены этих недостатков. Мы применяем широкопольные PDP, они имеют то преимущество, что генерация паттерна происходит почти одновременно на всей поверхности экрана, и при этом не возникает яркостных артефактов.
Функция мультисинхронности позволяет во время исследования быстро переключаться между стимулом и DVD с мультфильмом для удержания внимания пациента, саундтрек мультфильма во время предъявления паттерна не прерывается.
3. Размер поля. Большое значение в детской практике имеет широкопольная стимуляция (около 30°), при этой методике допустимо некоторое изменение направления взора, так как центральная 10° макулярная зона все равно получает адекватную стимуляцию. При стимуляции более узкого участка поля зрения из-за смещения направления взгляда чаще ошибочно регистрируется трансокципитальная асимметрия.
4. Размер клеток. При предъявлении паттерна рассеивание света предотвращается предъявлением одинакового количества черно-белых элементов (обычно клеток, реже — решеток), которые или меняют цвет в противофазу (с белого на черный и наоборот) или возникают на равномерно сером фоне с одинаковой средней освещенностью (onset-паттерн). Для обеспечения преемственности, определения базового уровня в широких пределах с целью наблюдения, и сравнения показателей парных глаз требуются паттерны с различными размерами клеток. Диагональный размер одной клетки является эквивалентом цикла на градус.
Электроды для ЭРГ. Для обследования детей требуется набор электродов — контактных линз различного размера, но в Соединенном королевстве и в Европе они не используются из-за опасения переноса инфекции. Более предпочтительны одноразовые роговичные электроды, напр. DTL, электрод из золотой фольги и электрод НК loop, у маленьких детей часто используются электроды, накладываемые на кожу нижней периорбитальной области. Амплитуда ЭРГ, записанной с накожного электрода, составляет 12-15% амплитуды ЭРГ, при регистрации которой использовался роговичный электрод, но даже такой сигнал превышает 10 мкВ, и этого достаточно для исследования (тогда как амплитуда сигнала мфЭРГ при записи с роговичного электрода измеряется в нановольтах, амплитуда ПЭРГ не превышает 2-5 мкВ, ЗВП взрослых
Читайте также:


