Медиаторы нервно мышечной передачи
Взаимодействие человека с внешней средой не возможно представить без его мышечной системы. Мышцы и иннервирующие их мотонейроны составляют нервно-мышечный аппарат человека.
Основным морфо-функциональным элементом нервно-мышечного аппарата является двигательная единица (ДЕ). ДЕ — это мотонейрон с иннервируемыми им мышечными волокнами. Аксон мотонейрона из спинного мозга проходит в составе периферических нервов до мышцы, внутри которой разветвляется на множество концевых веточек. Каждая концевая веточка заканчивается на одном мышечном волокне, образуя нервно-мышечный синапс. Импульсы, идущие по аксону мотонейрона, активируют все иннервируемые им мышечные волокна. Поэтому ДЕ функционирует как единое морфофункциональное образование.
Нервно-мышечные синапсы обеспечивают проведение возбуждения с нервного волокна на мышечное благодаря медиатору ацетилхолину, который при возбуждении нервного окончания переходит в синаптическую щель и действует на концевую пластинку мышечного волокна. Следовательно, как и межнейронный синапс, нервно-мышечный синапс имеет пресинаптическую часть, принадлежащую нервному окончанию, синаптическую щель, постсинаптическую часть (концевая пластинка), принадлежащую мышечному волокну.
В пресинаптической терминали образуется и скапливается в виде пузырьков ацетилхолин. При возбуждении электрическим импульсом, идущим по аксону, пресинаптической части синапса ее мембрана становится проницаемой для ацетилхолина.
Эта проницаемость возможна благодаря тому, что в результате деполяризации пресинаптической мембраны открываются ее кальциевые каналы. Ион Са2+ входит в пресинаптическую часть синапса из синаптической щели. Ацетилхолин высвобождается и проникает в синаптическую щель. Здесь он взаимодействует со своими рецепторами постсинаптической мембраны, принадлежащей мышечному волокну. Рецепторы, возбуждаясь, открывают белковый канал, встроенный в липидный слой мембраны. Через открытый канал внутрь мышечной клетки проникают ионы Na+, что приводит к деполяризации мембраны мышечной клетки, в результате развивается так называемый потенциал концевой пластинки (ПКП). Он вызывает генерацию потенциала действия мышечного волокна.
Нервно-мышечный синапс передает возбуждение в одном направлении: от нервного окончания к постсинаптической мембране мышечного волокна, что обусловлено наличием химического звена в механизме нервно-мышечной передачи.
Скорость проведения возбуждения через синапс намного меньше, чем по нервному волокну, так как здесь тратится время на активацию пресинаптической мембраны, переход через нее кальция, выделение ацетилхолина в синаптическую щель, деполяризацию постсинаптической мембраны, развитие ПКП.
Синаптическая передача возбуждения имеет рад свойств:
1) наличие медиатора в пресинаптической части синапса;
2) относительная медиаторная специфичность синапса, т. е. каждый синапс имеет свой доминирующий медиатор;
3) переход постсинаптической мембраны под влиянием медиаторов в состояние де- или гиперполяризации
4) возможность действия специфических блокирующих агентов на рецептирующие структуры постсинаптической мембраны;
5) увеличение длительности постсинаптического потенциала мембраны при подавлении действия ферментов, разрушающих синаптической медиатор;
6) развитие в постсинаптической мембране ПСП из миниатюрных потенциалов, обусловленных квантами медиатора;
7) зависимость длительности активной фазы действия медиатора в синапсе от свойств медиатора;
8) односторонность проведения возбуждения;
9) наличие хемочувствительных рецепторуправляемых каналов постсинаптической мембраны;
10) увеличение выделения квантов медиатора в синаптическую щель пропорционально частоте приходящих по аксону импульсов;
12) утомляемость синапса, развивающаяся в результате длительного высокочастотного его стимулирования. В этом случае утомление может быть обусловлено истощением и несвоевременным синтезом медиатора в пресинаптической части синапса или глубокой, стойкой деполяризацией постсинаптической мембраны (пессимальное торможение).
Перечисленные свойства относятся к химическим синапсам. Электрические синапсы имеют некоторые особенности, а именно: малую задержку проведения возбуждения; возникновение деполяризации как в пре-, так и в постсинаптической частях синапса; наличие большей площади синаптической щели в электрическом синапсе, чем в химическом.
Синаптические медиаторы являются веществами, которые имеют специфические инактиваторы. Например, ацетилхолин инактивируется ацетилхолинэстеразой, норадреналин — моноаминоксидазой, катехолометилтрансферазой.
Ряд химических веществ крови и постсинаптической мембраны изменяет состояние синапса, делает его неактивным. Так, простагландины тормозят секрецию медиатора в синапсе. Другие вещества, называемые блокаторами хеморецепторных каналов, прекращают передачу в синапсах. Например, ботулинический токсин, марганец блокируют секрецию медиатора в нервно-мышечном синапсе, в тормозящих синапсах ЦНС. Тубокурарин, атропин, стрихнин, пенициллин, пикротоксин и др. блокируют рецепторы в синапсе, в результате чего медиатор, попав в синаптическую щель, не находит своего рецептора.
Нейромедиа́торы — биологически активные химические вещества, посредством которых осуществляется передача электрического импульса от нервной клетки через синаптическое пространство между нейронами, а также, например, от нейронов к мышечной ткани.
· ГАМК — важнейший тормозной нейромедиатор центральной нервной системы человека
· Глутаминовая кислота — возбуждающий нейротрансмиттер в нервной системе позвоночных, в нейронах мозжечка и спинного мозга
· Аспарагиновая кислота — возбуждающий нейромедиатор в нейронах коры головного мозга.
· Адреналин — относят к возбуждающим нейромедиаторам
- Другие моноамины:
· Ацетилхолин — осуществляет нервно-мышечную передачу, а также основной нейромедиатор в парасимпатической нервной системе.
· Таурин — играет роль нейромедиаторной аминокислоты, тормозящей синаптическую передачу, обладает противосудорожной активностью, оказывает также кардиотропное действие.
· Триптамин — предполагается, что триптамин играет роль нейромедиатора и нейротрансмитера в головном мозге млекопитающих.
МЕДИАТОРЫ нервной системы (лат. mediator посредник; син.: нейротрансмиттеры, синаптические передатчики) — химические передатчики нервного импульса с нервного окончания на клетки периферических органов или на нервные клетки. Чаще всего в роли Медтаторов выступают низкомолекулярные (150—300 дальтон) вещества, выполняющие в организме человека и животных и другие функции. К Медиаторам относят ацетилхолин (см.), различные катехоламины (см.), в частности норадреналин (см.), некоторые аминокислоты (см.), пептиды (см.) и другие биологически активные вещества. Исследования Медиаторов дали важные практические результаты для клиники. Оказалось, что при ряде заболеваний нервной системы, некоторых видах отравлений нарушаются образование М., механизм их действия и распада. Знание особенностей хим. превращений М. в норме и при патологии позволило рекомендовать и ввести новые методы медикаментозного лечения.
Гипотеза о существовании веществ—посредников нервных влияний возникла в начале 20 в. Первоначально она основывалась на опыте фармакологии (имитация симпатических нервных влияний одними экзогенными веществами, а парасимпатических — другими) и относилась только к периферическим нейроэффекторным соединениям. Эллиотт (Th. R. Elliott, 1904) назвал адреналин веществом, к-рое могло бы опосредовать действие симпатических нервов на эффекторные органы. Экспериментально существование ОД. вегетативных нервов доказал в 1921 г. австр. фармаколог О. Леви, установивший, что перфузат сердца после раздражения блуждающего нерва способен оказывать вагоподобное действие. На этом основании М. первоначально называли гуморальными факторами нервного возбуждения. Впоследствии от этого названия отказались, т. к. стало ясно, что попадание М. в кровь — побочное и необязательное следствие процесса синаптической передачи.
Тип медиаторов вегетативных нейроэффекторных соединений не во всех случаях определяется их принадлежностью к тому или иному отделу в. н. с. В связи с этим возникло предположение, что он специфичен для клеточных, а не для анатомических единиц нервной системы. Г. Дейл (1933) предложил называть нервные волокна, выделяющие ацетилхолин, холинергическими, а волокна, выделяющие адреналин (фактически норадреналин),— адренергическими.
Значительный вклад в понимание механизмов действия М. внесли также советские ученые А. Г. Гинецинский, X. С. Коштоянц, М. Я. Михельсон, В. Н. Черниговский, С. В. Аничков и др. Уже в 30-х гг. в СССР развернулась работа по применению М. для лечения нервных болезней.
Участие М. в проведении возбуждения представляется следующим образом. Местом приложения М. является синапс (см.). Пресинаптическим звеном его может быть нейрон (см. Нервная клетка), либо рецепторная клетка (напр., палочки и колбочки сетчатки, волосковые клетки органов слуха и равновесия). Пресинаптической клетке, по-видимому, присуща медиаторная специфичность, т. е. способность синтезировать, запасать, секретировать и реутилизировать строго определенный М. Цитоплазматическими органеллами, в которых запасаются и посредством которых выделяются из клетки М., служат, по везикулярной гипотезе секреции М., особые окруженные мембраной пузырьки. Специализированный для секреции участок пресинаптической клетки (в нейроне — терминальные части аксона, а иногда и дендриты) имеет особую наружную так наз. секреторную мембрану, для к-рой характерно наличие потенциалзависимых кальциевых каналов. Секрецию вызывает входящий ток ионов кальция, возникающий при деполяризации пресинаптической клетки (т. е. при ее возбуждении). Тонкие механизмы действия ионов кальция на синаптические пузырьки еще не изучены; по-видимому, секреция протекает по типу экзоцитоза: мембрана пузырька соединяется с наружной клеточной мембраной так, что образуется отверстие, через к-рое содержимое пузырька выходит в межклеточную среду.
Выйдя в синаптическую щель, М. диффундирует к постсинаптической клетке и взаимодействует с ее специфическими рецепторами, вследствие чего происходит то или иное изменение в состоянии клетки. В основе этого регуляторного эффекта чаще всего лежит изменение ионной проводимости постсинаптической мембраны.
Для каждого М. стараются найти наиболее характерные признаки, позволяющие обнаруживать клеточные системы с данным М. С помощью различных гистохим, методов, в частности формальдегидной конденсации, удалось детально картировать системы моноаминергических нейронов мозга. Однако прямая гистохим. локализация пока возможна лишь для немногих М. Более перспективным и универсальным методом считается иммуногистохим, выявление фермента, участвующего в синтезе данного М. или другого специфического белка, связанного с определенным М. С этой целью используют также способность нейронов реутилизировать собственный М. Для этого в окружающую нейрон среду вводят М. или его метаболический предшественник с какой-либо (напр;, радиоактивной) меткой и изучают последующее распределение метки. О принадлежности к тому или иному известному типу М. помогает судить также изучение морфологии секреторных пузырьков пресинаптической клетки с помощью электронного микроскопа.
Распределение нейронов, обладающих одним и тем же М., и их функции сходны у систематически близких организмов. Это сходство прослеживается в пределах только одного зоол, типа и не наблюдается при сравнении разных типов (напр., позвоночных, членистоногих и моллюсков). Однако организмы, относящиеся к разным зоол, типам, имеют одни и те же медиаторные вещества, т. е. сходный клеточный состав нервных систем. Это указывает на глубокую древность медиаторных различий между нейронами и на консерватизм специфического секреторного химизма нервных клеток.
Значительная часть известных М. относится к группе биогенных аминов (см.), к-рую составляют декарбоксилированные производные ароматических аминокислот (так наз. арилэтиламины). В эту группу входят катехоламиновые М. Древнейшим (с эволюционной точки зрения) из них является, по-видимому, дофамин, представленный в специальной категории нейронов у большинства организмов, обладающих нервной системой. Медиаторная функция дофамина доказана на гигантском интернейроне педального ганглия некоторых водных улиток. У млекопитающих системы дофаминергических нейронов находятся преимущественно в среднем мозге — нигронеостриарная система (см. Лимбическая система). Кроме того, нейроны этого типа имеются в гипоталамической области, в сетчатке. Предполагают, что дофамин выступает в качестве М. интернейронов симпатических ганглиев (нейронный вариант хромаффинных клеток). Функция норадреналина в качестве М. наиболее изучена в нейроэффекторных окончаниях симпатических нервов. Группы нор адренергических нейронов имеются также в среднем мозге, мозговом варолиевом мосту, продолговатом и промежуточном мозге. Адреналин, являющийся метилированным производным норадреналина, служит М. симпатических нейронов у бесхвостых амфибий. В продолговатом мозге млекопитающих найдены небольшие группы нейронов, синтезирующих адреналин, однако вопрос о медиаторной функции адреналина у них изучен еще недостаточно.
Широко распространенный биогенный амин серотонин (см.) является производным триптофана. Медиаторная функция серотонина была впервые показана на моллюсках. Серотонинергические нейроны некоторых ядер ствола головного мозга иннервируют обширные области ц. н. с. млекопитающих, включая новую кору, гиппокамп, подбугровую область, спинной мозг. Содержащие серотонин нейроны найдены также в кишечном нервном сплетении у некоторых позвоночных животных.
Ацетилхолин — единственный известный Медиатор, относящийся к простым эфирам (уксуснокислый эфир холина). Медиаторная функция ацетилхолина детально исследована на некоторых нейроэффекторных соединениях и межнейронных синапсах периферической нервной системы у позвоночных животных. Их периферические секреторные терминали происходят из следующих групп холинергических нейронов: клеток моторных ядер, иннервирующих скелетные мышцы; спинномозговых нейронов, иннервирующих хромаффинную ткань; преганглионарных нейронов, иннервирующих клетки интрамуральных и экстрамуральных ганглиев; значительной части периферических нейронов, в особенности интрамуральных ганглиев. Холинергические нейроны найдены у многих беспозвоночных, часть из них хорошо изучена (моторные нейроны стоматогастрической системы и некоторые афферентные нейроны ракообразных, интернейроны центральных ганглиев моллюсков, мотонейроны соматических мышц круглых и кольчатых червей и др.). Значительно хуже в связи с методическими трудностями идентификации холинергических нейронов исследованы интернейроны головного и спинного мозга. Данные, на основании которых идентификация холинергических нейронов базировалась на гистохим, выявлении ацетилхолинэстеразы, следует считать в основном ошибочными.
Изучение медиаторных процессов входит в круг задач нейрохимии, которая в последние десятилетия добилась значительных успехов в понимании глубинных механизмов работы нервной системы в норме и патологии. Достижениия нейрохимии легли в основу развития нейро- и психофармакологии, нейро-и психоэндокринологии.
Информационные субстанции нервной системы можно классифицировать по разным признакам. Мы ограничимся разделением их на две группы: 1) классические медиаторы, выделяющиеся в пресинаптическом окончании и непосредственно передающие возбуждение в синапсе и 2) модуляторы, или регуляторные пептиды, изменяющие реакцию клетки на классические медиаторы или другие формы активности нервных клеток (хотя некоторые из них могут выполнять и передаточную функцию).
Классические медиаторы
Ацетилхолин (АХ) –один из первых изученных медиаторов. Его молекула состоит из азотсодержащего вещества холина и остатка уксусной кислоты. АХ работает в качестве медиатора в трех функциональных блоках нервной системы: 1) в нервно-мышечных синапсах скелетной мускулатуры (синтезируется в мотонейронах); 2) в периферической части ВНС (синтезируется в преганглионарных симпатических и парасимпатических нейронах, постганглионарных парасимпатических нейронах); 3) в больших полушариях, где холинэргические системы представлены нейронами некоторых ретикулярных ядер моста, интернейронами полосатого тела, нейронами ядер прозрачной перегородки. Аксоны этих нейронов направляются к различным структурам переднего мозга, в первую очередь, в новую кору и гиппокамп. Результаты последних исследований показывают, что холинэргическая система играет важную роль в процессах обучения и памяти. Так, в мозге умерших людей, страдавших болезнью Альцгеймера, наблюдается резкое снижение количества холинэргических нейронов в больших полушариях.
Синаптические рецепторы к АХ разделяются на никотиновые (возбуждаются АХ и никотином) и мускариновые (возбуждаются АХ и токсином мухомора мускарином). Никотиновые рецепторы открывают натриевые каналы и приводят к формированию ВПСП. Они расположены в нервно-мышечных синапсах скелетной мускулатуры, в вегетативных ганглиях и немного – в ЦНС. Наиболее чувствительны к никотину вегетативные ганглии, поэтому первые попытки курения приводят к выраженным вегетативным проявлениям – перепады артериального давления, тошнота, головокружение. По мере привыкания сохраняются в основном симпатическое действие. Никотиновые рецепторы присутствуют и в ЦНС, благодаря чему никотин, являясь психоактивным веществом, оказывает центральное стимулирующее действие. Антагонисты никотиновых рецепторов – соединения, подобные яду кураре - действуют в основном на нервно-мышечные синапсы, вызывая паралич скелетной мускаулатуры. Мускариновые рецепторы расположены в синапсах вегетативных постганглионарных (в основном парасимпатических) нейронов, в ЦНС. Их возбуждение может открывать как калиевые, так и натриевые каналы. Классический антагонист мускариновых рецепторов – атропин, вызывающий симпатические эффекты, двигательное и речевое возбуждение, галлюцинации. Инактивация АХ осуществляется ферментом ацетилхолинэстеразой. Обратимые блокаторы этого фермента улучшают нервно-мышечную передачу и используются в неврологической практике, необратимые – вызывают опасные отравления (хлорофос, нервно-паралитические газы).
Биогенные амины (БА) -группа медиаторов, имеющих в своем составе аминогруппу. Разделяются на катехоламины (норадреналин, дофамин) и серотонин.
Норадреналин (НА)в периферической НС синтезируется в нейронах симпатических ганглиев, в ЦНС – в голубом пятне и межножковом ядре среднего мозга. Аксоны клеток этих ядер широко распространены в различных структурах головного и спинного мозга. Возбуждение адренорецепторов может увеличивать как натриевую проводимость (ВПСП), так и калиевую (ТПСП). Агонистами НА-эргических синапсов являются эфедрин и др. средства от бронхиальной астмы, сосудосуживающие препараты - нафтизин, галазолин. Антагонисты – средства, использующиеся для снижения артериального давления (адреноблокаторы).
В ЦНС эффектами НА являются:
- повышение уровня бодрствования;
- тормозная регуляция сенсорных потоков, обезболивание;
- повышение уровня двигательной активности;
- повышение агрессивности, стенические эмоции во время стрессовых реакций (азарт, удовольствие от риска, преодоления усталости). При некоторых формах депрессии отмечается снижение уровня НА, а многие антидепрессанты стимулируют его образование.
Дофамин (ДА)–непосредственный предшественник НА. Функционирует в ЦНС, где выделяют три основных ДА-эргических системы:
1) черная субстанция – полосатое тело. Основная функция этой системы – поддержание общего уровня двигательной активности, обеспечение точности выполнения моторных программ, устранение лишних движений. Недостаточность дофамина в этой системе ведет к развитию паркинсонизма;
3) гипоталамус - гипофиз. Участвует в регуляции гипоталамо–гипофизарной системы (в частности, ДА тормозит секрецию пролактина), вызывает торможение центров голода, агрессивности, полового поведения, возбуждение центра удовольствия.
Средства, блокирующие рецепторы к дофамину, используются в медицине в качестве нейролептиков. Такие опасные психоактивные вещества, как психостимуляторы и кокаин, усиливают действие ДА (увеличивают выброс или блокируют обратный захват медиатора).
Инактивация серотонина, как и других биогенных аминов, происходит под действием фермента моноаминоксидазы (МАО). Интересно, что такая психологическая особенность людей, как стремление к поиску новых сильных ощущений, может быть связана с малым количеством этого фермента в ЦНС. Ингибиторы МАО или ингибиторы обратного захвата серотонина используются в медицине в качестве антидептессантов.
Аминокислотные медиаторы (АК).Более 80% нейронов ЦНС используют аминокислотные медиаторы. АК достаточно просты по своему составу, характеризуются большей специфичностью синаптических эффектов (имеют либо возбуждающие – глутаминовая и аспарагиновая кислоты, либо тормозные свойства – глицин и ГАМК).
Глутаминовая кислота (ГК)–основной возбуждающий медиатор ЦНС. Имеется в любой белковой пище, но пищевая ГК в норме очень плохо проникает через гематоэнцефалический барьер, что защищает мозг от сбоев в его деятельности. Практически вся ГК, необходимая мозгу, синтезируется в нервной ткани. Однако при употреблении в пищу большого количества солей ГК может наблюдаться ее нейротропное действие: происходит активация ЦНС, и это используют в клинике, назначая глутамат в таблетках (2-3г) при задержках психического развития или истощении нервной системы. Глутамат широко применяется в пищевой промышленности как вкусовая добавка, и входит в состав пищевых концентратов, колбасных изделий и пр. (имеет мясной вкус). При одномоментном употреблении с пищей 10-30г глутамата может произойти избыточное возбуждение сосудодвигательного центра, повышается АД, учащается пульс. Это опасно для здоровья, особенно для детей и людей, страдающих сердечно-сосудистыми заболеваниями. Антагонисты ГК, например калипсол (кетамин), используются в клинике как мощные анальгетики и средства для быстрого наркоза. Побочный эффект – появление галлюцинаций. Некоторые вещества этой группы являются сильными галлюциногенными наркотиками.
Инактивация ГК происходит путем захвата астроцитами, где происходит ее превращение в аспарагиновую кислоту и ГАМК.
Гамма-аминомасляная (ГАМК)–непищевая АК (полностью синтезируется в организме). Играет важную роль во внутриклеточном метаболизме; лишь небольшая часть ГАМК выполняет медиаторные функции. Является медиатором мелких тормозных нейронов, широко распространенных в ЦНС. Этот медиатор используют также клетки Пуркинье, нейроны бледного шара. На постсинаптической мембране открывает Ка + и Cl - - каналы. У рецепторов к ГАМК сложная структура, они имеют центры, связывающиеся с другими веществами, что приводит к изменению эффектов медиатора. Такие вещества используются как седативные и транквилизаторы, снотворные, противоэпилептические, средства для наркоза. Иногда все эти эффекты может вызывать одно и то же вещество в зависимости от дозы. Например, барбитураты, которые используются для наркоза (гексенал), при тяжелых формах эпилепсии (бензонал, фенобарбитал). В меньших дозах действуют как снотворные, но используются ограниченно, поскольку нарушают нормальную структуру сна (укорачивают парадоксальную фазу), после такого сна долго сохраняется заторможенность и нарушение координации движений. Длительное применение барбитуратов вызывает наркотическую зависимость. Алкоголь усиливает действие барбитуратов, легко возникает передозировка, приводящая к остановке дыхания. Другая группа агонистов ГАМК- бензодиазепины. Они действующие более избирательно и мягко, в качестве снотворных увеличивают глубину и продолжительность сна (реланиум, феназепам). В больших количествах также вызывают заторможенность после сна. Агонисты ГАМК используются как транквилизаторы (успокаивающие) или анксиолитики (снижающие тревожность). Возможно формирование зависимости. Лекарства на основе ГАМК используются в качестве мягких психостимуляторов при возрастных изменениях, сосудистых заболеваниях, умственной отсталости, после инсультов и травм. Они действуют за счет улучшения работы интернейронов и относятся к группе ноотропов, улучшающих обучение и память, повышающие устойчивость ЦНС к неблагоприятным воздействиям, восстанавливающие нарушенные функции мозга (аминалон, пантогам, ноотропил). Как и все нейротропные препараты, должны применяться только по строгим медицинским показаниям.
Глицин–тормозной медиатор, но менее распространенный, чем ГАМК. Глицинэргические нейроны в основном тормозят мотонейроны и предохраняют их от перевозбуждения. Антагонистом глицина является стрихнин (яд, вызывающий судороги и удушье). Глицин используют как успокаивающее и улучшающее мозговой метаболизм средство.
Модулирующие медиаторы
Пептидные медиаторы – вещества, состоящие из коротких аминокислотных цепочек.
Вещество Р (от англ.powder - порошок: его выделили из сухого порошка спинного мозга коров). Вырабатывается в нейронах спинальных ганглиев, участвующих в проведении болевых импульсов. В нейронах задних рогов спинного мозга вещество Р работает вместе с глутаминовой кислотой как классический медиатор, передавая болевые сигналы. Обнаруживается в чувствительных окончаниях кожи, откуда выделяется при повреждении, вызывая воспалительный процесс. Вырабатывается также некоторыми интернейронами ЦНС, выполняя функцию модулирующего медиатора.
Кроме перечисленных, функции модулирующих медиаторов выполняют некоторые гипоталамические, гипофизарные и тканевые гормоны. Например, тиролиберин вызывает эмоциональную активацию, повышение уровня бодрствования, стимулирует дыхательный центр. Холецистокинин – вызывает тревожность и страх. Вазопрессин – активирует запоминание. АКТГ – стимулирует внимание и улучшает обменные процессы в нервных клетках. Существуют нейропептиды, избирательно управляющие половым поведением, пищевой мотивацией, терморегуляцией. Все они образуют сложную иерархическую систему взаимодействий, тонко регулирующую работу ЦНС.
Лекция 5. ОСОБЕННОСТИ МОЗГОВОГО КРОВООБРАЩЕНИЯ. ЛИКВОР И ГЕМАТОЭНЦЕФАЛИЧЕСКИЙ БАРЬЕР
Кровоснабжение головного и спинного мозга
Работа мозга связана с большими энергетическими затратами. Головной мозг составляет около 2 % от массы тела, однако 15 % крови, выбрасываемой сердцем в аорту за одно сокращение, поступает в сосуды головного мозга. Нарушение мозгового кровообращения неизбежно сказывается на функционировании нервной системы.
Головной мозг снабжается артериальной кровью из двух основных источников – внутренних сонных артерий, отходящих от общих сонных артерий, берущих начало от дуги аорты, и от позвоночных артерий, отходящих от подключичных артерий. Общие сонные и подключичные артерии берут начало от дуги аорты.
Внутренние сонные артерии – крупные сосуды, их диаметр – около 1 см. Они входят в полость черепа через яремные отверстия в височных костях, проходят через твердую мозговую оболочку, разветвляются и кровоснабжают глазные яблоки, зрительные тракты, промежуточный мозг, базальные ядра, лобные теменные, височные, островковые доли больших полушарий. Наиболее крупные ветви – передняя и средняя мозговые артерии.
Позвоночные артерии начинаются от подключичных артерий на уровне 7 шейного позвонка, идут вверх через поперечные отверстия шейных позвонков и проникают в полость черепа через большое затылочное отверстие. Ветви этих артерий кровоснабжают спинной мозг, продолговатый мозг и мозжечок, а также оболочки мозга. У заднего края моста правая и левая позвоночные артерии соединяются, образуя базиллярную артерию, проходящую в одноименной борозде на вентральной поверхности моста. У переднего края моста базиллярная артерия делится на две задние мозговые артерии. Ее ветви кровоснабжают мост, мозжечок, продолговатый мозг, средний мозг, частично промежуточный мозг, затылочные доли больших полушарий.
На основании головного мозга ветви внутренней сонной артерии и базиллярной артерии соединяются между собой, образуя артериальный (виллизиев) круг большого мозга. Этот круг располагается в подпаутинном пространстве и охватывает зрительный перекрест и гипоталамус. Благодаря этому кругу уравниваются потоки крови к различным частям мозга, даже если один из сосудов (сонная или позвоночная артерия) пережимается или недостаточно развит.
Спинной мозг кровоснабжается ветвями позвоночных артерий (шейные сегменты), а также ветвями грудной и брюшной части аорты.
Ветви мозговых артерий расположены в мягкой мозговой оболочке, которую также называют сосудистой, и вместе с ее волокнами проникают в ткань мозга, где разветвляются на мелкие артериолы и капилляры.
Капилляры – это мельчайшие сосуды, стенка которых состоит из одного слоя клеток. Через эту стенку вещества, растворенные в крови, проникают в ткань мозга, а продукты мозгового метаболизма переходят в кровь. Капилляры собираются в венулы, затем в вены, лежащие в сосудистой оболочке мозга. Тонкие кровеносные сосуды мягкой мозговой оболочки проникают в желудочки мозга, где образуют сосудистые сплетения. В конечном итоге венозная кровь оттекает в синусы твердой мозговой оболочки, откуда попадает в крупные вены большого круга кровообращения.
Теория по нормальной физиологии на тему: Синапс. Физиология мышечных волокон. В данной статье рассматривается механизм синаптической передачи, НМС…
При создании данной страницы использовалась лекция по соответствующей теме, составленная Кафедрой Нормальной физиологии БашГМУ
Синапс — это специфическое место контакта двух возбудимых систем (клеток) для передачи возбуждения.
По способу передачи сигналов:
- механические,
- химические,
- электрические.
По виду медиатора: холинэргические и др.
Нервно-мышечный синапс (НМС) — химический, передача с помощью медиатора ацетилхолина.
Синонимы к слову НМС:
- Нервно-мышечное соединение;
- Моторная концевая пластинка.

Аксоны нервных клеток на своих окончаниях теряют миелиновую оболочку , ветвятся, и концевые веточки аксона утолщаются. Это пресинаптическая терминаль или бляшка или пуговка , которая погружается в углубление на поверхности мышечного волокна.
Покрывающая концевую веточку аксона поверхностная мембрана называется пресинаптической мембраной , т.е. это мембрана, покрывающая поверхность синаптической бляшки (терминали аксона).
Мембрана, покрывающая мышечное волокно в области синапса, называется постсинаптической мембраной , или концевой пластинкой. Она имеет извитую структуру, образуя многочисленные складки, уходящие вглубь мышечного волокна, за счет чего увеличивается площадь контакта.
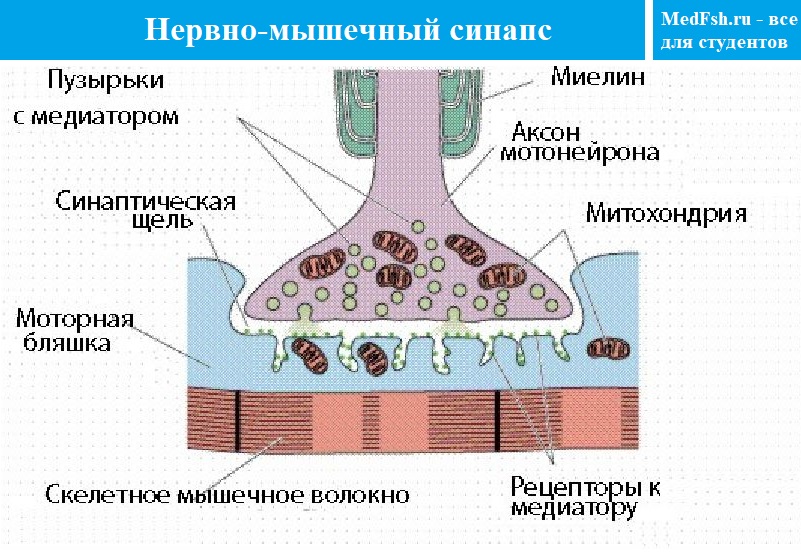
На постсинаптической мембране находятся белковые структуры — рецепторы , способные связывать медиатор . В одном синапсе количество рецепторов достигает 10-20 млн.
Между пре- и постсинаптическими мембранами находится синаптическая щель , размеры ее в среднем 50 нм, она открывается в межклеточное пространство и заполнена межклеточной жидкостью .
В синаптической щели находится мукополисахаридное плотное вещество в виде полосок, мостиков и содержится фермент ацетилхолинэстераза .
В пресинаптической терминали находится большое количество пузырьков или везикул , заполненных медиатором — химическим веществом посредником, осуществляющим передачу возбуждения.
В нервно-мышечном синапсе медиатор — ацетилхолин (АХ).
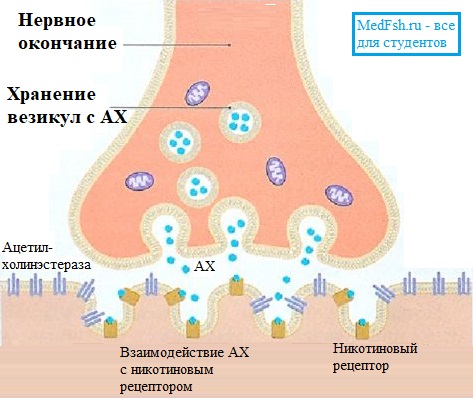
АХ синтезируется из холина и уксусной кислоты (ацетил-коэнзима А) с помощью фермента холинэстеразы. Эти вещества перемещаются из тела нейрона по аксону к пресинаптической мембране. Здесь в пузырьках происходит окончательное образование АХ.
3 фракции медиатора:
- Первая фракция — доступная — располагается рядом с пресинаптической мембраной.
- Вторая фракция — депонированная — располагается над первой фракцией.
- Третья фракция — диффузно рассеянная — наиболее удаленная от пресинаптической мембраны.
Механизм синаптической передачи

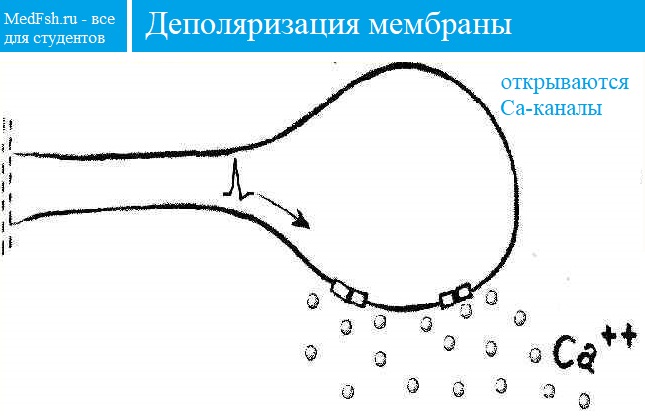
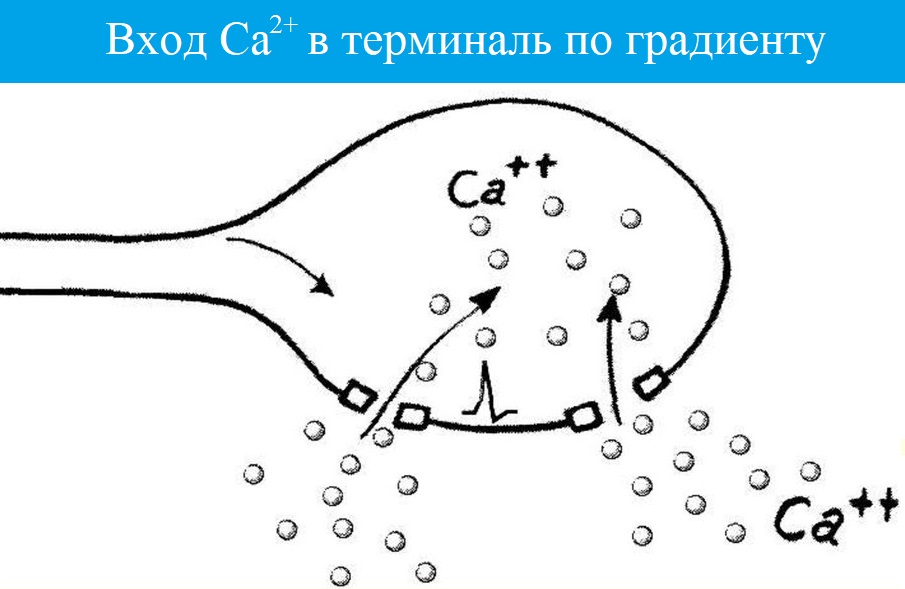
Ионы Ca вызывают образование специального белкового комплекса , который включает в себя везикулу и структуры, расположенные непосредственно около пресинаптической мембраны.
Они связаны между собой так называемыми белками экзоцитоза.
Часть белков расположена на везикулах (синапсин, синаптотагмин, синаптобревин), а часть — на пресинаптической мембране (синтаксин, синапсо-ассоциированный белок). Данный комплекс получил название секретосома .
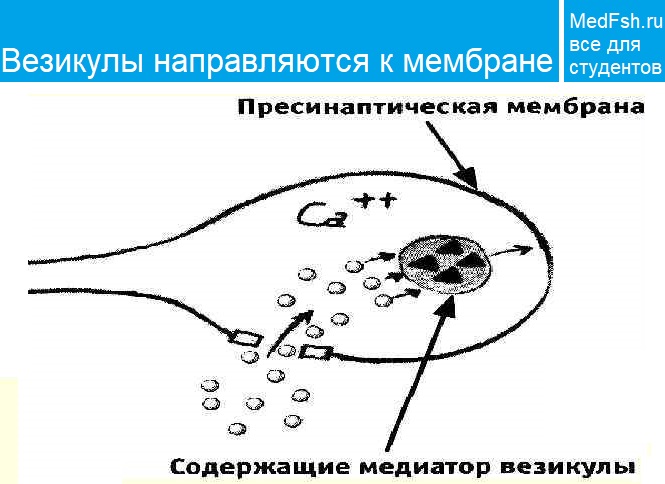
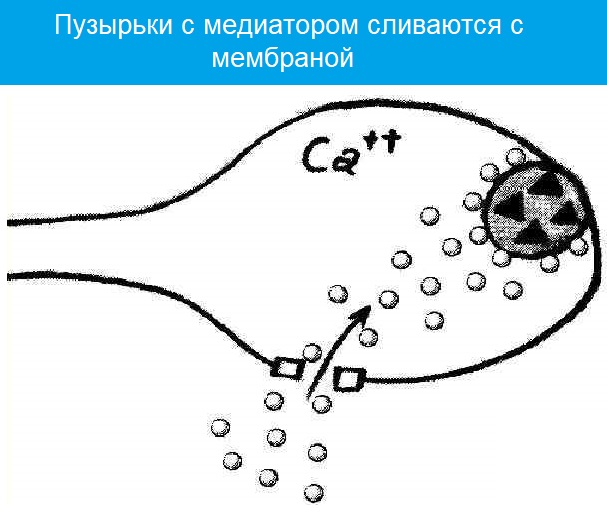
Излитию содержимого пузырька в щель способствует белок синаптопорин , формирующий канал, по которому идет выброс медиатора.
Квант медиатора — количество молекул, содержащихся в одной везикуле.
На 1 ПД выбрасывается 100 квантов АХ.
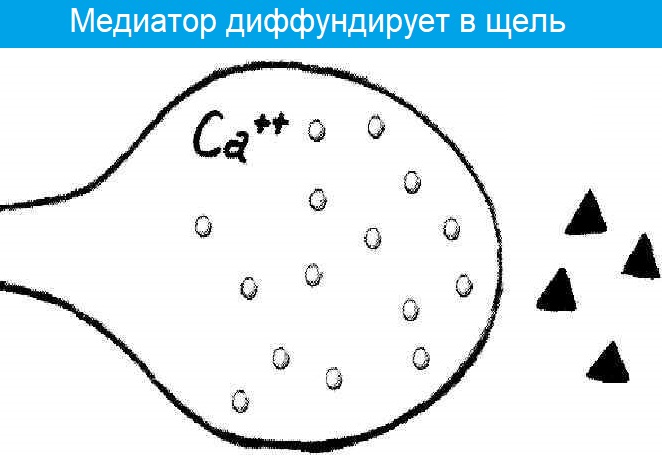
На постсинаптической мембране возникает потенциал концевой пластинки (ПКП). Он является аналогом локального ответа (ЛО).
Потенциал действия на постсинаптической мембране не возникает ! Он формируется на соседней мембране мышечного волокна.
- связывание с рецептором,
- разрушение ферментов (ацетилхолинэстеразой),
- обратное поглощение в пресинаптическую мембрану,
- вымывание из щели и фагоцитоз.
События в синапсе :
- ПД приходит к терминали аксона;
- Он деполяризует пресинаптическую мембрану;
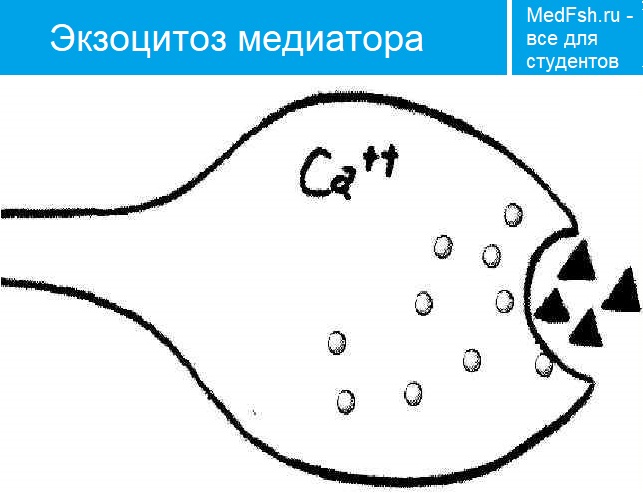
- Ca2+ входит в терминаль, что приводит к выделению АХ;
- В синаптическую щель выделяется медиатор АХ;
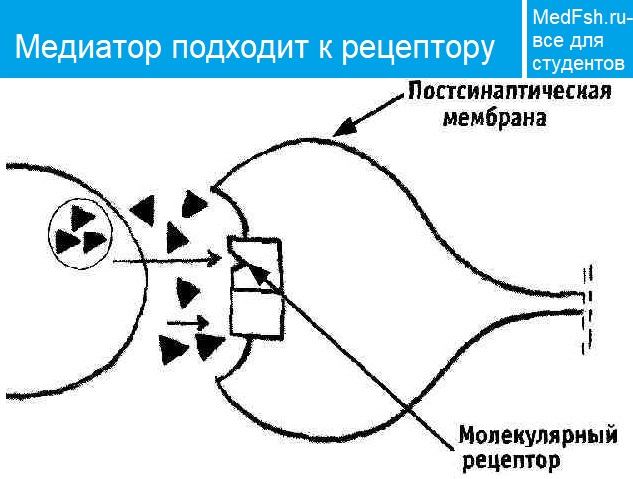
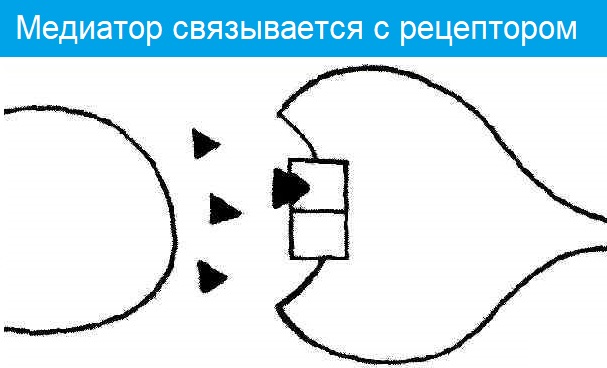
- Он диффундирует в щель и связывается с рецепторами постсинаптической мембраны;
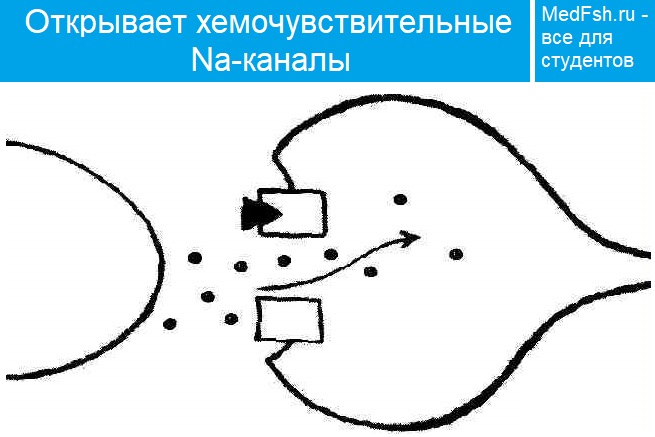
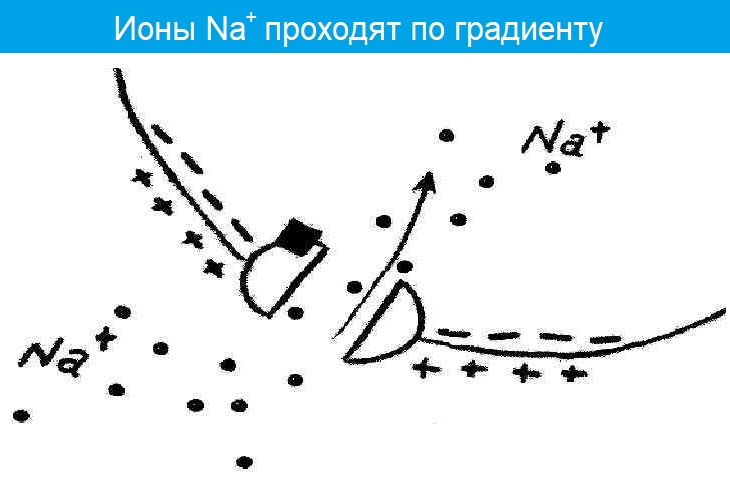
- Меняется проницаемость постсинаптической мембраны для ионов Na+;
- Ионы Na+ проникают в постсинаптическую мембрану и уменьшают ее заряд — возникает потенциал концевой пластинки (ПКП) .
На самой постсинаптической мембране ПД возникнуть не может, так как здесь отсутствуют потенциалзависимые каналы, они являются хемозависимыми!
- ПКП суммируются и достигают КУД на соседнем участке мышечного волокна, что приводит к возникновению ПД и его распространению по мышечному волокну (около 5 м/с).
Достигнув пороговой величины, то есть КУД, ПКП возбуждает соседнюю (внесинаптическую) мембрану мышечного волокна за счет местных круговых токов.

Особенности проведения возбуждения в нервно-мышечном синапсе
Одностороннее проведение возбуждения — только в направлении от пресинаптического окончания к постсинаптической мембране.
Суммация возбуждения соседних постсинаптических мембран.
Синаптическая задержка — замедление в проведении импульса от нейрона к мышце составляет 0,5-1 мс. Это время затрачивается на секрецию медиатора, его диффузию к постсинаптической мембране, взаимодействие с рецептором, формирование ПКП, их суммацию.
Низкая лабильность — она составляет 100-150 имп/с для сигнала, что в 5-6 раз ниже лабильности нервного волокна.
Чувствительность к действию лекарственных веществ, ядов, БАВ, выполняющих роль медиатора.
Утомляемость химических синапсов — выражается в ухудшении проводимости вплоть до блокады в синапсе при длительном функционировании синапса. Главная причина утомляемости — исчерпание запасов медиатора в пресинаптическом окончании.
Законы проведения возбуждения по нервам:
- Закон функциональной целостности нерва.
- Закон изолированного проведения возбуждения.
- Закон двустороннего проведения возбуждения.
В зависимости от скорости проведения возбуждения нервные волокна подразделяются на 3 группы: A, B, C. В группе A выделяют 4 подгруппы: альфа, бетта, гамма и сигма.
Физиология мышечных волокон
- скелетная (40-50% массы тела),
- сердечная (менее 1%),
- гладкая (8-9%).
Физиологические свойства скелетных мышц:
- Возбудимость — способность отвечать на действие раздражителя возбуждением.
- Проводимость — способность проводить возбуждение из места его возникновения к другим участкам мышцы.
- Лабильность — способность мышцы сокращаться в соответствии с частотой действия раздражителя (200-300 Гц для скелетной мышцы).
- Сократимость — для мышцы является специфическим свойством — это способность мышцы изменять длину или напряжение в ответ на действие раздражителя.
Физические свойства скелетных мышц:
- Растяжимость — способность мышцы изменять длину под действием растягивающей силы.
- Эластичность — способность мышцы восстанавливать первоначальную длину или форму после прекращения действия растягивающей силы.
- Силы мышц — способность мышцы поднять максимальный груз.
- Способность мышцы совершать работу.
Режимы сокращения:
- Изотонический,
- Изометрический,
- Ауксотонический.
Изотонический режим — сокращение мышцы происходит с изменением ее длины без изменения напряжения (тонуса) (напр.: сокращение мышц языка).
Изометрический режим — длина постоянная, увеличивается степень мышечного напряжения (тонуса) (напр.: при поднятии непосильного груза).
Ауксотонический режим — одновременно изменяется длина и напряжение мышцы (характерен для обычных двигательных актов).
Механизм сокращения поперечно-полосатых мышц
Любая скелетная мышца состоит из мышечных волокон, которые, в свою очередь, состоят из множества тонких нитей — миофибрилл , расположенных продольно. Каждая миофибрилла состоит из протофибрилл — нитей сократительных белков: миозина (миозиновая протофибрилла), актина (актиновая протофибрилла).
Кроме сократительных белков в миофибрилле имеются два регуляторных белка: тропомиозин и тропонин .
Миозиновые волокна соединены в толстый пучок, от которого в торону актиновых нитей отходят поперечные мостики. У каждого мостика выделяют шейку и головку.
Нить актина располагается в виде 2 скрученных ниток бус. На ней имеются актиновые центры.
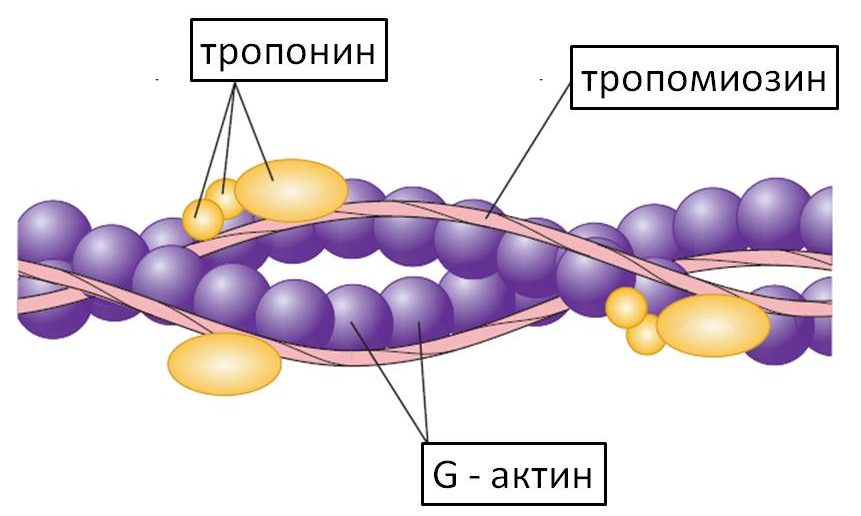
Тропомиозин в виде спиралей оплетает поверхность актина, закрывая в покое ее центры. Одна молекула тропомиозина контактирует с 7 молекулами актина.
Тропонин образует утолщение на конце каждой нити тропомиозина.
Под влиянием возникшего в мышечном волокне ПД из саркоплазматического ретикулума (СПР — депо Ca2+) высвобождаются ионы Ca. Кальций связывается с тропонином, который смещает тропомиозиновый стержень, что приводит к открытию актиновых центров.
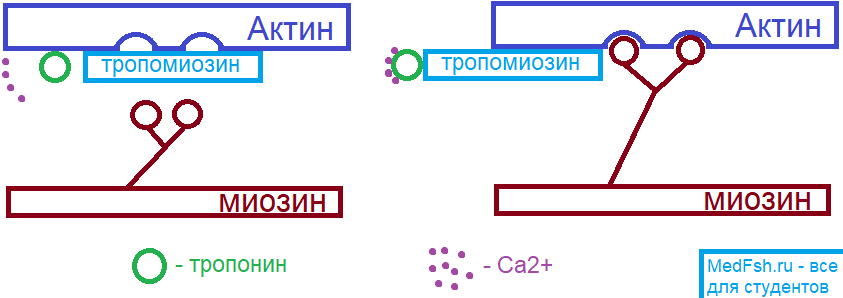
В результате, к актиновым центрам присоединяются головки поперечных миозиновых мостиков.
Процесс расслабления происходит в обратной последовательности с использованием энергии АТФ за счет функционирования кальциевого насоса.
При отсутствии повторного импульса ионы Ca не поступают из СПР. В результате отсутствия Ca-тропонинового комплекса, тропомиозин возвращается на свое прежнее место, блокируя актиновые центры актина. Актиновые протофибриллы легко скользят в обратном направлении благодаря эластичности мышцы, и мышца удлиняется (расслабляется).
Гладкие мышцы
Гладкие мышцы — это мышцы, формирующие слой стенок полых внутренних органов. Они построены из веретенообразных одноядерных мышечных клеток без поперечной исчерченности за счет хаотичного расположения миофибрилл.
Особенности гладких мышц:
- Иннервируются волокнами вегетативной нервной системы (ВНС);
- Обладают низкой возбудимостью:
- Обладают низкой величиной МП (мембранного потенциала) — -50 — -60 мВ из-за более высокой проницаемости для ионов Na+
- ПД (потенциал действия) отличается меньшей амплитудой и большей длительностью. Он формируется в основном за счет ионов Ca2+
- Медленная проводимость:
Клетки в гладких мышцах функционально связаны между собой посредством щелевидных контактов — нексусов, которые имеют низкое электрическое сопротивление. За счет этих контактов ПД распространяется с одного мышечного волокна на другое, охватывая большие мышечные пласты, и в реакцию вовлекается вся мышца.
Гладкие мышцы способны осуществлять относительно медленные ритмические и длительные тонические сокращения.
Медленные ритмические сокращения обеспечивают перемещение содержимого органа из одной области в другую.
Длительные тонические сокращения, особенно сфинктеров полых органов, препятствуют выходу из них содержимого.
Это способность сохранять приданную им при растяжении или деформации форму. Благодаря пластичности гладкая мышца может быть полностью расслаблена как в укороченном, так и в растянутом состоянии.
Особенность гладких мышц, отличающая их от скелетных. Благодаря автоматии гладкие мышцы могут сокращаться в условиях отсутствия иннервации . Важную роль в этом играет растяжение.
Растяжение является адекватным раздражителем для гладкой мускулатуры. Сильное и резкое растяжение гладких мышц вызывает их сокращение.
Сравнительная характеристика скелетных и гладких мышц:
Читайте также:


