Нервная регуляция мозгового кровообращения
Ауторегуляция мозгового кровообращения - это способность поддерживать постоянство объемного мозгового кровотока в условиях изменения перфузионного давления в основном за счет колебаний артериального давления (Мчедлишвили Г.И., 1968; Ганнушкина И.В., 1975; Москаленко Ю.Е., 1984; Москаленко Ю.Е. и соавт., 1988; Fog, 1938; Lassen, 1964; Harper, 1966; Ekstrom-Jodal et al., 1971; Berne et al., 1981; Paulson et al., 1989). При повышении артериального давления (АД) резистивные сосуды суживаются и ограничивают приток крови к мозгу, а при снижении - расширяются и увеличивают приток крови к мозгу, в результате мозговая перфузия остается неизменной при колебании системного АД (Зеликсон Б.Б., 1973; Wahl, Schilling, 1993).
В основе ауторегуляции мозгового кровообращения лежат три взаимосвязанных механизма, нейрогенный, гуморально-метаболический и миогенный (Aaslid, 1992; Wahl, Schilling, 1993). Заметим, что мозговая ауторегуляция не является каким-то особенным и обособленным видом регуляции церебральной гемодинамики. Этот достаточно сложный механизм базируется на известных для любого сосудистого региона видах регуляции сосудистого тонуса, имея при этом некоторые особенности. В связи с этим ниже представляем краткую характеристику основных вариантов регуляции мозгового кровообращения.
Регуляция мозгового кровообращения, как и других органов, включает нейрогенный, гуморальный, метаболический, миогенный и эндотелийзависимый механизмы.
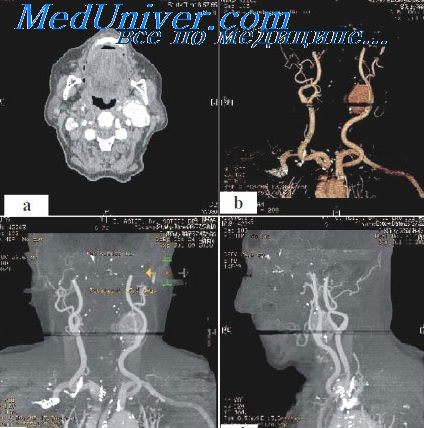
Гуморальная регуляция мозгового кровообращения в основном связана с функционированием ренин-ангиотензиновой и калликреин-кининовой систем. Ангиотензин II обладает констрикторным действием на мозговые сосуды (Enoch et al., 1978; Reynier-Rebuffel etal., 1983; Das, Ghosh, 1997). В некоторых случаях гуморальные стимулы избирательно изменяют резистентность крупных мозговых артерий, правда без изменений кровотока вследствие реакций мелких мозговых сосудов (Faraci et al., 1988), т.е. некоторые гуморальные факторы производят противоположные сосудистые эффекты в крупных и мелких артериях, что выражается в незначительных изменениях суммарного кровотока.
Согласно сформулированной более 100 лет назад метаболической концепции Roy и Sherrington, метаболическая регуляция мозговой гемодинамики в виде усиления локального мозгового кровотока является следствием увеличения концентрации в нейронах конечных продуктов метаболизма (Н+, К+, аденозина), в связи с повышением нейрональной активности (Шахнович А.Р., Шахнович В.А., 1996; Aaslid, 1987; Klingelhofer et al., 1996; Sandor, 1999). Наиболее изученной является реакция тонуса мозговых сосудов на изменение напряжения С02 в артериальной крови, о чем уже говорилось выше.
В основе миогенной регуляции мозгового кровообращения лежит способность сосудистой стенки реагировать сокращением на повышение и расслаблением на снижение внутрисосудистого давления. Этот феномен был впервые описан Остроумовым В.И., а затем подтвержден в опытах Бейлисса (Конради Г.П., 1973).
Эндотелийзависимая регуляция тонуса кровеносных сосудов осуществляется благодаря выработке эндотелиальными клетками биологически активных субстанций вазодилататорного и вазоконстрикторного действия. Важнейшими дилататорами являются оксид азота, эндотелиальный фактор гиперполяризации (EDHF), простациклин, натрийуретический пептид С-типа и адреномедуллин (Kukreja et al., 1993; Katusic et al., 1989)- Кроме того, в сосудистой стенке синтезируется важнейший дилататор - брадикинин. Изменение соотношения продукции эндотелием дилататоров и констрикторов, про- и антитромбогенных факторов и связанная с этим дизрегуляция сосудистого тонуса и реологии крови обозначается как дисфункция эндотелия (Luscher et al.,1993; Vanhoutte, 1997; Sobrevia, Mann, 1997).
Каждый орган нашего тела питается кровью. Без этого становится невозможным его правильное функционирование. В каждый момент времени органы нуждаются в определенном количестве крови. Поэтому поступление ее к тканям неодинаковое. Это становится возможным благодаря регуляции кровообращения. Что собой представляет этот процесс, его особенности будут рассмотрены далее.
Общее понятие
В процессе изменений функциональной активности каждого органа и ткани, а также их метаболических потребностей происходит регуляция кровообращения. Физиология человеческого организма такова, что этот процесс осуществляется по трем основным направлениям.
Первым из способов подстроиться к меняющимся условиям является регуляция через сосудистую систему. Чтобы измерить этот показатель, проводится определение количества крови в определенный временной промежуток. Это, например, может быть минута. Этот показатель называется минутным объемом крови (МОК). Такое ее количество способно обеспечить потребности тканей в процессе метаболических реакций.
Вторым направлением обеспечения процессов регуляции является поддержание необходимого давления в аорте, а также прочих крупных артериях. Это движущая сила, которая обеспечивает достаточный в каждый конкретный момент приток крови. Причем она должна двигаться с определенной скоростью.
Третьим направлением является объем крови, который определяется в системных сосудах в данный момент времени. Он распределяется между всеми органами и тканями. При этом происходит определение их потребности в крови. Для этого учитывается их активность, функциональные нагрузки в данный момент. В такие периоды метаболические потребности тканей возрастают.
Регуляция кровообращения происходит под воздействием этих трех процессов. Они связаны неразрывно. В соответствии с этим происходит регуляция работы сердца, локального и системного кровотока.
Чтобы подсчитать МОК, потребуется определить количество крови, которое выбрасывает левый или правый сердечный желудочек в систему сосудов за минуту. В норме этот показатель составляет около 5-6 л/минуту. Возрастные особенности регуляции кровообращения сопоставляются с другими нормами.
Движение крови
Регуляция мозгового кровообращения, а также всех органов и тканей организма происходит посредством движения крови по сосудам. Вены, артерии и капилляры имеют определенный диаметр и длину. Они практически не меняются под воздействием разных факторов. Поэтому регулировка движения крови происходит посредством изменения ее скорости. Она движется благодаря работе сердца. Этот орган создает разность давления между началом и концом русла сосудов. Как и все жидкости, кровь движется из области высокого в область низкого давления. Эти крайние точки находятся в определенных участках тела. Наиболее высокое давление определяется в аорте и легочных артериях. Когда кровь проходит через весь организм, она возвращается обратно к сердцу. Наиболее низкое давление при этом определяется в полых (нижняя, верхняя) и легочных венах.
Давление падает постепенно, так как много энергии тратится на проталкивание крови по капиллярным протокам. Также кровоток в процессе движения испытывает сопротивление. Оно определяется диаметром просвета кровеносных сосудов, а также вязкостью самой крови. Движение становится возможным благодаря еще нескольким причинам. Среди них основными являются:
- в венах есть клапаны, что препятствует обратному перемещению жидкости;
- разное давление в сосудах в начальной и конечной точке;
- существование присасывающей силы при вдохе;
- движение скелетных мышц.
Механизмы регуляции кровообращения принято разделять на местные и центральные. В первом случае этот процесс происходит в органах, местных тканях. В этом случае учитывается, как нагружен орган или отдел, сколько кислорода ему требуется для правильной работы. Центральная регуляция проводится под воздействием общих адаптивных реакций.
Местная регуляция
Если рассматривать регуляцию кровообращения кратко, можно отметить, что этот процесс происходит как на уровне отдельных органов, так и в целом в организме. Они имеют несколько отличий.
Кровь приносит клеткам кислород и уносит из них отработанные элементы их жизнедеятельности. Процессы местного регулирования связаны с поддержанием базального тонуса сосудов. В зависимости от интенсивности метаболизма в конкретной системе этот показатель может меняться.
Стенки сосудов покрыты гладкими мышцами. Они никогда не пребывают в расслабленном состоянии. Это напряжение называется мышечным тонусом сосудов. Он обеспечивается двумя механизмами. Это миогенная и нейрогуморальная регуляция кровообращения. Первый из названных механизмов является главным при поддержании тонуса сосудов. Даже если абсолютно отсутствуют внешние влияния на систему, остаточный тонус все равно сохраняется. Он получил название базального.
Этот процесс обеспечивается спонтанной активностью клеток гладких мышц сосудов. Это напряжение передается по системе. Каждая клетка передает другой возбуждение. Это провоцирует возникновение ритмических колебаний. Когда мембрана становится гиперполяризированной, спонтанные возбуждения исчезают. При этом исчезают и сокращения мышц.
В процессе метаболизма в клетках вырабатываются вещества, которые оказывают активное влияние на гладкие мышцы сосудов. Этот принцип называется обратной связью. Когда тонус прекапиллярных сфинктеров возрастает, кровоток в таких сосудах снижается. Концентрация продуктов метаболизма возрастает. Они способствуют расширению сосудов, увеличению кровотока. Этот процесс повторяется циклично. Он относится к категории местной регуляции кровообращения в органах и тканях.
Местная и центральная регуляция
Механизмы регуляции органного кровообращения подчиняются двум взаимосвязанным факторам. С одной стороны, в организме существует центральная регуляция. Однако для ряда органов с высоким показателем метаболических процессов этого недостаточно. Поэтому здесь ярко выражены местные механизмы регуляции.
К таким органам относятся почки, сердце и мозг. В тех тканях, которые не отличаются высоким уровнем метаболизма, подобные процессы выражены меньше. Местные механизмы регуляции необходимы для поддержания стабильной скорости и объема кровотока. Чем более ярко выражены процессы метаболизма в органе, тем больше он нуждается в поддержании стабильного притока и оттока крови. Даже при колебаниях давления в системном кровотоке, в этих участках организма поддерживается его стабильный уровень.
Однако местный механизм регуляции является все же недостаточным для обеспечения быстрого изменения притока и оттока крови. Если бы в организме существовали бы только эти процессы, они бы не смогли обеспечить правильное, своевременное приспособление к меняющимся внешним условиям. Поэтому местная регуляция обязательно добавляется процессами центральной нейрогуморальной регуляцией кровообращения.
Нервные окончания отвечают за процессы иннервации сосудов и сердца. Рецепторы, которые присутствуют в системе, реагируют на разные показатели крови. К первой категории относятся нервные окончания, которые реагируют на изменения давления в русле. Их называют механорецепторами. Если же меняется химический состав крови, на это реагируют другие нервные окончания. Это хеморецепторы.
Механорецепторы реагируют на растяжение стенок сосудов и изменение скорости перемещения в них жидкости. Они способны отличать колебания нарастающего давления или пульсовые рывки.
Единое поле нервных окончаний, которое расположено в сосудистой системе, составляют ангиорецепторы. Они скапливаются в определенных участках. Это рефлексогенные зоны. Они определяются в синокаротидной, аоральной области, а также в сосудах, которые сконцентрированы в легочном круге обращения крови. При повышении давления механорецепторы создают залп из импульсов. Они исчезают при понижении давления. Порог возбуждения механорецепторов составляет от 40 до 200 мм рт. ст.
Хеморецепторы реагируют на повышение или понижение концентрации гормонов, питательных веществ внутри сосудов. Они передают сигналы о собранной информации в центральную нервную систему.
Центральные механизмы
Центр регуляции кровообращения регулирует величину выброса из сердца, а также тонус сосудов. Этот процесс происходит за счет общей работы нервных структур. Их еще называют вазомоторным центром. Он включает в себя разные уровни регуляции. Причем здесь прослеживается четкая иерархическая подчиненность.
Центр регуляции кровообращения находится в гипоталамусе. Подчиненные структуры вазомоторной системы находятся спинном и головном мозге, а также в коре больших полушарий. Существует несколько уровень регуляции. Они имеют размытые границы.
Спинальный уровень представляет собой нейроны, которые находятся в поясничном и боковых рогах грудного отдела спинного мозга. Аксоны этих нервных клеток формируют волокна, суживающие сосуды. Их импульсы поддерживаются лежащими выше структурами.
Бульбарный уровень представляет собой сосудодвигательный центр, который расположен в продолговатом мозге. Он размещен на дне 4-го желудочка. Это основной центр регуляции процесса кровообращения. Он разделяется на прессорную, депрессорную части.
Первая из названных зон отвечает за повышение давления в русле. Вместе с этим увеличиваются частота, сила сокращений сердечной мышцы. Это способствует повышению МОК. Депрессорная зона выполняет противоположную функцию. Она снижает давление в артериях. При этом деятельность сердечной мышцы также уменьшается. Рефлекторно этот участок оказывает торможение нейронов, которые относятся к прессорной зоне.
Другие уровни регуляции
Нервно-гуморальная регуляция кровообращения обеспечивается работой и других уровней. Они занимают в системе иерархии более высокое положение. Так, на сосудодвигательный центр оказывает воздействие гипоталамический уровень регуляции. Это влияние имеет нисходящий характер. В гипоталамусе также различаются прессорная и депрессорная зоны. Это можно рассматривать как дубликат бульбарного уровня.
Существует также корковый уровень регуляции. В коре головного мозга есть зоны, которые оказывают нисходящее воздействие на центр, расположенный в продолговатом мозге. Этот процесс является результатом сопоставления данных, поступивших от высших рецепторных зон на основе информации различных рецепторов. Это формирует реализацию поведенческих реакций, сердечно-сосудистого компонента эмоций.
Перечисленные механизмы формируют центральное звено. Однако существует и еще один механизм нейрогуморальной регуляции. Он называется эфферентным звеном. Все части этого механизма вступают в сложное взаимодействие между собой. Они состоят из разных компонентов. Их взаимосвязь позволяет регулировать кровоток в соответствии с существующими потребностями организма.
Нервный механизм
Нервная регуляция кровообращения является частью эфферентного звена глобальной системы, которая управляет этими процессами. Этот процесс осуществляется за счет трех компонентов:
- Симпатические преганглионарные нейроны. Расположены в поясничном отделе и передних рогах спинного мозга. Также они определяются в симпатических ганглиях.
- Парасимпатические преганглионарные нейроны. Это ядра блуждающего нерва. Они находятся в продолговатом мозгу. Также сюда относятся ядра тазового нерва, который находится в крестцовом отделе спинного мозга.
- Эфферентные нейроны метасимпатической нервной системы. Они нужны для полых органов висцерального типа. Эти нейроны находятся в ганглиях интрамурального типа их стенок. Это конечный путь, по которому продвигаются центральные эфферентные влияния.
Практически все сосуды подлежат иннервации. Это нехарактерно только для капилляров. Иннервация артерий соответствует иннервации вен. Во втором случае плотность нейронов меньше.
Нервно-гуморальная регуляция кровообращения четко прослеживается до самых сфинктеров капилляров. Они оканчиваются на клетках гладких мышц этих сосудов. Нервная регуляция капилляров проявляется в виде эфферентной иннервацией посредством свободной диффузии метаболитов, направленных к стенкам сосудов.
Эндокринная регуляция
Регуляция системы кровообращения может выполняться посредством эндокринных механизмов. Главную роль в этом процессе играют гормоны, которые вырабатываются в мозге и корковых слоях надпочечников, гипофизом (задней доле), юкстагломерулярным почечным аппаратом.
Сосудосуживающее воздействие оказывает адреналин на артерии кожи, почек, органов пищеварения, легких. При этом это же вещество способно производить и обратное действие. Адреналин расширяет сосуды, которые проходят в мышцах скелета, в гладких мышцах бронхов. Этот процесс способствует перераспределению крови. При сильном возбуждении, переживаниях, напряжении кровоток усиливается в скелетных мышцах, а также в сердце и мозге.
Норадреналин также оказывает воздействие на сосуды, позволяя перераспределять кровь. При повышении уровня этого вещества на него реагируют специальные рецепторы. Они могут быть двух типов. Обе разновидности присутствуют в сосудах. Они контролируют процесс сужения или расширения протока.
Рассматривая физиологию регуляции кровообращения, следует рассмотреть и другие вещества, которые влияют на весь процесс. Одним из них является альдостерон. Он вырабатывается надпочечниками. Он влияет на чувствительность стенок сосудов. Этот процесс контролируется при помощи изменения всасывания натрия почками, слюнными железами, а также органами ЖКТ. Сосуды становятся больше или меньше подвержены воздействию адреналина и норадреналина.
Такое вещество, как вазопрессин, способствует сужению стенок артерий в легких и в органах брюшины. При этом сосуды сердца и мозга реагируют на это расширением. Вазопрессин также выполняет функцию перераспределения крови в организме.
Прочие компоненты эндокринной регуляции
Регуляция кровообращения эндокринного типа возможна при участии и иных механизмов. Один из них обеспечивает такое вещество, как ангиотензин-II. Он образуется в процессе расщепления ферментами ангиотензина-I. На этот процесс влияет ренин. Это вещество отличается сильным сосудосуживающим действием. Причем оно значительно мощнее, чем последствия выброса в кровь норадреналина. Однако, в отличие от этого вещества, ангиотензин-II не провоцирует выброс крови из депо.
Такое действие обеспечивается за счет присутствия чувствительных к веществу рецепторов только в артериолах при входе в капилляры. Они расположены в кровеносной системе неравномерно. Это объясняет неоднородность воздействия представленного вещества в разных участках организма. Так, снижение кровотока при повышении концентрации ангиотензина-II определяется в коже, кишке, а также почках. При этом сосуды расширяются в мозге, сердце, а также надпочечниках. В мышцах изменение кровотока в этом случае будет незначительным. Если же дозы ангиотензина будут очень большими, в мозге и сердце сосуды могут сузиться. Это вещество в комплексе с ренином образует отдельную систему регуляции.
Ангиотензин может оказывать также косвенное воздействие на эндокринную систему, а также автономную нервную систему. Это вещество стимулирует выработку адреналина, норадреналина, альдостерона. Это усиливает сосудосуживающие воздействия.
Расширить сосуды способны также местные гормоны (серотонин, гистамин, брадикинин и т. д.), а также биологически активные составы.
Возрастные реакции
Различают возрастные особенности регуляции кровообращения. В детском и взрослом возрасте они значительно отличаются. Также на этот процесс влияет тренированность человека. У новорожденных ярко выражены симпатические и парасимпатические нервные окончания. До трех лет у детей преобладает тоническое влияние нервов на сердце. Центр блуждающего нерва отличается в этом возрасте низким тонусом. Он начинает влиять на кровообращение еще в 3-4 месяца. Однако ярче этот процесс проявляется в более взрослом возрасте. Это становится заметно в школьном возрасте. В этот период частота сердечных сокращений у ребенка снижается.
Рассмотрев особенности регуляции кровообращения, можно сделать вывод о сложности этого процесса. Множество факторов, механизмов влияет на него. Это позволяет четко реагировать на любые изменения окружающей среды, регулировать поступление жизненно важных веществ к органам, которые в данный момент больше загружены.
Регуляция мозгового кровообращения осуществляется сложной системой, включающей интра- и экстрацеребральные механизмы. Эта система способна к саморегуляции (т.е. может поддерживать кровоснабжение головного мозга в соответствии с его функциональной и метаболической потребностью и тем самым сохранять постоянство внутренней среды), что осуществляется путем изменения просвета мозговых артерий. Эти гомеостатические механизмы, развившиеся в процессе эволюции, весьма совершенны и надежны. Среди них выделяют следующие основные механизмы саморегуляции.
Нервный механизм передает информацию о состоянии объекта регулирования посредством специализированных рецепторов, расположенных в стенках сосудов и в тканях. К ним, в частности, относятся механорецепторы, локализующиеся в кровеносной системе, сообщающие об изменениях внутрисосудистого давления (баро- и прессорецепторы), в том числе прессорецепторы каротидного синуса, при их раздражении расширяются мозговые сосуды; механорецепторы вен и мозговых оболочек, которые сигнализируют о степени их растяжения при увеличении кровенаполнения или объема мозга; хеморецепторы каротидного синуса (при их раздражении суживаются мозговые сосуды) и самой ткани мозга, откуда идет информация о содержании кислорода, углекислоты, о колебаниях рН и о других химических сдвигах в среде при накоплении продуктов метаболизма или биологически активных веществ, а также рецепторы вестибулярного аппарата, аортальной рефлексогенной зоны, рефлексогенные зоны сердца и коронарных сосудов, ряд проприорецепторов. Особенно велика роль синокаротидной зоны. Она оказывает влияние на мозговое кровообращение не только опосредовано (через общее АД), как это представлялось ранее, но и непосредственно. Денервация и новокаинизация этой зоны в эксперименте, устраняя сосудосуживающие влияния, ведет к расширению мозговых сосудов, к усилению кровоснабжения головного мозга, к повышению в нем напряжения кислорода.
Гуморальный механизм заключается в прямом воздействии на стенки сосудов-эффекторов гуморальных факторов (кислорода, углекислоты, кислых продуктов метаболизма, ионов К и др.) путем диффузии физиологически активных веществ в стенку сосудов. Так, мозговое кровообращение усиливается при уменьшении содержания кислорода и (или) увеличении содержания углекислого газа в крови и, наоборот, ослабляется, когда содержание газов в крови меняется в противоположном направлении. При этом происходит рефлекторная дилятация или констрикция сосудов в результате раздражения хеморецепторов соответствующих артерий мозга при изменении содержания в крови кислорода и углекислоты. Возможен и механизм аксонрефлекса.
Миогенный механизм реализуется на уровне сосудов-эффекторов. При их растяжении тонус гладких мышц возрастает, а при сокращении наоборот снижается. Миогенные реакции могут способствовать изменениям сосудистого тонуса в определенном направлении.
При венозном застое, обусловленном окклюзией крупных шейных вен, избыточное кровенаполнение сосудов головного мозга устраняется путем ослабления притока крови в его сосудистую систему вследствие констрикции всей системы магистральных артерий. В таких случаях регуляция происходит также рефлекторно. Рефлексы посылаются с механорецепторов венозной системы, мелких артерий и оболочек мозга (вено-вазальный рефлекс).
Система внутримозговых артерий представляет собой рефлексогенную зону, которая в условиях патологии дублирует роль синокаротидной рефлексогенной зоны.
Нарушения саморегуляции мозгового кровообращения возникают в следующих случаях.
1. При резком снижении общего АД, когда градиент давления в кровеносной системе мозга уменьшается настолько, что не может обеспечить достаточный кровоток в мозге (при уровне систолического давления ниже 80 мм рт. ст.). Минимальный критический уровень системного АД равен 60 мм рт. ст. (при исходном – 120 мм рт. ст.). При его падении мозговой кровоток пассивно следует за изменением общего АД.
3. При недостаточном метаболическом контроле мозгового кровотока. Так, иногда после восстановления кровотока в ишемизированном участке мозга концентрация углекислоты снижается, но рН сохраняется на низком уровне вследствие метаболического ацидоза. В результате сосуды остаются расширенными, а мозговой кровоток – высоким; кислород утилизируется не в полной мере и оттекающая венозная кровь имеет красный цвет (синдром избыточной перфузии).
4. При значительном снижении интенсивности насыщения крови кислородом или увеличении напряжения углекислоты в мозге. При этом активность мозгового кровотока также меняется вслед за изменением системного АД.
При срывах механизмов саморегуляции артерии мозга утрачивают способность к сужению в ответ на повышение внутрисосудистого давления, пассивно расширяются, вследствие чего избыточное количество крови под высоким давлением направляется в мелкие артерии, капилляры, вены. В результате повышается проницаемость стенок сосудов, начинается выход белков, развивается гипоксия, возникает отек мозга.
Таким образом, нарушения мозгового кровообращения компенсируются до определенных пределов за счет местных регуляторных механизмов. Впоследствии в процесс вовлекается и общая гемодинамика. Однако даже при терминальных состояниях в течение нескольких минут за счет автономности мозгового кровообращения в мозге поддерживается кровоток, а напряжение кислорода падает медленнее, чем в других органах, так как нервные клетки способны поглощать кислород при таком низком парциальном давлении его в крови, при котором другие органы и ткани поглощать его не могут. По мере развития и углубления процесса все более нарушаются взаимоотношения между мозговым кровотоком и системной циркуляцией, иссякает резерв ауторегулирующих механизмов, и кровоток в мозге все больше начинает зависеть от уровня общего АД.
Таким образом, компенсация нарушений мозгового кровообращения осуществляется при помощи тех же, функционирующих в нормальных условиях, регуляторных механизмов, но более напряженных.
Для механизмов компенсации характерна двойственность: компенсация одних нарушений вызывает другие циркуляторные расстройства, например, при восстановлении кровотока в ткани, испытавшей дефицит кровоснабжения, в ней может развиться постишемическая гиперемия в виде избыточной перфузии, способствующей развитию постишемического отека мозга.
Конечной функциональной задачей системы мозгового кровообращения являются адекватное метаболическое обеспечение деятельности клеточных элементов мозга и своевременное удаление продуктов их обмена, т.е. процессы, протекающие в пространстве микрососуд – клетка. Все реакции мозговых сосудов подчинены этим главным задачам. Микроциркуляция в головном мозге имеет важную особенность: в соответствии со спецификой его функционирования активность отдельных областей ткани меняется почти независимо от других областей ее, поэтому микроциркуляция также меняется мозаично – в зависимости от характера функционирования мозга в тот или иной момент. Благодаря ауторегуляции перфузионное давление микроциркуляторных систем любых частей мозга менее зависит от центрального кровообращения в других органах. В мозге микроциркуляция усиливается при повышении уровня метаболизма и, наоборот. Те же механизмы функционируют и в условиях патологии, когда имеет место неадекватность кровоснабжения ткани. При физиологических и патологических условиях интенсивность кровотока в микроциркуляторной системе зависит от величины просвета сосудов и от реологических свойств крови. Однако регулирование микроциркуляции осуществляется в основном путем активных изменений ширины сосудов, в то же время при патологии важную роль играют также изменения текучести крови в микрососудах.
Среди соматических органов головной мозг особенно чувствителен к гипоксии и наиболее уязвимый в случае ишемии по нескольким причинам: во-первых, в связи с высокими энергетическими потребностями ткани мозга, во-вторых из-за отсутствия тканевого депо кислорода; в-третьих - в связи с отсутствием резервных капилляров. Если величина мозгового кровотока снижается до 35-40 мл на 100 г вещества мозга в 1 мин, то из-за наступающего дефицита кислорода нарушается расщепление глюкозы, а это приводит к накоплению молочной кислоты, развитию ацидоза, к гемореологическим и микроциркуляторным нарушениям, возникновению обратимого неврологического дефицита.
Регуляция мозгового кровообращения обеспечивается комплексом миогенного, метаболического и неврогенного механизмов.
Мишенный механизм заключается в том, что повышение АД приводит к сокращению мышечного слоя сосудов, и наоборот, снижение АД вызывает снижение тонуса мышечных волокон и расширение просвети сосудов (эффект Остроумова-Бейлиса). Миогенный механизм может осуществляться во время колебания среднего АД в диапазоне 60-70 и 170 180 мм рт. ст. Если АД снижается до 50 мм рт. ст. или возрастает выше чем до 180 мм рт.ст. появляется пассивная зависимость АД - мозговой кровоток, т. е. возникает срыв реакции ауторегуляции мозгового кровообращения.
Какие же механизмы защищают головной мозг от избыточной перфузии? Оказывается, что такими механизмами являются рефлекторные изменения тонуса внутренних сонных и позвоночных артерий. Они не только регулируют объем крови, которая поступает в сосуды мозга, но и обеспечивают постоянство ее притока независимо от изменений уровня общего АД. Миогенная ауторегуляция тесно взаимосвязана с уровнем венозного давления и давления спинномозговой жидкости. Миогенный механизм ауторегуляции включается мгновенно, но он непродолжителен - от 1 с до 2 мин, а затем подавляется изменениями метаболизма.
Метаболический механизм ауторегуляции предусматривает тесную связь кровоснабжения мозга с его метаболизмом. Эту функцию обеспечивают артерии мягкой мозговой оболочки, которые широко разветвляются на поверхности мозга. Он осуществляется гуморальными факторами и продуктами метаболизма ткани мозга. Однако ни миогенный, ни метаболический механизмы самостоятельно не могут обеспечить сложные процессы регуляции тонуса мозговых сосудов и поддерживать мозговой кровоток на постоянном уровне. По-видимому, механизмы ауторегуляции осуществляются за счет взаимодействия двух факторов: миогенного рефлекса сосудистой стенки в ответ на изменения перфузионного давления и действия таких метаболитов мозговой ткани, как 02 и С02, а также ионов калия, кальция, водорода.
В регуляции мозгового кровотока участвует также неврогенный механизм, но значение его окончательно не изучено.
Ауторегуляция мозгового кровообращения легко нарушаемый механизм, который может поражаться в результате гипоксии, гиперкапнии, резкого повышения или снижения АД. Срыв реакции ауторегуляции это состояние, при котором тканевый мозговой кровоток пассивно зависит от системного АД. Это может сопровождаться синдромами избыточной перфузии (luxury perfusion syndrome) и реактивной гиперемии.
Читайте также:


