Основными клиническими симптомами при наследственных полиневропатиях являются
Виды наследственных полиневропатий. Амиотрофии. Лечение наследственных полиневропатий.
Выделяют два вида подобных невропатий: первый — наследственные моторные и сенсорные невропатии, второй — наследственные сенсорные и вегетативные невропатии.
Отдельные формы моторных и сенсорных невропатий ранее описывались как невральная амиотрофия Шарко — Мари, болезнь Рефсума и др. В настоящее время на основании результатов физиологических и гистологических исследований выделено семь типов таких невропатий. Идентифицированы гены некоторых из них. Заболевания наследуются по аутосомно-доминантному и аутосомно-рецессивному типу, в их основе лежит поражение миелиновой обкладки периферических нервов (миелинопатия) либо аксонов (аксонопатия).
Заболевания дебютируют обычно в детстве, имеют хроническое прогредиентное течение и характеризуются сочетанием сенсорных (дистальные парестезии, боль, нарушение чувствительности) и моторных (дистальные вялые парезы) нарушений.
Наиболее распространены полиневропатии I и II типов с медленным прогредиентным течением, поражением мышц пальцев ног, что ведет к деформации стопы (полая стопа), болыпеберцовых и малоберцовых мышц (конская стопа, степаж), а позднее и икроножных мышц.
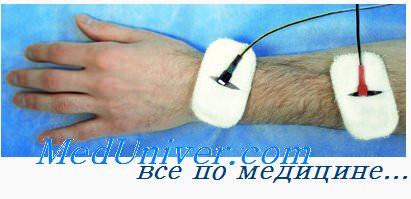
Ввиду дистальной локализации поражения (амиотрофии), ноги напоминают перевернутые бутылки. Деформации могут завершаться развитием контрактур. Нередки утолщения нервных стволов, в частности, малоберцового и большого ушного нервов (форма описана в свое время как гипертрофический неврит Дежерина — Сотта).
Другие формы имеют своеобразные клинические проявления. Например, при IV типе (гередитарная атактическая невропатия, или болезнь Рефсума) отличается сочетанием с мозжечковыми и другими признаками (пигментный ретинит, гемералопия, катаракта и др.), при V типе — с симптомами поражения пирамидной системы (нижний спастический парапарез) и др.
Важнейшим диагностическим признаком моторных и сенсорных полиневропатий является снижение скорости проведения по соответствующим нервам.
Формы с исключительно двигательными проявлениями иногда приходится дифференцировать с дистальными формами прогрессирующей мышечной дистрофии. При последних отсутствуют расстройства чувствительности, а скорость проведения по нервам не снижена.
В сомнительных случаях помочь может биопсия нервов — гистологические изменения в них при прогрессирующей мышечной дистрофии отсутствуют.
Генетическое консультирование членов семей больных одинаково необходимо как в сомнительных случаях, так и в явных.
Лечение возможно лишь у тех больных, у которых обнаружен специфический биохимический дефект. Например, при болезни Рефсума, в основе которой лежит нарушение обмена фитановой кислоты, необходимо соблюдение диеты с ограничением прекурса фитановой кислоты — фитана; при резком ухудшении заболевания применяется плазмаферез. В остальных случаях применяют массаж, ЛФК, ортопедическую коррекцию.
Что такое "Наследственные полинейропатии"?
Наследственные полинейропатии – это большая группа клинически разнообразных полинейропатий с возможным вовлечением различных органов и систем, в том числе и центральной нервной системы, которые развиваются в результате мутаций (поломок) в генах человека.
Какие мифы существуют среди населения относительно наследственных заболеваний?
- "Наследственные заболевания развиваются с рождения или в раннем детстве"
Это не так - дебют наследственной болезни возможен и во взрослом возрасте, в том числе и после 50 лет. Более того, зачастую пациенты не могут точно назвать возраст начала заболевания, так как симптомы развиваются незаметно. - "Наследственная патология должна быть и у близких родственников. А если в роду ни у кого нет, значит и у меня тоже нет".
Это не так - наследственные заболевания передаются разными путями: по аутосомно-доминантному, аутосомно-рецессивному, Х-сцепленному типу, также возможен митохондриальный тип наследования и др. Часто в семье есть асимптомные носители мутантного гена без клинических признаков заболевания, а симптомы болезни могут быть только у одного из членов семьи. Поэтому отсутствие отягощенного семейного анамнеза не исключает наследственный генез заболевания.

Какие бывают "Наследственная полинейропатии"?
Наследственных полинейропатий очень много, причиной из развития могут быть мутации более чем в 100 генах. Классифицируют наследственные нейропатии в основном по типу наследования, вовлечению тех или иных нервных волокон и характеру их поражения.
Ниже представлена лишь часть из них, преимущественно тех, которые на практике могут диагностироваться в возрасте старше 20 лет:
- Наследственные моторно-сенсорные нейропатии (НМСН)
- Наследственная нейропатия со склонностью к параличам от сдавления (ННСПС)
- Наследственные сенсорные и автономные нейропатии (НСАН)
- Болезнь Фабри
- Транстиретиновая семейная амилоидная нейропатия (ТТР-САП)

Как часто диагностируются наследственные полинейропатии среди населения?
Частота встречаемости всех форм НМСН варьирует от 10 до 40 случаев на 100 000 населения в различных популяциях. На НМСН 1 типа приходится до 70% всех случаев НМСН. Распространенность ННСПС 2-5 случая на 100 000 населения. Болезнь Фабри - 1 случай на 40 000 - 60 000 мужчин. По примерным подсчетам в США встречаемость ТТР-САП составляет 1 случай на 100 000 человек. Следует отметить, что настороженность относительно дебюта наследственной патологии во взрослом возрасте среди врачей разных специальностей достаточно низкая, поэтому некоторые цифры распространенности могут быть занижены.
Какие симптомы наблюдаются у пациентов с наследственными полинейропатиями?
Наследственные заболевания периферических нервов очень разнообразны по клиническим проявлениям. Ниже представлены данные некоторых из них.
Наследственная моторно-сенсорная нейропатия (НМСН) I типа (болезнь Шарко-Мари-Тута) – наиболее часто диагностируемая (в том числе во взрослом возрасте) наследственная полинейропатия, в основе развития которой лежит дефект гена PMP22, в результате чего повреждается миелиновая оболочка периферических нервов. Заболевание чаще всего имеет аутосомно-доминантный тип наследования. Соотношение мужчин и женщин с НМСН 1 типа примерно равно. Симптомы заболевания появляются на первом десятилетии жизни в 75% случаев, в начале второго десятилетия реже - до 10-25%. Обычно чем позднее манифестирует заболевание, тем более благоприятно оно протекает.
Клиническая картина НМСН 1 типа:
- пациентов беспокоят болезненные спазмы мышц голеней (крампи), слабость и деформация стоп, изменение походки, затруднения при беге или подъеме по лестнице;
- постепенно слабость развивается в кистях, в результате чего появляются затруднения при застегивании пуговиц, открывании двери ключом и т.д. В целом руки вовлекаются не ранее чем через 10 лет после появления первых симптомов болезни;
- в меньшей степени беспокоит онемение кистей и стоп, часто эти изменения игнорируются пациентом.
Особенностью является наличие несоответствия жалоб пациента (они минимальны) и неврологического дефицита (он более выражен), т.к. пациент за длительный период прогрессирования заболевания привыкает к тем или иным нарушениям.
При осмотре обращает внимание наличие деформации стоп, контрактур ахилловых сухожилий.
Клиническая картина других типов НМСН и НСАН вариабельна и определяется генетическим дефектом.
Наследственная нейропатия со склонностью к параличам от сдавления (ННСПС) - также часто диагностируемая во взрослом возрасте наследственная нейропатия (дебютирует, как правило, на 2–3-м десятилетии жизни), обусловленная мутацией в гене PMP22, характеризуется повышенной "чувствительностью" периферических нервов к сдавлению в костно-фиброзных каналах (туннелях), что приводит к повторяющимся эпизодам компрессионных туннельных мононевропатий.
Возможно поражение любого периферического нерва, но чаще всего сдавлению подвергаются:
- лучевой нерв на уровне плеча (спиральный канал), при этом развивается слабость разгибателей кисти, кисть "висит" как плеть, возникает онемение наружного края предплечья и кисти;
- малоберцовый нерв на уровне коленного сустава (фибулярный канал), при этом развивается слабость разгибателей стопы, стопа начинает "шлепать", возникает онемение наружного края голени и стопы;
- локтевой нерв на уровне локтевого сустава (кубитальный канал), при этом развивается слабость межкостных мышц кисти, мышцы - отводящих мизинец и других, возникает онемение 4 и 5 пальцев кисти;
- срединный нерв на уровне запястья (карпальный канал), при этом развивается слабость мышц возвышения большого пальца, возникает онемение 1-3 пальцев кисти, характерен болевой синдром;
- и т.д. с развитием соответствующей клинической картины поражения того или иного нерва.
Степень поражения нерва (защемления в канале) может быть различной - от незначительной, когда беспокоит только онемение и парестезии, до более выраженной, когда помимо чувствительных нарушений развивается и слабость мышц.
Развитию симптомов, как правило, предшествует незначительная травма, нахождение длительное время в неудобной статической поза (на четвереньках, на корточках, облокотившись на локоть и др.), ношение неудобной одежды, непривычная физическая нагрузка и прочее.
Мышечная слабость, как правило, сохраняется в течение нескольких дней или недель, а затем сила мышц постепенно восстанавливается (в течение нескольких недель или месяцев). Эпизоды "защемлений" нервов имеют тенденцию к повторению (всего у пациентов может быть от 1 до 10 таких эпизодов). Следует учитывать, что часто лечащие врачи не задумываются о том, что причиной рецидивирующих (повторяющихся) туннельных невропатий – является наследственная патология, что приводит к поздней диагностике и неоправданным медицинским вмешательствам (операциям по поводу туннельных невропатий).
Болезнь Фабри - редкое генетическое заболевание, обусловленное мутацией гена GLA, картированного на длинном плече хромосомы Хq 22.1 и контролирующего структуру фермента альфа-галактозидазы А. Нередко начало заболевания отмечается в подростковом возрасте. Тип наследования - сцепленное с Х-хромосомой.
Клиническая картина:
- жгучая колющая боль в ладонях и стопах; острые приступы мучительной боли в кистях и стопах (кризы Фабри);
- нарушение потоотделения; непереносимость жары/холода;
- сыпь на коже (ангиокератомы);
- помутнение роговицы в виде завитка, которое не ослабляет зрение;
- шум в ушах, потеря слуха;
- желудочно-кишечные расстройства, диарея;
- кардиологические проявления (включая увеличенное сердце и нарушение ритма);
- нарушение функции почек, которое в конечном итоге приводит к терминальной стадии хронической почечной недостаточности;
- нарушение мозгового кровообращения (чаще ишемический инсульт, но может быть и внутримозговое кровоизлияние, или венозный тромбоз).
Транстиретиновая семейная амилоидная полинейропатия (ТТР-САП) – редкое, прогрессирующее, аутосомно-доминантное заболевание, характеризующееся отложением мутантного амилоидного белка транстиретина (TTR) в тканях сердца, кишечника, стекловидного тела и периферических нервов. Заболевание обусловлено точковой мутацией в гене TTR, который кодирует одноименный белок. Симптоматика и степень выраженности нарушений чрезвычайно полиморфны.
Существуют “красные флаги” заболевания: отягощенный семейный анамнез, автономные нарушения (ортостатическая гипотензия, эректильная дисфункция, нарушение потоотделения), нарушение работы органов пищеварительного тракта (запоры, диарея, тошнота) и мочеиспускания, поражение сердца (рестриктивная кардиомиопатия, аритмии, блокады сердца), синдром карпального канала (идиопатический, часто двусторонний), потеря массы тела, помутнение стекловидного тела, прогрессирующая полинейропатия:
-
при раннем дебюте заболевания (
Под хронической демиелинизирующей полинейропатией подразумевают все те случаи заболевания, которые имеют подострое начало и хроническое, свыше двух месяцев, течение, характеризующееся обострениями и ремиссиями. К наиболее распространённым аутоиммунным полиневропатиям относятся острая и хроническая воспалительные демиелинизирующие полирадикулоневропатии. Наследственные полинейропатии представлены неоднородной группой заболеваний. При одних синдромах они бывают единственным проявлением мутации гена, а при других — это одно из проявлений мультисистемного заболевания.
Вид полинейропатии, локализацию и степень поражения тех или иных нервных волокон неврологи Юсуповской больницы устанавливают с помощью современных инструментальных и лабораторных диагностических методов.

Ведущие специалисты в области заболеваний периферической нервной системы проводят комплексную терапию полинейропатий, направленную на прекращение действия причинного фактора, механизмы развития патологического процесса и симптомы заболевания. Тяжёлые случаи полинейропатий профессора и врачи высшей категории обсуждают на заседании экспертного совета, коллегиально выбирают тактику дальнейшего ведения пациентов.
Больных полинейропатий госпитализируют в клинику неврологии в плановом порядке при обострении хронической воспалительной демиелинизирующей полинейропатии и нарастании очаговой неврологической симптоматики. Экстренной госпитализируют пациентов с впервые выставленным диагнозом. При наличии показаний (тяжёлой и крайне тяжелой степени неврологических расстройств, нестабильности гемодинамики, нарушении функции дыхания) пациентов переводят в отделение реанимации и интенсивной терапии.
Хроническая полинейропатия
Типичная форма хронической демиелинизирующей полинейропатии проявляется симметричной слабостью и чувствительными нарушениями во всех конечностях. Симптомы заболевания развиваются в течение более двух месяцев, сопровождаются отсутствием или снижением сухожильных рефлексов во всех конечностях. Иногда поражаются черепные нервы.
Атипичная форма заболевания протекает в виде следующих вариантов:
- асимметричного – сенсорные и двигательные нарушения не симметричные или располагаются в области иннервации отдельных нервов;
- фокального – двигательные и сенсорные нарушения локализуются в области иннервации пояснично-крестцового или плечевого сплетения, или же одного и более периферических нервов в одной нижней или верхней конечности;
- изолированного двигательного – определяются исключительно двигательные расстройства;
- изолированного сенсорного (включая хроническую иммунную сенсорную полирадикулопатию) – имеют место только чувствительные нарушения.
Хроническая воспалительная демиелинизирующая полинейропатия имеет 4 основных варианта течения: хронический монофазный, хронический рецидивирующе-ремиттирующий, ступенчато- прогрессирующий, неуклонно – прогрессирующий.
Пациенты предъявляют жалобы на слабость в дистальных или проксимальных отделах нижних конечностей, иногда асимметричную, онемение и чувство ползания мурашек в кистях и стопах, неустойчивость при ходьбе.
Первыми обычно поражаются нижние конечности. У пациентов затрудняется ходьба, подъём по ступенькам и из кресла, возникают падения. При вовлечении в патологический процесс верхних конечностей пациенты испытывают затруднения при пользовании кухонной утварью, захвате объектов, завязывании шнурков.
Выраженные парезы не сопровождаются нарастающей атрофией. Отмечается диффузное снижение тонуса мышц, снижение с последующим выпадением сухожильных рефлексов. Наиболее постоянно выпадает ахиллов рефлекс. В большинстве случаев заболевания отмечаются вегетативные нарушения:
- повышенная потливость кожи туловища, стоп и ладоней;
- преходящая сердечная аритмия с развитием обмороков;
- прогрессирующее уменьшение массы тела на 10-20 кг в течение года при нормальной температуре, отсутствии гипотиреоза и желудочно-кишечной дисфункции.
К отличительным клиническим признакам хронической воспалительной демиелинизирующей полинейропатии относят:
- преимущественно дистальный или смешанный (дистальный и проксимальный) характер неполных параличей конечностей;
- выраженную мышечную гипотонию и гипотрофию конечностей;
- более стойкие и частые вегетативные и чувствительные нарушения в руках.
Крайне редко присоединяются дыхательные и тазовые расстройства.
Неврологи назначают следующие лабораторные исследования:
- общий анализ крови;
- биохимические исследования крови на сахар, креатинин, мочевину, АСТ, АЛТ, билирубин, на электролиты;
- общий анализ мочи;
- исследование крови на гормоны щитовидной железы;
- определение антинуклеарных антител;
- полимеразную цепную реакцию крови на вирусы гепатита;
- исследование крови на ВИЧ-инфекцию;
- иммуноэлектрофорез сыворотки крови – исследование крови на белок, белковые фракции, моноклональный протеин;
- иммуноэлектрофорез мочи на моноклональный протеин, белок Бенс-Джонса.
Для исключения других видов полинейропатий и заболеваний внутренних органов, которые могут вызвать поражение периферических нервов, проводят инструментальные исследования:
- обзорную рентгенографию органов грудной клетки;
- ультразвуковое исследование органов брюшной полости, щитовидной железы;
- магнитно-резонансную томографию головного мозга;
- рентгенографию плоских костей;
- электронейромиографию (позволяет выявить признаки деструкции миелина и дегенерацию аксонов);
- игольчатую электромиографию – для того чтобы выявить признаки текущего денервационно-реиннервационного процесса при полинейропатии.
Амбулаторное лечение хронической воспалительной демиелинизирующей полинейропатии направлено на остановку процесса аутоиммунного воспаления и разрушения нервов, восстановление проводимости нервов, силы мышц и чувствительности, предотвращение повторных атак полинейропатии. Пациентам назначают глюкокортикоиды, иммуноглобулин и делают плазмаферез. Симптоматическая терапия при ХВДП включает препараты для купирования невропатических болей (габапентин, амитриптилин) и антихолинэстеразные препараты (неостигмин).
В клинике неврологии врачи предписывают больным хронической полинейропатией низкосолевую диету с высоким содержанием белка, но низким содержанием жира. Медицинский персонал обеспечивает адекватный уход с целью профилактики пролежней и контрактур.
Медикаментозная терапия в клинике неврологии складывается из патогенетического и симптоматического лечения. Патогенетическая терапия подразумевает использование иммуномодулирующих средств первой и второй линии. В качестве терапии первой линии используют глюкокортикоидные гормоны, иммуноглобулин человеческий нормальный для внутривенного введения, плазмаферез. В случае недостаточной эффективности средств первой линии применяют резервные препараты (средства второй линии) – азатиоприн, циклоспорин, циклофосфамид, метотрексат, микофенолата мофетил.
Реабилитологи проводят занятия лечебной физкультурой, делают массаж, отпускают физиотерапевтические процедуры для предотвращения формирования контрактур (электростимуляцию, теплолечение, лекарственный электрофорез). Эффективными методами лечения хронической полинейропатии являются иглорефлексотерапия и гипербарическая оксигенация.
Аутоиммунная полинейропатия
К аутоиммунным полинейропатиям относится острая воспалительная демиелинизирующая полирадикулоневропатия Гийена – Барре. Это заболевание периферической нервной системы, которое проявляется острым развитием периферических параличей и повышением концентрации белка в спинномозговой жидкости.
Причина болезни неизвестна. Иммунологические нарушения приводят к сегментарной демиелинизации в передних корешках и проксимальных (расположенных ближе к туловищу) отделах нервов конечностей и вегетативных узлов. У половины пациентов 1-3 недели до появления неврологических расстройств отмечаются заболевания верхних дыхательных путей, ангины, преходящие острые кишечные расстройства. Первыми неврологическими нарушениями являются боли и ощущение ползания мурашек в ногах или частичные параличи нижних конечностей. В дальнейшем двигательные расстройства в ногах прогрессируют, присоединяются нарушения движений верхних конечностей. Симптомы нарастают в течение первых 1-3 недель заболевания.
Определяются вялые параличи, которые часто распространяются в восходящем направлении, захватывают мышцы ног и тазового пояса, туловища, шеи, иногда дыхательную мускулатуру. Неврологи выявляют мышечную гипотонию, снижение или отсутствие рефлексов, незначительное снижение или повышение рефлексов в дистальных отделах конечностей, симптомы натяжения нервных стволов. У многих больных, имеющих выраженные двигательные нарушения, развиваются вегетативные расстройства: резкое снижение давления при вставании с постели, учащённого сердцебиения и пароксизмальной аритмии. При спинномозговой пункции выявляют белково-клеточную диссоциацию–повышение белка при незначительном увеличении клеток в ликворе. Во время электронейромиографии нейрофизиологи в 90% случаев выявляют снижение скорости проведения возбуждения по периферическим нервам.
Лечение аутоиммунной полинейропатии направлено на профилактику возможных осложнений. Персонал клиники неврологии обеспечивает профессиональный уход. При дыхательной недостаточности пациентам выполняют искусственную вентиляцию лёгких с помощью аппаратов ИВЛ экспертного класса, при нарушении глотания обеспечивают парентеральное питание. Восстановление ускоряет плазмаферез, начатый в первые 7 дней заболевания. Эффективно внутривенное медленное введение иммуноглобулина. Для профилактики тромботических осложнений используют гепарина. Реабилитологи проводят массаж нижних конечностей, занятия лечебной физкультурой.
Хроническая воспалительная демиелинизирующая полинейропатия также относится к аутоиммунным заболеваниям. Она проявляется симптомами, сходными с синдромом Гийена – Барре, но имеет хроническое, характеризующееся повторными периодами ослабления симптомов, или непрерывно прогрессирующее течение. В большинстве случаев причину заболевания установить не удаётся. Аутоиммунная полинейропатия может возникать при ВИЧ-инфекции, системной красной волчанке. В основе заболевания лежат расстройства иммунной системы. При невыясненной природе заболевания пациентам назначают преднизолон, азатиоприн, делают плазмаферез, внутривенно вводят иммуноглобулин.
Наследственная полинейропатия нижних конечностей
Неврологи выделяют полинейропатии с известной метаболической основой (наследственные амилоидозы, болезни обмена липидов, порфирии, заболевания, сопровождающиеся нарушением восстановления ДНК) и полинейропатии, при которых причина дефекта неизвестна (наследственные моторно-сенсорные, наследственные сенсорные и вегетативные полинейропатии, нейропатия с наследственными атаксиями и смешанные формы заболевания). Полинейропатия может наследоваться по доминантному или рецессивному типу.
Наследственно обусловленные полинейропатии рассматривают как системные заболевания, для которых характерно поражение нескольких органных систем. Нарушение обмена веществ имеет место при следующих наследственных полинейропатиях:
- метахроматической лейкодистрофии (нарушение клеточного метаболизма сульфатидов в клетках олигодендроглии центральной нервной системы и в шванновских клетках периферических нервов;
- болезни Фабри (гликосфинголипидозе);
- атактической полиневритоподобной гередопатии;
- болезни Бассена-Корнцвейга.
Специфического лечения наследственных полинейропатий нижних конечностей не существует. Слабость стопы корригируют с помощью фиксации или ортопедической операции. Подготовку молодых пациентов к прогрессированию заболевания проводит медицинский психолог. Пройти диагностику и курс лечения хронической, аутоиммунной и наследственной полинейропатии можно в клинике неврологии, записавшись на приём к неврологу по телефону Юсуповской больницы.
Полиневропатии — гетерогенная группа заболеваний, характеризующаяся системным поражением периферических нервов. Полиневропатии подразделяются на первично аксональные и первично демиелинизирующие. Независимо от типа полинейропатии ее клиническая картина характеризуется развитием мышечной слабости и атрофии, снижением сухожильных рефлексов, различными нарушениями чувствительности (парестезиями, гипо- и гиперестезией), возникающими в дистальных отделах конечностей, вегетативными расстройствами. Важным диагностическим моментом при установлении диагноза полиневропатии является определение причины ее возникновения. Лечение полинейропатии носит симптоматический характер, основной задачей является устранение причинного фактора.
- Этиология и патогенез полиневропатий
- Классификация полиневропатий
- Клиническая картина полиневропатии
- Диагностика полиневропатий
- Лечение полиневропатий
- Прогноз при полиневропатии
- Цены на лечение
Общие сведения
Полиневропатии — гетерогенная группа заболеваний, характеризующаяся системным поражением периферических нервов. Полиневропатии подразделяются на первично аксональные и первично демиелинизирующие. Независимо от типа полинейропатии ее клиническая картина характеризуется развитием мышечной слабости и атрофии, снижением сухожильных рефлексов, различными нарушениями чувствительности (парестезиями, гипо- и гиперестезией), возникающими в дистальных отделах конечностей, вегетативными расстройствами. Важным диагностическим моментом при установлении диагноза полиневропатии является определение причины ее возникновения. Лечение полинейропатии носит симптоматический характер, основной задачей является устранение причинного фактора или компенсация основного заболевания.

Этиология и патогенез полиневропатий
Независимо от этиологического фактора при полиневропатиях выявляют два типа патологических процессов — поражение аксона и демиелинизацию нервного волокна. При аксональном типе поражения возникает вторичная демиелинизация, при демиелинизирующем поражении вторично присоединяется аксональный компонент. Первично аксональными являются большинство токсических полиневропатий, аксональный тип СГБ, НМСН II типа. К первично демиелинизирующим полиневропатиям относятся классический вариант СГБ, ХВДП, парапротеинемические полиневропатии, НМСН I типа.
При аксональных полиневропатиях страдает главным образом транспортная функция осевого цилиндра, осуществляемая аксоплазматическим током, который несет в направлении от мотонейрона к мышце и обратно ряд биологических субстанций, необходимых для нормального функционирования нервных и мышечных клеток. В процесс вовлекаются в первую очередь нервы, содержащие наиболее длинные аксоны. Изменение трофической функции аксона и аксонального транспорта приводит к появлению денервационных изменений в мышце. Денервация мышечных волокон стимулирует развитие сначала терминального, а затем и коллатерального спраутинга, роста новых терминалей и реиннервацию мышечных волокон, что ведет к изменению структуры ДЕ.
При демиелинизации происходит нарушение сальтаторного проведения нервного импульса, в результате чего снижается скорость проведения по нерву. Демиелинизирующее поражение нерва клинически проявляется развитием мышечной слабости, ранним выпадением сухожильных рефлексов без развития мышечных атрофий. Наличие атрофий указывает на дополнительный аксональный компонент. Демиелинизация нервов может быть вызвана аутоиммунной агрессией с образованием антител к различным компонентам белка периферического миелина, генетическими нарушениями, воздействием экзотоксинов. Повреждение аксона нерва может быть обусловлено воздействием на нервы экзогенных или эндогенных токсинов, генетическими факторами.
Классификация полиневропатий
На сегодняшний день общепринятой классификации полиневропатий не существует. По патогенетическому признаку полиневропатии разделяют на аксональные (первично поражение осевого цилиндра) и демиелинизирующие (патология миелина). По характеру клинической картины выделяют моторные, сенсорные и вегетативные полиневропатии. Однако в чистом виде эти формы наблюдаются весьма редко, чаще выявляют сочетанное поражение двух или трех видов нервных волокон (моторно-сенсорные, сенсорно-вегетативные др.).
По этиологическому фактору полиневропатии разделяют на наследственные (невральная амиотрофия Шарко-Мари-Тута, синдром Русси-Леви, синдром Дежерина-Сотта, болезнь Рефсума и пр.), аутоиммунные (синдром Миллера-Флешера, аксональный тип СГБ, парапротеинемические полиневропатии, паранеопластические невропатии и др.), метаболические (диабетическая полинейропатия, уремическая полиневропатия, печеночная полинейропатия и др.), алиментарные, токсические и инфекционно-токсические.
Клиническая картина полиневропатии
Приобретенные демиелинизирующие полиневропатии могут проявляться проксимальной мышечной слабостью. При тяжелом течении может отмечаться поражение ЧН и дыхательных мышц, что чаще всего наблюдается при синдроме Гийена-Барре (СГБ). Для полиневропатий характерна относительная симметричность мышечной слабости и атрофии. Асимметричные симптомы характерны для множественных мононевропатий: мультифокальной моторной невропатии, мультифокальной сенсомоторной невропатии Самнера-Льюиса. Сухожильные и периостальные рефлексы при полиневропатии обычно снижаются или выпадают, в первую очередь снижаются рефлексы ахиллова сухожилия, при дальнейшем развитии процесса — коленные и карпорадиальные, сухожильные рефлексы с двуглавых и трехглавых мышц плеча могут оставаться сохранными длительное время.
Нарушение вегетативных функций наиболее ярко проявляется при аксональных полиневропатиях, так как вегетативные волокна являются немиелизированными. Чаще наблюдают симптомы выпадения: поражение симпатических волокон, идущих в составе периферических нервов, проявляется сухостью кожных покровов, нарушением регуляции сосудистого тонуса; поражение висцеральных вегетативных волокон приводит к дизавтономии (тахикардия, ортостатическая гипотензия, снижение эректильной функции, нарушение работы ЖКХ).
Диагностика полиневропатий
При выявлении медленно прогрессирующей сенсомоторной полиневропатии, дебютировавшей с перонеальной группы мышц, необходимо уточнить наследственный анамнез, особенно наличие у родственников утомляемости и слабости мышц ног, изменений походки, деформации стоп (высокий подъем). При развитии симметричной слабости разгибателей кисти необходимо исключить интоксикацию свинцом. Как правило, токсические полиневропатии характеризуются, помимо неврологических симптомов, общей слабостью, повышенной утомляемостью и редко абдоминальными жалобами. Кроме того, необходимо выяснить, какие препараты принимал/принимает пациент для того, чтобы исключить лекарственную полиневропатию.
Медленно прогрессирующее развитие асимметричной слабости мышц — клинический признак мультифокальной моторной полиневропатии. Для диабетической полиневропатии характерна медленно прогрессирующая гипестезия нижних конечностей в сочетании с чувством жжения и другими проявлениями в стопах. Уремическая полиневропатия возникает, как правило, на фоне хронического заболевания почек (ХПН). При развитии сенсорно-вегетативной полиневропатии, характеризующейся жжением, дизестезиями, на фоне резкого уменьшения массы тела необходимо исключить амилоидную полиневропатию.
Для наследственных полиневропатий характерны преобладание слабости разгибателей мышц стоп, степпаж, отсутствие ахилловых сухожильных рефлексов, высокий свод стопы. В более поздней стадии заболевания отсутствуют коленные и карпорадиальные сухожильные рефлексы, развиваются атрофии мышц стоп, голеней. Поражение мышц, соответствующее иннервации отдельных нервов, без сенсорных нарушений характерно для множественной моторной полиневропатии. В большинстве случаев преобладает поражение верхних конечностей.
Сенсорные полиневропатии характеризуются дистальным распределением гипестезий. В начальных стадиях заболевания возможна гиперестезия. Сенсомоторные аксональные невропатии характеризуются дистальными гипестезиями и дистальной мышечной слабостью. При вегетативных полиневропатиях возможны как явления выпадения, так и раздражение вегетативных нервных волокон. Для вибрационной полиневропатии типичны гипергидроз, нарушения сосудистого тонуса кистей, для диабетической полиневропатии, напротив, сухость кожных покровов, трофические нарушения, вегетативная дисфункция внутренних органов.
При подозрении на полиневропатии, связанные с интоксикацией свинцом, алюминием, ртутью проводят анализы крови и мочи на содержание тяжелых металлов. Возможно проведение молекулярно-генетического анализа на все основные формы НМСН I, IVA, IVB типов. Проведение игольчатой электромиографии при полиневропатиях позволяет выявить признаки текущего денервационно-реиннервационного процесса. Прежде всего, необходимо исследовать дистальные мышцы верхних и нижних конечностей, а при необходимости и проксимальные мышцы. Проведение биопсии нервов оправдано только при подозрении на амилоидную полиневропатию (выявление отложений амилоида).
Лечение полиневропатий
При наследственных полиневропатиях лечение носит симптоматический характер. При аутоиммунных полиневропатиях цель лечения заключается в достижении ремиссии. При диабетической, алкогольной, уремической и других хронических прогрессирующих полиневропатиях лечение сводится к уменьшению выраженности симптоматики и замедлению течения процесса. Один из важных аспектов немедикаментозного лечения — лечебная физкультура, направленная на поддержание мышечного тонуса и предупреждение контрактур. В случае развития дыхательных нарушений при дифтерийной полиневропатии может потребоваться проведение ИВЛ. Эффективного медикаментозного лечения наследственных полиневропатий не существует. В качестве поддерживающей терапии используют витаминные препараты и нейротрофические средства. Впрочем, эффективность их до конца не доказана.
Лечение диабетической полиневропатии проводится совместно с эндокринологом, основной его целью является поддержание нормального уровня сахара крови. Для купирования болевого синдрома применяют трициклические антидепрессанты, а также прегабалин, габапентин, ламотриджин, карбамазепин. В большинстве случаев применяют препараты тиоктовой кислоты и витамины группы В. Регресс симптомов на ранней стадии уремической полиневропатии достигается нефрологами при коррекции уровня уремических токсинов в крови (программный гемодиализ, трансплантация почки). Из лекарственных средств применяются витамины группы В, при выраженном болевом синдроме — трициклические антидепрессанты, прегабалин.
Прогноз при полиневропатии
При хронической воспалительной демиелинизирующей полирадикулоневропатии прогноз на жизнь достаточно благоприятный. Летальность очень низкая, однако, полное выздоровление наступает очень редко. До 90% пациентов на фоне иммуносупрессивной терапии достигают полной либо неполной ремиссии. В то же время заболевание склонно к обострениям, применение иммуносупрессивной терапии может быть в виду ее побочных действий, приводящих к многочисленным осложнениям.
При наследственных полиневропатиях редко удается добиться улучшения состояния, так как заболевание медленно прогрессирует. Однако пациенты, как правило, адаптируются к своему состоянию и в большинстве случаев до самых поздних стадий заболевания сохраняют способность к самообслуживанию. При диабетической полиневропатии прогноз на жизнь благоприятный при условии своевременного лечения и тщательного контроля гликемии. Лишь в поздних стадиях заболевания выраженный болевой синдром способен значительно ухудшить качество жизни пациента.
Прогноз на жизнь при уремической полиневропатии полностью зависит от выраженности хронической почечной недостаточности. Своевременное проведение программного гемодиализа либо трансплантация почки способны привести к полному либо почти полному регрессу уремической полиневропатии.
Читайте также:


