Перспективы создания лекарства для лечения болезни гентингтона
Поделиться сообщением в
Внешние ссылки откроются в отдельном окне
Внешние ссылки откроются в отдельном окне
Британские врачи впервые смогли устранить врожденный дефект, приводящий к болезни Хантингтона, нейродегенеративного заболевания, поражающего головной мозг.
Экспериментальное лекарство, введенное в спинномозговую жидкость пациентов, без негативных последствий для них снизило уровень токсичного белка, поражающего нейроны головного мозга.
Группа исследователей Университетского колледжа Лондона утверждает, что появилась надежда на излечение от этой смертельной болезни.
Эксперты называют проведенные испытания крупнейшим за последние полвека прорывом в лечении нейродегенеративных заболеваний.
Болезнь Хантингтона (также хорея Гентингтона) - одно из самых тяжелых заболеваний подобного рода.
Основной синдром этой болезни - гиперкинез, то есть непроизвольные подергивания мышц. Такой больной не способен контролировать свою мимику, и создается впечатление, будто он постоянно кривляется.
Бывает также гиперкинез конечностей - непроизвольное сгибание и разгибание пальцев или скрещивание и разведение ног.
Заболевание сопровождается деменцией, поражение переходит на кору головного мозга.
Некоторые пациенты рассказывают, что болезнь Хантингтона по своим симптомам - это "Паркинсон, Альцгеймер и нарушение моторики в одном флаконе".
51-летний Питер Аллен, принявший участие в испытаниях лекарства, находится на ранних стадиях Хантингтона. "Вы впадаете в почти вегетативное состояние, это ужасный конец", - говорит он.
"Постепенная деградация"
Неизбежная гибель клеток головного мозга при болезни Хантингтона приводит к постепенной деградации организма: ухудшаются моторика, поведение, память и способность больного сохранять ясное сознание.
Болезнь Хантингтона часто поражает людей в расцвете лет - тридцатилетних и сорокалетних. Больные обычно умирают в течение 10-20 лет после появления первых симптомов.
В Британии около 8,5 тыс. человек поражено этой болезнью. Еще 25 тысяч человек заболеют, когда станут старше.
Болезнь Хантингтона вызвана наличием в ДНК дефектного гена, приводящего к образованию мутантного белка хантингтина.
Белок хантингтина необходим для развития мозга, и соответствующий ген есть в ДНК любого здорового человека. Однако дефектный ген синтезирует токсичный хантингтин, поражающий клетки мозга.
Если такой ген есть у одного из родителей, будущий ребенок наследует его в 50% случаев.
Лечение, примененное группой врачей Университетского колледжа Лондона, направлено на угнетение этого гена.
В ходе испытаний препарат ввели 46 пациентам в спинномозговую жидкость, процедура была проведена в лондонской Национальной клинике неврологии и нейрохирургии.
Врачи не были уверены в результатах эксперимента. Они опасались, что инъекции приведут к смертельно опасной форме менингита.
Но первые испытания на людях показали, что препарат безопасен для человека, пациенты его хорошо переносят, и, самое важное, в ходе лечения сокращается количество хантингтина в мозге.
"В течение почти 20-ти лет я наблюдала множество таких пациентов в нашей клинике, многие из них умерли, - говорит директор Центра по изучению болезни Хантингтона при Университетском колледже Лондона Сара Табризи. - Впервые у нас появилась надежда получить курс лечения, способный остановить или предотвратить развитие болезни Хантингтона".
Врачи, впрочем, пока осторожны в своих прогнозах. Потребуются длительные наблюдения за пациентами, чтобы определить, как в долгосрочной перспективе снижение уровня хантингтина влияет на развитие болезни.
Опыты на животных подсказывают, что улучшение состояния больного возможно. Некоторые моторные функции у животных восстанавливаются в ходе такого лечения.

Распространенность генетического заболевания хореи Гентингтона составляет порядка 10 случаев на 100 тысяч человек в мире. Выраженными признаками при диагнозе становятся нарушения в работе опорно-двигательного аппарата, судороги, резкие неосознанные рывки конечностей и ухудшение сознания. Лечение хореи Гентингтона (заболевание по типу нарушения белковой структуры генов) еще не создано, можно только медикаментозно уменьшать симптомы больного, а также способствовать сокращению двигательных расстройств.
Хорея Гентингтона, что это за болезнь
Хорея Гентингтона относится по своей типологии к нейродегенеративной болезни, во время которой у человека происходит удлинение повторов гена, который отвечает за белок гентингтин. До сих пор ученые не смогли однозначно установить функцию, выполняемую белком. Однако, в медицине существуют определенные нормы, которые указывают на длину триплетов (генов) у здорового человека.
Хорея Гентингтона, что это за болезнь с точки зрения сложной генетики человека? У здоровых людей количество повторений белка гентингтина колеблется в зависимости от возраста и других особенностей в организме в пределах 11 – 34 триплетов. При диагнозе хореи Гентингтона количество повторений начинается с показателя 37 и может достигать 100 триплетов. Этот дефект генов начинает проявляться не с рождения, а только после достижения человеком возраста 30-40 лет.
Заболевание хорея Гентингтона
Учеными доказано, что более чем у 90% пациентов во всем мире заболевание хорея Гентингтона диагностируется в возрасте 40-50 лет. Именно в этот период жизни у больного начинают активно проявляться все симптомы и признаки генного заболевания, которые невозможно остановить. В настоящее время такая болезнь считается неизлечимой, поскольку проявляется на фоне нарушения генетического строения головного мозга. Лечение хореи построено на принципе облегчения жизни пациенту, и уменьшения проявления симптомов, связанных с нарушением функций опорно-двигательного аппарата.
Во всем мире заболевание имеет разную продолжительность периода дожития человека после появления диагноза. Средний срок продолжительности жизни больного хореей Гентингтона составляет 15 лет. Такой длительный срок наблюдается лишь у людей, получающих постоянное консервативное лечение. Не более 7-9 лет проживают те больные, которые не получают должного лечения и не наблюдаются у специалистов.
Симптомы хореи Гентингтона
Чаще всего начало симптоматики проявляется у взрослых людей, достигших 30 летнего возраста, но всегда есть исключения и болезнь может начать развиваться раньше. Все симптомы проявляются слабо в самом начале заболевания и начинают прогрессировать со временем. Основные симптомы хореи Гентингтона выглядят следующим образом:
- Очень сложно диагностировать специфическое заболевание простому человеку или родственнику больного, поскольку на протяжении первых 6-12 месяцев хорея может просто напоминать повышенную суетливость человека или неусидчивость.
- После развития первых симптомов постепенно начинает возрастать интенсивность нарушений в работе опорно-двигательного аппарата.
- Даже при спокойном состоянии и без физических нагрузок человек может испытывать внезапные судороги верхних и нижних конечностей тела. Одним из симптомов становятся спазмы мышечной мускулатуры лица, которые проявляются при разговоре или выглядят, как гримасничество. Со временем начинает проявляться усиленная жестикуляция, становящаяся не к месту. Внимание и мышление становится рассеянным, спутанным и затруднённым.
- На прогрессирующей стадии развития болезни к симптомам добавляется неуверенная походка, напоминающая человека в странном танце. Это происходит из-за нарушения координации опорно-двигательного аппарата при нагрузках.
Признаки хореи Гентингтона
В отличие от симптомов болезни признаки хореи Гентингтона можно распознать только профессиональному врачу. В медицинской практике для постановки диагноза необходимо выявить у больного 3 группы характерных признаков нервных и психических расстройств. Они являются самыми распространенными, и начинают проявляться после нарушения у человека двигательных рефлексов. Нервно-психические признаки условно подразделяются на 3 подгруппы:
- признаки в нарушении познавательной функции, которые чаще всего затрагивают ориентацию в пространстве и зрительного осязания предметов. Появляющиеся проблемы мешают больному человеку нормально видеть изображение или картину, происходящую вокруг него. С каждым днем все сложнее становится распознать какие-либо схематичные рисунка, элементы на экране телевизора или буквы в газете;
- признаки, связанные с нарушением сознания или нарушение интеллектуальной функции больного. Появляются сбои в работе памяти, но это сказывается не на способности помнить информацию из прошлого, а на работоспособность мозга. Человек уже не может, как прежде, заниматься продуктивно несколькими делами. Появляются затруднения больного при планировании своего времени либо организации деятельности;
- признаки, проявляющиеся в нарушении эмоциональных и поведенческих функций. За больным могут замечать резкие порывы агрессии или раздражительности, которые не были ни чем вызваны. Практически половина пациентов страдает от депрессии, но сама этого не осознает.
Диагностика хореи Гентингтона
Если человек жалуется на вышеперечисленные симптомы, а родственники или близкие наблюдают у больного развитие всех признаков болезни, то диагностика хореи Гентингтона в первую очередь начинается с похода к врачу и назначения пациенту генетического исследования.
Диагностика позволит выявить у человека паталогический ген, который привел к развитию хореи Гентингтона. Только в этом случае можно говорить о подтверждении данного диагноза. Кроме генетического исследования, в качестве видов диагностики заболевания в медицинской практике применяют компьютерную и магнитно-резонансную томографию коры головного мозга.
Сложное генетическое исследование состоит анализа ДНК, по результатам которого врач может судить о наличии у человека аномального гена. Заболевание может передаваться по наследству, поскольку с вероятностью более 50% повторные гены передаются детям от одного из больных родителей.
Лечение хореи Гентингтона
Болезнь заключается в генетическом отклонении человека, поэтому в настоящее время не существует её специфического лечения. Все силы врачей могут быть направлены на поддержание психического равновесия человека, а также на устранение двигательных и поведенческих расстройств. Благодаря специальным медикаментозным препаратам, удается свести к минимуму проблемы с походкой человека или его нахождением в обществе.
Для лечения и предупреждения развития болезни хореи Гентингтона используют комплексное лечение, но только после проведенного анализа дезоксирибонуклеиновой кислоты и медицинского генетического консультирования. Мутантный ген не поддается лечению, и важно на начальных этапах развития болезни не спутать её с шизофренией, наследственной атаксией или же болезнью Альцгеймера. Именно для этого проводят анализ ДНК, поскольку при иных психических расстройствах число повторов тринуклеотидов не увеличивается.
Лекарство для лечения хореи Гентингтона
До сих пор в мире не существует какого-либо лекарства, которое смогло бы полностью излечить человека от хореи Гентингтона. Но вся суть лечения в современной медицине сводится к уменьшению симптоматики заболевания. Лекарство для лечения хореи Гентингтона, точнее для устранения расстройств, связанных с поведенческими и двигательными функциями, можно подобрать из 3 основных фармакологических групп рецептурных препаратов:
- Фенотозианы способствуют блокировке дофаминовых рецепторов в организме человека. Большинство препаратов из этой группы, например, Прометазин или Фторфеназин, заглушают работу гистаминовых и серотониновых рецепторов человека.
- Галоперидоловая группа препаратов направлена на уменьшение расстройств поведения. Препараты оказывают нейролептическое свойство, помогают заблокировать дофаминовые рецепторы в организме человека и частично восстановить поведенческие функции. Однако, на фоне приема сильнодействующих средств у больного очень часто развиваются такие побочные эффекты, как постоянная сонливость, проявление резких двигательных движений, не поддающихся самоконтролю больного и снижение мышечной мускулатуры всего тела.
- Группа бензодиазепинов в составе лекарственных препаратов назначается пациентам для уменьшения судорожных реакций организма. Кроме того, препараты на основе бензодиазепинов способствуют более хорошему сну пациента. Эффект от таких лекарств достигается за счет торможения рецепторов ГАМК (аминомасляной кислоты), которые стимулируются работой нервной системы.
Клиника лечения хореи Гентингтона
Лечение заболевания должно проводиться только под руководством и присмотром врачей психиатрической клиники. Генетически сложная болезнь в любое время может проявляться по-разному, поэтому важно не упустить момент начала появления симптомов. Клиника лечения хореи Гентингтона должна специализироваться на неврологических отклонениях у людей.
Медленно прогрессирующее заболевание нервной системы и коры головного мозга неизлечимо, но человек с таким диагнозом должен постоянно находиться под наблюдением специалиста, который сможет в экстренной ситуации правильно рассчитать и применить медицинский препарат. За больными людьми необходим бережный уход, а также присмотр таких врачей, как психиатры, неврологи, психологи, окулисты и ортопеды.
Клинические рекомендации при хорее Гентингтона
Список основных рекомендаций должен составлять индивидуально после осмотра больного человека психиатром и неврологом. Выделяются основные клинические рекомендации при хорее Гентингтона, которым необходимо придерживаться во время нахождения в стационаре или при нахождении пациента дома. Больной должен регулярно получать препараты, снижающие активность дофаминов коры головного мозга, доза при этом увеличивается каждые 3 дня.
Родителям, у одного из которых выявлено генетическое заболевание, не рекомендуется заводить детей. Вероятность наследования хореи Гентингтона превышает 50%, при наступлении беременности требуется провести анализ ДНК будущему ребенку. По статистике, люди с хореей Гентингтона чаще всего умирают от пневмонии, сердечной деятельности или других застойных процессов в организме, поэтому важно своевременно проводить лечение любых второстепенных заболеваний.
Круглосуточные бесплатные консультации:
Сегодня, по данным Гарвардского центра нейроисследований, только в США около 5 млн человек страдают от болезни Альцгеймера; 1 млн – от болезни Паркинсона; 400 тыс. – от рассеянного склероза; по 30 тыс. – от бокового амиотрофического склероза (болезнь Лу Герига) и болезни Гентингтона. Эти расстройства, относящиеся к группе нейродегенеративных заболеваний, плохо изучены, и для них отсутствуют эффективные способы лечения. Решить эту проблему может помочь инструмент редактирования генов – система CRISPR/Cas9, которая на сегодняшний день активно и успешно применяется в биологии и медицине
Рассмотрим эту проблему на примере болезни Гентингтона (другие названия – синдром Гентингтона, хорея Гентингтона или Хантингтона), проявляющейся такими симптомами, как нарастающая потеря двигательного контроля и психические расстройства. Несмотря на то, что генетическая мутация, вызывающая это заболевание, была выявлена более 20 лет назад, молекулярные механизмы его развития все еще до конца не выяснены, так же как не найдено эффективной терапии этой болезни.
Моделируем болезнь
Причина болезни Гентингтона – увеличение числа тринуклеотидных повторов CAG в гене НТТ, кодирующем белок гентингтин. В норме в этом гене содержится от 8 до 36 повторов, но, когда это число достигает 37 и более, начинается развитие заболевания. Триплет CAG кодирует аминокислоту глутамин. Соответственно, при болезни Гентингтона синтезируется гентингтин с удлиненной полиглутаминовой цепочкой. Такой белок имеет неправильную пространственную структуру и не может выполнять свою функцию в клетках, которая, кстати сказать, до сих пор точно неизвестна. Кроме того, в стриатуме, одном из отделов мозга, регулирующих мышечный тонус, мутантный белок формирует агрегаты, обладающие токсическим эффектом. При этом тяжесть протекания болезни напрямую зависит от числа повторов CAG.
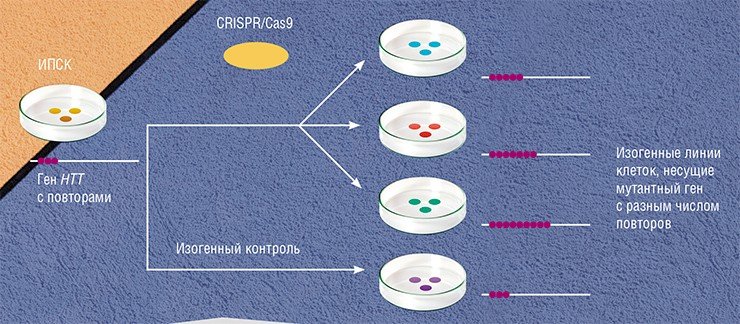
Для изучения болезни Гентингтона необходимо иметь клетки стриатума, но получить такой биоматериал затруднительно. Эта проблема решается с помощью индуцированных плюрипотентных стволовых клеток (ИПСК), которые достаточно легко с помощью перепрограммирования можно получить из клеток кожи или крови человека. Далее эти клетки можно наращивать в неограниченных количествах и дифференцировать (превращать) в практически любой нужный тип клеток.
Исследуем генное окружение
Несмотря на то, что болезнь Гентингтона является моногенным заболеванием, т. е. обусловлена мутацией в одном гене, известно более 100 так называемых генов-модификаторов, которые могут повлиять на время возникновения первых симптомов, тяжесть заболевания и т. д. Наиболее удобным инструментом для выяснения роли этих генов в патогенезе болезни Гентингтона является система GeCKO на основе CRISPR/Cas9 (Shalem et al., 2014). Она позволяет создавать целые библиотеки генных мишеней для CRISPR/Cas9 и выключать тысячи генов всего лишь за пару этапов. Таким образом, можно за короткий срок произвести нокаут (выключение) всех генов-модификаторов и выяснить, как это влияет на жизнеспособность клеток, скорость их деления и т. д.
Лечим?
CRISPR/Cas9 можно использовать и для лечения болезни Гентингтона. Есть два варианта воздействия: укорочение повторов CAG или специфическое выключение мутантной копии гена.
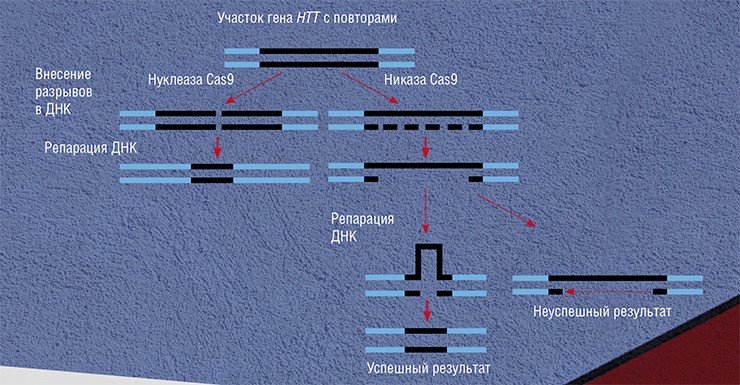
В первом случае с помощью CRISPR/Cas9 вносятся двунитевые разрывы в последовательность с повторами. Однако такое вмешательство имеет и обратный результат – увеличение числа повторов CAG. Проблема была решена путем использования никаз Cas9 – мутантных белков Cas9, которые вносят в ДНК однонитевые разрывы. Эксперимент показал, что последовательные однонитевые разрывы в регионах с повторами в худшем случае не изменяют длину участка с повторами, а в лучшем – приводят к его ожидаемому укорочению (Cinesi et al., 2016).
Исследования болезни Гентингтона с применением системы CRISPR/Cas9 сегодня проводятся и в России. Так, в лаборатории эпигенетики развития Института цитологии и генетики СО РАН (Новосибирск) ведутся работы по получению изогенных линий стволовых клеток, моделирующих болезнь Гентингтона, путем внесения удлиненных трактов CAG в нормальный ген НТТ, а также по дифференцировке ИПСК в нейроны стриатума. В дальнейшем новосибирские исследователи планируют перейти к изучению роли генов-модификаторов в патогенезе этой болезни с использованием клеточной модели.
Есть основания надеяться, что результаты исследований приведут к созданию эффективного метода лечения. Кроме того, они, возможно, помогут при изучении других нейродегенеративных заболеваний, развитие которых обусловлено подобной мутацией.
Медведев С. П. Как отредактировать наследственность // НАУКА из первых рук. 2014. Т. 55. № 1. С. 10—14.
Cinesi C., Aeschbach L., Yang B., Dion V. Contracting CAG/CTG repeats using the CRISPR-Cas9 nickase // Nat. Commun. 2016. V. 7. P. 13272—13281.
Shalem O., Sanjana N. E., Hartenian E. et al. Genome-scale CRISPR-Cas9 knockout screening in human cells // Science. 2014. V. 343. N. 6166. P. 84—87.
Shin J. W., Kim K.-H., Chao M. J., et al. Permanent inactivation of Huntington’s disease mutation by personalized allele-specific CRISPR/Cas9 // Hum. Mol. Genet. 2016. V. 25. N. 20. P. 4566—4576.

Общие сведения
Хорея, что за болезнь? Хорея (или хореический гиперкинез) — это непрерывные, быстрые, хаотичные движения. Гиперкинез вовлекает дистальные отделы рук и ног, мимические мышцы, мышцы гортани и туловища. Движения эти насильственные и напоминают гримасничанье, ужимки и кривляние. Гиперкинезы связаны с поражением структур головного мозга, объединяемых в экстрапирамидную систему. Эти двигательные расстройства значительно ограничивают возможности больного, приводя к социальной изоляции. Частыми формами хореи являются хорея Гентингтона и ревматическая хорея (синоним пляска Святого Витта и хорея Сиденгама), которые имеют различное происхождение и прогнозы.
Также к гиперкинезам, связанным с поражением экстрапирамидной системы, относятся кривошея, тремор, дистония, атетоз, тики, миоклония. Все эти состояния характеризуются гипотонико-гиперкинетическим синдромом — то есть сочетают гиперкинезы (непроизвольные, насильственные движения) и сниженный тонус мышц. Функция экстрапирамидной нервной системы состоит в создании условий для движений (распределение мышечного тонуса и подготовка мышц к движению) обеспечении позы и выполнении стереотипных рефлекторных движений. Все эти функции нарушаются при нарушении функции экстрапирамидной системы.
Патогенез
При данном заболевании имеет место преимущественное поражение базальных ганглиев головного мозга, которые имеют большое значение в контроле движения и поведения. Также снижается уровень нейромедиаторов (гамма-аминомасляной кислоты и субстанции Р). Данные нарушения возникают вследствие генных мутаций.
Ген хореи Гентингтона локализуется на четвертой хромосоме. Ген кодирует белок хантингтин (гентингтин), который необходим для развития и выживания клетки. В норме ген содержит цепочку из нуклеотидов цитозин-аденин-гуанин (CAG), которая повторяется. Число таких повторов в гене в норме от 8 до 35, а в мутагенном гене увеличивается количество повторов и это обуславливает болезнь Гентингтона. Поскольку триплет CAG кодирует аминокислоту глутамин, при этом заболевании глутамин накапливается в избытке и оказывает повреждающее действие. Чем больше CAG-копий, тем раньше развивается заболевание и больше выражены симптомы.
Классификация
Экстрапирамидные гиперкинезы бывают:
- Первичные (при различных нейродегенеративных заболеваниях, например, болезнь Гентингтона, нейроакантоцитоз, спиноцеребеллярная атаксия).
- Вторичные (симптом при аутоиммунных, сосудистых и метаболических заболеваниях, интоксикации тяжелыми металлами, энцефалитах различной этиологии).
По распространенности хореические гиперкинезы делятся на:
- Фокальные.
- Односторонние.
- Генерализованные.
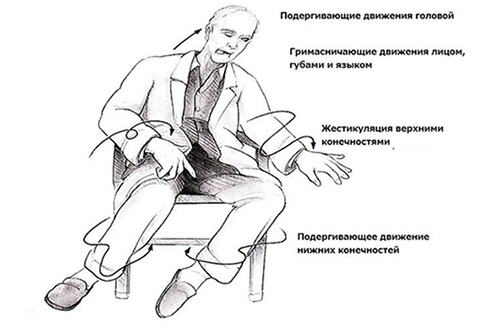
Уже на ранней стадии болезнь Гентингтона помимо двигательных расстройств появляется выраженное нарушение речи (замедленная аритмичная речь), расстройство глотания появляется на поздних стадиях и становится причиной аспирации, асфиксии и пневмонии. Изменения со стороны психической сферы представлены нарушением памяти, внимания, фобическими расстройствами и депрессией с суицидальными попытками.
Среди вторичных форм выделяется малая хорея (синоним хорея Сиденгама), которая является осложнением ревматизма. Это общепризнанный вариант ревматического поражения нервной системы, поэтому ревматическая хорея называется еще нейроревматизм. Первые описания эпидемии ревматической хореи сделаны в 1418 г., а полная характеристика болезни дана Сиденгамом через 200 лет. В 1831 г. Брайтом установлена связь малой хореи с ревматической лихорадкой и описаны тяжелые формы псевдопаралитической малой хореи.
В последние годы благодаря противоревматическому лечению хорея Сиденгама встречается очень редко, да и сам ревматизм ревматологи рассматривают как заболевание, теряющее свою актуальность. В начале 80-х годов нейроревматизм (пляска святого Витта) диагностировался у 36% детей с ревматизмом, а в настоящее время у 16% пациентов. При этом преобладает гемихорея (гиперкинезы одной стороны) и мышечная гипотония (умеренная и выраженная), нарушения координации, почерка и речи, повышение сухожильных рефлексов и эмоциональная лабильность.
Причины хореи Хантингтона
Причина данного заболевания — генетический дефект в четвертой хромосоме. Генетические причины хореи Хантингтона заключаются в изменении 4-й хромосомы, в которой увеличивается количество повторов одного из фрагментов ДНК, который кодирует белок гентингтин. Чем больше количество повторов, тем в более раннем возрасте развивается заболевание. Эти генетические причины и связанное с ними нарушение образования белка за счет полиглутаминовых повторов предопределяют гибель нейронов полосатого тела и хвостатого ядра.
Если говорить о вторичных формах хореи, то причинами их в детском возрасте могут быть ревматизм, системная красная волчанка, поражение сосудов (сосудистая хорея), антифосфолипидный синдром. У пожилых хорея может быть вызвана заболеваниями печени, инсультом, полицитемией. Хорея является самым частым постинсультным гиперкинезом и наблюдается у 1,3% пациентов с острым нарушением мозгового кровообращения. Хореический гиперкинез появляется остро в первые дни инсульта. Он чаще представлен гемихореей, а в случае двустороннего поражения сосудов — генерализованный. У большинства больных гиперкинез сочетается с мышечной слабостью этой же стороны.
Причиной сосудистой хореи является ишемическое или геморрагическое поражение таламуса, субталамического ядра и лентиформных ядер. Причиной сосудистой хореи также может стать поражение теменных, лобных или височных долей.
Симптомы хореи Гентингтона
Симптомы включают различные виды патологических движений. Они проявляются сначала в дистальных отделах конечностей, а затем становятся генерализованными, что нарушает выполнение обычных движений. Сначала у больных появляется неповоротливость, неуклюжесть, плохая координация движений и ухудшается почерк. Быстрые и беспорядочные движения в разных группах мышц связаны со снижением тормозного влияния головного мозга на двигательные нервы.
В 60% случаев до возникновения двигательных расстройств появляются психопатические нарушения.

Болезнь Гентингтона: симптомы и признаки, фото
Эмоциональные нарушения и повышенная возбудимость проявляются тем, что у больного появляются немотивированные приступы паники, ярости, тревоги. Также может развиться гиперсексуальность. Отмечаются нарушения сна.
Слабоумие развивается на поздних стадиях заболевания. Иногда развитие деменции приостанавливается, и оно далеко не всегда становится тотальным. Поэтому можно сказать, что слабоумие при хорее Гентингтона относительно доброкачественное. Некоторые больные могут долго выполнять привычную работу и оставаться вне психиатрической лечебницы. Расстройства интеллекта проявляются в снижении способности к мышлению, ослаблении внимания и отсутствии критики к своему поведению. Если рассматривать другие признаки, то нужно отметить высокую подверженность больных к депрессивным расстройствам и наклонность к суициду. Могут появиться бред и навязчивые состояния. Могут наблюдаться эпилептические приступы — чаще всего это встречается у больных с началом заболевания в молодом возрасте. Болезнь Хантингтона может сочетаться с сахарным диабетом. Поэтому у таких больных часто выявляют симптомы диабета: повышенная жажда, увеличение количества мочи, сухость во рту.
В зависимости от преобладания в клинике того или иного симптома, выделяют несколько клинических форм заболевания:
- Гиперкинетическая. Преобладает непроизвольное движение мускулатуры, усиливающееся при волнении. При ходьбе больные размахивают руками, пританцовывают, раскачиваются, гримасничают, издают посторонние звуки при разговоре. Гиперкинезы исчезают во сне. Со течением времени они нарастают и больные не способны обслуживать себя.
- Психическая форма. У больных на первый план выступают апатия, снижение критики, ухудшение памяти, возбуждение, бредовые идеи, возникают галлюцинации (слуховые и зрительные). Постепенно развивается деменция.
- Акинетико-ригидная форма. Эта форма проявляется мышечной ригидностью и контрактурами. Бывают приступы эпилепсии, атетоз (движения в дистальных отделах рук и ног), глазодвигательные нарушения, атаксия и дистония. Отмечаются также нарушение умственного развития.
Важное место занимают системные проявления ревматизма: одышка, сердцебиение в покое, увеличение печени, боли в суставах, наличие кольцевидной эритемы на коже. Поражения сердца (эндо— и миокардит) выявляется на ЭХО кардиографии: расширение отделов сердца, изменения клапанов сердца, дисфункция створок клапанов. То есть сочетается неврологическая симптоматика и признаки эндомиокардита.
Анализы и диагностика
- Синдром Хантингтона, как наследственное нейродегенеративное заболевание, нуждается в проведении медико-генетических обследований. Проводится генетическое тестирование — прямая ДНК-диагностика фрагментным анализом. Это дает возможность выявить носительство патологического гена у будущих родителей и дать точный прогноз в отношении здоровья потомства.
- МРТ и КТ выявляют атрофию хвостатого ядра, атрофию коры головного мозга (больше в лобной доле), но при генетически подтверждённом диагнозе эти обследования не имеют диагностического значения.
При исследовании больных с ревматической хореей выявляют:
- Лейкоцитоз.
- Нейтрофилез.
- Ускорение СОЭ.
- Увеличение С-реактивного белка и серомукоида.
- Повышение титров антистрептолизина О (от 1:500 до 1:1000).
- На ЭХО-КГ — увеличение размеров сердца, изменения клапанов.
Лечение хореи Гентингтона
Лечение при данном заболевании носит поддерживающий характер. Препаратами выбора при гиперкинезах являются нейролептики, которые блокируют дофаминовые рецепторы нейронов. Их применение позволяет частично подавить хорею и возбуждение (ажитацию) у больного.

Для лечения применяются типичные нейролептики Галоперидол, Пимозид, Модитен. Менее эффективными являются Сульпирид и Тиаприд, но они имеют меньше побочных действий, поэтому используются в виде препаратов выбора. Также широко применяются атипичные нейролептики — Рисперидон, Клозапин, Оланзапин, Арипипразол, Нормокинезтин. Нейролептики используются в низких дозах, а продолжительночть их применения ограничивается двумя неделями с постепенным уменьшением дозы и отменой.
Применение Нормокинезтина показано при хорее и отсутствии депрессии, агрессивного поведения или психоза. На поздних стадиях, когда развивается мышечная ригидность, препарат не показан, поскольку усиливает этот симптом. Арипипразол (нейролептик третьего поколения) обладает эффективностью сопоставимой с Нормокинезтином, но при этом в меньшей степени вызывает депрессию и седативный эффект.
При умеренном гиперкинезе нейролептики могут не назначаться, а больному рекомендуются препараты, блокирующие глутаматергические рецепторы (Амантадин, Мидантан, Мемантин Канон), антиконвульсанты (Топамакс, Топирамат) и симпатолитики (Резерпин). Также возможна комбинация нейролептик + антиглутаматергический препарат или антиконвульсант + симпатолитик. Существуют данные в пользу того, что длительный прием Мемантина и коэнзима Q10 несколько замедляет прогрессирование заболевания. Важно с помощью нейролептиков и антидепрессантов корригировать сопутствующие психические расстройства, прежде всего депрессию и вспышки агрессии.
При ревматической хорее комплексное лечение включает:
- Антибактериальную терапию (Пенициллин с переводом на формы длительного действия — Экстенциллин, Ретарпен, Бициллин-1, Бициллин-5).
- Противовоспалительную (Преднизолон до 10 дней с постепенным снижением дозы).
- Противоэпилептические препараты (Конвулекс, Депакин, Карбамазепин, Мазепин, Финлепсин). В случае, если они оказываются неэффективными, назначаются нейролептики в минимальной дозе.
- Физиотерапию (электросон, электрофорез с бромидом кальция, УВЧ по лобно-затылочной методике).
Читайте также:


