Штаммы вируса клещевого энцефалита
Среди переносчиков инфекционных заболеваний человека клещи занимают второе место после комаров: на сегодня выявлено не менее трех вирусных, 22 бактериальные и несколько протозойных инфекций, которые переносятся иксодовыми клещами. Ситуация зачастую осложняется тем, что при укусах клещи способны передавать человеку одновременно разные виды бактерий, вирусов и простейших, вызывая смешанные инфекции, часто протекающие в более тяжелых формах. Дополнительный риск заражения возникает из-за возможной циркуляции патогенов в сельскохозяйственных и домашних животных (например, инфекционные агенты могут сохраняться в молочных продуктах), а также при переливаниях крови и трансплантации органов. Наиболее опасными среди инфекций, переносимых клещами, считаются клещевой энцефалит, иксодовый клещевой боррелиоз, эрлихиоз, риккетсиоз и бабезиоз. Для России наиболее социально значимыми инфекционными агентами являются боррелии и конечно же вирус клещевого энцефалита, о котором пойдет речь ниже.
Таежная инфекция
В 30-х гг. XX в. шло интенсивное освоение Дальнего Востока: строились дороги, вырубались леса, из-за напряженных отношений с Японией в тайге дислоцировались крупные военные части. Врачи, работавшие в то время в Приморском крае, стали регулярно сообщать о неизвестной тяжелой болезни, поражающей как местных жителей, так и военных. Заболевание, считавшееся новой разновидностью тяжелого гриппа, сопровождалось резким повышением температуры и часто приводило к параличам и даже гибели заболевших.
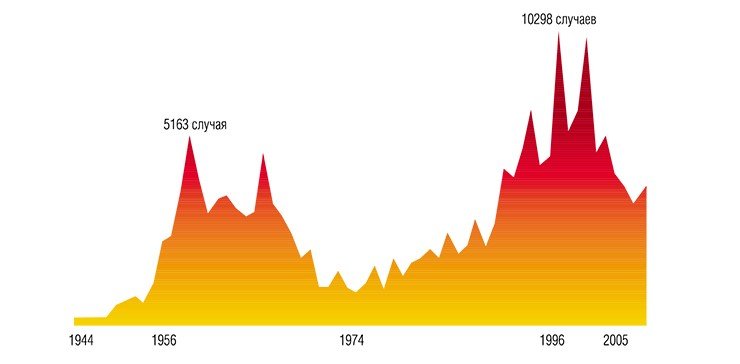
Правильно диагностировать неизвестную болезнь удалось лишь в 1935 г. местному врачу А. Г. Панову. Заболевание оказалось воспалением мозга, т. е. энцефалитом, похожим по симптомам на описанный ранее японский энцефалит. В 1936 г. врачи дальневосточной пастеровской станции пытались выделить возбудителя заболевания, вводя мышам в мозг эмульсию мозга людей, погибших от энцефалита. Но, несмотря на то, что у мышей появлялись признаки заболевания, исследования не увенчались успехом.
В январе 1937 г. военные медики обратились в Наркомздрав СССР, где и было принято решение об организации на Дальний Восток научной экспедиции под руководством Л. А. Зильбера. В тяжелых полевых условиях была развернута настоящая вирусологическая лаборатория. Ученые свою задачу выполнили: патоген, вызывающий тяжелые заболевания центральной нервной системы, был успешно выделен и описан. Кроме того, была четко установлена определяющая роль иксодовых клещей в передаче инфекционного агента. Выяснилось, что источником заражения клещей служили дикие позвоночные животные, на основе чего были разработаны рекомендации по необходимым профилактическим мерам.
К сожалению, это поистине блестящее открытие, ставшее важной вехой в истории вирусологии, не обошлось без жертв среди самих участников научной экспедиции. Так, М. П. Чумаков – будущий академик и создатель Института по изучению полиомиелита – перенес тяжелейшую форму инфекции, перешедшую у него в хроническую пожизненную форму; последствием заболевания у В. Д. Соловьева стала шестимесячная слепота.
Опасный сосед
Что на сегодня известно о вирусе клещевого энцефалита (ВКЭ)? Вирус относится к достаточно старому в эволюционном плане семейству флавивирусов (Flaviviridae), включающему более 70 вирусов животных и человека, в том числе такие опасные, как вирус желтой лихорадки, японского энцефалита, вирус лихорадки Денге и вирус гепатита C.

Лев Александрович ЗИЛЬБЕР (1894—1966) – один из основоположников медицинской науки в СССР. С его именем связаны фундаментальные исследования изменчивости у бактерий и природы иммунитета, организация первых в стране вирусологических центров, создание и экспериментальная разработка вирусо-генетической теории происхождения опухолей, а также совершенно нового направления – иммунологии рака.
За работу по выявлению возбудителя и переносчика весенне-летнего энцефалита в 1937 г. был награжден премией Наркомздрава СССР, но в том же году арестован по ложному обвинению, что экспедиция, которую возглавлял Зильбер, тайно распространяла японский энцефалит на Дальнем Востоке, и освобожден лишь через полтора года. В короткий промежуток времени между освобождением и новым арестом работал над монографией об эпидемических энцефалитах, подготовил несколько статей.
Основным природным резервуаром ВКЭ служат мелкие млекопитающие (полевки, мыши, насекомоядные). Вирус способен заражать животных и размножаться в их организме, однако заболевание протекает у них зачастую без видимого вреда для здоровья. Переносчиками вируса являются клещи, питающиеся кровью лесных зверьков, – европейский лесной клещ, таежный, луговой клещи, а также ряд других, более редко встречающихся видов. ВКЭ может размножаться и в их организме. Точно не известно, был ли вирус первоначально связан только с клещами, или только с позвоночными животными, но в процессе эволюции он приспособился к существованию в организмах как тех, так и других.
В настоящее время вирус клещевого энцефалита встречается в лесных регионах по всей территории Евразии от Атлантического океана до Тихого, причем в целом область его распространения совпадает с ареалами европейского лесного и таежного клещей. В последние десятилетия ареал ВКЭ неуклонно расширяется, что связано с усилением хозяйственной деятельности человека. Так, заброшенные лесные вырубки зарастают мелкими кустарниками и заболачиваются, что создает идеальные условия для обитания мелких млекопитающих и связанных с ними клещей.
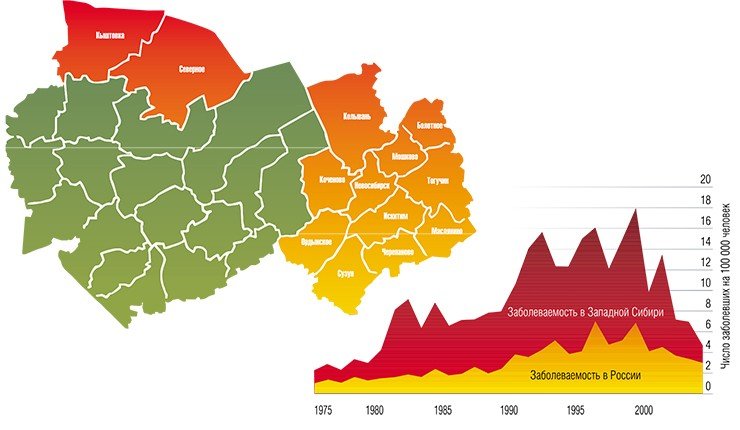
Кроме того, все большее число людей предпочитает проводить свободное время на природе, отдыхая или работая на приусадебных участках. В той же Новосибирской области около 75% населения проживает на территории, условия которой благоприятны для жизни клещей, здесь же сосредоточена и основная масса летних оздоровительных учреждений, зон массового отдыха, садово-дачных участков.
В Институте химической биологии и фундаментальной медицины были исследованы 95 штаммов вируса клещевого энцефалита из коллекции Института систематики и экологии животных СО РАН, выделенных от взрослых особей таежного клеща, собранных с растительности в восточной части Новосибирской области в 1980—2001 гг.
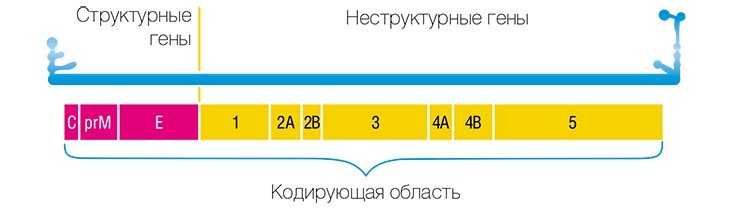
Анализ нуклеотидных последовательностей фрагмента гена Е, кодирующего белок оболочки вируса, показал, что все штаммы соответствуют сибирскому генетическому типу.
С другой стороны, в крови людей, госпитализированных с подозрением на клещевые инфекции, в совместных исследованиях с новосибирскими медиками были обнаружены изоляты ВКЭ, относящиеся к дальневосточному генетическому типу.
Ранее считалось, что этот тип вызывает только тяжелые формы заболевания, тогда как сибирский – преимущественно хронические. Наши исследования, подтвержденные данными других авторов, показали, что вирус дальневосточного генетического типа способен вызывать различные формы клещевого энцефалита, начиная от самых тяжелых и заканчивая стертыми, никак не проявляющимися.
Геном вируса клещевого энцефалита был расшифрован в 1989—1990 гг. практически одновременно в нашей стране (в том числе и в Институте химической биологии и фундаментальной медицины СО РАН (Pletnev et al., 1990)) и за рубежом (Mandl et al., 1989). На сегодня выделено три генетических типа вируса, различающихся по своим свойствам: дальневосточный, сибирский и западноевропейский. Такая привязка генетического типа к географическому местоположению достаточно условна, поскольку в одном регионе могут встречаться штаммы, относящиеся к разным типам.
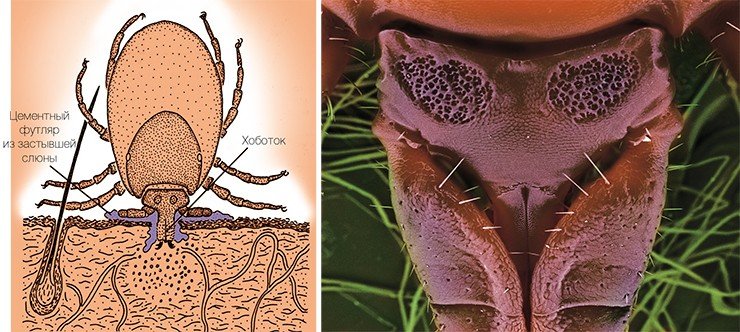
Для вируса клещевого энцефалита, как и для большинства других вирусных инфекций, не существует высокоспецифических методов лечения – в этом заключается его опасность. Лечение всех вирусных заболеваний направлено в основном на стимуляцию иммунитета и устранение внешних симптомов заболевания, а дальше организм должен сам справляться с инфекцией. ВКЭ опасен еще и тем, что способен вызывать хронические формы заболевания, а его последствиями могут быть параличи и инвалидность. Поэтому важнейшим делом в исследовании этого инфекционного агента является разработка методов диагностики и профилактики заболевания.
Диагностика и профилактика
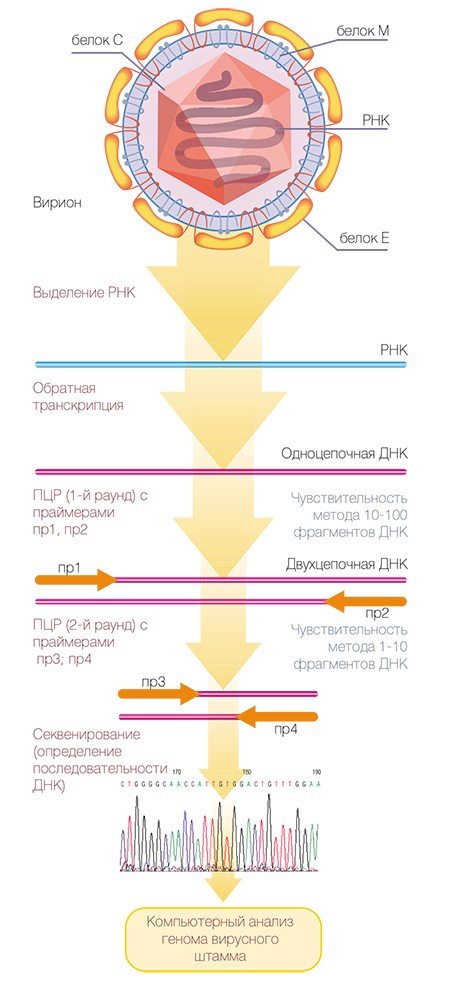
В клинической диагностике вируса клещевого энцефалита наиболее распространены серологические методы, с помощью которых в крови пациента определяют наличие антител, специфических защитных белков, или наличие самого агента. Однако чувствительность этих методов не слишком высока, к тому же существует вероятность ошибки из-за возможных перекрестных реакций с другими патогенами. Кроме того, с их помощью невозможно получить подробную характеристику самого возбудителя (например, определить его генетический тип).
Молекулярно-генетические методы, направленные на специфическое распознавание генетического материала вируса, обладают более высокой чувствительностью. Особенно это относится к методу полимеразной цепной реакции** (ПЦР), благодаря которой можно размножить, а потом идентифицировать ничтожное количество наследственного материала вируса, что позволяет провести диагностику в течение первых дней после заражения. Однако при некоторых обстоятельствах достоинства могут переходить в недостатки: генодиагностика ВКЭ молекулярно-генетическими методами благодаря высокой чувствительности может также приводить к ошибкам, обусловленным многочисленными новыми мутациями вирусных геномов, а кроме того, предъявляет высокие требования к чистоте экспериментов.

Живые вакцины
Живые вакцины – способ стимуляции иммунитета введением в организм ослабленных вирусов, открытый еще в 1796 г. английским врачом Э. Дженнером. С тех пор была получена живая вакцина против вируса желтой лихорадки, отличающаяся от высокопатогенных штаммов многочисленными заменами нуклеотидов в геноме; продолжаются поиски ослабленных штаммов флавивирусов Денге, Западного Нила и Лангат для разработки на их основе живых вакцин.
Были предприняты попытки создания живой вакцины и против вируса клещевого энцефалита. В 1957 г. в качестве такой живой вакцины было решено использовать ослабленный штамм флавивируса Лангат, вызывающий в организме выработку антител, подобных антителам к ВКЭ. Однако выяснилось, что при внутримозговом введении этот штамм сам становится патогенным и вызывает энцефалиты и атрофию участков мозга без внешних клинических проявлений. В дальнейшем были обнаружены ослабленные штаммы самого ВКЭ, но, к сожалению, все они оказались генетически нестабильными.
Вот трагический пример использования живых вакцин против ВКЭ. В 1969 г. от больного, у которого после укуса клеща в течение 4 лет не было клинических проявлений заболевания, но в крови сохранялись высокие титры антител, был выделен ослабленный штамм вируса клещевого энцефалита. Лабораторные исследования выявили его низкую нейровирулентность, после чего были проведены клинические испытания на добровольцах, давшие положительные результаты. В конечном счете ослабленным штаммом ВКЭ было иммунизировано около 650 тыс. человек. Однако 35 вакцинированных получили тяжелые осложнения в виде менингитов и менингоэнцефалитов, причем у 22 из них тяжелые последствия заболевания остались на всю жизнь, а один человек умер. Использование этого штамма в качестве живой вакцины было прекращено (Timofeev, Karganova, 2003).
ДНК-копии
С помощью подобных манипуляций были созданы живые химерные вакцины, содержащие, например, часть генов вируса желтой лихорадки и часть генов других флавивирусов. При этом в функционально важные участки их геномов были введены точечные мутации, вызывающие ослабление патогенности (Pletnev et al., 2006).
Тем не менее в настоящее время применение ослабленных живых вакцин, в том числе и против ВКЭ, ограничено, поскольку существует вероятность превращения ослабленных штаммов в высокопатогенные штаммы дикого типа. Это происходит потому, что в клетке-хозяине отсутствуют системы коррекции мутаций, которые могут возникнуть в вирусной РНК. Гарантией безопасности таких вакцин могла бы служить утрата больших фрагментов вирусных геномов, однако это приводит к значительному снижению жизнеспособности самих вирусов-мутантов.
Нужно отметить, что исследования флавивирусов, как и многих других патогенов, осложняются их высокой инфекционностью, следствием которой являются строгие требования безопасности, а также дороговизной самих вирусных препаратов. И в этом смысле использование неинфекционных ДНК-копий генома ВКЭ является очень перспективным направлением.
В ИХБФМ был получен ряд генно-инженерных ДНК, содержащих в том числе и полноразмерную ДНК-копию генома вируса клещевого энцефалита (Dobrikova et al., 1996). Конструирование подобных стабильных ДНК-копий вирусных геномов открывает широкие возможности для исследования хода размножения вируса в клетках, изучения функций отдельных вирусных белков и их комплексов.
Иммунизация генами
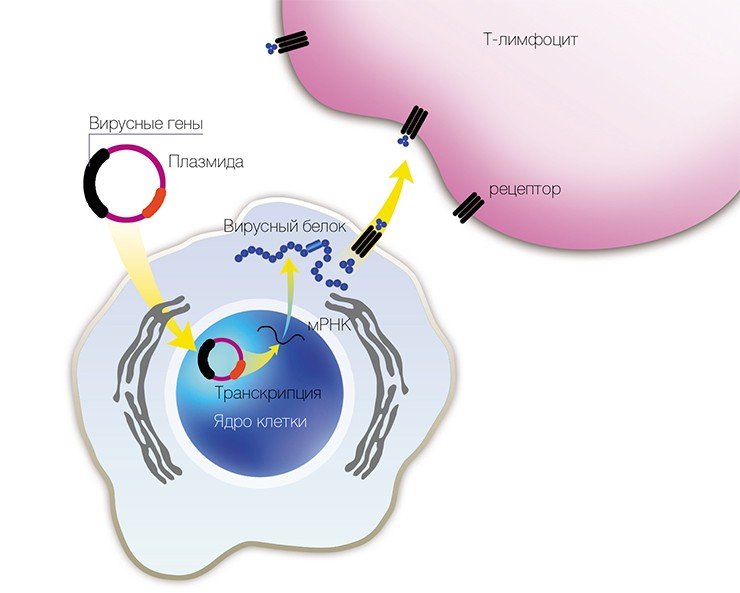
В 1993 г. появился новый подход к профилактике инфекционных заболеваний – генная иммунизация, основанная на прямом введении в организм генно-инженерной ДНК, рекомбинантных плазмид (векторов-переносчиков), содержащих не весь геном, но отдельные гены возбудителя заболевания.
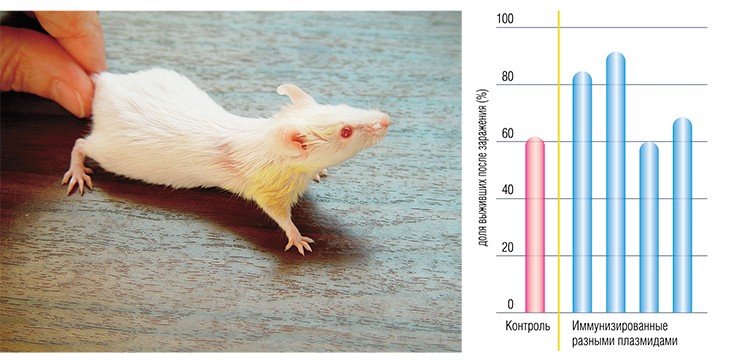
Учеными из ИХБФМ были сконструированы четыре таких плазмиды, содержащие различные гены одного из штаммов вируса клещевого энцефалита. Для оценки эффекта генной иммунизации привитых мышей заражали летальными дозами того же штамма ВКЭ. В результате оказалось, что некоторые плазмиды обладают определенным защитным эффектом.
В качестве вакцин против вирусных заболеваний ученые предполагают использовать генно-инженерные плазмиды, в которые встроены отдельные гены вирусов
Чтобы изучить возможные нежелательные эффекты этих вакцин, плазмиды вводили в различные клеточные культуры. В результате выяснилось, что при увеличении времени культивирования клеток до нескольких месяцев наблюдалась существенная модификация плазмид и встраивание их в хозяйский геном.
Таким образом, несмотря на положительные результаты генной вакцинации, вопрос о применении ДНК-вакцин в настоящее время остается открытым, поскольку препятствием к их использованию также является проблема безопасности. Возможно, преодолеть это препятствие удастся созданием РНК-вакцин с аналогичным принципом действия, для которых не существует риска интеграции в ДНК-геном хозяйской клетки. Но это уже задачи будущих исследований.
Возможно ли полностью избавиться от ВКЭ, например, уничтожив его основных переносчиков, иксодовых клещей? В свое время такая попытка была сделана с использованием печально известного ДДТ, но последствия массовой обработки лесов сильнейшим ядом были поистине ужасающими.
Аннотация научной статьи по фундаментальной медицине, автор научной работы — Леонова Галина Николаевна, Крылова Н.В., Павленко Е.В., Беликов С.И., Кондратьев И.Г.
Показано, что на Дальнем Востоке России разные формы клещевого энцефалита вызывают штаммы вируса только дальневосточного субтипа. Определены иммунопатогенетические особенности разных форм инфекции от инаппарантной до очаговых с летальным исходом. Охарактеризованы штаммы вируса клещевого энцефалита по нейровирулентности и нейроинвазивности.
Похожие темы научных работ по фундаментальной медицине , автор научной работы — Леонова Галина Николаевна, Крылова Н.В., Павленко Е.В., Беликов С.И., Кондратьев И.Г.
THE VALUE OF THE FAR EASTERN TICK-BORNE ENCEPHALITIS VIRUS STRAINS OF INFECTIOUS DISEASES
It is shown that in the Russian Far East different forms of tick-borne encephalitis virus strains cause only the Far Eastern subtype. Are defined features of immunopathogenicity of different forms of inapparent infection to focal forms with a lethal outcome. Characterized strains of tick-borne encephalitis virus in neurovirulence and neuroinvazivnosti.
ЗНиСО ЯНВАРЬ №1 (226)
ЗНАЧЕНИЕ ДАЛЬНЕВОСТОЧНЫХ ШТАММОВ ВИРУСА КЛЕЩЕВОГО ЭНЦЕФАЛИТА В ИНФЕКЦИОННОЙ ПАТОЛОГИИ
Т.Н. Леонова1, Н.В. Крылова1, Е.В. Павленко1, С.И. Беликов2, И. Г. Кондратьев2
THE VALUE OF THE FAR EASTERN TICK-BORNE ENCEPHALITIS VIRUS STRAINS OF INFECTIOUS DISEASES
G.N.. Leonova, N.V. Krylova, E.V. Pavlenko, S.I. Belikov, I.G. Kondratyev
'Научно-исследовательский институт эпидемиологии и микробиологии СО РАМН, 2Лимнологический институт СО РАН
Показано, что на Дальнем Востоке России разные формы клещевого энцефалита вызывают штаммы вируса только дальневосточного субтипа. Определены иммунопатогенетические особенности разных форм инфекции от инаппарантной до очаговых с летальным исходом. Охарактеризованы штаммы вируса клещевого энцефалита по нейровирулентности и нейроинвазивности. Ключевые слова: вирус клещевого энцефалита, биологическая вариабельность, иммунопатогенез. It is shown that in the Russian Far East different forms of tick-borne encephalitis virus strains cause only the Far Eastern subtype. Are defined features of immunopathogenicity of different forms of inapparent infection to focal forms with a lethal outcome. Characterized strains of tick-borne encephalitis virus in neurovirulence and neuroinvazivnosti.
Keyword: tick-borne encephalitis. immunopathogenicity, neurovirulence, strains of virus.
Вирус клещевого энцефалита (ВКЭ) впервые был открыт в 1937 г. Л.А. Зильбером на территории Дальнего Востока. В настоящее время эта нейроинфекция известна на Евразийском континенте от островов Тихоокеанского бассейна (Япония, Сахалин) до берегов Атлантического океана и имеет выраженную географическую неоднородность по эпидемической напряженно -сти и по тяжести клинического течения инфекции. На территории Приморского края в разные годы удельный вес лихорадочной формы клещевого энцефалита (КЭ) колебался от 20 до 50 %, менингеальной — до 20 % и очаговых форм — от 30 до 60 %.
Наши исследования были направлены на изучение биологической и молекулярной характеристики штаммов ВКЭ, попавших в организм человека при укусе клеща, а также выявление особенностей влияния их на иммунную систему пациента.
Для решения этих вопросов мы применили авторские способы экспресс-диагностики КЭ и изоляции вируса из крови лиц после укуса клеща. Выявление антигена ВКЭ в крови проводили с помощью иммуноферментного анализа (ИФА). За этот период обследовано несколько тысяч лиц с жалобами на укус клеща, а также больных КЭ. Установили, что в 70 % случаев происходила быстрая элиминация вирусного антигена из крови лиц, которые фактически оставались абсолютно здоровыми. У 30 % лиц регистрировали различные формы манифестного течения инфекции. Патологию при КЭ следует рассматривать с позиций единого механизма, лежащего в основе защитного и повреждающего действий имму-номорфологических реакций. Это обусловливает широкий диапазон проявлений инфекционного процесса — от инаппарантных и апаралитических форм до тяжелых очаговых форм острого КЭ с летальными исходами, а иногда с хронически-прогредиентным течением заболевания.
Представил интерес изучить начальный этап (на 2—4-е сутки после укуса клеща) иммунопа-тогенеза инфекции у лиц, в крови которых был выявлен антиген вируса КЭ, но эти люди не заболели. Повторное обследование их на наличие антигена проводили через месяц и при необходимости — через 6 и более месяцев.
При изучении гуморальных факторов иммунитета у таких лиц было отмечено, что в указанные сроки исследования не только клинические проявления заболевания, но и вирусспецифи-ческие антитела класса ^М к антигену ВКЭ не были зарегистрированы.
На ранней стадии инфицирования вирусом КЭ важно было определить иммунологические маркеры, характеризующие либо быструю элиминацию вируса из организма, либо его длительную персистенцию. При иммунофенотипи-ровании субпопуляций лимфоцитов на ранней стадии инфицирования ВКЭ отличительным признаком в группе лиц с кратковременной антигенемией являлось повышение относительного количества естественных киллеров ^К-клеток), Т-лимфоцитов-киллеров ^КТ-клеток) и активированных Т-лимфоцитов (CD3+CD25+, CD3+CD95+) по сравнению с показателями у здоровых доноров.
В то же время у лиц с длительной персистен-цией вируса на начальном этапе инфицирования ВКЭ выявляли сниженный уровень NKT-клеток и активированных Т-лимфоцитов, что можно считать прогностически неблагоприятным признаком. Кроме того, при анализе содержания про- и противовоспалительных цитокинов на ранней стадии инфицирования ВКЭ в крови этих пациентов не выявлена стимуляция продукции провоспалительных цитокинов (^-ф, 1КК-а). И только уровень TNF-а был выше в 1,6 раза, по сравнению с таковым у здоровых доноров, а концентрация №N-7 находилась на уровне контрольных значений. Эти данные, ка-
сающиеся неактивной продукции ^-ф, IFN-a и №N-7, помогают понять причину задержки элиминации вируса у пациентов с длительной анти-генемией.
Следующим этапом наших исследований было выявление особенностей иммунопатогене-за манифестных форм КЭ. Обследовано 50 пациентов в возрасте от 18 до 55 лет, которые были разделены на 3 группы: 1-я группа — 28 пациентов с лихорадочной формой КЭ; 2-я группа — 16 пациентов с благоприятным исходом при очаговых формах КЭ; 3-я группа — 6 пациентов с летальным исходом при очаговых формах КЭ.
Установлено, что при лихорадочной форме КЭ изменения параметров клеточного иммунитета носили компенсаторный характер: снижение количества CD3+- и CD4+-клеток сопровождалось увеличением количества NK-клеток и усилением экспрессии активационных антигенов (CD25+, CD95+). У пациентов данной группы отмечался умеренный характер активации системы комплемента и системного цитокинового ответа ТЫ-типа. Результаты этих исследований показали, что иммунологическая реактивность при лихорадочной форме КЭ соответствует общеизвестным иммунологическим закономерностям и может рассматриваться как адекватный иммунный ответ на вирусную инфекцию.
При очаговых формах КЭ развивается параллельно как противовирусный, так и иммунопатологический ответ. Их суммарное действие влияет на течение и исход инфекции. У пациентов с благоприятным исходом при очаговых формах КЭ в начальной стадии заболевания наблюдался глубокий дефицит Т-клеточного звена иммунитета. Несмотря на активацию гуморального звена иммунной системы, у этих пациентов отмечалась диспропорция содержания подклассов IgG. Низкие концентрации одного или нескольких подклассов IgG служат индикаторами дисфункции Т- и В-клеток, и могут возникнуть в результате нарушения продукции цитокинов. Известно, что дефект в продукции 1Г№-у замедляет переключение синтеза антител с ^М на IgG1 и IgG3. У пациентов этой группы в остром периоде отмечалось повышение уровня противовоспалительных цитокинов, что, с одной стороны, свидетельствует о своевременной активации противовоспалительных механизмов защиты, а с другой стороны, характеризует недостаточность клеточного иммунного ответа на фоне низких значений ТЫ-цитокинов.
Особого внимания заслуживает группа пациентов с летальным исходом при очаговых формах КЭ. Изменения показателей клеточного иммунитета у них характеризовались дефицитом содержания зрелых Т-лимфоцитов (CD3+) на фоне повышения количества незрелых активированных Т- и В-лимфоцитов. Отмечалась также депрессия киллерных механизмов цитотоксической активности (снижение количества CD8+-, NK-, NKT-клеток). В гуморальном звене иммунитета выявлена гиперактивация системы комплемента, в
цитокиновом — ранняя гиперпродукция про- и противовоспалительных цитокинов.
Таким образом, у пациентов этой группы наблюдалась дисфункция различных звеньев иммунной системы активационного типа как системного воспалительного избыточного ответа, характерного для острой фазы инфекционного процесса. Но неадекватность ответа в острой фазе является серьезной предпосылкой к формированию в патогенезе общей иммуно-депрессии, указывающей на тяжелое течение и неблагоприятный прогноз заболевания.
Разнообразие типов иммунного ответа у пациентов с разными формами КЭ обусловлено исходным уровнем иммунокомпетентности организма пациента, дозой антигена вируса, а также степенью вирулентности возбудителя.
В этой связи наши научные поиски были направлены на изоляцию и изучение характеристики вирусной популяции, попавшей в организм человека после укуса клеща и вызвавшей ту или иную форму инфекции. Получена полногеномная характеристика 36 штаммов ВКЭ, изолированных от больных с очаговыми формами в 11 случаях (30,5 %), лихорадочной — в 4 (11,1 %) и в 21 случае (58,3 %) — от лиц с инаппарантной формой инфекции. Показано, что все изученные штаммы принадлежали только к дальневосточному субтипу ВКЭ. На филогенетическом древе они расположились в двух крупных кластерах. Штаммы 1-го кластера заняли близкие позиции к штамму ОБЫша, 2-го кластера — к штамму Со-фьин. В кластере 1 доминировали штаммы, вызвавшие инаппарантную форму КЭ (82 %), здесь же по 9 % пришлось на штаммы с лихорадочной и очаговыми формами инфекции. Второй кластер в большинстве случаев состоял из штаммов, вызвавших манифестные формы. Из них 9 штаммов из группы очаговых форм и 2 — лихорадочной, здесь же расположились 3 штамма, вызвавших инаппарантную форму инфекции. Основная доля инаппарантных штаммов была изолирована на юге Приморского края. Штаммы ВКЭ, которые вызвали очаговые формы с летальным исходом, изолированы в отдаленных таежных районах среднего Сихотэ-Алиня.
Известно, что вирулентность возбудителей инфекционных болезней является одним из наиболее важных биологических свойств микроорганизма. Ведущим патогенетическим маркером, позволяющим дифференцировать штаммы ВКЭ, является, по нашему мнению, уровень периферической активности изолятов, отражающий способность возбудителя проникать в мозг. Причем, при периферической инокуляции вируса проявляется важный компонент нейровирулент-ности — нейроинвазивность.
На модели белых мышей разного возраста дана характеристика нейровирулентности и ней-роинвазивности штаммов ВКЭ, принадлежащих к разным группам. Показано, что вирусная активность всех штаммов для белых мышей при внутримозговом (в/м) заражении чаще имела
ЗНиСО ЯНВАРЬ №1 (226)
высокий уровень (7,7—11,0 ^ LD50/мл), что указывало на выраженную их вирулентность. При подкожном (п/к) заражении титр вируса у инап-парантных штаммов был ниже и колебался от 3,7 до 7,7 ^ LD50/мл. Все изученные штаммы ВКЭ проявили достаточно высокую инфекционную активность. Средняя продолжительность жизни (СПЖ) при в/м заражении мышей весом 18—20 г штаммами, вызвавшими очаговые формы, варьировала от 4,6 до 10,0 дней и в среднем составила 6,1 ± 0,5, а при п/к заражении — 8,9 ± 1,7. Для штаммов, вызвавших инаппарантное течение инфекции при в/м заражении белых мышей, СПЖ составила 14,4 ± 3,2, а при п/к заражении мышей для некоторых штаммов СПЖ резко увеличивалась до 28 дней, в среднем она составила (20,3 ± 3,9) дней. Штаммы, вызвавшие манифестные формы инфекции, как правило, более активно проявляли нейровирулентные и нейро-инвазивные свойства.
Проведено изучение гемагглютинирующей активности (ГА) штаммов при значениях рН 5,4; 6,2 и 6,8. Штаммы, вызвавшие очаговые формы увеличивали ГА активность от рН 5,4 к рН 6,8. Инаппарантные штаммы наоборот имели наибольшую активность при рН 5,4 и наименьшую — при рН 6,8.
Таким образом, показано, что на Дальнем Востоке России инфекционный процесс при КЭ с разной степенью тяжести вызывают штаммы только дальневосточного субтипа ВКЭ, которые вариабельны по параметрам как биоло-
гической (иммунопатогенетической, физико-химической, вирулентности), так и молекулярно-генетической характеристики.
Работа выполнена при поддержке гранта МНТЦ № 4006.
1. Ерман Б.А. Патологическая анатомия современного клещевого энцефалита на Урале. Екатеринбург:1999. 80 с.
3. Леонова Г.Н., Беликов С.И., Павленко Е.В., Кулакова Н.В., Крылова Н.В. Биологическая и молекулярно-генетическая характеристика дальневосточной популяции вируса клещевого энцефалита и ее патогенетическое значение //Вопр. вирусологии. 2007. № 6. С. 13—17.
4. Онищенко Г.Г., Федоров Ю.М., Пакскина Н.Д. Организация надзора за клещевым вирусным энцефалитом и меры по его профилактике в Российской Федерации //Вопр. вирусол. 2007. № 5. С. 8—10.
5. Офицеров В.И. Подклассы иммуноглобулина G: возможности использования в диагностической практике. Кольцово, 2005. 35 с.
Леонова Галина Николаевна, тел.: 8-924-2396480
Contact information: Leonova Galina, phone: 8-924-2396480

Знаете ли Вы, что при насасывании крови участки тела между склеритами (уплотнённые участки хитинового покрова клеща) растягиваются и клещи (самки, нимфы, личинки) увеличиваются в размерах до 300 раз?
Знаете ли Вы, что выход клещей из укрытий из подстилки после зимы, может быть растянут на несколько месяцев. Известно, что пик выхода клещей после зимы происходит, когда распускаются почки берёз. Суточная активность клещей связана с освещённостью, (ночью обычно не нападают). Если очень жарко днём, то активность больше утром и вечером, если температура ниже 10 – 12 град. С - клещи не активны. Клещи не любят влажность, (пока роса не высохла – не нападают).
В России встречается 6 родов клещей. Самка нападает на хозяина, прикрепляется и в течение 10 дней питается кровью, затем отпадает, откладывает яйца в почву и погибает.
Угроза, которую представляют клещи, обитающие на территории России, остаётся самой высокой в мире не только по распространённости заболеваний, но и тяжести последствий. Штамм вируса клещевого энцефалита, который циркулирует в странах Европы, не представляет опасности для жизни, в то время как России зарегистрированы летальные исходы после укуса заражённого клеща, а более 25% пострадавших от нападения клещей остались инвалидами.
Каждый год по данным лечебных учреждений за медицинской помощью обращаются 7-8 тыс. жителей Москвы и Подмосковья, пострадавшие от укусов клещей. Сам укус клеща не опасен, однако если клещ заражён вирусом клещевого энцефалита, или боррелиозом, то возникает угроза для здоровья пострадавшего.
Где регистрируется заболевание?
В настоящее время заболевание клещевым энцефалитом регистрируется почти на всей территории России (зарегистрировано около 50 территорий субъектов Российской Федерации), где имеются основные его переносчики - клещи. Наиболее неблагополучными регионами по заболеваемости являются: Уральский, Западно-Сибирский, Восточно-Сибирский и Дальне-Восточный регионы, а из прилегающих к Московской области - Тверская и Ярославская.
При выезде в эндемичную по клещевому энцефалиту территорию необходимо получить профилактические прививки против этого заболевания? Специфический иммуноглобулин против клещевого энцефалита (серопрофилактика) показано вводить лицам с присасыванием клеща, случившемся на эндемичной по клещевому энцефалиту территории, не позднее 4-х суток с момента присасывания. Территория Москвы и Московской области является благополучной по клещевому энцефалиту.
Где можно узнать, есть ли риск заражения на интересующей территории и нужно ли делать прививку?
Исследование клещей на заражённость вирусом клещевого энцефалита можно провести в отделении особо опасных инфекций микробиологической лаборатории ФГУЗ «Центр гигиены и эпидемиологии в г. Москве (Графский пер.д.4/9 тел.687-40-47).
Какие основные признаки болезни?
Для заболевания характерна весенне-летняя сезонность, связанная с периодом наибольшей активности клещей. Инкубационный (скрытый) период длится чаще 10-14 дней, с колебаниями от 1 до 60 дней.
Болезнь начинается остро, сопровождается ознобом, сильной головной болью, резким подъемом температуры до-38-39 градусов, тошнотой, рвотой. Беспокоят мышечные боли, которые наиболее часто локализуются в области шеи и плеч, грудного и поясничного отдела спины, конечностей. Внешний вид больного характерен - лицо гиперемировано (красное), гиперемия нередко распространяется на туловище.
Кто подвержен заражению?
К заражению клещевым энцефалитом восприимчивы все люди, независимо от возраста и пола. Наибольшему риску подвержены лица, деятельность которых связана с пребыванием в лесу: работники леспромхозов, геологоразведочных партий, строители автомобильных и железных дорог, нефтепроводов и газопроводов, линий электропередач, топографы, охотники, туристы. Горожане заражаются в пригородных лесах, лесопарках, на садово-огородных участках.
Система защиты населения – основа санитарно-просветительная работа.
Специальные средства индивидуальной защиты:
- обработка одежды химическими препаратами;
- специальная (противоэнцефалитная) одежда.
Мера по преобразованию окружающей среды:
- расчистка территории (в детских оздоровительных лагерях лучше вдоль дорожек не кусты, а клумбы);
- уничтожение переносчиков клещей – проведение дератизации;
- ликвидация условий для жизни и привлечения грызунов (расчистка территорий, уборка мусора и др.)
Как можно защитится от клещевого энцефалита ?
Заболевание клещевым энцефалитом можно предупредить с помощью неспецифической и специфической профилактики.
Неспецифическая индивидуальная (личная) защита людей включает в себя:
- Соблюдение правил поведения в опасной в отношении клещей территории (проводить само и взаимоосмотры каждые 10-15 минут для обнаружения клещей; не рекомендуется садится и ложится на траву; устраивать стоянки и ночёвки в лесу следует на участках, лишённых травяной растительности или в сухих сосновых лесах на песчаных почвах; после возвращения из леса или перед ночёвкой необходимо снять одежду, тщательно осмотреть тело и одежду; не рекомендуется вносить в помещение свежесорванные растения, верхнюю одежду и другие предметы, на которых могут оказаться клещи; осматривать собак и других животных для обнаружения и удаления с них прицепившихся и присосавшихся клещей);
- Ношение специальной одежды. При отсутствии специальной одежды одеваться следует таким образом, чтобы облегчить быстрый осмотр для обнаружения клещей; носить однотонную светлую одежду; брюки заправлять в сапоги, гольфы или носки с плотной резинкой, верхнюю часть одежды – в брюки; манжеты рукавов должны плотно прилегать к руке; ворот рубашки и брюки должны иметь застёжки или иметь плотную застёжку, под которую не может проползти клещ; на голову надевать капюшон, пришитый к рубашке, куртке или заправлять волосы под косынку, шапку.
Как снять клеща?
Для удаления клеща и первичной обработки места укуса следует обратиться в травматологический пункт, либо снять самостоятельно. Снимать клеща следует очень осторожно, чтобы не оборвать хоботок, который глубоко и сильно укрепляется на весь период присасывания.
При удалении клеща необходимо соблюдать следующие рекомендации:
- захватить клеща пинцетом или обернутыми чистой марлей пальцами как можно ближе к его ротовому аппарату и держа строго перпендикулярно поверхности укуса повернуть тело клеща вокруг оси, извлечь его из кожных покровов;
- место укуса продезинфицировать любым, пригодным для этих целей, средством (70% спирт, 5% йод, спиртосодержащие средства).
- после извлечения клеща необходимо тщательно вымыть руки с мылом.
- если осталась черная точка (отрыв головки или хоботка) обработать 5% йодом и оставить до естественной элиминации.
Снятого клеща рекомендуется исследовать на заражённость боррелиями и вирусом КВЭ в лаборатории. Клещей, снятых с человека помещают в герметично закрывающуюся ёмкость с небольшим кусочком чуть влажной ваты и направляют в лабораторию. При невозможности исследования клеща следует сжечь или залить кипятком.
Меры специфической профилактики клещевого энцефалита:
Профилактические прививки против клещевого энцефалита проводятся лицам отдельных профессий, работающим в эндемичных очагах или выезжающих в них (командированные, студенты строительных отрядов, туристы, лица, выезжающие на отдых, на садово-огородные участки). Все лица, выезжающие на работу или отдых в неблагополучные территории, должны быть обязательно привиты.
Экстренная серопрофилактика проводится не привитым лицам, обратившимся в связи с присасыванием клеща на эндемичной по клещевому вирусному энцефалиту территории.
Где можно сделать прививку от клещевого энцефалита?
Когда нужно сделать прививку от клещевого энцефалита?
Консультацию по вакцинопрофилактике может дать только врач.
Вакцинацию против клещевого энцефалита необходимо начинать за 1,5 месяца (Россия) или за 1 мес. (Германия) до выезда в неблагополучную территорию.
Прививка отечественной вакциной состоит из 2 инъекций, минимальный интервал между которыми - 1 месяц. После последней инъекции должно пройти не менее 14 дней до выезда в очаг. За это время вырабатывается иммунитет. Через год необходимо сделать ревакцинацию, которая состоит только из 1 инъекции, далее ревакцинацию повторяют каждые 3 года.
Если до отъезда человек не успевает сделать прививку в экстренных случаяхможно ввести человеческий иммуноглобулин против клещевого энцефалита до выезда в неблагополучную территорию (доэкспозиционная профилактика), действие препарата проявляется через 24 - 48 часов и продолжается около 4 недель.
Что нужно делать и куда обращаться, если Вы не привиты и произошло присасывание клеща во время посещения территории, неблагополучной по клещевому энцефалиту?
Не привитым лицам проводится серопрофилактика - введение человеческого иммуноглобулина против клещевого энцефалита не позднее 4 –го дня после присасывания клеща (круглосуточно):.
- взрослым в НИИ скорой и неотложной медицинской помощи им. Склифосовского (Москвы, Сухаревская пл.,д.3);;
- детям в Детской клинической больнице № 13 им. Филатова (Москва, Садовая-Кудринская, д.15).
Где провести лабораторное исследование клещей?
При обращении в лабораторию необходимо дать информацию о дате и территории, на которой пароизошло присасывание клеща (регион, область, населённый пункт).
Где провести лабораторное исследование крови?
При получении положительного результата лабораторного исследования необходимо срочно обратиться за медицинской помощью в лечебно-профилактические учреждения.
КЛЕЩЕВЫЕ БОРРЕЛИОЗЫ (синонимы: болезнь Лайма, Лайм-боррелиоз, иксодовый клещевой боррелиоз) – трансмиссивные природно-очаговые инфекции с острым или хроническим течением, при которых возможно поражение кожи. Нервной, сердечно-сосудистой систем, печени и опорно-двигательного аппарата.
Возбудитель болезни Лайма- спирохета Borrelia burgdorferi, передаётся иксодовыми клещами.
Человек заражается трансмиссивным путём – при присасывании клеща возбудитель передаётся со слюной.
Официальный перечень территорий, эндемичных по клещевым боррелиозам, отсутствует. Ареал распространения данного заболевания шире ареала клещевого энцефалита. Случаи заболевания клещевым боррелиозом регистрируются и на территориях благополучных по клещевому энцефалиту.
Инкубационный период колеблется от 3 до 45 дней ( в среднем 12-14 дней), по данным некоторых авторов до 60 дней. Способность возбудителя к длительной персистенции в организме определяет формирование хронических форм заболевания, протекающего в виде системного поражения органов.
Клинические проявления. У большинства больных на месте входных ворот развивается характерное поражение кожи в виде мигрирующей кольцевой эритемы. Однако не всегда патологический процесс может ограничиваться только кожным поражением. Наблюдаются изменения со стороны регионарного лимфатического аппарата, боли в мышцах, суставах, повышение температуры, признаки интоксикации. В случаях, обусловленных большой дозой и патогенностью возбудителя, наступает его распространение по кровеносным и лимфатическим сосудам в ЦНС, миокард, мышцы, суставы, печень, селезёнку. В таких случаях развивается вторая стадия заболевания, при которой могут проявляться разнообразные симптомы нейроборрелиоза (менингит,полиневриты, миелиты), артриты, миозиты, перикардиты, гепатиты и др.
У 20-45% борльных наблюдается форма заболевания без местных кожных изменгений. Диагностика в таких случаях по клиническим признакам практически невозможна. Только проведение серологических методов диагностики может дать возможность поставить правильный диагноз.
Часто болезнь протекает в лёгких, стёртых формах.
Меры специфической профилактики клещевого боррелиоза не разработаны. В связи с этим основными мерами предупреждения заболевания являются методы неспецифической профилактики (см.Клещевой энцефалит).
При присасывании клеща в лесопарковых зонах Морсквы и Московской области необходимо снять клеща и провести первичную обработку места присасывания в травматологических пунктах города, желательно сохранить клеща для дальнейшего исследования на заражённость боррелиями (см. Клещевой энцефалит).
При появлении клинических проявлений следует обратиться к инфекционисту в лечебное учреждение. Больному при подозрении на заболевание клещевым боррелиозом следует провести серологические исследования крови.
Исследования клещей на заражённость боррелиями можно провести в лаборатории, выполняющей данный вид исследования (см. Клещевой энцефалит).
При получении положительных результатов лабораторного исследования клеща на заражённость боррелиями, необходимо обратиться к инфекционисту или лечащему врачу для осмотра и возможного назначения антибиотиков.
Читайте также:


