Токсическая энцефалопатия при химиотерапии
Энцефалопатия может вызывать припадки, а припадки, в свою очередь, могут способствовать прогрессированию энцефалопатии.
Состояние после припадков может напоминать проявления энцефалопатии. У ослабленных и пожилых больных оно может длиться до недели.
Если основное заболевание неизлечимо, то назначают только поддерживающую терапию.
1. Наиболее частыми возбудителями являются Listeria monocytogenes, Cryptococcus neoformans и Aspergillus fumigatus.
2. Нередко возбудители инфекций ЦНС представлены грамотрицательными микроорганизмами, Candida albicans и вирусом Herpes zoster.
3. Возможна реактивация латентных микобактериальных инфекций.
4. Клинические проявления
- Инфекции ЦНС проявляются повышением температуры, психическими нарушениями и припадками.
- Головная боль и менингеальные знаки могут быть слабовыраженными или вообще отсутствовать у ослабленных больных.
- У больных с выраженной лейкопенией цереброспинальная жидкость может не быть гнойной и из нее может не выделяться патогенный микроорганизм.
- Окрашенный по Граму или Цилю-Нильсену осадок ЦСЖ (после центрифугирования) может выявить патоген до получения результатов посева.
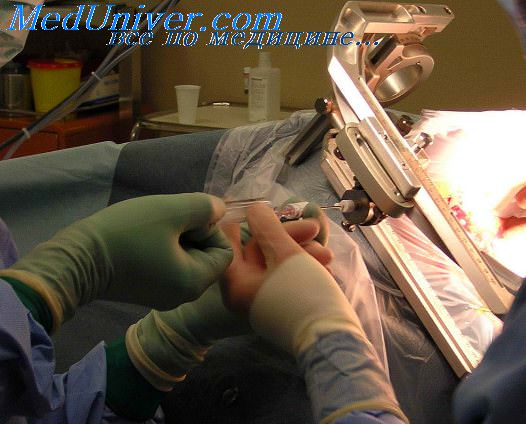
5. Люмбальную пункцию следует проводить с большой осторожностью из-за риска развития вклинения у больных с повышенным внутричерепным давлением, а также эпидуральной гематомы у больных с тромбоцитопенией.
6. Лечение включает антибиотикотерапию и поддерживающие средства.
7. Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ)
- Это оппортунистическая инфекция ЦНС, вызываемая паповавирусом (JCV).
- Течение неуклонно прогрессирующее, в редких случаях наблюдается длительная ремиссия.
- ПМЛ проявляется психическими расстройствами, нарушением речи и зрения, парезами.
- Диагноз подтверждают данными биопсии фокального очага в белом веществе мозга.
- Лечение проводят ара-А (аденин-арабинозидом) или ара-С (цитозин-арабинозидом).
1. По данным аутопсии, у 15% онкологических больных обнаружены изменения, характерные для цереброваскулярной болезни, в половине случаев она протекала бессимптомно.
2. Основной причиной инфарктов мозга были атеросклеротические изменения, при этом лишь у 15% больных имели место клинические проявления инфаркта.
3. Цереброваскулярная болезнь у больных раком может быть осложнением опухолевого процесса или лечения.
4. У онкологических больных ишемические инсульты встречаются чаще, чем геморрагические. Частыми причинами манифестных церебральных инфарктов в этой группе больных являются небактериальный тромботический эндокардит и синдром внутрисосудистого свертывания.
5. Наиболее частые причины кровоизлияния в паренхиму мозга — коагулопатии и кровоизлияние в метастазы меланомы или опухоли стволовых клеток.
6. Рак слизистых может стать причиной инфаркта в результате распространенной окклюзии (муцином) любой мозговой артерии.
7. У многих пациентов с клинически выраженной цереброваскулярной болезнью и лейкемией развиваются геморрагические инфаркты.
8. Не существует специфических методов лечения перечисленных осложнений.
9. Острые и отсроченные окклюзии сосудов могут наблюдаться при химиотерапии, особенно при использовании цисплатина, а также после курса химиотерапии.
10. К поздним осложнениям лучевой терапии относятся воспалительная артериопатия с окклюзией крупных и мелких сосудов, минерализующая микроангиопатия и быстро прогрессирующий атеросклероз сосудов.
11. Имеет место гиподиагностика тромбоза синусов твердой оболочки, особенно верхнего сагиттального синуса.
- Тромбоз верхнего сагиттального синуса часто протекает бессимптомно и кровоток в нем восстанавливается через некоторое время самопроизвольно.
- Это осложнение чаще всего наблюдается у больных лейкемией, получающих химиотерапию, и у больных с коагулопатией или распространенным раком.
- Тромбоз венозного синуса клинически проявляется головными болями, припадками, отеком диска зрительного нерва, фокальными двигательными нарушениями и энцефалопатией.
- Диагноз ставится на основании данных ангиографии, КТ или МРТ с контрастированием и МРТ-ангиографии.
- Лечение только поддерживающее. Если нет кровоизлияния, то коротким курсом можно назначить антикоагулянты, хотя мнения специалистов на этот счет расходятся.
12. Неопластический ангиоэндотелиоз или внутрисосудистый лимфоматоз — это закупорка мелких сосудов злокачественными клетками мононуклеарного ряда.
- Это редкое осложнение лимфомы.
- При окклюзии мелких сосудов в ЦНС у больного отмечается рассеянный очаговый неврологический дефицит и энцефалопатия, которые в короткие сроки (или иногда подостро) приводят к летальному исходу.
- Этот синдром трудно отличить от прогрессирующей мультифокальной лейкоэнцефалопатии, васкулита или множественной эмболии.
VI РОССИЙСКАЯ ОНКОЛОГИЧЕСКАЯ КОНФЕРЕНЦИЯ
НЕЙРОТОКСИЧНОСТЬ СОВРЕМЕННЫХ ЦИТОСТАТИКОВ
Нейротоксичность является одним из специфических системных осложнений противоопухолевой химиотерапии, в том числе новых эффективных цитостатиков различных классов: паклитаксела, доцетаксела, винорельбина, оксалиплатина, иринотекана, гемцитабина и др. В ряде случаев она не только снижает качество жизни пациентов, но и ограничивает дозу цитостатиков, поэтому ранняя диагностика, профилактика и лечение нейротоксичности весьма актуальны.
Обусловленное химиотерапией поражение периферической, центральной и вегетативной нервной системы может быть как изолированным, так и сочетанным. Периферическая нейротоксичность проявляется дистальной и краниальной нейропатией и сегментарными вегетативными нарушениями, в частности, холинэргическим синдромом, синдромом Рейно, нарушением функции кишечника и мочевого пузыря, импотенцией, нарушением потоотделения и ортостатической гипотензией. Наиболее часто развивается токсическая полинейропатия (ПНП) - сенсорная, моторная или смешанная - в основе которой лежит поражение аксонов (аксонопатия), их миелиновых оболочек (миелинопатия) или тел нейронов (нейронопатия). В группу риска развития периферической нейротоксичности следует включать больных сахарным диабетом, злоупотребляющих алкоголем, а также ранее получавших нейротоксичные препараты. Уже до начала химиотерапии у них могут быть проявления полинейропатии, которые, как правило, не являются противопоказанием для цитостатического лечения.
Центральная нейротоксичность может проявиться на уровне спинного мозга миелопатией (встречается крайне редко при интратекальном введении препаратов), на уровне головного мозга - различными психовегетативными нарушениями и острой, подострой или прогрессирующей энцефалопатией с развитием синдрома нарушенного сознания; судорожного синдрома; двигательных нарушений (пирамидных, экстрапирамидных, мозжечковых); когнитивных расстройств и др. Часто наблюдаются такие проявления токсичности как головная боль и головокружение. Центральные вегетативные (надсегментарные) и психовегетативные нарушения включают вегетативную лабильность, вегетативные кризы (панические атаки), эмоционально-аффективные расстройства и астенические состояния. В группу риска развития центральной нейротоксичности следует включать пациентов старшей возрастной группы, страдающих энцефалопатией, сочетающейся с артериальной гипертензией.
Оценка степени тяжести нейротоксичности до настоящего времени остается весьма условной и во многом зависит от используемой шкалы и опыта врача. Наиболее распространены такие критерии токсичности, как СТС-NCIC и СТС-NCI, version 2.0.
Нейротоксичность является дозолимитирующим осложнением цисплатина, её частота достигает 50% и зависит от разовой (≥100 мг/м 2 ) и кумулятивной дозы (≥300-600 мг/м 2 ) цитостатика, одновременного или предшествующего использования других нейротоксичных препаратов, характера сопутствующей патологии. При высоких дозах нейротоксичность возникает практически в 100% и может проявляться нейропатией, симптомом Лермитта, судорожным синдромом, энцефалопатией, преходящей корковой слепотой, ретробульбарным невритом, возможен также преходящий двусторонний паралич голосовых связок. Наиболее часто развивается периферическая ПНП в виде симметричных дистальных парестезий, снижения вибрационной и проприоцептивной чувствительности с развитием сенситивной атаксии при относительной сохранности тактильной и температурной. Первыми обычно страдают стопы. Ранний признак токсичности - снижение ахилловых рефлексов. Наряду с сенсорной развивается моторная или смешанная ПНП. Нередко встречаются мышечные судороги. В течение нескольких месяцев после окончания химиотерапии наблюдается медленный регресс неврологических нарушений, однако, в ряде случаев они могут прогрессировать или впервые возникать даже после прерывания лечения. Центральная нейротоксичность цисплатина проявляется острой и подострой энцефалопатией, частота которой составляет 0,2-2,7% при кумулятивной дозе препарата 200-700 мг/м 2 . Как правило, симптомы транзиторны и в большинстве случаев исчезают в течение недели без каких-либо резидуальных явлений даже после повторных эпизодов при продолжении химиотерапии. Поздняя (отсроченная) токсичность цисплатина крайне редко может проявиться транзиторными ишемическими атаками, церебральными инфарктами, синдромом Рейно. У 30-50% больных при кумулятивной дозе цисплатина 100-300 мг/м 2 развивается ототоксичность в виде шума или звона в ушах и прогрессирующей нейросенсорной потери слуха в диапазоне высоких частот (4000-8000 Hz), а иногда и в диапазоне речевых частот. Обратимость осложнения сомнительна. В тяжелых случаях возникают и вестибулярные расстройства - головокружение, нистагм, атаксия.
Нейротоксичность паклитаксела - также дозозависимое осложнение, достигающее 100%. Обычно симптомы появляются после нескольких курсов стандартных разовых доз препарата (135-250 мг/м 2 ), но могут наблюдаться уже через 24-72 часа после введения высоких доз (>250 мг/м 2 ). Особую настороженность следует проявлять при достижении кумулятивной дозы ≥350 мг/м 2 . В большинстве случаев развивается синдром ПНП различной степени тяжести в виде симметричных, преимущественно сенсорных расстройств (обычно онемения) в дистальных отделах конечностей (чаще нижних). Особенностью являются жгучие боли в подошвах и стопах (чаще при разовой дозе ≥220 мг/м 2 ). Субъективные изменения нередко превалируют над объективными. В процессе химиотерапии парестезии могут распространяться одновременно на дистальные отделы рук и ног, после её завершения, как правило, наблюдается регресс нарушений чувствительности, однако выпадение сухожильных рефлексов, особенно ахилловых, может сохраняться довольно долго. Восстановление сухожильных рефлексов, как правило, происходит в порядке, обратном выпадению, в течение первых 6-12 месяцев после окончания химиотерапии. Редко встречаются преходящие двигательные (моторная ПНП) и вегетативные (синкопы, паралитический илеус) нарушения, краниальная нейропатия (парестезии в периоральной области, паралич лицевого нерва). Острые нарушения функции центральной нервной системы также встречаются редко (менее 1%) и включают генерализованные эпилептические припадки (grand mal), энцефалопатию в виде преходящей спутанности сознания, афазии, нарушений поведения, атаксии. При высоких дозах паклитаксела (>250 мг/м 2 ) описаны зрительные расстройства в виде преходящих мерцающих скатом, при комбинации паклитаксела (250 мг/м 2 ) с цисплатином отмечена миопатия. Из сопутствующих нейротоксичности осложнений химиотерапии паклитакселом следует отметить артралгии и миалгии (при разовой дозе ≥220 мг/м 2 ).
Основным проявлением нейротоксичности доцетаксела также является дозозависимый синдром ПНП, частота которого достигает 50-70%, при этом только у 2-7% больных он соответствует III-IV степени тяжести. Как правило, разовая доза составляет 100 мг/м 2 , кумулятивная - 300-400 мг/м 2 . Возникает преимущественно аксональная нейропатия, затрагивающая крупные хорошо миелинизированные волокна, чаще сенсорные. Признаки моторной нейропатии наблюдаются крайне редко. Характерный для доцетаксела синдром задержки жидкости усугубляет проявления периферической нейротоксичности. Из признаков центральной нейротоксичности обращает внимание астенический синдром, тяжесть которого у 10-22% больных достигает II-III степени. Транзиторные миалгии при лечении доцетакселом наблюдаются сравнительно редко (7-10%).
Нейротоксичность винорельбина проявляется периферической нейропатией и запором. Признаки токсичности чаще возникают после 5-го введения (25-30 мг/м 2 еженедельно) и носят вначале обратимый непостоянный характер, по мере продолжения лечения они могут стать постоянными и нарастать по тяжести. Во время клинической апробации винорельбина в России у 60% больных отмечен астенический синдром в виде нарастающей слабости и "усталости от лечения", что иногда требовало перерыва в проведении химиотерапии.
Частота нейротоксических эффектов фторурацила мала (5-10%). В основном это острая мозжечковая дисфункция (атаксия, нистагм, дисметрия, дизартрия). Наблюдается и диффузное поражение головного мозга в виде энцефалопатии, проявляющейся головной болью, нарушением сознания, дезориентацией, летаргией, судорогами, экстрапирамидными расстройствами, дефектами познавательной деятельности. Встречаются глазодвигательные нарушения (парезы III и IV краниальных нервов), проявления фокальной дистонии. Периферическая нейропатия встречается крайне редко и может смешиваться с плантарно-пальмарной эритродизестезией (hand-foot syndrome), являющейся проявлением кожной токсичности. Нейротоксические эффекты цитостатика обычно дозо- и режимозависимы и, как правило, обратимы при отмене или редукции дозы. У больных с нарушенным метаболизмом пиримидина, таким как дефицит энзима дигидропиримидин дегидрогеназы, встречающимся примерно у 3% больных раком, риск развития нейротоксичности при лечении фторурацилом повышается до 40%.
Из нейротоксических эффектов капецитабина можно отметить лишь единичные случаи ПНП легкой степени; гемцитабина - нейропатию I-II степени у 3% больных, легкую или умеренную сонливость (10-15%) и слабость, которые наблюдают при уровне разовых доз препарата порядка 1200 мг/м 2 , отмечены также единичные случаи транзиторного нарушения сознания с развитием преходящих церебральных симптомов и психовегетативные расстройства.
Основное проявление нейротоксичности иринотекана - острый холинэргический синдром, развивающийся в первые сутки после введения у 80-85% больных и характеризующийся повышенной потливостью, гиперсаливацией, ринореей, слезотечением, диареей, коликообразными болями в животе, "затуманиванием" зрения. Эта периферическая (сегментарная) вегетативная нейротоксичность обусловлена способностью иринотекана ингибировать фермент антихолинэстеразы и активировать тем самым парасимпатическую иннервацию. Кроме того, встречаются единичные случаи токсической ПНП легкой степени и психовегетативные проявления.
Неврологический контроль и терапия нейротоксичности цитостатиков у больных солидными злокачественными опухолями в каждом конкретном случае должны быть индивидуальными. Общепринятых схем лечения в настоящее время нет, терапия носит в основном симптоматический характер и проводится при достижении II (умеренной) степени. Однако, как показывает практика, в тех случаях, когда симптомы периферической нейротоксичности ухудшают качество жизни пациентов, их лечение следует начинать уже при I (легкой) степени. Симптоматическое лечение проявлений центральной нейротоксичности необходимо начинать уже при I степени тяжести. При достижении II степени следует решать вопрос о редукции дозы цитостатика, прерывании или, в некоторых случаях, прекращении химиотерапии. Центральная нейротоксичность III-IV степени требует прекращения химиотерапии.
Симптоматическое лечение включает ноотропные и сосудистые препараты, средства, улучшающие тканевой обмен, и блокаторы кальциевых канальцев. При болях целесообразно назначение ненаркотических анальгетиков и антидепрессантов. При явлениях центральной нейротоксичности по показаниям назначают кортикостероиды, противосудорожные, психотропные, гипотензивные и мочегонные препараты, а также b-блокаторы. При своевременно начатой корригирующей терапии симптомы центральной нейротоксичности, как правило, обратимы. При нейротоксичности III-IV степени на фоне общей детоксикационной терапии следует назначать инфузии плазмозамещающих растворов, сосудистых и ноотропных препаратов. В определенной степени могут быть действенны комплексоны, такие как унитиол, показаны также вспомогательные препараты, стимулирующие метаболические процессы (фосфаден), при парезах назначают антихолинэстеразные средства.
Проводя терапию, направленную на коррекцию неврологических проявлений периферической токсичности, необходимо учитывать, что регресс симптоматики наблюдается, как правило, после завершения химиотерапии. Так как больные солидными злокачественными опухолями наряду с химиотерапией нередко получают и другое сопутствующее лечение, целесообразно ограничить назначение препаратов, направленных на коррекцию проявлений нейротоксичности, необходимым минимумом.

Каковы неврологические побочные эффекты химиотерапии?
Химиотерапия часто является лучшим способом лечения рака, но она не лишена рисков или значительных побочных эффектов, в том числе для мозга и нервной системы.
Многие из лекарств, используемых для борьбы с раком, также затуманивают наши умы и нервы, которые посылают информацию в наш мозг.
Не всегда легко отличить симптомы друга от врага. Является ли конкретный симптом из-за рака, или лекарства, борющегося с этим раком? Или это из-за чего-то совершенно другого?
Есть много различных способов, которыми химиотерапевтические агенты могут повредить нервную систему. То, что следует, далеко не исчерпывающее, но дает обзор некоторых способов химиотерапии, которые могут повредить нервную систему.
Осложнения могут произойти рано или поздно
Цитарабин иногда используется для лечения лейкемии и лимфом, а также может привести к осложнениям вскоре после введения. Например, это может привести к путанице и энцефалопатии, а также к таким признакам мозжечка, как неуклюжесть (атаксия). Лечение должно быть немедленно прекращено, если это происходит. Некоторые пациенты выздоравливают, но некоторые нет. Цитарабин также можно вводить интратекально, но иногда это может привести к поперечной миелопатии с параличом ног и дисфункцией сфинктера. Опять же, лечение должно быть немедленно прекращено, если это произойдет. Повреждение позвоночника от цитарабина обычно носит постоянный характер.
Метотрексат может быть использован для лечения широкого спектра раковых заболеваний, а также вызывает широкий спектр потенциальных побочных эффектов, некоторые из которых могут возникнуть рано, а другие поздно. Например, это может вызвать асептический менингит, который возникает почти сразу, когда препарат вводится интратекально. Асептический менингит обычно следует за интратекальным введением и встречается у 10-50% пациентов, которые получают препарат таким образом. Симптомы включают головную боль и ригидность затылочных мышц, а также тошноту, рвоту и жар. Лечение обычно не требуется, так как симптомы проходят самостоятельно.
Рак часто вызывает то, что врачи называют гиперкоагуляционным состоянием, а это означает, что сгустки крови более склонны к форматированию в неподходящее время. Например, сгусток может образоваться в мозге, вызывая инсульт. К сожалению, некоторые химиотерапии могут также вызвать инсульты, такие как метотрексат, цисплатин, иматиниб и другие.
Некоторые агенты, такие как бевацизумаб и сунитиниб, преднамеренно нацелены на кровеносные сосуды, поскольку опухоли часто создают новые сосуды для отправки питательных веществ к аномальному росту. К сожалению, побочные эффекты могут включать кровоизлияние или ишемические инсульты. В качестве другого примера, L-аспарагиназа часто используется для лечения острого лимфобластного лейкоза (ALL) и иногда вызывает образование тромбоза венозного синуса даже у детей. Это обычно решается с перерывом в режиме лечения. Если затем вводится разбавитель крови, иногда лечение может быть возобновлено.
Периферические невропатии являются распространенным побочным эффектом химиотерапии, особенно для платиносодержащих агентов, таких как цисплатин и оксалиплатин. Периферическая невропатия, вызванная цисплатином, вызывает прогрессирующее онемение и парестезии, которые начинаются по краям пальцев рук и ног и распространяются внутрь. Хотя ощущение тела в космосе повреждено, ощущение боли и температуры почти всегда сохраняется, что отличает невропатию цисплатина от большинства невропатий, которые могут быть вызваны самим раком. Риск снижения дозы или перехода на менее нейротоксический агент, такой как карбоплатин, необходимо сопоставить с преимуществами продолжения терапии цисплатином. Невропатия может ухудшиться или даже начаться через несколько месяцев после прекращения приема цисплатина.
Нервно-мышечные повреждения
Нервно-мышечное повреждение встречается реже, чем периферическая невропатия, но все же может возникнуть в результате химиотерапии. Доксорубицин, цисплатин, этопозид и другие могут на самом деле привести к симптому, похожему на миастению. Иматиниб, используемый для лечения некоторых форм лейкемии, может вызывать мышечные спазмы и миалгию, но они обычно слабо выражены и реагируют на такие лекарства, как кальций или магний.
Ни для кого не секрет, что химиотерапия является очень мощным препаратом с высоким риском побочных эффектов. То, что написано здесь, это только очень общий план. Существует причина, по которой эти лекарства обычно хранятся в резерве для таких серьезных заболеваний, как рак, при которых польза от приема препарата перевешивает даже значительные риски. Цель этой статьи не в том, чтобы отговорить тех, кто нуждается в этих лекарствах, от их приема, а в том, чтобы люди знали о потенциальных побочных эффектах, чтобы лучше ориентироваться в сложностях лечения рака.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
- Причины
- Симптомы
- Формы
- Лечение
- Профилактика
Полинейропатия после химиотерапии возникает вследствие токсического поражения нервных волокон и определённых зон в головном мозге применёнными препаратами. В первую очередь пациентов беспокоит появившаяся слабость.
Полинейропатия - это поражение периферической нервной системы, которое проявляется в периферических вялых параличах, нарушениях чувствительности, трофических и вегетососудистых расстройствах. Если игнорировать данный симптом во время химиотерапии и не назначить необходимого симптоматического лечения, то возникают и другие признаки полинейропатии. Они становятся более интенсивными и разнообразными.

[1], [2], [3], [4]
Причины полинейропатии после химиотерапии
Механизм повреждения нервной системы может быть следующим:
- Вызывать аксональную дегенерацию.
- Провоцировать появление сегментарной демиелинизации.
Степень проявления и частота симптомов полинейропатии после химиотерапии зависят от лекарственного средства, влияет также и его разовая и кумулятивная доза. Имеются и иные факторы риска, например, нейропатии наследственного и приобретённого характера, наличие сахарного диабета, имеющийся алкоголизм, имеющаяся почечная и/или печёночная дисфункции, предшествующие курсы химиотерапии.

[5], [6], [7]
Симптомы полинейропатии после химиотерапии
Специалисты выделяют несколько видов полинейропатии после химиотерапии:
- Дистальная – данный синдром проявляется в симметричных нарушениях чувствительности и /или нарушениях двигательных функций у больного.
- Сенсорная – проявляется в ощущениях онемения, покалывания, холода или жжения в разных частях тела. Также проявляется и в дизестезии – нарушении чувствительности нервных волокон, вследствие чего при прикосновении к коже больной испытывает неприятные, а иногда аномальные и извращённые ощущения. Например, холод может ощущаться теплом, простое прикосновение – как боль. Возможно проявление данного вида полинейропатии только в качестве болевых ощущений.
Все вышеперечисленные признаки начинаются сот стоп и кончиков пальцев ног, с кончиков пальцев и кистей рук. Постепенно данные ощущения распространяются на руки и ноги, поднимаясь к позвоночнику.
Формы
Нейропатия после химиотерапии возникает вследствие поражения периферической нервной системы, а в редких случаях – центральной нервной системы. Проявляется нейропатия в нарушении двигательных (моторных) функций больного, а также в снижении чувствительности кожных покровов, появлении извращённой (аномальной) чувствительности, уменьшением вибрационной чувствительности, снижением рефлексов сухожилий, появлением чувства онемения конечностей и частей тела и так далее.

[8], [9], [10], [11], [12]
- Почему возникает химио мозга?
- Какие химиопрепараты вызывают самые тяжелые побочные эффекты со стороны головного мозга?
- Основные симптомы
- Как бороться с химио мозга?
- Что можете сделать вы?
- Сможет ли нервная система восстановиться полностью?
- Химио мозга: результаты недавних исследований
Химио мозга — не менее неприятный и мучительный побочный эффект, чем выпадение волос, проблемы с приемом пищи, анемия или снижение иммунитета. Эффективных средств его профилактики не существует. Лечить данное состояние сложно, у некоторых пациентов проблемы с памятью, вниманием и мышлением сохраняются в течение многих лет.

Почему возникает химио мозга?
Позже оказалось, что все намного сложнее.
Химио мозга развивается под действием многих факторов. Это могут быть побочные эффекты противоопухолевых средств, препаратов от тошноты и обезболивающих, анемия, последствия хирургического вмешательства и применения наркоза, хронический стресс, нарушение сна, подавленность, страх, депрессия, плохое питание, боли. Раковые клетки выделяют вещества, некоторые из которых способны влиять на работу нервной системы.
Считается, что далеко не последнюю роль в развитии химио мозга играет наследственность и индивидуальные особенности организма. Видимо, в группе повышенного риска находятся люди, у которых хуже происходит репарация ДНК, медленнее восстанавливаются нервные клетки, слабее работают нейротрансмиттеры — вещества, которые передают сигналы между нейронами.
Были проведены исследования, посвященные химио мозга, они помогли установить некоторые факты:
- Нарушения не всегда возникают после курса химиотерапии. Известны случаи, когда серьезные симптомы появлялись у больных, которые вообще не получали химиопрепаратов. Иногда ухудшения начинаются после операции или применения гормонов.
- Исследование, проведенное на лабораторных животных, показало, что после применения химиопрепаратов в головном мозге замедляется высвобождение медиаторов дофамина и серотонина.
- Однажды ученые измерили объем головного мозга у женщин, которые 21 год назад проходили курсы химиотерапии по поводу рака молочной железы, и сравнили результаты с показателями здоровых женщин. Оказалось, что после применения химиопрепаратов в мозге уменьшается количество серого вещества, в котором находятся нейроны.
- В другом исследовании ученые обнаружили, что белое вещество головного мозга у женщин, прошедших курсы химиотерапии 9 лет назад, тоже пострадало. У них отмечалась дегенерация (разрушение) аксонов (длинных отростков нервных клеток) и демиелинизация — разрушение оболочки нервных волокон, необходимой для нормального проведения импульсов.
Риски химио мозга повышены у людей старшего возраста, при сопутствующих заболеваниях (сахарный диабет, атеросклероз и др.), применении больших доз химиопрепаратов и лучевой терапии, облучении области головы, локализации основной опухоли или метастазов в головном мозге.
Какие химиопрепараты вызывают самые тяжелые побочные эффекты со стороны головного мозга?
Ученые впервые задались этим вопросом в 2015 году. Было проведено исследование с участием женщин, которые ранее получали лечение разными химиопрепаратами по поводу рака молочной железы.
Участницы, которые лечились химиопрепаратами из группы антрациклинов, хуже справлялись с тестами, и у них в мозге были выявлены более значительные изменения по данным функциональной МРТ.
Основные симптомы
Сами пациенты зачастую описывают свои симптомы так:
Многие онкологические пациенты с умеренными нарушениями памяти, внимания и мышления испытывают депрессию, повышенную тревожность, быстро устают. Сложно сказать, что является первопричиной, а что — следствием.
Как бороться с химио мозга?
Не существует препаратов, которые могли бы повлиять на причину химио мозга и устранить это состояние, потому что сама причина до конца не известна. Однако, врач может помочь. Существуют препараты для симптоматической терапии. Нужно проводить противоопухолевое лечение, бороться с состояниями, которые могут ухудшить работу мозга: анемией, мучительными болями, нарушением сна, ранней менопаузой на фоне гормональной терапии.

В Европейской клинике с пациентами работает психоонколог, он помогает привыкнуть к новому состоянию, вернуться к максимально полноценной жизни.
Что можете сделать вы?
Большое значение в борьбе с побочными эффектами химиотерапии в отношении головного мозга имеет образ жизни. Основные рекомендации:
Сможет ли нервная система восстановиться полностью?
Это индивидуально. Зачастую симптомы химио мозга сохраняются около года, а затем сильно уменьшаются или исчезают. У некоторых больных они довольно сильны в течение многих лет. Из-за проблем с памятью, вниманием и мышлением может потребоваться смена места работы. Некоторые больные получают группу инвалидности.
Обычно симптомы химио мозга становятся более заметными в следующих ситуациях:
- после выхода на работу;
- когда человек одновременно пытается выполнять несколько дел;
- при утомлении.
Химио мозга: результаты недавних исследований
Хотя полная картина механизмов развития химио мозга пока неясна, проведены многие исследования, которые попытались объяснить, что происходит под действием химиопрепаратов в нервной системе на клеточном и молекулярном уровне. Так, согласно одной из теорий, химиопрепараты усиливают выработку цитокинов — сигнальных молекул, которые активируют работу иммунной системы и усиливают воспаление в нервной ткани. Согласно другому предположению, виновниками являются свободные радикалы и окислительный стресс.
В 2018 году ученые из Стэнфордского университета в Калифорнии в экспериментах на мышах показали, что в результате применения химиопрепарата метотрексата в головном мозге повышается активность микроглии — клеток, которые обеспечивают защиту от чужеродных агентов. В итоге нарушается созревание олигодендроцитов (клеток, которые формируют миелиновую оболочку, необходимую для нормального проведения нервных импульсов) и функция астроцитов (клеток, которые обеспечивают питание нейронов и передачу нервных импульсов). Уже существует препарат, который может это исправить, и он проходит испытания на животных.
Современные ученые пока еще пытаются ответить на ряд вопросов:
- Какие препараты сильнее всего нарушают работу головного мозга?
- Можно ли как-то предотвратить это осложнение?
- Как разновидность и доза химиопрепарата, генетические особенности пациента влияют на вероятность развития и степень выраженности химио мозга?
- Какие лекарства помогут бороться с этим состоянием?
Читайте также:


