План обследования менингококкового менингита
- Общий анализ крови
- Общий анализ мочи
- Мазок из носоглотки на менингококк до начала антибактериальной терапии
ПЛАН ЛАБОРАТОРНОГО ОБСЛЕДОВАНИЯ ПАЦИЕНТА С МЕНИНГОКОККОВОЙ ИНФЕКЦИЕЙ, МЕНИНГИТОМ И МЕНИНГОЭНЦЕФАЛИТОМ.
- Общий анализ крови
- Общий анализ мочи
- биохимия крови (мочевина, креатинин, СРБ, ЩФ, K, Na, Ca, Cl, ПТИ, АЛТ, АСТ, сахар крови, общий белок и фракции)
- Мазок из носоглотки на менингококк до начала антибактериальной терапии
- Люмбальная пункция. Исследование ликвора (цитоз, плеоцитоз, белок, реакция Панди, сахар)
- Бактериологическое исследование ликвора на менингококк.
- Бактериоскопия ликвора на менингококк (окраска метиленовым синим).
- Исследование глазного дна.
- МРТ головного мозга.
-РНГА с эритроцитарными антигенными менингококковыми диагностикумами в парных сыворотках крови (при поступлении и на 10-15 день болезни).
- ПЦР на менингококк (материал - ликвор).
1 ВИЧ (вирус иммунодефицита человека) относится к семейству ретровирусов, подсемейству лентивирусы. Выделяют 2 типа ВИЧ – ВИЧ-1 и ВИЧ-2. Наиболее распространен в мире ВИЧ-1, ВИЧ-2 по морфологии ближе вирусу иммунодефицита обезьян – тому самому, который был найден в крови шимпанзе.
При попадании в кровь ВИЧ избирательно прикрепляется к клеткам крови, ответственным за иммунитет, что обусловлено наличием на поверхности этих клеток специфических молекул CD 4, которые распознает ВИЧ. Внутри этих клеток ВИЧ активно размножается и еще до формирования какого-либо иммунного ответа, быстро распространяется по всему организму. В первую очередь поражает лимфоузлы, поскольку там содержится большое количество иммунных клеток.
При прогрессировании заболевания ВИЧ приводит к поражению все большего количества иммунных клеток – лимфоцитов CD 4, количество которых постепенно снижается, достигая в конечном итоге критического числа, что можно считать началом СПИДа.
ПУТИ ЗАРАЖЕНИЯ ВЫ ВСЕ ЗНАЕТЕ.
Пандемия ВИЧ , СПИДА продолжает развиваться (35,3млн чел. – 0,8% чел), максимум в Африке. Выявление вич-инфекции в Новосибе 2012год- 3015 ( общее число-17 315)
Классификация вич- инфекции (рнмц пб спид, в.В.Покровский и о.Г.Юрин, 2001г.)
1.Стадия инкубации -период от момента заражения до ответа организма на него.
2. Стадия ранней ВИЧ-инфекции - первичный ответ организма на инфекцию в виде выработки антител, появления неспецифической клинической симптоматики, развития транзиторного иммунодефицита и проходящих вторичных заболеваний. Эта стадия характеризуется активной репродукцией ВИЧ, кроме того, имеются данные, что выраженность клинической симптоматики, отмечающейся в периоде острой ВИЧ-инфекции коррелирует со скоростью дальнейшего прогрессирования.
В стадии ранней ВИЧ-инфекции различают варианты течения:
- Бессимптомная сероконверсия;
- Острая ВИЧ-инфекция без вторичных заболеваний;
- Острая ВИЧ-инфекция с вторичными заболеваниями;
3. Субклиническая стадия – латентный период, когда компенсаторные возможности макроорганизма способны поддерживать уровень иммунитета, достаточный для защиты от оппортунистических заболеваний. Латентная стадия заменена на субклиническую с учетом возможности в этой стадии высокой репродуктивной активности вируса. Учитывая, что стадии 2Б и 2В не отличаются по прогностическому значению и тактике ведения больного, они объединены в одну субклиническую стадию.
4. Стадия вторичных заболеваний 4А,4Б,4В (в предлагаемом варианте классификации - соответствуют стадиям 3А,3Б,3В в классификации 1989г.) – период обратимой декомпенсации, когда на фоне угнетения иммунитета развиваются вторичные заболевания, но возможны ремиссии (как спонтанные, так и терапевтические) и возможно даже возвращение в латентное состояние.
Фаза 4А обычно начинает развиваться через 3-5 лет от момента заражения. Для нее характерно потеря массы тела менее 10%; развитие бактериальных, грибковых и вирусных поражений слизистых и кожных покровов: поверхностная локализованная кожно-слизистая форма рецидивирующего простого герпеса, кандидоз слизистых оболочек дерматомикозы, себорея и другие; рецидивирующий опоясывающий лишай; повторные воспалительные заболевания верхних дыхательных путей (фарингиты, синуситы, отиты, трахеобронхиты и другие). В этой фазе периоды обострения заболеваний могут чередоваться с периодами ремиссии , но имеют довольно добро-качественное течение и купируются обычными терапевтическими средствами.
Фаза 4Б развивается обычно через 5-7 лет от момента заражения и характеризуется: необъяснимой диареей или лихорадкой более 1 месяца; волосатой лейкоплакией языка; развитием туберкулеза легких; повторными или стойкими вирусными, бактериальными, грибковыми, протозойными поражениями внутренних органов; кожными поражениями, которые носят более глубокий характер и склонны к затяжному течению; повторным или диссеминированным опоясывающим лишаем; локазованной саркомой Капоши. Потеря веса составляет более 10% от исходного. В данной фазе периоды обострения заболеваний чередуются с периодами ремиссии, однако изменения становятся более глубокими, не реагируют на стандартные методы лечения, приобретают упорный, затяжной характер.
Фаза 4 В развивается через 7-10 лет. Характеризуется развитием тяжелых, угрожающих жизни вторичных заболеваний, их генерализованным характером ( генерализованные бактериальные, вирусные, грибковые, протозойные и паразитарные заболевания); поражением ЦНС различной этиологии; кандидозом пищевода, бронхов, легких; развитием внелегочного туберкулеза; атипичными микобактериозами; пневмоцистной пневмонией; кахексией, диссеминированной саркомой Капоши.
В этой фазе периоды обострения могут чередоваться с периодами ремиссии заболевания.
В каждой из них выделяют:
- фазу прогрессирования ( спонтанное; после ранее проводимой противовирусной терапии; на фоне противовирусной терапии);
- фазу ремиссии ( спонтанная; после ранее проводимой противовирусной терапии; на фоне противовирусной терапии).
Однако, без учета уровня вирусной нагрузки и количества СD4 клеток весьма сложно и даже невозможно выделить фазу ремиссии.
5. Терминальная стадия – заболевание неуклонно прогрессирует даже на фоне адекватной противовирусной терапии.
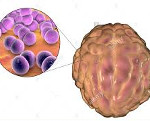
Менингококковый менингит – это форма менингококковой инфекции, которая характеризуется гнойным воспалением мягкой и арахноидальной оболочек головного мозга. Заболевание сопровождается типичной триадой клинических признаков (головной болью, лихорадкой и рвотой), менингеальными знаками, общемозговыми и общетоксическими симптомами. Менингит может сочетаться с менингококцемией, осложняться инфекционно-токсическим шоком, недостаточностью надпочечников, энцефалитом. Решающее значение в диагностике играют методы лабораторной идентификации возбудителя. Основу лечения составляет антибактериальная и патогенетическая терапия.
МКБ-10
- Причины
- Патогенез
- Классификация
- Симптомы менингококкового менингита
- Осложнения
- Диагностика
- Лечение менингококкового менингита
- Прогноз и профилактика
- Цены на лечение
Общие сведения

Причины
Этиологическим фактором менингококкового менингита является менингококк – Neisseria meningitidis. Это парно расположенная шаровидная грамотрицательная бактерия (диплококк), окруженная капсулой с ресничками. Возбудитель обладает низкой устойчивостью к факторам внешней среды, быстро погибает под действием ультрафиолетовых лучей, высоких и низких температур. Менингококки относятся к аэробам, чувствительны к показателям pH, дезинфицирующим агентам.
Микроб имеет сложную антигенную структуру. Различают 13 серогрупп N. meningitidis, отличающихся составом специфического капсульного полисахарида. Наиболее распространены штаммы групп A, B, C, в последнее время регистрируют рост частоты выявления бактерий с антигенами Y и W-135. Возбудителю присуща высокая изменчивость: он подвергается L-трансформации с потерей капсулы, показывает гетероморфный рост, приобретает резистентность к химиопрепаратам.
Главным фактором патогенности менингококка считается эндотоксин – липоолигосахаридный комплекс, выделяющийся при разрушении микробной клетки. Возбудитель способен вырабатывать и ряд других повреждающих веществ (гемолизин, протеазы, гиалуронидазу), проникать сквозь гематоэнцефалический барьер. Фиксация к назофарингеальному эпителию происходит благодаря ресничкам, а капсула защищает бактерию от механизмов фагоцитоза.
Предрасположенность к развитию менингококкового менингита формируется в условиях снижения местной и общей резистентности организма. Факторами риска признаются врожденный дефицит комплемента, ВИЧ-инфекция, анатомическая или функциональная аспления. Слизистая оболочка носоглотки повреждается при курении и ОРВИ, что повышает риск бактериальной инвазии. Распространению инфекции способствует большая скученность населения.
Патогенез
Передача возбудителя происходит воздушно-капельным путем от больных менингококковой инфекцией или бессимптомных носителей. Входными воротами становится слизистая носоглотки, где развивается первичный воспалительный процесс. В 10-20% случаев микробы, преодолев защитные механизмы, проникают в кровоток, где размножаются, инициируя кратковременную бактериемическую фазу. В субарахноидальные пространства головного мозга нейссерии заносятся гематогенным путем, реже – лимфогенно, периваскулярно и периневрально через пластинку решетчатой кости.
При размножении менингококка развивается вначале серозно-гнойное, затем гнойное воспаление мягкой и паутинной оболочек. Чаще всего поражаются конвекситальные поверхности и основание головного мозга, иногда процесс распространяется в спинальном направлении. Макроскопически мягкая оболочка выглядит отечной, гиперемированной, мутной, поверхность мозга будто покрыта шапочкой из гноя. Микроскопическая картина представлена выраженной инфильтрацией полиморфноядерными мононуклеарными клетками. Спаечный процесс может вызвать закупорку путей ликворооттока.
Классификация
Согласно клинической классификации менингококковой инфекции, менингит относится к ее генерализованным формам. С учетом выраженности патологического процесса инфекция может протекать в легкой, среднетяжелой, тяжелой или крайне тяжелой формах. Менингит, вызванный N. meningitidis, является гнойным. Клинически он представлен следующими вариантами:
- Классический. Инфекционный процесс имеет изолированный характер, поражаются только мягкая и паутинная оболочки головного мозга.
- Смешанный. Картина менингита дополняется признаками воспаления мозгового вещества (менингоэнцефалита), бактериемией (менингококцемией).
- Осложненный. Сопровождается развитием локальных и системных осложнений, обусловленных влиянием воспалительных изменений или токсинов возбудителя.
По длительности патологический процесс бывает острым (до 3 месяцев), затяжным (до полугода), хроническим (свыше 6 месяцев). В зависимости от локализации пораженных церебральных структур менингит подразделяется на конвекситальный (большие полушария), базальный (нижняя поверхность) и спинальный. Дополнительно выделяют ограниченную и тотальную формы.
Симптомы менингококкового менингита
Началу болезни обычно предшествует назофарингит, но симптомы могут возникнуть внезапно, на фоне полного благополучия. С большим постоянством в клинической картине обнаруживают так называемую менингеальную триаду – головные боли, лихорадку, рвоту. Температура резко поднимается до 40-42° C, сопровождается сильным ознобом. Мучительные головные боли носят диффузный давяще-распирающий или пульсирующий характер, локализуются преимущественно в лобно-теменной области, усиливаются в ночное время, при перемене положения головы, действии внешних раздражителей.
Среди объективных симптомов на первое место выходят менингеальные знаки, которые появляются в самом начале заболевания и быстро прогрессируют. Наиболее постоянными являются ригидность затылочных мышц, симптомы Кернига и Брудзинского (верхний, средний, нижний). У детей отмечают признак Лесажа, выбухание и пульсацию родничка. Пациент принимает вынужденную позу – лежа на боку с запрокинутой назад головой и подтянутыми к животу коленями. Выраженность менингеального синдрома может не соответствовать тяжести патологии.
При неврологическом осмотре часто выявляют асимметрию сухожильных и кожных рефлексов, ослабляющихся по мере нарастания интоксикации, патологические стопные знаки. Базальные менингиты сопровождаются поражением черепных нервов, особенно III, IV, VII, VIII пар. Наличие стойкого красного дермографизма говорит о сопутствующих вегетативных расстройствах. Признаками интоксикации являются вначале тахикардия, а затем относительная брадикардия, гипотония, приглушенность сердечных тонов. У пациентов учащается дыхание, язык обложен грязно-коричневым налетом, сухой.
Осложнения
Крайне неблагоприятным вариантом является молниеносное течение болезни с отеком-набуханием головного мозга. Ситуация угрожает вклинением стволовых структур в большое затылочное отверстие черепа, что ведет к нарушению витальных функций. Медленное разрешение гнойного воспаления опасно развитием гидроцефалии, у детей младшего возраста могут возникать церебральная гипотония, субдуральный выпот.
Результатом тяжелых или сочетанных форм менингококкового менингита становятся инфекционно-токсический шок, острая надпочечниковая недостаточность. При запоздалом или неадекватном лечении гнойный процесс переходит на эпендиму желудочков и мозговое вещество, осложняясь вентрикулитом (эпендиматитом), энцефалитом. В поздние сроки отмечается риск глухоты, эпилепсии, задержки психомоторного развития у детей.
Диагностика
Установить происхождение менингококкового менингита на основании клинических данных удается при его сочетании с бактериемией. На вероятную этиологию изолированных форм болезни косвенно указывает эпидемиологическая и анамнестическая информация (наличие назофарингита, контакт с больным). Точную верификацию патологии обеспечивают лабораторно-инструментальные методы:
- Клинические анализы. Гемограмма показывает выраженный лейкоцитоз со сдвигом формулы влево, анэозинофилию, ускорение СОЭ. В спинномозговой жидкости отмечается полиморфноядерный плеоцитоз, снижение концентрации глюкозы, повышение белка. Изменения в анализе мочи неспецифичны, свидетельствуют о токсических явлениях.
- Бактериоскопия и посев. Менингококки выявляются в нейтрофилах при прямой бактериоскопии окрашенных по Граму мазков. Посев ликвора на сывороточный агар или другие питательные среды дает возможность уточнить культуральные, ферментные, антигенные свойства возбудителя, определить его чувствительность к антибиотикам.
- Серологические тесты. После выделения менингококка идентифицировать его по серогруппам можно при постановке реакции агглютинации. Для обнаружения антител в крови применяют РНГА, экспресс-диагностику проводят с помощью ИФА, методов встречного иммуноэлектрофореза.
- Молекулярно-генетический анализ. В дополнение к стандартным процедурам используют ПЦР, позволяющую выявить бактериальную ДНК. Это быстрый и чувствительный диагностический тест. Особую ценность он приобретает при невозможности выделить возбудителя из ликвора или крови.
- Нейровизуализация. Показаниями для церебральной томографии могут быть нарушения сознания, очаговые неврологические симптомы. КТ головного мозга подтверждает ликворную гипертензию, внутримозговые кровоизлияния, церебральный отек. МРТ с контрастированием предпочтительнее, так как лучше визуализирует менингеальную оболочку, субарахноидальное пространство.
В качестве дополнительного исследования при судорогах для регистрации биоэлектрической активности мозга назначают ЭЭГ. Помощь в диагностическом поиске оказывают офтальмолог (осмотр глазного дна), инфекционист. Заболевание необходимо дифференцировать с менингитами иной этиологии, эпидуральным абсцессом, субдуральной эмпиемой. Следует исключать энцефалиты, острый рассеянный энцефаломиелит, субарахноидальную гематому.
Лечение менингококкового менингита
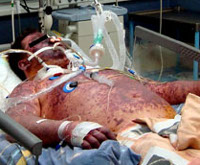
Любые формы генерализованной инфекции сопряжены с высокой опасностью летального исхода и тяжелых осложнений. Поэтому менингококковый менингит должен рассматриваться как неотложное состояние, требующее срочной госпитализации в профильный стационар. Обычно пациенты сразу попадают в палату интенсивной терапии под круглосуточное наблюдение специалистов. Им показан строгий постельный режим. Основой лечения является фармакотерапия:
- Этиотропная. Центральное место отводится антибиотикотерапии препаратами пенициллинового (бензилпенициллином, ампициллином) или цефалоспоринового ряда (цефтриаксоном, цефотаксимом). Альтернативными медикаментами выступают карбапенемы, хлорамфеникол. Сначала назначается эмпирическая терапия, которая затем корректируется с учетом данных антибиотикочувствительности.
- Патогенетическая. Для купирования отека головного мозга используются глюкокортикоиды, осмотические и петлевые диуретики (маннитол, фуросемид). Гемодинамическая нестабильность и токсикоз требуют инфузионной поддержки (кристаллоидами, коллоидами, плазмой), введения вазопрессоров, оксигенотерапии. В тяжелых случаях проводят экстракорпоральную детоксикацию.
- Симптоматическая. В комплексном лечении менингококкового менингита применяют симптоматические препараты. При судорожной активности показаны антиконвульсанты (диазепам, натрия оксибутират). Высокую лихорадку купируют жаропонижающими средствами.
Выписка из стационара осуществляется при полном клиническом выздоровлении. Все пациенты, перенесшие менингококковый менингит, должны находиться под диспансерным наблюдением невролога с прохождением регулярного обследования. Последствия и остаточные явления устраняются комплексной реабилитацией, которая включает физиотерапию, лечебную гимнастику, когнитивную коррекцию.
Прогноз и профилактика
При своевременной специфической терапии менингококкового менингита прогноз относительно благоприятный, сочетанные и осложненные формы существенно ухудшают исход. Генерализованная инфекция всегда сопряжена с риском жизнеугрожающих состояний – даже на фоне лечения уровень летальности составляет 10-15%. Плохими прогностическими факторами считают очаговую неврологическую симптоматику, нарушение сознания, лабораторные сдвиги (анемию, тромбоцитопению, лейкопению).
Профилактика подразумевает воздействие на все звенья эпидемического процесса. В отношении источника инфекции проводят раннее выявление, изоляцию и лечение больных, санацию носителей. Разорвать механизмы передачи помогают санитарно-гигиенические мероприятия, дезинфекция в очаге. Для создания специфического иммунитета у восприимчивых лиц рекомендуют вакцинацию против менингококковой инфекции. Повышению неспецифической резистентности способствует закаливание, своевременная терапия респираторных заболеваний.
![]()
– серьезное воспаление оболочек головного мозга, вызываемое различными бактериями. Как у взрослых, так и у детей основными возбудителями являются Streptococcus pneumoniae, Neisseria meningitidis и Haemophilus influenzae типа b (Hib).
Основное внимание в этом обзоре уделяется бактериальному менингиту, приобретенному вне лечебного учреждения (внебольничная форма); менингит также может быть приобретен в результате инвазивных процедур и травм головы, однако, нозокомиальный менингит выходит за рамки рассмотрения данного обзора.
Наиболее распространенной причиной бактериального менингита в США и во многих странах мира является S. pneumoniae. Однако после введения 13-валентной пневмококковой конъюгированной вакцины (PCV13) количество случаев инвазивной пневмококковой инфекции в Англии и Уэльсе сократилось на 32% по сравнению с исходным уровнем до введения PCV13.
В исследовании было приведено доказательство сопутствующего роста инвазивной пневмококковой инфекции у детей младше 5 лет, вызванной серотипами, не входящими в состав PCV13. В отличие от H. influenzae, которая, главным образом, является возбудителем заболевания у младенцев, S. pneumoniae (и N. meningitidis) может вызвать системную инфекцию в любом возрасте как у детей, так и у взрослых. Listeria monocytogenes является распространенной причиной бактериального менингита у больных, получающих иммуносупрессивные препараты, злоупотребляющих алкоголем и пациентов с сахарным диабетом. У новорожденных основными возбудителями бактериального менингита являются Escherichia coli и Streptococcus agalactiae (стрептококки группы B). Грамотрицательные кишечные палочки (например, Serratia, Acinetobacter, Klebsiella и Pseudomonas aeruginosa) вызывают Патофизиология
Бактерии достигают ЦНС либо гематогенным путем (наиболее распространенный путь), либо путем прямого проникновения из смежного участка. Новорожденные могут заразиться патогенными микроорганизмами в результате соприкосновения с влагалищными выделениями матери при родах, через плаценту или же из окружающей среды.
Как только бактерии попадают в субарахноидальное пространство, они быстро размножаются. Бактериальные компоненты в цереброспинальной жидкости индуцируют выработку различных воспалительных медиаторов, что, в свою очередь, увеличивает приток лейкоцитов в цереброспинальную жидкость.Воспалительный каскад приводит к отеку головного мозга и увеличению внутричерепного давления, что способствует неврологическому повреждению и даже смерти.
Признаки и симптомы бактериального менингита зависят от возраста пациента. Клинически невозможно дифференцировать вирусный и бактериальный менингит. Диагноз подтверждается в ходе физикального обследования и по результатам полимеразной цепной реакции (ПЦР), бактериального исследования ликвора, взятого с помощью люмбальной пункции (ЛП), или бактериального исследования крови (если выполнение ЛП клинически небезопасно).
Классические симптомы менингита у детей и взрослых включают лихорадку, сильную головную боль, ригидность затылочных мышц, светобоязнь, измененный психический статус, рвоту и судороги. У детей чаще наблюдаются судороги при заражении Streptococcus pneumoniae и Haemophilus influenzae типа b (Hib), чем в случае менингококкового менингита.
В раннем детском возрасте, у пожилых людей или больных с ослабленным иммунитетом часто наблюдаются атипичные клинические проявления. У младенцев признаки и симптомы могут быть неспецифическими и включать лихорадку, гипотермию, раздражительность, пронзительный мозговой крик, летаргию, отсутствие аппетита, судороги, апноэ и выбухание родничка. Часто у пожилых пациентов (>65 лет) единственным признаком менингита является дезориентация или нарушение психического состояния.
Необходимо тщательно изучить анамнез, чтобы исключить возможные вирусные инфекции, такие как энтеровирусы (например, другие больные дети или члены семьи) или вирус герпеса (например, высыпание на губах или генитальные поражениях). Следует изучить историю иммунизации против Hib, S. pneumoniae и Neisseria meningitidis.
После исследования состояния жизненно важных показателей и психического состояния необходимо изучить следующие признаки:
![]()
-
Ригидность затылочных мышц
-
Ригидность мышц затылка — сопротивление при наклоне головы к груди — является классическим признаком менингита. Присутствует у 84 % взрослых, однако может присутствовать только у 30 % детей.
-
Петехиальная или пурпурная сыпь обычно сопровождает менингококковый менингит. Хотя только в некоторых случаях у пациентов с лихорадкой и петехиальной сыпью в конечном счете обнаруживается менингококковая инфекция, полученные результаты должны быть срочно проанализированы с целю исключения менингококцемии и следует незамедлительно начать эмпирическую антибактериальную терапию, если не будет поставлен альтернативный диагноз.
-
Присутствие этих признаков указывает на повышенное внутричерепное давление.
-
Пациент может также иметь синусит, пневмонию, мастоидит или средний отит.
-
На это указывает проблематичность попыток двигать глазными яблоками, что, вероятно, связано с увеличением внутричерепного давления. Вследствие повышения внутричерепного давления и воспаления могут поражаться VII и VIII пара черепных нервов. Это повреждение может привести к парезу лицевой мускулатуры, нарушению равновесия и слуха.
-
Положительные признаки являются показателями менингита, обычно наблюдаются у детей старшего возраста и взрослых, но могут отсутствовать у 50 % взрослых. Симптом Кернига: когда пациент лежит на спине, а бедро согнуто под прямым углом, попытка разгибания ноги в коленном суставе вызывает сопротивление. Симптом Брудзинского: при сгибании шеи к груди происходит непроизвольное сгибание коленей и бедер либо пассивное сгибание ноги с одной стороны вызывает контралатеральное сгибание противоположной ноги.
-
При подозрении на бактериальный менингит самым важным анализом является люмбальная пункция для получения ликвора. При бактериальном менингите давление спинномозговой жидкости обычно повышается (>40 см H2O). Количество лейкоцитов в ликворе повышается (обычно >1×10⁹/л [>1000 клеток/мкл]), из которых более 90% составляют полиморфноядерные лейкоциты. Концентрация глюкозы в ликворе по сравнению с сывороткой крови снижается, а содержание белка повышается. Если забрать ликвор у пациента, который еще не начал получать терапию, то при окрашивании по Граму и при бактериальном исследовании ликвора обычно удается выявить возбудитель. В 80% случаев бактериальное исследование ликвора показывает положительный результат. Однако диагностическая ценность этого анализа значительно ниже у пациентов, которые получили антибиотики до того, как был произведен бакпосев. Полисахаридные антигены серогрупп А, В, С, Y и W-135 можно обнаружить с помощью метода латексной агглютинации у 22–93% пациентов с менингококковым менингитом. Антиген может сохраняться в ликворе в течение нескольких дней, что делает этот тест информативным у пациентов, получавших антибиотики до момента забора диагностических образцов, а также для быстрого подтверждения предполагаемого диагноза менингококковой инфекции. В связи с тем, что полисахариды N. meningitidis серогруппы B перекрестно реагируют с полисахаридами Escherichia coli серотипа K1, у новорожденных результаты теста следует интерпретировать с осторожностью. Определение антигена в других биологических жидкостях организма, кроме ликвора (включая сыворотку или мочу) не рекомендовано из-за низкой чувствительности и специфичности. Краниальная КТ должна быть исследована до проведения ЛП, чтобы обнаружить очаговый неврологический дефицит, вновь возникающие судороги, папиллоэдему, аномальный уровень сознания или состояние сниженного иммунитета, и чтобы исключить абсцесс головного мозга или генерализованный отек головного мозга.
-
ПЦР-амплификация бактериальной ДНК, выделенной из крови и ликвора, более чувствительна и специфична, чем традиционные микробиологические методы. Это метод особенно эффективен для дифференцирования бактериального и вирусного менингита. Он также может быть информативен при диагностике бактериального менингита у пациентов, которые уже получили курс антибиотиков.
-
Рутинный анализ крови: необходимо выполнить, включая развернутый анализ крови, электролиты, кальций, магний, фосфор и коагулограмму. Бактериологическое исследование крови: следует проводить у всех пациентов. Как и в случае с ликвором, на результат может повлиять предыдущая антибиотикотерапия. Например, положительные результаты бактериологических исследований крови были зарегистрированы только в 40–70% случаев клинически подозреваемой менингококковой инфекции. Сывороточный С-реактивный белок (CRP): его значение, как правило, повышается у пациентов с бактериальным менингитом. У пациентов, у которых окрашивание ликвора по Граму оказалось отрицательным , а дифференциальный диагноз — между бактериальным и вирусным менингитом, нормальная концентрация С-реактивного белка (CRP) в сыворотке крови исключает бактериальный менингит с достоверностью приблизительно 99%. Прокальцитонин сыворотки крови: имеет чувствительность 99 % и специфичность 83 % при использовании для распознавания бактериального и вирусного менингита. Поэтому нормальная концентрация прокальцитонина в сыворотке обычно исключает бактериальный менингит.
-
Краниальная КТ должна быть исследована до проведения ЛП, чтобы обнаружить очаговый неврологический дефицит, вновь возникающие судороги, папиллоэдему, аномальный уровень сознания или состояние сниженного иммунитета, и чтобы исключить абсцесс головного мозга или генерализованный отек головного мозга. Краниальная визуализация с помощью МРТ может использоваться для выявления основных патологий и осложнений, связанных с менингитом. Инфаркт головного мозга, отек головного мозга и гидроцефалия являются частыми осложнениями, особенно при пневмококковом менингите. Следует обращать внимание на наличие очаговой неврологической симптоматики.
-
≤5 или ≥65 лет
-
Люди крайних возрастных групп обычно подвержены заболеваниям, что обусловлено ослабленным или сниженным иммунитетом. Особенно восприимчивы грудные дети и новорожденные.
-
Обеспечивает идеальную среду для распространения бактерий. Вспышки были зарегистрированы в общежитиях колледжей и в учебных лагерях для новобранцев.
-
Высокий риск заражения Haemophilus influenzae типа b, пневмококковым или менингококковым менингитом.
-
Повышает риск генерализации бактериальных инфекций, вызванных инкапсулированными бактериями, в частности, Streptococcus pneumoniae, Neisseria meningitidis и Haemophilus influenzae.
-
Врожденные или приобретенные анатомические дефекты краниального отдела могут увеличить риск заболевания бактериальным менингитом. При рецидивирующем менингите следует заподозрить анатомические дефекты.
-
У реципиентов систем кохлеарной имплантации риск заболевания бактериальным менингитом значительно выше, чем у населения в целом.
Бактериальный менингит может стать смертельным в течение нескольких часов. Пациентов с подозрением на острый бактериальный менингит следует быстро госпитализировать и определить, нет ли клинических противопоказаний для проведения ЛП. Следует незамедлительно назначить противомикробные препараты. Если ЛП откладывают, поскольку требуется компьютерная томография, антибиотик следует ввести перед сканированием (но после забора образцов крови для бактериологического исследования). Когда идентифицируют конкретный микроорганизм и известны результаты чувствительности к антибиотику, лечение может быть соответствующим образом адаптировано.
При подозрении на бактериальный менингит следует как можно скорее назначить эмпирическую парентеральную антибактериальную терапию широкого спектра (лучше после того, как была выполнена ЛП).
В некоторых странах, если транспортирование в больницу откладывается, рекомендовано введение антибиотиков (например, внутримышечного бензилпенициллина, цефотаксима или цефтриаксона) на этапе первичной медицинской помощи. Хотя доказательства такого подхода неоднозначны.
Выбор эмпирического антибиотика зависит от возраста пациента и условий, которые могут спровоцировать у пациента менингит. Выбранные терапевтические методы должны быть достаточно широкими, чтобы охватить потенциальные патогенные микроорганизмы и другие причины заболевания для данной возрастной группы. В начале терапии следует предположить вероятную резистентность к противомикробным препаратам. Большинство схем эмпирической терапии включают цефалоспорин третьего или четвертого поколения плюс ванкомицин. Ампициллин добавляют в ситуациях, когда Listeria monocytogenes может быть вероятным патогеном (например, пожилые люди, люди с ослабленным иммунитетом и новорожденные).
Далее следует предлагаемая стратегия лечения, основанная на возрасте и конкретных предрасполагающих условиях.
-
Возраст ≤ 1 месяц иммунокомпетентный пациент: цефотаксим или цефтриаксон + ампициллин Возраст > 1 месяц и Возраст ≥ 50 лет или пациент с ослабленным иммунитетом: ампициллин + цефотаксим или цефтриаксон + ванкомицин.
Если цефалоспорин нельзя вводить (например, аллергия), альтернативные антибиотики включают карбапенем (например, меропенем) или хлорамфеникол. Для новорожденных можно использовать аминогликозид (например, гентамицин). Триметоприм/сульфаметоксазол являются альтернативой ампициллину (это не касается новорожденных).
Было показано, что дополнительная терапия дексаметазоном, назначенная до первой дозы антибиотиков и продолжающаяся в течение 4-х дней, улучшает исход заболевания. Как правило, дополнительный дексаметазон рекомендован всем взрослым и детям, которые были до этого здоровы и не страдали иммунодефицитом. Его не следует назначать пациентам с ослабленным иммунитетом и тем, кто уже получил антимикробную терапию. Существуют отдельные доказательства низкого качества, согласно которым дексаметазон может снизить смертность и избежать потери слуха у новорожденных. Однако, ввиду низкого их качества, в настоящее время кортикостероиды для новорожденных не рекомендованы.
Добавление кортикостероидов к антибактериальной терапии обусловливало незначительное снижение смертности, но при этом отмечалось значительное снижение показателей потери слуха и неврологических последствий. Однако потенциальная польза была доказана только для бактериального менингита, вызванного Haemophilus influenzae или Streptococcus pneumoniae. Существует мало доказательств в поддержку применения дексаметазона в случаях, вызванных другими бактериями (например, в случае менингококкового менингита); дексаметазон следует отменить, как только будет исключена инфекция H. influenzae и S. pneumoniae.
Анализ данных в подгруппах показал, что кортикостероиды снижают смертность при менингите, вызванном S. pneumoniae, но неэффективны при менингите, вызванном Haemophilus influenzae типа b (Hib) или Neisseria meningitidis. Кортикостероиды уменьшают тяжелую потерю слуха у детей с менингитом Hib, но не так эффективны у детей с менингитом, вызванном другими патогенами, а не Haemophilus.
После подтверждения диагноза (обычно в течение 12–48 часов после госпитализации) антибиотикотерапия может быть скорректирована в зависимости от возбудителя и его чувствительности к антибиотику. Как правило, продолжительность антибиотикотерапии зависит от клинического ответа и микробиологического ответа ликвора после начала лечения. Поддерживающая терапия, например инфузионная, должна продолжаться.
Читайте также:


