Сепация при муковисцидозе болит горло и голова
Как лечить?


Муковисцидоз представляет собой генетическое заболевание, то есть единственной причиной болезни выступает наследственность. Она поражает в первую очередь железы внешней секреции, органы дыхательной и пищеварительной систем. Организм больного претерпевает патологические изменения, потому своевременное выявление заболевания и его лечение необходимы. В данной статье мы расскажем, каким бывает муковисцидоз у взрослых, каковы его симптомы, методы диагностики и терапия.
Формы болезни
Форма заболевания определяется наиболее пораженной им зоной. То есть, если в первую очередь поражены, например, легкие, то мы наблюдаем муковисцидоз легких. Однако это не означает, что остальные органы не подвержены воздействию патологии, поскольку при любой ее форме, как правило, происходят сбои в разных системах организма.
Таким образом, муковисцидоз делится на следующие формы:
- легочная;
- кишечная;
- мекониевая непроходимость кишечника (встречается у детей нескольких дней жизни и почти никогда — у взрослых);
- смешанная.
Симптомы и осложнения муковисцидоза
Каждая форма муковисцидоза проявляется по-разному и имеет свои симптомы, которые следует рассмотреть отдельно.
Для данного вида болезни характерно появление кашля, сопровождающегося рвотными позывами. Если заболевание проявляется с раннего возраста (а в большинстве случаев его признаки наблюдаются уже в первые годы жизни ребенка), то у взрослого больного кашель будет иметь хроническую форму.
Итак, главные симптомы при легочном муковисцидозе:
- бледность кожи и ее землистый оттенок;
- апатия и вялость;
- пониженный вес при нормальном аппетите;
- коклюшеподобный кашель, сопровождающийся густой мокротой, со слизью и гноем – в случае наслоения бактериальной флоры.
Вязкость мокроты постепенно приводит к мукостазу, а также закупорке бронхов, что чревато пневмонией в тяжелой форме. Тогда наблюдаются также следующие признаки:
- общий цианоз;
- грудная клетка приобретает форму бочки;
- кожные покровы приобретают синеватый оттенок;
- искривление грудной клетки;
- одышка в покое;
- понижение аппетита и уменьшение веса;
- искривление пальцевых фаланг.
Если болезнь имеет длительное течение, то поражается также носоглотка. В таком случае добавляются следующие патологии:
- аденоиды;
- образование полипов в носоглотке;
- синусит;
- тонзиллит в хронической форме.
Для данного вида в первую очередь характерна секреторная недостаточность ЖКТ. В кишечнике наблюдаются гнилостные процессы, что провоцирует накопление газов, а, следовательно, и вздутие живота.
Кроме того, в этом случае отмечаются следующие симптомы:
- учащение дефекации;
- сильная сухость во рту;
- понижение тонуса мышц;
- гипотрофия, приводящая к снижению веса;
- полигиповитаминоз;
- болевые ощущения в животе, в зоне правого подреберья и в мышцах.
Осложнениями при этой форме выступают:
- язва двенадцатиперстной кишки;
- язва тонкого кишечника;
- вторичная форма пиелонефрита;
- вторичная форма дисахаридазной недостаточности;
- мочекаменная болезнь;
- непроходимость кишечника.
В некоторых случаях может развиваться билиарный цирроз, при котором к симптомам добавляется жжение кожных покровов и желтуха.
Советуем к прочтению также материалы: причины и лечение экзогенного альвеолита, причины и избавление от свиста при выдохе, что такое ХОБЛ.
Данная форма болезни считается самой тяжелой, поскольку она протекает с симптомами легочной и кишечной форм вместе. Степень их выраженности разная в каждом отдельном случае. Разделяют 4 стадии болезни данного вида:
- Сухой кашель без отхождения мокроты. Одышка возникает лишь после физических нагрузок. Эта стадия заболевания может длиться до 10 лет.
- Появление хронического бронхита, что приводит к возникновению мокроты при кашле. Одышка возникает от напряжений. Происходит искривление пальцевых фаланг. Эта стадия длится от 2 до 15 лет.
- Бронхолегочный процесс на этой стадии прогрессирует и провоцирует осложнения. Дыхательная и сердечная недостаточность четко выражены. Стадия длится 3 — 5 лет.
- Дыхательная и сердечная недостаточность на данной стадии приобретают тяжелую форму. Состояние может продолжаться несколько месяцев и закончиться летальным исходом.
Диагностика
Для выявления муковисцидоза применяются следующие методы диагностики:
- Бронхоскопия . Проводится для изучения консистенции мокроты.
- Общие анализы . Включают анализы крови и мочи.
- Потовый тест . Выступает самым информативным для установления диагноза при муковисцидозе.
- Бронхография . Для обнаружения бронхоэктазов.
- Анализ ДНК . Для установления мутаций гена, приводящих к заболеванию.
- Микробиологическое исследование . Изучение мокроты.
- Спирометрия . Проводится для изучения состояния легких.
- Рентгенография . Для исследования изменений в легких и бронхах.
- Копрограмма . Исследование кала для установления объема жира, содержащегося в нем.
Лечение муковисцидоза
К сожалению, муковисцидоз не поддается излечению, поэтому терапия при данном заболевании симптоматическая, направлена на восстановление органов дыхания и желудочно-кишечного тракта и зависит от степени выраженности проявлений.
- Легочная форма болезни . Здесь необходимо восстановить проходимость бронхов и снизить вязкость мокрот, а также предотвратить воспаление и инфекции. В таком случае назначаются муколитики в виде аэрозолей и ингаляций и ферментативные средства. Кроме того, рекомендуются лечебная физкультура и массаж грудины.
- Кишечная форма . Рекомендуется пища с высоким содержанием протеинов. Больным следует употреблять рыбу, мясо, творог, яйца. Углеводы и жиры необходимо сократить. Лечение может включать применение пищеварительных ферментов и витаминов. Эффективность терапии выявляется на основе состояния кала, исчезновения болей и нормализации массы тела.
- Если болезнь сопровождается пневмонией или бронхитом, то потребуется проведение антибактериальной терапии. Тяжелое течение пневмонии создает необходимость применения кортикостероидов на протяжении пары месяцев.
- С целью улучшения питания миокарда следует использовать метаболитики.
- В случаях отсутствия эффекта от вышеописанного лечения может применяться бронхоскопия с промыванием бронхов, которое осуществляют с помощью хлорида натрия и ацетилцистеина.
В последнее время широко используются так называемые откашливатели, которые имитируют кашель давлением в дыхательных путях. Такие приборы очень важны для эффективного устранения мокроты.
Пересадка легких
Поскольку рассматриваемая нами болезнь не поддается полному лечению, специалисты все чаще сходятся во мнении, что выходом из ситуации может стать пересадка легких.
С одной стороны трансплантация дает возможность избавиться от большого количества проявлений заболевания, а также предотвратить развитие инфекционных процессов в легких в будущем.
Но с другой стороны важно отметить, что после хирургического вмешательства все же существует вероятность отторжения трансплантата. К тому же больному понадобится по-прежнему принимать различные медикаментозные средства для борьбы с болезнью, а также препараты, препятствующие отторжению. Следует отметить, что подобное серьезное вмешательство при ослабленном болезнью организме может закончиться летальным исходом.

Burkholderia cepacia представляет собой палочковидную бактерию, которая передается от пациента к пациенту. Таким образом, пациенты МВ-носители сепации могут заразить других пациентов с МВ.
1. Характеристика Буркхолдерия сепация
Burkholderia (B.) cepacia представляет собой палочковидную бактерию длиной 1,6-3,2 мкм (для сравнения: один волосок имеет толщину около 100 мкм). Он был обнаружен в 1949 году Уолтером Х. Буркхолдером и до 1992 года считался Pseudomonas (см. Часть 1: Pseudomonas aeruginosa).
Возбудитель B. cepacia очень адаптируется. Обладая нитевидными клеточными процессами, он присоединяется в дыхательных путях к компонентам слизи и к клеткам слизистой оболочки. B. cepacia образует биопленки, которые защищают ее от антибиотиков. Патогенные микроорганизмы устойчивы ко многим различным антибиотикам. Им даже удается выжить в легких или иммунных клетках.
В 1997 году уже было известно пять геномоваров, позже стало десять. Тем временем все геномовары были официально переименованы в их собственные бактериальные разновидности. Комплекс Burkholderia cepacia в настоящее время включает не менее 17 различных видов.
Важными для муковисцидоза являются B. cenocepacia (ранее Genomovar III), B. dolosa (ранее Genomovar VI) и B. multivorans (ранее Genomovar II). Эти бактерии различаются тем, насколько они опасны, и насколько серьезные осложнения они вызывают.
Есть ли другие виды буркхолдерий?
Есть много других видов Burkholderia, которые не имеют ничего общего с комплексом Burkholderia cepacia. Это, например, B. gladioli и B. pseudomallei. Хотя B. gladioli при муковисцидозе также играют определенную роль.
Burkholderia pseudomallei встречается в тропических регионах Юго-Восточной Азии и в Австралии в основном в сезон дождей (см. Часть 6: Редкие патогены). Это может вызвать опасную для жизни инфекцию легких под названием мелиоидоз. Многие врачи предостерегают больных муковисцидозом от соответствующих поездок.
2. Путь заражения
Откуда берутся бактерии?
Как бактерии попадают в организм?
Бактерии B. cepacia передаются от пациента к пациенту. Это означает, что инфицированные пациенты с муковисцидозом могут инфицировать других пациентов. Респираторные выделения и мокрота играют важную роль, поскольку они содержат большое количество бактерий Burkholderia.
Во многих случаях возбудитель также поглощается из источников окружающей среды, таких как почва или гнилой лук. Также климатические условия, возможно, играют определенную роль, потому что в Австралии было больше B. cepacia, когда было много дождей.
3. Осложнения и болезни
Насколько распространена сепация при муковисцидозе?
В целом, только несколько пациентов из амбулаторных клиник по муковисцидозу в Германии инфицированы сепацией; их доля всегда была ниже 5% в последние годы.
Также известно, что разные виды сепации встречаются по-разному в разных странах и что их распределение со временем также меняется. Например, B. cenocepacia была менее распространена в некоторых странах после введения строгих правил гигиены (см. Ниже). В Германии преобладают Б. multivorans и Б. cenocepacia.
Какие осложнения и расстройства вызывает комплекс B. cepacia?
Патогенные микроорганизмы опасны для людей со слабым иммунитетом, например, страдающим гранулематозом с полиангиитом. При этом заболевании функция белых кровяных клеток настолько нарушена, что они больше не способны адекватно уничтожать вторгающиеся патогены. У этих пациентов сепация вызывают опасную для жизни пневмонию.
Иммунная система отдельных пациентов по-разному реагирует на возбудителя. Хотя у некоторых пациентов с B. cepacia, они не развиваются. Когда инфекция, вызванная B. cenocepacia, становится хронической, наиболее распространенным эффектом является несколько более быстрое прогрессирование заболевания легких, как это наблюдается например при инфекции Pseudomonas aeruginosa.
У пациентов с муковисцидозом B. cenocepacia (Genomovar III) и B. multivorans (Genomovar II) вызывают самые большие осложнения. Наблюдалось значительное сокращение выживаемости, чем у неинфицированных пациентов. Даже после трансплантации легкого часто наблюдали более плохое течение, когда пациенты с МВ были инфицированы комплексом B. cepacia. Перед трансплантацией имеет смысл провести детальное исследование бактерий у пациентов с сепацией.
4. Диагностика
Как выявить бактерии?
Взятие мазка из зева или образца мокроты является одним из обычных обследований во время ежеквартального амбулаторного посещения центра МВ. Целью является поиск комплекса Burkholderia cepacia с использованием специальных питательных сред. Затем проверяется, какие антибиотики эффективны против патогенов (тест на резистентность).
Поскольку доступны более мощные аналитические методы, идентификация бактерий Burkholderia для микробиологической лаборатории больше не является такой сложной, как раньше. В Ганновере и Мюнхене две консультационные лаборатории по бактериологии муковисцидоза позволяют провести детальный анализ отправленных образцов мокроты.
5. Лечение
Каким правилам должны следовать люди, живущие с Burkholderia cepacia?
Эти бактерии могут передаваться от пациента к пациенту. Поэтому гигиенические меры чрезвычайно важны для предотвращения перекрестного инфицирования. Амбулаторные клиники МВ разработали для этой цели специальные правила гигиены.
При посещении машины скорой помощи МВ или в больнице инфицированный пациент должен тщательно дезинфицировать руки. Ношение маски рекомендуется. Следует соблюдать осторожность, чтобы отделить пациентов с сепацией от других пациентов с МВ. Они получают специальные назначения для консультации, используют отдельный вход в здание и проходят лечение в определенной консультационной комнате.
Во время пребывания в больнице носители сепации обычно находятся в отдельной палате. Персонал и посетители надевают в комнате специальную защитную одежду, одноразовые перчатки и хирургическую маску.
Если люди с сепацией приходят к врачу или обращаются к физиотерапевтам или другим медицинским работникам, они должны информировать врача о своем носительстве.
Сообщество МВ просит пациентов с проблемными микробами, такими как сепация, добровольно воздерживаться от участия в мероприятиях и семинарах. В обычных социальных контактах, в повседневной жизни или в школе никаких специальных мер не требуется.
Какие антибиотики подходят для лечения?
Если сепация была впервые высеяна у пациента, результаты будут перепроверены. Нередко бактерии снова исчезают сами собой. Лечение антибиотиками необходимо в любом случае, если состояние легких резко ухудшается. Тогда говорят об обострении.
Лечение сепации нелегко, потому что бактерии устойчивы ко многим антибиотикам, которые обычно используются при муковисцидозе. Тем не менее, есть несколько хороших эффективных антибиотиков, которые можно использовать. Их выбор производится после теста на чувствительность (антибиограмма).
Обычно внутривенная комбинированная терапия (инфузионная терапия) проводится с двумя различными антибиотиками. Эффективные агенты обычно включают меропенем в комбинации с цефтазидимом, амикацином или миноциклином. Котримоксазол и тетрациклины также действуют против сепации. Некоторые эксперты также рекомендуют высокие дозы ингаляционного тобрамицина в качестве партнера по комбинации.
Бактерии комплекса B. cepacia по своей природе устойчивы к колистину. Если пациент инфицирован только сепацией, а не другими бактериями, он не должен использовать этот антибиотик для ежедневного ингалирования.
Исследователи в настоящее время разрабатывают новые антибиотики, в которых препарат помещается в крошечные жировые капли (липосомы). Такие препараты могли бы лучше проникать в клетки сепации и, возможно, работать лучше.
Насколько успешно лечение антибиотиками?
Большинство пациентов хорошо реагируют на лечение. Если инфекция Burkholderia cepacia существует в течение длительного времени, бактерии действительно подавляются лечением антибиотиками, но не уничтожаются. Следовательно, сепация все еще будет встречается в мокроте после лечения.
6. Защита от инфекции
Как защитить себя от заражения?
Важным потенциальным источником инфекции являются другие пациенты с муковисцидозом, инфицированные сепацией. Поэтому, отделяют пациентов с сепацией от других пациентов с муковисцидозом, например разделяя по часам консультаций и специальным кабинетам.
Кроме того, амбулаторные клиники по поводу муковисцидоза установили правила гигиены в больницах, которые должны соблюдаться как персоналом, так и пациентами и родителями. Особенно важную роль играет тщательное мытье и дезинфекция рук. Насколько успешны эти гигиенические меры, показывает исследование из Манчестера. Там частота выявления сепации у взрослых была снижена с 16% до 3%.
Во влажных помещениях с нормальной домашней обстановкой сепация встречается редко. Даже свежие фрукты и овощи, как правило, не являются источником опасности, с другой стороны, гнилой лук может стать источником Burkholderia cepacia, поэтому его следует избегать.
Можете ли вы сделать прививку против сепации?
До сих пор нет вакцины против комплекса B. cepacia. Усилия исследователей пока не увенчались успехом, в том числе потому, что слишком мало известно об иммунном ответе организма.
Находятся ли другие люди в группе риска, если они находятся в контакте с пациентами с сепацией?
У пациентов с МВ носителей комплекса B. cepacia нет особого риска для здоровых членов семьи, друзей или одноклассников.
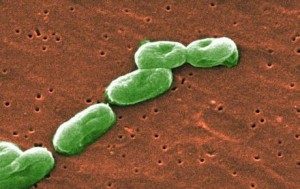
Что такое Burkholderia cepacia
Burkholderia cepacia комплекс (B. cepacia) состоит из нескольких видов граммотрицательных аэробных палочек.
В природе бактерия встречается в почве, воде и на растениях и живет преимущественно во влажной среде при температуре 30 — 35 градусов по Цельсию. Впервые бактерия была обнаружена в 1949 году Вальтером Буркхолдером в Корнельском университете в гниющем луке. В 1950-х годах стали появляться сообщения о развитии инфекций, вызванных B. Cepacia у пациентов, которым проводилась установка венозных и мочевыводящих катетеров. В 1970-х годах впервые было сообщено о заражении больных МВ B. Cepacia.
С этого времени началось быстрое распространение инфекции в различных европейских центрах МВ, что потребовало введения жестких ограничений на социальные и внутрибольничные контакты больных МВ с различной бактериальной флорой. В настоящее время инфицирование пациентов с МВ B. Cepacia во многих клиниках является противопоказанием к пересадке легких из за значительно более худшего прогноза выживаемости. Однако некоторые клиники в мире, тем не менее, принимают таких пациентов.
Виды B. cepacia
В 1992 году были выделены 9 основных вариантов Burkholderia
| Вид | Genomovar |
| Burkholderia cepacia | I |
| Burkholderia multivorans | II |
| Burkholderia cenocepacia | III |
| Burkholderia stabilis | IV |
| Burkholderia vietnamiensis | V |
| Burkholderia dolosa | VI |
| Burkholderia ambifaria | VII |
| Burkholderia anthina | VIII |
| Burkholderia pyrrocinia | IX |
С тех пор дополнительно изучено до 60 вариантов Burkholderia, большинство из которых клинического значения не имеют.
Как влияет инфицирование B.
cepacia на течение муковисцидоза
В настоящее время выделяют 3 типа реакций больного на заражение, зависимых от штамма В. сepacia, а именно:
1. отсутствие явных изменений в респираторном тракте, стабильное течение заболевания;
2. быстрое ухудшение респираторной функции с лихорадкой, потерей массы тела с развитием Cepacia-синдрома (сопровождающегося высокой лихорадкой, бактериемией, прогрессирующим ухудшением показателей функции внешнего дыхания);
3. фульминантное ухудшение респираторного статуса.
Считается, что наиболее тяжелые последствия в виде развития Cepacia-синдрома может вызвать заражение видами Burkholderia cenocepacia и Burkholderia multivorans. Burkholderia dolosa вызывает весьма быстрое ухудшение легочной функции.
Геном Burkholderia cepacia устроен так, что микроорганизм крайне быстро мутирует, вырабатывая все новые механизмы защиты от антибиотиков. Именно такая высокая способность защиты создает серьезную опасность заражения больных МВ этой палочкой.
Каковы способы заражения B. cepacia? Меры профилактики
Пациенты с МВ могут заразиться B. cepacia от других пациентов, заражение происходит воздушно-капельным путем, при рукопожатии и других близких контактах, а также косвенно, при использовании общих санузлов и предметов обихода. В сухой внешней среде бактерия выживает до 2 часов, во влажной – более суток.
Медицинская практика показывает, что большинство людей с B. cepacia заразились при случайном контакте с уже инфицированными пациентами при участии в общественных мероприятиях, в больницах.
В центрах помощи больным МВ, в больницах необходима строгая изоляция пациентов, как на амбулаторном приеме, так и при нахождении в стационаре, соблюдение гигиены рук и помещений, использование разного респираторного оборудования.
Большое внимание больным МВ следует уделить стерилизации небулайзеров и правильному их хранению. В ряде исследований показано, что в неблайзерах можно обнаружить до 15 видов различых бактерий, в том числе и B. cepacia, которые быстро вырабатывают устойчивость к антибиотикам, вдыхаемым через небулайзер.
Симптомы и диагностика
Симптомы при заражении B. Cepacia такие же, как симптомы любого воспаления у людей с МВ: лихорадка, кашель, заложенность носа, одышка, свистящее дыхание. Единственный способ диагностики – посев мокроты на специальных средах.
Больные МВ с колонизацией B. cepacia, должны быть еще более ответственными и выполнять абсолютно все рекомендации специалистов из центра МВ. Бронхолитики, муколитики, хорошее питание, очистка дыхательных путей, предотвращение простудных заболеваний, своевременная плановая антибиотикотерапия должны применяться постоянно.
К сожалению, бактерия очень устойчива к антибиотикам, но некоторые комбинации лекарств способны успешно сдерживать рост этих бактерий.
Разработаны схемы лечения инфекции при первичном высеве, хронической инфекции вне обострения, и при обострении. Важно регулярно проводить посевы мокроты на чувствительность к антибиотикам и своевременно корректировать антибиотикотерапию.
Схемы лечения Burkholderia cepacia
(Семыкин С.Ю. (Отделение медицинской генетики Российской детской клинической больницы,) Постников С.С.(Кафедра клинической фармакологии РГМУ) Поликарпова С.В (ГКБ № 15)
| Клиническая ситуация | Лечение |
| Первый высев B. Cepacia complex (B. multivorans | Цефтазидим 300 мг/кг + меропенем 120 мг/кг + тобрамицин 12 мг/кг в/в – 14 дней ингаляции тобрамицина (Брамитоб, TOBI) 300 мг х 2 р.д. – 3 месяца |
| Хроническая колонизация B. Cepacia complex | Бисептол 12-20 мг/кг по триметоприму per os Хлорамфеникол 25 мг/кг х 4 р.д. Per os Доксициклин (старше 12 лет) 100-200 мг х 1 р.д. Per os Ингаляции амилорида (1 мг/мл в 4,5 мл 0,12% NaCl) и тобрамицина (Брамитоб, TOBI) х 3 раза в день -1-6 месяцев |
| обострение хронической инфекции | Цефтазидим 300 мг/кг + меропенем 120 мг/кг + бисептол 12-20 мг/кг по триметоприму в/в – 3 недели |
Перспективные научные исследования
Инфицирование пациентов с МВ B. Cepacia является большой проблемой во всем мире. В среднем количество инфицированных пациентов составляет около 2-3%, но сильно варьирует в разных странах и в разных центрах МВ. В России за период 2003-2009 годы количество инфицированных B. Cepaci пациентов возросло с 2% до 8%. (Семыкин С.Ю., Постников С.С., Поликарпова С.В.)
Научные разработки ведутся, как в области поиска новых антибиотиков, так и в области поиска путей преодоления антиботикорезистентности бактерий. Кратко отметим несколько исследований, опубликованных недавно.

В Кемеровской области завершена проверка по факту заражения 20 детей с муковисцидозом смертельной для них бактерией — цепацией. Этот микроорганизм сокращает жизнь больных в разы. Роспотребнадзор не обнаружил в местной больнице ни следов инфекции, ни связи между госпитализацией маленьких пациентов и их массовым инфицированием. Чиновники уверяют, что цепацию дети могли подхватить где угодно. Однако эксперты утверждают, что после ремонта и дезинфекции стационара искать там цепацию было бесполезно, а система оказания помощи детям с муковисцидозом в России организована так, что массовое заражение может в любой момент произойти в любом регионе.
Муковисцидоз — неизлечимое генетическое заболевание, связанное с поражением желез внешней секреции. Это самая распространенная болезнь среди так называемых орфанных (редких). В России ею страдают более 3 тыс. человек. Раньше такие пациенты практически не доживали до совершеннолетия. Современные методы позволяют продлевать больным жизнь на десятилетия, но таких пациентов надо беречь. У больных муковисцидозом людей есть своя смертельно опасная бактерия — цепация (Burkhodelia cepacia). Безвредный для здорового человека микроорганизм очень хорошо себя чувствует в легких больного муковисцидозом, где скапливается мокрота, приводит к ухудшению состояния и даже смерти.
Типичная проблема
— К сожалению, наши лечебные учреждения не адаптированы к нуждам такой категории пациентов, — пояснила Елена Кондратьева. — Это повсеместная проблема. Такая ситуация, как в Кемерово, может сложиться и в других местах. Наша цель — сделать так, чтобы больше этого не повторилось.
Долгий путь бактерии
Вопрос о том, как инфекция оказалась в областной больнице, остается открытым. Местные чиновники говорят, что заразиться больные дети могли где угодно.
В письме, разосланном в августе в регионы, указывается именно штамм 709 — как эпидемически значимый. Интересен и список адресатов. Это главные специалисты по детству и главные пульмонологи региональных минздравов. И одно федеральное учреждение — РДКБ Минздрава России.
Зампредседателя комиссии Общественной палаты РФ по социальной политике Екатерина Курбангалеева, которая первая в Москве забила тревогу в связи с кемеровской ситуацией, обратилась к руководителям Росздравнадзора и Роспотребнадзора с просьбой провести проверку во всех медучреждениях, где в последние годы лечились инфицированные кемеровские дети. Это в первую очередь педиатрическое отделение РДКБ и областная кемеровская больница. По мнению члена ОП, это позволит избежать кривотолков, а главное — принять меры по ликвидации источника заражения там, где он будет выявлен.
Она считает результаты проверки местного Роспотребнадзора недостаточными.
Вспышка из прошлого
Родителям больных муковисцидозом детей, перешагнувших 10-летний возраст, название штамма 709 может сказать о многом. В 2008 году бактерией этого типа заразились почти все, кого тогда госпитализировали в РДКБ. Местные медики долго не признавали проблему, однако в итоге замять скандал не удалось.
Председатель московской областной ассоциации больных муковисцидозом Ольга Алекина вспоминает, как в 2008-м ей надо было пролечить в стационаре 14-летнего сына Алексея. Уже тогда среди родителей ходили тревожные слухи, и класть мальчика в РДКБ она не решилась, ограничившись амбулаторным лечением. Сейчас Алексею 23, заражения цепацией он избежал.
До ремонта, вспоминает Ольга Алекина, в отделении жил грибок, был один туалет на всех. Помещение перестроили, сделали палаты на двух человек, организовали цепационное отделение.
— Отделение педиатрии разделено на два отсека, — рассказал Петр Шумилов. — Отдельно отгорожены стеклянной перегородкой боксы, где находятся дети с цепацией. Они просто так не гуляют по другим палатам, а находятся в своих боксах. Когда доктора заходят в цепационное отделение, они меняют халат, обрабатывают перед выходом руки.
Петр Шумилов заверил, что у пациентов с цепацией и без нее разное оборудование, заражение больных через поверхности исключено. В то же время он признал, что между двумя категориями пациентов возможны контакты.
— Это же не тюрьма. И это дети. Чтобы пройти в отсек с цепацией, пациент должен пройти через отделение, — отметил замглавврача.
Особая проблема — в том, что вновь поступившие дети направляются в общее отделение, если только в их истории болезни не указано наличие цепации. Анализы у них берут, но результаты приходят только через неделю. Получается, что, если региональная лаборатория проглядела бактерию, ребенок, у которого она есть, несколько дней контактирует с незараженными.
По мнению Петра Шумилова, ответить на вопрос, где впервые появился штамм 709, без серьезного бактериологического расследования вряд ли возможно. Инфицированные пациенты приезжают из регионов в РДКБ, из Москвы разъезжаются по регионам. Без создания системы раздельного лечения разных категорий больных этот вопрос не решить. Причем это касается не только цепации и больных муковисцидозом. Аналогичная проблема и у пациентов со многими другими сложными диагнозами.
Специалисты по муковисцидозу сходятся во мнении, что таких больных надо лечить амбулаторно и не госпитализировать без особой необходимости. Это позволило бы минимизировать контакты между пациентами. Тем более что такова мировая практика. Однако в России она не распространена. Осложняет положение то, что госпитализация лучше оплачивается учреждениям, чем амбулаторное лечение. Прием у врача стоит 320 рублей. Госпитализация больного с муковисцидозом по квоте на высокотехнологичную медицинскую помощь (ВМП) обходится в 140 тыс. рублей, по системе ОМС — от 80 до 180 тыс. в зависимости от региона.
Читайте также:


