Гипоксически ишемический церебральный паралич
Гипоксия или асфиксия в родах может привести к ДЦП. Одним из наиболее распространенных типов повреждения мозга, вызванного недостатком кислорода, называют гипоксическо-ишемическую энцефалопатию. Она часто приводит к развитию серьезных двигательных или когнитивных нарушений, которые становятся более очевидными, как ребенок продолжает развиваться .
Гипоксически-ишемическая энцефалопатия - это повреждение головного мозга, вызванное гипоксией или асфиксией в родах. Если недостаток кислорода происходит в течение короткого периода, организм новорожденного способен скомпенсировать это состояние. Но если асфиксия длится слишком долго, ткани мозга разрушаются. Гипоксически-ишемическая энцефалопатия плода или новорожденного является ведущей причиной смерти или тяжелых нарушений среди детей.
Нарушения могут включать в себя эпилепсию, задержку развития, двигательные нарушения, психомоторную задержку и когнитивные нарушения. Как правило, тяжесть нарушений не может быть определена, пока ребенок не достигнет возраста трех-четырех лет.
Когда возникает гипоксически-ишемическая энцефалопатия?
Гипоксически-ишемическоая энцефалопатия чаще развивается у доношенных новорожденных, хотя это случается также и у недоношенных детей. . Если травма происходит до 35 недели развития плода, гипоксически-ишемическая энцефалопатия, приведет к перивентрикулярной лейкомаляции (ПВЛ).
В 40 недель степень гипоксии повлияет на область поражения головного мозга; легкая гипоксия повлияет на парасагиттальной белое вещество, а тяжелая гипоксия влияет на скорлуу, таламус и парацентральное белое вещество. Область пораженного мозга будет иметь значительное влияние на симптомы, которые ребенок испытывает.
Каковы факторы риска и причины гипоксически-ишемической энцефалопатии?
Асфиксия является наиболее значимым фактором риска для ГИЭ. От степени и продолжительности кислородного голодания зависит, разовьется гипоксически-ишемическая энцефалопатия или нет, и насколько серьезными будут последствия. Факторы, могут привести к асфиксии:
- Острая гипотония матери
- Кровь, содержащая меньше кислорода из-за плохо функционирующих легких
- Осложнения со стороны сердца
- Травмы от клинически узкого таза
- Травмы от осложнений со стороны пуповины
- Нарушение кровоснабжения мозга во время родов
- Остановка дыхания или гипоксия
- Кровотечение в родах
- Медицинская халатность
- Выпадение пуповины
- Отслойка плаценты
- Давление на череп с изменение его формы, в результате чего развивается кровотечение или ишемия
- Низкое предлежание плаценты
- Стресс во время родов
- Травма
- Разрыв матки
Инсульт плода также увеличивает вероятность развития гипоксии-ишемической энцефалопатии. Факторы, которые могут привести к инсульта плода включают в себя:
- Нарушения свертывания крови
- Нарушение кровотока в плаценте
- Аномальные кровеносные сосуды, которые могут привести к разрыву
- Высокое или низкое давление у матери
- Инфекции у матери, особенно воспаление тазовых органов
Как поставить диагноз гипоксически-ишемической энцефалопатии?
При подозрении на гипоксически-ишемическую энцефалопатию проводятся методы нейровизуализации, чаще всего магнитно-резонансная томография.
Для того, чтобы выполнить эти исследования, врачи должны сначала заподозрить гипоксически-ишемическую энцефалопатию. Если роды были травматические, или если значительные факторы риска, такие как инсульт плода были известны во время беременности, гипоксически-ишемическая энцефалопатия может быть заподозрена при рождении. В противном случае, родители, врачи, воспитатели должны обратить внимание на видимые признаки, которые могут развиваться в течение длительного времени – задержку психо-моторного развития и задержку роста.
Некоторые признаки могут появиться вскоре после рождения. Дисфункция органов, особенно сердца, легких, почек, печени и крови будут указать возможность развития ГИЭ. Судороги в первые 24 часов жизни также может указывать на вероятность гипоксически-ишемической энцефалопатии.
Как лечится гипоксически-ишемическая энцефалопатия?
Лечение гипоксически-ишемической энцефалопатии сосредоточено на оказании помощи ребенку адаптироваться к нарушениям, которые возникают в результате травмы головного мозга. Методы реабилитации обычно используются для лечения церебрального паралича, вызванного гипоксической-ишемической энцефалопатией.
Асфиксия обычно вызывает стойкое повреждение, которое иногда продолжает прогрессировать даже после выхода из асфиксии. Чтобы предотвратить дальнейшее повреждение ребенка может быть медицинской контролировать, чтобы:
- Поддержание нормального уровня глюкозы в крови
- Поддержание нормального артериального давления
- Предотвращение или контроль за судорогами
- Предотвратщение или минимизация отека мозга
Как предотвратить гипоксически-ишемическую энцефалопатию?
Лучший способ предотвратить ГИЭ - это предотвращение асфиксии во время беременности и родов. Осознание наличия факторов риска возникновения гипоксии-ишемической энцефалопатии может помочь родителям и медицинскому персоналу предотвратить возможные осложнения .
Профилактические меры должны быть приняты во время беременности и во время родов включают в себя:
- Узнайте о важности электронного мониторинга плода во время родов
- Подтвердите практикующих врачей, выбранных для участия в процессе доставки квалифицированы, чтобы контролировать беременность и рождение
- Обеспечить определенный медицинский совет и личные предпочтения для персонала при прибытии в больницу, особенно если врач матери не доступен
- Убедитесь, что квалифицированный, сертифицированный и должным образом обучены и акушер анестезиолог доступны во время родов
- Поймите прав пациентов, в частности право на второй взгляд, право не быть ворвались в трудное решение, когда требуется, и право требовать личных медицинских записей

Четыре типа травмы или пороков развития головного мозга, которые вызывают ДЦП
Перивентрикулярная лейкомаляция
После перенесенной церебральной ишемии (любой степени) новорожденный ребенок должен наблюдаться у невропатолога. Последствия церебральной ишемии могут быть самыми разными — от минимальных отклонений в развитии до довольно тяжелых.

Прогноз во многом зависит от тяжести перенесенной гипоксии и степени тяжести энцефалопатии.
Так, при I степени гипоксически-ишемической энцефалопатии, прогноз благоприятный; при II степени — сомнительный (т. е. многое зависит от наличия или отсутствия сопутствующей патологии и от особенностей организма ребенка); при III степени — прогноз для полного выздоровления, как правило, неблагоприятный.
Российская ассоциация специалистов перинатальной медицины разработала классификацию последствий перинатальный поражений нервной системы у детей первого года жизни.
Согласно этой классификации различают следующие виды последствий церебральной ишемии:
- Последствия церебральной ишемии-гипоксии I-II степени (перинатальная транзиторная гипоксически-ишемическая энцефалопатия).
Основные клинические формы последствий церебральной ишемии I-II степени:
- Доброкачественная внутричерепная гипертензия;
- Расстройство вегетативной автономной нервной системы;
- Гиперактивной поведение, гипервозбудимость;
- Нарушение/задержка моторного развития;
- Сочетанные формы задержки, умственная отсталость не уточненная;
- Симптоматические судороги и ситуационно обусловлены пароксизмальные расстройства.
- Следует отметить, что при перинатальной транзитронной гипоксически-ишемической энцефалопатии проходит полная компенсация неврологических отклонений на первом году жизни. В некоторых случаях могут сохраняться не грубые функциональные нарушения.
- Последствия церебральной ишемии-гипоксии II-III степени (перинатальное стойкое(органическое) постгипоксическое поражение ЦНС).
Основные клинические формы последствий церебральной ишемии II-III степени:
- Различные формы гидроцефалии;
- Органические формы нарушения психического развития;
- Детские церебральные параличи (ДЦП);
- Симптоматические эпилепсии и эпилептические синдромы раннего детского возраста.
- Для перинатального стойкого постгипоксического поражения ЦНС характерно то, что неврологические отклонения не компенсируются к 1 году. При этом сохраняются тотальный или парциальный неврологический дефицит. В этом заключается главное отличие транзиторного (проходящего) поражения ЦНС от стойкого (органического).
Последствия церебральной ишемии-гипоксии 1-2 степени
Клинические проявления: течение данного симптомокомплекса подострое (нарастание симптомов происходит постепенно). Отмечается увеличение окружности головы ребенка в первом полугодии, которое несколько отличается от нормы. У доношенных увеличение отмечается более чем на 1 см (но не более 3 см), у недоношенных более 2 см (но не более 4 см). Также имеет место расхождение черепных швов, напряжение и выбухание большого родничка, срыгивания, не связанные с приемом пищи, повышенная возбудимость и раздражительность у ребенка, трудности при засыпании, поверхностный сон, оживление сухожильных рефлексов.
Обследование при доброкачественной внутричерепной гипертензии
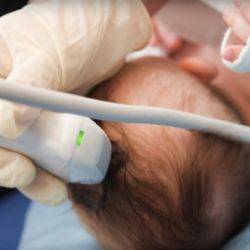
На НСГ, чаще всего, выявляют умеренное расширение ликворосодержащих пространств, усиленная пульсация крупных церебральных артерий.
На фоне проводимого лечения, при данной патологии ,компенсация неврологических нарушений наступает к 3-6 месяцам жизни.
При этом, следует отметить, что данный симптомокомплкес имеет диагностическое значение, только при исключении соматических заболеваний у ребенка.
Компенсация неврологических нарушений, как правило, наступает к 3-6 месяцам жизни, на фоне проводимой терапии.
Для данной патологии характерно: чрезмерная двигательная активность, мышечная дистония, эмоциональная лабильность. У детей отмечается неустойчивая концентрация внимания и сосредоточения, быстрая их истощаемоть. Дети плохо засыпают, сон у них поверхностный, часто просыпаются. Часто отмечается тремор и оживление рефлексов.
Обследование при синдроме гипервозбудимости и гиперактивности

На ЭЭГ — может не быть отклонений от возрастной нормы. В состоянии спокойного бодрствования может отмечаться замедление и дезорганизация основного коркового ритма, признаки задержки созревания БЭА, а также регуляторные нарушения со стороны подкорковых систем, различной степени тяжести.
На НСГ структурные изменения, как правило, не выявляются.
Компенсация неврологических расстройств, также отмечается в возрасте 3-6 месяцев (на фоне проводимой консервативной терапии).
Небольшая задержка сроков редукции (угасания) безусловных двигательных автоматизмов. Немного запоздалое формирование возрастных физиологических моторных реакций у ребенка — установочных реакций, зрительно-мотороного возаимодействия, мануальной деятельности (работа руками), выпрямляющих реакций (подготовка к стоянию, ходьбе), функции равновесия, ходьбы. В результате чего, дети начинают позже держать голову, сидеть, ползать, стоять, ходить. Могут отмечаться нарушения мышечного тонуса в виде гипотонии, гипертонуса или дистонии. Указанные нарушения имеют преходящий характер и на фоне корригирующих мероприятий компенсируются к 1-1,5 годам.
Дополнительные методы обследования
По показаниям (для исключения структурных повреждений мозга) проводят НСГ, КТ, МРТ.
ЭЭГ — для оценки состояния биоэлектрической активности мозга.
ЭНМГ — для оценки состояния нервно-мышечной проводимости.
Данный симптомокоплекс имеет диагностическое значение в тех случаях, когда исключены другие причины (рахит, метаболические нарушения и др.)
Клинические признаки: судороги, пароксизмальные расстройства, впервые возникшие после периода новорожденности. Причиной приступа могут быть: повышение температуры тела, чрезмерное возбуждение, боль, токсикоз, эксикоз, инфекционный процесс и другие. Приступы могут проявляться в виде различных судорог (клонические, тонические, тонико-клонические), а также в виде атонических пароксизмов.
Для симптоматических судорог характерно: носят транзиторный характер, быстро купируются самостоятельно либо при назначении симптоматического лечения, отсутсвует стереотипность возникновения и протекания припадков (это свойственно для эпилепсии).
- ЭЭГ — для оценки состояния биоэлектрической активности мозга.
- НСГ — как правило, структурных изменений головного мозга не выявляется.
- МРТ и КТ проводят по показаниям.
Для транзиторной гипоксически-ишемической энцефалопатии характерно, то что судорожные приступы (на фоне монотерапии минимальными дозами антиконвульсантов) отсутствуют в течение трех месяцев и более и больше не повторяются на протяжении первого года жизни ребенка.
Также, не следует забывать о том, что мозг детей раннего возраста обладает огромными пластическими и репаративными (восстановительными) возможностями и при проведении всех методов восстановительного лечения можно добиться очень хороших результатов.
Аннотация научной статьи по клинической медицине, автор научной работы — Медведев М.И., Дегтярева М.Г., Горбунов А.В., Гребенникова О.В., Дуленков А.Б.
Среди наблюдаемых 104 доношенных новорожденных с гипоксическим перинатальным поражением ЦНС после проведения комплексного лучевого обследования выделена группа риска (6 пациентов) по формированию детского церебрального паралича (ДЦП). Данная группа выделялась на основе выявления ранних структурных изменений головного мозга. Проведение ЭЭГ-обследования у данных детей выявляло неблагоприятные паттерны биоэлектрической активности головного мозга. Патологические клинические симптомы формирования ДЦП у всех доношенных детей проявлялись уже в первом полугодии жизни, диагноз был установлен к 6 месяцам. Выявление детей группы риска по ДЦП позволяет на более ранних сроках проводить комплексную нейрореабилитацию.
Похожие темы научных работ по клинической медицине , автор научной работы — Медведев М.И., Дегтярева М.Г., Горбунов А.В., Гребенникова О.В., Дуленков А.Б.
М.И. Медведев1, М.Г. Дегтярева1, А.В. Горбунов1, О.В. Гребенникова1,
А.Б. Дуленков2, В.В. Воронов2
ПОСЛЕДСТВИЯ ПЕРИНАТАЛЬНЫХ ГИПОКСИЧЕСКИ-ИШЕМИЧЕСКИХ ПОРАЖЕНИЙ ГОЛОВНОГО МОЗГА У ДОНОШЕННЫХ НОВОРОЖДЕННЫХ: ДИАГНОСТИКА И ПРИНЦИПЫ ВОССТАНОВИТЕЛЬНОГО ЛЕЧЕНИЯ
1Кафедра неонатологии и научно-исследовательская лаборатория профилактики и лечения постгипоксических состояний у новорожденных ГОУ ВПО Российский государственный медицинский университет им. Н.И. Пирогова Росздрава; 2Городская больница № 8, Москва
Среди наблюдаемых 104 доношенных новорожденных с гипоксическим перинатальным поражением ЦНС после проведения комплексного лучевого обследования выделена группа риска (6 пациентов) по формированию детского церебрального паралича (ДЦП). Данная группа выделялась на основе выявления ранних структурных изменений головного мозга. Проведение ЭЭГ-обследования у данных детей выявляло неблагоприятные паттерны биоэлектрической активности головного мозга. Патологические клинические симптомы формирования ДЦП у всех доношенных детей проявлялись уже в первом полугодии жизни, диагноз был установлен к 6 месяцам. Выявление детей группы риска по ДЦП позволяет на более ранних сроках проводить комплексную нейрореабилитацию. Ключевые слова: дети, перинатальная церебральная гипоксия-ишемия, асфиксия, судороги, нейро-визуализация, лейкомаляция, электроэнцефалография, детский церебральный паралич.
Examination of 104 full-term neonates with hypoxic perinatal CNS damage included complex X-ray examination permitted to select risk group of cerebral palsy development (6 patients). Selection of this group was based on detection of early structural brain changes. EEG-examination of these patients showed unfavorable patterns of brain bioelectric activity. Pathologic clinical signs of cerebral palsy development appeared in first half-year of life and diagnosis was proved in the age of 6 months. Selection of children with high risk of cerebral palsy remits to begin complex neurorehabilitation as early as possible.
Key words: children, perinatal brain hypoxia-ischemia, asphyxia, seizures, neurovisualization, leucomalacia, electroencephalography, cerebral palsy.
Перинатальные гипоксически-ишемические поражения головного мозга у новорожденных детей различного гестационного возраста (ГВ) и их последствия представляют собой одну из актуальных проблем современной медицины. У новорожденных, рожденных в срок, они наблюдаются в 15-30%, а у недоношенных новорожденных, включая детей с экстремально низкой массой тела, - в 40-60% [1, 2]. В дальнейшем у них могут сформироваться такие тяжелые заболевания, как детские церебральные параличи (ДЦП), симптоматические формы эпилепсии, органические формы слабоумия и др. 4. Эти заболевания
нервной системы являются одними из причин ранней детской инвалидности и социальной дезадаптации 2. Важнейшими задачами для специалистов перинатальной медицины на сегодняшний день являются разработка методов комплексной диагностики перинатальной церебральной гипоксии-ишемии начиная с антенатального периода с оценкой состояния нервной системы плода и новорожденного и определения критериев по будущему психомоторному развитию, а также создание эффективной системы комплексной нейрореаби-литации, включающей эффективную медикаментозную церебропротекцию.
Медведев Михаил Иванович - д.м.н., проф. каф. неонатологии ГОУ ВПО РГМУ
им. Н.И. Пирогова Росздрава
Адрес: 117997 г. Москва, ул. Островитянова, 1
Тел.: (495) 612-78-81, E-mail: medvedok57@gmail.com
Статья поступила 15.12.10, принята к печати 23.12.10.
Целью настоящего исследования явилась разработка системы оценки состояния нервной системы у доношенных новорожденных и в первые месяцы жизни при перинатальных гипоксичес-ки-ишемических поражениях головного мозга для выявления ранних симптомов церебрального паралича, используя комплекс следующих показателей: клинических, данных методов нейрови-зуализации, изучения становления биоэлектрической активности (БЭА) головного мозга с помощью ЭЭГ.
Материалы и методы исследования
Наблюдали 104 доношенных новорожденных, перенесших церебральную гипоксию-ишемию средней и тяжелой степени в перинатальном периоде. Данные по результатам исследования неблагоприятных исходов перинатальных поражений ЦНС и лечения 246 недоношенных детей представлены в нашей предыдущей публикации [6].
Настоящее исследование носило проспективно-ретроспективный характер (начиная с неона-тального периода). Церебральные параличи сформировались в группе доношенных детей у 6 пациентов из 104. Основной причиной формирования ДЦП во всех случаях явилась церебральная гипоксия-ишемия тяжелой степени.
Диагноз перинатального гипоксически-ишемичес-кого поражения головного мозга и его степень тяжести устанавливали в соответствии с классификацией РАСПМ, а последствия этого поражения и форму ДЦП -в соответствии с классификацией РАСПМ и МКБ 10 [5]. Группа риска по развитию ДЦП формировалась после выявления структурных изменений головного мозга.
ГВ наблюдаемых детей варьировал от 37 до 41 недели. Во всех случаях отмечен отягощенный акушерско-гинекологический анамнез по хронической гипоксии плода или острой асфиксии новорожденных. Среди 104 доношенных новорожденных с перинатальной гипоксией у 6 сформировался ДЦП, что составило около 5% в обследованной
Результаты и их обсуждение
Клинической иллюстрацией может служить наблюдение ребенка Г., пострадавшего от тяжелой асфиксии в родах, рожденного на сроке 37 недель гестации с оценкой по шкале Апгар 2/4 балла. После рождения проводились реанимационные мероприятия, ИВЛ. Со 2-х суток появились неонатальные судороги клонического характера. На рис. 1 представлена ЭЭГ, на рис. 2 - КТ головного мозга ребенка Г.
Динамическое наблюдение за ребенком Г. после купирования синдрома угнетения в возрасте 3 недель выявило резкое нарастание мышечного тонуса в раз-
Рис. 1. Фрагмент ЭЭГ ребенка Г., в возрасте 3 недель. Клинический диагноз: тяжелая асфиксия в родах, синдром угнетения, церебральная ишемия III степени (диффузный некроз коры, субкортикальная лейкома-ляция, ранние неонатальные судороги). Общий паттерн БЭА не соответствует возрасту и степени гестационной зрелости ребенка и свидетельствует о нарушении функционального состояния ЦНС тяжелой степени. Сон не дифференцирован на фазы и представлен однородным паттерном угнетения БЭА на протяжении 45 мин регистрации. На этом фоне регистрируются периодические латерализованные разряды эпилепти-формной активности в левом полушарии, длительностью от 3,5-4 до 7-8 с, сопровождающиеся клонически-ми судорогами конечностей.
Рис. 2. КТ головного мозга ребенка Г. в возрасте 2 мес. Диагноз: последствия церебральной ишемии Ш степени, формирующийся ДЦП, тетраплегическая форма, субкортикальная лейкомаляция.
Определяются субкортикальные кисты в лобных и височных областях, выраженное расширение боковых желудочков мозга и субарахноидальных пространств -формирующаяся кортикальная атрофия.
Другой иллюстрацией может служить наблюдение ребенка Л., родившегося в срок, но в родах перенесшего тяжелую асфиксию - оценка по шкале Апгар 2/4 балла. С первых часов жизни отмечены неонатальные судороги полиморфного характера с периодическими длительными апное. Ребенку проводилась ИВЛ в течение 7 дней. По данным НСГ в первые 5 дней жизни выявлялись явления отека головного мозга, а со 2-й недели начали формироваться множественные кисты. Уже со 2-й недели в неврологическом статусе появилась выраженная спастика в разгибательных группах мышц и патологические симптомы (клонусы, синкинезии). В возрасте 3 недель для уточнения характера структурных изменений головного мозга была проведена КТ, где были выявлены грубые деструктивные изменения в виде кистозной энцефалолейкомаляции (рис. 3).
Объективными клиническими критериями для установления диагноза ДЦП у ребенка Л., 3 недель, были следующие:
2) отсутствие формирования произвольных мотивированных движений;
Рис. 3. КТ ребенка Л. в возрасте 3 недель, перенесшего тяжелую интранатальную асфиксию. Диагноз: гипок-сически-ишемическое поражение головного мозга тяжелой степени, синдром угнетения, неонатальные судороги, формирующийся ДЦП, тетраплегическая форма, диффузная энцефалолейкомаляция. Вещество мозга представлено множеством кистозных полостей, плотность которых приближается к плотности ликвора, и визуализируется в виде стенок кист и желудочков.
3) нарушение формирования возрастных цепных реакций с доминированием патологических рефлексов и дистонических эпизодов после 1 месяца;
4) наличие патологических рефлексов: рефлекторных синкинезий, клонусов, псевдобульбарных автоматизмов.
Таким образом, уже в первом полугодии у наблюдаемых 6 из 104 детей, родившихся доношенными с перинатальной гипоксией, был установлен клинический диагноз ДЦП.
Таким образом, в результате проведенного нами динамического наблюдения за 104 доношенными детьми, рожденными с перинатальной церебральной гипоксией-ишемией, выявлено, что для раннего выявления группы риска по развитию ДЦП необходимо проведение комплексного обследования, как клинического с использованием балльных шкал развития, так и с обязательным применением этапной лучевой диагностики, позволяющей выявлять структурные изменения головного мозга, детерминирующих формирование неврологических расстройств и развитие ДЦП [4, 5, 8]. Клинические показатели психомоторного развития для детей, перенесших перинатальную гипоксию, должны быть дополнены показателями БЭА головного мозга с помощью ЭЭГ. Среди клинических показателей, определяющих неблагоприятный исход по развитию ДЦП, наиболее важными являются неонатальные судороги. Раннее выявление патологических паттернов IV и V типов на ЭЭГ коррелирует с неблагоприятым исходом -формированием ДЦП [6, 7]. Комплексная терапия детей с последствиями перинатальных гипокси-чески-ишемических поражений головного мозга должна проводиться с обязательным использованием ноотропных препаратов - производных нейропептидов и аминокислот, улучшающих обменные процессы головного мозга, стимули-рущих синаптогенез, что является необходимым для лечения и профилактики неблагоприятных последствий перинатальной церебральной гипоксии-ишемии [6, 9-11].
1. Барашнев Ю.И. Перинатальная неврология. M.: Триа-да-Х, 2001: 640.
2. Неонатология: Национальное руководство. Под ред. Н.Н. Володина. М.: ГЭОТАР-Медиа, 2007: 848.
3. Барашнев Ю.И. Клинико-морфологическая характеристика и исходы церебральных расстройств при гипоксически-ишеми-ческих энцефалопатиях. Акуш. и гин., 2000; 5: 39-42.
4. Volpe J. Neurology of Newborn. N.Y.: Ch. L., 2002: 930 р.
6. Володин Н.Н., Медведев М.И., Горбунов А.В. и др. Ранняя диагностика неблагоприятных последствий перинатальных гипоксически-ишемических поражений головного мозга у недоношенных детей и оптимизация их лечения. Педиатрия, 2010; 89 (2): 101-107.
7. Строганова ТА., Дегтярева М.Г., Володин Н.Н. Электроэнцефалография в неонатологии. Под ред. Н.Н. Володина. М.: ГЭОТАР-МЕД, 2005.
8. Володин Н.Н., Медведев М.И., Горбунов А.В. Компьютерная томография головного мозга у новорожденных и детей раннего возраста. М.: ГЭОТАР-Медиа, 2002: 117.
10. Асташкин Е.И. Влияние актовегина на энергетический обмен клеток при ишемии. Труды ММА им. И.М. Сеченова. М., 2009: 1-4.
11. Wahlgren NG, Ahmed N. Neuroprotection in cerebral ischaemia: facts and fancies - the need for new approaches. Cerebrovasc Dis. 2004; 17 (Suppl. 1): 153-166.
DC Ппипип! Ы R Кплптпип! Ы R Нпиплпртт! Г A 4niiii^un2
Нехватка кислорода в организме человека в считаные секунды наносит иногда непоправимый вред. Гипоксически-ишемическая энцефалопатия (ГИЭ) иногда звучит страшным приговором как для ребенка, так и для взрослого. Давайте разберемся, что это за болезнь, ее симптомы и насколько опасно гипоксически-ишемическое поражение головного мозга в любом возрасте.

Особенности патологии
У взрослых частой причиной патологии становятся травмы или имеющиеся серьезные заболевания. Если при приступе удушья помощь не будет оказана вовремя, то есть серьезный риск летального исхода или инвалидности. Немаловажную роль играет и степень тяжести патологии, чем она выше, тем меньше шансов у человека на возврат к полноценной жизни.
Когда наступает кислородное голодание в важнейшей части центральной нервной системы, это приводит к дефициту этого вещества в клетках мозга, что замедляет кровоток и все метаболические процессы. При таком недостатке питания нейроны мозга в некоторых участках органа начинают отмирать, приводя к неврологическим нарушениям.
Ускоряет процесс отек мозга, возникающий также из-за сбоя в кровообращении. Давление растет, и клетки начинают быстрее гибнуть. Чем быстрее проходит процесс, тем больше шансов на то, что повреждения будут необратимыми.
Причины возникновения
Гипоксическая энцефалопатия у взрослых и у детей возникает по разным причинам. Их важно знать, чтобы принять все меры для ее предупреждения.
Гипоксическая ишемическая энцефалопатия возникает на фоне нехватки кислорода, к чему приводят следующие причины:
- состояние удушья;
- удушение;
- сбой дыхательной системы любого рода происхождения;
- наркотическая зависимость, передозировка;
- патологии кровеносной системы, приводящие к ее непроходимости или разрыву;
- цианид, окись углерода — отравление;
- длительное пребывание в задымленном месте;
- травма трахеи;
- остановка сердца;
- болезни, приводящие к параличу мышечной ткани дыхательной системы.
Острая гипоксическая энцефалопатия наступает, если кислород не поступал в организм несколько минут. Это тяжелое течение патологии, которое чаще всего заканчивается летальным исходом. Зафиксированы единичные случаи, когда люди выживали, но для них это заканчивалось тяжелой формой серьезных психических болезней.
Причиной такого состояния у только родившегося ребенка может быть:
- удушье во время родов из-за слабой родовой деятельности;
- преждевременный родовой процесс или с патологическими факторами, такими как выпадение пуповины;
- болезни инфекционного генеза у матери;
- ряд физических факторов от грязного воздуха до радиационного излучения.

Именно асфиксия у грудничков является самым частым фактором, приводящим к ГИЭ. Врачи выделяют следующие факторы риска для ее возникновения:
- гипотония острой формы у роженицы;
- недоразвитость легких, что приводит к недостатку кислорода в крови;
- сложности в работе сердца;
- травмирование плода узким тазом матери или из-за проблем с пуповиной;
- сложности в родовой деятельности, травма, стресс;
- гипоксия;
- родовое кровотечение;
- халатность медицинского персонала;
- отслойка плаценты;
- изменение формы черепа плода из-за давления;
- родовая травма, разрыв матки;
- низкое предлежание плаценты.
Степени тяжести и характерные симптомы
Гипоксически-ишемическая энцефалопатия имеет 3 степени тяжести, для которых характерны свои проявления. По ним врачи часто дают предварительную характеристику повреждений мозговой деятельности и приблизительный прогноз.
При такой степени у больного будет:
- расширен зрачок и широко открыты веки;
- отсутствовать концентрация внимания;
- нарушена координация движений, блуждающее поведение;
- выявлена либо сонливость, либо гипервозбудимость;
- высокая степень раздражительности;
- отсутствовать аппетит;
- нарушено мозговое кровообращение.
Неврология при ней будет более выражена, т. к. нарушение насыщения мозга кислородом более длительное:
- у малыша спонтанные крики без причины;
- защитный и опорный рефлекс либо ослаблен, либо отсутствует вовсе;
- признаки мышечной слабости;
- опущение верхнего века;
- увеличение давления цереброспинальной жидкости;
- метаболический ацидоз крови;
- невралгические приступы;
- сбой в глотательном процессе.
Поражение в таких случаях более тяжелое, что проявляется в:
- судорожности;
- синюшности кожи;
- потере сознания;
- гипертензии;
- отсутствии двигательных возможностей;
- косоглазии;
- коме или прекоме;
- отсутствии реакции зрачков на свет;
- сбое дыхательного процесса с сильной аритмией;
- тахикардии.

ПЭП — это разновидность гипоксически-ишемической энцефалопатии у детей раннего возраста. Ее диагностируют как сразу после рождения, так и на первом году жизни. Развивается ПЭП как внутриутробно, в процессе родовой деятельности, так и в первые 10 дней с момента рождения.
Она может быть трех степеней тяжести с характерной симптоматикой и протекать в острой форме — до месяца, в раннем восстановлении функций — до 4 месяцев, при позднем восстановлении — до 2 лет.
Диагностика
Перинатальный синдром ишемии на фоне гипоксии мозга начинают диагностировать, делая визуальный осмотр ребенка. Так же и со взрослыми. Несмотря на все достижения медицины, уникальный тест, позволяющий точно выявить ГИЭ, до сих пор не придуман. Все лабораторные методики направлены на выявление того, насколько сильно поврежден мозг и текущее состояние всего организма.
Какими будут исследования, зависит от симптомов, и как они развивались. Для расшифровки анализов есть специальные биомаркеры, которые дают полную картину о степени ГИЭ. Для исследования нужна кровь больного.
Нейровизуализацию проводят с помощью:
- нейросонографа и/или МРТ, томографа, показывающего внутренние повреждения мозга и изменения в нем;
- доплерографа, фиксирующего работу мозгового кровотока;
- электронейромиографа для определения чувствительности волокон периферии нервной системы.
Дополнительного могут использовать:
- электроэнцефалограф для выявления задержки развития на ранней стадии и есть ли эпилепсия;
- видеомониторинг для изучения двигательной активности малышей.

При необходимости пострадавшего осматривает окулист, чтобы определить состояние зрительных нервов и глазного дна, а также на наличие болезней генетического типа в этой области.
Лечение и уход
За пострадавшими должен быть особый уход, а за детьми, перенёсшими ГИЭ, он строится на контроле за:
- Хирургически, для восстановления и улучшения кровообращения в мозгу. Чаще всего для этих целей используют эндоваскулярную методику, которая не нарушает целостность тканей.
- Медикаментозно, выбирая препараты в зависимости от того, насколько тяжелая степень поражения и ее клинической картины.
- На антиконвульсантах, которые купируют судороги. Обычно это Фенобарбитал, дозировку которого подбирают индивидуально. Внутривенный способ самый быстрый. Но сам препарат противопоказан при сверхчувствительности, тяжелой форме гипоксической и гиперкаптической дыхательной недостаточности, проблемах с почкам и печенью, при беременности. Может быть использован Лоразепам, у него аналогичное воздействие и список противопоказаний.
- На сердечно-сосудистых средствах, чтобы увеличить системное сопротивление сосудов и сократительную функцию миокарда, что приводит к повышенному сердечному выбросу. Все средства этой группы влияют на почки, а при передозировке побочные эффекты предсказать сложно. Чаще всего используют Допамин, Добутамин.
Дальнейшее наблюдение
Из стационара выписывают только после прохождения полного курса физической терапии и комплексной оценки нервно-психического развития. Чаще всего после выписки пациенты не требуют специфического ухода, но регулярные осмотры в клинике обязательны, особенно для детей.
Если болезнь была тяжелой, то ребенок будет наблюдаться в специальном центре, где ему будет помогать врач по нервно-психическому развитию.
Лечение судорожности зависит от симптоматики центральной нервной системы и результатов исследований. Выписывают только с легким отклонением от нормы или вовсе в ее пределах. Фенобарбитал убирают постепенно, но обычно его пьют после выписки не менее 3 месяцев.
Прогноз и последствия
У взрослых прогноз зависит от степени поражения мозга патологией. Самыми частыми последствиями перинатальной ГИЭ являются:
- задержка в развитии ребенка;
- дисфункции мозга в плане внимания, сосредоточенности на обучении;
- нестабильная работа внутренних систем организма;
- эпилептические припадки;
- гидроцефалия;
- вегетососудистая дистония.

Не нужно думать, что это приговор, даже разлад в центральной нервной системе корректируют, обеспечивая нормальную жизнь пациентам. Треть людей с этим расстройством излечивается полностью.
Профилактика
Если речь идет о взрослых, то все профилактические мероприятия должны быть направлены на полный отказ от вредных привычек. При этом нужно регулярно заниматься спортом, избегая чрезмерных нагрузок, правильно питаться, проходить регулярные медицинские осмотры, чтобы выявить опасные патологии на ранней стадии для их успешного купирования.
От травм никто не застрахован, но если более осторожно себя вести, то и их можно минимизировать.
Снизить риск ГИЭ у новорожденного может только его мама еще в период беременности. Для этого нужно:
- строго следить за режимом дня и личной гигиеной;
- отказаться от никотина и алкоголя даже в минимальной дозировке;
- проходить вовремя обследования у врачей и диагностику, особенно у невролога;
- доверить роды только квалифицированному персоналу.
Гипоксически-ишемическая энцефалопатия опасная болезнь, но ее можно предотвратить, и даже вылечить, но только если помощь была оказана вовремя и в дальнейшем врачебные рекомендации не нарушаются.
Читайте также:


