Нутритивный статус при дцп
В статье рассматриваются нарушения нутритивного статуса у детей с церебральным параличом (ДЦП). Обсуждаются значение ожирения, гипотрофии, мальнутриции и факторов риска по их развитию. Отдельно рассматривается микронутриентный статус при ДЦП.
Abnormalities in nutritional status of children with cerebral palsy (CP) are considered. The significance of obesity, hypotrophy, malnutrition and risk factors for its development are discussed. Micronutrient status in patients with CP is specially addressed.
О проблемах с приемом пищи и нарушениях ассимиляции нутриентов при детском церебральном параличе (ДЦП) на протяжении последних 50 лет неоднократно сообщалось в работах исследователей из различных стран. Общеизвестно, что проблемы с приемом и утилизацией пищи могут сопровождаться нарушениями нутритивного статуса [1, 2]. Направленность последних может быть диаметрально противоположной, то есть у пациентов с ДЦП встречаются как мальнутриция, так и ожирение.
Как указывают K. L. Bell и P. S. Davies (2003), у детей с церебральным параличом чаще встречаются изменения в составе тела, они оказываются ниже ростом и имеют массу тела меньше, чем их здоровые сверстники [3]. Выраженные нарушения нутритивного статуса (мальнутриция) при отсутствии их соответствующей адекватной коррекции могут вызывать нарушения со стороны иммунной и эндокринной систем, приводить к нейромышечной дисфункции и нарушениям когнитивной деятельности [3].
У части детей с ДЦП, при отсутствии выраженных орально-моторных проблем, например, при спастическом тетрапарезе, может отмечаться избыточная прибавка в весе. Это происходит в связи с тем, что ограниченный объем физической активности в совокупности с пониженным показателем обезжиренной массы тела (FFM) способствует снижению энерготрат организма.
При спастических типах ДЦП отмечаются низкие уровни физической активности и расход энергии. В этой связи E. Denhoff и S. A. Feldman (1981) указывают, что таким больным необходимо всего около 1200 ккал/сут [2]. В соответствии с их рекомендациями, потребность в энергии лучше всего определять на основании единиц измерения роста пациентов (ккал/см). Детям с тяжелыми поражениями центральной нервной системы (ЦНС) (в условиях клиники) потребуется 11,1 ккал/см (то есть 75% от обычной потребности для нормального развития).
L. G. Bandini и соавт. (1991) подчеркивают, что при спастическом тетрапарезе суточные энерготраты и потребность пациентов в пищевых калориях ниже, а не выше нормы, как было принято считать ранее [4].
Кроме того, известно, что дети, страдающие ДЦП, по достижении школьного возраста нередко отдают предпочтение высококалорийным продуктам питания. При ДЦП избыточное потребление пищи и ожирение менее значимы, чем алиментарный дефицит. Тем не менее, проблеме ожирения при ДЦП посвящены работы P. Khattraa и M. Seearb (2007), B. M. Rogozinski и соавт. (2007), J. H. Rimmer и соавт. (2010, 2011), D. G. Kwon и соавт. (2011), E. S. Park и соавт. (2011), а также M. D. Peterson и соавт. (2013) [5–11].
Причины гипотрофии и мальнутриции при ДЦП довольно многочисленны. Так, недостаточность питания у детей с церебральными параличами может являться следствием следующих причин и факторов:
1) сложностей вскармливания в результате нарушений жевания и глотания (дискоординация деятельности мышц губ, языка, неба и глотки);
2) замедленного развития в результате повреждения мозговых центров, обеспечивающих питание и рост (гипоталамические центры);
3) зубного кариеса/гипоплазии эмали и других стоматологических проблем;
4) несоответствия пищевых привычек индивидуальному выходу (расходу) энергии;
5) дефицита минеральных веществ, вызванного хроническим приемом антиконвульсантов или отсутствием активных движений [1, 2].
Eсть мнение, что многие дети с умеренными/тяжелыми формами ДЦП подвержены дефициту питательных веществ, поскольку потребляют в избыточных количествах молоко и молочные продукты, что имеет место наряду с недостаточным включением в их рацион мяса, фруктов и овощей.
J. W. Hung и соавт. (2003) среди факторов риска сниженного нутритивного статуса у детей со спастическими формами церебрального паралича называют следующие: потеря пищи при ее приеме (p = 0,026), наличие более чем одной проблемы со вскармливанием (p = 0,044), разнообразие консистенции пищи (p
В. М. Студеникин 1 , доктор медицинских наук, профессор, академик РАЕ
А. А. Букш
ФГАУ НЦЗД МЗ РФ, Москва

Нутритивный статус у детей-инвалидов, тема сегодняшней статьи. У детей с неврологическими проблемами нарушение нутритивного статуса может быть связано как непосредственно с нутритивными расстройствами (недостаточностью питания), так и с другими, ненутритивными факторами — типом и тяжестью неврологических расстройств, нарушениями эндокринной функции, когнитивными расстройствами и т.п.
Приветствуем вас дорогие читатели! Рассмотрим подробнее причины недостаточности питания у таких детей, поскольку их понимание позволит повлиять на них.
Причиной недостаточного питания
Конечно, основной причиной недостаточного питания у детей с неврологическими расстройствами является несоответствие потребленной ими пищи и их потребности в питательных веществах и энергии.
Такие исследователи, как S. Reilly и V. Stallings показали, что дети с ДЦП в целом потребляют меньше нутриентов и энергии, чем здоровые сверстники.
Данная ситуация обусловлена факторами, которые представлены далее.

У детей с ДЦП недостаточное питание чаще всего является следствием заболевания. Обычно выразительность орально-моторной дисфункции коррелирует с тяжестью задержки моторного развития ребенка.
Часто родительские жалобы при этом следующие:
- проблемы с сосанием
- грудным вскармливанием
- глотанием
- введением твердой пищи
- питьем
- откусыванием
- жеванием
- першением и кашлем во время кормления
Можно только представить, насколько стрессовым (а не приятным, как должно быть) является процесс и продолжительность такого кормления для родителей и что они чувствуют.
Однако для эффективного потребления пищи ребенком важно именно хорошее настроение опекунов во время кормления, так как ребенок полностью зависит от них в удовлетворении своей базовой потребности.
Кроме того, такой процесс кормления и его продолжительность утомляет не только опекунов, но и самого ребенка, что не может не влиять на его аппетит и способность съесть надлежащее количество.
К сожалению, даже такое существенное увеличение времени кормления ребенка не обязательно компенсирует имеющиеся трудности и не всегда означает достаточности потребленных калорий.
При обследовании орально-моторной функции детей можно выявить такие проблемы как:
- затрудненное закрывание рта
- слюнотечение
- постоянное выдвижение языка, что вызывает утечку пищи
- затруднено формирование комка пищи вследствие плохой координации произвольных движений мышц
- задержка развития возрастных оральных навыков
- задержка реализации глотательного рефлекса, что может вызвать аспирацию

Тяжелая орально-моторная дисфункция часто сочетается с плохими показателями нутритивного статуса.
Дети с тяжелыми поражениями (не могут есть сами, не способны удерживать голову) имеют больший риск аспирации.
Дети, у которых наблюдаются ранние, постоянные и выраженные трудности при кормлении, рассматриваемые как маркеры прогнозирования плохого нутритивного статуса, должны относиться к группе, в которой может быть полезной применение гастростома.
- Значительная потеря пищи. Дети с неврологическими поражениями, которые способны есть самостоятельно, могут иметь плохую координацию рука/рот, что приведет к потере пищи. A. Ravelli et al. установили, что у детей с неврологическими поражениями гораздо чаще наблюдается гастроэзофагеальный рефлюкс (ГЭР) и задержка опорожнения желудка, что приводит к увеличению потери питательных веществ в результате частой рвоты.
- Нарушение естественной регуляции питания. Из-за коммуникативных трудностей инвалиды дети не могут четко дать знать о своем голоде, сытости, вкусовых предпочтениях. Таким образом, естественная регуляция питания заменяется выбором и ответственностью взрослых. Опекуны же склонны преувеличивать количество потребленной ребенком еды и недооценивать необходимое для кормления время, поскольку этот процесс, как отмечалось выше, может быть слишком нелегким и длительным, что в результате приводит к недостаточности потребленной энергии относительно энергетических потребностей ребенка.
Для полного понимания причины возникновения у особого ребенка проблем с недостаточностью питания обычно проводят:
- изучение медицинского
- нутритивного
- социального анамнеза
- адекватные антропометрические измерения
- физикальное обследование
- наблюдение за процессом приема пищи
- проведение специальных диагностических процедур
Медицинский анамнез важен для понимания причины, длительности и тяжести поражения нервной системы и, соответственно, ожидаемых последствий.
Важно отметить применение ребенком противосудорожных препаратов, поскольку некоторые антиконвульсанты могут менять пищевой паттерн ребенка, влиять на уровень его сознания и, как следствие, на орально-моторную ловкость и защиту дыхательных путей.
Особенно тщательно следует изучать наличие признаков респираторных или гастроинтестинальных проблем, потому что они будут влиять на все аспекты нутритивной поддержки.
Такие симптомы, как частая рвота, отказ от еды, беспокойное поведение, анемия позволяют заподозрить ГЭР.
Согласно исследованиям J. Sondheimer и B. Morris, дети с тяжелой отсталостью, выраженным сколиозом чаще страдают от кислотного рефлюкса.
О возможности аспирации свидетельствуют хронический кашель, частые пневмонии, плохо контролируемая астма.
- как у ребенка происходил процесс приобретения новых соответствующих навыков при кормлении, какие трудности при этом наблюдались и каково кормление ребенка сейчас (ответ на эти вопросы часто помогает выявить очевидную причину плохого усваивания);
- какой была при этом динамика роста и массы тела ребенка (дети с низким весом при рождении составляют группу риска по развитию недостаточности питания; хорошо иметь записи действительно потребленной ребенком еды в течение трех дней для изучения привычного питания, его энергетической и питательной ценности).
Социальный анамнез

Социальный анамнез помогает понять, насколько семья, воспитывающая ребенка-инвалида, учреждение, которое им занимается, обладает ресурсами (информационными, человеческими, финансовыми, профессиональными и т.д.) для адекватного нутритивного ухода.
Общеизвестно, что нутритивный статус большинства детей можно оценить по их массе тела и росту. Однако мониторинг этих показателей у детей с ДЦП затруднен из-за следующих факторов.
1. Трудно получить надежные показатели роста или длины тела из-за деформаций, фиксированных контрактур суставов, непроизвольных мышечных спазмов и неадекватности поведения вследствие когнитивного дефицита. Поэтому для детей с ДЦП разработаны формулы на основе показателей длины плеча, длины голени и высоты колена, которые советуют использовать как заменители роста или длины тела при невозможности проведения точных измерений.
2. Общепринятые стандарты для здоровых детей могут быть неадекватными для детей с существенными неврологическими расстройствами. Так, для определенных генетических диагнозов (синдромы: Дауна, Тернера, Марфана, Прадера-Вилли, ломкой Х-хромосомы и т.д.) разработаны свои, специфические к диагнозу, кривые роста и массы тела.
ДЦП не относится к генетическим заболеваниям, однако многие специалисты пытались разработать специфические для этого диагноза кривые роста и массы тела.

И хотя специфические кривые роста и массы тела для детей могут быть полезными для клиницистов, любая представительная выборка лиц с тяжелыми или средними формами тяжести ДЦП является гетерогенной.

Окружность плеча измеряется обычной сантиметровой лентой на середине расстояния между акромиальным и локтевым отростками.
Не требует много времени и оборудования, низкие показатели четко коррелируют со смертностью и заболеваемостью.
При этом некоторые исследования установили такую же надежность этого критерия для диагностики гипотрофии, как и показатели массы для возраста.
У детей от 6 до 59 месяцев окружность плеча мало меняется, поэтому может использоваться как независимый от возраста показатель в этом возрастном промежутке.
Так, в соответствии с рекомендациями рабочих групп Всемирной организации здравоохранения (ВОЗ), которые работают над стандартизацией оценки нутритивного статуса, в возрасте 6-59 месяцев тяжелая степень гипотрофии диагностируется при окружности плеча 110 мм, а умеренная — при 110-125 мм.

Толщина кожно-жировой складки (из четырех типовых локализаций — над бицепсом, трицепсом, гребнем подвздошной кости и под лопаткой — чаще всего клиницисты применяют измерение над трицепсом)
характеризует жировой запас в теле; полученные результаты сравниваются с центильными таблицами (создана база данных для всех возрастов и пола).
Относительно детей с ДЦП, в некоторых исследованиях обнаружено, что низкие показатели толщины кожно-жировой складки лучше идентифицируют в этой когорте детей с гипотрофией, чем вес/рост/возраст (96 против 45-55% соответственно).
Интересно заметить, что Комитет по питанию педиатрического общества Канады еще в 1994 году рекомендовал метод определения толщины кожно-жировой складки как лучший скрининговый тест гипотрофии у детей с ДЦП.
Физикальное обследование

Физикальное обследование позволяет выявить признаки гипотрофии и дефицита микроэлементов.
Если у ребенка с ДЦП наблюдаются такие симптомы, как повышение мышечного тонуса и гиперкинезы, это будет означать повышенные энергетические потребности по сравнению с детьми, которые таких проявлений не имеют. Контрактуры и сколиоз могут существенно ухудшать положение ребенка во время приема пищи.
Наблюдение за процессом потребления пищи ребенком, который имеет проблемы с питанием, является обычной процедурой в Канаде, США, Голландии и т.д.
Часто для адекватности оценки используют видеосъемку процесса кормления в привычных домашних условиях.
Проведение такой оценки представляет интерес не только для врача, который будет иметь бесценный фактический материал для диагностического процесса, но и для логопеда, который будет иметь возможность наблюдать за орально-моторными навыками и проблемами, для физического терапевта, который выяснит адекватность и безопасность положения ребенка во время кормления, оценит соответствие используемых средств для кормления, для поведенческого психолога, который сможет оценить детско-родительское взаимодействие во время приема пищи.
А дальше — каждый из специалистов изложит свое видение проблемы и, что самое важное, свои предложения последующих действий, возможностей и тактики вмешательства.
Диагностика процедур

Проведение специальных диагностических процедур необходимо для выявления определенных симптомов.
Для определения аспирации и ее условий уместно провести видеофлюороскопическое обследование процесса глотания, используя пищу различной текстуры и напитки.
Иногда такое обследование может выявить бессимптомную (тихую) аспирацию при отсутствии кашля.
Также важно учитывать и положение ребенка во время проведения процедуры, поскольку у некоторых детей аспирация зависит от их позиции.
Уместно проводить такое обследование процесса глотания в конце кормления, поскольку усталость ребенка может провоцировать аспирацию. Видеофлюороскопическое обследование процесса глотания поможет выбрать безопасную текстуру пищи и адекватную технику кормления.

Диагностика ГЭР (при рвоте, боли в груди и животе, раздражительности, отказе от пищи) может иногда требовать проведения таких исследований, как тест на опорожнение желудка, эндоскопическое обследование верхних отделов пищеварительного тракта, 24-часовое рН-зондирование.
После идентификации детей с недостаточным питанием или риском недостаточного питания составляется индивидуальный план нутритивной поддержки, цель которого — достижение целевых антропометрических показателей (целевого веса, толщины кожно-жировой складки и т.д.), что в результате оптимизирует здоровье ребенка, его функциональную способность и качество жизни.
Прежде всего команда специалистов пытается безопасным путем максимально увеличить пероральный прием пищи ребенком.
Для этого можно подбирать оптимальное положение тела ребенка для кормления и необходимое адаптационное оборудование, корректировать состав пищи и ее калорийность, менять текстуру пищи и средства для кормления, увеличивать частоту кормлений, подбирать соответствующие техники кормления, проводить поведенческую модификацию, устранять медицинские проблемы.
Особенно актуальны попытки улучшить моторно-оральные навыки детей-инвалидов до 5 лет.
Зондовое питание

Если же, несмотря на оптимизацию приема кормления, ребенок не способен обеспечить свои пищевые и энергетические потребности, необходимо начать зондовое питание.
Кроме того, зондовое питание показано при слишком большой продолжительности процесса кормления (более 3 часов в день) и риске аспирации.
Кормление через зонд стало признанным стандартом лечения детей с тяжелой инвалидностью. При выборе данного метода необходимо продумать следующие пункты:
- что будет поставляться через зонд (перемолотая еда, готовые коммерческие смеси)
- какой доступ к желудочно-кишечному тракту будет оптимальным (назогастральный, назоеюнальный зонд, гастростома)
- какой режим поступления нутриентов выбрать (порционный, инфузионный в течение дня и/или ночи, комбинированный)
Считается, что применение назогастральных зондов показано при кратковременном использовании (в течение 3-8 недель, в зависимости от материала, из которого изготовлен зонд).
Гастростома

При необходимости проведения более длительного зондового питания (более 6- 8 месяцев) уместно рассмотреть целесообразность гастростома.
Гастростома может использоваться либо для прикорма (преимущественно в ночное время; в течение дня ребенка нужно поощрять к оральному кормлению, при его безопасности), либо для полной замены способа кормления.
Исследования, проведенные специалистами, показали целесообразность использования гастростома у детей с тяжелыми формами ДЦП для улучшения физического роста, общего состояния здоровья и качества жизни семей.
Сегодня возможно вы получили много новой информации, и конечно не все понимают о чем прочитали. Но, дорогие мои, это дает вам толчок отправится к лечащему врачу и узнать чем из выше прочитанного страдает ваш ребенок.
И, если вы раньше не обращали на это внимание, то теперь по вашей просьбе-требованию, врачи тщательно проведут обследование.
Почему я вам об этом написала, да все просто, я сама раскормила ребенка и мне помогали родственники. Каждый жалеет ее, хочет подбавить в тарелку кусок по вкуснее, угостить вкусняшкой.
Вот теперь мы пожимаем плоды своей любви, лечимся у диетолога-гастроэнтеролога, плюс из этого, теперь мы много времени отдаем физическим нагрузкам, жизнь стала подвижной.
Значит теперь мы ведем здоровый образ жизни!
Все, на этом мы прощаемся, не забывайте подписаться на новые публикации и поделитесь статьей с друзьями.Пока!
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
Детский церебральный паралич (ДЦП) — группа стабильных нарушений развития моторики и поддержания позы, ведущих к двигательным дефектам, обусловленным непрогрессирующим повреждением и/или аномалией развивающегося головного мозга у плода или новорожденного ребенка. Пациенты с ДЦП составляют группу риска по развитию нарушений нутритивного статуса, которые выявляются в среднем у половины детей с данным заболеванием. Правильная оценка пищевого статуса с последующей коррекцией рациона позволяет стабилизировать биохимические показатели макро- и микронутриентов сыворотки крови, улучшить самочувствие ребенка за счет коррекции проявлений сопутствующей патологии, повысить эффективность реабилитационных мероприятий. При составлении рациона для ребенка с ДЦП необходимо учитывать возрастные потребности в пищевых веществах и энергии, патогенез основного заболевания и характер сопутствующей патологии (запоры, гастроинтестинальная пищевая аллергия, дисфагия, гастроэзофагеальная рефлюксная болезнь и др.). Данная работа иллюстрирует опыт диетологической коррекции нутритивного статуса у пациентов с ДЦП. В связи с наличием у пациентов нутритивной недостаточности и пищевой аллергии, в т. ч. к белку коровьего молока, с целью коррекции использовались специализированные элементные и полуэлементные энтеральные лечебные смеси.
Ключевые слова: детский церебральный паралич, нутритивная поддержка, диетотерапия, энтеральное питание, дефицит массы тела, пищевая аллергия.
Для цитирования: Титова О.Н., Строкова Т.В., Таран Н.Н. и др. Опыт коррекции пищевого статуса у детей с детским церебральным параличом: клиническое наблюдение. РМЖ. 2019;7:16-21.
Experience of nutritional condition correction in children with infantile cerebral palsy: clinical review
O.N. Titova 1 , T.V. Strokova 1,2 , N.N. Taran 1,2 , E.V. Pavlovskaya 1 , I.A. Matinyan 1,2
1 Federal Research Center for Nutrition, Biotechnology and Food Safety, Moscow
2 Pirogov Russian National Research Medical University, Moscow
Infantile cerebral palsy (ICP) is a group of stable disorders in the motor skills development and maintaining posture, leading to motor defects caused by non-progressive damage and/or developing brain anomaly in fetus or newborn baby. Patients with ICP are at the development risk of nutritional condition disorders, which are detected in average of half of children with this disease. Correct assessment of the nutritional condition with subsequent dietary correction can stabilize the biochemical parameters of macro-and micro-nutrients in blood serum, improve the health of the child by correcting the comorbidity manifestations, improve the rehabilitation measures effectiveness. When compiling a diet for a child with ICP, it is necessary to take into account age-related needs for nutrients and energy, the pathogenesis of the underlying disease and the nature of the comorbidity (constipations, gastrointestinal food allergy, dysphagia, gastroesophageal reflux disease, etc.). This article illustrates the dietary correction experience of nutritional condition in patients with ICP. Due to the presence of nutritional insufficiency and food allergy, including cow’s milk protein, specialized elemental and semi-elemental enteric therapeutic mixtures were used for correction.
Keywords: infantile cerebral palsy, nutritional support, diet therapy, enteric nutrition, weight deficit, food allergy.
For citation: Titova O.N., Strokova T.V., Taran N.N. et al. Experience of nutritional condition correction in children with infantile cerebral palsy: clinical review. RMJ. 2019;7:16–21.
В статье представлен опыт диетологической коррекции нутритивного статуса у пациентов с ДЦП. Описано клиническое наблюдение.
Введение
Детский церебральный паралич (ДЦП) — группа стабильных нарушений развития моторики и поддержания позы, ведущих к двигательным дефектам, обусловленным непрогрессирующим повреждением и/или аномалией развивающегося головного мозга у плода или новорожденного ребенка, с дальнейшим формированием патологического мышечного тонуса (преимущественно спастичности) при сохранении позотонических рефлексов и сопутствующих нарушений становления цепных установочных выпрямительных рефлексов [1]. Основным отличием ДЦП от других центральных параличей является время воздействия патологического фактора: пренатальное, интранатальное и в раннем постнатальном периоде [2].
По данным ВОЗ, ДЦП является основной причиной детской неврологической инвалидности в мире, частота встречаемости его в мире составляет 3–4 случая на 1000 новорожденных [3]. В Российской Федерации распространенность зарегистрированных случаев ДЦП составляет 2,2–3,3 случая на 1000 новорожденных [1].
Пациенты с ДЦП составляют группу риска по нутритивной недостаточности. Нарушения нутритивного статуса выявляются в среднем у половины детей данной категории [4]. Нарушения питания у детей с ДЦП включают дефицит веса разной степени, замедление темпов роста, остеопению (более чем у 70%) и ожирение (10–15%) [3]. Дети, страдающие ДЦП, нуждаются в тщательном мониторинге пищевого статуса, разработке рациона с назначением нутритивной поддержки по показаниям и ее обязательной коррекцией в динамике наблюдения с учетом возраста, характера течения основного заболевания, наличия сопутствующей патологии, а также объема и интенсивности реабилитационных мероприятий.
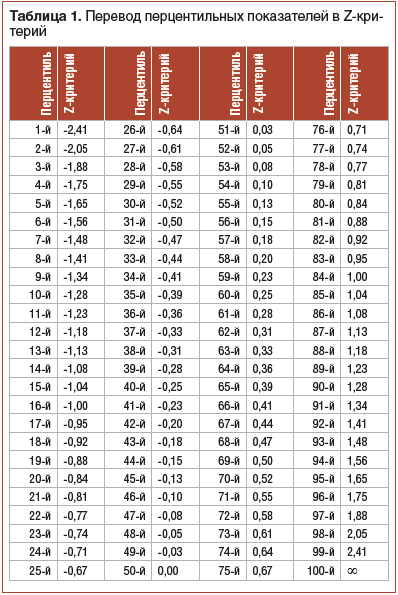
Оценка физического развития пациентов с ДЦП проводится с использованием центильных таблиц, разработанных для пациентов с данной патологией с учетом моторного класса по системе оценки глобальных моторных функций (Gross Motor Function Classification System, GMFCS). Z-критерий ИМТ может определяться путем перевода перцентильных показателей в Z-критерии с использованием таблиц (табл. 1). Критерии оценки показателей физического развития представлены в таблице 2.

Клиническое наблюдение 1
Анамнез: мальчик от II беременности (I беременность замершая), протекавшей на фоне хронической фетоплацентарной недостаточности, угрозы прерывания на всем сроке. Роды I самостоятельные, преждевременные (35–36 нед. гестации), с двойным обвитием пуповиной вокруг шеи. При рождении масса тела — 2480 г, длина — 51 см. Оценка по шкале Апгар — 7/8 баллов. В связи с тяжелым состоянием, обусловленным дыхательной недостаточностью и неврологической симптоматикой, госпитализирован в отделение интенсивной терапии, где в течение 3 сут проводилась ИВЛ. На 7-е сут жизни переведен в отделение патологии новорожденных с диагнозом: гипоксически-ишемическое поражение ЦНС. Грудное вскармливание проводилось до 2 мес., смешанное — до 4 мес., затем искусственное (адаптированные молочные смеси на основе цельного белка). Введение прикорма с 4 мес. (начиная с творога). В 5 мес. введены овощи, в 6 мес. — коровье молоко (2,5% жирности). На первом году наблюдался у специалистов по поводу задержки психомоторного и речевого развития.
В возрасте 3 мес. появились признаки внутричерепной гипертензии (по данным нейросонографии) и тетрапареза. В 1 год 2 мес. установлен диагноз ДЦП. Спастический тетрапарез. Постоянно наблюдается специалистами по месту жительства, проводятся реабилитационные мероприятия по поводу резидуально-органического поражения ЦНС; ДЦП, спастического левостороннего гемипареза с преимущественным поражением левой верхней конечности, GMFCS I уровень. Сопутствующие заболевания: аутоиммунный тиреоидит, субклинический гипотиреоз, медикаментозная компенсация. Миопия слабой степени. Множественные приводящие контрактуры левой верхней и нижней конечности. Нарушение осанки. Поло-эквино-варусные стопы. Дизартрия псевдобульбарная. Смешанное специфическое расстройство развития.
Наследственность: по линии матери: у мамы — хронический гастрит; у дедушки — рак желудка; по линии отца: у папы — артериальная гипертензия; у бабушки — сахарный диабет 2 типа; у деда — артериальная гипертензия, инфаркт миокарда.
Перенесенные заболевания: ОРВИ; анемия в раннем возрасте; в 7 лет — ветряная оспа, эписклерит, оперативные вмешательства: в 7,5 года — сухожильно-мышечная пластика на левой кисти.
Со слов матери, с рождения у ребенка отмечаются ежедневные колики, задержка стула до 4–5 дней, низкие темпы прибавки массы тела (рис. 1).
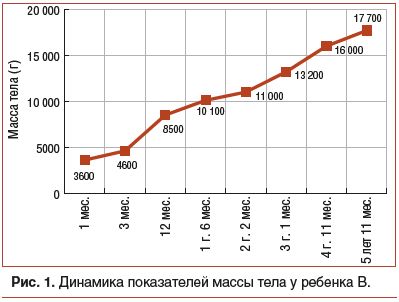
С 3 мес. до 4 лет большая часть приемов пищи осуществлялась во сне в связи с наличием позывов на рвоту или рвоты при приеме еды во время бодрствования. До 4 лет в рационе присутствовала исключительно протертая пища. На момент госпитализации в рационе преобладали молочные и кисломолочные продукты, крупы (гречневая, кукурузная, овсяная, рисовая 1 раз в неделю), макаронные изделия, мясо в протертом виде (курица, индейка, говядина), хлеб и хлебобулочные изделия, овощи (капуста цветная, свежие огурцы, картофель, морковь, лук репчатый, свекла), фрукты (яблоки, бананы, груши). Специализированное лечебное питание не получал.
Объективно: положение ребенка активное. I класс GMFCS. Масса тела — 27,5 кг, рост — 149 см. ИМТ — 12,4 кг/м 2 ; Z-критерий ИМТ/возраст — 2 . Z-критерий ИМТ Литература
Только для зарегистрированных пользователей
Читайте также:


