Болезнь паркинсона пересадка клеток

Пациенту с болезнью Паркинсона впервые пересадили нейроны, полученные из его собственных клеток кожи. Эксперимент держали в секрете, однако он оказался абсолютно легальным и безопасным. С момента операции прошло два с половиной года, за это время никаких побочных эффектов не появилось. За это время его состояние стабилизировалось — о прогрессе говорить рано, но и признаков нейродегенерации врачи не обнаружили. Исследование опубликовано в журнале The New England Journal of Medicine.
В обоих случаях первопроходцами стали японские исследователи — с тех пор, как японские же биологи придумали репрограммировать взрослые клетки в стволовые, эта страна стала одним из лидеров в области клеточной терапии. В 2018 году в Японии появился проект еще одного метода: ученые собрались опробовать репрограммирование против болезни Паркинсона, то есть превратить взрослые клетки в эмбриональные, вырастить из них клетки-предшественники нейронов и подсадить в мозг пациента. Клинические испытания стартовали осенью 2018 года, но их результаты еще не опубликованы.
Японская команда была первой, кто заговорил о подобном эксперименте, но, как оказалось, не первой, кто его запустил. Как выяснил журнал STAT, в США подобный план созревал с 2014 года. В 2017 году, когда в Японии только строили планы испытания, первый пациент уже получил инъекцию клеток, а теперь команда медиков под руководством Кван Су Кима (Kwang-Soo Kim) из больницы МакЛин в Массачусетсе опубликовала отчет об этой экспериментальной терапии.
По данным STAT, первый пациент — американский бизнесмен, бывший врач Джордж Лопес — нашел Кима сам 2013 году и предложил проспонсировать его исследования. К тому времени Лопес уже знал, что у него болезнь Паркинсона, но не рассчитывал на то, что врачи сумеют ему помочь. Тем не менее, получив финансирование и ускорив исследования, через несколько лет Ким уже был готов опробовать на Лопесе свой метод.
Исследователи взяли человеческие клетки кожи, репрограммировали их в эмбриональные стволовые, а затем дифференцировали в предшественники дофаминергических нейронов — тех самых, которые гибнут у пациентов с болезнью Паркинсона. Чтобы убедиться в том, что их протокол надежен, Ким и коллеги проверяли его на гуманизированных мышах — это животные с иммунодефицитом, которым пересаживают человеческие клетки крови. Им имплантировали полученные нейроны в мозг, а затем следили за уровнем иммунной агрессии. Как и следовало ожидать, если клетки крови и нейроны были получены от одного пациента, иммунного ответа не возникало, а если от разных, в мозге развивалось воспаление.
Ким и коллеги держали свой эксперимент в тайне и не публиковали предварительных заявлений. Тем не менее, он был абсолютно легальным: они получили разрешение от FDA на применение своего метода в исключительных обстоятельствах — то есть только у неизлечимо больного человека, причем каждый раз процедуру необходимо согласовывать заново. На первом этапе работы FDA согласовало введение клеток только в левое полушарие мозга. На вторую серию инъекций — в правое полушарие — ведомство согласилось только полгода спустя, когда стало понятно, что процедура не вызывает побочных эффектов.

Иммуногенность нейронов в мозге мыши. Слева направо: иммунодефицитные мыши после пересадки нейронов, иммунодефицитные мыши после трансплантации клеток крови и нейронов от одного донора, иммунодефицитные мыши после трансплантации клеток крови и нейронов от разных доноров. Синий - ядра клеток, красный - лимфоциты, признак воспаления.
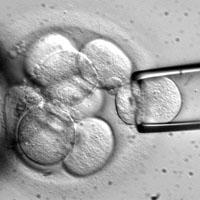
Восполнение утраченных клеток мозга посредством трансплантации может помочь обратить вспять нарушения, вызванные болезнью Паркинсона. К такому выводу пришли европейские ученые, принявшие участие в проекте TransEuro. Результаты исследования были опубликованы сегодня в журнале Horizon: The EU Research & Innovation Magazine.
Болезнью Паркинсона страдают более 4,6 миллионов человек по всему миру, и ожидается, что к 2030 году эта цифра увеличится вдвое по причине старения населения. И хотя существуют методы облегчения симптомов, в настоящее время данная болезнь считается неизлечимой. Отчасти развитие заболевания обусловлено потерей клеток, производящих нейромедиатор дофамин. Одной из самых эффективных терапий является применение леводопы, которая увеличивает уровень дофамина, однако эффективность этого метода со временем падает, и проявляются побочные эффекты. Эксперименты по трансплантации клеток, синтезирующих дофамин, проводятся с 1980-х годов, и хотя был достигнут определенный успех, ученые продолжают уточнять протоколы проведения терапии и стремятся выявить, какая именно категория пациентов имеет наибольшую вероятность положительного результата терапии. Ранее в эту группу вошли пациенты, у которых болезнь диагностирована менее 10 лет назад, поддающиеся лечению леводопой без значительных побочных эффектов и в возрасте до 65 лет.
С мая 2015 года было проведено 17 операций по трансплантации клеток, и 10 операций запланировано на будущее. Каждый пациент подвергается двум процедурам: по одной на каждую сторону мозга. В некоторых случаях невозможно проводить операцию на обоих полушариях за один раз ввиду ограниченного запаса необходимых клеток. Результаты этого исследования ожидаются к 2020 году, когда пройдет три года после операции, чтобы можно было оценить эффективность и безопасность подобной манипуляции. Кроме того, у ученых появилась надежда на выявление биомаркера болезни Паркинсона – одним из претендентов на его роль является вещество в жидкости, которая окружает мозг и позвоночник. Взяв у больных болезнью Паркинсона и здоровых людей образцы цереброспинальной жидкости, исследователи проанализировали количество в ней растворимого альфа-синуклеина – белка, который связан с данным заболеванием.
Данное вещество может стать первым биомаркером болезни Паркинсона, что теоретически позволит диагностировать заболевание на раннем этапе, когда нарушения в мозге не столь значительны, и, соответственно, раньше начать необходимое лечение. Что касается операции по трансплантации клеток, то по утверждению ученых, на распространение подобной практики может уйти около 10 лет. К тому времени, как они надеются, будет разработан метод развития стволовых клеток из взрослых клеток, что позволит проводить операции в нужном объеме. Проводимые эксперименты могут стать первым шагом на пути к осуществлению операций по трансплантации стволовых клеток, а затем и произведенных из них нейронов, вырабатывающих дофамин, и восполнению ими утраченных клеток.

Пересаженные стволовые клетки при болезни Паркинсона функционируют в мозге как минимум еще 14 лет
Лечение болезни Паркинсона стволовыми клетками – это одно из самых обнадеживающих направлений. Некоторые мировые клиники уже лечат болезнь Паркинсона при помощи стволовых клеток. Вчера было опубликовано исследование, в котором показано, что пересаженные стволовые клетки в мозге функционируют на протяжении 14 лет. Пересаженные стволовые клетки плода обещают быть эффективными для лечения болезни Паркинсона. 5.06.2014. Исследование было проведено в Маклин больнице. Дофаминовые стволовые клетки плода, пересаженные в мозг пациентов с болезнью Паркинсона, оставались здоровыми и функционировали до 14 лет. Исследователи проверили мозг 5 умерших пациентов (не от болезни Паркинсона), которым 14 лет назад были трансплантированы стволовые клетки. В этом исследовании показано, что пересаженные стволовые клетки подключаются и хорошо выживают, вследствие чего на длительное время сохраняются все необходимые функции нервных клеток. Эти выводы имеют важное значение для развития методов лечения болезни Паркинсона на основе стволовых клеток дофаминовых нейронов.
Пока только 25 пациентов с болезнью Паркинсона во всем мире прошли такое лечение стволовыми клетками (при помощи метода пересадки дофаминовых клеток плода) в течение двух десятилетий, а их симптомы заметно улучшились. Трансплантация стволовых клеток может уменьшить симптомы болезни Паркинсона на протяжении многих лет и может уменьшить потребность замены препаратов дофамина, даже несмотря на то, что они могут принимать несколько месяцев или лет, чтобы начать работать.
Доказательство того, что пересаженные клетки остаются здоровыми, имеет важное значение для дальнейших исследований в области пересадки стволовых клеток. Все пациенты были на поздних стадиях болезни Паркинсона во время их пересадки. Болезнь Паркинсона – это заболевание, характеризующееся тремором, ригидностью, медленным передвижением. Это хроническое, прогрессирующее заболевание, в результате которого в мозге погибают дофамин-производящие нервные клетки. Необходимо понять, как пересаженные нейроны могут выжить, несмотря на продолжающийся патологический процесс в мозге пациентов. Существуют разногласия среди ученых: некоторые считают, что пересаженные клетки могут быть повреждены токсичными белками, связанными с течением болезни Паркинсона, даже несмотря на то, что многие пациенты чувствуют себя значительно лучше.
Метод, применяемый для трансплантации стволовых клеток в мозг этих пациентов с болезнью Паркинсона отличается от другого метода, который был применен к 60 другим пациентам во всем мире. В некоторых из этих исследований ученые отметили, что клетки вероятно повреждены в результате патологического процесса. Возможно, в этом исследовании был применен метод, при котором вводили крошечных размеров дофаминовые нервные клетки в мозг через тонкую иглу. В других же исследованиях были пересажены более крупные части нервных клеток с помощью больших игл.
В этом исследовании ученые сравнили дофаминовые клетки пациентов с пересаженными клетками. Было замечено отличие у дофаминовых клеток и митохондрий, которые оставались нездоровыми вокруг нейронов дофамина пациентов и оставались здоровыми возле пересаженных клеток. Пересаженные клетки не имели болезни Паркинсона. Очень трудно получить нервные клетки дофамина из ткани плода. Было бы гораздо проще выращивать клетки в лаборатории из стволовых клеток. Это была не классическая транплантация стволовых клеток при болезни Паркинсона. Источник: Cell Reports, June 2014

Болезнь Паркинсона — серьезное заболевание разрушительного действия, которое поражает нейронные клетки черного вещества, находящегося в среднем мозге. Благодаря данной субстанции мы можем двигать глазами, выполнять мелкие и точные движения, в частности, пальцами; жевать и глотать. Вначале болезнь проявляется в двигательных нарушениях, а затем прогрессирует и сопровождается психическими расстройствами.
На данный момент ученые точно не могут установить причины развития заболевания, а также не могут найти лечение, однако одним из перспективных методов лечения является пересадка предшественников нейронов дофамина, который отвечает за внимание и концентрацию, мотивирует и стимулирует к активной жизни, в базальные ядра головного мозга. Какие же есть аспекты данной клеточной заместительной терапии и с какими сложностями придется столкнуться при ее внедрении в клиническую практику?
На эти вопросы ответили в обзоре, не так давно опубликованном в биологическом научном журнале Nature Reviews Neuroscience.
Причины болезни Паркинсона
Одно можно утверждать точно — основной причиной болезни Паркинсона является гибель клеток черной субстанции. Как говорилось выше, это вещество отвечает за движения, поэтому первыми проявлениями болезни и становятся двигательные нарушения, такие как тремор, отказ мускулатуры, реже появляются недвигательные — психические отклонения и снижение познавательной деятельности. Причиной разрушения нейронов выступают клетки Леви, которые представляют собой скопления белка. Именно они приводят сначала к распаду связи между нейронами, а затем к их гибели.
Болезнью Паркинсона страдает примерно каждый сотый человек старше 60 лет, а с возвратом болезнь развивается все сильнее. Но благодаря тому, что болезнь можно, хотя и сложно, обнаружить на ранних периодах, это позволяет сильно затормозить ее развитие. Очень важно знать, что большое влияние на появление заболевания оказывают генетические факторы (больные родственники) и факторы окружающей среды.
Лечение заболевания
Благодаря особенности Паркинсона, которая отличает ее от других нейродегенеративных болезней, можно найти конкретное место в мозге, куда нужно направить усилия (так как гибнут нейроны одного вида), а это облегчает поиск метода лечения. В настоящий момент учеными разрабатывается генная методика, при которой с помощью инъекции в субталамическое ядро, находящееся сбоку от черного вещества, усиливается синтез важнейшего тормозного нейромедиатора центральной нервной системы человека, который гасит неверную деятельность нейронов. Есть и другие способы, например, введение факторов роста или генов синтеза дофамина в клетки мозга, которые его не образуют, чтобы восполнить гибель этих клеток. Но самой перспективной тенденцией в лечении Паркинсона является пересадка новых клеток в черное вещество или базальные ядра.
Подсадка клеток в черное вещество
Этот метод уже не является новым. 30 лет назад прошли первые испытания, при которых были удачно подсажены новые клетки. Но сложности возникают с источниками этих клеток, так как эмбриональные ткани не являются надежным ресурсом. Кроме того, очень сложно рассчитать нужную дозу клеток для отдельного пациента. Использованные нейроны из зародышей могут быть смешаны с другими, например с серотонином, что приведет к тяжелым побочным эффектам. Поэтому нужно было найти другой источник. Предлагались клетки из мозгового вещества надпочечников и дофамин из клеток каротидных телец. Но пересадка из других материалов, отличных от эмбриональных, как выяснилось абсолютно неэффективна, так как клетки быстро гибли. Как оказалось, последние испытания опровергли то, что мозг отрезан от иммунной системы, что и стало причиной неэффективности этого метода.
Но ученым удалось сделать прорыв в этой области, они открыли способ получения стволовых клеток из тканей взрослого человека, которые можно заставлять разделяться в нейроны. Такие клетки можно получить из тканей самого больного, что делает их идентичными и не вызывает иммунный ответ. Их можно стандартизировать, а значит рассчитать нужное количество. Кроме того, этот способ исключает возможность загрязнения другими клетками при пересадке. И их можно заморозить, что упрощает работу с ними.
В 2018 году Япония первой начала испытания данного метода с целью изучения его эффективности. В данном эксперименте участвуют несколько компаний.
Чего же можно ждать от этой терапии?
Вероятнее всего, она поможет убрать двигательные повреждения, за которые отвечают клетки черной субстанции. Но неизвестно, как это повлияет на нарушения, не связанные с движением, так как это не их источник. Спорным также остается вопрос о приживаемости клеток, может ли их постигнуть такая же судьба, что и их предшественников. Эксперименты на крысином мозге показали положительные результаты, а значит остается только ждать итогов исследований на человеческом мозге.

Пересадка клеток мозга не может служить панацеей от болезни Паркинсона. Посмертное вскрытие нескольких пациентов показало, что заболевание может поражать и трансплантированные клетки, сообщает журнал Nature Medicine.
Американские и шведские ученые исследовали структуру мозга пациентов с болезнью Паркинсона, перенесших пересадку мозговой ткани абортированных эмбрионов. Болезнь Паркинсона сопровождается гибелью клеток, вырабатывающих нейротрансмиттер дофамин. Трансплантаты должны были заменить погибшие клетки в мозге больных и восстановить выработку необходимого вещества.
Джеффри Кордовер (Jeffrey H. Kordower) и его коллеги из Медицинского центра при Университете Раш (Чикаго) изучали мозг женщины, скончавшейся спустя 14 лет после пересадки мозговой ткани. По их данным, после трансплантации, проведенной в 1993 году, состояние пациентки улучшилось. Однако в 2004 году болезнь вновь начала прогрессировать, и в 2007 году пациентка скончалась. В свою очередь, шведские ученые из Неврологического центра Валленберга исследовали мозг двоих пациентов, умерших спустя 11 и 16 лет после трансплантации.
По данным исследователей, у всех троих пациентов были обнаружены признаки, свидетельствующие о поражении трансплантатов болезнью Паркинсона. В частности, некоторые из пересаженных нейронов содержали так называемые тельца Леви – скопления белка альфа-синуклеина, характерные для этого заболевания.
Пока неизвестно, будет ли болезнь поражать собственные стволовые клетки пациентов (например, полученные из клеток кожи). Для ответа на этот вопрос необходимы дальнейшие углубленные исследования, отмечают ученые.
NAME] => URL исходной статьи [
Ссылка на публикацию: MedPortal
Пересадка клеток мозга не может служить панацеей от болезни Паркинсона. Посмертное вскрытие нескольких пациентов показало, что заболевание может поражать и трансплантированные клетки, сообщает журнал Nature Medicine.
Американские и шведские ученые исследовали структуру мозга пациентов с болезнью Паркинсона, перенесших пересадку мозговой ткани абортированных эмбрионов. Болезнь Паркинсона сопровождается гибелью клеток, вырабатывающих нейротрансмиттер дофамин. Трансплантаты должны были заменить погибшие клетки в мозге больных и восстановить выработку необходимого вещества.
Джеффри Кордовер (Jeffrey H. Kordower) и его коллеги из Медицинского центра при Университете Раш (Чикаго) изучали мозг женщины, скончавшейся спустя 14 лет после пересадки мозговой ткани. По их данным, после трансплантации, проведенной в 1993 году, состояние пациентки улучшилось. Однако в 2004 году болезнь вновь начала прогрессировать, и в 2007 году пациентка скончалась. В свою очередь, шведские ученые из Неврологического центра Валленберга исследовали мозг двоих пациентов, умерших спустя 11 и 16 лет после трансплантации.
По данным исследователей, у всех троих пациентов были обнаружены признаки, свидетельствующие о поражении трансплантатов болезнью Паркинсона. В частности, некоторые из пересаженных нейронов содержали так называемые тельца Леви – скопления белка альфа-синуклеина, характерные для этого заболевания.
Пока неизвестно, будет ли болезнь поражать собственные стволовые клетки пациентов (например, полученные из клеток кожи). Для ответа на этот вопрос необходимы дальнейшие углубленные исследования, отмечают ученые.
Город G20
Болезнь Паркинсона нередко приходит после тяжелого переживания. Вот одна из историй. Антонина Сергеевна пережила стресс: сын с невесткой подали на развод. После нервного потрясения у нее стала дрожать рука. Вскоре дети забрали из загса заявление. Драма ушла, а дрожь в руке осталась. Женщина обратилась к врачу. У пациентки выявили дрожательный паралич. Это дегенеративное поражение центральной нервной системы. Дрожание и скованность мышц — основные проявления недуга. Заболевание хроническое, порой быстро прогрессирующее. Приводит к инвалидности и смерти.
Остановить болезнь нельзя. Все нарушения необратимые. Сегодня медики работают над тем, чтобы затормозить разрушительный процесс.
Число пациентов с болезнью Паркинсона неуклонно растет. Тенденцию связывают с постарением населения. Но это не единственная причина болезни. В практике врача-невролога Александра Бойко были пациенты и 25—40 лет. Ученые обнаружили немало других факторов, которые провоцируют дрожательный паралич.
Все ароматы гладиолуса
Бывает, паркинсонизм набирает силу исподволь, годами. Возникают нетипичные для обывателя признаки. Например, человек вдруг теряет обоняние. Способность ощущать запахи не возвращается месяцами. И долгое время обонятельный паралич остается единственным симптомом надвигающегося недуга.
— Была пациентка 60 лет, — вспоминает Александр Бойко. – У нее пропало обоняние после перенесенной инфекции. Есть люди, которые и десять, и двадцать лет живут без ощущения запахов, а только потом присоединяются двигательные расстройства. Вообще, болезнь Паркинсона рассматривают как основную причину потери обоняния у лиц 40—60 лет. На домоторной стадии паркинсонизма возникают проблемы со стулом, нарушается сон. Но обычно к неврологу обращаются уже на этапе двигательных нарушений, когда дрожание и скованность очевидны и долго не исчезают.
Как помогают таким больным?
— Лечение болезни сейчас во всем мире пока только симптоматическое. Устранить нарушения, которые случились, уже невозможно, например, вернуть обоняние, убрать дрожь в руке, скованность в плече. Вся терапия направлена на восстановление баланса нейромедиаторов в головном мозге. Считается, что ввиду различных причин снижается уровень дофамина в межклеточном пространстве. И препараты направлены на то, чтобы его поднять. Выраженность двигательных расстройств уменьшается, но сама болезнь развивается. Применяют электростимуляцию глубинных структур мозга. Это нейрохирургический метод.
Пробуждение клетками
Сотрудники БелМАПО, среди которых и доктора медицинских наук Владимир Пономарев и Марина Зафранская, впервые предложили системный подход к лечению паркинсонизма с помощью клеточных технологий. Доклинические испытания на лабораторных крысах доказали эффективность терапии. В следующем году медики приступят к работе с пациентами.
— Программы перехода от доклинических исследований к пациенту нигде нет, — обращает внимание Александр Васильевич. – Сейчас мы проводим исследования на культурах клеток и лабораторных животных. Параллельно у пациентов осуществляем забор крови, ликвора, костного мозга, смотрим иммунный статус, степень нейродегенеративных и нейровоспалительных изменений. Оцениваем эффективность лечения стволовыми клетками крыс. Ведем дорогу к человеку. Пытаемся определить, какая группа пациентов лучше всего ответит на клеточный метод.
— Что же удалось обнаружить во время работы над проектом?
— Мы нашли дополнительные доказательства участия иммунной системы в возникновении и прогрессировании болезни Паркинсона. А также обнаружили у пациентов с паркинсонизмом нарушение гематоэнцефалического барьера – механизмов, которые регулируют потоки веществ между кровью и тканью мозга. Провоцирующий фактор в каждом конкретном случае определяет схему поведения иммунной системы. Эти открытия позволяют перейти к индивидуальному подходу в лечении пациентов с одним и тем же диагнозом в зависимости от причины болезни. Аутотрансплантация мезенхимальных стволовых клеток будет эффективна для пациентов, у которых болезнь связана с иммунными нарушениями.
— Как же работает трансплантат после пересадки?
— Клеточный материал вводили животным интраназально, внутривенно, в спинномозговую жидкость, — поясняет Александр Бойко. — Клетки проникали в нервную систему, встраивались, оказывали нейропротекторное и иммуномоделирующее действие, улучшалось состояние животных, которым смоделировали болезнь Паркинсона. В итоге двигательные признаки болезни у крыс ослабевали.
Клеточные технологии направлены на то, чтобы модифицировать течение болезни: замедлить ее прогрессирование и уменьшить выраженность моторных и немоторных симптомов. По данным работы с лабораторными животными мы предвидим однозначное улучшение состояния у правильно подобранных для трансплантации пациентов.
В октябре 2018 японские исследователи из университета Киото (Япония) в рамках экспериментальной терапии болезни Паркинсона пересадили в мозг пациента полученные от здоровых доноров индуцированные плюрипотентные стволовые клетки (иПСК), которые способны превращаться в любую клетку организма. Исследовательская группа профессора Джуна Такахаши (Jun Takahashi) ожидает, что иПСК будут дифференцироваться в дофамин-продуцирующие нейроны, число которых при болезни Паркинсона снижается.
Пациентом стал 50-летний доброволец с болезнью Паркинсона. Во время первой операции нейрохирурги под руководством Такаюки Кикучи (Takayuki Kikuchi) в течение трёх часов вводили 2,4 миллиона иПСК в левую часть мозга пациента, а именно — в 12 регионов, считающихся центрами дофаминергической активности. В течение месяца после операции состояние мужчины остается стабильным, но говорить о безопасности и эффективности процедуры можно будет лишь после двух лет наблюдений. В течение следующих шести месяцев состояние пациента будет тщательно контролироваться, и при отсутствии побочных эффектов, исследователи трансплантируют еще 2,4 миллиона иПСК в правую часть мозга пациента.
К 2020 году в исследование планируется включить еще шесть пациентов-добровольцев в возрасте от 50 до 69 лет. В случае успеха этот способ терапии может произвести революцию в лечении болезни Паркинсона, поскольку для этого заболевания существует лишь симптоматическое лечение, а проводимые ранее эксперименты по терапии стволовыми клетками показали лишь скромные результаты.
Исследования эффективности эмбриональных стволовых клеток для лечения болезни Паркинсона ведутся уже около 40 лет и первоначально проводились на крысах и обезьянах. Результаты этих исследований оказались достаточно перспективными и около 30 лет назад были запущены первые клинические испытания на добровольцах.
Трансплантация стволовых клеток для лечения болезни Паркинсона достаточно сложна: для неё требуется, во-первых, эти стволовые клетки получить, а во-вторых, провести хирургическое вмешательство, чтобы ввести их пациенту. Существует несколько различных источников, используемых для получения дофаминергических клеток человека для трансплантации при болезни Паркинсона. В различных исследованиях использовали: эмбриональные дофаминергические нейроны, аутологичные дофамин-секретирующие нейроны, мезенхимальные стволовые клетки, полученные из костного мозга, а также эмбриональные стволовые клетки, полученные из костного мозга. Наибольшая эффективность была показана для дофаминергических нейронов, полученных из плюрипотентных стволовых клеток, и репрограммированных соматических клеток взрослого человека.
На сегодняшний день имеются данные о результатах небольших клинических испытаний, среди которых — сведения об исходе трансплантации, проведённой более 10 лет назад.
Так, в статье, опубликованной в JAMA Neurology исследователями из Лунда (Швеция), описаны два пациента, которым в полосатое тело (стриатум) головного мозга был трансплантирован участок вентральной мезенцефалической области мозга плода человека, богатый дофаминергическими нейробластами. Состояние одного из пациентов оценивалось через 15 лет после трансплантации, второго — через 18 лет. В последнем случае пациенту не требовалась заместительная терапия дофамином, наблюдалась устойчивость моторных функций без каких-либо изменений и пациент мог выполнять все повседневные действия без посторонней помощи. После введения стволовых клеток, у данного пациента наблюдались дискинезии, но терапия амантадина гидрохлоридом и буспирона гидрохлоридом ослабляла их, а степень этих побочных эффектов была менее выраженной по сравнению с дискинезиями, к которым приводила терапия леводопой до трансплантации. У пациента, состояние которого оценивалось через 15 лет после трансплантации, наблюдалась сохранность моторных функций и ему также не требовались дофаминергические препараты и посторонняя помощь в повседневных делах. После трансплантации у него также наблюдались дискинезии, которые незначительно ослабевали при терапии амантадином.
Авторы исследования отмечают, что результаты, наблюдаемые у этих двух пациентов, являются, скорее, исключением из общей массы существующих данных об исходе трансплантации стволовых клеток.
В другой статье описывается пациент, перенесший одностороннюю трансплантацию эмбриональных дофаминэргических нейронов, полученных от четырех доноров, в область скорлупы чечевицеобразного ядра справа. На момент операции пациенту было 59 лет и он прожил еще 24 года после операции. В течение примерно 12 месяцев после операции состояние пациента не изменялось (наблюдался латентный период) и лишь затем началось клиническое улучшение. Ещё через несколько лет он смог прекратить прием леводопы, однако возобновил его примерно через пять лет после операции. В целом клиническое улучшение продолжалось приблизительно 10 лет, прежде чем у пациента вновь начали проявляться нарушения моторных функции и симптомы слабоумия. Вскрытие показало, что из трансплантированных дофаминергических нейронов прижилось примерно 42 000, а в скорлупе наблюдалась значительная дофаминергическая иннервация.
На данный момент (как показано в одном из последних мета-анализов), исследованию эффективности терапии стволовыми клетками при болезни Паркинсона посвящена 21 статья. В силу того, что достоверность имеющихся доказательств низка, требуются дополнительные исследования, посвященные изучению вопроса о том, могут ли стволовые клетки улучшить течение болезни Паркинсона. Сейчас такие исследования ведутся в Гонконге, США, Великобритании и, как указано в начале поста, Японии.
Болезнь Паркинсона: клетка отсчета



- К сожалению, широко используемые сегодня лекарства только снимают симптомы болезни Паркинсона и не позволяют замедлить ее прогрессирование, — признает Владимир Владимирович. — Более того, известные противопаркинсонические средства неэффективны против таких проявлений недуга, как, например, способность удерживать равновесие или депрессия, а сам длительный прием препаратов сопряжен с развитием серьезных побочных эффектов. Вот почему в повестке дня поиск альтернативных методов, среди них клеточная терапия представляется наиболее перспективной. Ведь при болезни Паркинсона нейродегенеративный процесс локализован, затрагивает преимущественно компактную часть черного вещества головного мозга, а значит, это удобная мишень.
Подспорьем медикам здесь могут послужить 5 типов стволовых клеток. У каждого свои не только достоинства, но, увы, и недостатки. Скажем, к эмбриональным стволовым клеткам у многих есть вопросы морально–этического и религиозного толка, плюс к этому у них, как и у соматических клеток взрослого организма, очень высока способность к самообновлению и дифференциации. А значит, словно дамоклов меч, нависает угроза запустить раковый процесс. В этом плане нервные стволовые клетки безопаснее, но поскольку получают их из мозга, материал в больших количествах не выделить и потом нужно долго культивировать, что сложно технически. Есть еще так называемые плюрипотентные линии партеногенетических клеток, однако что они дают на практике — ученым предстоит тщательно изучить. В общем, четко прослеживается пока только один путь — мезенхимальные стволовые клетки. Их можно получить из любого участка соединительной ткани, от плаценты до костного мозга, а с ними и как минимум 10 важных функциональных особенностей, которые трансплантации в помощь. Такие клетки вообще все чаще используются в борьбе с нейродегенеративными заболеваниями, и болезнь Паркинсона не оказалась исключением.
Спросите: а при чем здесь наша страна, какое отношение она имеет ко всем этим глубоко научным спорам? Самое непосредственное. По словам Владимира Пономарева, мы тоже встали на этот путь и на нем продвинулись:
— Проведенные нашей кафедрой исследования дают основания полагать, что клеточная терапия наиболее подходит пациентам, у которых болезнь Паркинсона быстро развивается. Их в общей когорте больных — около 10%. Еще раньше мы обнаружили, что у них есть выраженные иммунные изменения в сыворотке крови и цереброспинальной жидкости. Все это позволило обосновать иммунную концепцию быстропрогрессирующего типа болезни.
Шанс столкнуться с болезнью Паркинсона в течение жизни — 2,5%. Однако риск унаследовать недуг, показали скрининги на Западе, велик — 1 к 2, и у каждого десятого человека старше 50 он на старте. По официальной статистике, как минимум 10 тысяч белорусов страдают дрожательным параличом, еще около 2 тысяч имеют так называемый паркинсонизм плюс, который при тех же симптомах является отголоском других заболеваний нервной системы.
Жизнестойкость донорских клеток тоже волнует ученых. Они же могут погибнуть, скажем, из–за недостатка кислорода или глюкозы, механического повреждения в ходе процедуры, атаки свободных радикалов. Хуже того, точно установлено, что патологический процесс из клеток–хозяек способен перекидываться и на клетки–помощницы, хотя потом и медленно идет. Еще одна опасность — возникновение после операции непроизвольных движений. Как бы то ни было, пациенты с болезнью Паркинсона намного дольше чувствуют облегчение после клеточной терапии, чем на фоне использования только привычных лекарств. Это доказанный факт.
Эксперименты по пересадке в мозг клеток зародышей велись с 1960–х годов во многих странах, пионерами здесь выступили нейрохирурги на Кубе. Однако жизнь показала, что такие клетки у человека по каким–то причинам не приживаются.
Будьте в курсе
5 — 6 пациентов с паркинсонизмом из каждых 10 жалуются на ухудшение настроения. А 9 из 10 — на обоняние: первой жертвой недуга становится именно обонятельная луковица.
Читайте также:


