Чем вызваны нервно мышечная передача
Передача стимула от аксона на скелетное мышечное волокно происходит на двигательной концевой пластинке (A), которая представляет собой вид химического синапса. Медиатором, участвующим в данном процессе, является ацетилхолин (АХ), связывающийся с N (никотинергическим) холинорецептором мембраны постсинаптической мышечной клетки (АЗ). N-холинорецепторы ионотропны - они функционируют как ионные каналы (А4). N-Холинорецептор двигательной концевой пластинки состоит из 5 субъединиц (2а, 1 р, 1у, 16), каждая из которых содержит 4 пересекающих мембрану а-спирали.
Канал ненадолго открывается (Б1) (примерно на 1 мс) после связывания молекулы АХ с двумя субъединицами N-холинорецептора (А4). В отличие от зависимых от потенциала Na + -каналов, вероятность открывания (рo) N-холинорецептора не увеличивается при деполяризации, а зависит от концентрации ацетилхолина в синаптической щели.
- от количества открытых каналов, которое равно произведению количества каналов (л) на вероятность их открывания (д0), что, в свою очередь, определяется концентрацией ацетилхолина в синаптической щели (до 1 ммоль/л);
- проводимости одиночного канала у (примерно 30 пСм);
- мембранного потенциала Еm (в слабой степени): электрическая движущая сила (Еm-ENaK) уменьшается, когда Еm менее отрицателен.
ЕNа.к - это общий равновесный потенциал для Na + и К + , близкий к 0 мВ. Эта величина также называется обратным потенциалом, потому что направление тока Iкп(INa. + IK) становится противоположным, если Еm меняет знак: Iкп направлен в клетку, когда Еm + больше оттока К + ) и из клетки при Еm > 0 (отток К + больше притока Na + ). В результате
Iкп = n * po * y * (Em-ENaK) [А]. [2.1]
Поскольку в скелетной мышце индуцированный нейроном потенциал концевой пластинки (деполяризация примерно до 70 мВ) гораздо выше, чем возбуждающий постсинаптический потенциал (всего несколько несколько мВ), потенциал действия одиночного двигательного аксона выше порогового уровня. Потенциал концевой пластинки проводится электротонически до ближайшей сарколеммы, где генерируется мышечный потенциал действия при помощи потенциалзависимых Na + -каналов, приводящий к мышечному сокращению.
Окончание синаптической передачи в двигательной концевой пластинке наступает (1) из-за быстрой деградации ацетилхолина в синаптической щели под действием ацетилхолинэстеразы, локализованной на постсинаптической базальной мембране, и (2) при диффузии ацетилхолина из синаптической щели.
Двигательная концевая пластинка может быть блокирована некоторыми ядами и лекарствами, что приводит к мышечной слабости и иногда к параличу. Нейротоксин ботулин, например, ингибирует высвобождение нейромедиаторов из везикул, а а-бунгаротоксин из яда кобры блокирует открывание ионных каналов. Курареподобные агенты, такие как D-тубокурарин, используют как мышечные релаксанты при хирургических операциях. Они вытесняют ацетилхолин из его центров связывания (конкурентное ингибирование), но не имеют собственного деполяризующего эффекта. Их тормозной эффект можно снять ингибиторами холинэстеразы, например неостигмином (декураризация). Эти вещества увеличивают концентрацию ацетилхолина в синаптической щели, вытесняя кураре. Вход антихолинэстеразных агентов в интактный синапс ведет к увеличению концентрации ацетилхолина и, таким образом, к параличу из-за непрерывной деполяризации. Ацетилхолиноподобные вещества, такие как суксаметоний, оказывают похожий деполяризующий эффект, но разрушаются медленнее, чем ацетилхолин. В этом случае паралич, наступающий из-за непрерывной деполяризации, также необратимо инактивирует Na + -каналы вблизи двигательной концевой пластинки на сарколемме.
Развитие нервно-мышечной активности происходит независимо от роста мышц. Вот почему вы никогда не можете сказать наверняка, насколько силен какой-либо человек, руководствуясь размером его мышц. Человек с относительно небольшими мускулами и высоким уровнем нервно-мышечной активности с большей вероятностью сможет победить человека с большими мускулами и низким уровнем нервно-мышечной активности.
В идеале тренировки на увеличение площади поперечного сечения мускулов отличаются от тренировок на повышение нервно-мышечной активности. Если вы новичок, то, скорее всего, вы не заметите этой разницы и любой вид тренировок поможет вам как увеличить размеры мускулов, так и повысить нервно-мышечную активность. Увеличивая количество упражнений или вес штанги, вы продолжите развивать площадь поперечного сечения ваших мускулов, а также повышать нервно-мышечную активность. Хотя, становясь более опытным, вы придете к выводу, что это просто невозможно найти такой вид тренировок, который бы увеличил размеры и силу мускулов одновременно. На самом деле вы не можете увеличить количество упражнений и вес штанги одновременно. Если вы хотите увеличить объем ваших тренировок, вам неминуемо придется ограничить количество веса, который вы поднимаете, таким образом, ваши мускулы не станут изнуренными очень быстро. Но если вы решите увеличить вес, который вы поднимаете, то вам нужно ограничить объем тренировок, потому что поднятие (работа) с очень тяжелым весом утомляет мускулы.
Поднимать очень тяжелые грузы — это наиболее эффективный способ увеличить нервно-мышечную активность. Поэтому если вы предпочтете увеличить количество упражнений вместо весов, с которыми вы их выполняете, вы, вероятнее всего, придете к такому состоянию, когда количество упражнений, которые вы выполняете для того, чтобы увеличить размеры своих мускулов, выполняются за счет вашей нервно-мышечной активности, а сила мышц вообще перестает развиваться. Хотя если вашей целью является повышение максимальной силы мышц настолько, насколько это возможно, то вам нужно тренироваться таким способом, который бы сбалансировал рост мышц и развитие нервно-мышечной активности.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Нарушение нервно-мышечной передачи происходит вследствие дефектов постсинаптических рецепторов (например, при миастении) или пресинаптического высвобождения ацетилхолина (например, ботулизм), а также распада ацетилхолина в синаптической щели (действие лекарственных или нейротоксических препаратов). Типичны флюктуации степени мышечной слабости и утомляемости.
Код по МКБ-10
Болезни, при которых происходит нарушение нервно-мышечной передачи
Синдром Итона-Ламберта развивается при нарушении высвобождения ацетилхолина из пресинаптических нервных окончаний.
Ботулизм - последствие нарушения высвобождения ацетилхолина пресинаптической терминалью из-за необратимого связывания с нею токсина Clostridium botulinum. Среди симптомов выраженная слабость вплоть до нарушений дыхания и признаки увеличения симпатического тонуса из-за блокирования парасимпатической активности: мидриаз, сухость во рту, запор, задержка мочи, тахикардия, чего не бывает при миастении. На ЭМГ умеренное снижение ответа на низкочастотное (2-3 в 1 секунду) раздражение нерва и рост ответа при увеличении частоты раздражения (50 имп/с) или после кратковременной (10 с) мышечной работы.
Лекарства или токсические вещества могут нарушать функцию нервно-мышечного синапса. Холинергические препараты, фосфорорганические инсектициды и большинство нервнопаралитических газов блокируют нервно-мышечную передачу, деполяризуя постсинаптическую мембрану из-за избыточного действия ацетилхолина на ее рецепторы. Результат: миоз, бронхорея, миастеноподобная слабость. Аминогликозиды и полипептидные антибиотики уменьшают пресинаптическое высвобождение ацетилхолина и чувствительность к нему постсинаптической мембраны. На фоне латентной миастении высокие концентрации этих антибиотиков в сыворотке усугубляют нервно-мышечный блок.
Продолжительное лечение пеницилламином может сопровождаться обратимым синдромом, который клинически и по ЭМГ напоминает миастению. Избыток магния (уровень в крови 8-9 мг/дл) чреват развитием выраженной слабости, что также напоминает миастенический синдром. Лечение включает устранение токсического воздействия, интенсивное наблюдение и при необходимости ИВЛ. Для уменьшения избыточной бронхиальной секреции назначают атропин 0,4-0,6 мг внутрь 3 раза/ день. При отравлении фосфорорганическими инсектицидами или нервно-паралитическим газом могут потребоваться более высокие дозы (2-4 мг в/в за 5 мин).
Синдром ригидного человека - это внезапное появление прогрессирующей ригидности мышц туловища и живота, в меньшей степени - конечностей. Других отклонений, в том числе и на ЭМГ, нет. Этот аутоиммунный синдром развивается как паранеопластический (чаще при раке груди, легких, прямой кишки и при болезни Ходжкина). Аутоантитела против нескольких белков, связанных с ГАМК глициновыми синапсами, воздействуют преимущественно на ингибиторные нейроны передних рогов спинного мозга. Лечение симптоматическое. Диазепам существенно уменьшает мышечную ригидность. Результаты плазмафереза противоречивы.
Синдром Исаакса (синонимы: нейромиотония, синдром броненосца) проявляется, главным образом, жалобами на работу конечностей. Появляются миокимии - мышечные фасцикуляции, выглядящие как конгломерат шевелящихся под кожей червей. Другие жалобы: карпопедальные спазмы, интермиттирующие крампи, повышенное потоотделение и псевдомиотония (нарушение расслабления после сильного мышечного сокращения, но без типичного для истинной миотонии нарастания - убывания на ЭМГ). Первоначально поражает периферический нерв, поскольку кураре снимает жалобы, а под общим наркозом симптомы сохраняются. Причина неизвестна. Карбамазепин или фенитоин уменьшают жалобы.

Молекулы ацетилхолина диффундируют через синаптическую щель и взаимодействуют с никотиночувствительными холинорецепторами (н-холинорецепторами) специализированной части мембраны мышечной клетки — концевой пластинкой скелетной мышцы.
Каждый холинорецептор состоит из пяти белковых субъединиц, две из которых (?-субъединицы) одинаковы и способны связывать молекулы ацетилхолина (одна ?-субъединица — одно место связывания). Если оба места связывания заняты двумя молекулами ацетилхолина, то конформация субъединиц изменяется, что приводит к кратковременному (на 1 мс) открыванию ионного канала, проходящего через толщу рецептора (рис. 9-2).
Через открытый канал начинают поступать катионы (натрий и кальций — извне внутрь клетки, калий — из клетки наружу), что вызывает появление потенциала концевой пластинки. Содержимое одного синаптического пузырька — квант ацетилхолина — вызывает миниатюрный потенциал концевой пластинки (1 квант — 10 000 молекул ацетилхолина). Если ацетилхолином занято достаточное количество рецепторов, то суммарный потенциал концевой пластинки становится достаточно мощным для того, чтобы деполяризовать постсинаптическую мембрану вокруг синапса. Натриевые каналы в этой части мембраны мышечной клетки открываются под воздействием разности потенциалов (в отличие от каналов в рецепторах концевой пластинки, которые открываются при взаимодействии с ацетилхолином). Возникающий потенциал действия распространяется вдоль мембраны мышечной клетки и системы Т-трубочек, что вызывает открывание натриевых каналов и выброс ионов кальция из цистерн саркоплазматической сети. Высвобожденный кальций опосредует взаимодействие сократительных белков актина и миозина, что приводит к сокращению мышечного волокна. Количество высвобожденного ацетилхолина обычно значительно превосходит минимум, необходимый для развития потенциала действия. Некоторые заболевания нарушают процесс нервно-мышечной передачи: при миастеническом синдроме Итона-Ламберта высвобождается недостаточное количество ацетилхолина, при миастении (myasthenia gravis) снижено число холинорецепторов.
Субстратспецифический фермент ацетилхолинэстераза быстро гидролизует ацетилхолин на уксусную кислоту и холин. Молекулы этого фермента (называемого также специфической, или истинной, холинэстеразой) фиксированы в концевой пластинке в непосредственной близости от холинорецепторов. В конечном счете ионные каналы закрываются, что приводит к реполяриза-ции концевой пластинки. Когда распространение потенциала действия прекращается, ионные каналы в мембране мышечного волокна тоже закрываются. Кальций поступает обратно в сарко-плазматическую сеть, и мышечное волокно расслабляется.

Рис. 9-2. Связывание ацетилхолина с рецептором концевой пластинки скелетной мышцы приводит к открыванию канала и вызывает ионный ток
Передача возбуждения в нервно-мышечном синапсе
ВОПРОС: 80. Сократимость. Механизмы мышечного сокращения.
Для скелетной мышцы характерны два основных режима сокращения - изометрический и изотонический. Изометрический режим проявляется в том, что в мышце во время ее активности нарастает напряжение (генерируется сила), но из-за того, что оба конца мышцы фиксированы (например, мышца пытается поднять большой груз) - она не укорачивается. Изотонический режим проявляется в том, что мышца первоначально развивает напряжение (силу), способную поднять данный груз, а потом мышца укорачивается - меняет свою длину, сохраняя напряжение, равное весу поднимаемого груза. Так как изотоническое сокращение не является "чисто" изотоническим (элементы изометрического сокращения имеют место в самом начале сокращения мышцы), а изометрическое сокращение тоже не является "чисто" изотоническим (элементы смещения все-таки есть, несомненно), то предложено употреблять термин "ауксотоническое сокращение" - смешанное по характеру.
Понятия "изотонический", "изометрический" важны для анализа сократительной активности изолированных мышц и для понимания биомеханики сердца.
Режимы сокращения гладких мышц. Целесообразно выделить изометрический и изотонический режимы (и, как промежуточный - ауксотонический). Например, когда мышечная стенка полого органа начинает сокращаться, а орган содержит жидкость, выход для которой перекрыт сфинктером, то возникает ситуация изометрического режима: давление внутри полого органа растет, а размеры ГМК не меняются (жидкость не сжимается). Если это давление станет высоким и приведет к открытию сфинктера, то ГМК переходит в изотонический режим функционирования - происходит изгнание жидкости, т.е. размеры ГМК уменьшаются, а напряжение или сила - сохраняется постоянной и достаточной для изгнания жидкости.
Виды сокращений
У скелетной мышцы выделяют одиночное сокращение и суммированное сокращение, или тетанус. Одиночное сокращение - это сокращение, которое возникает на одиночный стимул, достаточный для вызова возбуждения мышцы. После короткого скрытого периода (латентный период) начинается процесс сокращения. При регистрации сократительной активности в изометрических условиях (два конца неподвижно закреплены) в первую фазу происходит нарастание напряжения (силы), а во вторую - ее падение до исходной величины. Соответственно эти фазы называют фазой напряжения и фазой расслабления. При регистрации сократительной активности в изотоническом режиме (например, в условиях обычной миографической записи) эти фазы будут называться соответственно фазой укорочения и фазой удлинения. В среднем сократительный цикл длится около 200 мс (мышцы лягушки) или 30-80 мс (у теплокровных). Если на мышцу действует серия прямых раздражении (минуя нерв) или непрямых раздражении (через нерв), но с большим интервалом, при котором всякое следующее раздражение попадает в период после окончания 2-й фазы, то мышца будет на каждый из этих раздражителей отвечать одиночным сокращением.
Суммированные сокращения возникают в том случае, если на мышцу наносятся 2 и более раздражения, причем всякое последующее раздражение (после предыдущего) наносится либо во время 2-й фазы (расслабления или удлинения), либо во время 1-й фазы (укорочения или напряжения).
В случае, когда всякое второе раздражение попадает в период фазы расслабления (удлинения), возникает частичная суммация - сокращение еще полностью не закончилось, а уже возникло новое. Если подается много раздражителей с подобным интервалом, то возникает явление зубчатого тетануса. Если раздражители наносятся с меньшим интервалом и каждое последующее раздражение попадает в фазу укорочения, то возникает так называемый гладкий тетанус.
ВОПРОС: 81.Оценка возбудимости нервной клетки, пороговая сила раздражителя. Аккомодация.Общим свойством живой материи является ее раздражимость. Раздражимость – это реакция отдельных клеток или тканей на действие раздражителя. Раздражитель – это любое изменение внешней или внутренней среды организма, воспринимаемое клетками и вызывающее ответную реакцию. По природе раздражители бывают физические (электрические, механические, температурные, световые) и химические. Частным случаем раздражимости является возбудимость. Возбудимость – это свойство нейрона генерировать потенциал действия (ПД) на раздражение. К возбудимым клеткам относятся только те клетки, которые генерируют потенциал действия. К ним относятся нейроны и мышечные клетки. Проводимость (как общее понятие) – это способность ткани и клетки проводить возбуждение.
Оценка возбудимости клетки
Возбудимость клетки изменяется не только в процессе возбуждения, но и при изменении химического состава внеклеточной жидкости. При снижении концентрации Na + вне клетки этот ион в меньшем количестве входит в клетку, в результате чего снижается ее возбудимость вследствие гиперполяризации мембраны. Показателями состояния возбудимости ткани являются пороговый потенциал, пороговая сила и пороговое время.
1. Пороговый потенциал – минимальная величина, на которую надо уменьшить МП, чтобы вызвать возбуждение. Возбудимость и пороговый потенциал находятся в обратном соотношении: чем меньше пороговый потенциал, тем выше возбудимость клетки. Однако во всех случаях ПД возникает только при достижении критического уровня деполяризации клеточной мембраны.
2. Пороговая сила – наименьшая сила раздражителя, способная вызвать импульсное возбуждение при неограниченном ее действии во времени. Большая пороговая сила свидетельствует о низкой возбудимости ткани. Обычно раздражителем в эксперименте используется электрический ток. Наименьшая сила тока, способная вызвать ПД, называется реобазой. Если раздражитель по своей амплитуде меньше реобазы, то возбуждение не возникает. Если раздражитель нарастает постепенно и медленно, то возникает аккомодация, то есть понижение возбудимости клетки, вплоть до полного исчезновения ПД. Аккомодация – это своеобразное привыкание клетки к раздражителю.
3. Пороговое время – минимальное время, в течение которого раздражитель пороговой силы должен действовать на ткань, чтобы вызвать ее возбуждение. Пороговое время называют также полезным временем, так как раздражитель обеспечивает деполяризацию только до критического уровня. Затем ПД развивается независимо от действия раздражителя. В эксперименте и в клинической практике обычно используют не полезное время, а хронаксию – наименьшее время, в течение которого должен действовать ток в две реобазы, чтобы вызвать возбуждение. Измерение хронаксии позволяет уточнить характер повреждения мышцы и ее нерва.
Описание
Передача возбуждения с соматических нервов на скелетную мускулатуру осуществляется с помощью ацетилхолина. Он выделяется пресинаптической мембраной и связывается н-холинорецепторами; активация последних инициирует комплекс изменений, приводящий к сокращению мышцы. Усиление сократительной деятельности можно получить агонистами ацетилхолина или препаратами, вызывающими накопление медиатора в синаптической щели — антихолинэстеразными средствами (см. Холиномиметические средства).
Противоположное действие оказывают миорелаксанты (см. н-Холинолитики (миорелаксанты)). В группу миорелаксантов объединяют лекарственные средства, расслабляющие скелетную мускулатуру.
Кураре и курареподобные препараты применяют в медицине для расслабления скелетной мускулатуры, главным образом, при хирургических операциях. Действие этих препаратов связано с экранирующим влиянием на н-холинорецепторы постсинаптической мембраны поперечно-полосатых мышц.
Кураре представляет собой смесь сгущенных экстрактов из южноамериканских растений видов Strychnos (S. toxifera и др.) и Chondodendron (Ch. Tomentosum, Ch. Platyphyllum и др.); он с давних пор использовался аборигенами в качестве яда для стрел (вызывает обездвиживание или смерть животного в результате асфиксии, обусловленной прекращением сокращений дыхательной мускулатуры). Еще в прошлом столетии было установлено, что вызываемое при помощи кураре обездвиживание зависит от прекращения передачи возбуждения с двигательных нервов на мышцы (Клод Бернар, Е.В. Пеликан).
Оказалось, что сходными свойствами обладают синтетические курареподобные соединения, некоторые алкалоиды и их производные.
Антидеполяризующие или недеполяризующие миорелаксанты (пахикураре) парализуют нервно-мышечную передачу, уменьшая чувствительность н-холинорецепторов синаптической области к ацетилхолину, исключая возможность деполяризации концевой пластинки и возбуждения мышечного волокна. К ним относятся d-тубокурарин, диплацина дихлорид, пипекурония бромид, атракурия безилат и др. Соединения этой группы являются истинными курареподобными веществами. Их антагонисты — антихолинэстеразные вещества: ингибирование холинэстеразы приводит к накоплению в области синапсов ацетилхолина, который при повышенной концентрации вытесняет курареподобные вещества с н-холинорецепторов и восстанавливает нервно-мышечную проводимость.
Деполяризаторы (лептокураре) расслабляют мускулатуру, вызывая, напротив, стойкую деполяризацию концевой пластинки, делая ее (подобно избыточным количествам ацетилхолина) невосприимчивой к новым импульсам и в конечном итоге также нарушая проведение возбуждения с нерва на мышцу. Препараты этой группы относительно быстро гидролизуются холинэстеразой и при однократном введении дают кратковременный эффект; разумеется, антихолинэстеразные средства усиливают их действие. Основным представителем этой группы является суксаметония йодид.
Отдельные миорелаксанты могут оказывать смешанное действие — антидеполяризующее и деполяризующее.
Ряд препаратов расслабляет соматическую мускулатуру по центральным механизмам. Миорелаксацию могут вызывать анксиолитики (см. Анксиолитики). В последние годы найдены соединения (толперизон, баклофен, тизанидин и др.), миорелаксантный эффект которых связан со специфическим влиянием на ретикулярную формацию мозга, спинальные моно- и полисинаптические рефлексы. Они устраняют повышенный тонус произвольных мышц без существенного нарушения двигательных функций. Их используют при спастических состояниях, поясничном радикулите, ревматических и других заболеваниях, сопровождающихся спазмом скелетных мышц. В механизме действия этих препаратов важную роль играет модуляция ГАМКергических процессов мозга.
Теория по нормальной физиологии на тему: Синапс. Физиология мышечных волокон. В данной статье рассматривается механизм синаптической передачи, НМС…
При создании данной страницы использовалась лекция по соответствующей теме, составленная Кафедрой Нормальной физиологии БашГМУ
Синапс — это специфическое место контакта двух возбудимых систем (клеток) для передачи возбуждения.
По способу передачи сигналов:
- механические,
- химические,
- электрические.
По виду медиатора: холинэргические и др.
Нервно-мышечный синапс (НМС) — химический, передача с помощью медиатора ацетилхолина.
Синонимы к слову НМС:
- Нервно-мышечное соединение;
- Моторная концевая пластинка.

Аксоны нервных клеток на своих окончаниях теряют миелиновую оболочку , ветвятся, и концевые веточки аксона утолщаются. Это пресинаптическая терминаль или бляшка или пуговка , которая погружается в углубление на поверхности мышечного волокна.
Покрывающая концевую веточку аксона поверхностная мембрана называется пресинаптической мембраной , т.е. это мембрана, покрывающая поверхность синаптической бляшки (терминали аксона).
Мембрана, покрывающая мышечное волокно в области синапса, называется постсинаптической мембраной , или концевой пластинкой. Она имеет извитую структуру, образуя многочисленные складки, уходящие вглубь мышечного волокна, за счет чего увеличивается площадь контакта.
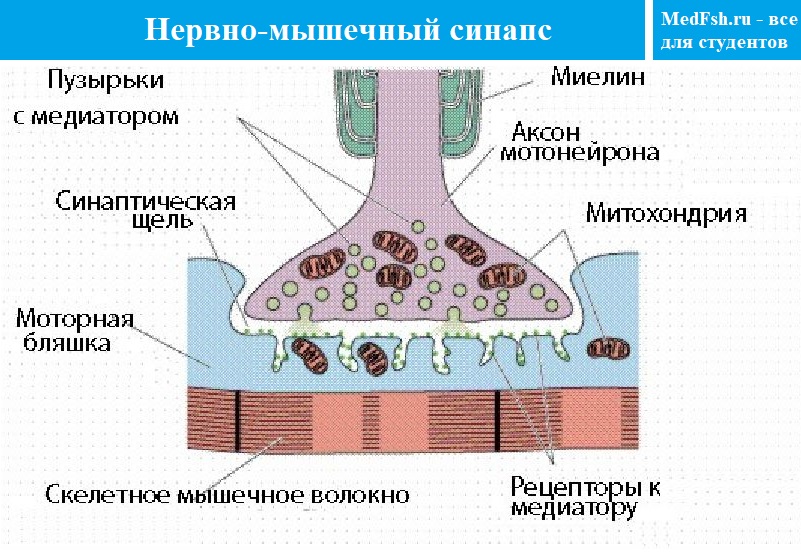
На постсинаптической мембране находятся белковые структуры — рецепторы , способные связывать медиатор . В одном синапсе количество рецепторов достигает 10-20 млн.
Между пре- и постсинаптическими мембранами находится синаптическая щель , размеры ее в среднем 50 нм, она открывается в межклеточное пространство и заполнена межклеточной жидкостью .
В синаптической щели находится мукополисахаридное плотное вещество в виде полосок, мостиков и содержится фермент ацетилхолинэстераза .
В пресинаптической терминали находится большое количество пузырьков или везикул , заполненных медиатором — химическим веществом посредником, осуществляющим передачу возбуждения.
В нервно-мышечном синапсе медиатор — ацетилхолин (АХ).
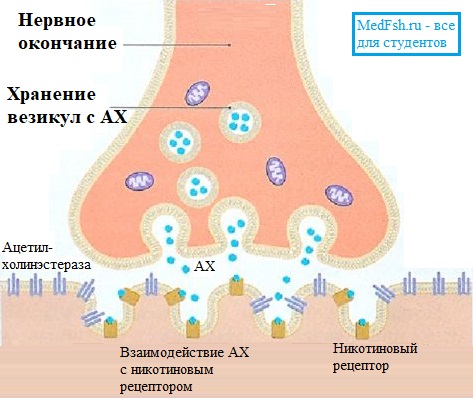
АХ синтезируется из холина и уксусной кислоты (ацетил-коэнзима А) с помощью фермента холинэстеразы. Эти вещества перемещаются из тела нейрона по аксону к пресинаптической мембране. Здесь в пузырьках происходит окончательное образование АХ.
3 фракции медиатора:
- Первая фракция — доступная — располагается рядом с пресинаптической мембраной.
- Вторая фракция — депонированная — располагается над первой фракцией.
- Третья фракция — диффузно рассеянная — наиболее удаленная от пресинаптической мембраны.
Механизм синаптической передачи

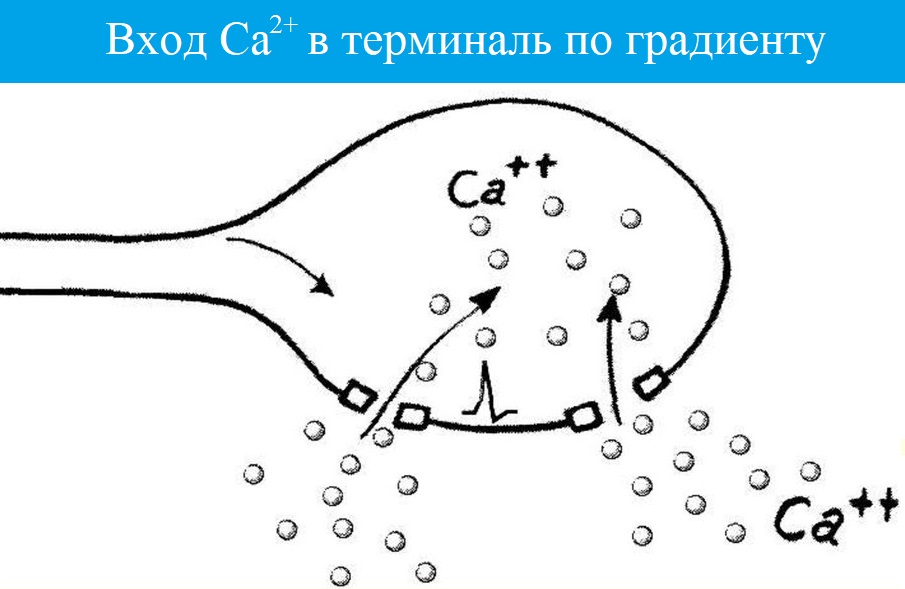
Ионы Ca вызывают образование специального белкового комплекса , который включает в себя везикулу и структуры, расположенные непосредственно около пресинаптической мембраны.
Они связаны между собой так называемыми белками экзоцитоза.
Часть белков расположена на везикулах (синапсин, синаптотагмин, синаптобревин), а часть — на пресинаптической мембране (синтаксин, синапсо-ассоциированный белок). Данный комплекс получил название секретосома .
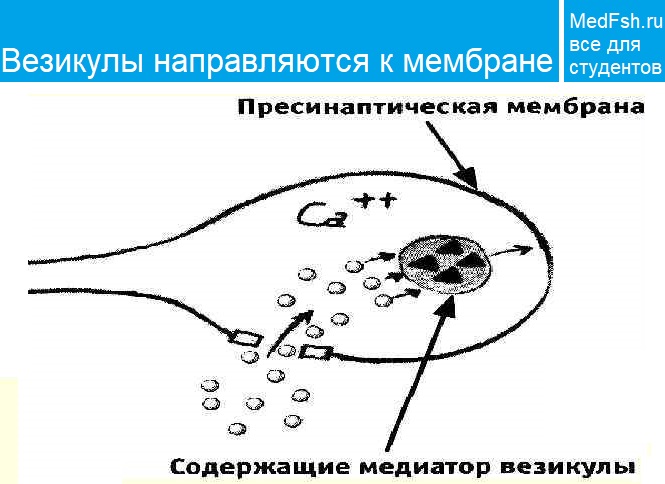
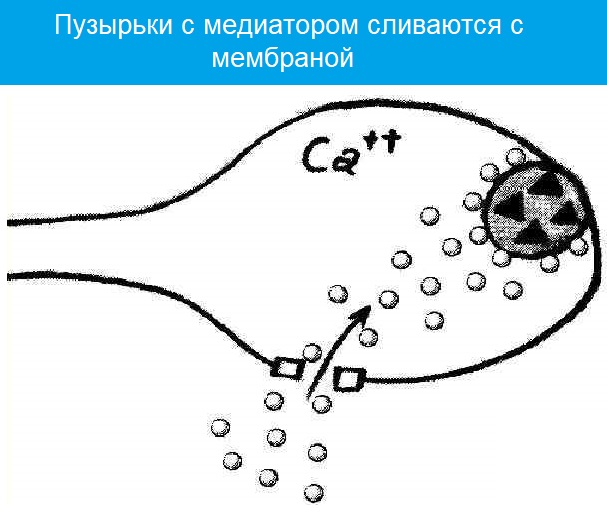
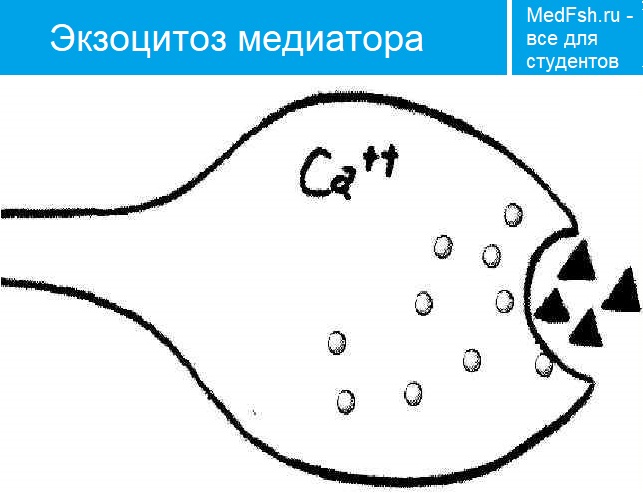
Излитию содержимого пузырька в щель способствует белок синаптопорин , формирующий канал, по которому идет выброс медиатора.
Квант медиатора — количество молекул, содержащихся в одной везикуле.
На 1 ПД выбрасывается 100 квантов АХ.
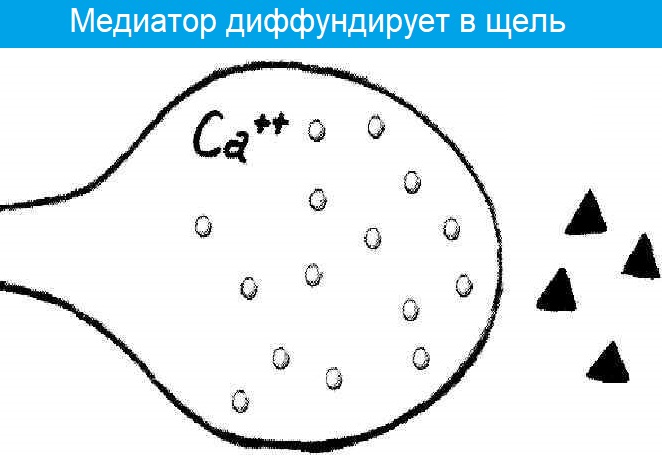
На постсинаптической мембране возникает потенциал концевой пластинки (ПКП). Он является аналогом локального ответа (ЛО).
Потенциал действия на постсинаптической мембране не возникает ! Он формируется на соседней мембране мышечного волокна.
- связывание с рецептором,
- разрушение ферментов (ацетилхолинэстеразой),
- обратное поглощение в пресинаптическую мембрану,
- вымывание из щели и фагоцитоз.
События в синапсе :
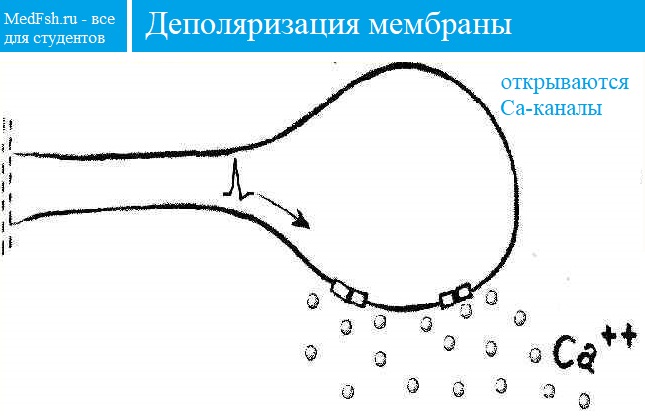
- ПД приходит к терминали аксона;
- Он деполяризует пресинаптическую мембрану;
- Ca2+ входит в терминаль, что приводит к выделению АХ;
- В синаптическую щель выделяется медиатор АХ;
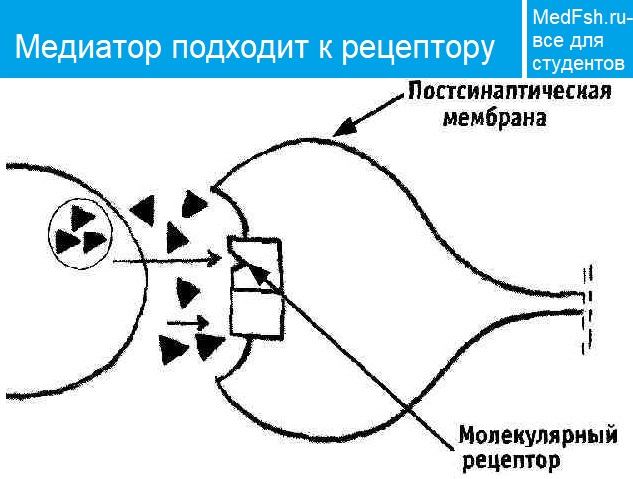
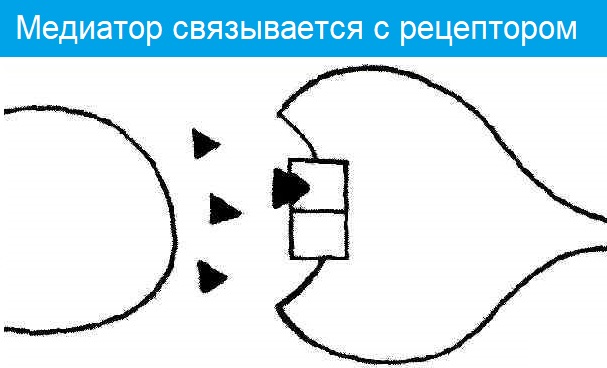
- Он диффундирует в щель и связывается с рецепторами постсинаптической мембраны;
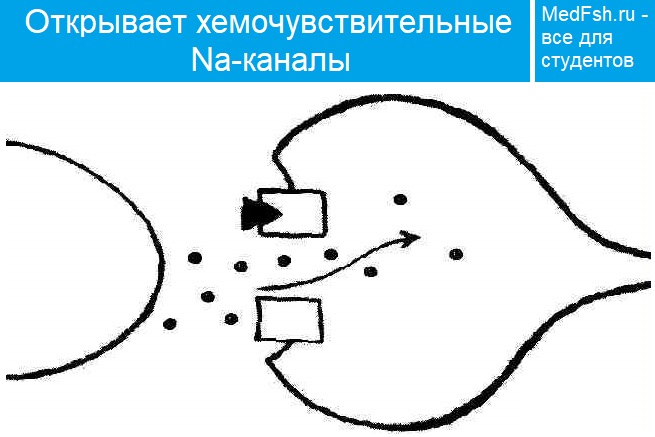
- Меняется проницаемость постсинаптической мембраны для ионов Na+;
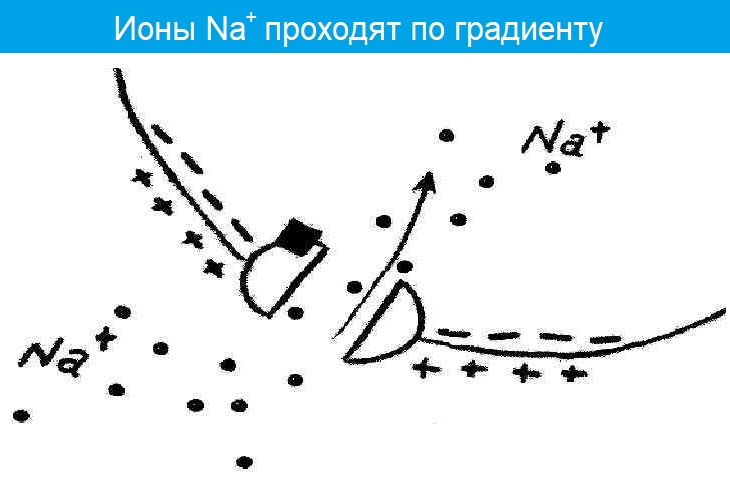
- Ионы Na+ проникают в постсинаптическую мембрану и уменьшают ее заряд — возникает потенциал концевой пластинки (ПКП) .
На самой постсинаптической мембране ПД возникнуть не может, так как здесь отсутствуют потенциалзависимые каналы, они являются хемозависимыми!
- ПКП суммируются и достигают КУД на соседнем участке мышечного волокна, что приводит к возникновению ПД и его распространению по мышечному волокну (около 5 м/с).
Достигнув пороговой величины, то есть КУД, ПКП возбуждает соседнюю (внесинаптическую) мембрану мышечного волокна за счет местных круговых токов.

Особенности проведения возбуждения в нервно-мышечном синапсе
Одностороннее проведение возбуждения — только в направлении от пресинаптического окончания к постсинаптической мембране.
Суммация возбуждения соседних постсинаптических мембран.
Синаптическая задержка — замедление в проведении импульса от нейрона к мышце составляет 0,5-1 мс. Это время затрачивается на секрецию медиатора, его диффузию к постсинаптической мембране, взаимодействие с рецептором, формирование ПКП, их суммацию.
Низкая лабильность — она составляет 100-150 имп/с для сигнала, что в 5-6 раз ниже лабильности нервного волокна.
Чувствительность к действию лекарственных веществ, ядов, БАВ, выполняющих роль медиатора.
Утомляемость химических синапсов — выражается в ухудшении проводимости вплоть до блокады в синапсе при длительном функционировании синапса. Главная причина утомляемости — исчерпание запасов медиатора в пресинаптическом окончании.
Законы проведения возбуждения по нервам:
- Закон функциональной целостности нерва.
- Закон изолированного проведения возбуждения.
- Закон двустороннего проведения возбуждения.
В зависимости от скорости проведения возбуждения нервные волокна подразделяются на 3 группы: A, B, C. В группе A выделяют 4 подгруппы: альфа, бетта, гамма и сигма.
Физиология мышечных волокон
- скелетная (40-50% массы тела),
- сердечная (менее 1%),
- гладкая (8-9%).
Физиологические свойства скелетных мышц:
- Возбудимость — способность отвечать на действие раздражителя возбуждением.
- Проводимость — способность проводить возбуждение из места его возникновения к другим участкам мышцы.
- Лабильность — способность мышцы сокращаться в соответствии с частотой действия раздражителя (200-300 Гц для скелетной мышцы).
- Сократимость — для мышцы является специфическим свойством — это способность мышцы изменять длину или напряжение в ответ на действие раздражителя.
Физические свойства скелетных мышц:
- Растяжимость — способность мышцы изменять длину под действием растягивающей силы.
- Эластичность — способность мышцы восстанавливать первоначальную длину или форму после прекращения действия растягивающей силы.
- Силы мышц — способность мышцы поднять максимальный груз.
- Способность мышцы совершать работу.
Режимы сокращения:
- Изотонический,
- Изометрический,
- Ауксотонический.
Изотонический режим — сокращение мышцы происходит с изменением ее длины без изменения напряжения (тонуса) (напр.: сокращение мышц языка).
Изометрический режим — длина постоянная, увеличивается степень мышечного напряжения (тонуса) (напр.: при поднятии непосильного груза).
Ауксотонический режим — одновременно изменяется длина и напряжение мышцы (характерен для обычных двигательных актов).
Механизм сокращения поперечно-полосатых мышц
Любая скелетная мышца состоит из мышечных волокон, которые, в свою очередь, состоят из множества тонких нитей — миофибрилл , расположенных продольно. Каждая миофибрилла состоит из протофибрилл — нитей сократительных белков: миозина (миозиновая протофибрилла), актина (актиновая протофибрилла).
Кроме сократительных белков в миофибрилле имеются два регуляторных белка: тропомиозин и тропонин .
Миозиновые волокна соединены в толстый пучок, от которого в торону актиновых нитей отходят поперечные мостики. У каждого мостика выделяют шейку и головку.
Нить актина располагается в виде 2 скрученных ниток бус. На ней имеются актиновые центры.
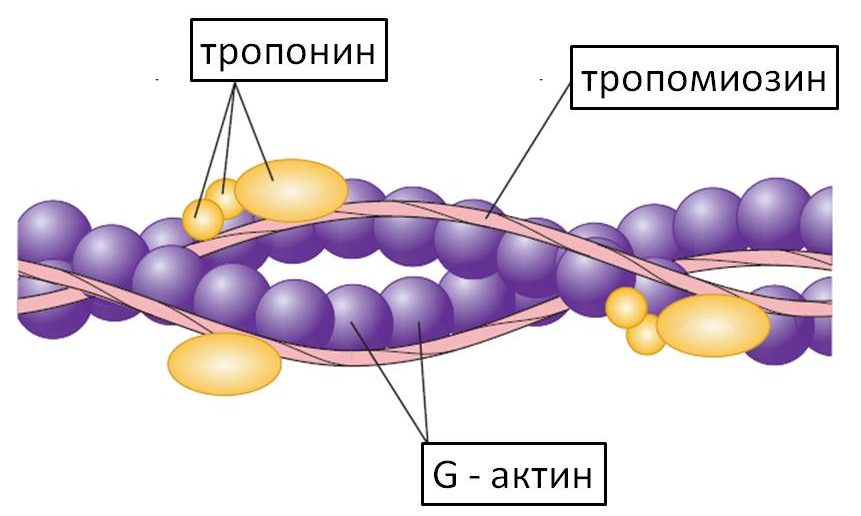
Тропомиозин в виде спиралей оплетает поверхность актина, закрывая в покое ее центры. Одна молекула тропомиозина контактирует с 7 молекулами актина.
Тропонин образует утолщение на конце каждой нити тропомиозина.
Под влиянием возникшего в мышечном волокне ПД из саркоплазматического ретикулума (СПР — депо Ca2+) высвобождаются ионы Ca. Кальций связывается с тропонином, который смещает тропомиозиновый стержень, что приводит к открытию актиновых центров.
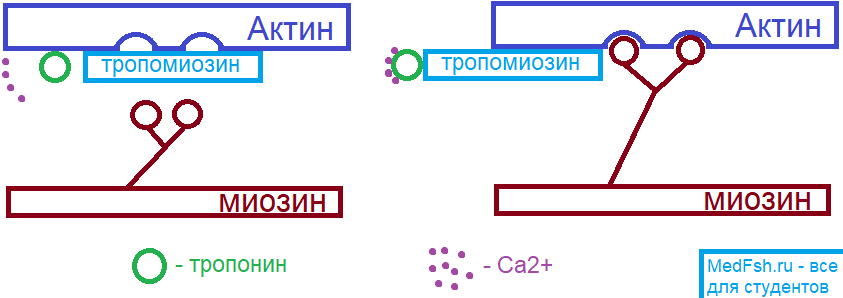
В результате, к актиновым центрам присоединяются головки поперечных миозиновых мостиков.
Процесс расслабления происходит в обратной последовательности с использованием энергии АТФ за счет функционирования кальциевого насоса.
При отсутствии повторного импульса ионы Ca не поступают из СПР. В результате отсутствия Ca-тропонинового комплекса, тропомиозин возвращается на свое прежнее место, блокируя актиновые центры актина. Актиновые протофибриллы легко скользят в обратном направлении благодаря эластичности мышцы, и мышца удлиняется (расслабляется).
Гладкие мышцы
Гладкие мышцы — это мышцы, формирующие слой стенок полых внутренних органов. Они построены из веретенообразных одноядерных мышечных клеток без поперечной исчерченности за счет хаотичного расположения миофибрилл.
Особенности гладких мышц:
- Иннервируются волокнами вегетативной нервной системы (ВНС);
- Обладают низкой возбудимостью:
- Обладают низкой величиной МП (мембранного потенциала) — -50 — -60 мВ из-за более высокой проницаемости для ионов Na+
- ПД (потенциал действия) отличается меньшей амплитудой и большей длительностью. Он формируется в основном за счет ионов Ca2+
- Медленная проводимость:
Клетки в гладких мышцах функционально связаны между собой посредством щелевидных контактов — нексусов, которые имеют низкое электрическое сопротивление. За счет этих контактов ПД распространяется с одного мышечного волокна на другое, охватывая большие мышечные пласты, и в реакцию вовлекается вся мышца.
Гладкие мышцы способны осуществлять относительно медленные ритмические и длительные тонические сокращения.
Медленные ритмические сокращения обеспечивают перемещение содержимого органа из одной области в другую.
Длительные тонические сокращения, особенно сфинктеров полых органов, препятствуют выходу из них содержимого.
Это способность сохранять приданную им при растяжении или деформации форму. Благодаря пластичности гладкая мышца может быть полностью расслаблена как в укороченном, так и в растянутом состоянии.
Особенность гладких мышц, отличающая их от скелетных. Благодаря автоматии гладкие мышцы могут сокращаться в условиях отсутствия иннервации . Важную роль в этом играет растяжение.
Растяжение является адекватным раздражителем для гладкой мускулатуры. Сильное и резкое растяжение гладких мышц вызывает их сокращение.
Сравнительная характеристика скелетных и гладких мышц:
Читайте также:


