Электрический способ от одной нервной клетки
Нервная система человека выступает своеобразным координатором в нашем организме. Она передаёт команды от мозга мускулатуре, органам, тканям и обрабатывает сигналы, идущие от них. В качестве своеобразного носителя данных используется нервный импульс. Что он собой представляет? С какой скоростью работает? На эти, а также на ряд других вопросов можно будет найти ответ в этой статье.
Чем является нервный импульс?
Исследование строения и работы
Впервые прохождение нервного импульса было продемонстрировано немецкими учеными Э. Герингом и Г. Гельмгольцем на примере лягушки. Тогда же и было установлено, что биоэлектрический сигнал распространяется с указанной ранее скоростью. Вообще, такое является возможным благодаря особенному построению нервных волокон. В некотором роде они напоминают электрический кабель. Так, если проводить параллели с ним, то проводниками являются аксоны, а изоляторами – их миелиновые оболочки (они являют собой мембрану шванновской клетки, которая намотана в несколько слоев). Причем скорость нервного импульса зависит в первую очередь от диаметра волокон. Вторым по важности считается качество электрической изоляции. Кстати, в качестве материала организмом используется липопротеид миелин, который обладает свойствами диэлектрика. При прочих равных условиях, чем больше будет его слой, тем быстрее будут проходить нервные импульсы. Даже на данный момент нельзя сказать, что эта система полноценно исследована. Многое, что относится к нервам и импульсам, ещё остаётся загадкой и предметом исследования.
Особенности строения и функционирования
Где они создаются?
Типы клеток
- Рецепторные (чувствительные). Ими кодируются и превращаются в нервные импульсы все температурные, химические, звуковые, механические и световые раздражители.
- Вставочные (также называются кондукторными или замыкательными). Они служат для того, чтобы перерабатывать и переключать импульсы. Наибольшее их число находится в головном и спинном мозге человека.
- Эффекторные (двигательные). Они получают команды от центральной нервной системы на то, чтобы были совершены определённые действия (при ярком солнце закрыть рукой глаза и так далее).
Каждый нейрон имеет тело клетки и отросток. Путь нервного импульса по телу начинается именно с последнего. Отростки бывают двух типов:
- Дендриты. На них возложена функция восприятия раздражения расположенных на них рецепторов.
- Аксоны. Благодаря им нервные импульсы передаются от клеток к рабочему органу.
Интересный аспект деятельности
О потенциале действия
Как всё работает в мозгу?
Работа нейромедиаторов
Когда они передают нервные импульсы, то существует несколько вариантов, что произойдёт с ними:
- Они будут диффундированы.
- Подвергнутся химическому расщеплению.
- Вернутся назад в свои пузырьки (это называется обратным захватом).
В конце 20-го века сделали поразительное открытие. Ученые узнали, что лекарства, что влияют на нейромедиаторы (а также их выброс и обратный захват), могут изменять психическое состояние человека коренным образом. Так, к примеру, ряд антидепрессантов вроде "Прозака" блокируют обратный захват серотонина. Есть определённые причины считать, что в болезни Паркинсона виноват дефицит в головном мозге нейромедиатора дофамина.
Если кратко, то они могут работать с тысячами нейромедиаторов, которые посылаются их соседями. Детали относительно обработки и интеграции данного типа импульсов нам почти не известны. Хотя над этим работает много исследовательских групп. На данный момент получилось узнать, что все полученные импульсы интегрируются, а нейрон выносит решение – необходимо ли поддерживать потенциал действия и передавать их дальше. На этом фундаментальном процессе базируется функционирование головного мозга человека. Ну что ж, тогда это неудивительно, что мы не знаем ответа на эту загадку.
Некоторые теоретические особенности
Где же создаются нервные импульсы?
Откуда они начинают свой путь? Ответ на этот вопрос может дать любой студент, который прилежно изучал физиологию возбуждения. Есть четыре варианта:
- Рецепторное окончание дендрита. Если оно есть (что не факт), то возможным является наличие адекватного раздражителя, что создаст сначала генераторный потенциал, а потом уже и нервный импульс. Подобным образом работают болевые рецепторы.
- Мембрана возбуждающего синапса. Как правило, такое возможно только при наличии сильного раздражения или их суммирования.
- Триггерная зона дентрида. В этом случае локальные возбуждающие постсинаптические потенциалы формируются как ответ на раздражитель. Если первый перехват Ранвье миелинизирован, то они на нём суммируются. Благодаря наличию там участка мембраны, которая обладает повышенной чувствительностью, здесь возникает нервный импульс.
- Аксонный холмик. Так называют место, где начинается аксон. Холмик – это наиболее частый создать импульсов на нейроне. Во всех остальных местах, которые рассматривались ранее, их возникновение гораздо менее вероятное. Это происходит из-за того, что здесь мембрана имеет повышенную чувствительность, а также пониженный критический уровень деполяризации. Поэтому, когда начинается суммирование многочисленных возбуждающих постсинаптических потенциалов, то раньше всего на них реагирует холмик.
Пример распространяющегося возбуждения
Вспомните сводки из новостей прошлого лета (также это скоро можно будет услышать опять). Пожар распространяется! При этом деревья и кустарники, которые горят, остаются на своих местах. А вот фронт огня идёт всё дальше от места, где был очаг возгорания. Аналогичным образом работает нервная система.
Часто бывает необходимо успокоить начавшееся возбуждение нервной системы. Но это не так легко сделать, как и в случае с огнем. Для этого совершают искусственное вмешательство в работу нейрона (в лечебных целях) или используют различные физиологические средства. Это можно сравнить с заливанием пожара водой.
Нервные импульсы распространяются при перемещении ионов через мембрану нервной клетки и передаются из одной нервной клетки в другую с помощью нейромедиаторов.
В результате эволюции нервной системы человека и других животных возникли сложные информационные сети, процессы в которых основаны на химических реакциях. Важнейшим элементом нервной системы являются специализированные клетки нейроны. Нейроны состоят из компактного тела клетки, содержащего ядро и другие органеллы. От этого тела отходит несколько разветвленных отростков. Большинство таких отростков, называемых дендритами, служат точками контакта для приема сигналов от других нейронов. Один отросток, как правило самый длинный, называется аксоном и передает сигналы на другие нейроны. Конец аксона может многократно ветвиться, и каждая из этих более мелких ветвей способна соединиться со следующим нейроном.
Во внешнем слое аксона находится сложная структура, образованная множеством молекул, выступающих в роли каналов, по которым могут поступать ионы — как внутрь, так и наружу клетки. Один конец этих молекул, отклоняясь, присоединяется к атому-мишени. После этого энергия других частей клетки используется на то, чтобы вытолкнуть этот атом за пределы клетки, тогда как процесс, действующий в обратном направлении, вводит внутрь клетки другую молекулу. Наибольшее значение имеет молекулярный насос, который выводит из клетки ионы натрия и вводит в нее ионы калия (натрий-калиевый насос).
Когда клетка находится в покое и не проводит нервных импульсов, натрий-калиевый насос перемещает ионы калия внутрь клетки и выводит ионы натрия наружу (представьте себе клетку, содержащую пресную воду и окруженную соленой водой). Из-за такого дисбаланса разность потенциалов на мембране аксона достигает 70 милливольт (приблизительно 5% от напряжения обычной батарейки АА).
Однако при изменении состояния клетки и стимуляции аксона электрическим импульсом равновесие на мембране нарушается, и натрий-калиевый насос на короткое время начинает работать в обратном направлении. Положительно заряженные ионы натрия проникают внутрь аксона, а ионы калия откачиваются наружу. На мгновение внутренняя среда аксона приобретает положительный заряд. При этом каналы натрий-калиевого насоса деформируются, блокируя дальнейший приток натрия, а ионы калия продолжают выходить наружу, и исходная разность потенциалов восстанавливается. Тем временем ионы натрия распространяются внутри аксона, изменяя мембрану в нижней части аксона. При этом состояние расположенных ниже насосов меняется, способствуя дальнейшему распространению импульса. Резкое изменение напряжения, вызванное стремительными перемещения ионов натрия и калия, называют потенциалом действия. При прохождении потенциала действия через определенную точку аксона, насосы включаются и восстанавливают состояние покоя.
Когда импульс достигает конца основной части тела аксона, его необходимо передать либо следующему нижележащему нейрону, либо, если речь идет о нейронах головного мозга, по многочисленным ответвлениям многим другим нейронам. Для такой передачи используется абсолютно иной процесс, нежели для передачи импульса вдоль аксона. Каждый нейрон отделен от своего соседа небольшой щелью, называемой синапсом. Потенциал действия не может перескочить через эту щель, поэтому нужно найти какой-то другой способ для передачи импульса следующему нейрону. В конце каждого отростка имеются крошечные мешочки, называющие (пресинаптическими) пузырьками, в каждом из которых находятся особые соединения — нейромедиаторы. При поступлении потенциала действия из этих пузырьков высвобождаются молекулы нейромедиаторов, пересекающие синапс и присоединяющиеся к специфичным молекулярным рецепторам на мембране нижележащих нейронов. При присоединении нейромедиатора равновесие на мембране нейрона нарушается. Сейчас мы рассмотрим, возникает ли при таком нарушении равновесия новый потенциал действия (нейрофизиологи продолжают искать ответ на этот важный вопрос до сих пор).
После того как нейромедиаторы передадут нервный импульс от одного нейрона на следующий, они могут просто диффундировать, или подвергнуться химическому расщеплению, или вернуться обратно в свои пузырьки (этот процесс нескладно называется обратным захватом). В конце XX века было сделано поразительное научное открытие — оказывается, лекарства, влияющие на выброс и обратный захват нейромедиаторов, могут коренным образом изменять психическое состояние человека. Прозак (Prozac*) и сходные с ним антидепрессанты блокируют обратный захват нейромедиатора серотонина. Складывается впечатление, что болезнь Паркинсона взаимосвязана с дефицитом нейромедиатора допамина в головном мозге. Исследователи, изучающие пограничные состояния в психиатрии, пытаются понять, как эти соединения влияют на человеческий рассудок.
- 3656
- 2,3
- 1
- 7
![]()
Олег Жуков
![]()
Анна Петренко![]()
Андрей Панов




Происхождение подхода
С середины ХХ века известно, что головной мозг потребляет значительную часть энергоресурсов всего организма: четверть всей глюкозы и ⅕ всего кислорода в случае высшего примата [1–5]. Это вдохновило Уильяма Леви и Роберта Бакстера из Массачусетского технологического института (США) на проведение теоретического анализа энергетической эффективности кодирования информации в биологических нейронных сетях (рис. 1) [6]. В основе исследования лежит следующая гипотеза. Поскольку энергопотребление мозга велико, ему выгодно иметь такие нейроны, которые работают наиболее эффективно — передают только полезную информацию и затрачивают при этом минимум энергии.
Это предположение оказалось справедливым: на простой модели нейронной сети авторы воспроизвели экспериментально измеренные значения некоторых параметров [6]. В частности, рассчитанная ими оптимальная частота генерации импульсов варьирует от 6 до 43 имп./с — почти так же, как и у нейронов основания гиппокампа. Их можно подразделить на две группы по частоте импульсации: медленные (
10 имп./с) и быстрые (
40 имп./с). При этом первая группа значительно превосходит по численности вторую [7]. Аналогичная картина наблюдается и в коре больших полушарий: медленных пирамидальных нейронов (
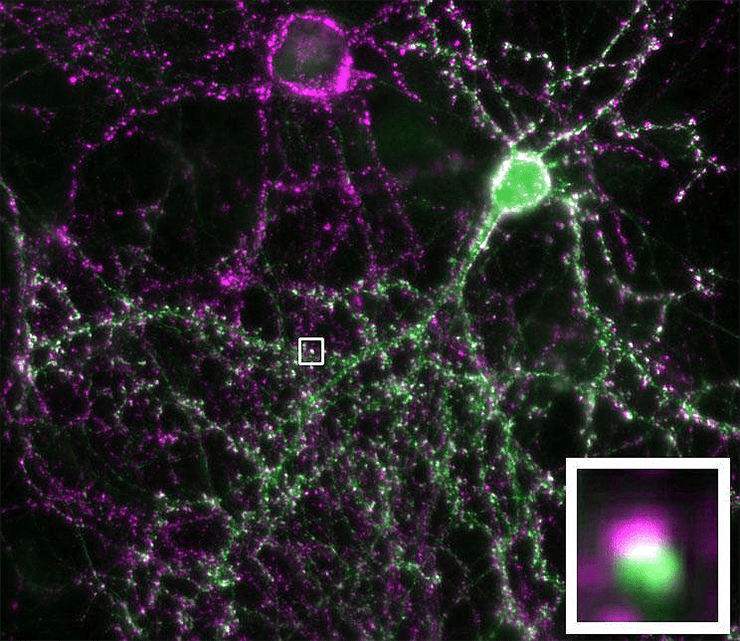
Нейроны центральной нервной системы разделяются на активирующие (образуют активирующие синапсы) и тормозящие (образуют тормозящие синапсы). Последние в значительной степени представлены интернейронами, или промежуточными нейронами. В коре больших полушарий и гиппокампе они ответственны за формирование гамма-ритмов мозга [15], которые обеспечивают слаженную, синхронную работу других нейронов. Это крайне важно для моторных функций, восприятия сенсорной информации, формирования памяти [9], [11].
За последнее время этот подход нашел множество подтверждений [10], [22], [24–26]. Он позволил по-новому взглянуть на устройство мозга на самых разных уровнях организации — от молекулярно-биофизического [20], [26] до органного [23]. Он помогает понять, каковы компромиссы между выполняемой функцией нейрона и ее энергетической ценой и в какой степени они выражены.
Положим, у нас есть модель нейрона, описывающая его электрофизиологические свойства: потенциал действия (ПД) и постсинаптические потенциалы (ПСП) (об этих терминах — ниже). Мы хотим понять, эффективно ли он работает, не тратит ли неоправданно много энергии. Для этого нужно вычислить значения параметров модели (например, плотность каналов в мембране, скорость их открывания и закрывания), при которых: (а) достигается максимум отношения полезной информации к энергозатратам и в то же время (б) сохраняются реалистичные характеристики передаваемых сигналов [6], [19].
Потенциал действия
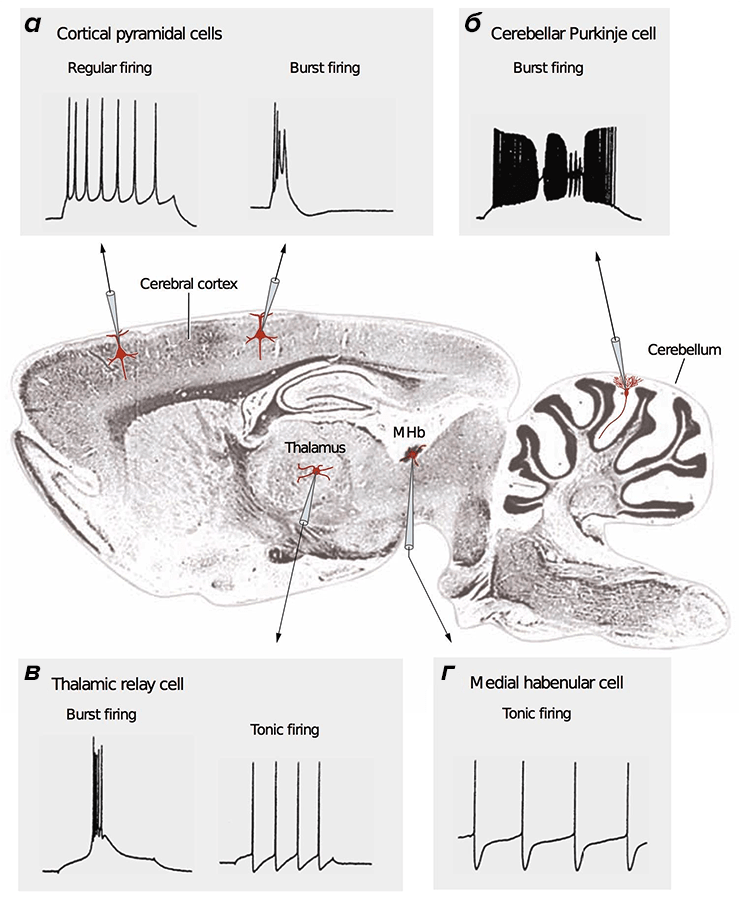
Рисунок 2. Разные типы нейронов генерируют различные сигналы. В центре — продольный срез мозга млекопитающего. Во вставках представлены разные типы сигналов, зарегистрированные методами электрофизиологии [15], [38]. а — Кортикальные (Cerebral cortex) пирамидальные нейроны могут передавать как низкочастотные сигналы (Regular firing), так и короткие взрывные, или пачечные, сигналы (Burst firing). б — Для клеток Пуркинье мозжечка (Cerebellum) характерна только пачечная активность на очень высокой частоте. в — Релейные нейроны таламуса (Thalamus) имеют два режима активности: пачечный и тонический (Tonic firing). г — Нейроны средней части поводка (MHb, Medial habenula) эпиталамуса генерируют тонические сигналы низкой частоты.
Большое разнообразие сигналов обусловлено огромным количеством комбинаций разных типов ионных каналов, синаптических контактов, а также морфологией нейронов [28], [29]. Поскольку в основе сигнальных процессов нейрона лежат ионные токи, стоит ожидать, что разные ПД требуют различных энергозатрат [20], [27], [30].
- Мембрана и ионы. Плазматическая мембрана нейрона поддерживает неравномерное распределение веществ между клеткой и внеклеточной средой (рис. 3б) [31–33]. В числе этих веществ есть и маленькие ионы, из которых для описания ПД важны К + и Nа + .
Ионов Na + внутри клетки мало, снаружи — много. Из-за этого они постоянно стремятся попасть в клетку. Напротив, ионов К + много внутри клетки, и они норовят из нее выйти. Самостоятельно ионы этого сделать не могут, потому что мембрана для них непроницаема. Для прохождения ионов через мембрану необходимо открывание специальных белков — ионных каналов мембраны.
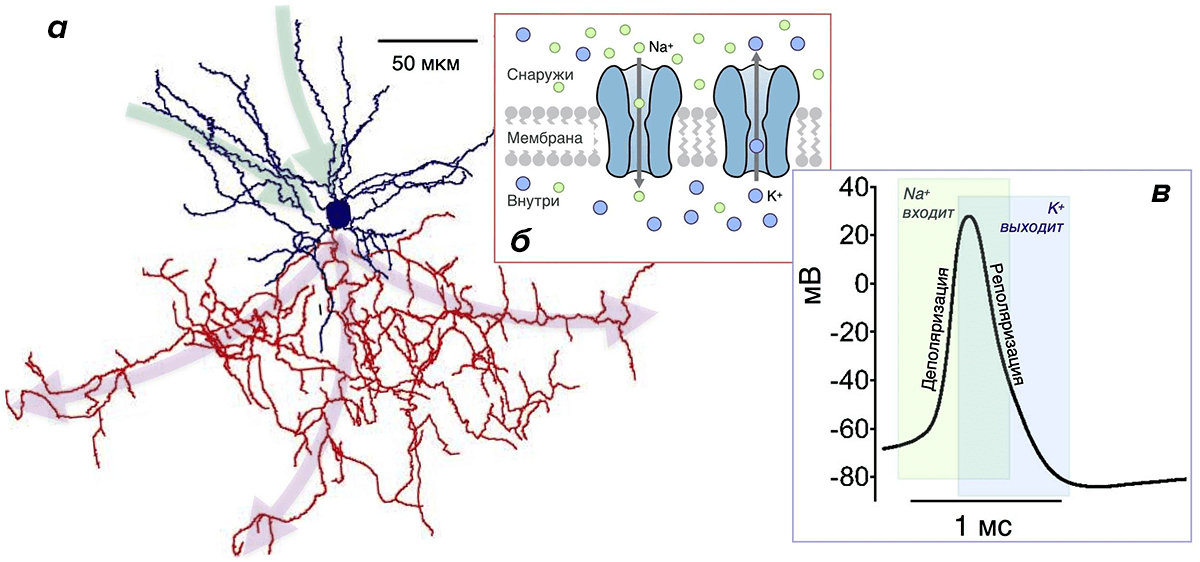
Рисунок 3. Нейрон, ионные каналы и потенциал действия. а — Реконструкция клетки-канделябра коры головного мозга крысы. Синим окрашены дендриты и тело нейрона (синее пятно в центре), красным — аксон (у многих типов нейронов аксон разветвлен намного больше, чем дендриты [8], [11], [35]). Зеленые и малиновые стрелки указывают направление потока информации: дендриты и тело нейрона принимают ее, аксон — отправляет ее к другим нейронам. б — Мембрана нейрона, как и любой другой клетки, содержит ионные каналы. Зеленые кружки — ионы Na + , синие — ионы К + . в — Изменение мембранного потенциала при генерации потенциала действия (ПД) нейроном Пуркинье. Зеленая область: Na-каналы открыты, в нейрон входят ионы Na + , происходит деполяризация. Синяя область: открыты К-каналы, К + выходит, происходит реполяризация. Перекрывание зеленой и синей областей соответствует периоду, когда происходит одновременный вход Na + и выход К + .
ПД — это относительно сильное по амплитуде скачкообразное изменение мембранного потенциала.
Анализ разных типов нейронов (рис. 4) показал, что нейроны беспозвоночных не очень энергоэффективны, а некоторые нейроны позвоночных почти совершенны [20]. По результатам этого исследования, наиболее энергоэффективными оказались интернейроны гиппокампа, участвующего в формировании памяти и эмоций, а также таламокортикальные релейные нейроны, несущие основной поток сенсорной информации от таламуса к коре больших полушарий.
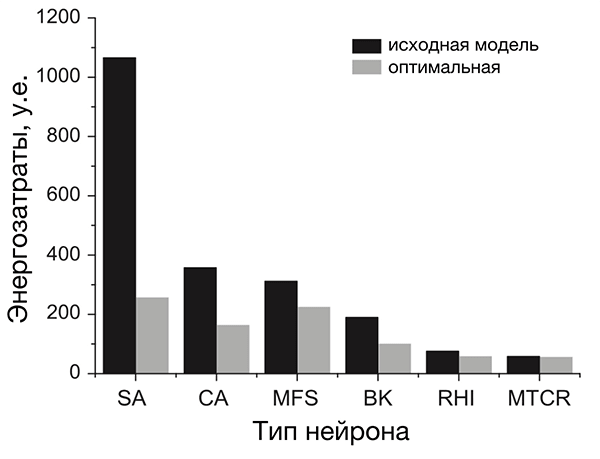
Рисунок 4. Разные нейроны эффективны по-разному. На рисунке представлено сравнение энергозатрат разных типов нейронов. Энергозатраты рассчитаны в моделях как с исходными (реальными) значениями параметров (черные столбцы), так и с оптимальными, при которых с одной стороны нейрон выполняет положенную ему функцию, с другой — затрачивает при этом минимум энергии (серые столбцы). Самыми эффективными из представленных оказались два типа нейронов позвоночных: интернейроны гиппокампа (rat hippocampal interneuron, RHI) и таламокортикальные нейроны (mouse thalamocortical relay cell, MTCR), так как для них энергозатраты в исходной модели наиболее близки к энергозатратам оптимизированной. Напротив, нейроны беспозвоночных менее эффективны. Условные обозначения: SA (squid axon) — гигантский аксон кальмара; CA (crab axon) — аксон краба; MFS (mouse fast spiking cortical interneuron) — быстрый кортикальный интернейрон мыши; BK (honeybee mushroom body Kenyon cell) — грибовидная клетка Кеньона пчелы.
Кстати, интернейроны гораздо более активны, чем большинство других нейронов мозга. В то же время они крайне важны для слаженной, синхронной работы нейронов, с которыми образуют небольшие локальные сети [9], [16]. Вероятно, высокая энергетическая эффективность ПД интернейронов является некой адаптацией к их высокой активности и роли в координации работы других нейронов [20].
Синапс
Передача сигнала от одного нейрона к другому происходит в специальном контакте между нейронами, в синапсе [12]. Мы рассмотрим только химические синапсы (есть еще электрические), поскольку они весьма распространены в нервной системе и важны для регуляции клеточного метаболизма, доставки питательных веществ [5].
Такие синапсы называются возбуждающими: они способствуют активации нейрона и генерации ПД. Существуют также и тормозящие синапсы. Они, наоборот, способствуют торможению и препятствуют генерации ПД. Часто на одном нейроне есть и те, и другие синапсы. Определенное соотношение между торможением и возбуждением важно для нормальной работы мозга, формирования мозговых ритмов, сопровождающих высшие когнитивные функции [49].
Что еще?
Энергетическая эффективность клеток мозга исследуется также и в отношении их морфологии [35], [52–54]. Исследования показывают, что ветвление дендритов и аксона не хаотично и тоже экономит энергию [52], [54]. Например, аксон ветвится так, чтобы суммарная длина пути, который проходит ПД, была наименьшей. В таком случае энергозатраты на проведение ПД вдоль аксона минимальны.
Снижение энергозатрат нейрона достигается также при определенном соотношении тормозящих и возбуждающих синапсов [55]. Это имеет прямое отношение, например, к ишемии (патологическому состоянию, вызванному нарушением кровотока в сосудах) головного мозга. При этой патологии, вероятнее всего, первыми выходят из строя наиболее метаболически активные нейроны [9], [16]. В коре они представлены ингибиторными интернейронами, образующими тормозящие синапсы на множестве других пирамидальных нейронов [9], [16], [49]. В результате гибели интернейронов, снижается торможение пирамидальных. Как следствие, возрастает общий уровень активности последних (чаще срабатывают активирующие синапсы, чаще генерируются ПД). За этим немедленно следует рост их энергопотребления, что в условиях ишемии может привести к гибели нейронов.
Еще раз обо всем
В конце ХХ века зародился подход к изучению мозга, в котором одновременно рассматривают две важные характеристики: сколько нейрон (или нейронная сеть, или синапс) кодирует и передает полезной информации и сколько энергии при этом тратит [6], [18], [19]. Их соотношение является своего рода критерием энергетической эффективности нейронов, нейронных сетей и синапсов.
Использование этого критерия в вычислительной нейробиологии дало существенный прирост к знаниям относительно роли некоторых явлений, процессов [6], [18–20], [26], [30], [43], [55]. В частности, малая вероятность выброса нейромедиатора в синапсе [18], [19], определенный баланс между торможением и возбуждением нейрона [55], выделение только определенного рода приходящей информации благодаря определенной комбинации рецепторов [50] — все это способствует экономии ценных энергетических ресурсов.
Более того, само по себе определение энергозатрат сигнальных процессов (например, генерация, проведение ПД, синаптическая передача) позволяет выяснить, какой из них пострадает в первую очередь при патологическом нарушении доставки питательных веществ [10], [25], [56]. Так как больше всего энергии требуется для работы синапсов, именно они первыми выйдут из строя при таких патологиях, как ишемия, болезни Альцгеймера и Хантингтона [19], [25]. Схожим образом определение энергозатрат разных типов нейронов помогает выяснить, какой из них погибнет раньше других в случае патологии. Например, при той же ишемии, в первую очередь выйдут из строя интернейроны коры [9], [16]. Эти же нейроны из-за интенсивного метаболизма — наиболее уязвимые клетки и при старении, болезни Альцгеймера и шизофрении [16].
В общем, подход к определению энергетически эффективных механизмов работы мозга является мощным направлением для развития и фундаментальной нейронауки, и ее медицинских аспектов [5], [14], [16], [20], [26], [55], [64].
Благодарности
Физиолог Вячеслав Дубынин о свойствах нейронов, потенциалах действия и цитоплазме нервных клеток
Можно сравнить потенциалы действия с двоичным кодом компьютера. В компьютере, как известно, вся информация кодируется последовательностью нулей и единиц. Потенциалы действия — это, по сути, единички, которые кодируют все наши мысли, чувства, сенсорные переживания, движения и так далее. Подключившись к правильному месту нейросети и подавая на нервные клетки подобного рода электрические импульсы, мы можем заставить человека почувствовать, например, положительные или отрицательные эмоции, или вызвать какие-то сенсорные иллюзии, или управлять работой внутренних органов. Это, конечно, очень перспективный раздел современной нейрофизиологии и нейромедицины.
Для того чтобы управлять потенциалами действия, нужно понимать, откуда они берутся. В принципе, потенциалы действия можно сравнить с ситуацией, когда вы с помощью электрического фонарика подаете сигналы своему товарищу на другом берегу реки. То есть вы нажимаете на кнопку, фонарик вспыхивает, и дальше каким-то секретным кодом вы что-то передаете. Для того чтобы ваш фонарик работал, внутри нужна батарейка, то есть некий заряд энергии. Нервные клетки, для того чтобы генерировать потенциал действия, должны тоже обладать таким зарядом энергии, и этот заряд называется потенциал покоя. Он существует, он присущ всем нервным клеткам и составляет примерно -70 мВ, то есть -0,07 В.
Изучение электрических свойств нейронов началось достаточно давно. То, что в живых организмах присутствует электричество, поняли еще в эпоху Возрождения, когда заметили, что лягушачья лапка подергивается от ударов током, когда поняли, что электрический скат излучает потоки энергии. Дальше был поиск тех технических приемов, которые позволили бы уже всерьез подойти к нервным клеткам и посмотреть, какие электрические процессы там происходят. Здесь мы должны поблагодарить кальмара, потому что кальмар — это такое замечательное животное, которое обладает очень толстыми аксонами. Это связано с особенностями его образа жизни: у него существует складка-мантия, которая сокращается и выбрасывает воду, возникает реактивный импульс, и кальмар движется вперед. Для того чтобы много мышц мантии сокращались энергично и одновременно, нужен мощный аксон, который сразу бы на всю эту мышечную массу передавал импульсы. Аксон имеет толщину 1–1,5 мм. Еще в середине XX века научились его выделять, вставлять внутрь тонкие электрические проволочки, измерять и регистрировать те электрические процессы, которые происходят. Тогда стало уже понятно, что существует потенциал покоя и потенциал действия.
Принципиальный рывок произошел в тот момент, когда изобрели стеклянные микроэлектроды, то есть научились делать очень тонкие стеклянные трубочки, которые внутри заполнены раствором соли, скажем KCl. Если такую трубочку очень аккуратно (это надо, конечно, делать под микроскопом) подвести к нервной клетке и проколоть мембрану нейрона, то нейрон, немного повозмущавшись, продолжает нормально работать, и вы видите, какой у него внутри заряд и как этот заряд меняется, когда происходит передача информации. Стеклянные микроэлектроды — это базовая технология, которая используется и сейчас.
Ближе к концу XX века появился еще один способ, он называется patch-clamp, когда стеклянный микроэлектрод не протыкает мембрану, а очень аккуратно к ней подводится, кусочек мембраны присасывается, при этом очень небольшая площадь мембраны клетки подвергается анализу, и можно смотреть, как работают, например, отдельные белковые молекулы, такие как различные ионные каналы.
Использование всех этих технологий позволило для начала понять, откуда берется потенциал покоя, откуда берется заряд внутри нервных клеток. Оказалось, что потенциал покоя связан прежде всего с накоплением ионов калия. Электрические процессы в живых организмах отличаются от тех электрических процессов, которые происходят в компьютере, потому что физическое электричество — это в основном движение электронов, а в живых системах — движение ионов, то есть заряженных частиц, прежде всего ионов натрия, калия, хлора, кальция. Эта четверка в основном обеспечивает разные электрические явления в нашем организме: и в нервной системе, и в мышцах, и в сердце — это очень важный раздел современной физиологии.
Когда стали анализировать состав цитоплазмы нервных клеток, то оказалось, что в цитоплазме нейронов по сравнению с внешней средой много калия и мало натрия. Эта разница возникает за счет работы особой белковой молекулы — натрий-калиевого насоса (или натрий-калиевой АТФазы). Надо сказать, что натрий-калиевый насос находится на мембранах всех клеток, потому что живые клетки так устроены, что им необходим избыток калия внутри цитоплазмы, например, для того, чтобы нормально работали многие белки. Клетки обменивают внутриклеточный натрий на внеклеточный калий, закачивают калий, удаляют из цитоплазмы натрий, но при этом пока заряд не меняется, потому что обмен более-менее эквивалентен. У обычной клетки, не нервной, внутри избыток калия, но никакого заряда нет: сколько положительно заряженных частичек, столько и отрицательно заряженных; есть, например, калий, хлор или анионы различных органических кислот.
Когда стали изучать, откуда берется потенциал действия, то заметили, что для пробуждения клетки, чтобы она сгенерировала импульс, нужно стимулировать ее довольно определенной силой. Стимул, как правило, должен поднять заряд внутри нервной клетки до уровня примерно -50 мВ, то есть потенциал покоя — -70 мВ, а так называемый порог запуска потенциала действия — где-то -50 мВ. Если поднять заряд до такого уровня, нейрон как будто просыпается: вдруг в нем возникает очень большой положительный заряд, который доходит до уровня примерно +30 мВ, а потом быстро опускается примерно до уровня потенциала покоя, то есть от 0 до 1, а потом опять к 0. Вот она, ступенька тока, которая дальше способна передавать информацию.
Откуда она берется? Почему нейрон вдруг проснулся и выдал этот импульс? Оказалось, что здесь работают другие ионные каналы — не постоянно открытые, а ионные каналы со створками. В тот момент, когда заряд в нервной клетке достигает уровня -50 мВ, эти створки начинают открываться, начинается движение ионов. Сначала открывается натриевый канал, примерно на полмиллисекунды, в нейрон успевает войти порция ионов натрия. Натрий входит потому, что, во-первых, его в цитоплазме мало — примерно в 10 раз меньше, чем снаружи, и, во-вторых, он положительно заряженный, а цитоплазма заряжена отрицательно, то есть плюс притягивается к минусу. Поэтому вход идет очень быстро, тотально, и мы наблюдаем восходящую фазу потенциала действия. Потом натриевые каналы (одновременно работают тысячи каналов) закрываются, и открываются калиевые каналы, электрочувствительные и тоже со створками. Это не те, которые постоянно открыты, а это каналы, у которых есть специальная белковая петля (канал — это цилиндр, внутри которого есть проход), которая открывается, как турникет, и ионы калия получают возможность выходить из цитоплазмы и выносят большое количество положительного заряда, и в целом заряд в нейроне опускается до уровня потенциала покоя. Калий в этот момент мощно выходит наружу, потому что мы находимся на вершине потенциала действия, уже нет -70 мВ, калия внутри много, а снаружи мало, он выходит, выносит положительный заряд, и система перезарядилась.
Мембрана нервной клетки организована таким образом, что если в одной точке возник такой импульс — а он в основном возникает в зоне синапсов, там, где медиатор возбудил нервную клетку, — то этот импульс способен распространяться по мембране нервной клетки, и это есть передача. Распространение импульса по мембране нейрона — отдельный процесс. К сожалению, он происходит довольно медленно — максимум 100 м/с, и на этом уровне мы, конечно, уступаем компьютерам, потому что электрический сигнал по проводам распространяется со скоростью света, а у нас максимум 100–120 м/с, это немного. Поэтому мы довольно медленные организмы по сравнению с компьютерными системами.
Для того чтобы изучать работу ионных каналов, физиологами используются специальные токсины, которые блокируют эти каналы. Самый известный из этих токсинов — тетродотоксин, яд рыбы фугу. Тетродотоксин выключает электрочувствительный натриевый канал, натрий не входит, потенциал действия не развивается, и сигналы по нейронам вообще не распространяются. Поэтому отравление рыбой фугу вызывает постепенно развивающийся паралич, потому что нервная система перестает передавать информацию. Подобным действием, только более мягким, обладают местные анестетики вроде новокаина, которые используются в медицине для того, чтобы очень локально прекратить передачу импульсов и не запускать болевые сигналы. Для того чтобы изучать нейроны, используются животные модели, записать нервные клетки человека можно только по очень особым поводам. Во время нейрохирургических операций бывают такие ситуации, когда это не только допустимо, но и необходимо. Например, для того чтобы точно выйти на ту зону, которую нужно разрушить, скажем, при какой-нибудь хронической боли.
Есть способы, чтобы записывать электрическую активность мозга человека более тотально. Это делается во время регистрации электроэнцефалограммы, там одновременно записываются суммарные потенциалы действий миллионов клеток. Есть еще одна технология, она называется технология вызванных потенциалов. Эти технологии дополняют то, что нам дают томографические исследования, и позволяют достаточно полно представить ту картину электрических процессов, которая имеет место в мозге человека.
Читайте также:





