Гипергликемия при поражении цнс
Пути регуляции обмена углеводов крайне разнообразны. На любых уровнях организации живого углеводный обмен регулируется факторами, влияющими на активность ферментов, участвующих в реакциях углеводного обмена. К этим факторам относятся: концентрация субстратов, содержание продуктов (метаболитов) отдельных реакций, кислородный режим, температура, проницаемость биологических мембран, концентрация коферментов, необходимых для отдельных реакций, и т. д. По ходу изложения материала в данной главе мы старались показать влияние перечисленых выше факторов на активность ферментных систем углеводного обмена.
У человека и животных на всех стадиях синтеза и распада углеводов регуляция углеводного обмена осуществляется с участием ЦНС и гормонов.
Например, установлено, что падение концентрации глюкозы в крови ниже 3,3-3,4 ммоль/л (60-70 мг/100 мл) приводит к рефлекторному возбуждению высших метаболических центров, расположенных в гипоталамусе. Возбуждение, возникающее в ЦНС, быстро распространяется по нервным путям в спинном мозгу, переходит в симпатический ствол и по симпатическому нерву достигает печени. В результате часть гликогена печени распадается с образованием глюкозы. Концентрация глюкозы в крови при этом повышается. В регуляции углеводного обмена ЦНС особая роль принадлежит ее высшему отделу - коре головного мозга. Наряду с ЦНС важное влияние на содержание глюкозы в крови оказывают гормональные факторы, т. е. регуляция уровня сахара в крови осуществляется ЦНС не только путем прямого воздействия на печень, но через ряд эндокринных желез.
При ряде состояний можно наблюдать повышение содержания сахара в крови - гипергликемию, а также понижение концентрации сахара - гипогликемию.
Гипергликемия
Гипергликемия является довольно частым симптомом при различных заболеваниях, прежде всего связанных с поражением эндокринной системы.
Сахарный диабет. В регуляции гликолиза и глюконеогенеза большую роль играет инсулин. При недостаточности инсулина возникает заболевание, которое носит название сахарного диабета. Повышается концентрация глюкозы в крови (гипергликемия), появляется глюкоза в моче (глюкозурия) и уменьшается содержание гликогена в печени. При этом мышечная ткань утрачивает способность утилизировать глюкозу крови. В печени при общем снижении интенсивности биосинтетических процессов (биосинтеза белков, синтеза жирных кислот из продуктов распада глюкозы) наблюдается усиленный синтез ферментов глюконеогеназа. При введении инсулина больным диабетом происходит коррекция метаболических сдвигов: нормализуется проницаемость мембран мышечных клеток для глюкозы, восстанавливается соотношение между гликолизом и глюконеогенезом. Инсулин контролирует эти процессы на генетическом уровне как индуктор синтеза ключевых ферментов гликолиза: гексокиназы, фосфофруктокиназы и пируваткиназы. Инсулин также индуцирует синтез гликогенсинтазы. Одновременно инсулин действует как репрессор синтеза ключевых ферментов глюконеогенеза. Заметим, что индукторами синтеза ферментов глюконеогенеза служат глюкокортикоиды. В связи с этим при инсулярной недостаточности и при сохранении или даже повышении инкреции кортикостероидов (в частности, при диабете) устранение влияния инсулина приводит к резкому повышению синтеза и концентрации ферментов глюконеогенеза, особенно фосфоенол-пируваткарбоксикиназы, определяющей возможность и скорость глюконеогенеза в печени и почках.
Развитие гипергликемии при диабете можно рассматривать также как результат возбуждения метаболических центров в ЦНС импульсами с хеморецепторов клеток, испытывающих энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда тканей.
Гипергликемия может возникнуть не только при заболевании поджелудочной железы, но и в результате расстройств функции других эндокринных желез, участвующих в регуляции углеводного обмена. Так, например, гипергликемия может наблюдаться при гипофизарных заболеваниях, при опухолях коры надпочечников, гиперфункции щитовидной железы. Гипергликемий иногда появляется во время беременности. Наконец, гипергликемия может встречаться также при органических поражениях ЦНС, при расстройствах мозгового кровообращения или сопровождать заболевания печени воспалительного или дегенеративного характера. Поддержание постоянства уровня сахара крови, как уже отмечалось, является важнейшей функцией печени, резервные возможности ее в этом направлении весьма велики, поэтому гипергликемия, связанная с нарушением функции печени, выявляется обычно лишь при тяжелых поражениях печени.
Большой клинический интерес представляет изучение реактивности организма на сахарную нагрузку у здорового и больного человека. В связи с этим в клинике довольно часто применяют многократное исследование уровня сахара обычно после приема per os 50 или 100 г глюкозы, растворенной в теплой воде,- так называемые сахарные кривые. При оценке сахарных кривых обращают внимание на время максимального подъема, высоту этого подъема и время возврата концентрации сахара к исходному уровню. Для оценки сахарных кривых введено несколько показателей, из которых наиболее важное значение имеет коэффициент Бодуэна: ((B-A) / A) x 100%, где А - уровень сахара в крови натощак; В - максимальное содержание сахара в крови после нагрузки глюкозой. В норме этот коэффициент составляет около 50%. Цифры, превышающие 80%, говорят о серьезном нарушении углеводного обмена.
Гипогликемия
Гипогликемия нередко связана с понижением функций тех эндокринных желез, повышение функции которых приводит, как это было отмечено выше, к гипергликемии. В частности, гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой болезни, гипотиреозе. Резкое снижение сахара в крови отмечается при аденомах островковой ткани поджелудочной железы вследствие повышенной продукции инсулина β-клетками островков Лангерганса. Кроме того, гипогликемия может быть вызвана голоданием, продолжительной физической работой, приемом β-ганглиоблокаторов. Низкий уровень сахара в крови иногда отмечается при беременности, лактации.
Гипогликемия может возникнуть также при введении больным сахарным диабетом больших доз инсулина. Гипогликемия, как правило, сопровождает почечную глюкозурию, возникающую вследствие снижения почечного порога для сахара.
Глюкозурия
Чаще всего присутствие глюкозы в моче (глюкозурия) является результатом расстройства углеводного обмена на почве патологических изменений в поджелудочной железе (сахарный диабет, острый панкреатит и т. д.). Реже встречается глюкозурия почечного происхождения, связанная с недостаточностью резорбции глюкозы в почечных канальцах. Как временное явление глюкозурия может возникнуть при некоторых острых инфекционных и нервных заболеваниях, после приступов эпилепсии, сотрясения мозга.
Отравления морфином, стрихнином, хлороформом, фосфором и др. также обычно сопровождаются глюкозурией. Наконец, необходимо помнить о глюкозурии алиментарного происхождения, глюкозурии беременных и глюкозурии на почве нервных стрессовых состояний (эмоциональная глюкозурия).
Изменение углеводного обмена
при гипоксических состояниях
Отставание окисления пирувата от интенсивности гликолиза наблюдается чаще всего при гипоксических состояниях, обусловленных различными нарушениями кровообращения или дыхания, высотной болезнью, анемией, понижением активности системы тканевых окислительных ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозах, а также развивается в результате относительной гипоксии при чрезмерной мышечной работе.
При усилении гликолиза происходит накопление пирувата и лактата в крови, что сопровождается обычно изменением кислотно-основного состояния, уменьшением щелочных резервов.
Увеличение содержания лактата и пирувата в крови может наблюдаться также при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т. п.) в результате торможения процессов глюконеогенеза в печени.
| Таблица 28. Типы гликогенозов и их характеристика | |||
| Тип гликогеном и название болезни | Фермент с нарушенной активностью | Структура гликогена | Основные органы ткани и клетки, депонирующие гликоген |
| I тип Болезнь Гирке | Глюкозо-6-фосфатаза | Нормальная | Печень, почки |
| II тип Болезнь Помпе | Кислая α-1,4-глюкозидаза | " | Печень, селезенка, почки, мышцы, нервная ткань, эритрициты |
| III тип Болезнь Форбса | Амило-(1-->6)-глюкозидаза | Короткие многочисленные внешние ветви (лимитдекстрин) | Печень, мышцы, лейкоциты, эритроциты |
| IV тип Болезнь Андерсена | Гликоген-ветвящий фермент | Длинные внешние и внутренние ветви с малым числом точек ветвления (амилопектин) | Печень, мышцы, лейкоциты |
| V тип Болезнь Мак-Ардла | Фосфорилаза мышц | Нормальная | Скелетная мускулатура |
| VI тип Болезнь Херса | Фосфорилаза печени | " | Печень, лейкоциты |
| VII тип Болезнь Томсона | Фосфоглюкомутаза | " | Печень и (или) мышцы |
| VIII тип Болезнь Тарун | Фосфофруктокиназа | " | Мышцы, эритроциты |
| IX тип Болезнь Хага | Киназа фосфорилазы "в" | " | Печень |
Гликогенозы
Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с дефицитом ферментов, катализирующих процессы распада или синтеза гликогена, и характеризуются избыточным его накоплением в различных органах и тканях. В табл. 28 приведены типы гликогенозов и их характеристика.
Болезнь Гирке - чаще встречающийся гликогеноз. Патологические симптомы появляются уже на 1-м году жизни ребенка: увеличена печень, нередко у величены в размерах почки. В результате гипогликемии появляются судороги, задержка роста, возможен ацидоз. В крови обнаруживается повышенное количество лактата и пируватз. Введение адреналина или глюкагона вызывает значительную гиперлактацидемию, но не гипергликемию, так как глюкозо-6-фосфатаза в печени отсутствует и не происходит образования свободной глюкозы.
При некоторых состояниях можно наблюдать повышение содержания глюкозы в крови – гипергликемию, а также понижение концентрации глюкозы – гипогликемию. Гипергликемия является довольно частым симптомом различных заболеваний, прежде всего связанных с поражением эндокринной системы.
Развитие гипергликемии при диабете можно рассматривать также как результат возбуждения метаболических центров в ЦНС импульсами с хе-морецепторов клеток, испытывающих энергетический голод в связи с недостаточным поступлением глюкозы в клетки ряда тканей. Роль системы фруктозо-2,6-бисфосфата в регуляции метаболизма углеводов, а также нарушения ее функционирования при сахарном диабете см. главу 16.
Гипергликемия может возникнуть не только при заболевании поджелудочной железы, но и в результате расстройства функции других эндокринных желез, участвующих в регуляции углеводного обмена. Так, гипергликемия может наблюдаться при гипофизарных заболеваниях, опухолях коркового вещества надпочечников, гиперфункции щитовидной железы. Иногда гипергликемия появляется во время беременности. Наконец, гипергликемия возможна при органических поражениях ЦНС, расстройствах мозгового кровообращения, болезнях печени воспалительного или дегенеративного характера. Поддержание постоянства уровня глюкозы в крови, как отмечалось,– важнейшая функция печени, резервные возможности которой в этом отношении весьма велики. Поэтому гипергликемия, обусловленная нарушением функции печени, выявляется обычно при тяжелых ее поражениях.
Большой клинический интерес представляет изучение реактивности организма на сахарную нагрузку у здорового и больного человека. В связи с этим в клинике довольно часто исследуют изменения во времени уровня глюкозы в крови, обычно после приема per os 50 г или 100 г глюкозы, растворенной в теплой воде,– так называемая сахарная нагрузка. При оценке построенных гликемических кривых обращают внимание на время максимального подъема, высоту этого подъема и время возврата концентрации глюкозы к исходному уровню. Для оценки гликемических кривых введено несколько показателей, из которых наиболее важное значение имеет коэффициент Бодуэна:
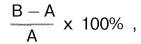
где А – уровень глюкозы в крови натощак; В – максимальное содержание глюкозы в крови после нагрузки глюкозой. В норме этот коэффициент составляет около 50%. Значения, превышающие 80%, свидетельствуют о серьезном нарушении обмена углеводов.
Гипогликемия. Нередко гипогликемия связана с понижением функций тех эндокринных желез, повышение функций которых приводит, как отмечалось, к гипергликемии. В частности, гипогликемию можно наблюдать при гипофизарной кахексии, аддисоновой болезни, гипотиреозе. Резкое снижение уровня глюкозы в крови отмечается при аденомах поджелудочной железы вследствие повышенной продукции инсулина β-клетками панкреатических островков. Кроме того, гипогликемия может быть вызвана голоданием, продолжительной физической работой, приемом β-ганглиоблока-торов. Низкий уровень глюкозы в крови иногда отмечается при беременности, лактации.
Глюкозурия. Обычно присутствие глюкозы в моче (глюкозурия) является результатом нарушения углеводного обмена вследствие патологических изменений в поджелудочной железе (сахарный диабет, острый панкреатит и т.д.). Реже встречается глюкозурия почечного происхождения, связанная с недостаточностью резорбции глюкозы в почечных канальцах. Как временное явление глюкозурия может возникнуть при некоторых острых инфекционных и нервных заболеваниях, после приступов эпилепсии, сотрясения мозга.
Отравления морфином, стрихнином, хлороформом, фосфором также обычно сопровождаются глюкозурией. Наконец, необходимо помнить о глюкозурии алиментарного происхождения, глюкозурии беременных и глюкозурии при нервных стрессовых состояниях (эмоциональная глюкозурия).

Изменение углеводного обмена при гипоксических состояниях. Отставание скорости окисления пирувата от интенсивности гликолиза наблюдается чаще всего при гипоксических состояниях, обусловленных различными нарушениями кровообращения или дыхания, высотной болезнью, анемией, понижением активности системы тканевых окислительных ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозах, а также в результате относительной гипоксии при чрезмерной мышечной работе.
При усилении гликолиза происходит накопление пирувата и лактата в крови, что сопровождается обычно изменением кислотно-основного равновесия, уменьшением щелочных резервов крови. Увеличение содержания лактата и пирувата в крови может наблюдаться также при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т.п.) в результате торможения процессов глюконеогенеза в печени.
Гликогенозы. Ряд наследственных болезней связан с нарушением обмена гликогена. Эти болезни получили название гликогенозов. Они возникают в связи с дефицитом или полным отсутствием ферментов, катализирующих процессы распада или синтеза гликогена, и характеризуются избыточным его накоплением в различных органах и тканях (табл. 10.2).
Гликогеноз I типа (болезнь Гирке) встречается наиболее часто, обусловлен наследственным дефектом синтеза фермента глюкозо-6-фосфатазы в печени и почках. Болезнь наследуется по аутосомно-рецессивному типу. Патологические симптомы появляются уже на первом году жизни ребенка: увеличена печень, нередко увеличены почки. В результате гипогликемии появляются судороги, задержка роста, возможен ацидоз. В крови – повышенное количество лактата и пирувата. Введение адреналина или глюка-гона вызывает значительную гиперлактатацидемию, но не гипергликемию, так как глюкозо-6-фосфатаза в печени отсутствует и образования свободной глюкозы не происходит.
Как снижение, так и повышение уровня глюкозы в крови имеют важное значение в возникновении нарушений ЦНС вплоть до комы. При изучении влияния уровня глюкозы на метаболизм головного мозга установлено, что при гипогликемии или гипергликемии мозговой кровоток остается неизменным или может повыситься.
Гипогликемия. Гипогликемия может быть вызвана имеющимся заболеванием или введением инсулина или другого гипогликемического препарата и т.д.
Нервная система (НС) осуществляет регуляцию всех жизненных процессов в организме и его взаимодействие с внешним миром и представляет собой высшую интегрирующую систему. НС функционирует на основе рефлексов -- ответных реакций организма, осуществляемых при посредстве ЦНС. Морфологическим субстратом рефлексов является рефлекторные дуги, состоящие из цепи афферентных, ассоциативных и эффекторных нейронов.
Число нейроцитов в человеческом мозге достигает порядка 1011 или по мнению других авторов на порядок больше. Общее число синапсов ориентировочно 1015-1018.
Эволюция нервной системы тесно связано с эволюцией мышечных тканей. Клетки многоклеточных животных постепенно специализируется для выполнения различных функций. Мышечные клетки появляются в эволюции раньше, чем нервные клетки. Эти первопредки мышечных клеток находятся на поверхности тела и способны реагировать на внешние воздействия сокращением. Хлопин называл их мионейроэпителиальными клетками.
В ходе дальнейшего развития многоклеточных организмов мышечные клетки уходят в более глубокие слои тела, поэтому появляется необходимость в чувствительных клетках, доступных к поверхностной стимуляции раздражителями и способные передавать возбуждение глубже лежащим мышечным клеткам. Так появились организмы, имеющие нейроны на поверхности тела, отростки которых находятся в прямом контакте с мышечными клетками.
Следующей ступенью развития нервной системы является появление нервных цепей, сначала из 2-х нейронов, а затем и с большим количеством нейронов. Например, такие 2-х нейронные цепи имеются в каждом сегменте дождевого червя. 1-й нейрон (афферентный, чувствительный) лежит на поверхности тела, аксон 1-го нейрона передает импульс глубже лежащему 2-му нейроны (эфферентный, моторный), а 2-й нейрон вызывает сокращение мышечных клеток сегмента.
На следующем этапе появляются межсегментные нейроны у сегментированных животных. Это позволяет координировать совгласованные действия сегментов.
Увеличение числа этих соединений привело к появлению пучка, тянущегося вдоль тела близко к центральной оси, в конечном виде -- спинного мозга и головного мозга.
В целом для эволюции нервной системы характерно консервативность: у высших сохраняется признаки сегментарности, присущие низшим; химическая передача импульсов в синапсах и у низших, и у высших. Чем выше уровень организации, тем выраженнее в эмбриональном периоде опережающее развитие и созревание нервной системы. Чем выше уровень организации вида, тем большее число бластомеров зародыша используется для закладки нервной системы. Так, у человека 1/3 площади поверхности оплодотворенной яйцеклетки является презумптивной зоной (будущей зоной) нервной трубки.
Развитие нервной системы начинается с утолщения дорсальной ЭКТОДЕРМЫ и формированием нервной пластинки, тянущейся вдоль оси тела. В дальнейшем нервная пластинка прогибается и образуется нервный желобок, который смыкаясь превращается в трубку. Вначале нервная трубка сохраняет связь с эктодермой, в последующем отрывается и располагается под ней самостоятельно. При этом из материала зоны прикрепления нервной трубки с эктодермой обособляются парные ганглиозные пластинки или нервные гребни, тянущиеся вдоль нервной трубки.
Материал ганглиозных пластинок дифференцируется в структуры:
- 1. Клетки ганглиозной пластинки в головном конце вместе с клетками плакод участвуют в формировании ядер V, VII, IX, X пар черепных нервов.
- 2. Часть клеток мигрирует латерально, обратно включаются в состав эктодермы и в дальнейшем дифференцируются в меланоциты эпидермиса кожи.
- 3. Часть клеток мигрирует вентрально между нервной трубкой и сомитами, дифференцируются в нервные ткани ганглиев вегетативной нервной системы и хромофинные клетки корковой части надпочечников.
- 4. Часть клеток остается на месте ганглиозной пластинки и в дальнейшем становятся закладкой спинальных ганглиев (спинномозговых узлов).
Нервная трубка в момент закладки состоит из 1 слоя клеток -- медулобластов, однако вскоре клетки начинают пролиферацию и нервная трубка становится многослойной. При этом базальный слой медулобластов располагается на границе с каналом нервной трубки, часть клеток в ходе деления вытесняется в вышележащие слои, т.е. в направлении к наружной поверхности трубки. Медулабластов базального слоя называют герменативными или вентрикулярными клетками. Вентрикулярные клетки дифференцируются в 2-х направлениях:
- 1. Спонгиобласты Глиобласты Макроглиоциты (эпиндимоциты, астроциты, олигодендроглиоциты.
- 2. Нейробласты Молодые нейроциты Зрелые нейроциты.
Микроглиоциты закладываются из внедряющихся в нервную трубку мезенхимных клеток.
I. Морфологическая классификация:
- 1. ЦНС (спинной мозг, головной мозг).
- 2. Периферическая НС (периферические нервные стволы, нервы, ганглии, нервные окончания, нервные узлы).
III. Физиологическая классификация:
- 4. Соматическая НС (иннервирует все тело, за исключением внутренних органов, сосудов, желез).
- 5. Вегетативная (автономная) НС (регулирует деятельность внутренних органов, сосудов, желез).
СПИННОМОЗГОВЫЕ УЗЛЫ (СПИНАЛЬНЫЕ ГАНГЛИИ) -- закладываются в эмбриональном периоде из ганглиозной пластинки (нейроциты и глиальные элементы) и мезенхимы (микроглиоциты, капсула и сдт прослойки). мозг травма гематома внутричерепной
Спинномозговые узлы (СМУ) расположены по ходу задних корешков спинного мозга. Снаружи покрыты сдт капсулой, от капсулы внутрь отходят прослойки-перегородки из рыхлой сдт с кровеносными сосудами. Под капсулой группами располагаются тела нейроцитов. Нейроциты СМУ крупные, диаметр тел до 120 мкм. Ядра нейроцитов крупные, с четкими ядрышками, располагаются в центре клетки; в ядрах преобладает эухроматин. Тела нейроцитов окружены клетками сателлитами или мантийными клетками -- разновидность олигодендроглиоцитов. Нейроциты СМУ по строению псевдоуниполярные -- аксон и дендрит отходят от тела клетки вместе как один отросток, далее Т-образно расходятся. Дендрит идет на периферию и образует в коже, в толще сухожилий и мышц, во внутренних органах чувствительные рецепторные окончания, воспринимающие болевые, температурные, тактильные раздражители, т.е. нейроциты СМУ по функции чувствительные. Аксоны по заднему корешку поступают в спинной мозг и передают импульсы на ассоциативные нейроциты спинного мозга. В центральной части СМУ располагаются параллельно друг другу нервные волокна, покрытые леммоцитами.
Обилие нейроцитов обуславливает серый цвет серого вещества СМ. По морфологии нейроциты СМ в своем подавляющем большинстве мультиполярные. Нейроциты в сером веществе окружены спутанными как войлок нервными волокнами -- нейропилью. Аксоны в нейропиле слабомиелинизированы, а дендриты и вовсе не миелинизированы. Сходные по размерам, тонкому строению и функциям нейроциты СМ располагаются группами и образуют ядра.
Среди нейроцитов СМ различают следующие типы:
- 1. Корешковые нейроциты -- располагаются в ядрах передних рогов, по функции являются двигательными; аксоны корешковых нейроцитов в составе передних корешков покидают СМ, проводят к скелетной мускулатуре двигательные импульсы.
- 2. Внутренние клетки -- отростки этих клеток не покидают пределы серого вещества СМ, оканчиваются в пределах данного сегмента или соседнего сегмента, т.е. по функции являются ассоциативными.
- 3. Пучковые клетки -- отростки этих клеток образуют нервные пучки белого вещества и направляются в соседние сегменты или вышележащие отделы НС, т.е. по функции тоже являются ассоциативными.
Задние рога СМ более короткие, узкие и содержат следующие виды нейроцитов:
- а) пучковые нейроциты -- располагаются диффузно, получают чувствительные импульсы от нейроцитов спинальных ганглиев и передают по восходящим путям белого вещества в вышележащие отделы НС (в мозжечок, в кору больших полушарий);
- б) внутренние нейроциты -- передают чувствительные импульсы со спинальных ганглиев в двигательные нейроциты передних рогов и в соседние сегменты.
В задних рогах СМ имеются 3 зоны:
- 1. Губчатое вещество -- состоит из мелких пучковых нейроцитов и глиоцитов.
- 2. Желатинозное вещество -- содержит большое количество глиоцитов, нейроцитов практически не имеет.
- 3. Собственное ядро СМ -- состоит из пучковых нейроцитов, передающих импульсы в мозжечок и зрительный бугор.
- 4. Ядро Кларка (Грудное ядро) -- состоит из пучковых нейроцитов, аксоны которых в составе боковых канатиков направляются в мозжечок.
В боковых рогах (промежуточная зона) имеются 2 медиальные промежуточные ядра и латеральное ядро. Аксоны пучковых ассоциативных нейроцитов медиальных промежуточных ядер передают импульсы в мозжечок.. Латеральное ядро боковых рогов в грудном и поясничном отделе СМ является центральным ядром симпатического отдела вегетативной НС; аксоны нейроцитов этих ядер идут в составе передних корешков СМ как преганглионарные волокна и оканчиваются на нейроцитах симпатического ствола (превертебральные и паравертебральные симпатические ганглии). Латеральное ядро в сакральном отделе СМ является центральным ядром парасимпатического отдела вегетативной НС.
Передние рога СМ содержат большое количество мотонейронов (двигательных нейронов), образующие 2 группы ядер:
- 1. Медиальная группа ядер -- иннервирует мышцы туловища.
- 2. Латеральная группа ядер хорошо выражена в области шейного и поясничного утолщения -- иннервирует мышцы конечностей.
По функции среди мотонейронов передних рогов СМ различают:
- 1. -мотонейроны большие -- имеют диаметр до 140 мкм, передают импульсы на экстрафузальные мышечные волокна и обеспечивают быстрое сокращение мышц.
- 2. -мотонейроны малые -- поддерживают тонус скелетной мускулатуры.
- 3. -мотонейроны -- передают импульсы интрафузальным мышечным волокнам (в составе нервно-мышечного веретена).
- - мотонейроны -- это интегративная единица СМ, они испытывают влияние и возбуждающих и тормозных импульсов. До 50% поверхности тела и дендритов мотонейрона покрыты синапсами. Среднее число синапсов на 1 мотонейроне СМ человека составляет 25-35 тысяч. Одномоментно на 1 мотонейрон могут передавать импульсы с тысячи синапсов идущие от нейронов спинального и супраспинальных уровней.
Возможно и возвратное торможение мотонейронов благодаря тому, что ветвь аксона мотонейрона передает импульс на тормозные клетки Реншоу, а аксоны клеток Реншоу оканчиваются на теле мотонейрона тормозными синапсами.
Аксоны мотонейронов выходят из СМ в составе передних корешков, достигают скелетных мышц, заканчиваются на каждой мышечной волокне моторной бляшкой.
Белое вещество СМ состоит из продольно ориентированных преимущественно миелиновых нервных волокон, образующие задние (восходящие), передние (нисходящие) и боковые (и восходящие и нисходящие) канатики, а также из глиальных элементов.
ГОЛОВНОЙ МОЗГ -- является высшим центральным органом регуляции всех жизненноважных функций организма, играет исключительную роль в психической или высшей нервной деятельности.
ГМ развивается из нервной трубки. Краниальный отдел нервной трубки в эмбриогенезе подразделяется на три мозговых пузыря: передний, средний и задний. В дальнейшем за счет складок и изгибов из этих пузырьков формируется пять отделов ГМ:
- - продолговатый мозг;
- - задний мозг;
- - средний мозг;
- - промежуточный мозг;
- - конечный мозг.
Дифференцировка клеток нервной трубки в краниальном отделе при развитии ГМ протекает в принципе аналогично с развитием спинного мозга: т.е. камбием служит слой вентрикулярных (герменативных) клеток, расположенных на границе с каналом трубки. Вентрикулярные клетки интенсивно делятся и мигрируют в вышележащие слои и дифференцируются в 2-х направлениях:
- 1. Нейробласты нейроциты. Между нейроцитами устанавливаются сложные взаимосвязи, формируются ядерные и экранные нервные центры. Причем в отличие от спинного мозга в ГМ преобладают центры экранного типа.
- 2. Глиобласты глиоциты.
Проводящие пути ГМ, многочисленные ядра ГМ -- их локализацию и функции Вы подробно изучаете на кафедре нормальной анатомии человека, поэтому на этой лекции мы сосредоточимся на особенностях гистологического строения отдельных частей ГМ.
СТВОЛ МОЗГА -- к нему относят продолговатый мозг, мост, мозжечок и образования среднего и промежуточного мозга.
ПРОДОЛГОВАТЫЙ МОЗГ состоит из серого вещества, организованного в виде ядер и пучков нисходящих и восходящих нервных волокон. Из ядер различают:
- 1. Чувствительные и двигательные ядра черепных нервов -- ядра подьязычного, добавочного, блуждающего, языкоглоточного, предверно-улиткового нервов продолговатого мозга. Причем двигательные ядра располагаются преимущественно медиально, а чувствительные -- латерально.
- 2. Ассоциативные ядра -- нейроны которых образуют связи с мозжечком и таламусом.
Гистологически все эти ядра состоят из мультиполярных нейроцитов.
В центральной части ПМ находится ретикулярная формация (РФ), которая начинается в верхней части спинного мозга, проходит через ПМ, распространяется далее в задний, средний и промежуточный мозг. РФ состоит из сети нервных волокон и мелких групп мультиполярных нейроцитов. Эти нейроциты имеют длинные, слабоветвящиеся дендриты и аксон с многочисленными коллатералями, благодаря которым образуются многочисленные синаптические связи с огромным числом нейроцитов и восходящими и нисходящими нервными волокнами. Нисходящее влияние РФ обеспечивает регуляцию вегетативно-висцеральных функций, контроль над тонусом мышц и стереотипными движениями. Восходящее влияние РФ обеспечивает фон возбудимости коры БПШ как необходимое условие для бодроствующего состояния мозга. РФ передает импульсы не в строго определенные участки коры, а диффузно. В целом РФ образует окольный афферентный путь в кору ГМ, по который импульсы проходят в 4-5 раз медленнее, чем по прямым афферентным путям.
Кроме ядер и РФ в продолговатом мозге имеются как нисходящие и восходящие пути.
МОСТ. В дорсальной части моста находятся ядра V, VI, VII, VIII черепных нервов, ретикулярная формация и волокна проводящих путей. В вентральной части моста имеются собственные ядра моста и волокна пирамидных путей.
СРЕДНИЙ МОЗГ в качестве наиболее крупных и важных образований имеет красные ядра; они состоят из гигантских нейроцитов, от которых начинается руброспинальный путь. В красном ядре переключаются волокна от мозжечка, таламуса и двигательных центров коры БПШ.
Читайте также:


