Госпитальные штаммы формируют вирусы полиомиелита
Вирусы полиомиелита
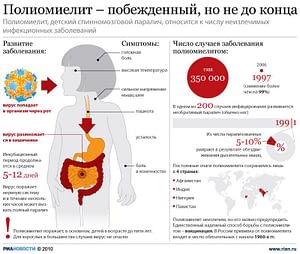
Полиомиелит – острое лихорадочное заболевание, которое иногда сопровождается поражением серого вещества (от греч. polios – серый) спинного мозга и ствола головного мозга, в результате чего развиваются вялые параличи и парезы мышц ног, туловища, рук.
Полиомиелит известен с глубокой древности. Заболевание впервые описано в монографии Хайне в 1840 г. Эпидемиология этого заболевания установил в 1890 г Медина (болезнь Хайне-Медина). Вирусную этиологию болезни доказали К. Ландштайнер и Э. Поппер в 1909 г. В 1951 г выделено три штамма вируса полиомиелита: Брунгильд, Лэнсинг и Леон.
Возбудитель полиомиелита относится к семейству Picornaviridae, роду Enterovirus, виду Poliovirus.
Эпидемии полиомиелита охватывали в 1940-1950 гг. тысячи и десятки тысяч человек, из которых 10 % умирали и примерно 40 % становились инвалидами.
Структура вирусов полиомиелита.По структуре полиовирусы – типичные представители рода Enterovirus.
Антигенные свойства.Различают три серотипа внутри вида: 1, 2, 3, не вызывающие перекрестного иммунитета. Все серотипы патогенны для обезьян, у которых возникает заболевание, сходное по клиническим проявлениям с полиомиелитом человека.
Патогенез. Естественная восприимчивость человека к вирусам полиомиелита высокая. Входными воротами служат слизистые оболочки верхних дыхательных путей и пищеварительного тракта. Первичная репродукция вирусов происходит в лимфатических узлах глоточного кольца и тонкой кишки. Это обусловливает обильное выделение вирусов из носоглотки и с фекалиями еще до появления клинических симптомов болезни. Из лимфатической системы вирусы проникают в кровь (виремия), а затем в ЦНС, где избирательно поражают клетки передних рогов спинного мозга (двигательные нейроны). В результате этого возникают параличи мышц. В случае накопления в крови вируснейтрализующих антител, блокирующих проникновение вируса в ЦНС, ее поражения не наблюдается.
Клиническая картина. Инкубационный период продолжается в среднем 7-14 дней. Различают клинические формы полиомиелита: паралитическую (1 % случаев), менингеальную (без параличей), абортивную (легкая форма, инаппарантная инфекция без клинически выраженных симптомов). Заболевание начинается с повышения температуры тела, общего недомогания, головных болей, рвоты, болей в горле. Полиомиелит нередко имеет двухволновое течение, когда после легкой формы и наступившего значительного улучшения развивается тяжелая форма болезни. Паралитическую форму чаще вызывает вирус полиомиелита серотипа 1.
Иммунитет. После перенесенной болезни остается пожизненный типоспецифический иммунитет. Иммунитет определяется в основном наличием вируснейтрализующих антител, среди которых важная роль принадлежит местным секреторным антителам слизистой оболочки глотки и кишечника (местный иммунитет). Эффективный местный иммунитет играет важнейшую роль в прерывании передачи диких вирусов и способствует вытеснению их из циркуляции. Пассивный естественный иммунитет сохраняется в течение 3-5 недель после рождения ребенка.
Диагностика.Материалом для исследования служат кал, отделяемое носоглотки, при летальных исходах кусочки головного и спинного мозга, лимфатические узлы. Вирусы полиомиелита выделяют путем заражения исследуемым материалом первичных и перевиваемых культур клеток. О репродукции вирусов судят по цитопатическому действию. Идентифицируют (типируют) выделенный вирус с помощью типоспецифических сывороток в реакции нейтрализации в культуре клеток. Важное значение имеет внутривидовая дифференциация вирусов, которая позволяет отличить дикие патогенные штаммы от вакцинных штаммов, выделяющихся от людей, иммунизированных живой полиомиелитной вакциной. Различия между дикими и вакцинными штаммами выявляют с помощью ИФА, реакции нейтрализации цитопатического действия вируса в культуре клеток со штаммоспецифической иммунной сывороткой, а также в ПЦР.
Серологическая диагностика основана на использовании парных сывороток больных с применением эталонных штаммов вируса в качестве диагностикума. Содержание сывороточных иммуноглобулинов классов IgG, IgA, IgM определяют методом радиальной иммунодиффузии по Манчини.
Лечение патогенетическое. Применение гомологичного иммуноглобулина для предупреждения развития паралитических форм весьма ограничено.
Профилактика. Основной мерой профилактики полиомиелита является иммунизация. Массовое применение вакцины против полиомиелита привело к резкому снижению заболеваемости.
Первая инактивированная вакцина для профилактики полиомиелита была разработана американским ученым Дж. Солком в 1953 г. Однако парентеральная вакцинация этим препаратом создавала лишь общий гуморальный иммунитет, не формировала местную резистентность слизистых оболочек желудочно-кишечного тракта и не обеспечивала надежную специфическую защиту.
Естественно аттенуированные штаммы вирусов полиомиелита всех трех типов получил в 1956 г. А. Сэбин, а в 1958 г. М.П. Чумаков и А.А. Смородинцев разработали первую пероральную живую культуральную вакцину из трех серотипов штаммов Сэбина. Вакцину используют для массовой иммунизации детей, она создает стойкий общий и местный иммунитет.
ВОЗ в 1988 г. приняла решение о глобальной ликвидации полиомиелита путем охвата прививками всего детского населения планеты. Под ликвидацией подразумевали прекращение заболеваний и искоренение вируса полиомиелита.
Использование оральной поливакцины привело практически к полному исчезновению случаев полиомиелита в развитых странах Европы и в Америке и резкому снижению заболеваемости в развивающихся странах.
У живой полиомиелитной вакцины имеются некоторые недостатки, наиболее серьезным из которых является возникновение вакцино-ассоциированного полиомиелита у привитых и контактных лиц, инфицированных вирусами, выделяемыми привитыми детьми. Контактное инфицирование происходит обычно вирусом одного серотипа.
Показано, что у иммунокомпетентных лиц отсутствует длительное носительство поливируса после вакцинации, в то время как у лиц с иммунодефицитами вакцинный штамм может выделяться в течение 7-10 лет. Риск развития вакциноассоциированного паралитического полиомиелита у лиц с иммунодефицитами, особенно с нарушениями В-клеточного иммунитета, выше, чем у иммунокомпетентных лиц.
Неспецифическая профилактика сводится к санитарно-гигиеническим мероприятиям: обеспечению населения доброкачественными водой, пищевыми продуктами, соблюдению личной гигиены, выявлению больных и подозрительных на заболевание лиц.
Специфическая профилактика полиомиелита заключается в вакцинации инактивированными и живыми вакцинами в соответствии с национальным календарем прививок. В РФ в настоящее время зарегистрированы две взаимозаменяемые вакцины – ЖВС (пероральная 1, 2, 3 типов, раствор для приема внутрь; ранее использовали в виде антиполиодраже) и Полио Сэбин Веро – отечественного и зарубежного производства соответственно.
Не нашли то, что искали? Воспользуйтесь поиском:
Госпитальные штаммы. Особенности госпитальных штаммов возбудителей внутрибольничных инфекций.
Циркулирующие в стационарах возбудители внутрибольничных инфекций постепенно формируют так называемые госпитальные штаммы, т. е. штаммы наиболее эффективно адаптированные к местным особенностям того или иного отделения.
Главной особенностью госпитальных штаммов является повышенная вирулентность (во всех случаях это первая и главная особенность госпитального штамма), а также специфическая адаптация к используемым лечебным препаратам (антибиотики, антисептики, дезинфектанты и т. п.). В настоящее время сложилась система, по которой о госпитальном штамме судят по спектру устойчивости к антибиотикам.

Это удобная и доступная в практических условиях система контроля формирования госпитального штамма возбудителями внутрибольничных инфекций, поскольку имеются неопровержимые данные о связи между используемыми антибиотиками в стационаре и спектром резистентности возбудителей. Но при этом надо иметь в виду, что такие штаммы оказываются чрезвычайно опасными не только из-за устойчивости к лечебным препаратам, но и в связи с их повышенной (причем иногда значительно) вирулентностью (у них меньшая инфицирующая доза, приобретены дополнительные факторы патогенности и т. д.).
Итак, госпитальный штамм — это штамм, который в процессе циркуляции адаптировался к условиям стационара, т. е. приобрел большие возможности к паразитированию, специфичному для больных данного стационара, а именно, вирулентность, устойчивость к неблагоприятным внешним факторам, также специфичным для данного стационара, и способность вызывать групповые внутрибольничные случаи заболеваний.
Госпитальные штаммы в результате устойчивой циркуляции в лечебном учреждении приобретают дополнительные внутривидовые характеристики, позволяющие эпидемиологам устанавливать эпидемиологические связи между пациентами, определять пути и факторы передачи.
Не нашли то, что искали? Воспользуйтесь поиском:
Внутрибольничная инфекция, ее типы. Госпитальные штаммы. Особенности лабораторной диагностики внутрибольничных инфекций.
Внутрибольничная инфекция— это инфекция, заражение которой происходит в больничных учреждениях: наслаиваясь на основное заболевание, она утяжеляет клиническое течение болезни, затрудняет диагностику и лечение, ухудшает прогноз и исход заболевания, нередко приводя к смерти больного.
Классификация ВБИ
1. В зависимости от путей и факторов передачи ВБИ классифицируют:
- Воздушно-капельные (аэрозольные)
- Вводно-алиментарные
- Контактно-бытовые
- Контактно-инструментальные
- Постинъекционные
- Постоперационные
- Послеродовые
- Посттрансфузионные
- Постэндоскопические
- Посттрансплантационные
- Постдиализные
- Постгемосорбционные
- Посттравматические инфекции
- Другие формы.
2. От характера и длительности течения:
- Тяжелые
- Среднетяжелые
- Легкие формы клинического течения.
В зависимости от степени распространения инфекции:
- Генерализованные инфекции: бактериемия (виремия, микемия), септицемия, септикопиемия, токсико-септическая инфекция (бактериальный шок и др.).
- Локализованные инфекции
- Инфекции кожи и подкожной клетчатки (ожоговых, операционных, травматический ран, Постинъекционные абсцессы, омфалит, рожа, пиодермия, абсцесс и флегмона подкожной клетчатки, парапроктит, мастит, дерматомикозы и др.);
- Респираторные инфекции (бронхит, пневмония, легочный абсцесс и гангрена, плеврит, эмпиема и др.);
- Инфекции глаза (конъюнктивит, кератит, блефарит и др.);
- ЛОР-инфекции (отиты, синуситы, ринит, мастоидит, ангина, ларингит, фарингит, эпиглоттит и др.);
- Стоматологические инфекции (стоматит, абсцесс, др.);
- Инфекции пищеварительной системы (гастроэнтероколит, энтерит, колит, холецистит, гепатиты, перитонит, абсцессы брюшины и др.);
- Урологические инфекции (бактериурия, пиелонефрит, цистит, уретрит, др.);
- Инфекции половой системы (сальпингоофорит, эндометрит, др.);
- Инфекции костей и суставов (остеомиелит, инфекция сустава или суставной сумки, инфекция межпозвоночных дисков);
- Инфекции ЦНС (менингит, абсцесс мозга, вентрикулит и др.);
- Инфекции сердечно-сосудистой системы (инфекции артерий и вен, эндокардит, миокардит, перикардит, постоперационный медиастинит).
Отличия госпитального штамма от обычного:
- Способность к длительному выживанию
- Повышенная агрессивность
- Повышенная устойчивость
- Повышенная патогенность
- Постоянная циркуляция среди больных и персонала
Выявление и характеристика ВБИ невозможна без выявления и характеристики микробных ассоциаций в больницах и контроля за ВБИ. Для этого необходимо получать информацию из самых различных источников.
Диагностика госпитальных инфекций проводится по обычным методикам, которые применяются в бактериологических лабораториях. Специальные методики для внутрибольничных инфекций не разработаны. Однако при микробиологических исследованиях для выделения возбудителей госпитальных инфекций есть некоторые особенности.
Необходимо установить этиологический фактор по многим признакам: род, тип, подтип. — биоценотический принцип.
Необходимо иметь данные по чувствительности выделенных микробов к антибиотикам, антисептикам, дезинфектантам, для организации правильного лечения и профилактики. — Химиотерапевтический принцип.
Всегда следует учитывать степень обсеменения обследуемого материала так как при массивном обсеменении вероятность заболевания увеличивается Количественный принцип.
Надо соблюдать, так называемый, популяционный принцип. Это значит что надо снимать с плотных питательных сред несколько колоний, ибо две колонии одного и того же вида могут отличаться друг от друга.
Больные должны обследоваться в течение пребывания в стационаре несколько раз, т.к. возможна смена возбудителя. — Динамический принцип.
Обязательно изучаются факторы патогенности: выработка токсина, факторов препятствующих фагоцитозу и лизису микроорганизмов, гемолиз выработка лецитиназы у стафилококков и т.д.
Необходимо типирование выделенных микробов (фаготипирование, серотипирование и т.д.) — эпидемиологический приниип.
При изучении специфичности и чувствительности набора тестов, характеризующих внутрибольничный эковар, установлены два высокоспецифичных признака: контаминация штаммом 30% и выше необработанных предметов отделения, в значительной степени представленных медицинскими аппаратами и санитарно-техническим оборудованием, а также контаминация дезинфектанта (Ю.А.Захарова, И.В.Фельдблюм, 2008).
Эпидемиологический стандарт внутрибольничного штамма (эковара) может быть рекомендован к использованию в рамках микробиологического мониторинга в системе эпидемиологического надзора за ВБИ, что позволит улучшить предэпидемическую диагностику ГСИ в ЛПУ с целью принятия своевременных адекватных управленческих решений по снижению заболеваемости ГСИ.
Современные вакцинные препараты:
1. Корпускулярные (живые и инактивированные) – из целых м/о, это вакцины первого поколения
2. Растворимые (химические и анатоксины) — из отдельных фракций возбудителей или продуктов их жизнедеятельности – второе поколение вакцин
3. Генно-инженерные — рекомбинантные вакцины, третье поколение
Требования к вакцинам:
— высокая иммуногенность и создание достаточно стойкого иммунитета
— остаточная вирулентность аттенуированных штаммов и стабильность их свойств
— безвредность
— отсутствие выраженных побочных действий (ареактивность)
— гипоаллергенность (минимально сенсибилизирующее действие)
— отсутствие в препарат контаминирующих м/о
— доступность производства
Вакцины могут вводиться: перорально, парэнтерально (внутримышечно, подкожно, внутрикожно, в поврежденную кожу (скарифицированную)), интраназально, в свечах и клизмах.
Для выработки прочного и длительного иммунитета необходим достаточный контакт макроорганизма и Аг => применяют ревакцинации черз определенное количество времени, зависящее от свойств биопрепарата.
Не у всех вакцинированных возникает прочный иммунитет (может быть недостаточная иммунореактиность/иммунодефицитные состояния).
Эффективность вакцинации зависит от типа и качества биопрепарата и способности возбудителя вызывать стойкий постинфекционный иммунитет.
Вакцины требуют строгого соблюдения правил хранения и транспортировки.
Преимущества живых вакцин:
высокая иммуногенность (формируют длительный напряженный иммунитет), простота способа введения; при естественных путях введения – местный иммунитет (секреторный IgA)
Недостатки: длительный и трудоемкий процесс получения; особый режим хранения (2-8*С) и чувствительность к его нарушению; есть опасность реверсии вакцинного штамма в вирулентный (при производстве или в организме вакцинированного); возможны осложнения после вакцинации; людям с иммунодефицитами противопоказаны живые вакцины, только инактивированные. После введения живой вакцины противопоказаны антибиотики в течение 2-2,5 мес.
Сейчас применяют вакцины для профилактики:
— бактериальных инфекций (туберкулезная- БЦЖ, сибиреязвенная, чумная, туляремийная, бруцеллезная)
— вирусных инфекций (корь, грипп, краснуха, паротит, желтая лихорадка)
— риккетсиозов (лихорадку-Ку и сыпной тиф)
Вакцины живые выпускают в сухом виде, лиофильно высушенные с добавлением стабилизаторов (желатиново-сахарозная среда). Исключение – живая полиомиелитная вакцина – жидкая.
Генная инженерия.
Генная инженерия — раздел молекулярной генетики, связанный с конструированием несуществующих в природе сочетаний генов при помощи генетических и биохимических методов.
Метод генетической инженерии относится к числу перспективнейших при получении многих белковых биологических веществ, представляющих ценность для медицины.
Генно-инженерные вакцины – это препараты, полученные с помощью биотехнологии, которая по сути сводиться к генетической рекомбинации .
Для начала получают ген, который должен быть встроен в геном реципиента. Небольшие гены могут быть получены методом химического синтеза. Для этого расшифровывается число и последовательность аминокислот в белковой молекуле вещества, затем по этим данным узнают очерёдность нуклеотидов в гене, далее следует синтез гена химическим путем.
Крупные структуры, которые довольно сложно синтезировать получаются путем выделения(клонирования), прицельного выщепления этих генетических образований с помощью рестриктаз.
Полученный одним из способов целевой ген с помощью ферментов сшивается с другим геном, который используется в качестве вектора для встраивания гибридного гена в клетку. Вектором могут служить плазмиды, бактериофаги, вирусы человека и животных. Экспрессируемый ген встраивается в бактериальную или животную клетку, которая начинает синтезировать несвойственное ей ранее вещество, кодируемое эксперссируемым геном.
В качестве реципиентов экспрессируемого гена чаще всего используется E. coli, B. subtilis, псевдомонады, дрожжи, вирусы. некоторые штаммы способны переключаться на синтез чужеродного вещества до 50% своих синтетических возможностей – эти штамм называются суперпродуцентами.
Иногда к генно-инженерным вакцинам добавляется адъювант.
Примерами таких вакцин служат вакцина против гепатита В (энджерикс), сифилиса, холеры, бруцеллёза, гриппа, бешенства.
Есть определённые сложности в разработке и применении:
— длительное время к генно-инженерным препаратам относились настороженно.
— на разработку технологии для получения вакцины затрачиваются значительные средства
— при получении препаратов данным способом возникает вопрос об идентичности полученного материала природному веществу.
Дисбактериоз.
Последнее изменение этой страницы: 2017-01-19; Нарушение авторского права страницы
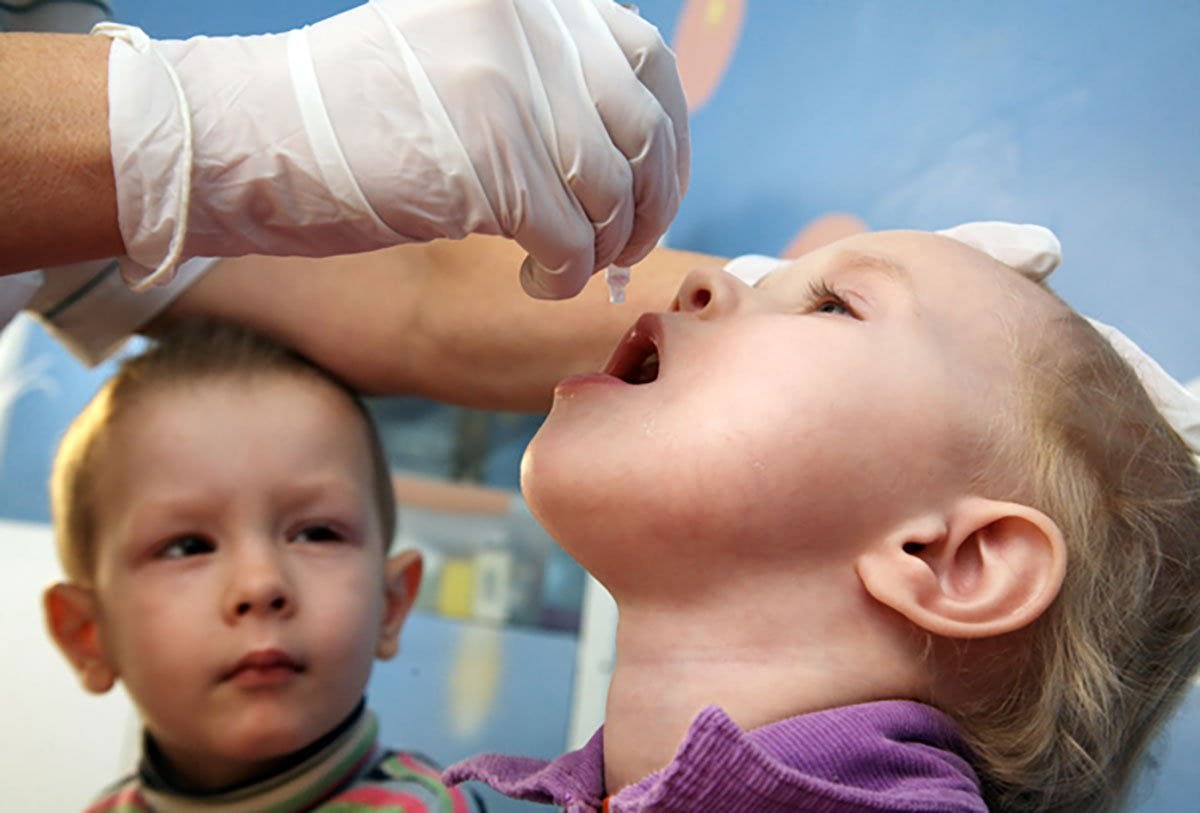
Полиомиелит (болезнь Гейне-Медина) – это опасное вирусное заболевание вследствие инфицирования человека полиовирусом. Группа высокого риска заболеваемости – дети до 7 лет. Характеризуется высокой контагиозностью (передачей возбудителя через непосредственный контакт или предметы обихода) особенно в межсезонный период. Заражение вирусом вызывает глубокое поражение двигательных клеток серого вещества спинного мозга, что обуславливается необратимыми процессами атрофирования в области спины, верхних и нижних конечностей (спинномозговой паралич). Болезнь классифицируется по МКБ-10 под кодами А80-А80.9 как неизлечимая патология центральной нервной системы.
Вирус полиомиелита, структура вируса, как распространяется, от чего погибает
Возбудитель болезни полиомиелита – вирус P oliovirus hominis. Выделен из организма инфицированного носителя в начале ХХ века. Относится к кишечной группе энтеровирусов (разновидности ЕСНО-вирусы и Коксаки). 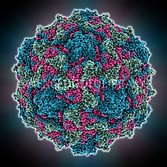
Патогенез полиомиелита
Источником инфицирования является больной носитель. Поскольку характеристика болезни чаще всего является практически бессимптомной, или с идентичными легкой простуде признаками недомогания, носитель может не подозревать о существующем заражении.
Заражение полиомиелитом происходит
- фекально-оральным путем — немытые руки, предметы общего использования, пищевые продукты, мухи;
- воздушно-капельный – тесный контакт с вирусоносителем или больным на любой стадии болезни полиомиелит.

Проникновение вируса полиомиелита в здоровый организм происходит через рот. Попадая на слизистую оболочку, вирион начинает активное размножение в области миндалин, кишечнике. Затем бактерия проникает в кровоток и лимфу, парализует функции и разрушает структуру двигательных клеток спинного мозга.
Прогноз выздоровления зависит от иммунной защиты организма инфицированного. При сильно ослабленном иммунитете в 2% случаев последствием перенесенного полиомиелита является вялотекущий паралич нижних конечностей (поражение поясничных позвонков). Грудные и шейные атрофии встречаются редко. Большинство заразившихся людей переносят легкую форму болезни без последствий, приобретают стойкий иммунитет и становятся полностью невосприимчивыми к последующим атакам вируса.
Полиомиелит: у стойчивость возбудителя
Вирион обладает стабильной устойчивостью к внешней среде вне носителя. Зафиксированы случаи активной жизнедеятельности бактерии до 100 суток в воде и до 6 месяцев в фекалиях зараженного человека. Вирион устойчив к воздействию желудочных кислот и не чувствителен к антибиотикам. Резкая смена температурного режима переводит возбудитель в более пассивную стадию, однако случаи инфицирования замороженным вирусом не исключаются.
При нагревании более 50 градусов Цельсия наблюдались необратимые структурные изменения в молекуле до полного разрушения в течение получаса. Температура кипения воды, ультрафиолетовое облучение полностью уничтожают молекулярную активность возбудителя. Дезинфекция хлористыми содержащими растворами деактивирует способность вириона к популяризации.
Заболеваемость полиомиелитом
Вирусной популяризации полиомиелита способствуют климатические условия, образ жизни, постоянное нахождение в социуме, отсутствие нормальных условий медицинского обслуживания. Инфицирование фекально-оральным способом чаще всего происходит через грязное полотенце, не мытые продукты, зараженную воду, использование общих вещей — полотенца, чашки, тарелки или игрушек. Воздушное заражение обуславливается контактом с больным через рукопожатие, разговор, поцелуй.
![]()
Клинические симптомы полиомиелита
Степень проявления видимых показателей заболевания полиомиелитом зависит от устойчивости иммунитета ребенка. На развитие болезни также влияет количество находящихся в организме молекул вируса. При слабой иммунной системе после заражения полиомиелитом у детей развивается вирусемия (быстрое проникновение в кровь). Вирион в основном характеризуется поражением клеток ЦНС, однако способен инфицировать легкие, сердце, миндалины.
Период инкубации колеблется от 5 до 14 дней. Временной промежуток зависит от иммунной сопротивляемости, однако уже зараженный носитель является распространителем возбудителя. В период с 7 до 40 дней больным выделяется огромная концентрация вириона вместе с фекалиями.
- Инаппаратная
Бессимптомное течение болезни. Период активной выработки организмом иммунной защиты к вирусу. В это время вирион полиомиелита можно обнаружить только в лабораторных анализах при выделении антител. - Висцеральная (абортивная) – первый этап болезни (1-3 дня)
Наиболее распространенная классификация – до 80% больных. Проходит под обычными простудными симптомами: боль в голове, насморк, вялость, отсутствие аппетита, кашель и субфебрильная температура тела. Заканчивается через недели, обычно прогноз благоприятный. - Поражение ЦНС
Болезнь осложняется наступлением дефектного атрофирования у 50% больных. - Непаралитическая
Характерна проявлением более выраженных симптомов висцеральной классификации. Диагностировать полиомиелит можно по наличию миненгиальных проявлений – отсутствие или затрудненность двигательной реакции затылочных мышц, резкая боль в голове. Процесс выздоровления занимает около месяца, осложнений в виде паралича не наблюдалось. - Паралитическая (появление 4-6 день заболевания)
Отмечается быстрое нарастание признаков болезни, состояние больного ухудшается. Поражение ЦНС характеризуется бредом, головной болью, судорогами, нарушением сознания. Больной жалуется на боль по ходу нервных окончаний, симптомы менингии выражены. При обследовании смена местоположения тела больного очень болезненна, пальпаторно определяется локализация болевого синдрома в области позвонков.
Поскольку развитие паралитической классификации болезни бывает редко, в зависимости от места локализации вирусного поражения выделены несколько форм последствий полиомиелита (замещений погибших клеток глиозной органической тканью).
- спинальный – паралич вялый в области конечностей, туловища;
- бульбарный – нарушение функций глотания и дыхания, возможно речевое замедление;
- понтинный – атрофирование лицевых мышц;
- энцефалитный – поражение участков головного мозга с утратой подведомственных функций.


Внезапное возникновение полного паралича развивается на фоне сниженной температуры тела и сопровождается массовой гибелью третьей части нервных клеток переднероговой области спинного мозга. Вследствие клеточного отмирания атрофируются мышцы нижних конечностей, пациент прикован к постели по причине отказа двигательной функции ног и нуждается в сестринском уходе. Редко наблюдаются случаи атрофирования туловища или группы дыхательной мускулатуры.
Летальный исход заболевания полиомиелитом обусловлен поражением продолговатого мозга, где расположен центр жизнеобеспечения человеческого организма. Нередко значительно осложняющими исход болезни причинами являются бактериальное заражение крови, развитие воспалительного процесса дыхательных путей (более 10% летального исхода от полиомиелита).
Диагностика полиомиелита
Идентифицирование возбудителя проводится микробиологическим выделением белкового, лимфоцитного содержания, а также обнаружению антител классового расположения M и G , по биоматериалу больного – спинномозговой жидкости, крови, слизи носовых проходов и испражнениях.
Лечение полиомиелита

На основании микробиологических данных разрабатывается комплекс назначений при обнаружении и классифицировании текущей стадии болезни. Поскольку сегодня эффективных лекарств для лечения полиомиелита не существует, комплексная терапия ограничивается снижением болевых ощущений и облегчением состояния больного до полного выздоровления.
Первоначальным этапом терапии является полная госпитализация выявленного больного с назначением обезболивающих, успокаивающих средств и тепловых процедур. С целью ограничения параличных осложнений пациенту обеспечивается полная физическая неподвижность, для стимуляции иммунной защиты применяются иммуноглобулины и витаминизированные инъекции. Использование физиопроцедур (парафиновое обертывание, диатермия, влажные аппликации) помогает минимизировать риски развития паралича. В восстановительном периоде применяются процедуры бассейного плавания, массаж и лечебные гимнастики.
Прогноз выздоровления после полиомиелита чаще всего благоприятен при непаралитической классификации заболевания. В случаях мышечного поражения велика вероятность последующей дефектной атрофии, поэтому очень важно своевременное соблюдение раннего ортопедического режима.

При формировании паралича очень важно начать быструю восстановительную терапию для развития и укрепления соседних участков головного мозга. Утрату подведомственных функций пораженной области могут восполнить неповрежденные участки ЦНС.
Полиомиелит — вакцинация
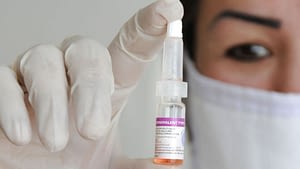
Вакцинирование – самый лучший и действующий способ профилактики полиомиелита. Учитывая специфику последствия заболевания, вакцина от полиомиелита включена МОЗ в список обязательных детских прививок до года.
На практике используются два вида прививок от полиомиелита:
- первая (живая вакцина полиомиелита) разработана А.Себиным на основе живого, но ослабленного вириона. Выпускается в виде драже или розовых капель от полиомиелита;
- вторая (инактивированная) синтезирована Д.Солком из синтетического полиовируса, деактивированная формалином. Применяется в виде инъекций.
Новорожденный грудничок находится под надежной защитой материнского иммунитета, поэтому до достижения 3 месяцев ребенок непривитый. Первая вакцинация проводится живой вакциной в виде розовых капель в рот детям 3, 4, 5 месячного возраста. Введение живой бактерии способствует возникновению и мощной стимуляции иммунной защиты организма, направленной на подавление ослабленного вибриона и активной выработке антител.

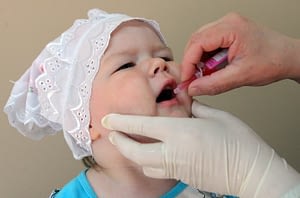
Следующий период ревакцинации полиомиелита проводится в 1,5 года, 6 лет и 14 лет, ребенку вводится инактивированная прививка после АКДС. Троекратное внутримышечные прививки вакцины стимулирует развитие гуморального иммунитета у ребенка, начиная с периода профилактики полиомиелита в саду и заканчивая профилактическими мерами в школе.
Взрослым требуется вакцинация от полиомиелита в случаях, когда человек не был привит с детства, а также при посещении опасных зон по заболеванию. Последующая ревакцинация должна производиться каждые 5-10 лет.
На сегодняшний день обе вакцины являются самыми эффективными в профилактике полиомиелита. Однако современные врачи отдают предпочтение живой вакцине – вирионы, размножаясь в кишечнике, выделяются и циркулируют в социуме, постепенно вытесняя дикие неподконтрольные штаммы полиовируса.
С 1950 гг. эпидемии полиомиелита возникали во многих развитых странах. Вспышки характеризовались до 40% инвалидностью, и 10 % смертельного исхода. После разработки и введения живой вакцины (начало 1960гг.) заболеваемость резко снизилась. Инактивированная вакцина доказала свою эффективность. Широкая иммунизация привела к резкому упадку уровня заболеваемости среди населения. В некоторых населенных пунктах были полностью ликвидированы очаги болезни. Начиная с 1980 года, в России регистрируются единичные очаги инфекции, что составляет 0,0002% общего населения. Одиночные вспышки обусловлены миграцией не вакцинированных людей из стран подверженных возникновению и развитию очагов болезни (Таджикистан, Чечня, Дагестан, Ингушетия).

Существует тенденция к возникновению заболевания в самый уязвимый период – 4-5 лет. Во время стремления и окружающего познавания отмирающие клетки особо невосприимчивы к реабилитации и восстановлению. Заболевание полиомиелитом опасно и для взрослых, поэтому очень важно проводить своевременную вакцинацию населенного пункта повсеместно. Каждая новая вспышка полиомиелита способствует дальнейшему распространению вируса, поэтому пока есть риск заболевания полиомиелитом, необходимо строго соблюдать периоды вакцинации во избежание популяризации обширных эпидемий.
Читайте также: