Можно ли принимать глиатилин при болезни паркинсона
Для лечения заболеваний центральной нервной системы, последствий инсульта или черепно-мозговой травмы неврологи Юсуповской больницы используют современный ноотропный препарат глиатилин. Отзывы врачей и пациентов о лекарственном средстве положительные. Врачи Юсуповской больницы назначают глиатилин после комплексного обследования пациентов с помощью современной диагностической аппаратуры ведущих европейских и американских фирм.
Все тяжёлые случаи заболеваний, при которых возникает необходимость в назначении глиатилина, обсуждаются на заседании Экспертного Совета с участием профессоров и врачей высшей категории. Ведущие неврологи коллегиально принимают решение о выборе дозы, пути введения препарата и длительности терапевтического курса индивидуально каждому пациенту. На форумах содержится информация, что при приёме глиатилина можно похудеть, отзывы людей, принимающих препарат для снижения массы тела. Глиатилин не влияет на обмен липидов и относится к средствам для похудения. Это препарат, оказывающий выраженное комплексное действие на центральную и периферическую нервную систему. Применять его можно по показаниям под контролем врача.

Форма выпуска, состав препарата
Глиатилин выпускается в овальных жёлтых непрозрачных мягких желатиновых капсулах, которые содержат вязкий бесцветный раствор. В одной капсуле находится 400мг основного действующего вещества холина альфосцерат и вспомогательные компоненты: глицерол, вода очищенная. Оболочка капсул состоит из следующих ингредиентов:
- Желатина;
- Эзитола;
- Сорбитана;
- Натрия этилпарагидроксибензоата;
- Натрия пропилпарагидроксибензоата;
- Титана диоксида;
- Железа (III) метагидроксида.
Блистер с четырнадцатью капсулами и инструкцией по применению помещён в картонную пачку. Цена препарата и отзывы о нём есть в интернете.
Глиатилин в ампулах – это прозрачный без цвета и запаха раствор для внутривенного и внутримышечного введения. Одна ампула имеет объём 1мл. Один миллилитр раствора содержит 250мг холина альфосцерата. В ячейковую контурную упаковку помещены 3 ампулы бесцветного стекла объёмом 4мл. В картонной коробке находится 1 контурная упаковка и инструкция по применению препарата глиатилин. Отзывы можно прочитать на медицинских форумах.
Фармакологическое действие лекарственного средства
Глиатилин – холиномиметик центрального действия с преимущественным влиянием на центральную нервную систему. Высвобождение холина из активного вещества препарата происходит в головном мозге. Холин принимает участие в биосинтезе одного из основных медиаторов нервного возбуждения – ацетилхолина. Альфосцерат биологическим путём превращается до глицерофосфата, который является предшественником фосфолипидов.
Ацетилхолин улучшает передачу нервных импульсов, а глицерофосфат принимает участие в выработке мембранного фосфолипида фосфатидилхолина, в результате чего улучшается эластичность мембран и функция рецепторов. Глиатилин оказывает следующее действие:
- Увеличивает мозговой кровоток;
- Усиливает обменные процессы и активирует структуры ретикулярной формации головного мозга;
- Восстанавливает сознание при травматическом поражении мозговой ткани.
Препарат оказывает профилактическое и корректирующее действие на такие факторы инволюционного психоорганического синдрома, как изменение фосфолипидного состава мембран нейронов и снижение холинергической активности. Глиатилин действует на синаптическую, в том числе холинергическую передачу нервного импульса, функцию рецепторов, пластичность мембраны нейронов.
После приёма внутрь всасывается 88% препарата. Он легко проникает через гематоэнцефалический барьер, накапливается преимущественно в головном мозге, печени и лёгких. 85% основного действующего вещества выводится из организма лёгкими в виде диоксида углерода, 15% – почками и кишечником.
Показания и противопоказания к применению
Неврологи Юсуповской больницы назначают глиатилин в острый период черепно-мозговой травмы преимущественно со стволовыми поражениями, в том числе пациентам с нарушением сознания и пребывающим в коме. Лекарственное средство оказывает выраженное терапевтическое действие в остром и восстановительном периоде нарушения мозгового кровообращения по ишемическому типу и в восстановительном периоде геморрагического инсульта.
Глиатилин для пожилых людей применяют при старческой псевдомеланхолии. Препарат показан при наличии изменений в эмоциональной и поведенческой сфере: эмоциональной лабильности, повышенной раздражительности, снижении интереса. Глиатилин, как свидетельствуют отзывы взрослых, улучшает состояние пациентов, страдающих дегенеративными и инволюционными психоорганическими синдромами и последствиями цереброваскулярной недостаточности, такими как первичные и вторичные нарушения мнестических функций. Они характеризуются следующими симптомами:
- Нарушениями памяти;
- Дезориентацией;
- Спутанностью сознания;
- Снижением инициативности, мотивации и способности к концентрации внимания.
Отзывы врачей, которые имеют опыт применения глиатилина для лечения пожилых пациентов, свидетельствуют о высокой эффективности лекарственного средства при следующих состояниях:
- Изменениях в эмоциональной и поведенческой сфере пациента (эмоциональной лабильности, повышенной раздражительности, снижении интереса);
- Старческой псевдомеланхолии;
- Мультиинфарктной деменции.
Врачи Юсуповской больницы не назначают глиатилин при повышенной чувствительности к компонентам препарата, беременности и кормлении грудью.
Инструкция по применению препарата у детей
Отзывы родителей, чьим детям детские неврологи назначали глиатилин, положительные. В педиатрической практике лекарственное средство применяется при повышенной раздражительности и других эмоциональных нарушениях. Врачи назначают глиатилин детям при наличии следующих показаний:
- Аутизм;
- СДВГ (синдроме дефицита внимания и гиперактивности);
- Нервных тиках и других неврозах;
- ДЦП (детский церебральный паралич).
Неонатологи применяют препарат в составе комплексной терапии младенцев, которые перенесли гипоксию во время родов, имеют родовые травмы мозга или страдают гидроцефалией. Препарат показан детям с ЗРР (задержкой психического или речевого развития). Отзывы родителей превосходные.
Возрастные ограничения в инструкции по применению глиатилина отсутствуют, поэтому препарат назначают новорожденных и детям до года. Малышам до 2 лет назначают уколы препарата, а капсулы рекомендуют давать внутрь детям школьного возраста и старше. Капсулы малыша следует научить проглатывать полностью, не раскусывая, запивая водой.
Раствор можно делить в ампуле, получая меньшую дозировку, которая подходит конкретному ребёнку по возрасту. Уколы глиатилина делают внутримышечно. Препарат также назначают детям в виде внутривенных инфузий. Инъекцию делают перед едой в первой половине дня. Неиспользованный для укола раствор выливают.
Получите консультацию невролога по поводу наличия показания и противопоказаний к применению препарата глиатилин, записавшись на приём. После обследования врач назначит необходимую дозу лекарственного средства, определит длительность курса лечения. Медицинский персонал Юсуповской больницы профессионально выполняет внутримышечные инъекции и внутривенные инфузии глиатилина. Для уколов используются одноразовые стерильные шприцы, капельные системы, современные дезинфицирующие средства.
Эффективность Глиатилина в улучшении качества жизни пациентов, живущих с болезнью Паркинсона
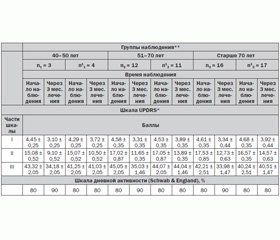
Статья опубликована на с. 22-25
Введение
Болезнь Паркинсона (БП) является неуклонно прогрессирующим хроническим заболеванием центральной нервной системы, в основе которого лежит дегенерация дофаминергических нейронов черной субстанции, проявляющаяся сочетанием гипокинезии с ригидностью, тремором покоя и постуральной не-устойчивостью, определенную негативную роль играет дисбаланс ацетилхолина, глутамата, норадреналина и серотонина [1, 3, 5, 14, 16, 22]. Среди факторов, ведущих к дегенерации и апоптозу этих нейронов, важную роль играют нарушение митохондриального дыхания, энергетический дефицит нейрона, усиление свободнорадикального окисления, избыточное накопление свободных ионов кальция и повышение эксайтотоксичности глутамата, вызывающее деполяризацию мембраны нейрона, нарушение ионной проницаемости с массивным входом ионов кальция в клетку (глутамат-кальциевый каскад) [4, 8, 9, 23]. Патоморфологически БП характеризуется избирательной гибелью нейронов черной субстанции, стадийным распространением и накоплением телец Леви (ольфакторная луковица и передние ольфакторные ядра, другие ядра ствола, черная субстанция, кора головного мозга), согласно гипотезе H. Braak [10, 11, 15]. Значимость БП обусловлена влиянием на качество жизни пациентов, трудоспособность, инвалидизацию. Снижение качества жизни пациентов с болезнью Паркинсона происходит преимущественно за счет двигательных нарушений, наличия болевого синдрома. При БП, кроме того, что появляются двигательные нарушения, также страдают эмоциональная и когнитивная сферы личности, и эти расстройства обусловлены преморбидными особенностями и естественным течением патологического процесса, а также влиянием применяемой терапии, ее закономерными побочными действиями. Помимо классических двигательных нарушений для БП характерен широкий спектр немоторных проявлений, включающий психические, вегетативные, сенсорные расстройства, нарушения сна и бодрствования, которые отражают вовлечение других структур центральной нервной системы, а также периферической нервной системы в патологический процесс [12, 13, 18]. Одним из наиболее частых немоторных проявлений БП является боль. В классической физиологии изложено несколько аспектов возникновения боли:
2) теория генераторных и системных механизмов боли, развитая Г.Н. Крыжановским (1976), согласно которой сильная ноцицептивная стимуляция, поступающая с периферии, вызывает в клетках задних рогов спинного мозга каскад процессов, которые запускаются возбуждающими аминокислотами и пептидами (субстанцией Р);
3) кроме того, болевые синдромы могут возникать вследствие деятельности в системе болевой чувствительности новых патологических интеграций — агрегата гиперактивных нейронов, который является генератором патологически усиленного возбуждения и патологической алгической системы, представляющей собой новую структурно-функциональную организацию, которая состоит из первично и вторично измененных ноцицептивных нейронов, и являющейся патогенетической основой болевого синдрома;
Исследователи полагают, что боль у пациентов может быть связана с основными симптомами паркинсонизма, прежде всего мышечной ригидностью, сопутствующей скелетно-мышечной патологией, или может быть самостоятельным симптомом, отражающим нарушение функции ноцицептивной системы при БП [20, 25]. У пациентов с БП боль может также зависеть от нейромедиаторных изменений и возникать на фоне как гиподофаминергического, так и гипердофаминергического состояния [17]. В связи с этим развитию болевого синдрома могут способствовать осложнения длительной терапии леводопой, включая как моторные и немоторные флюктуации, так и дискинезии [21]. Все это предопределяет гетерогенность болевых синдромов при БП. Ряд болезненных ощущений может быть связан с развивающимися при этом заболевании моторными осложнениями, такими как мышечная дистония, дискинезии и др. При этом нужно иметь в виду, что характерный для БП церебральный дофаминергический дефицит изменяет состояние ноцицептивной системы, приводя к снижению порога боли. Все это делает актуальным комплексный клинический анализ хронических болевых синдромов у больных БП, их взаимосвязь с заболеванием и их реакции на дофаминергическую терапию [2, 6, 7]. Особенностью болевых синдромов при БП, с которой соглашаются все исследователи, является высокая частота встречаемости хронической боли различной локализации. Было показано, что возникновение болевых синдромов может опережать развитие других симптомов БП.
Пациенты с БП часто предъявляют жалобы на сжимающие и тянущие ощущения в шее, спине, ногах, жгучие, покалывающие ощущения в различных областях тела, в том числе в полости рта и в области гениталий. Часто пациенты описывают боль как тупую, грызущую и обжигающую. Примерно в 1/3 случаев выявляется связь интенсивности сенсорных ощущений с флюктуациями моторного симптомокомплекса и уменьшением дозы леводопы. Одной из наиболее частых зон локализации боли является область плечевого сустава. Эта боль описывается пациентами как постоянная, плохо локализованная, сжимающая или спазмирующая, иногда жгучая. Обычно после назначения или коррекции дофаминергической терапии происходит уменьшение ощущения дискомфорта и боли в области плечевого сустава. Также часто при БП выявляется боль в пояснице. Ее интенсивность и частота не связаны с длительностью и выраженностью заболевания. В литературных источниках, посвященных этой проблеме, описаны возможные механизмы возникновения боли при БП:
1) первичным является увеличение периферической афферентации, происходящее за счет наличия разнообразных двигательных нарушений, приводящих к изменению взаимоотношения состояния мышц агонистов и антагонистов; это нарушение меняет привычную биомеханику движения, обусловливая микротравматизацию мышц, связочного аппарата, суставных капсул, вызывая в них асептическое воспаление, которое приводит к активации периферических ноцицепторов;
2) в качестве возможной причины возникновения боли при БП обсуждаются нейромедиаторные нарушения, сопровождающие различные стадии этой болезни, которые приводят к снижению болевого порога, при этом имеющиеся двигательные нарушения усиливают афферентный ноцицептивный поток, в результате которого появляется боль;
3) предполагается, что скелетно-мышечные болевые синдромы возникают из-за нарушения нормальной физиологической биомеханики двигательного акта вследствие постуральных и других двигательных нарушений, а также изменений мышечного тонуса, для них характерны ноющие, ломящие боли, судороги; наличие гипокинезии приводит к изменению привычного двигательного стереотипа, нарушению биомеханики движения на разных уровнях, ограничению функционирования защитных и компенсаторных движений; предпосылками к развитию периферической невропатической боли являются дегенеративные заболевания позвоночника; примечательно, что при этом их интенсивность часто снижается на фоне повышения дозы леводопы, однако полностью боли на фоне дофаминергической терапии не регрессируют;
4) точные клинические характеристики и механизмы развития так называемой центральной боли (жгучая боль, сопровождающаяся ощущением покалывания и пощипывания, ползания мурашек) при БП остаются неясными; в основе формирования центрального болевого синдрома при БП предположительно лежит нарушение баланса между ноцицептивной и антиноцицептивной системами, заключающееся в снижении активности последней на фоне нейромедиаторных нарушений при сохранном восходящем ноцицептивном потоке;
5) в формировании болевых синдромов при БП не исключена определенная роль изменения центральных дофаминергических механизмов, принимающих участие в обработке болевой информации.
Целью данной работы явилось изучение влияния препарата Глиатилин (холина альфосцерат) на регресс боли и улучшение когнитивно-мнестического потенциала при БП у пациентов разного возраста и стажа заболевания с учетом применения комплексной терапии.
Материалы и методы исследования
Всем пациентам основной группы (n = 31) до назначения Глиатилина и спустя 3 месяца мы проводили клинико-неврологическое и нейропсихологическое исследование, мониторинг артериального давления, ЭЭГ, МРТ головного мозга. Для обработки полученных результатов применялись расчетные и табличные критерии Фишера — Снедекора для 12 степеней свободы выборок у данных больных, а также интеграл вероятности (функция Лапласа). Моделирование велось в Microsoft Excel с использованием встроенной таблицы квазислучайных чисел.
Результаты и их обсуждение
В 2013 г. из когорты больных, ранее взятых на учет в региональном кабинете (среди 154 пациентов с БП в возрасте от 34 до 80 лет акинетико-ригидный синдром преобладал в 69 % случаев, дрожательно-ригидный — в 31 %, феномен on-off — в 26 %, тремор, резистентный к леводопе, — в 24 %, снижение дневной активности — в 53 %, 94 % пациентов жаловались на тянущую, ноющую боль в верхней половине спины, руках), мы отобрали 31 пациента с БП (основная группа) с жалобой на боль в теле, конечностях для дообследования и уточнения степени функциональных нарушений. При анализе проведенных ЭЭГ в 63 % регистрировалась низкоамплитудная ЭЭГ с дисфункцией стволовых структур. При МРТ головного мозга у 57 % пациентов визуализировалась умеренная внутренняя гидроцефалия, у 73 % больных отмечена субтрофия коры полушарий головного мозга и мозжечка. При оценке неврологического статуса у этих больных мы пользовались клиническими диагностическими критериями Банка мозга Общества болезни Паркинсона Великобритании (1992), критериями шкалы UPDRS (1987), модифицированной шкалой оценки стадии заболевания по Hoehn & Yahr, шкалой MMSE, шкалой дневной активности (Schwab & England). Первая стадия болезни была выявлена у 3 пациентов, вторая — у 12, третья — у 16 пациентов. В нашей работе мы использовали следующие критерии включения: стадию болезни, жалобы на боль (симптом, обусловленный изменением мышечного тонуса — ригидность, дистония; моторные флюктуации и дискинезии; боль центрального типа — локальная акатизия), умеренные когнитивные нарушения, понимание пациентом и его родственниками необходимости медикаментозной коррекции. В ходе нашей работы были проанализированы симптомы цервикоторакалгии, люмбалгии и боли в конечностях у включенных в исследование пациентов с ригидной, тремор-доминантной и ригидно-дрожательной формами БП (ВАШ, шкала Ликерта, NADCS (дельта составила 0,55–1,95 и 0,75–1,05 балла), метод описательных определений боли). В когорту исследуемых пациентов с БП мы не включили больных с разным преморбидным фоном (боль, не исключающая вертеброгенный, дискогенный и миофасциальный генез, дегенерацию суставов конечностей).
Акцент терапии был сделан на применении Глиатилина у пациентов, получавших рутинную схему терапии (леводопа и агонисты дофаминовых рецепторов). Глиатилин, как пресинаптический холинергический препарат, восстанавливает нейрональные связи, оптимизирует нейротрансмиссию (высвобождение холина в головном мозге и увеличение биосинтеза ацетилхолина, что улучшает информационный обмен между нейронами), не связывается с рецепторами ацетилхолина и не влияет на холинэстеразу, нормализует функцию и структуру нейронов, репарацию нейрональных мембран (глицерофосфат улучшает синтез фосфатидилхолина, что ведет к восстановлению пластичности нейрональной мембраны, оптимизации функции рецепторного аппарата), обладает вторичной дофаминергической активностью. Пациенты, получавшие Глиатилин, были в основной группе наблюдения, контрольную группу составили больные, которым проводилась стандартная терапия. Анализ рекомендованной терапии и оценка динамики критериев шкал UPDRS (1987), шкалы дневной активности (Schwab & England) проводились нами с момента начала наблюдения за конкретным пациентом и через три месяца лечения.
Положительный эффект терапии с применением Глиатилина у пациентов с болезнью Паркинсона основной группы наблюдения (табл. 1) проявлялся в виде улучшения процессов мышления, поведения, настроения (первая часть UPDRS), повышения повседневной жизненной активности (вторая часть UPDRS), улучшения показателей дневной активности (шкала Schwab & England); показатели двигательной активности (третья часть UPDRS) изменились в меньшей степени.
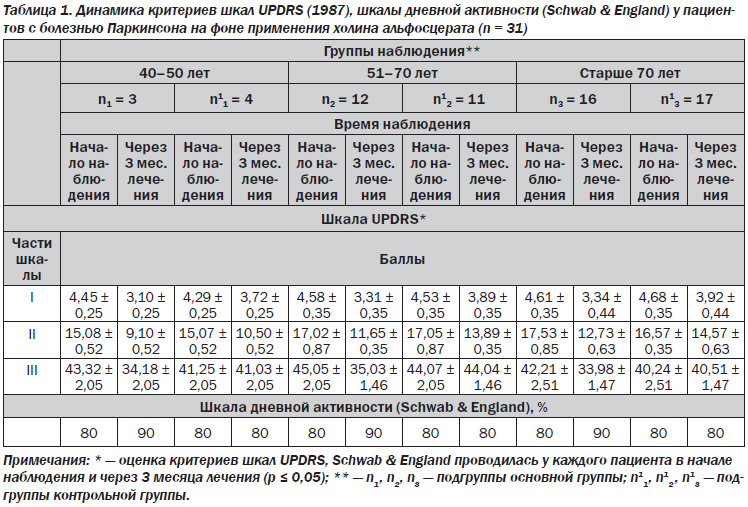
Следует указать, что практически 75 % пациентов основной группы отметили уменьшение интенсивности боли. При проведении психодиагностических тестов нами выявлено достоверное различие между результатами исследования пациентов основной и контрольной группы (р Список литературы
1. Бархатова В.П. Нейротрансмиттеры и экстрапирамидная патология. — М.: Медицина, 1988. — 175 с.
2. Вейн А.М. Болевые синдромы в неврологической практике / А.М. Вейн, Т.Г. Вознесенская, А.Б. Данилов. — М., 1999. — С. 372 .
3. Голубев В.Л. Особенности клинического течения и фармакотерапии болезни Паркинсона на разных этапах развития заболевания / В.Л. Голубев, Я.И. Левин, А.М. Вейн // Международный медицинский журнал. — 2005. — Т. 11, № 4. — С. 47-51.
4. Карабань Н.В. Комплексная патогенетическая терапия болезни Паркинсона (клинические, диагностические, медико-социальные аспекты): Автореф. дис… д-ра мед. наук. — К., 2007. — 33 с.
5. Крыжановский Г.Н. Болезнь Паркинсона (этиология, патогенез, клиника, диагностика, лечение, профилактика) / Г.Н. Крыжановский, И.Н. Карабань, С.В. Магаева, В.Г. Кучеряну, Н.В. Карабань. — М.: Медицина, 2002. — 335 с.
6. Крыжановский Г.Н. Общая патофизиология нервной системы. — М.: Медицина, 1997. — 352 с.
7. Махнев С.О. Болевые синдромы при болезни Паркинсона: Автореф. дис. канд. мед. наук. — М., 2011. — 32 с.
8. Шток В.Н. Экстрапирамидные расстройства: Руководство по диагностике и лечению / В.Н. Шток, И.А. Иванова-Смоленская, О.С. Левин. — М.: Медпресс, 2002. — 600 с.
9. Arundinc М. Molecular mechanisms of calcium-dependent neurodegeneration in excitotoxicity / М. Arundinc, М. Tymianski // Cell. Calcium. — 2003. — 34. — 325-337.
10. Braak H. Staging of brain pathology related to sporadic Parkinson’s disease / H. Braak, К. Del Tredici, V. Rub // Lancet Neurology. — 2008. — Р. 223-233.
11. Croisier Е. Microglial inflammation in the parkinsonian substantia nigra; relationship to a-synuclein deposition / E. Croisier, L.B. Moran, D.T. Dexter // J. Neuroinflamm. — 2005. — Vol. 2. — P. 14-21.
12. De Lau L.M. Epidemiology of Parkinson’s disease / L.M. De Lau, M.M. Breteler // Lancet Neurol. — 2006. — 5. — P. 525-535.
13. Hartmann A. Pathophysiology of Parkinson’s disease // Parkinson Disorders in Clinical Practice / A. Hartmann, A. Schapira, Y. Agid. —Blackwell Publishing Ltd. — 2009. — P. 1-10.
14. Jenner P. Oxidative stress in Parkinson’s disease / P. Jenner // Ann. Neurol. — 2003. — Vol. 53, Suppl. 3. — P. S26-S36.
15. Jellinger K.A. Lewy body-related alpha-synudeinopathy in the aged human brain / К.А. Jellinger // J. Neurоl. — 2004. — Vol. 111. — P. 1219-1235.
16. Koutsilieri Е. Free radicals in Parkinson’s disease / E. Koutsilieri, C. Scheller, E. Grunblatt // J. Neurol. — 2002. — Vol. 249, Suppl. 2. — P. S1-S5.
17. Langston J.W. The Parkinson’s complex: parkinsonism is just the tip of the iceberg / J.W. Langston // Ann. Neurol. — 2006. — 59. — P. 591-596.
18. Olanow C. An algorithm for the management of Parkinson’s disease (2001): treatment guidelines / C. Olanow, R. Watts, W. Roller // Neurology. — 2001. — V. 56, Suppl. 5. — P. S1-S88.
При различных проблемах с мозговым кровообращением, патологий со стороны сердечно-сосудистой системы и ЦНС возникает необходимость в использовании ноотропов.
Одним из популярных средств является Глиатилин .

Информация о Глиатилине включена в систему лекарственных средств, прошедших регистрацию в РФ.
Основные данные о нейропротекторе:
- название на латыни – Gliatilin ;
- основа состава – холина альфосцерат;
- анатомо-терапевтическо-химическая классификация – N07AX02, ноотропы.
Последняя актуализация проводилась 12.07.2011 г.
Состав
Основу состава представляет химическое соединение холина альфосцерат .

Область действия компонента распространяется на холиновые рецепторы в ЦНС.
Чтобы средство лучше усваивалось организмом, действующее вещество дополнено:
- эзитолом;
- этилпарагидроксибензоат натрием;
- желатином;
- пропилпарагидроксибензоат натрием;
- сорбитансом;
- метагидроксидом;
- диоксидом титана, железа.
Для изготовления жидкой формы действующий компонент дополняется глицерином и жидкостью в виде очищенной воды.
Фармакология
Терапевтический эффект с высокой результативностью обеспечивается благодаря физическим и химическим свойствам составляющих химических соединений.

Среди основных:
- влияние на системный кровоток путём ускорения кровообращения;
- активизация обменных функций;
- стимулирование ретикулярной формации;
- восстановление утерянного функционала при разного рода травмах (при повреждении мозговых тканей).
Ноотроп корректирует факторы инволюционного психоорганического синдрома.
Этот процесс основан на подавлении холинергической активности, в результате чего меняется количество фосфолипидов в нейроновых мембранах.
Под воздействием обменных процессов вещество преобразуется в диоксид углерода, после чего выводится из организма с помощью кишечника и почек.
Цена и формы выпуска
Стоимость лекарства зависит от формы выпуска и дозировки:
- Капсулы (400 мг, 14 шт.) – цена в диапазоне 720-780 руб .
![]()
- Раствор для приёма внутрь (600 мг/7 мл, 10 ед.) – цена 520 руб .
![]()
- Инъекционная жидкость (1000 мг, ампулы 4 мл, 3 ед.) – цена в диапазоне 565-630 руб .
![]()
Купить ноотропное средство доступно как в сети аптек, так и интернет-магазине.
Одним из главных условий отпуска фармакологического продукта является наличие рецепта.
При оформлении заказа через интернет-аптеку возможен вариант приобретения лекарства без рецептурного листа.
Показания к применению
В медицине ноотропное лекарство используется при следующих патологиях:
- нарушения зрительной памяти, речевых функций;
- синдромы, характеризующиеся снижением интеллекта, памяти и других дегенеративных разрушений (когда причиной их развития является цереброваскулярная недостаточность);
- снижение познавательной деятельности, слабоумие.

Препарат проявляет высокую эффективность при коррекции психоэмоционального состояния, нарушениях в поведении, других патологий ЦНС.
Другое применение лекарства:
- при инсультах для снятия острых симптомов;
- для реабилитации после приступа инсульта (способствует восстановлению физических навыков и сознания).
Нейропротектор используется также в терапии для детей.

Считается обоснованным применение лекарства при следующих проблемах:
- неврозах, нервном тике;
- аутизме;
- СДВГ;
- гидроцефальном синдроме;
- ДЦП;
- при задержке психического развития, ЗРР;
- при родовых травмах мозга;
- при родовой гипоксии.
Инструкция по применению
Инъекционная жидкость разработана для ввода лекарства с помощью иглы в/в или в/м способом.
Внутривенные уколы (капельницы) выполняются с предварительным растворением 1 ампулы лекарства с 50 мл физраствора.

Скорость движения жидкости по системе – 80 капель/мин.
- Лечение острых форм заболеваний начинается с внутримышечных инъекций. Суточная норма средства составляет 600-1000 мг. Иногда рационально применять внутривенное введение лекарства (до 3000 мг).
- Как только отмечается положительная динамика в состоянии пациента, осуществляется переход на таблетки . На это требуется в среднем 5-10 дней.
Нейропротектор в капсулах принимается перорально. Время приёма – за 40-60 минут перед едой.

Схема терапии предусматривает 2-3 кратное употребление лекарства по 1 таблетке на протяжении 3-6 месяцев (продолжительность курса зависит от этиологии заболевания, интенсивности его развития, состояния пациента).
Инструкция по применению для детей:
- приём средства лучше перенести на утро перед завтраком;
- запивать целую таблетку нужно только очищенной водой (100-150 мл);
- при назначении капельных в/в инфузий препарат предварительно разбавляется физиологическим раствором;
- в/м уколы делают в мышечную ткань (чаще задействуется плечевая или бедренная часть);
- время проведения инъекций – до 12-14 часов.
При ЧМТ рекомендовано использовать по 1 ампуле в день на протяжении 1 недели. После этого осуществляется переход на капсулы (по 1 ед. дважды в сутки на протяжении 2-х месяцев).
Продолжительность терапии родовой травмы/гипоксической энцефалопатии проводится около полугода. На протяжении 10-12 дней инъекции ставятся раз в день (1-2 мл). Суточная норма для детей 1-3 лет может увеличиваться до 2-3 мл, для возрастной группы более 3-х лет – 4 мл. Следующий этап терапии – применение таблетированного средства. Капсулы употребляют по схеме: по 1 шт. 2 раза в день. Через 2-3 месяца лечение может корректироваться специалистом, под наблюдением которого находится пациент.
Глиатилин при беременности и лактации
Нейропротектор беременным пациентам не назначается.

Исключается одновременный приём лекарства и кормление грудью ребёнка.
При возникновении необходимости в использовании Глиатилина кормящей женщине предлагается временно отказаться от грудного вскармливания младенца.
Ограничение к применению
Отказаться от использования лекарственного средства стоит тем пациентам, у которых имеется аллергия на один из компонентов состава.
Ограничения затрагивают также возрастную группу моложе 18 лет. С осторожностью Глиатилин используют в педиатрии.
При введении инъекции соблюдается запрет на смешивание нейропротектора с другими лекарствами в одном шприце.
Побочные проявления
В процессе проведённого исследования по изучению действия холина альфосцерата на организм человека были выявлены редкие случаи побочных проявлений.
На начальном этапе терапии могут появиться тошнота, лёгкая спутанность сознания, боль в эпигастрии.

О неприятных симптомах информируется врач, у которого пациент наблюдается. Специалист скорректирует дозу, подберёт аналог, внесёт другие изменения в лечебный курс.
Передозировка
О передозировке лекарственного средства свидетельствует необоснованная тошнота. Сопутствующие симптомы: отрыжка, метеоризм или жидкий стул.
Пациенту предлагается принять сорбент и снизить суточную дозировку.
Отзывы пациентов
Альбина:
Терапия длилась 4 месяца (1 капсула в день). Положительная динамика стала заметна спустя 10 дней.
Через месяц ребёнок выглядел абсолютно уравновешенным, невзирая на не всегда адекватное поведение по отношению к нему сверстников. Побочных проявлений весь лечебный период я не наблюдала.

Виктор, 37 лет:
Через пару недель ощутил первые улучшения: исчезла раздражительность, речь стала чёткой и понятной, усилилась концентрация внимания. Никаких побочек при употреблении капсул замечено не было.

Отзывы врачей-неврологов
А. П. Степанов, стаж работы 22 года:
Длительный приём лекарства снижает когнитивный дефицит.
Особенности использования ноотропа: из-за повышенной возбудимости рекомендовано принимать до обеденного времени, чтоб избежать негативного влияния на здоровый сон. Эффективность повышается при курсовой терапии, предусматривающей использование на начальном этапе инъекций, затем – капсул.

Татьяна Михайловна Кузнецова, практикующий специалист со стажем 12 лет:
Высокий терапевтический эффект достигается при астении, ВСД, ДЦП и пр.
Удобным считается и наличие разных форм выпуска, что позволяет достичь желаемого результата при минимальной нагрузке на печень и почки.

Аналоги препарата
Для терапии гипотетически подходит любое средство, которое разработано на основе холина альфосцерата.
На деле специалист выбирает аналог с учётом нескольких важных факторов.
Наиболее эффективными считаются лекарства:
- Церепро;
![]()
- Ноохолин Ромфарм;
![]()
- Делецит;
![]()
- Церетон;
![]()
- Холитилин;
![]()
- Глеацер.
![]()
Для детей врач предлагает:
- Анвифен (в капсулах) – рекомендовано с 3-х летнего возраста, активное вещество – аминофенилмасляная кислота;
![]()
- Кортексин (в инъекционных ампулах) – допускается включать в терапию для недоношенных детей;
![]()
- Аминалон (в таблетках) – состав содержит ГАМК, применяется с 1 года;
![]()
- Пантогам (в виде сиропа) – состав разработан на основе гопантеновой кислоты, препарат подходит для любого возраста;
![]()
- Ноотропил (разные формы) – состав разработан на основе пирацетама, используется с годовалого возраста.
![]()
Видео
Читайте также:
















