Нервная регуляция работы поджелудочной железы
Регуляция поджелудочной экзокринной секреции осуществляется нервными и гуморальными механизмами. Блуждающий нерв усиливает секрецию поджелудочной железы. Симпатические нервы уменьшают количество секрета, но усиливают синтез органических веществ. Снижение секреции происходит также и за счет уменьшения кровоснабжения поджелудочной железы путем сужения кровеносных сосудов. Напряженная физическая и умственная работа, боль, сон вызывают торможение секреции. Гастроинтестинальные гормоны усиливают секрецию поджелудочного сока. Секретин стимулирует выделение сока, богатого бикарбонатами. Секрецию поджелудочной железы усиливают гастрин, серотонин, бомбезин, инсулин, соли желчных кислот. Тормозящее действие оказывают ЖИП, ПП, глюкагон, кальцитонин, соматостатин.
Выделяют 3 фазы панкреатической секреции: сложнорефлекторную, желудочную и кишечную. На отделение сока поджелудочной железы влияет характер принятой пищи. Эти влияния опосредованы через соответствующие гормоны. При длительном преобладании в пищевом рационе только углеводов, или белков, или жиров происходит и соответствующее изменение ферментного состава панкреатического сока.
Поджелудочная железа обладает и внутрисекреторной активностью, продуцируя инсулин, глюкагон, соматостатин, панкреатический полипептид, серотонин, ВИП, гастрин.
Поджелудочная железа ребенкаимеет внешнесекреторную и внутрисекреторную функции. Она вырабатывает поджелудоч ный сок, состоящий из альбуминов, глобулинов, микроэлемен тов и электролитов, ферментов, необходимых для переваривания пищи. В число ферментов входят протеолитические ферменты: трипсин, химотрипсин, эластаза, — а также липолитические фер менты и амилолитические ферменты. Регуляцию поджелудочной железы обеспечивает секретин, стимулирующий отделение жид кой части панкреатического сока, и панкреозимин, который уси ливает секрецию ферментов наряду с другими гормоноподобны ми веществами, которые вырабатываются слизистой оболоч кой двенадцатиперстной и тонкой кишок.
35. Состав и свойства желчи. Роль желчи в пищеварении. Желчеобразование механизмы регуляции. Методы исследования желчевыделения у человека
Желчь — продукт секреции печеночных клеток, представляет собой жидкость золотисто-желтого цвета, имеющую щелочную реакцию (рН 7,3—8,0) и относительную плотность 1,008—1,015.
У человека желчь имеет следующий состав: воды 97,5%, сухого остатка 2,5%. Основными компонентами сухого остатка являются желчные кислоты, пигменты и холестерин. Желчные кислоты относят к специфическим продуктам обмена веществ печени. У человека в желчи обнаруживают преимущественно холевую кислоту. Среди желчных пигментов различают билирубин и биливердин, которые придают желчи характерную окраску. В желчи человека содержится главным образом билирубин. Пигменты желчи образуются из гемоглобина, который освобождается после разрушения эритроцитов. Кроме того, в желчи содержатся муцин, жирные кислоты, неорганические соли, ферменты и витамины.
У здорового человека в сутки выделяется 0,5—1,2 л желчи. Секреция желчи осуществляется непрерывно, а поступление ее в двенадцатиперстную кишку происходит во время пищеварения. Вне пищеварения желчь поступает в желчный пузырь. Поэтому различают желчь пузырную и печеночную. Пузырная желчь темная, имеет вязкую и тягучую консистенцию, плотность ее 1,026—1,048, а рН—6,8. Отличия пузырной желчи от печеночной обусловлены тем, что слизистая оболочка желчных путей и пузыря продуцирует муцин и обладает способностью всасывать воду.
Желчь выполняет многообразные функции, тесно связанные с деятельностью желудочно-кишечного тракта. Желчь относят к пищеварительным сокам.
Однако она выполняет и экскреторную функцию, так как с ней выводятся из крови различные экзо- и эндогенные вещества. Это отличает желчь от других пищеварительных соков.
Регуляция желчеобразовательной и желчевыделительной функций печени
Желчеобразование — это сложный процесс, который состоит из трех взаимосвязанных компонентов. Первый компонент желчеобразования представлен фильтрационными процессами (поступление из крови через мембраны капилляров в желчь некоторых веществ — воды, глюкозы, ионов натрия, кальция, хлора). Вторым компонентом желчеобразования является процесс активной секреции печеночными клетками желчных кислот. Третий компонент желчеобразования связан с обратным всасыванием воды и ряда других веществ из желчных капилляров, протоков и желчного пузыря.
Желчеобразовательная функция печени находится под воздействием разнообразных факторов. Стимуляторами желчной секреции являются компоненты желчи, находящиеся в крови, хлористоводородная и другие кислоты, под влиянием которых в двенадцатиперстной кишке образуется секретин. Этот гормон не только способствует образованию поджелудочного сока, но и гуморально, воздействуя на печеночные клетки, стимулирует продукцию желчи.
В регуляции желчеобразовательной функции печени участвует нервная система. Установлено, что блуждающие и правый диафрагмальный нервы при их возбуждении усиливают выработку желчи печеночными клетками, симпатические нервы ее тормозят. На образование желчи оказывают влияние и рефлекторные воздействия, идущие со стороны интерорецепторов желудка, тонкого и толстого кишечника и других внутренних органов. Доказано влияние коры большого мозга на продукцию желчи печеночными клетками.
Ряд факторов способствует поступлению желчи в двенадцатиперстную кишку. Отделение желчи усиливается во время еды в результате рефлекторного влияния на все секреторные процессы, осуществляемые в желудочно-кишечном тракте.
Изучение влияния количества и вида принятой пищи на выделение желчи показало, что желчегонным эффектом обладают молоко, мясо, хлеб. У жиров это действие выражено в большей степени, чем у белков и углеводов. Обнаружено, что продолжительность желчевыделения при потреблении мяса равняется в среднем 7 ч, хлеба —10 ч и молока примерно 9 ч. Желчь выделяется в большем количестве на мясо и молоко, в меньшем — на хлеб. Максимум секреции на мясо наблюдается на 2-м часу, на хлеб и молоко на 3-м часу после приема пищи. Было также установлено, что наибольшее количество желчи выделяется при смешанном питании.
Методы изучения желчеобразовательной и желчевыделительной функции печени
В деятельности печени следует различать желчеобразование, то есть продукцию желчи печеночными клетками, и желчеотделение — выход, эвакуацию желчи в кишечник. В экспериментальной физиологии существует два основных метода, позволяющих изучить эти две стороны деятельности печени.
Для исследования желчеобразовательной функции печени у собак перевязывают общий желчный проток, исключая тем самым поступление желчи в кишечник. Одновременно на желчный пузырь накладывают фистулу. При помощи такой операции собирают всю оттекающую и непрерывно вырабатываемую печеночными клетками желчь.
Для изучения желчевыделительной функции печени и роли желчи в процессе пищеварения И.П. Павловым была предложена следующая операция. У собак, находящихся под наркозом, из стенки двенадцатиперстной кишки иссекают небольшой лоскут, в центре которого находится общий желчный проток. Этот кусочек кишки выводят на поверхность и вшивают в кожную рану брюшной стенки. Целость кишечника восстанавливают наложением швов. При этой операции иннервация сфинктера общего желчного протока сохраняется.
При наблюдении за оперированными животными было установлено, что выделение желчи идет одновременно с секрецией поджелудочного сока. Желчь выделяется почти тотчас после приема пищи, секреция ее достигает максимума к 3-му часу и затем довольно быстро убывает. Было также обнаружено, что выраженным желчегонным действием обладает жирная пища, в меньшей степени это свойственно углеводам. Мясо занимает среднее положение в ряду продуктов, способных усилить желчеотделение. Следовательно, интенсивность поступления желчи в двенадцатиперстную кишку зависит от вида принимаемой пищи.
Для изучения секреции желчи у человека применяют рентгенологический метод и дуоденальное зондирование. При рентгенологическом исследовании вводят вещества, не пропускающие рентгеновские лучи и удаляющиеся из организма с желчью. С помощью этого метода можно установить появление первых порций желчи в протоках, желчном пузыре, момент выхода пузырной и печеночной желчи в кишку. При дуоденальном зондировании получают фракции печеночной и пузырной желчи.
Секреторная функция кишечника. состав и свойства кишечного сока. Роль в пищеварении. Механизмы регуляции. Полостной и мембранный гидролиз питательных веществ тонком кишечнике. Особенности пищеварения в тонком кишечнике у детей.
Секреторная функция связана с выделением в полость кишечника кишечного сока, играющего большую роль в пищеварении, который является ре-зультатом активной деятельности энтероцитов. Ос-тановимся на секреторной функции тонкого кишеч-ника.
Кишечный сок - секрет, выделяемый железами различных отделов кишечника Кишечный сок на 98% состоит из воды и 2% сухо-го остатка: (рН - 8-8,6), в котором находятся органи-ческие и неорганические вещества. К последним от-носятся бикарбонаты и соли Nа+, К+, Са2+ и др. К ор-ганическим - мочевина, мочевая кислота, аминокис-лоты, слизи и многочисленные ферменты, которые действуют на промежуточные продукты распада, фактически завершая гидролиз. В кишечном соке обнаружено 22 фермента: различные протеазы - лей-цинаминопептидаза, аминопептидаза, карбоксипеп-тидаза, трипептидаза, дипептидаза, кислые катепси-ны, энтеропептидаза и др. Кроме того, в кишечном соке содержатся фосфатаза, фосфорилаза, нуклеаза и др. К амилолитическим ферментам относятся карбо-гидразы - сахараза,
. Среда щелочная 1) Некоторые вещества, содержащиеся в кишечном соке гидролизируют определенные вещества, превращая их в активные ферменты, которые нужны для расщепления остатков непереваренный пищи. 1) кишечная липаза расщепляет жиры 2) ферменты кишечного сока действуют на продукты промежуточного гидролиза питательных веществ 3) защита стенок кишечника от механического воздействия непереваренных остатков пищи (смачивание их) 4) в тонком кишечнике идет окончательное расщепление веществ, продуктов питания и тд Выделение кишечного сока может быть как условным, так и безусловным. Безусловное - выделение секрета кишечника на рефлекторный сокращения желудка Условное - при искусственном создании рефлекса, при котором бы выделялся кишечный секрет. Как правило, преобладает - безусловный рефлекс
Регуляция секреции жидкой части сока осуществляется нервными и гуморальными механизмами. Причем нервная регуляция преимущественно обеспечивается интрамуральными нервными сплетениями кишки - мейснеровым и ауэрбаховым. При поступлении химуса в кишечник он раздражает его механорецепторы. Нервные импульсы от них идут к нейронам сплетений, а затем к кишечным железам. Выделяется большое количество сока богатого муцином. Ферментов в нем мало, так как на слущивание и распад энтероцитов нервные механизмы и гуморальные факторы не влияют. Усиливают выделение сока продукты переваривания белков и жиров, панкреатический сок, желудочный ингибирующий пептид, вазоактивный интестинальный пептид, мотилин. Тормозит соматостатин. Полостное и пристеночное пищеварение.
Пищеварение в тонком кишечнике осуществляется с помощью двух механизмов: полостного и пристеночного гидролиза. При полостном пищеварении
ферменты действуют на субстраты, находящиеся в полости кишки, т.е. на расстоянии от энтероцитов. Они гидролизуют лишь крупномолекулярные
вещества, поступившие из желудка. В процессе полостного пищеварения расщепляется всего 10-20% связей белков, жиров и углеводов. Гидролиз оставшихся связей обеспечивает пристеночное или мембранное пищеварение. Оно осуществляется ферментами адсорбированными на
мембранахэнтероцитов. На мембранеэнтероцита имеется до 3000 микроворсинок. Они образуют щеточную кайму.
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.
Регуляция секреции поджелудочной железы . Секреция поджелудочной железы регулируется нервными и гуморальными механизмами.
Нервная регуляция . И. П. Павлов показал, что раздражение блуждающего нерва вызывает выделение большого количества сока поджелудочной железы , богатого ферментами. Холинергические волокна блуждающих нервов с помощью АХ действуют на М-холинорецепторы панкреацитов. Затем высвобождающиеся ион Са2+ и комплекс ГЦ — цГМФ в роли вторичных мессенджеров стимулируют секрецию панкреоцитами ферментов и гидрокарбонатов. Холинергические нейроны, кроме того, потенцируют секреторные эффекты секретина и ХЦК. Хирургическая ваготомия существенно снижает секрецию поджелудочной железы.
Симпатические волокна, иннервирующие поджелудочную железу через β-адренорецепторы, тормозят ее секрецию , усиливают синтез органических веществ в ней. Адренергические эффекты снижения секреции обеспечиваются также уменьшением кровоснабжения поджелудочной железы путем сужения кровеносных сосудов через их α-адренорецепторы.
Торможение секреции вызывают болевые раздражения, сон, напряженная физическая и умственная работа и др.
Поджелудочная железа имеет также пептидергическую иннервацию. Окончания этих нейронов выделяют ряд нейропептидов, одни из которых стимулируют, другие — тормозят секрецию поджелудочной железы .
Гуморальная регуляция . Первым открытым (и на званным гормоном) явился секретин — стимулятор обильного сокоотделения и секреции гидрокарбонатов. Высвобождение этого гормона в кровь S-клетками двенадцатиперстной кишки происходит при действии на ее слизистую оболочку перешедшего в кишку кислого желудочного содержимого. Секретин стимулирует секрецию в большей мере через соответствующие мембранные рецепторы и вторичные мессенджеры АЦ — цАМФ центроацинозные и протоковые клетки, в меньшей мере — ацинозные клетки, поэтому выделяется секрет с высокой концентрацией гидрокарбонатов и низкой ферментативной активностью.
Вторым гормоном, усиливающим секрецию поджелудочной железы , является холецистокинин (ХЦК). Высвобождение гормона в кровь из ССК-клеток слизистой оболочки двенадцатиперстной и тощей кишки происходит под влиянием пищевого химуса (особенно продуктов начального гидролиза пищевых белков и жиров, углеводов, некоторых аминокислот). Стимулируют высвобождение ХЦК присутствие ионов Са2+ и снижение рН в двенадцатиперстной кишке.
ХЦК действует преимущественно на ацинусы поджелудочной железы , поэтому выделяющийся в ответ на стимуляцию этим гормоном сок богат ферментами. Вторичными мессенджерами являются ионы Са2+ и комплекс ГЦ — цГМФ. Одновременное действие на железу секретина и ХЦК (при приеме пищи) усиливает их стимуляторный эффект. Секретин и ХЦК применяются в клинике как стимуляторы секреции при диагностике заболеваний поджелудочной железы . Пептид химоденин стимулирует секрецию химотрипсиногена.
Секреция поджелудочной железы усиливается также гастрином, серотонином, инсулином, бомбезином, солями желчных кислот. Тормозят выделение поджелудочного сока глюкагон, соматостатин, вазопрессин, вещество Р, АКТГ, энкефалин, кальцитонин, ЖИП, ПП, УУ. ВИП может возбуждать и тормозить секрецию поджелудочной железы .
Фазы секреции поджелудочной железы . Секреция сока поджелудочной железы резко усиливается через 2—3 мин после приема пищи и продолжается 6—14 ч. От количества и качества пищи зависят объем, состав выделяющегося сока, динамика выделения. Чем выше кислотность пищевого содержимого желудка, поступающего в двенадцатиперстную кишку, тем больше выделяется сока поджелудочной железы и тем больше гидрокарбонатов в его составе. Поэтому кривая секреции поджелудочной железы в некоторой мере повторяет кривую желудочного сокоотделения. Отличия кривых секреции желудка и поджелудочной железы определяются в основном буферными свойствами пищи, которая частично нейтрализует кислоту желудочного сока, и скоростью эвакуации содержимого желудка в двенадцатиперстную кишку.
Фазы секреции поджелудочной железы при стимуляции ее приемом пищи те же, что были описаны для желудочной секреции , но в отличие от них более выражены гормональные влияния на поджелудочную железу , особенно в кишечную фазу. Секреция имеет характерную динамику, зависящую от вида принятой пищи (рис. 9.15).
Первая, или мозговая, фаза секреции поджелудочной железы обусловлена видом, запахом пищи и другими раздражителями, связанными с приемом пищи (условнорефлекторные раздражения), а также воздействиями на рецепторы слизистой оболочки рта, жеванием и глотанием (безусловно-рефлекторные раздражения). Нервные импульсы, возникающие в рецепторах, достигают продолговатого мозга и затем по волокнам блуждающего нерва поступают к железе и вызывают ее секрецию .
У человека с фистулой протока поджелудочной железы наблюдали условнорефлекторное выделение сока поджелудочной железы через 2—3 мин после того, как испытуемому говорили о пище, которую ему дадут. В реализации первой фазы секреции принимают участие и регуляторные пептиды, высвобождение которых стимулировалось рефлекторными механизмами блуждающих нервов.
Вторая, или желудочная, фаза характеризуется тем, что секреция во время нее стимулируется и поддерживается путем ваговагального рефлекса с механо- и хеморецепторов желудка и с помощью гастрина.
С переходом желудочного содержимого в двенадцатиперстную кишку начинается третья, или кишечная, фаза секреции поджелудочной железы . В эту фазу секреция стимулируется ваговагальным дуоденопанкреатическим рефлексом, но ведущее значение имеет высвобождение в кровь секретина и ХЦК. Высвобождение их происходит при действии на слизистую оболочку двенадцатиперстной кишки кислого ее содержимого. Чем больше свободных ионов Н+, тем больше высвобождается секретина и тем выше объем сока поджелудочной железы и секреция гидрокарбонатов. Гидрокарбонаты связывают ионы Н+, что приводит к повышению рН среды и уменьшает высвобождение секретина и соответственно объем сока и секрецию гидрокарбонатов. Секреция ферментов в кишечную фазу стимулируется ХЦК и рефлекторно за счет ваговагального рефлекса.
В кишечную фазу велика роль саморегуляции секреции поджелудочной железы по принципу отрицательной обратной связи в зависимости от свойств содержимого двенадцатиперстной кишки. Установлено, что отведение сока поджелудочной железы из двенадцатиперстной кишки вызывает гиперсекрецию поджелудочной железы , обратное введение сока в кишку тормозит эту секрецию . Введение в кишку гидрокарбонатов снижает объем секреции , концентрацию и дебит (выделение) гидрокарбонатов в составе сока. Введение сока поджелудочной железы в двенадцатиперстную кишку особенно выраженно тормозит секрецию поджелудочной железой ферментов. При этом повышение триптической активности химуса двенадцатиперстной кишки тормозит секрецию протеаз, повышение амилолитической активности химуса тормозит секрецию амилазы, повышенная липолитическая активность в наибольшей мере тормозит секрецию панкреатической липазы. Тормозные эффекты ферментов снимаются или снижаются их специфическими ингибиторами и пищевыми субстратами (Г. Ф. Коротько).
Таким образом, свойства секрета поджелудочной железы в кишечную фазу в большой мере определяются соотношением в химусе двенадцатиперстной кишки ферментов и гидролизуемых ими субстратов: избыток ферментов селективно тормозит их секрецию , избыток субстрата снимает эти тормозные влияния, и продукты гидролиза субстрата стимулируют секрецию соответствующих ферментов поджелудочной железой . Этот механизм направлен на срочную адаптацию секреции ферментов поджелудочной железы к виду принятой пищи. Его реализация обеспечивается М-холинергическими и (β-адренергическими влияниями, ХЦК, секретином.
В целом нервные влияния при приеме пищи обеспечивают пусковые воздействия на поджелудочную железу , в последующей коррекции ее секреции большую роль играют гуморальные механизмы. Однако высвобождение гормонов двенадцатиперстной кишкой и действие их на поджелудочную железу более выражены при сохраненной ее иннервации, что подчеркивает единство нервных и гуморальных механизмов регуляции секреции поджелудочной железы . При стимуляции секреции поджелудочной железы усиливается ее кровоснабжение, что важно для поддержания секреции на высоком уровне.
Секреция гуморально корригируется и всосавшимися питательными веществами. Эти влияния осуществляются непосредственно на панкреоциты, выражено влияние на них некоторых аминокислот и глюкозы, опосредуются через центральные нервные механизмы (например, гипоталамический и бульварный центры автономной нервной системы) и регуляторные пептиды.
Влияние пищевых режимов на секрецию поджелудочной железы . Прием пищи вызывает увеличение выделения всех ферментов в составе сока, но для разных видов пищи это увеличение выражено в разной мере. В случае приема пищи с большим содержанием углеводов в наибольшей мере увеличивается секреция амилазы, белков — трипсина и химотрипсина, прием жирной пищи вызывает секрецию сока с более высокой липолитической активностью. Спектр ферментов сока поджелудочной железы срочно адаптируется к виду принимаемой пищи во все три фазы секреции и особенно в кишечную фазу.
Существуют и медленные адаптации секреции ферментов в зависимости от длительного режима питания. Суть адаптации состоит в том, что поджелудочная железа синтезирует и секретирует больше того фермента, который гидролизует преобладающие в рационе питательные вещества. Преобладание в рационе белков повышает выделение в составе сока поджелудочной железы протеаз, преимущественное углеводное питание вызывает увеличение выделения с соком амилазы, а большое количество жира в рационе — выделение с соком липазы.
Эти изменения носят согласованный с изменениями функционирования других отделов пищеварительного тракта характер, составляя часть интегрированных адаптации всего пищеварительного конвейера.
Поможем написать любую работу на аналогичную тему
Слабое сокоотделение натощак резко усиливается во время (через 2— 3 мин) и после приема пищи. Панкреатическое сокоотделение начинается уже на вид, запах пищи как условно-рефлекторный механизме секреции. При раздражении пищевыми веществами рецепторов слизистой оболочки ротовой полости, глотки и пищевода возникает безусловно-рефлекторное отделение панкреатического сока. Нервные импульсы от раздражаемых рецепторов по афферентным путям достигают бульбарного центра панкреатической секреции, где они переключаются на преганглионарные нейроны ядер блуждающего нерва, по эфферентным волокнам которого достигают постганглионарных нейронов. Их аксоны образуют синаптические окончания на базальных мембранах панкреацитов.
Выделяющийся при возбуждении этих окончаний ацетилхолин активирует М-холинорецепторы постсинаптической мембраны.
При раздражении чревных нервов, осуществляющих симпатическую иннервацию поджелудочной железы, ее сокоотделение тормозится (за счет активации р-адренорецепторов медиатором норадреналином). Но торможение секреции сопровождается накоплением секреторного материала в панкреацитах.
Поступление пищи в желудок во время приема пищи вызывает раздражение хемо- и механорецепторов желудка.
Поступление в двенадцатиперстную кишку желудочного содержимого вызывает вместе с дуоденопанкреатическим секреторным рефлексом (с рецепторов слизистой оболочки) выделение из эндокринных клеток гастро-интестинальных гормонов, стимулирующих или тормозящих сокоотделение поджелудочной железой.
Роль основных гуморальных регуляторов выполняют секретин и ХЦК, которые вырабатываются S- и ССК-клетками слизистой оболочки двенадцатиперстной кишки. Секретин и ХЦК усиливают влияние друг друга на панкреоциты, особенно на фоне выделения ацетилхолина в синаптических окончаниях холинергических нервных волокон, иннервирующих железу. Важным гуморальным возбудителем панкреатической секреции является гастрин.
Изменится ли амплитула потенциала действия нервной клетки, если на нее воздейсвовать стимулами сверхпороговой силы
Билет № 5
1.потенциал действия,с графиком, возбудимость,мера возбудимости,
Потенциал действия (ПД) – быстрое изменение мембранного потенциала в ответ на действия раздражителя пороговой силы. ПД имеет стандартные амплитуду и временные параметры, не зависящие от силы стимула - правило "ВСЕ ИЛИ НИЧЕГО".
Начальная деполяризация мембраны под действием раздражителя:
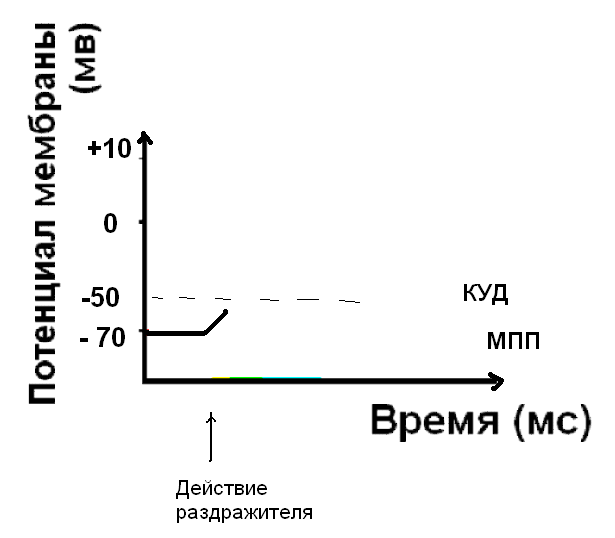
Если сила раздражителя достаточна, чтобы деполяризовать мембрану до КУД, открываются быстрые потенциал-зависимые натриевые каналы. Клетка возбуждена – возник нервный импульс.
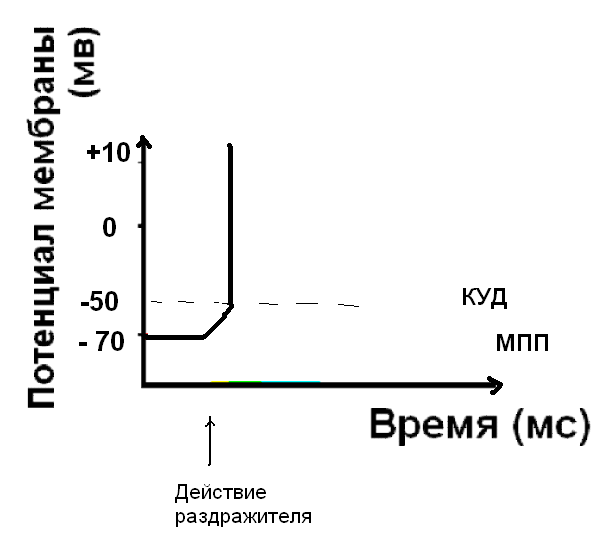
Восстановление мембранного потенциала покоя - реполяризация мембраны.
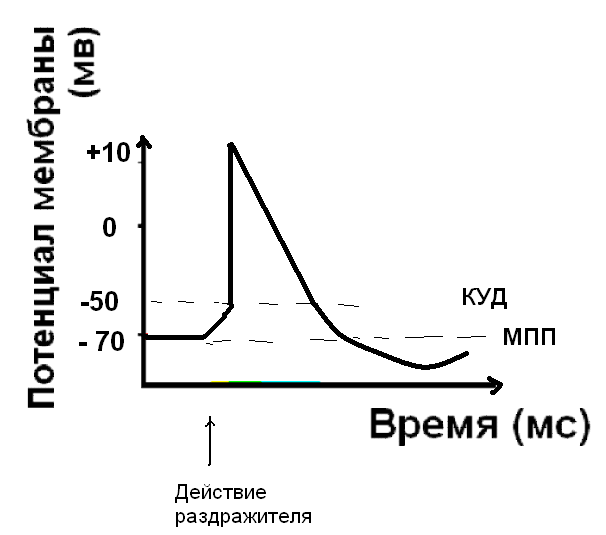
Следующий этап – восстановление мембранного потенциала покоя - реполяризация, обусловлена активным ионным транспортом. Наиболее важен процесс активного транспорта - это работа Na/K - насоса, который выкачивает ионы натрия из клетки, одновременно закачивая ионы калия внутрь клетки. Восстановление мембранного потенциала происходит благодаря току ионов калия из клетки – калиевые каналы активируются и пропускают ионы калия до достижения равновесного калиевого потенциала. Это процесс важен потому, что до тех пор, пока не восстановлен МПП, клетка не способна воспринимать новый импульс возбуждения.
ГИПЕРПОЛЯРИЗАЦИЯ - кратковременное увеличение МП после его восстановления, которое обусловлено повышением проницаемости мембраны для ионов калия и хлора. Гиперполяризация бывает только после ПД.
- Деполяризация мембраны до КУД – могут открыться любые натриевые каналы, иногда кальциевые, и быстрые, и медленные, и потенциал-зависимые, и рецептор-управляемые. Это зависит от вида раздражителя и типа клеток
- Быстрое поступление натрия в клетку - открываются быстрые, потенциал-зависимые натриевые каналы, и деполяризация достигает точки реверса потенциала – происходит перезарядка мембраны, знак заряда меняется на положительный.
- Восстановление градиента концентрации по калию – работа насоса. Калиевые каналы активированы, калий переходит из клетки во внеклеточную среду – реполяризация, начинается восстановление МПП
- Следовая деполяризация, или отрицательный следовой потенциал - мембрана еще деполяризована относительно МПП.
- Следовая гиперполяризация. Калиевые каналы остаются открытыми и дополнительный ток калия гиперполяризует мембрану. После этого клетка возвращается к исходному уровню МПП. Длительность ПД составляет для разных клеток от 1 до 3-4 мс.
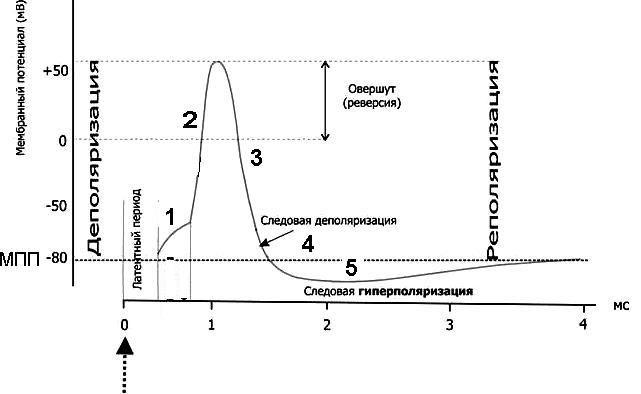
Обратите внимание на три величины потенциала, важные и постоянные для каждой клетки ее электрические характеристики.
- МПП - электроотрицательность мембраны клетки в покое, обеспечивающая способность к возбуждению - возбудимость.
- КУД - критический уровень, величина мембранного потенциала, при достижении которой открываются быстрые, потенциал зависимые натриевые каналы и происходит перезарядка мембраны за счет поступления в клетку положительных ионов натрия. Чем выше электроотрицательность мембраны, тем труднее деполяризовать ее до КУД, тем менее возбудима такая клетка.
- Точка реверса потенциала (овершут) - такая величина положительного мембранного потенциала, при которой положительно заряженные ионы уже не проникают в клетку - кратковременный равновесный натриевый потенциал.
При действии раздражителя подпороговой силы возникает неполная деполяризация - ЛОКАЛЬНЫЙ ОТВЕТ (ЛО). Неполная, или частичная деполяризация – это такое изменение заряда мембраны, которое не достигает критического уровня деполяризации (КУД).
Секреция ПЖ находится под контролем нервных и гуморальных механизмов. Начальную секрецию ПЖ вызывают вид, запах пищи и другие раздражители (условнорефлекторные сигналы), а также жевание и глотание (безусловнорефлекторные сигналы). При этом нервные сигналы, формирующиеся в рецепторах полости рта и глотки, достигают продолговатого мозга, и затем эфферентные влияния по волокнам блуждающего нерва поступают к железе и вызывают её секрецию.
У человека с фистулой ГПП выделение панкреатического сока начинается через 2—3 мин после того, как он увидел пищу или услышат о ней. Это пример условнорефлекторного пути возбуждения панкреатической секреции. Симпатические волокна, иннервирующие ПЖ, тормозят её секреторную активность и в то же время изменяют реактивность железы по отношению к другим воздействиям, усиливая синтез органических веществ.
Торможение панкреатической секреции происходит при раздражении многих чувствительных нервов, при болевых реакциях, во время сна, при напряжённой физической и умственной работе.
Для стимуляции панкреатической секреции прямые нервные влияния имеют меньшее значение, нежели гуморальные. Ведущее значение в гуморальной регуляции секреции ПЖ принадлежит желудочно-кишечным гормонам.
Большинство регуляторов секреции ферментов ПЖ действуют на рецепторы мембраны ацинарных клеток, расположенные на их базолатеральной поверхности. Выделяют рецепторы ХК, бомбезина, ацетилхолина, субстанции Р, ВИП, секретина.
Стимуляторы панкреатической секреции. ВИП и секретин стимулируют панкреатическую секрецию, активируя аденилатциклазу. Как и в других типах клеток, аденилатциклаза способствует образованию циклического аденозинмонофосфата, в результате чего протеинкиназа А, усиливающая секрецию панкреатического сока, богатого бикарбонатами, переходит в активную форму. Другие стимуляторы поджелудочной секреции (ХК, ацетилхолин, гастрин-рилизинг пептид, субстанция Р) действуют на специфические рецепторы, во внутриклеточной передаче сигнала от которых задействованы альтернативные вторичные мессенджеры.
Эти вещества повышают внутриклеточное содержание циклического гуанозинмонофосфата, что приводит к увеличению внутриклеточного содержания инозитолтрифосфата, диацилглицерола, арахидоновой кислоты и кальция. Эти промежуточные вещества-посредники активируют различные протеинкиназы, в результате этого повышается секреция ферментов. Данные, полученные в опытах на животных, свидетельствуют, что действие комбинации агонистов на различные мембранные рецепторы может вызывать синергический, но не суммарный (аддитивный) эффект. Например, ХК увеличивает секрецию бикарбонатов, стимулированную секретином, но секретин не повышает секреторный ответ на действие ХК.
Ингибиторы секреции поджелудочной железы. Различные вещества, ответственные за подавление панкреатической секреции, действуют по принципу отрицательной обратной связи во время и после приёма пищи.
Панкреатический полипептид (ПП) представляет собой пептидный гормон, образующийся в островках Лангерганса и подавляющий панкреатическую секрецию воды, бикарбонатов и ферментов. Концентрация ПП в плазме крови возрастает после мнимого кормления, после приёма пищи, после экспериментального закисления среды ДПК, а также при стимуляции блуждающего нерва, при действии ХК, секретина, ВИП. ПП может выступать как антагонист мускариновых рецепторов и способен ингибировать выделение ацетилхолина из постганглионарных нейронов ПЖ; его конечный эффект проявляется на уровне ацинарных клеток.
Пептид YY высвобождается в дистальной части подвздошной кишки и и толстой кишке в ответ на поступление пищи смешанного характера, по жиры, находящиеся в просвете кишки, в большей степени способны стимулировать его секрецию. Пептид YY уменьшает чувствительность ПЖ к действию секретина и ХК, возможно, за счёт уменьшения секреции ацетилхолина и норадреналина и ингибирования выделения ХК слизистой оболочкой ДПК.
Соматостатин ингибирует секрецию секретина слизистой оболочкой ДПК, а также уменьшает чувствительность к секретину рецепторных полей. Единственный эффект соматостатина — снижение секреции ферментов и бикарбонатов ПЖ. Соматостатин синтезируют клетки слизистой оболочки желудка и кишечника, а также D-клетки островков Лангерганса. Его активность составляет только около 25% от активности гипоталамического соматостатина. Но только соматостатин, продуцируемый слизистой оболочкой тонкой кишки, оказывает угнетающее действие на секрецию ПЖ.
Выделение соматостатина происходит при участии автономной нервной системы в ответ на поступление жиров и аминокислот с пищей.
Соматостатин блокирует панкреатическую секрецию несколькими способами. Во-первых, он действует путём угнетения продукции стимулирующих пептидов (ХК). Во-вторых, посредством угнетающего воздействия на ЦНС и регулируя работу интрапанкреатических ганглиев, соматостатин ингибирует поступление ацетилхолина в пресинаптическую щель и, возможно, ингибирует выработку инсулина. Хотя рецепторы к соматостатину найдены также в ацинарных клетках, эти рецепторы скорее способствуют увеличению секреции, чем блокируют её.
Другие ингибиторы, представленные среди гормонов эндокринных клеток островков Лангерганса, включают панкреатический глюкагон и панкреастатин, а также нейропептиды: кальцнтонин-генерирующий пептид и энкефалины (табл. 1-3). Панкреатический глюкагон ингибирует секрецию ПЖ, стимулированную ХК, секретином или пищей; угнетает секрецию бикарбонатов, воды и ферментов. Панкреастатин ингибирует панкреатическую секрецию, тормозя высвобождение ацетилхолина эфферентными окончаниями блуждающего нерва. Кальцитонин-генерирующий пептид может проявлять свою активность через стимуляцию выделения соматостатина. Энкефалины и подобные им опиоиды снижают выделение секретина слизистой оболочкой ДПК и могут также ингибировать высвобождение ацетилхолина.
Читайте также:


