Нервно мышечная проводимость что это такое
"Препараты, блокирующие нервно-мышечную проводимость"
Что такое препараты, блокирующие нервно-мышечную проводимость?
Это препараты, имеющие общее название "мышечные релаксанты" и нарушающие проводимость в нервно-мышечном синапсе.
Эти вещества вызывают релаксацию скелетных мышц и, таким образом, облегчают интубацию трахеи, помогают при ИВЛ и улучшают условия работы хирургов.
Кроме того, их применяют для снижения энергетической цены дыхания, при лечении эпилептического состояния (хотя они не снижают активность ЦНС), астматического статуса или столбняка, для снижения высокого внутричерепного давления.
Эти препараты нарушают функцию всех скелетных мышц, включая диафрагму, и могут применяться только специально подготовленным персоналом, способным поддержать проходимость дыхательных путей и вентиляцию легких.
Поскольку эти препараты, вызывая полный паралич мышц, не угнетают сознание, показано одновременное применение препаратов седативно-гипнотического или амнестического действия.
Как передается импульс в нервно-мышечном синапсе?
В структуру нервно-мышечного синапса входит пресинаптическое окончание двигательного нерва и постсинаптическая рецепторная зона мембраны скелетной мышцы.
Как только импульс достигнет нервного окончания, в него входит кальций и активизирует ацетилхолин. Последний взаимодействует с холинорецептором, расположенным на постсинаптической мембране.
Каналы рецептора открываются, внеклеточные ионы по градиенту концентрации начинают проникать в клетку и снижают трансмембранный потенциал; распространение этого процесса вдоль мышечного волокна вызывает его сокращение.
Быстрый гидролиз ацетилхолина ацетилхолинэстеразой (истинной холинэстеразой) восстанавливает нормальный градиент концентрации ионов, а в нервно-мышечном синапсе и мышечном волокне - недеполяризированное состояние.
Как классифицируют миорелаксанты?
В соответствии с влиянием на нервно-мышечный синапс выделяют 2 группы препаратов:
Деполяризующие миорелаксанты (сукцинилхолин). Сукцинилхолин действует подобно ацетилхолину, деполяризуя постсинаптическую мембрану нервно-мышечного синапса.
Поскольку рецептор, расположенный на постсинаптической мембране, занят, ацетилхолин не действует.
Недеполяризующие миорелаксанты. Эти препараты вызывают конкурентную блокаду постсинаптической мембраны, и ацетилхолин, изолированный от рецептора, не может вызвать его деполяризацию.
Каков механизм действия сукцинилхолина?
Сукцинилхолин - единственный из деполяризующих миорелаксантов - довольно широко распространен в анестезиологической практике. Он действует подобно ацетилхолину.
Однако, поскольку сукцинилхолин гидролизуется плазменной холинэстеразой (псевдохолин-эстеразой), которой нет в нервно-мышечном синапсе, длительность блокады напрямую зависит от скорости диффузии сукцинилхолина из нервно-мышечного синапса.
Следовательно, деполяризация длится дольше, чем у ацетилхолина. Деполяризация постепенно снижается, но релаксация сохраняется, пока сукцинилхолин фиксирован на рецепторе постсинаптической мембраны.
Каковы показания для применения сукцинилхолина?
Клинические ситуации, когда у пациента полный желудок и существует риск регургитации и аспирации во время анестезии, быстрый паралич и сохранность дыхательных путей от попадания в них желудочного содержимого играют приоритетную роль.
Эти ситуации включают сахарный диабет, диафрагмальную грыжу, ожирение, беременность, выраженный болевой синдром, травму.
Сукцинилхолин обеспечивает самое быстрое начало действия из всех известных ныне миорелаксантов. К тому же, продолжительность сукцинилхолиновой блокады - 5-10 мин.
Функция дыхательных мышц восстанавливается довольно быстро, что очень важно, если больного трудно интубировать (см. вопрос 11).
Если сукцинилхолин действует так быстро и предсказуемо, почему бы не применять его все время?
Сукцинилхолин, в самом деле, действует быстро и предсказуемо и применяется в клинике в течение многих десятилетий. За это время выявлено несколько его побочных действий и связанных с ними опасностей.
Действие сукцинилхолина может быть непредсказуемо продолжительным, если у больного имеется дефицит псевдохолинэстеразы (патология печени, беременность, истощение, злокачественные опухоли).
Сукцинилхолин возбуждает все холинергические рецепторы - никотиночувствительные в вегетативных ганглиях и, что особенно важно, мускариночувствительные в синусовом узле. Поэтому могут развиться все типы аритмий, особенно брадикардия.
Если у пациента имеется пролиферация экстрасинаптических рецепторов, может развиться гиперкалиемия. Экстрасинаптические рецепторы, во-первых, явление аномальное, и, во-вторых, нормальная невральная активность подавляет их.
Однако при ряде ситуаций (например, при ожогах, мышечных дистрофиях, длительной иммобилизации, спинальной травме, поражении мотонейронов, закрытой черепно-мозговой травме) отмечается угнетение двигательной активности и пролиферация экстрасинаптических рецепторов.
Деполяризация таких рецепторов сукцинилхолином может привести к массивному выбросу ионов калия из клеток, выраженной плазменной гиперкалиемии и опасной желудочковой аритмии.
Сукцинилхолин может запустить механизм злокачественной гипертермии, поэтому следует избегать его применения у больных, родственники которых перенесли эту патологию, не говоря уже о них самих.
При внутричерепной гипертензии или открытой травме глаза сукцинилхолин может повысить внутричерепное и внутриглазное давление.
(Вместе с тем, риск подъема давления в указанных полостях необходимо сравнить с риском аспирации у этих больных, и использование сукцинилхолина может быть оправдано).
Сукцинилхолин повышает внутрижелудочное давление, однако рост нижнепищеводного давления более значительный и поэтому риск аспирации не возрастает.
После длительного и массивного (7-10 мг/кг) применения сукцинилхолина характер нервно-мышечного блока может измениться и стать схожим с недеполяризующим блоком.
Это называется развитием II фазы блока, или десенситизирующего блока.
Что должен выяснить анестезиолог у больного с подозрением на риск осложнения после введения сукцинилхолина?
Были ли у пациента или членов его семьи случаи лихорадки или необъяснимой смерти во время анестезий в прошлом.
Не было ли у пациента или членов его семьи необъяснимого плохого самочувствия и слабости после прошлых анестезий или необходимости в проведении ИВЛ после обычных хирургических операций.
Не было ли у пациента или членов его семьи во время прошлых анестезий "кризиса", который невозможно было объяснить существующими медицинскими проблемами.
Не было ли у пациента или членов его семьи лихорадки или выраженной миалгии после физической нагрузки.
Что такое плазменная холинэстераза (псевдохолинэстераза)?
Плазменная холинэстераза вырабатывается печенью, метаболизирует сукцинилхолин, эстеризированные местные анестетики и мивакуриум (недеполяризующий миорелаксант).
Снижение уровня холинэстеразы плазмы, выявленное при печеночной патологии, беременности, злокачественных опухолях, истощении, системных заболеваниях соединительной ткани и гипотиреоидизме, может обусловить продленный сукцинилхолиновый блок.
Объясните важность дибукаинового числа
Псевдохолинэстераза имеет качественную и количественную характеристику, что уточняется пробой с дибукаином. Дибукаин угнетает нормальную псевдохолинэстеразу на 80%, тогда как атипичную псевдохолинэстеразу лишь на 20%. У больных с нормальным метаболизмом сукцинилхолина дибукаиновое число 80.
Если дибукаиновое число 40-60, больного следует отнести к гетерозиготным по атипичной псевдохолинэстеразе, у него будет среднее удлинение сукцинилхолинового блока.
Если дибукаиновое число 20, больной относится к гомозиготным по атипичной псевдохолинэстеразе, у него будет выраженное продление сукцинилхолинового блока.
Важно помнить, что дибукаиновое число - это качественная, а не количественная оценка псевдохолинэстеразы, т.е. у больного с дибукаиновым числом 80 может быть продленный сукцинилхолиновый блок из-за низкой концентрации нормальной псевдохолинэстеразы.
Мой больной прекрасно восстановился после "учебной" анестезии, но жаловался на боли во всем теле. Что произошло
Сукцинилхолин - единственный миорелаксант, вызывающий миалгию. Ее частота колеблется от 10 до 70%. Она чаще всего развивается у лиц мышечного телосложения и амбулаторно оперируемых.
Хотя частота миалгии не зависит от фасцикуляций, частота ее снижается после применения небольших доз недеполяризующих релаксантов, например тракриума 0,025 мг/кг.
Как классифицируются недеполяризующие миорелаксанты?
| релаксанты | ed95, мг/кг | интубационная доза, мг/кг | начало действия после введения интубационной дозы, мин | длительность действия, мин* |
| Коротко действующие | ||||
| Сукцинилхолин | 0,3 | 1,0 | 0,75 | 5-10 |
| Мивакуриум | 0,08 | 0,2 | 1,0-1,5 | 15-20 |
| Рокурониум | 0,3 | 0,6 | 2-3 | 30 |
| Рокурониум | - | 1,2 | 1,0 | 60 |
| Средней длительности | ||||
| действия | ||||
| Векурониум | 0,05 | 0,15-0,2 | 1,5 | 60 |
| Векурониум | - | 0,3-0,4 | 1,0 | 90-120 |
| Атракуриум (тракриум) | 0,23 | 0,7-0,8 | 1,0-1,5 | 45-60 |
| Цисатракуриум | 0,05 | 0,2 | 2 | 60-90 |
| Длительно действующие | ||||
| Панкурониум | 0,07 | 0,08-0,12 | 4-5 | 90 |
| Пипекурониум | 0,05 | 0,07-0,085 | 3-5 | 80-90 |
| Доксакуриум | 0,025 | 0,05-0,08 | 3-5 | 90-120 |
* Продолжительность определяется по восстановлению 25% исходного ответа. ED95 - доза, обеспечивающая угнетение ответа на 95%.
Электронейромиография (ЭНМГ) – инновационный метод исследования функции нервной и мышечной системы, который врачи Юсуповской больницы широко используют в диагностике различных заболеваний. Нейрофизиологи Юсуповской больницы применяют все известные сегодня методы электронейрографии.
Врачи Юсуповской больницы с помощью ЭНМГ выявляют заболевания нервов и мышц на ранних стадиях, когда при клиническом осмотре отклонений ещё не наблюдается, устанавливают уровень поражения нерва. Индивидуальный подход к выбору метода электронейромиографии позволяет провести дифференциальную диагностику между периферическим поражением нерва, нервного корешка и сплетения, оценить тяжесть поражения мышц и периферической нервной системы и мышц, оценить результаты лечения и степень восстановления, характер течения заболевания. С помощью ЭНМГ неврологи определяют причину нарушения мочеиспускания и эректильной дисфункции.
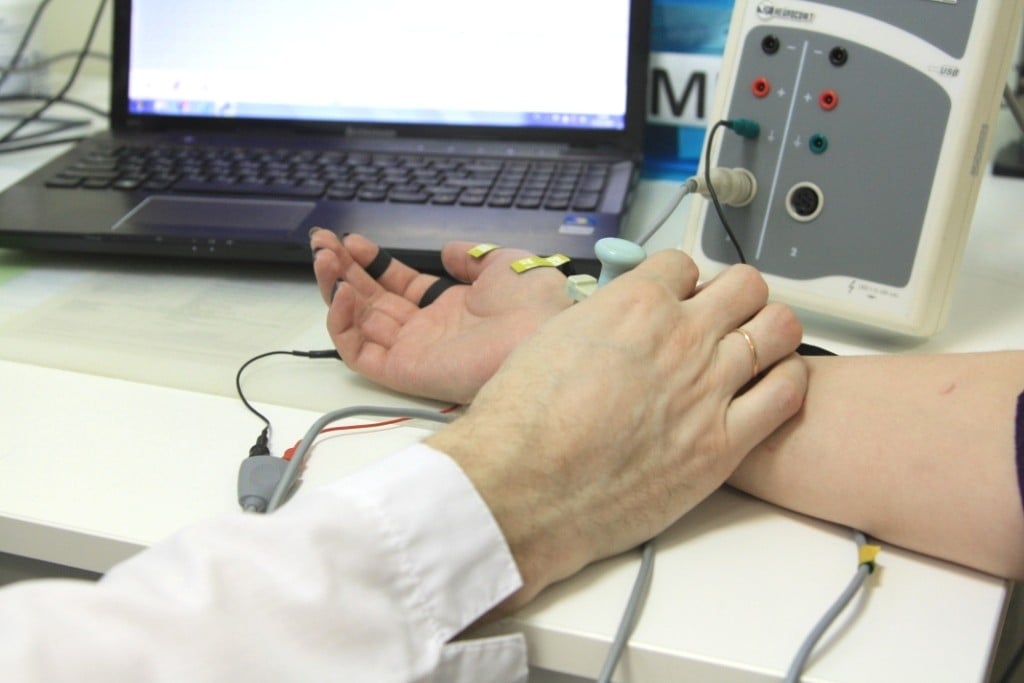
Методики
- компактный;
- молниеносно регистрирует ЭНМГ;
- вызванные потенциалы всех модальностей находятся в базовом комплекте;
- регистрирует электронейромиограмму по мировым стандартам.
Мышечные волокна сокращаются за счёт происходящих в нём электрохимических реакций, в результате чего возникает очень слабый электрический потенциал. Электромиограф усиливает его и выводит в виде кривой на мониторе компьютера. Расшифровав полученный результат, нейрофизиологи определяют, какие патологические изменения имеются в нервах и мышцах.
- моторные – отвечают за работу мышц;
- сенсорные – обеспечивают чувствительность;
- вегетативные – в компетенции которых находится работа внутренних органов.
Нервные корешки выходят из спинного мозга и образуют парные сплетения (шейные, плечевые, поясничные и крестцовые. Они распадаются на периферические нервы. Сенсорные нервы получают информацию от болевых, температурных, тактильных и рецепторов, фиксирующих давление. Моторные нейроны связаны с мышечными волокнами посредством нервно-мышечных синапсов. С помощью синапсов контактируют с внутренними органами и вегетативные нервы.
Патологический процесс может локализоваться на любом уровне – от клетки спинного мозга до нервно-мышечного синапса. Иногда проводимость нервного импульса блокируется за счёт повреждения нерва или его оболочки. Анализ ЭНМГ позволяет найти место повреждения и определить его характер.
Стандартная методика исследования моторных и сенсорных волокон периферических нервов врач проводит согласно алгоритму:
- на кожу над поверхностью мышцы, иннервируемой изучаемым нервом, накладывает электроды;
- подключает их к электронейромиографу;
- фиксирует электрические потенциалы;
- убирает электроды и протирает кожу спиртовым раствором антисептика.
Исследование и анализ состояния большинства крупных нервов не вызывает сложностей. Сплетения образуются из множества периферических нервов. Часто возникает необходимость исследовать каждый из них. ЭНМГ периферических нервов выполняют в Юсуповской больнице.
Игольчатая ЭНМГ применяется для исследования мышц. Процедуру проводят при наличии следующих показаний:
- подозрение на патологию двигательного нейрона спинного мозга;
- заболевания мышц;
- необходимость в определении степени поражения мышцы при неврологической патологии.
Врач вводит тонкую иглу-электрод в исследуемую мышцу, регистрирует электрическую активность мышцы в покое и при умеренном напряжении. Игольчатая ЭНМГ представляет собой более сложный с точки зрения интерпретации метод. Исследование часто занимает больше времени, чем поверхностная электронейромиография.
Показания для исследования функции мышц и нервов
ЭНМГ неврологи назначают при наличии следующих симптомов и синдромов:
Врачи клиники неврологии применяют ЭНМГ для диагностики и мониторинга результативности проводимой терапии пациентам, страдающим боковым амиотрофическим склерозом, диабетической полинейропатией, миастеническим синдромом Ламберта-Итона. Исследование показано больным миастенией, миелодисплазией спинного мозга, миозитом и полимиозитом. Электронейромиография проводится в случае миопатии, неврита тройничного нерва, невропатии лицевого нерва (паралича Белла).
Показанием к ЭНМГ периферических нервов являются следующие заболевания:
- мононевропатия;
- плексопатия, плексит;
- невропатия седалищного нерва;
- полимиалгия, полиневрит;
- радикулопатия при грыже межпозвонкового диска.
Подготовка к процедуре
Электронейромиография не требует особых приготовлений. Невролог предупреждает пациента, что за сутки до исследования необходимо прекратить принимать лекарственных препаратов, которые снижают тонус скелетных мускулов (миорелаксантов), блокируют ацетохинолин (антихолинергиков), влияют на процессы передачи нервных импульсов. В течение 3 дней, предшествующих процедуре, следует исключить приём алкоголя, а в день исследования не курить.
Для того чтобы предотвратить кровоподтёки в местах введения игольчатых электродов, врачи Юсуповской больницы назначают пациентам анализ свёртываемости крови. Если показатели не соответствуют норме, проводят корригирующую терапию. При наличии воспаления или гнойничков кожи в месте введения электродов назначают лечение основного заболевания, а затем делают ЭНМГ. Процедуру не выполняют беременным и кормящим грудью женщинам. Больным эпилепсией и пациентам, страдающим расстройствами психического здоровья, процедуру выполняют после стабилизации их состояния на фоне поддерживающей терапии. Не проводят ЭНМГ пациентам, у которых в организме присутствуют эндопротезы, металлические пластины, стимуляторы сердечной деятельности.
Этапы процедуры и анализ результатов
Перед началом исследования пациента информируют обо всех последующих манипуляциях и о том, что он может чувствовать во время процедуры. Получить точные результаты ЭНМГ врачам Юсуповской больницы позволяет точное соблюдение этапов исследования:
- пациент принимает комфортное положение – сидя или лёжа;
- врач накладывает накожные электроды на определённые точки;
- при проведении игольчатой электронейромиографии вводит в мышцу стерильную разовую иглу-электрод;
- нейрофизиолог направляет к электроду сигнал, который определяет скорость проведения импульса по нервным волокнам и результаты реакции мышц.
Во время обследования пациент может ощущать лёгкое покалывание в местах присоединения электродов. Процедура длится от 30 минут до 1 часа, в зависимости от объёма исследования. ЭНМГ позволяет оценить общее состояние функции периферических нервных волокон, выявить патологические участки нервной и мышечной систем, определить выраженность выявленных нарушений.
В Юсуповской больнице расшифровку результатов ЭНМГ проводят неврологи-нейрофизиологи, кандидаты медицинских наук. Они сверяют полученные показания с нормой, определяют степень отклонения и на основании этих данных ставят диагноз. При поражении периферического нерва скорость проведения импульсов значительно снижена как по чувствительному, так и по двигательному нерву. Амплитуда потенциала действия нерва и ответа иннервируемых мышц в этом случае уменьшена, растянута и имеет изменённую форму.
При наличии диффузного аксонального повреждения изменения скорости незначительны, но хорошо прослеживается снижение амплитуды М-ответа мышцы и потенциала действия нерва. У пациентов с туннельным синдромом и демиелинизирующими заболеваниями нервной системы изменяется скорость проведения возбуждения по нервам. Сегментарные поражения спинного мозга или его передних рогов диагностируют по снижению амплитуды М-ответа, вплоть до полного его исчезновения.
Для того чтобы сделать электронейромиографию периферических нервов, запишитесь на приём к неврологу-нейрофизиологу Юсуповской больницы по телефону. Врач не только проведёт обследование перед процедурой и при отсутствии противопоказаний выполнит исследование, но и проведёт анализ ЭНМГ, установит диагноз и назначит лечение.

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Нарушение нервно-мышечной передачи происходит вследствие дефектов постсинаптических рецепторов (например, при миастении) или пресинаптического высвобождения ацетилхолина (например, ботулизм), а также распада ацетилхолина в синаптической щели (действие лекарственных или нейротоксических препаратов). Типичны флюктуации степени мышечной слабости и утомляемости.
Код по МКБ-10
Болезни, при которых происходит нарушение нервно-мышечной передачи
Синдром Итона-Ламберта развивается при нарушении высвобождения ацетилхолина из пресинаптических нервных окончаний.
Ботулизм - последствие нарушения высвобождения ацетилхолина пресинаптической терминалью из-за необратимого связывания с нею токсина Clostridium botulinum. Среди симптомов выраженная слабость вплоть до нарушений дыхания и признаки увеличения симпатического тонуса из-за блокирования парасимпатической активности: мидриаз, сухость во рту, запор, задержка мочи, тахикардия, чего не бывает при миастении. На ЭМГ умеренное снижение ответа на низкочастотное (2-3 в 1 секунду) раздражение нерва и рост ответа при увеличении частоты раздражения (50 имп/с) или после кратковременной (10 с) мышечной работы.
Лекарства или токсические вещества могут нарушать функцию нервно-мышечного синапса. Холинергические препараты, фосфорорганические инсектициды и большинство нервнопаралитических газов блокируют нервно-мышечную передачу, деполяризуя постсинаптическую мембрану из-за избыточного действия ацетилхолина на ее рецепторы. Результат: миоз, бронхорея, миастеноподобная слабость. Аминогликозиды и полипептидные антибиотики уменьшают пресинаптическое высвобождение ацетилхолина и чувствительность к нему постсинаптической мембраны. На фоне латентной миастении высокие концентрации этих антибиотиков в сыворотке усугубляют нервно-мышечный блок.
Продолжительное лечение пеницилламином может сопровождаться обратимым синдромом, который клинически и по ЭМГ напоминает миастению. Избыток магния (уровень в крови 8-9 мг/дл) чреват развитием выраженной слабости, что также напоминает миастенический синдром. Лечение включает устранение токсического воздействия, интенсивное наблюдение и при необходимости ИВЛ. Для уменьшения избыточной бронхиальной секреции назначают атропин 0,4-0,6 мг внутрь 3 раза/ день. При отравлении фосфорорганическими инсектицидами или нервно-паралитическим газом могут потребоваться более высокие дозы (2-4 мг в/в за 5 мин).
Синдром ригидного человека - это внезапное появление прогрессирующей ригидности мышц туловища и живота, в меньшей степени - конечностей. Других отклонений, в том числе и на ЭМГ, нет. Этот аутоиммунный синдром развивается как паранеопластический (чаще при раке груди, легких, прямой кишки и при болезни Ходжкина). Аутоантитела против нескольких белков, связанных с ГАМК глициновыми синапсами, воздействуют преимущественно на ингибиторные нейроны передних рогов спинного мозга. Лечение симптоматическое. Диазепам существенно уменьшает мышечную ригидность. Результаты плазмафереза противоречивы.
Синдром Исаакса (синонимы: нейромиотония, синдром броненосца) проявляется, главным образом, жалобами на работу конечностей. Появляются миокимии - мышечные фасцикуляции, выглядящие как конгломерат шевелящихся под кожей червей. Другие жалобы: карпопедальные спазмы, интермиттирующие крампи, повышенное потоотделение и псевдомиотония (нарушение расслабления после сильного мышечного сокращения, но без типичного для истинной миотонии нарастания - убывания на ЭМГ). Первоначально поражает периферический нерв, поскольку кураре снимает жалобы, а под общим наркозом симптомы сохраняются. Причина неизвестна. Карбамазепин или фенитоин уменьшают жалобы.
Общие сведения
Нервная система представлена различными нервными сплетениями, периферическими нервами, спинным и головным мозгом. Нейропатия — это поражение нервной системы невоспалительного характера.
Периферические нервы имеют очень тонкую структуру и неустойчивы к воздействию повреждающих факторов. По уровню поражения выделяют:
- Мононейропатию. Характеризуется поражением одного единственного нерва. Мононевропатия считается довольно распространённым вариантом. Чаще всего диагностируется мононевропатия верхней конечности (мононеврит лучевого или локтевого нерва).
- Множественная нейропатия с поражением нескольких нервных окончаний.
- Полинейропатия, для которой характерно вовлечение в процесс нескольких нервов, локализованных в одной зоне.
Патогенез
Нейропатию принято определять характером повреждения нерва и его расположением. Чаще всего патология формируется после травматического повреждения, после перенесенных общих заболеваний и при интоксикации.
Выделяют 3 основные формы нейропатии:
- Посттравматическая нейропатия. Нарушение целостности нервной миелиновой оболочки происходит в результате острой травмы либо сильного удара. При отёке ткани, неправильном формировании рубца и переломе костей происходит сдавливание нервных волокон. Посттравматическая нейропатия характерна для локтевого, седалищного и лучевого нервов.
- Диабетическая нейропатия. Поражение нервных окончаний регистрируется и при высоком содержании в крови сахара и липидов крови.
- Токсическая нейропатия. В результате таких инфекционных заболеваний, как герпес, ВИЧ, дифтерия и др., происходит токсическое поражение нервного сплетения. Отравление химическими соединениями и передозировка некоторых медикаментов может привести к нарушению целостности нервного ствола.
Нейропатия может развиться на фоне заболевания печеночной системы, патологии почек, при остеохондрозе позвоночника, артрите, наличии новообразований и при недостаточном содержании в организме гормонов щитовидной железы.
Классификация
По локализации классифицируют:
Причины
Крайне редко нейропатия развивается как отдельное самостоятельное заболевание. Чаще всего нервные окончания поражаются на фоне хронически протекающей патологии, которая выступает в качестве травмирующего фактора. Развитию нейропатии предшествуют следующие заболевания и состояния:
- гиповитаминоз;
- нарушение метаболизма;
- снижение реактивности;
- интоксикация, отравление;
- травма нервного волокна;
- новообразования (злокачественные и доброкачественные);
- сильное переохлаждение;
- наследственная патология;
- диагностированные эндокринные заболевания.
Симптомы нейропатии
При поражении нервных окончаний происходит истончение мышечных волокон и нарушение их рефлекторной функции. Параллельно отмечается снижение сократительной способности и частичная потеря чувствительности к раздражителям, которые вызывают болевой синдром.
Клиническая картина нейропатии может быть самой разной, а патологический процесс локализоваться в любом месте, вызывая нейропатию малоберцового нерва, тройничного нерва, лицевого нерва, локтевого и лучевого нерва. Поражение чувствительной, двигательной или вегетативной функции нерва отрицательно сказывается на качестве жизни пациента. У пациентов с сахарным диабетом встречается несколько форм нейропатии:
- Периферическая нейропатия. Характерно поражение периферических нервов, которые отвечают за иннервацию верхних и нижних конечностей. Симптомы нейропатии верхних конечностей проявляются в виде нарушения чувствительности в пальцах рук и ног, чувстве покалывания, ощущении онемения верхних конечностей. Симптомы нейропатии нижних конечностей идентичны: отмечаются покалывания и нарушения чувствительности нижних конечностей.
- Проксимальная форма. Характеризуется нарушением чувствительности в основном в нижних конечностях (ягодицы, бедро, голень).
- Автономная форма. Отмечается функциональное нарушение органов мочеполовой системы и органов пищеварительного тракта.
На начальной стадии пациенты предъявляют жалобы на мышечную слабость и парестезии. У каждого второго больного заболевание поражает сначала нижние конечности, а затем и верхние. Бывает и одновременное поражение верхнего и нижнего пояса.
Характерные симптомы алкогольной нейропатии:
- резкое снижение, а в будущем полное отсутствие сухожильных рефлексов;
- диффузное снижение мышечного тонуса.
Алкогольная нейропатия характеризуется нарушением работы и мимической мускулатуры, а в более запущенных случаях отмечается задержка мочеиспускания. В развёрнутой стадии для алкогольной полинейропатии характерно:
- мышечная слабость в конечностях: односторонняя или симметричная;
- парезы и параличи;
- нарушение поверхностной чувствительности;
- резкое угнетение сухожильных рефлексов с последующим их полным угасанием.
Анализы и диагностика
Нейропатия считается довольно сложным для диагностики заболеванием, поэтому так важно грамотно и тщательно собрать анамнез. Трудность заключается в длительном отсутствии определённой симптоматики. Доктору предстоит выяснить: принимались ли медикаменты, переносились ли вирусные заболевания, был ли контакт с некоторыми химическими веществами.
Дебют заболевания может произойти на фоне злоупотребления алкогольсодержащими напитками. Диагноз собирается по крупицам на основании многих факторов. Нейропатия может протекать по-разному: прогрессируя в течение нескольких дней или лет, и даже молниеносно.
При помощи пальпации доктор обследует нервные стволы, выявляя болезненность и утолщение по их ходу. Обязательно проведение пробы Тиннеля. Данный метод основан на поколачивании по нервному окончанию и выявлении покалывания в зоне чувствительной иннервации.
Лабораторно проводится анализ крови с определением СОЭ, измеряется уровень сахара. Дополнительно проводится рентгенографическое исследование грудной клетки. Также выполняется электрофорез сывороточных белков.
Лечение
Терапия поражения нервных окончаний невоспалительного характера носит индивидуальный характер и требует не только комплексного подхода, но и регулярной профилактики.
Методы лечения подбираются в зависимости от формы, степени и причин, которые способствовали поражению нервно-мышечной проводимости. Вся терапия направлена на полноценное восстановление проводимости нерва. При токсическом поражении нервной системы проводятся дезинтоксикационные мероприятия (устранение влияющих факторов, введение антидота).
При диабетической форме рекомендуются мероприятия по поддержанию нормального уровня сахара в крови. Параллельно рекомендуется избавление от вредных привычек. Нарушение метаболизма при сахарном диабете способствует повышению уровня свободных радикалов, циркулирующих в кровяном русле, при нарушенной антиоксидатной активности собственных органов и систем. Всё это ведёт к нарушению целостности внутренней оболочки сосуда и нервного волокна.
При диабетической нейропатии показана применение медикаментов на основе Альфа-липоевой кислоты:
Традиционный неврологический набор подразумевает введение витаминов группы В для полноценного восстановления нервно-мышечной проводимости. Не рекомендуется прибегать к лечению народными средствами.
При посттравматической форме устраняются травмирующие факторы. Назначаются обезболивающие средства, витаминные комплексы, а также медикаменты, усиливающие регенеративную способность и нормализующие обмен веществ.
Эффективно проведение физиотерапевтических процедур.
Лекарства
Лечение нейропатии нижних конечностей включает назначение следующих медикаментов:
- Нейропротекторы или ускорители обмена веществ в нервных клетках. Препараты для лечения:Милдронат; Пирацетам.
- Антихолинэстеразные медикаменты, действие которых направлено на оптимизацию сенсорной работы нервных окончаний. Препараты улучшают нервно мышечную проводимость нижних конечностей. К ним относятся:Прозерин; Ипидакрин.
- Антиоксиданты. Предупреждают негативные последствия от влияния свободных радикалов на работу нервной системы. Высокая концентрация свободных радикалов оказывает разрушающее воздействие на состояние тканей периферической нервной системы. Препараты: Цитофлавин; Мексидол.
- Альфа-липоевая кислота. Препараты способствуют восстановлению нейроцитов, ускоряют метаболизм. Высокая эффективность наблюдается при диабетической нейропатии.
- Иные медикаменты. Хороший эффект даёт применение витаминов группы В, в частности пациентам с нейропатиями показаны В1, В6, В12. Витаминные комплексы способствуют восстановлению нервно-мышечной проводимости. Есть таблетированная и инъекционная форма: Мильгамма; Нейромультивит; Комбилипен.
Не рекомендуется проводить самостоятельное лечение в домашних условиях.
Нейропатическая боль возникает при нарушении передачи импульсных сигналов по нервам. У взрослых нейропатический болевой синдром описывается как колющий, обжигающий, стреляющий и часто ассоциируется с поражением электрическим током.
Терапию начинают с самых простых обезболивающих средств (Ибупрофен, Кетонал). При их неэффективности и сильной выраженности болевого синдрома назначаются антидепрессанты и противоэпилептические средства (например, Тебантин).

Препараты данной группы довольно часто применяются для купирования нейропатической боли. Считается, что механизм их воздействия основан на препятствовании передачи нервных импульсов. Самым часто назначаемым медикаментом является Амитриптилин. Эффект может наступить уже через несколько дней, но в некоторых случаях противоболевая терапия растягивается на 2-3 недели. Максимальный эффект терапии регистрируется на 4-6 неделе интенсивного лечения. Побочным эффектом терапии является сонливость, именно поэтому лечение начинают с самых маленьких доз, постепенно увеличивая дозировку для лучше переносимости. Рекомендуется обильное питьё.
При невозможности применять антидепрессанты назначаются анти-эпилептические средства (Прегабалин, Габапентин). Помимо терапии эпилепсии медикаменты отлично купируют нейропатический болевой синдром. Лечение начинают с самых маленьких доз, идентично терапии антидепрессантами.
Процедуры и операции
Нейропатия малоберцового нерва помимо медикаментозной терапии включает и физиотерапевтические процедуры:
- Магнитотерапия. Основывается на воздействии магнитного поля на организм человека, что способствует купированию болевого синдрома, восстановлению нервных клеток, уменьшению выраженности воспалительной реакции.
- Амплипульс. Основывается на воздействии на поражённую область модулированного тока, благодаря которому происходит восстановление нервных клеток, уменьшается отёчность. Оказывает противовоспалительное воздействие.
- Электрофорез с лекарственными средствами. Основывается на воздействии электрического поля, благодаря чему медикаменты попадают в очаг воспаления.
- Ультразвуковая терапия. При воздействии ультразвука стимулируется кровообращение, уменьшается выраженность болевого синдрома. Оказывает тонизирующее и противовоспалительное воздействие.
- Электростимуляция. Восстановление нервно-мышечной проводимости происходит под воздействием электрического тока.
Аналогично проводится лечение нейропатии лучевого нерва. Для восстановления лучевого нерва также рекомендован курсовой массаж.
Профилактика
Профилактические мероприятия включают своевременное лечение инфекционных и системных заболеваний, нормализацию общего метаболизма. Важно понимать, что патология может приобрести хроническое течение, именно поэтому так важно проведение своевременного и грамотного лечения.
При слабовыраженном течении заболевания и хронической форме нейропатии показано санаторно-курортное лечение, где проводится:
- аромафитотерапия;
- лазерное и световое лечение;
- магнитотерапия;
- массаж, ЛФК;
- иглорефлексотерапия;
- психотерапия.
Последствия и осложнения
Осложнений при периферической нейропатии много и зависят они в первую очередь от причинного фактора, который привёл к поражения нервного ствола. Основные осложнения:
- Диабетическая стопа. Считается одним из самых страшных осложнений сахарного диабета.
- Гангрена. Причиной гнилостного процесса является полное отсутствие кровотока в поражённой области. Патология требует экстренного хирургического лечения: иссечение некротизированных участков, ампутация конечности.
- Автономная сердечно-сосудистая нейропатия. Характерно нарушение различных вегетативных нервных функций, в том числе потоотделение, контроль над мочевым пузырём, частота сердечных сокращений, уровень кровяного давления.
Список источников

Опыт работы: С 2011 по 2014 год работала терапевтом и кардиологом в МБУЗ Поликлиника №33 г. Уфа. С 2014 года работала кардиологом и врачом функциональной диагностики в МБУЗ Поликлиника №33 г. Уфа. С 2016 года работает кардиологом в ГБУЗ Поликлиника №50 г. Уфа. Является членом Российского кардиологического общества.
Читайте также:


