Неврологические осложнения при миеломной болезни

Оглавление диссертации Давтян, Анаит Арташесовна :: 2008 :: Москва
ГЛАВА 1. Нозологическая оценка неврологических осложнений, возникающих у пациентов при лечении множественной миеломы (состояние вопроса по данным литературы)
ГЛАВА 2. Материалы и методы исследования.
ГЛАВА 3. Клинический анализ неврологических нарушений, возникающих у пациентов при проведении лечения множественной ^ миеломы.
ГЛАВА 4. Принципы профилактики и методы коррекции неврологических нарушений, возникающих у пациентов при лечении множественной миеломы
Введение диссертации по теме "Нервные болезни", Давтян, Анаит Арташесовна, автореферат
Миеломная болезнь (множественная миелома - ММ) составляет не более 1,0 % от всех злокачественных опухолей или около 10 - 15% всех случаев онкогематологических заболеваний, однако, у 4 - 5 человек на каждые 100 ООО населения, ежегодно развивается ММ. Наряду с этим, показатели смертности при ММ остаются стабильно высокими, а пятилетняя выживаемость много лет держится на уровне не более 28,0 %. Во многом это обусловлено трудностью диагностики, как следствие, чрезвычайной вариабельностью клинических проявлений и значительной активностью патологического процесса, однако, и лечение ММ, несмотря на достижения современной онкогематологии, остается крайне сложной проблемой [4, 6, 18, 90].
К факторам, оказывающим негативное влияние на эффективность проводимого лечения ММ, относятся многообразные осложнения, нередко возникающие при проведении курса химиотерапии, при этом к осложнениям, значительно отягощающим течение заболевания, в первую очередь относятся различные нарушения со стороны нервной системы.
Так, известно, что отдельные проявления неврологической симптоматики могут быть дебютом ММ, а оссалгический болевой синдром присутствует фактически во всех случаях заболевания, тем не менее, при проведении лечения ММ возможно возникновение целого комплекса неврологических расстройств с вовлечением не только периферического и вегетативного отделов нервной системы, но и ЦНС.
Вместе с тем, на сегодняшний день проблема неврологических осложнений у больных при лечении множественной миеломы остается мало изученной, а в научных публикациях вопросом диагностики и коррекции указанных расстройств уделяется недостаточно внимания [7 ,36, 102].
Поскольку выявленные особенности и уточненный характер нарушений со стороны нервной системы, вероятных при лечении ММ, позволят избрать наиболее адекватную лечебную тактику, предотвращающую их дальнейшее развитие и, тем самым, улучшить качество жизни больных, цель и задачи настоящего исследования представляются актуальными и значимыми.
Цель исследования Определить характер и уточнить клинические особенности осложнений со стороны нервной системы, возникающих у пациентов при лечении миеломной болезни, для возможности их адекватной коррекции.
1. Определить клинические особенности поражения нервной системы, возникающие у пациентов при лечении множественной миеломы.
2. Изучить личностные психологические характеристики и нейропсихологические показатели у пациентов при лечении множественной миеломы.
3. Исследовать состояние церебральной гемодинамики и системной микрогемоциркуляции у пациентов при лечении множественной миеломы.
4. На основе полученных результатов комплексного обследования разработать принципы коррекции осложнений со стороны нервной системы, возникающих у пациентов при лечении множественной миеломы.
5. Оценить эффективность применения разработанных методов профилактики и коррекции осложнений со стороны нервной системы, возникающих у пациентов при лечении множественной миеломы.
Впервые на основании проведенного комплексного обследования у пациентов с ММ выявлен характерный симптомокомплекс клинических проявлений со стороны нервной системы, возникающий при проведении специфического лечения основного заболевания. Показано, что наличие указанных изменений со стороны нервной системы оказывает существенное влияние на эффективность проведения лечения и качество жизни пациентов.
При этом установлено, что в основе нарушений со стороны нервной системы, возникающих при , лечении ММ, лежат реакция на специфическую медикаментозную терапию, при этом преморбидный фон болезни и эмоционально-личностные нарушения являются усугубляющими факторами.
Впервые научно обоснована необходимость всесторонней оценки характера клинических проявлений у пациентов с ММ с позиций возможных предикторов возникновения у них неврологических осложнений при проведении специфического лечения, разработаны основные принципы профилактики и коррекции указанных расстройств.
Полученные результаты исследования расширяют возможности клинической оценки неврологических нарушений, возможных у пациентов при проведении лечения ММ, а, следовательно, важны для их своевременного распознавания, информативны в отношении прогноза, позволяют определить объем и тактику лечебных мероприятий, оптимизировать воздействия, направленные на редукцию и профилактику болезненных проявлений.
Полученные данные обосновывают необходимость внедрения в клиническую практику деятельности врача-онкогематолога диагностических подходов, направленных на выявление у пациентов с ММ нарушений со стороны нервной системы.
Разработанные алгоритм для раннего выявления и прогнозирования, методы коррекции и профилактики нарушений со стороны нервной системы, возможных у пациентов при лечении ММ, могут быть предложены для практического внедрения в ЛПУ, что будет способствовать улучшению качества оказания медицинской помощи.
Основные положения, выносимые на защиту.
1. Пациенты, получающие лечение по поводу ММ, представляют особую группу риска по возникновению у них разнообразных нарушений со стороны нервной системы и эмоционально-личностных расстройств.
2. Снижение резерва адаптации и высокий уровень эмоционально-психологической напряженности, свойственные пациентам, получающим лечение по поводу ММ, могут быть рассмотрены как факторы, способствующие возникновению у данной категории пациентов нарушений со стороны нервной системы.
3. Включение в комплекс специфического лечения основного заболевания у пациентов с ММ антиоксидантных, мембранопротективных, психофармакотерапевтических препаратов и препаратов, нормализующих церебральную гемодинамику, способствует повышению эффективности проводимого лечения.
Диссертационная работа апробирована на заседании кафедры нервных болезней и нейростоматологии ИПК ФМБА России (март 2008 г.). Основные положения и результаты исследования по теме диссертации доложены на 2 научно-практических конференциях.
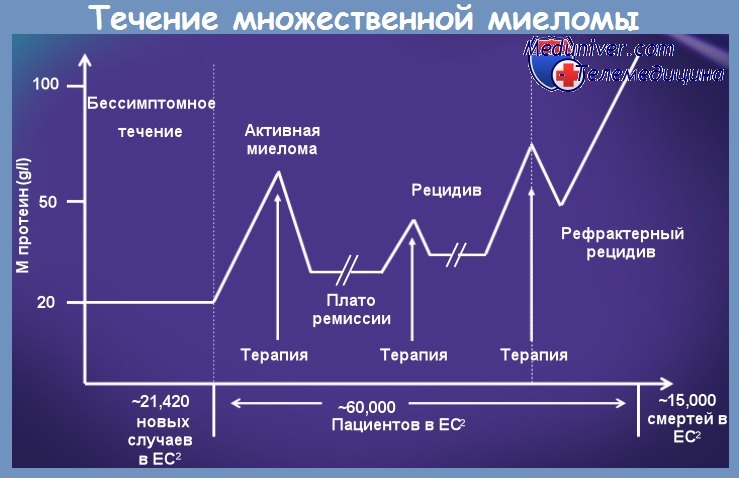
Выживаемость больных с множественной миеломой варьирует от случая к случаю, причем некоторые из них имеют очень скоротечную эволюцию (несколько месяцев), в то время как другие — 10—12 лет. Этим подразумевается выживаемость с момента постановки диагноза, так как доказано, что миелома имеет очень длительную эволюцию до клинической фазы, но которую до сих пор было невозможно обнаружить.
Среднее выживание больных с множественной миеломой, нелеченных или леченных уретаном длится приблизительно 7 месяцев (Osgood, Holland). Новые терапевтические средства привели к значительному увеличению жизненного срока. Большие статистики показывают выживаемость в 18—21 месяцев (Alexaninan и сотр., Medical Research Council, Bergsagel, George и сотр.). В статистике Бухарестского Института Внутренней Медицины, средняя выживаемость равняется 20 месяцам (Вегсеапг. и сотр.).
Делались попытки установить связь между секретируемой формой Ig и выживаемостью. Повидимому при миеломе IgD наблюдается более низкая средняя выживаемость — 60% больных умирают в течение первого года болезни (Jancelewicz). Протеинурия Бене-Джонса типа ламбда оказывает отрицательное влияние на эволюцию (Acute leukaemia Group В), факт, оспариваемый однако Witts и сотр..
Эффективным показателем эволюции является уровень мочевины в крови до лечения; так, больные, которые подвергаются первому курсу лечения, имея мочевину ниже 40 мг/100 мл сыворотки выживают в среднем 33 месяцев, в то время как пациенты, у которых в момент начала первого курса лечения, уровень мочевины в сыворотке превышает 80 мг/ 100 мл, выживают в среднем лишь 2 месяца (Medical Research Council).
Эволюция множественной миеломы характеризуется периодами обострения и ремиссий. Вместе с развитием болезни во времени, боли усиливаются, приковывая больного к постели; к этому могут ассоциироваться параплегии вследствие позвоночных провалов. В конечной фазе наступает кахексия с суровой анемией и почечной недостаточностью.
До настоящего времени прогноз множественной миеломы остается неблагоприятным, а единственно известные излечения относятся к единичной плазмоцитоме, оперированной в начальной стадии.
Почечные осложнения множественной миеломы бывают чрезвычайно часто в течение множественной миеломы: они встречаются в 40% случаев. Их тяжесть варьирует от простых протеинурий до почечной недостаточности и уремической комы. Азотемия при множественной миеломе не сопровождается артериальной гипертензией.
У больных с миеломой цитируются случаи острой почечной недостаточности, вызванной обычно производством урографии (Myers и Witten). Главным разрешающим фактором является дегидратация, которая связана с урологическим исследованием.
На уровне мочевых путей часто происходят отложения кальция, которым способствует гиперкальцемия, гиперкальциурия, протеинурия, а также и изменение мочевого рН благодаря инфекциям.
Неврологические осложнения множественной миеломы происходят часто и бывают разнообразными. На первом плане стоят осложнения по поводу компрессий (10—30% случаев, согласно Silverstein и Doniger). Они вызваны позвоночными переломами и провалами, которые влекут за собой парезы и параличи. Их число повидимому возросло за последние годы, вероятно вследствие продления эволюции болезни в результате соответствующих лечений.
Туморальные инфильтраты, амилоидные или протеиновые, на уровне нервных корешков или же по протяжению периферических нервов могут порождать явления радикулитов или невритов и являются иногда первыми признаками болезни. Более редким неврологическим осложнением (6% случаев, согласно Cohen и Bundles) является периферическая невропатия, несвязанная с костными повреждениями или туморальными инфильтратами. Она может появляться и в случаях единичной плазмоцитомы и исчезает в результате местного лечения болезни.
Мочевым инфекциям, которые возникают также часто, благоприятствует наличие камней в почках и почечной недостаточности.
Миеломная болезнь – один из видов рака крови, злокачественное перерождение плазматических клеток (дифференцированных В-лимфоцитов, подвида лейкоцитов, являющихся частью иммунной системы и синтезирующих антитела, помогающие организму в борьбе с инфекциями). В норме в костном мозге вырабатываются плазматические клетки (плазмоциты) и В-лимфоциты в необходимом организму количестве. В какой-то момент этот процесс дает сбой, и вместо нормальных клеток начинают продуцироваться атипичные (опухолевые) плазмоциты, которые постепенно замещают собой нормальные клетки в костном мозге. Вместо антител такие клетки вырабатывают парапротеины, белки, которые повреждают почечную ткань.
При миеломной болезни возникают множественные опухолевые очаги, прежде всего, в костном мозге, но также в костях (чаще плоских, таких как черепные кости и ребра, но также могут повреждаться и трубчатые, в частности, бедренная кость), лимфатических узлах и других органах. Множественностью поражений обусловлено другое название миеломной болезни – множественная миелома. Поскольку опухолевые клетки продуцируют парапротеин, что относит заболевание к парапротеинемическим гемобластозам, злокачественным иммунопролиферативным заболеваниям.
В основном миеломной болезни подвержены люди пожилого возраста – 70 лет и старше, хотя изредка заболевают и молодые люди до 40 лет, мужчины несколько чаще женщин (соотношение заболевших мужчин и женщин – 1,4:1). По неустановленной причине эта болезнь у людей негроидной расы возникает в два раза чаще, чем у любой другой.
Множественная миелома – неизлечимое заболевание с хроническим течением, однако, хотя полное излечение современными медицинскими средствами недостижимо, лечение позволяет достигать многолетней ремиссии, во время которой люди живут полноценной жизнью.
Синонимы: множественная миелома (ММ), плазмоцитома, болезнь Рустицкого – Калера (по имени ученых, впервые описавших заболевание).
Код миеломной болезни по МКБ 10 – C90 (множественная миелома и злокачественные плазмоклеточные новообразования).
Причины и факторы риска
Причина, по которой происходит озлокачествление плазматических клеток, не установлена. Предположительно, имеет место генетическая предрасположенность. В качестве мутагенных факторов могут выступать вирусные инфекции, ионизирующая радиация (в том числе лучевая терапия), канцерогены, цитостатические препараты (химиотерапия), хроническая интоксикация. У 10% людей, страдающих моноклональной гаммапатией, она трансформируется в миеломную болезнь.
К предрасполагающим факторам относятся все то, что оказывает подавляющее действие на иммунную систему: ожирение, вредные привычки, нездоровый образ жизни, стрессонеустойчивость и т. д.
Формы
Существует несколько классификаций ММ.
По клиническим проявлениям:
- симптоматическая;
- бессимптомная (тлеющая);
- моноклональная гаммапатия неопределенного значения (MGUS, Monoclonal gammopathy of undetermined significance).
По клеточному составу:
- пламоцитарная;
- плазмобластная;
- полиморфноклеточная;
- мелкоклеточная.
В зависимости от распространенности очагов:
- очаговая;
- диффузно-очаговая;
- диффузная.
В зависимости от типа продуцируемого парапротеина:
- G-миелома (75% всех случаев);
- А-миелома;
- D-миелома;
- Е-миелома;
- миелома Бенс-Джонса;
- М-миелома;
- несекретирующая (последние две относятся к редким формам).
- медленно прогрессирующие;
- быстро прогрессирующие.
- множественно-очаговая;
- диффузно-поротическая;
- изолированная.
- очаговая;
- узловатая;
- сетчатая;
- остеолитическая;
- остеопоротическая;
- смешанная.
Стадии заболевания
В протекании множественной миеломы выделяют три стадии:
- Начальная.
- Развернутая.
- Терминальная.
Существует несколько критериев для их определения.
Международная система стадирования (ISS, International Scoring System) ориентирована на количество бета-2 микроглобулина (β2M) и альбумина в сыворотке крови:
- β2M 100 г/л; кальций крови – норма; сывороточный парапротеин 120 мг/л; сывороточный парапротеин >70 г/л для IgG, и > 50 г/л для IgA; экскреция белка Бенс-Джонса с мочой > 12 г/сутки; три или более очага остеолизиса (для определения III стадии достаточно соблюдения лишь одного из перечисленных критериев).
Каждая из трех стадий классификации Дьюри – Салмона делится на подстадии А и В в зависимости от содержания сывороточного креатинина, который служит показателем функции почек:
- Креатинин 2 г/дл (> 177 мкмоль/л).
Симптомы миеломной болезни
Прежде чем появятся первые симптомы, заболевание длительно бессимптомно прогрессирует (этот период может составлять от 5 до 15 лет). В это время в анализе крови может быть обнаружена высокая РОЭ, парапротеинемия, а в анализе мочи – протеинурия. Но поскольку количество плазматических клеток в костном мозге не увеличено, диагноз поставить невозможно.
Развернутая стадия характеризуется появлением и нарастанием симптоматики, которая проявляется целым рядом синдромов, которые у разных пациентов имеют разную степень выраженности.
Симптомы связаны как с очаговым опухолевым ростом плазматических клеток в виде костных опухолей, так и с тем, что плазмоциты синтезируют вещества, способствующие лизису, т. е. разрушению костной ткани. В первую очередь, страдают плоские кости (кости таза, черепа, лопатки, ребра, позвоночник), реже – трубчатые кости (бедренная, плечевая). В результате появляется интенсивная боль в костях, усиливающаяся при надавливании, во время движения, появляются патологические (не вызванные травмой) переломы костей, костные деформации.
Поражение кроветворной системы
Лейкопения, тромбоцитопения, плазмоциты в периферической крови, повышение РОЭ, в миелограмме содержание плазмоцитов > 15% (при некоторых формах ММ миелограмма может не иметь отклонений от нормы).
Синдром белковой патологии
Обусловлен гиперпродукцией парапротеинов (патологических иммуноглобулинов или белка Бенс-Джонса), что сопровождается гиперпротеинемией (проявляется жаждой, сухостью кожи и слизистых оболочек), протеинурией, появлением холодовых антител (проявляется холодовой аллергией, акроцианозом, трофическими нарушениями в конечностях), амилоидозом (проявляется нарушением функционирования тех участков организма, где произошло отложение амилоида, увеличением губ и языка).
Наблюдается у 80% пациентов с ММ, характеризуется развитием хронической почечной недостаточности, что проявляется слабостью, тошнотой, снижением аппетита, потерей массы тела. Не характерны отеки, асцит, гипертензия (один из диагностических признаков).
В результате опухолевой плазмоклеточной инфильтрации во всех внутренних органах развиваются поражения печени, селезенки (чаще), желудочно-кишечного тракта, плевры (реже) с развитием характерной симптоматики.
Подверженность инфекциям, обычные респираторные вирусные заболевания носят тяжелый характер, часто осложняются присоединением бактериальной инфекции, нередки инфекционно-воспалительные заболевания мочевыводящих путей, опоясывающий лишай, грибковые поражения.
Повышение вязкости крови
Характеризуется нарушением микроциркуляции, что проявляется ухудшением зрения, мышечной слабостью, головной болью, развитием трофических поражений кожи, тромбозами. Наблюдается у 10% пациентов с ММ.
Развивается вследствие снижения функциональности тромбоцитов и активности факторов свертывания крови. Проявляется кровоточивостью десен, носовыми кровотечениями, множественными гематомами.
Обусловлен плазмоклеточной инфильтрацией твердой мозговой оболочки, деформацией костей черепа и позвонков, сдавлением нервных стволов опухолями. Проявляется периферической нейропатией, мышечной слабостью, ухудшением всех видов чувствительности, парестезиями, снижением сухожильных рефлексов и др. симптомами в зависимости от области поражения.
Обусловлена вымыванием кальция из костной ткани вследствие лизиса. Проявляется тошнотой, рвотой, сонливостью, расстройствами сознания, потерей ориентации.
Для терминальной стадии характерно обострение имеющейся симптоматики, быстрое разрушение костей, прорастание опухолей в соседние ткани, нарастающая почечная недостаточность, тяжелая анемия, инфекционные осложнения.
Диагностика миеломной болезни
Основные признаки множественной миеломы – костномозговой плазмоцитоз (> 10%), очаги остеолизиса, М-градиент (моноклональный протеин) или белок Бенс-Джонса в сыворотке или моче. Именно по этим признакам идет диагностический поиск при подозрении на заболевание, причем для диагноза достаточно установления плазмоцитоза и М-градиента (или белка Бенс-Джонса) вне зависимости от наличия костных изменений.
Применяются следующие методы диагностики:
- Рентгенография черепа, грудной клетки, таза, позвоночника, плечевого пояса, плечевых и бедренных костей.
- Спиральная компьютерная томография.
- Магниторезонансная томография.
- Позитронно-эмиссионная томография.
- Аспирационная биопсия костного мозга с целью определения миелограммы.
- Лабораторные анализы крови и мочи.
- Цитогенетическое исследование.
Костные и внекостные поражения при миеломной болезни обозначаются аббревиатурой CRAB:
- С – Calcium (кальций) – гиперкальцемия, содержание Са > 2,75;
- R – Renal (почечные) – нарушения почечной функции, креатинин сыворотки > 2 мг/дл;
- A – Anaemia (анемия) – нормоцитарная и нормохромная, гемоглобин

Образование: Ростовский государственный медицинский университет, специальность "Лечебное дело".
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
Миелома позвоночника – это не совсем верный термин. Есть такое заболевание, которое называется миеломная болезнь. Она развивается в результате злокачественного перерождения предшественников лимфоцитов. В результате образуется клон злокачественных клеток, который постепенно распространяется по всему организму, поражая костный мозг и внутренние органы.
- Причины заболевания
- Механизм прогрессирования заболевания
- Ранние признаки миеломы позвоночника
- Диагностика
- Лечение
- Дает ли миелома позвоночника метастазы?
- Прогноз выживаемости
- Осложнения
- Ремиссия
Поражение позвоночника при миеломе может быть представлено двумя вариантами:
- Единичный очаг остеодеструкции. В этом случае речь идет о солитарной плазмоцитоме.
- Множественные очаги остеодеструкции. Картина соответствует множественной миеломе.
Ряд авторов считает солитарную плазмоцитому ранней стадией развития множественной миеломы, поскольку у большинства больных она со временем диссеминирует по всему организму даже на фоне, казалось бы, радикального излечения.
Поражение костей при миеломе – это неизбежный процесс, который на поздних стадиях заболевания сопровождает каждого больного. При этом отмечаются следующие признаки:
- Остеолизис — расплавление костной ткани.
- Остеопороз — снижение плотности костной ткани.
- На фоне остеолизиса и остеопороза неизбежно возникают патологические переломы — нарушение целостности кости без воздействия выраженного травмирующего фактора.
- Гиперкальциемия — увеличение содержания ионов кальция в крови за счет его выхода из костной ткани.
Причины заболевания
Миелома развивается из-за злокачественного перерождения В-лимфоцитов, точнее их предшественников. Что вызывает эти мутации, не ясно, но есть некоторые закономерности, на фоне которых вероятность развития заболевания увеличивается по сравнению с общей популяцией людей. Эти закономерности называют факторами риска. Для миеломы это:
- Возраст старше 40 лет.
- Мужской пол.
- Негроидная раса.
- Наличие иммунодефицитных состояний, причем как врожденных, так и приобретенных: ВИЧ, лечение цитостатиками, необходимость приема иммуносупрессивной терапии при трансплантации органов и др.
- Наличие миеломы у близких родственников.
- Воздействие радиации, в том числе и лучевая терапия при лечении онкологии.
- Моноклональная гаммапатия.
Механизм прогрессирования заболевания
Механизмы прогрессирования солитарной плазмоцитомы во множественную миелому до конца не изучены ввиду редкости данной патологии. Тем не менее, есть основания полагать что трансформацию вызывает нестабильность генома, когда случайные генетические поломки приводят к тому, что нарушается процесс дифференцировки плазматических клеток, блокируется механизм апоптоза и они начинают бесконтрольно делится и размножаться.

Ранние признаки миеломы позвоночника
На ранних этапах поражения позвоночника симптомы могут отсутствовать, и заболевание обнаруживается случайно, при обследовании по другому поводу. Первым признаком являются боли. Сначала они не интенсивны и не постоянны. Чаще всего, локализуются в области поясницы и грудного отдела. Симптоматика имеет неспецифический характер, поэтому больным часто выставляют неверный диагноз, типа остеохондроза, радикулитов или невралгии.
По мере прогрессирования заболевания, усиливается разрушение костной ткани, что приводит к нарастанию симптоматики. Боли в позвоночнике становятся постоянными, усиливаются от малейшего движения. В некоторых случаях миелома манифестирует с внезапной острой боли, которая возникает из-за патологических переломов. В ряде случаев последние осложняются компрессионным сдавлением спинного мозга и его корешков.
В целом интенсивность болей находится в прямой зависимости от опухолевой массы. Чем больше злокачественных клеток, тем сильнее деструкция костной ткани, соответственно более ярче выражены симптомы.
При очаговой миеломе неврологическая симптоматика в основном развивается на фоне сдавления опухолевой массой нервных корешков и спинного мозга. При этом будут наблюдаться парезы и параличи, в зависимости от уровня поражения. Второй причиной развития неврологических симптомов являются патологические переломы позвонков.
При трансформации во множественную миелому, неврологические осложнения обнаруживаются у 10-40% больных. Они связаны как с неопластическим действием опухоли на нервные ткани, так и с побочным влиянием химиотерапии, применяющейся для специфического лечения. При этом может поражаться как центральная, так и периферическая нервная система:
- Вегетативная дисфункция — головокружение, быстрая утомляемость, тошнота, тахикардия, нарушения сна и др.
- Пирамидальная недостаточность — нарушается деятельность мышц, снижается их двигательная активность и тонус, постепенно это приводит к атрофическим изменениям. Могут быть клонические судороги.
- Мозжечковая недостаточность — нарушение координации движения, выраженное в виде непроизвольных мышечных сокращений (хорея, миоклонии), нарушение мимики, речи и интеллекта, тремор головы и конечностей.
Под действием опухолевых клеток, в ткани кости возникают очаги деструкции. Во-первых, это связано с непосредственным замещением костной ткани опухолью. Во-вторых, злокачественные клетки выделяют вещества, которые подавляют деятельность остеобластов (клеток, отвечающих за репарацию костного вещества) и активируют действия остеокластов, которые наоборот, приводят к разрушению кости за счет растворения ее минеральной составляющей.
Диагностика
Для постановки диагноза необходимо проведение комплексного обследования, включающего ряд инструментальных исследований.
Анализ крови и мочи
В общем анализе крови часто обнаруживается нормохромная, реже – макроцитарная анемия. Характерным признаком является увеличение СОЭ, у некоторых пациентов оно может превышать 100 мм/час. При обширном поражении костного мозга выявляется нейтропения и тромбоцитопения.
В общем анализе мочи обнаруживается нарастающая протеинурия, которая связана с прогрессированием нефропатии. При специальных исследованиях обнаруживается специфический белок — М-белок, М-градиент, белок Бенс-Джонса.
В миелограмме (изучение образца костного мозга под микроскопом) обнаруживается увеличение содержания плазматических клеток. Диагноз миелома выставляется, если количество плазмоцитов превышает 10%.
Лечение
Большинство больных с миеломой позвоночника проходят лечение с помощью лучевой терапии в суммарной дозе 40 Гр, поскольку миеломные клетки очень чувствительны к ионизирующему излучению. При размере опухоли более 5 см, дозу могут увеличить до 50Гр. Поле облучения должно включать минимум по одному непораженному позвонку сверху и снизу от места локализации опухоли. Признаками эффективности лечения является склероз и реминерализация очага поражения.
При лечении множественной миеломы с поражением позвоночника, облучение применяется в рамках паллиативной терапии для облегчения болевого синдрома и замедления остеолизиса.
Хирургическое лечение показано пациентам с функциональной нестабильностью позвоночника и при наличии неврологической симптоматики. В ряде случаев, при наличии показаний, пациенту предлагают провести операцию превентивно, не дожидаясь патологических переломов. В рамках лечения применяются различные виды вертебропластики.
Применение химиотерапии для пациентов с солитарной плазмоцитомой остается спорным моментом. А вот для пациентов с множественной миеломой с поражением позвоночника, это ключевой метод лечения. Большие успехи были достигнуты при включении в протоколы талидомида, леналидомида и бортезомиба:
- Бортезомиб — ингибитор протеасом – ферментов, которые играют важную роль в поддержании гомеостаза клетки, ее росте и размножении. Подавление действия протеасом блокирует селективный протеолиз, что влияет на многие внутриклеточные процессы, в том числе на передачу сигналов. Все вместе это приводит к гибели клетки. Помимо этого, экспериментально было подтверждено, что бортезомиб усиливает активность остеобластов и подавляет функции остеокластов у больных с миеломой.
- Талидомид — препарат, оказывающий иммуномодулирующее, антиангиогенное и цитотоксическое действие. Предпосылкой к применению данного препарата послужили данные о том, что у больных с миеломой в костном мозге обнаруживается усиление ангиогенеза, что способствует пролиферации и рассеиванию злокачественных клеток. При дальнейших испытаниях было выявлено, что помимо антиангиогенного действия, препарат вызывает клеточный апоптоз. В настоящее время талидомид применяется у больных, лечение которым еще не назначалось, при рецидивах после предыдущих курсов химиотерапии, а также у больных, резистентных к другим видами препаратов. Может применяться как в качестве монотерапии, так и в схемах полихимиотерапии.
- Леналидомид. С точки зрения структуры, аналогичен талидомиду, но оказывает более выраженное биологическое действие. Наибольшую эффективность показал при терапии гемопоэтических опухолей, особенно при наличии мутаций 5 хромосомы.
Пациенты с костными миеломами, в том числе с миеломой позвоночника являются сложной категорией больных, сложно поддающихся терапии. Поэтому им по возможности назначаются 4-5 компонентные схемы химиотерапии, например, VDCR или VD-PACE, которые имеют в своем составе бортезомиб.
Дает ли миелома позвоночника метастазы?
К сожалению, все имеющиеся на сегодняшний день методы терапии солитарной плазмоцитомы не гарантируют полного излечения. Могут развиваться рецидивы, которые локализуются как вне пределов первичной опухоли, так и на месте бывшего очага. Реже поражаются регионарные лимфатические узлы.
Также очаговая миелома (плазмоцитома) может трансформироваться в миеломную болезнь. У половины больных, трансформация обнаруживается в течении 5 лет после лечения плазмоцитомы, и у 72% – в течение 10 лет. Среднее время до прогрессирования составляет 2 года, но могут быть существенные различия. Ключевым моментом является возраст больного – чем он старше, тем выше риск трансформации.
Прогноз выживаемости
При хороших результатах лечения первичной опухоли и отсутствии трансформации в множественную миелому, прогнозы относительно неплохие. Общая пятилетняя выживаемость таких больных составляет 74%, 10-летняя 34-54%. Главным фактором, влияющим на выживаемость, является возраст больного. Для пациентов младше 60 лет, прогноз более благоприятный.
Осложнения
Основными осложнениями миеломы позвоночника являются компрессионные переломы со сдавлением спинного мозга и спинномозговых корешков. При этом развиваются выраженные боли, парезы и параличи. Для устранения таких осложнений применяются реконструктивные хирургические вмешательства.
Ремиссия
О достижении ремиссии свидетельствует склероз и реминерализация опухолевого очага. Все пациенты, прошедшие лечение по поводу очаговой плазмоцитомы, должны находиться под пожизненным медицинским наблюдением, поскольку всегда сохраняется вероятность прогрессирования заболевания во множественную миелому.
Читайте также:


