Синдром печеночно-клеточной недостаточности печеночная энцефалопатия
Данное состояние характеризуется быстрым отмиранием нейронов из-за тяжелой гипоксии (кислородное голодание) либо прямого влияния нейротропных токсинов и лучевого воздействия. Понятие печеночной энцефалопатии (ПЭ) подразумевает нервно-психические расстройства на фоне поражения ЦНС, возникшие в связи с неспособностью гепатоцитов очищать кровь от отравляющих веществ, в частности от аммиака.
В результате развивается сильная интоксикация, которая может привести к необратимым нарушениям и летальному исходу.
Что это такое?
Простыми словами, печеночная энцефалопатия – это органическое поражение головного мозга из-за нарушений работы печени. Проявляется снижением умственных способностей, депрессивным состоянием, расстройством личности.
Почему развивается болезнь?
Сказать точно, почему развивается печеночная энцефалопатия, ученые до сих пор не могут. Существует три теории, объясняющие, почему при отмирании ткани печени нарушается деятельность мозга, и каждая из них имеет убедительные доказательства:
Острое или хроническое поражение печени, приводящее к повреждению мозговой ткани, провоцируются такими факторами:
- печеночная недостаточность;
- вирусный, алкогольный гепатит;
- злоупотребление лекарствами;
- цирроз печени;
- гепатоцеллюлярная карцинома;
- дисбактериоз кишечника;
- злоупотребление белковой пищей;
- фиброз печени;
- алкогольная зависимость;
- частые запоры;
- глистные инвазии;
- желчнокаменная болезнь;
- аутоиммунные нарушения;
- перитонит на фоне брюшной водянки;
- послеоперационные осложнения;
- инфекционные болезни;
- кровотечения из желудка.
Энцефалопатия появляется при патологических состояниях, которые сопровождаются гепатоцитолизом – массовой гибелью печеночных клеток (гепатоцитов).
Симптомы и первые признаки
В клинических проявлениях различают неврологические нарушения и расстройства психики. К характерным проявлениям энцефалопатии относят астериксис – крупноразмашистые подергивания конечностей. Появляются из-за тонического напряжения мышц на фоне нарушения функций нервной системы.
Общие признаки печеночной энцефалопатии:
- фиксация взгляда;
- пространственная дезориентация;
- бессонница;
- монотонность речи;
- забывчивость;
- тревожность;
- печеночный тремор;
- снижение интеллекта;
- безучастность;
- нарушение речи и письма;
- понижение температуры тела;
- обмороки;
- отсутствие полового влечения.
Заторможенность, сонливость, бессонница – первые признаки патологии. В связи с нарушением метаболизма появляется неприятный запах изо рта. На декомпенсированной стадии пациенты становятся агрессивными или апатичными, неадекватно реагируют на окружающую обстановку.
На предпоследней (терминальной) стадии происходит угнетение ЦНС. Больные не реагируют на раздражающие факторы, кроме боли. В коматозном состоянии нередки сильные судороги, которые спровоцированы гипертонусом мышц. На стадии комы 9 из 10 пациентов погибают, не приходя в сознание.

Стадии развития
В развитии печеночной энцефалопатии выделяют четыре стадии.
Таблица. Стадии печеночной энцефалопатии:
В таблице выше представлены стадии печеночной энцефалопатии, описывающие прогрессирование поражения мозга и ЦНС. Скорость ухудшения состояния пациента зависит от формы диагностированного патологического состояния и сопутствующих триггерных факторов.
- наблюдаются характерные невропатические симптомы болезни Вильсона – Коновалова, однако проблем с метаболизмом меди нет;
- важным инструментом для постановки диагноза является ЭЭГ.
В острой фазе ПЭ пациент возбужден и галлюцинирует, а в подострой, наоборот, он апатичен и слабо реагирует на внешние раздражители. Первыми признаками наличия у человека хронической ПЭ являются изменения характера: апатия, лень, отсутствие интереса к чувствам других людей либо наоборот, раздражительность и нервозность. Здесь важную роль играет темперамент человека: меланхолик будет прятаться в одиночестве, холерик начнет винить окружающих во всех своих проблемах, а сангвиник и флегматик, скорее всего, будут показывать равнодушие к окружающему миру.
Помимо этого, врачи используют еще несколько форм, описывающих особенности протекания печеночной энцефалопатии при циррозе печени, токсических гепатитах и других врожденных и приобретенных заболеваниях гепатобилиарной системы:
- эпизодическая — подразумевает приходящие нейро-психические нарушения, которые могут возникать при ухудшении общего состояния человека: при ослаблении иммунитета, при болезнях верхних дыхательных путей, при алкогольной интоксикации и др.;
- молниеносная (фульминантная) — обычно развивается при острой печеночной недостаточности, вызванной отравлением токсинами, и характеризуется быстрым нарастанием клинической картины;
- спонтанная — проявляется так же, как фульминантная ПЭ, но подразумевается, что дисфункция печени наступила без участия гепатотоксичного фактора;
- персистирующая — такая форма указывается в диагнозе пациента, когда в результате острой печеночной энцефалопатии развивается затяжная клиническая картина, которая ограничивает повседневную активность;
- минимальная (субклиническая) — характерные симптомы ПЭ не проявляются, однако с помощью инструментальной диагностики врачи могут установить протекающие неврологические нарушения; такая форма ПЭ все равно через некоторое время перейдет в эпизодическую, а затем в фульминантную.
При обследовании большого количества пациентов с циррозом печени оказалось, что минимум у трети из них наблюдается субклиническая ПЭ.
Диагностика
При подозрении на патологию назначается комплексное обследование. Диагностика заболеваний печени начинается с консультации врача: он собирает анамнез и осматривает больного. Проводится психометрическое тестирование. С его помощью определяют точность тонкой моторики и скорость познавательной реакции. Результаты оценивают исходя из времени, затраченного больным на выполнение задания и исправление ошибок. Точность такого теста в выявлении энцефалопатии органа – 70 %.
После этого специалист выдает направления на прохождение таких лабораторных и инструментальных видов исследования:
- Общий анализ крови – проводится, чтобы определить уровень тромбоцитов и гемоглобина, лейкоцитов (при энцефалопатии первые два показателя ниже нормы, последний – выше оптимального значения).
- Коагулограмма – показывает наличие ДВС-синдрома.
- Печеночные пробы (наблюдается повышенное количество содержания билирубина в крови).
- УЗИ печени, желчного пузыря.
- Электроэнцефалография – позволяет оценить степень изменений в головном мозге. При скрытом течении патологии информативность этой диагностической процедуры невысока – всего 30%.
- МРТ или КТ брюшной полости.
Завершающий этап диагностики – проведение гистологического исследования тканей печени, взятых при биопсии. При необходимости назначают дополнительные лабораторные тесты, с помощью которых можно обнаружить полиорганную недостаточность.
Лечение печеночной энцефалопатии
Первым делом необходимо установить и устранить причину поражения печени. Затем определяется дальнейшая лечебная тактика. Так, рекомендуется диетотерапия, очищение кишечника и медикаментозная поддержка.
Лечение печеночной энцефалопатии должно проводиться с использованием ряда медикаментов, таких как:
- антибактериальное лекарство для профилактики инфекционных осложнений и борьбы с присутствующими возбудителями;
- сорбенты, которые необходимы для предупреждения всасывания токсинов в кишечнике, увеличивающих интоксикацию и усугубляющие течение энцефалопатии.
По показаниям назначаются клизмы;
- дезинтоксикационные растворы для внутривенного введения (Реосорбилакт);
- противовирусные (рибавирин, альфа-интерферон — виферон) при инфекционном гепатите;
- метаболические для поддержания функций нейронов и нормализации их питания;
- препарат для снижения аммиака лактулоза, гепа-мерц и гепасол. Последний также используется для парентерального питания и восполнения дефицита аминокислот;
- флумазенил. Данное лекарственное средство назначается для уменьшения торможения работы мозга.
В зависимости от причины и течения болезни могут использоваться:
Основные принципы диетического питания:
- ограничение поступления белков до 20 г в сутки (на 3,4 стадиях) и до 50 г на начальном этапе развития энцефалопатии. Это необходимо для снижения уровня аммиака в кровеносном русле, который оказывает токсическое влияние на мозг;
- строгий контроль соли;
- рекомендуется белковая пища растительного происхождения;
- питание должно быть дробным (прием пищи каждые два часа небольшими порциями);
- в сутки необходимо пить не меньше 1,5 литра жидкости под строгим контролем диуреза (для предупреждения нарастания отека мозга).
Питательный рацион может расширяться по мере облегчения самочувствия пациента, улучшения лабораторных показателей и нервно-психического статуса. Энергетические потребности частично покрываются внутривенным введением раствора глюкозы.

Профилактика
Для предупреждения развития представленного заболевания необходимо выполнять следующие рекомендации:
- Терапия основного заболевания, способствующего развитию печёночной энцефалопатии.
- Исключить другие факторы, провоцирующие нарушение сознания.
- Не ограничивать питание, так как для пациентов с гипотрофией очень важно насыщать организм необходимой дозировкой калорий в сутки.
- Приём лактулозы. При её расщеплении в кишечнике и брожении она способствует изменению рН кала и утилизации азота кишечной флорой.
- Приём Лацитол, который оказывает сходное с лактулозой действие, но имеет меньше побочных эффектов.
- Фосфатные клизмы – эффективный метод очищения кишечника. Такие мероприятия крайне важны при остро образовавшейся перегрузке толстой кишки.
Печёночная энцефалопатия – это достаточно серьёзная патология, которая в случае отсутствия соответствующего лечения может привести к печёночной коме. Придерживаясь всех вышеописанных рекомендаций и советов, можно не только избежать этого недуга, но и улучшить своё состояние при постановке такого диагноза.
Прогноз для жизни
Прогноз печеночной энцефалопатии определяется выраженностью симптоматики и глубиной поражения паренхимы органа.
При остром течении он хуже — на фоне молниеносного гепатита развивается печеночная кома, которая приводит к смерти в 85% случаев. Если неврологические нарушения развиваются при циррозе, который уже осложнился асцитом, гипоальбуминемией, то прогноз будет хуже, но при своевременном лечении шансы на сохранение жизни повышаются. При длительной недостаточности клеток печени высок риск развития смертельно опасной комы.
При тяжелых степенях печеночной энцефалопатии умирают до 80% больных, которым не проведена пересадка печени, в то время как на первых двух стадиях показатель выживаемости доходит до 65%. Смерть может наступить и без развития цирроза от кровотечений, нарушения дыхания и сердечной деятельности, отека мозга, почечной недостаточности.
Печеночная энцефалопатия – одно из наиболее тяжелых осложнений печеночной недостаточности, заключающееся в токсическом поражении ЦНС и проявляющееся изменениями личности, снижением интеллекта, депрессией, неврологическими и эндокринными расстройствами. Для установления диагноза проводят биохимические пробы печени, УЗИ печени и желчного пузыря, МРТ и КТ печени и желчевыводящих путей, электроэнцефалографию. Лечение печеночной энцефалопатии включает диетотерапию, эрадикацию инфекционного агента, очищение кишечника, подавление кишечной микрофлоры, симптоматические мероприятия.
- Причины печеночной энцефалопатии
- Симптомы печеночной энцефалопатии
- Диагностика печеночной энцефалопатии
- Лечение печеночной энцефалопатии
- Прогноз и профилактика печеночной энцефалопатии
- Цены на лечение
Общие сведения
Печеночная энцефалопатия при заболеваниях печени встречается не так уж часто, однако имеет очень тяжелый исход – до 80% случаев печеночной комы заканчиваются смертью пациента. Гепатологи отмечают интересный факт: развитие энцефалопатии на фоне острой печеночной недостаточности практически всегда является фактором, исключающим цирроз печени в будущем. При хронических поражениях печени это осложнение развивается гораздо чаще, чем при острых; является потенциально обратимым, но при этом оказывает значительное влияние на социальную активность и трудоспособность пациента. Патогенез и механизмы развития ПЭ на сегодняшний день до конца не изучены, исследованием этой проблемы занимаются ведущие специалисты в области гастроэнтерологии. Раскрытие механизмов развития печеночной энцефалопатии приведет к разработке патогенетического лечения и позволит снизить смертность от этого грозного осложнения печеночной недостаточности.
Причины печеночной энцефалопатии
Выделяют несколько типов печеночной энцефалопатии, в зависимости от причин ее развития: ПЭ, связанная с острой печеночной недостаточностью, с попаданием в кровоток кишечных нейротоксинов, с циррозом печени. Факторами развития острой печеночной недостаточности с печеночной энцефалопатией могут служить острые вирусные гепатиты, алкогольный гепатит, рак печени, другие заболевания, сопровождающиеся гепатоцитолизом, лекарственные и другие интоксикации. Причиной попадания в кровоток кишечных нейротоксинов может быть активное и чрезмерное размножение облигатной флоры кишечника, употребление слишком больших количеств белковой пищи. Цирроз печени с развитием печеночной энцефалопатии характеризуется замещением нормально функционирующих гепатоцитов соединительной рубцовой тканью с угнетением всех печеночных функций.
Запустить процесс гибели гепатоцитов и токсического поражения головного мозга могут следующие факторы: кровотечения из желудка и кишечника, злоупотребление алкоголем, неконтролируемый прием медикаментов, постоянные запоры, избыточное употребление белка, инфекции, операции, развитие перитонита на фоне асцита.
При печеночной недостаточности в организме развивается целый комплекс патологических нарушений: изменение КОС и водно-электролитного состояния крови, гемостаза, онкотического и гидростатического давления и т. д. Все эти изменения значительно нарушают работу таких клеток, как астроциты, которые представляют собой треть всей клеточной массы головного мозга. На астроциты возложена функция регуляции проницаемости барьера между тканью головного мозга и кровью, обезвреживания токсинов, обеспечения поступления в клетки мозга электролитов и нейротрансмиттеров. Постоянное воздействие на астроциты аммиака, в избытке поступающего в кровоток при печеночной недостаточности, приводит к ухудшению их функционирования, повышению ликворопродукции, развитию внутричерепной гипертензии и отека головного мозга. Кроме аммиака, токсическое воздействие на астроциты способны оказывать ложные нейротрансмиттеры, жирные кислоты и аминокислоты, магний, продукты распада углеводородов и жиров.
Симптомы печеночной энцефалопатии
В клинической картине печеночной энцефалопатии выделяют различные неврологические и психические нарушения. Обычно к ним относят расстройства сознания (патологическая сонливость, фиксация взгляда, заторможенность с последующим развитием сопора, комы), нарушения сна (в дневное время пациент патологически сонлив, а в ночное предъявляет жалобы на бессонницу), нарушения поведения (раздражительность, эйфория, безучастность, апатия), интеллекта (забывчивость, рассеянность, нарушения письма), монотонность речи. Появление либо усиление сладковатого печеночного запаха изо рта связано с нарушением метаболизма меркаптанов (продуктов жизнедеятельности кишечной флоры) в печени, в связи с чем они начинают выводиться через дыхательные пути.
У многих пациентов признаком печеночной энцефалопатии является астериксис – несимметричные крупноразмашистые аритмичные подергивания, возникающие в мышцах конечностей, туловища и шеи при их тоническом напряжении. Обычно астериксис выявляется при вытягивании рук вперед, напоминает суетливые движения кистей и пальцев. Достаточно часто при печеночной энцефалопатии поражается терморегуляционный центр, из-за чего может отмечаться пониженная или повышенная температура, либо же чередование эпизодов гипотермии и гипертермии.
По течению выделяют острую и хроническую форму печеночной энцефалопатии. Острая энцефалопатия развивается очень быстро и может приводить к развитию комы в течение нескольких часов или дней. Хроническая форма развивается медленно, иногда в течение нескольких лет.
В своем развитии печеночная энцефалопатия проходит несколько стадий. В начальной стадии (субкомпенсации) появляются незначительные изменения психики (апатия, бессонница, раздражительность), сопровождающиеся иктеричностью кожи и слизистых. На стадии декомпенсации изменения психики усугубляются, пациент становится агрессивным, появляется астериксис. Возможны обмороки, неадекватность поведения. В терминальной стадии происходит угнетение сознания вплоть до сопора, однако реакция на болевые раздражители еще сохраняется. Последняя стадия печеночной энцефалопатии – кома, реакция на раздражители отсутствует, развиваются судороги. На этой стадии погибает девять из десяти пациентов.
Диагностика печеночной энцефалопатии
Целью диагностики при печеночной энцефалопатии служит выявление ее симптомов, установление степени тяжести и стадии заболевания. Большое значение для выявления печеночной энцефалопатии имеет правильно собранный анамнез (упоминание о перенесенных вирусных гепатитах, злоупотреблении алкоголем, бесконтрольном приеме медикаментов). Консультация гастроэнтеролога должна быть проведена как можно раньше, и данный специалист обязан уделить достаточно внимания неврологической симптоматике и признакам расстройств психики. Следует помнить, что появление симптомов поражения стволовых структур мозга у пациентов в коме говорит о возможности летального исхода в ближайшие часы.
Проводят общий анализ крови (выявляет анемию, снижение количества тромбоцитов, лейкоцитоз с токсической зернистостью нейтрофилов), исследуют коагулограмму (из-за угнетения белково-синтезирующей функции печени развивается коагулопатия дефицита, затем ДВС-синдром), печеночные пробы (отмечается повышение активности трансаминаз, ЩФ, Г-ГТП, растет уровень билирубина). При необходимости возможно проведение других лабораторных тестов, которые укажут на поражение внутренних органов (полиорганную недостаточность).
Для выяснения степени поражения печени могут потребоваться такие неинвазивные исследования, как УЗИ печени и желчного пузыря, МРТ печени и желчевыводящих путей, КТ желчевыводящих путей. Обязательно производится пункционная биопсия печени для выяснения точной причины печеночной недостаточности. Оценка степени поражения головного мозга осуществляется с помощью электроэнцефалографии.
Дифференциальный диагноз печеночной энцефалопатии проводят с другими (внепеченочными) причинами поражения головного мозга: внутричерепная катастрофа (геморрагический инсульт, кровоизлияние в желудочки мозга, разрыв аневризмы церебральных сосудов и пр.), инфекции ЦНС, метаболические расстройства, внепеченочные причины повышения уровня азота в крови; алкогольные, лекарственные и послесудорожные энцефалопатии.
Лечение печеночной энцефалопатии
Терапия печеночной энцефалопатии является сложной задачей, и начинать ее нужно с устранения причин этого состояния, лечения острой либо хронической печеночной недостаточности. В схему лечения печеночной энцефалопатии включают диетотерапию, очищение кишечника, снижение уровня азота, симптоматические мероприятия.
Следует снизить количество поступающего с пищей белка до 1г/кг/сут. (при условии переносимости такого рациона пациентом) на достаточно длительное время, так как у некоторых больных возврат к нормальному содержанию белка вызывает повторное появление клиники печеночной энцефалопатии. На время диеты назначаются препараты аминокислот, ограничивается содержание соли.
Для обеспечения эффективного выведения аммиака с калом необходимо достигнуть опорожнения кишечника не менее двух раз за сутки. С этой целью производятся регулярные очистительные клизмы, назначаются препараты лактулозы (их прием необходимо продолжить и на этапе амбулаторного лечения). Также улучшает утилизацию аммиака орнитин, сульфат цинка.
Антибактериальная терапия включает назначение препаратов широкого спектра действия, проявляющих активность преимущественно в просвете кишечника (неомицин, ванкомицин, метронидазол и др.). С седативной целью при печеночной энцефалопатии нежелательно назначать препараты бензодиазепинового ряда, предпочтение отдают галоперидолу.
Течение печеночной энцефалопатии может осложниться отеком головного мозга, кровотечениями, аспирационной пневмонией, панкреатитом; поэтому лечение пациентов на 3-4 стадии заболевания должно осуществляться в отделении реанимации.
Прогноз при печеночной энцефалопатии зависит от нескольких факторов, но в целом неблагоприятный. Выживаемость лучше в случаях, когда энцефалопатия развилась на фоне хронической печеночной недостаточности. При циррозе печени с печеночной энцефалопатией прогноз ухудшается при наличии желтухи, асцита, пониженного уровня белка в крови. При острой печеночной недостаточности прогноз хуже у детей до 10 лет и взрослых после 40 лет, на фоне вирусного гепатита, желтухи и гипопротеинемии. Летальность на 1-2 стадиях печеночной энцефалопатии 35%, на 3-4 стадии – 80%. Профилактика данной патологии заключается в отказе от алкоголя и неконтролируемого приема медикаментов, лечении заболеваний, которые приводят к развитию печеночной энцефалопатии.
Общие сведения
Причиной декомпенсации функций является массивный некроз гепатоцитов при токсическом, вирусном или ишемическом повреждении первоначально здоровой печени, или обострение хронического заболевания печени, когда в силу каких-либо причин (кровотечение, операция на печени по поводу цирроза или опухоли) развивается острая декомпенсация хронического заболевания. Развитие печеночной недостаточности свидетельствует о том то, что из функционирования выпало более 75-80% печеночных клеток. Нарушается детоксикационная функция органа и ряд токсических веществ (индол, аммиак, скатол, фенол, жирные кислоты) поступают в системный кровоток, вызывая развитие энцефалопатии и комы.
Печеночная недостаточность чаще всего развивается на фоне острых и хронических вирусных гепатитов. На втором месте среди причин у мужчин стоит алкогольное поражение печени с развитием цирроза. Острая печеночная недостаточность у женщин связана большей частью с вирусным гепатитом Е, особенно при беременности, увеличивая смертность до 25%. В данной статье мы рассмотрим симптомы этого состояния и основные направления коррекции его.
Патогенез
В основе патогенеза данного состояния лежит массивное повреждение печеночных клеток (некроз), в результате чего нарушаются функции печени и других органов — прежде всего ЦНС, легких, почек, гемодинамики, перфузии тканей и развитие метаболического ацидоза. В конечном счете развивается тяжелая полиорганная недостаточность. Некроз является результатом гипериммунного ответа на повреждающий фактор. Процесс распространяется, вовлекая большое количество здоровых гепатоцитов, и имеет характер цепной реакции с развитием массивного повреждения. Тяжесть печеночной недостаточности зависит от количества поврежденных гепатоцитов и от продолжительности периода их гибели. Если ранее считалось, что механизм гибели клеток печени заключается в развитии некроза, то сейчас рассматривается и изучается другой механизм их гибели, а именно — апоптоз (то есть самопрограммируемая смерть клеток). Выявлено, что при выраженных повреждениях клеток развивается некроз, а при незначительных — преобладает апоптоз.
Поскольку печень принимает участие в углеводном, жировлм и белковом обменах, синтезе витаминов при нарушении ее функции все эти показатели изменяются. Нарушения углеводного обмена характеризуются склонностью к гипогликемии, что связано с уменьшением количества гликогена в печени. Гипогликемия у больных проявляется головокружением, слабостью и различными вегетативными расстройствами. Нарушения жирового обмена проявляется нарушением синтеза триглицеридов, холестерина, фосфолипидов, желчных кислот, липопротеидов. В крови снижается уровень липопротеидов и холестерина, а в кишечнике возникает дефицит желчных кислот. Нарушения белкового обмена проявляется уменьшением альбуминов в крови, синтез которых резко снижается. Дефицит их приводит к появлению гипергидратации тканей и отеков (при портальной гипертензии появляется асцит). Также уменьшается синтез α и β-глобулинов. Диспротеинемия влечет снижение альбумино-глобулинового коэффициента.
Нарушается синтез важных факторов свертывания, что влечет развитие кровоточивости. Протромбиновый индекс служит маркером тяжести недостаточности печени — чем он ниже, тем тяжелее ее поражение. Нарушается синтез транспортных белков, что вызывает развитие железодефицитной и В12-дефицитной анемии. Нарушается и синтез витаминов, в частности витамина А и В6. Возникают гормональные расстройства в связи с дефицитом транспортных белков и в связи с нарушением преобразования гормонов в печени.
Поскольку аминокислоты не используются при синтезе белка, их количество в крови увеличивается (гипераминоацидемия) и увеличивается выделение их с мочой (почки не в состоянии реабсорбировать их и вернуть в кровоток). Чем больше нарушена функция печени, тем больше уровень аммиака в крови (это токсичный конечный продукт белкового обмена), поскольку печень является главным органом обезвреживания этого продукта и не доводит процесс метаболизма его до образования мочевины.
Ослабление антитоксической функции выражается в снижении обезвреживания также токсических продуктов — индол, скатол, нитробензол, фенол, путресцин, которые поступают из кишечника. Ослабление печеночных макрофагов снижает барьерную функцию печени: в кровь попадают антигены, микробы, токсины, иммунные комплексы, поэтому часто у таких больных развиваются инфекционные, аллергические и иммунные заболевания. Даже развивается токсемия, сопровождающаяся высокой температурой, лейкоцитозом, гемолизом эритроцитов, почечной недостаточностью и появлением эрозий в кишечнике. Воздействие токсических веществ на головной мозг (преимущественно аммиака) угнетает процессы в нем, вызывая печеночную энцефалопатию, переходящую в кому.
Классификация
В зависимости от скорости развития печеную недостаточность разделяют на:
- Острую.
- Хроническую.
Острая печеночная недостаточность развивается при вирусных гепатитах, отравлении ядами, промышленными токсинами, суррогатами алкоголя, лекарственными препаратами, поражении вирусом герпеса и цитомегаловирусом, вирусом Коксаки, септицемии при абсцессе печени, переливании иногруппной крови. При своевременном лечении эта форма может быть обратимой.
Хроническая печеночная недостаточность встречается при циррозах печени, опухолях этого органа. Также хроническая недостаточность возможна при электролитных нарушениях и развивается после операций портосистемного шунтирования.
Развивается медленно — несколько недель или месяцев. Однако, наличие провоцирующих факторов (употребление алкоголя, желудочное кровотечение сопутствующая инфекция, переутомление, удаление большого объема асцитической жидкости или прием высоких доз мочегонных препаратов) быстро вызывает развитие печеночной комы.
Выделяют следующие стадии недостаточности печени:
- Начальная (или компенсированная).
- Выраженная (характеризуется декомпенсацией функции печени).
- Терминальная.
Также различают виды:
- Абсолютная и относительная печеночная недостаточность (она появляется на фоне перегрузки печени).
- Тотальная — при ней снижаются все функции печени.
- Парциальная — имеет место нарушение отдельных функций.
- Малая печеночная недостаточность — протекает без энцефалопатии.
- Большая печеночная недостаточность протекает с энцефалопатией.
Причины
Причины развития хронической недостаточности:
- Цирроз.
- Опухоли.
- Паразитарные заболевания печени (альвеококкоз).
- Тяжелые формы прогрессирующих хронических гепатитов.
- Склерозирующий холлангит.
Факторы, провоцирующие печеночную недостаточность при хронических заболеваниях:
- Прием алкоголя.
- Избыточная нагрузка белком.
- Физические нагрузки.
- Потеря жидкости в следствие диареи, рвоты, приема диуретиков или удаления асцитической жидкости.
- Кровотечение с развитием анемии и гиповолемии.
- Переливание крови.
- Хирургические вмешательства.
- Прием бензодиазепина, антидепрессантов, морфина.
Если говорить об острой печеночной недостаточности, то ее вызывают:
- Прием лекарственных препаратов. Гепатотоксичными являются нитрофураны, парацетамол, барбитураты,рифампицин, ингаляционные анестетики, хлорпромазин, сульфаниламиды.
- Лекарственные поражения протекают по-разному: от бессимптомного повышения печеночных ферментов до острой недостаточности и цирроза печени. Известно, что гепатотоксичной является суточная доза парацетамола 10 г, но случаи развития почечной недостаточности могут наблюдаться при приеме 3-4 г в сутки. Случаи острой недостаточности печени встречаются при лечении цефотаксимом, цефтриаксоном, цефазолином, цефуроксимом, а также фторхинолонов (ципрофлоксацин, левофлоксацин). Самым гепатотоксичным из сульфаниламидов является сульфасалазин. Чаще всего гепатотоксические реакции при приеме сульфаниламидов протекают легко, но зарегистрированы случаи фульминантной недостаточности после применения ко-тримоксазола. Также стоит указать цитостатики, применяемые у онкологических больных, которые нередко приводят к печеночной недостаточности.
- Отравление гепатотропными ядами (тетрахлорэтаном, фосфор, четыреххлористый углерод, нитраты толуола, мышьяк, дихлорэтан, хлороформ).
- Травмы печени.
- Отравления грибами.
- Септические состояния.
- Обширные ожоги, септический аборт, шок.
- Вирусные повреждения печени.
- Аутоиммунный гепатит, который характеризуется быстро прогрессирующим тяжелым течением.
- Тромбоз печеночных вен и артерий.
- Ишемическое повреждение печени при остром инфаркте миокарда, остановке сердца и длительном периодом реанимации.
Симптомы печеночной недостаточности
Общие признаки печеночной недостаточности, характерные для мужчин и женщин:
- Желтуха, которая связана с тем, что печень не в состоянии метаболизировать билирубин. Ее появление считается неблагоприятным признаком, поскольку свидетельствует об обширном поражении ее ткани. Чем выше показатель билирубина, тем у больного тяжелее недостаточность.
- Землисто-серый цвет кожи с желтушностью.
- Плохое зрение в темноте, что является показателем нарушения обмена витаминов.
- Тошнота, рвота, плохой аппетит, слабость и быстрая утомляемость.
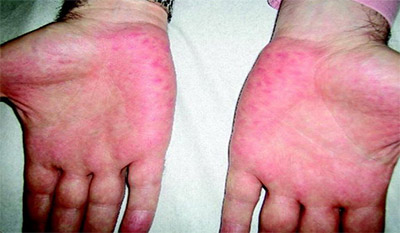
- Печеночные ладони (пальмарная эритема) — симметричное покраснение ладоней, особенно в области возвышения первого пальца. При надавливании покраснение исчезает и снова быстро появляется после прекращения воздействия.
- Малиновый гладкий за счет атрофии сосочков язык.
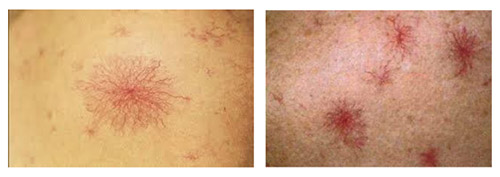
- Сосудистые звездочки — ангиомы, от которых в виде лучей отходят мелкие веточки сосудов. Они появляются на коже шеи, лица, плеча, кистей и туловища. Выявляются сосудистые звездочки (их называют телеангиэктазии) на слизистых оболочках рта.
- Постоянное повышение температуры при декомпенсированном циррозе отмечается у трети больных. Это связано с попаданием бактерий из кишечника через портосистемные коллатерали в ток крови. В терминальной стадии печеночной недостаточности возможно развитие септицемии.
- Развитие асцита отмечается при прогрессирующем фиброзном поражении органа и развитии портальной гипертензии. Асцит также связан со снижением уровня альбуминов.
- Желудочно-кишечное кровотечение, кровотечения носа, глотки или мест инъекций.
- Аритмии (фибрилляция, желудочковые экстрасистолы), миокардит, перикардит, брадикардия, отёк лёгких свидетельствуют о декомпенсированной печёночной недостаточности.
- Печеночный запах.
- Двигательные расстройства и нарушение психики — это признаки развивающейся энцефалопатии.
- Почечная недостаточность.
Имеются также половые особенности:
- У мужчин выявляют увеличение молочных желез (гинекомастия односторонняя или двухсторонняя), импотенцию, атрофию яичек. Также появляется женский тип оволосения, исчезновение волос на груди, животе и подбородке. Это связано с тем, что печень утрачивает способность инактивировать эстрогены и они в избытке накапливаются у мужчин.
- Симптомы у женщин характеризуются уменьшением роста волос на лобке, снижается влечение, атрофируется матка и молочные железы, также отмечается нарушение менструального цикла.
В начальной стадии печеночной недостаточности состояние больных остается удовлетворительным, имеется невыраженная диспепсия (тошнота, рвота). Показатели функции печени незначительно изменены. На выраженной стадии появляются значительная слабость, желтуха, лихорадка, диспепсический синдром, гиповитаминоз, отеки, геморрагические проявления.
Характерны глубокие нарушения обмена веществ, дистрофические явления в различных органах, выраженное истощение. Признаки наступающей печеночной комы. В терминальной стадии отмечается выраженная слабость, желтуха, печеночный запах изо рта, зуд, отеки, асцит. Возможно развитие септической лихорадки. После этого развиваются гипотермия и снижается давление. Рефлексы снижены, лицо маскообразное, клонические судороги и мышечные подергивания. Изменяется ритм дыхания, реакция зрачков исчезает и развивается прекома и кома.
Прекома проявляется спутанностью сознания, делирием, тремором рук и век, нарушениями речи, повышением рефлексов, расстройством почерка. На электроэнцефалограмме — замедления α-ритма и появляются σ-волны. При печеночной коме сознание отсутствует, лицо становится маскообразным, появляется печеночный запах, исчезает реакция на раздражители, появляются клонические судороги, нарушается функция сфинктеров, происходит остановка дыхания.
Анализы и диагностика
Диагностика печеночной недостаточности основывается на биохимических клинических и электроэнцефалографических данных:
- Увеличивается уровень билирубина (прямого и непрямого).
- Повышается уровень АСТ, АЛТ и щелочной фосфатазы.
- Увеличивается уровень остаточного азота, аммиака и других токсических продуктов.
- Снижается содержание альбумина в крови.
- Увеличен показатель тимоловой пробы.
- Снижается уровень фибриногена, натрия, калия и холестерина.
- Снижение количества тромбоцитов.
- Уменьшение уровня факторов свертывания крови.
- Гипогликемия из-за увеличения уровня инсулина.
- Серологические тесты на вирусные гепатиты.
- Аутоиммунные маркеры.
Иногда применяется инструментальный метод исследования — гепатография, который проводится с препаратом бенгальский розовый. По тому как изменяется скорость и степень поглощения печенью бенгальского розового делают вывод о степени печеночной недостаточности.
Лечение печеночной недостаточности
Лечение этого состояния включает:
- Лечение основного заболевания.
- Инфузионная терапия для устранения волемических и водно-электролитных нарушений.
- Снижение уровня аммиака в крови.
- Лечение коагулопатии (применяют гемостатический препарат аналог витамина К-Менадион 300 мг в день).
- Борьба с отеком мозга (мочегонные препараты внутрь и осмотический диуретик Маннит внутривенно).
- Ограничение поступления белка (белок ограничивается до 30-40 г, жиры до 60 г в день, а углеводы до 200 г).
- При острой печеночной недостаточности проводят очищение кишечника для уменьшения всасывания продуктов гниения. Внутривенно вводят жидкости до 3000 мл в день. Это может быть раствор Глюкозы, Неогемодез, 30% Маннит, Рефортан, Гелофузин, Стабизол. Для устранения нарушений гемостаза переливают плазму, а при анемии — эритроцитарную массу.
При вирусном гепатите В назначают аналоги нуклеозидов: Ламивудин, Энтекавир, Тенофовир, Телбивудин, которые дают хорошие результаты. Аналоги нуклеозидов назначают непродолжительно. При гепревирусных гепатитах проводится лечение ацикловиром (10-30 мг на кг веса в сутки). При недостаточности печени, причиной которых стали вирусные гепатиты А, Е и С, противовирусные препараты не рекомендуется назначать. При лекарственном поражении парацетамолом назначают активированный уголь (1 г/кг веса в течение первого часа). Его назначают как можно раньше, если с момента приема парацетамола прошло меньше 4-х часов. В последующем переходят на введение N-ацетилцистеина.
При отравлении грибами лечение начинают с промывания желудка, введения через зонд активированного угля. Он связываете амотоксин (яд грибов), что дает лучшую выживаемость больных. Затем проводится инфузионная терапия для восполнения водно-электролитного состава крови.
Дополнительные методы лечения предусматривают назначение гепатопротекторов на основе силимарина — биологически активные вещества расторопши. Действие силимарина (препарты Карсил, Дарсил, Гепарсил, Легалон, Силарсил) основывается на способности его противостоять захвату α-аманитина (наиболее ядовитый токсин) печеночными клетками. Однако препарат эффективен, если его принять в первые 48 часов после отравления грибами. Силимарин назначается по 30-40 мг на кг веса в день, курс его приема 3-5 дней. Часто прием силимарина дополняют введением N-ацетилцестеина.
Лечение печеночной недостаточности при аутоиммунных гепатитах предусматривает назначение глюкокортикостероидов (Преднизолон 40-60 мг в день). Если у пациента есть показания и возможности проведения ранней трансплантации печени, то ее выполняют даже во время приема глюкокортикостероидов.
При хронической печеночной недостаточности важно:
- Соблюдение диеты с ограничением белка 20-40 г в день.
- Введение раствора глюкозы.
- Введение в кишечник антибиотиков (Неомицин, Ванкомицин), которые будут подавлять образование аммиака бактериями в кишечнике.
- Дезинтоксикационная терапия (до 2,5-3 л различных растворов).
- Препараты для уменьшения в крови аммиака.
Гипераммониемия наблюдается у больных при хронических заболеваниях печени на стадии до появления цирроза. Учитывая роль аммиака в развитии печеночной энцефалопатии, медикаментозная тактика должна быть направленная на все звенья образования и абсорбции аммиака в кишечнике и нейтрализацию его в печени и крови. Выделяют три группы препаратов, которые:
- уменьшают поступление аммиака из кишечника (дисахариды, невсасывающиеся антибиотики, подавляющие микрофлору, очищение кишечника);
- связывающие аммиак в крови (фенилацетат натрия и бензоат натрия);
- обезвреживают аммиак в мышцах и печени (препарат Гепа-Мерц с активным веществом L-орнитин-L- аспартат).
Для подавления флоры, которая продуцирует аммиак, назначают антибиотики (Ванкомицин, Ципрофлоксацин). Прием антибиотиков сочетают с высокими клизмами, которые максимально очищают толстую кишку. Санация кишечника проводится для удаления азотсодержащих веществ, и она особенно важна при появившихся желудочно-кишечных кровотечениях. Также с целью уменьшения содержания аммиака в кишечнике применяют лактулозу (препараты Дюфалак, Нормолакт, Гудлак, Порталак), которые назначают внутрь до 30-120 мл в день или вводят в прямую кишку).
Лактулоза является синтетическим дисахаридом, который подавляет активность аммониегенных бактерий и способствует уменьшению в кишечнике аммиака. Препарат, который усиливает метаболизм аммиака — L-орнитин -L-аспартат. В зависимости от состояния больных могут назначаться препараты эти препараты внутривенно (Орнилатекс, Ларнамин, Орницетил) или внутрь (Орнитин-Канон, Гепа-Мерц). Последний назначают по 3 г внутрь 3 раза в день в течение месяца, а по 10 дней ежемесячно еще три месяца. Такая схема является эффективной для снижения уровня аммиака. При прогрессировании энцефалопатии больные должны занимать положение с приподнятым головным концом, им проводится интубация трахеи. Для снижения внутричерепного давления назначается Маннит внутривенно.
Читайте также:


