Вегетативная нервная система в фармакологии
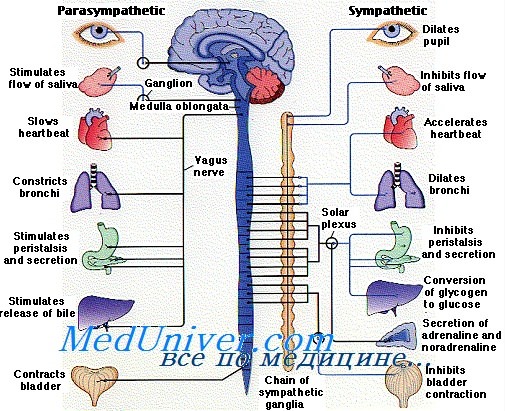
Вегетативная нервная система поддерживает гомеостаз. ВНС управляет такими висцеральными функциями, как кровообращение, пищеварение и выделение, главным образом без условного или сознательного контроля. ВНС также модулирует функцию эндокринных желез, регулирующих метаболизм. ВНС имеет сенсорные и моторные компоненты и разделяется на симпатическую и парасимпатическую системы. Первые нейроны симпатической системы расположены в промежуточных рогах тораколюмбального отдела спинного мозга; синапс со вторым набором нейронов находится в параили превертебральном симпатическом ганглии. В парасимпатической системе первые нейроны расположены либо в черепно-мозговом нерве, в автономных ядрах, либо в промежуточном роге сакрального отдела спинного мозга; синапс со вторым набором нейронов находится или в автономном ганглии (в случае черепно-мозговых нервов), или в эффекторной ткани непосредственно. ВНС имеет три главных компонента:
• афферентный (центростремительный, чувствительный);
• центральный объединяющий;
• эфферентный.
Афферентный компонент несет информацию от нейрональных физиологических рецепторов, расположенных в концах центростремительных нервов, к спинному мозгу и более высоким областям ЦНС. Большая часть этой информации обрабатывается в пределах гипоталамуса и других нижележащих областей мозга. После обработки соответствующий сигнал посылается от ЦНС вниз по эфферентным нервам к исполнительным органам (см. рис. 8.1, 8.9), названным так потому, что они отвечают на деятельность в ЦНС.
На основе различий анатомии и медиаторов эфферентную часть ВНС подразделяют на три системы:
• парасимпатическую (холинергическую);
• симпатическую (адренергическую);
• неадренергическую нехолинергическую (НАНХ).
Ацетилхолин — нейромедиатор холинергической системы. Ацетилхолин — нейромедиатор, высвобождаемый из пресинаптического окончания в автономном ганглии и в окончаниях нервов в исполнительном органе. Рецепторами для ацетилхолина служат холинорецепторы, которые подразделяют на мускариновые и никотиновые.
Норадреналин — нейромедиатор адренергической системы. Другая важная составляющая ВНС — адренергическая система. До сих пор неизвестно, какой нейромедиатор использовался в этой системе первоначально — эпинефрин или норэпинефрин. Сейчас известно, что за исключением надпочечников, которые секретируют эпинефрин (адреналин), нейроме-диатором в адренергической системе является норэпинефрин.
Ацетилхолин — ганглионарный медиатор для холинергической и адренергической систем. Эфферентные нервы и для холинергической, и для адренергической систем происходят из соответствующих частей ствола мозга и спинного мозга. Эфферентные нервы образуют синапс в ганглии, расположенном вне органа, где основным нейромедиатором является АХ:
• в адренергической системе ганглии находятся в цепочке вблизи спинного мозга, известной как паравертебральная симпатическая цепочка;
• в холинергической системе ганглий обычно располагается внутри или вблизи эффекторного органа.
Несмотря на явное анатомическое различие, оба типа ганглиев используют АХ как основной ганглионарный нейромедиатор, активирующий никотиновые рецепторы.
Нейромедиаторы могут модулировать собственное высвобождение. Нейромедиаторы могут модулировать собственное высвобождение. Нейромедиаторы могут активировать пресинаптические рецепторы на нейроне, что ингибирует высвобождение самих нейромедиаторов.
Учебное видео анатомии вегетативной нервной системы (ВНС)
- Вернуться в оглавление раздела "фармакология"
Вещества, Действующие Преимущественно На Вегетативную Нервную Систему
Эфферентные нервы делятся на двигательные (иннервирующие скелетные мышцы) и вегетативные нервные волокна. В отличие от двигательных нервов, вегетативная иннервация не подчиняется произвольному управлению.
Вегетативная нервная система иннервирует внутренние органы, кровеносные и лимфатические сосуды, железы внутренней и внешней секреции, гладкую и поперечнополосатую мускулатуру. Она делится на симпатический и парасимпатический отделы. Деятельность этих отделов находится под регулирующим влиянием коры головного мозга. Волокна вегетативной иннервации, идущие от центральной нервной системы к периферии, прерываются в ганглиях. Ганглии симпатической иннервации расположены вдоль спинного мозга, а парасимпатической — в непосредственной близости к иннервируемым органам. Прерыв волокон в ганглиях позволяет их делить на пре- и постганглионарные. Импульсы возбуждения на рабочий орган передаются при помощи медиаторов (передатчиков), образование и разрушение которых происходят при участии ферментов. В большинстве органов имеются симпатические и парасимпатические волокна, которые вызывают противоположный эффект (табл. 3).
В фармакологии принято делить вегетативные нервы с учетом медиаторов, выделившихся на их окончания, на холинергические, когда медиатором служит ацетилхолин, и адренергические, когда медиатором является норадреналин. К холинергическим нервам относятся постганглионарные парасимпатические волокна, двигательные волокна скелетных мышц, преганглионарные парасимпатические и симпатические волокна. К адренергическим нервам относятся постганглионарные симпатические волокна. Ткани, воспринимающие импульсы с холинергических нервов, называют холинорецепторами (холинореактивными системами), а с адренергических нервов — адренорецепторами (адренореактивными системами). С учетом этого лекарственные вещества делятся на холинергические и адренергические (рис. 15).
Ацетилхолин (эндогенный) образуется из холина в присутствии фермента холинацетилазы и аденозинтрифосфата при возбуждении холинергических нервов. В области холинергических нервов постоянно образуется ацетилхолинэстераза (холинэстераза), которая разрушает ацетилхолин на холин и уксусную кислоту. Процесс синтеза и разрушения ацетилхолина протекает очень быстро (доли секунды), и это обеспечивает усиление или уменьшение возбуждения холинергических нервов и рабочих органов.
Холинореактивные системы делят на мускариночувствительные, или М-холинореактивные, и никотиночувствительные, или Н-холинореактивные, системы. М-холинореактивные системы (М-холинорецепторы) находятся в тканях, получающих постганглионарную парасимпатическую иннервацию (сердце, мускулатура желудка, кишечника, бронхов, матки, потовые железы, глаза, железы желудочно-кишечного канала и др.). Н-холинореактивные системы (Н-холинорецепторы) имеются в ганглиях парасимпатической и симпатической иннервации, в скелетных мышцах, в каротидных клубочках сосудов, в преганглионарных нервных волокнах, в центральной нервной системе.
Холинергические вещества делят на возбуждающие, которые называются холиномиметиками, и угнетающие, называемые холинолитиками. Аналогично вещества, возбуждающие адренергическую иннервацию, называют адреномиметиками, а угнетающие — ад ре политиками.
Холиномиметики и холинолитики, применяемые в больших дозах, могут вызвать отравление. При отравлении холиномиметиками развиваются понос, колики, ослабление работы сердца, одышка, судороги, сужение зрачков.
Противоядием при отравлении холиномиметиками служит атропин (холинолитики).
Вегетативная нервная система иннервирует сосуды, гладкую мускулатуру внутренних органов, экзокринные и эндокринные железы и паренхиматозные клетки во всех системах органов. Функционирующая на подсознательном уровне, она быстро и непрерывно реагирует на возмущения, угрожающие постоянству внутренней среды. К числу многих функций, осуществляемых под управлением этой системы, относятся распределение кровотока и поддержание перфузии тканей, регуляция артериального давления, регуляция объема и состава внеклеточной жидкости, расходование энергии обмена веществ и снабжение субстратами, а также контроль за функционированием гладкой мускулатуры внутренних органов и желез.
Реакции вегетативной нервной системы, подобно реакциям соматической нервной системы, индуцируются немедленно и рассеиваются быстро в противоположность более медленным и более длительным реакциям, опосредуемым циркулирующими в крови гормонами. Подобно эндокринной системе, вегетативная нервная система регулирует скорость процессов, обладающих своей собственной внутренней активностью, в то время как соматическая нервная система инициирует реакции de novo. Хотя определенные вегетативные реакции являются специфическими, многие из них генерализованные и влияют на ряд эффекторов в различных органах. Разграничение между функциями вегетативной нервной системы и эндокринной системы можно пояснить на примере мозгового вещества надпочечника. Эта железа, гомологичная во многих отношениях с постганглионарным симпатическим нейроном, секретирует гормон (адреналин) в систему кровообращения для взаимодействия с адренорецепторами по всему организму.
Нейроны вегетативной нервной системы, расположенные в ганглиях вне пределов центральной нервной системы, образуют постганглионарные вегетативные нервы, иннервирующие органы и ткани по всему организму. Активность вегетативных нервов регулируется центральными нейронами, отвечающими на разнообразные афферентные импульсы. В результате центральной интеграции афферентной информации эфферентный поток вегетативных импульсов оказывается отрегулированным таким образом, чтобы обеспечить функционирование основных систем органов в соответствии с потребностями организма в целом. Связи между корой большого мозга и вегетативными центрами в стволе мозга координируют эфферентный поток вегетативных импульсов с высшими психическими функциями.
Симпатическая и парасимпатическая части вегетативной нервной системы. Преганглионарные нейроны парасимпатической части вегетативной нервной системы покидают центральную нервную систему в составе III, VII, IX и Х черепных нервов, а также в составе II и III крестцовых нервов, в то время как Преганглионарные нейроны симпатической части вегетативной нервной системы выходят из спинного мозга в промежутке между 1-м грудным и 2-м поясничным сегментами. Реакции на стимуляцию, исходящую от симпатической и парасимпатической систем, часто бывают антагонистичными, примером чего является их противоположное влияние на частоту сердечных сокращений и двигательную активность кишечника. Этот антагонизм отражает высоко координированные взаимодействия внутри центральной нервной системы; возникающие в результате этих взаимодействий изменения в активности парасимпатической и симпатической систем (часто направленные противоположно) обеспечивают более точный контроль вегетативных реакций, чем тот, которого можно было бы достичь модулированием лишь одной из этих систем.
Нейромедиаторы. Ацетилхолин служит преганглионарным нейромедиатором обегх частей вегетативной нервной системы, а также постганглионарным нейромедиатором парасимпатических нейронов. Нервные волокна, в которых происходит высвобождение ацетилхолина, носят название холинергических. Норадреналин является нейромедиатором постганлионарных симпатических нейронов; эти нервы называют адренергическими. Входящие в состав симпатических волокон постганглионарные нейроны, иннервирующие экзокринные потовые железы (и, возможно, некоторые кровеносные сосуды, снабжающие кровью скелетную мускулатуру), являются холинергическими.
Предназначение вегетативной нервной системы – контроль и коррекция деятельности внутренних органов. Процесс осуществляется автономно – без участия сознания людей. Это позволяет молниеносно реагировать на изменения во внешней среде, агрессиях извне. Однако, при необходимости люди могут оказывать влияние на вегетативные проявления – опосредованно, к примеру, с помощью медикаментов либо физиотерапевтических процедур.
Что собой представляет вегетативная часть нервной системы
Несмотря на огромное влияние вегетативной системы на организм каждого человека, как биологической единицы, по сути, никто не может сказать, что способен ежесекундно чувствовать ее работу. При правильном функционировании люди просто ощущают себя здоровыми.

В этом и состоит главная цель вегетативного сегмента – создание внутри организма аппарата, который бы соединял все органы и ткани в единый конгломерат для сохранения человека, как цельной природной единицы. К примеру, при повышении температуры внешней среды сразу же корректируется деятельность, дыхательной, сердечнососудистой и обменной системы. Они, взаимодействуя, создают комфортные условия для работы головного мозга и жидких тканей – профилактика обезвоживания.
К тому же вегетативный отдел контролирует пищеварительную, мочевыделительную и репродуктивную функцию. Ни одна внутренняя структура не остается без двойного присмотра – к примеру, одни импульсы замедляют частоту пульса, а иные – учащают сердцебиение. В этом заключается преимущество организма людей перед растительным или же животным миром.
По сути, на протяжении эволюции вегетативные отделы позволили людям приспосабливаться к меняющимся внешним условиям и выживать человеческому роду. В новых обстоятельствах сердечнососудистая и дыхательная система, а также пищеварение обеспечивали внутренние ткани питательными веществами. Это гарантировало сохранность особи. В последующем иннервация усложнялась и видоизменялась. В конечном итоге у современного человека без вегетативной регуляции не происходит ни одного вида деятельности, пусть и на бессознательном уровне.
Структурные особенности системы
В целом, вегетативная нервная регуляция – это сложная комбинация, как по анатомическим, так и функциональным признакам нервных элементов. В первую очередь, специалисты выделяют в ней центральный, а также периферический сегмент. Так, скопления нейронов – особых клеток, образуют своеобразные ядра в толще головного либо спинного мозга. Эти центры несут ответственность за реакцию зрачков, работу пищеварительных и дыхательных отделов.
Особое место отведено гипоталамусу и мозговой лимбической системе, как важным частям вегетативной регуляции. И если первый из них хорошо работает, то у людей железы внутренней и внешней секреции здоровы и вырабатывают биологические вещества в требуемом количестве. Поведенческие реакции также будут здоровыми – эмоции, сновидения, работоспособность.
Тогда как периферическая вегетативная нервная часть – это вегетативные нервы, а также отдельные клетки, либо сплетения. С их помощью регулирующий импульс доходит до требуемой зоны и осуществляется коррекция внутренней среды.

Помимо этого, вегетативная система обязательно рассматривается специалистами как совокупность двух крупных отделов – парасимпатического, а также симпатического. Их различают функциональные обязанности. Так, парасимпатический отдел своими нейромедиаторами – химическими молекулами, регулирует образование слюны, правильность сердечного ритма, параметры давления, моторику петель кишечника.
Тогда как, спинной мозг, где находятся центры симпатической части вегетативного отдела, несет ответственность за противоположные реакции – учащение сердцебиение, частоты дыхания, расслабление желчного пузыря, расширение зрачка. В большинстве случаев автономный отдел преганглионарными волокнами и постганглионарными сплетениями самостоятельно справляется со всеми задачами. Головной мозг далеко не всегда вмешивается в его работу.
Функции системы
Описать все многообразие функций вегетативной системы можно тем, что она регулирует физиологические процессы в тканях и обеспечивает постоянство жизнедеятельности – особь приспосабливается и выживает. Для этого нервные импульсы поступают непосредственно в иннервируемый орган, сосуд либо участок ткани. К примеру, гладкомышечные клетки кишечника.
Регулированию подлежат все метаболические процессы – приспособление к снижению/повышению концентрации гормонов, пищеварительных ферментов. Это адаптационно-трофическая вегетативная функция. В ее основе лежит транспорт питательных веществ, их перемещение внутрь клеток. Одни активизируют метаболизм, другие усиливают трофику тканей.
Функции симпатических волокон:
- изменение сокращения сердечной мышцы, возрастание ритма;
- повышение систолического давления;
- расширение диаметра бронхов, а также зрачков;
- снижение тонуса гладких мышц в кишечнике;
- повышение скорости свертывания крови и активности ферментов.
Функции парасимпатических волокон:
- снижение сердечного ритма;
- уменьшение артериального давления;
- обеспечение бронхоспазма;
- повышение тонуса мышечного слоя стенки кишечника.
При этом не следует рассматривать перечисленные функции систем в отдельности – они тесно взаимодействуют. Без одной из них не будут осуществляться и другие виды вегетативного контроля.
Формирование и развитие системы
После оплодотворения яйцеклетки в женском организме, происходит слияние двух клеток – развивается плод. Формирование непосредственно нервной системы происходит уже на 3–4 недели роста малыша.
Из особых первичных клеток нейробластов постепенно формируются симпатические узлы – для локализации в полостных органах. К примеру, в районе сердца и кишечника. Подобное формирование в период эмбриогенеза заканчивается к началу 8–9 недели.

Парасимпатический сегмент изначально размещается в районе лицевой части будущего головного мозга – из тех же нейробластов. В этот же период происходит закладка вегетативных спинномозговых центров – из симпатобластов.
Высшая вегетативная регуляция начинается с образования головного мозга. Требуемые параметры приобретает лимбическая подсистема и гиппокамп, гипоталамус и кора мозговых полушарий. Дальнейшая дифференциация вегетативных структур осуществляется по мере роста плода.
Поэтому так важно для будущей матери избегать малейших негативных воздействий – приема медикаментов, алкогольной и табачной продукции, токсических растворов. В противном случае высок риск появления различных отклонений в дальнейшем функционировании нервной системы ребенка. При тяжелых вегетативных поражениях дети становятся инвалидами и требуют специализированного наблюдения и лечения.
Отличительные признаки систем
Помимо непосредственно функциональных обязанностей, для сравнительной характеристики соматической и вегетативной нервной системы присуще иное расположение ядер – в головном, а также спином мозге. Они имеют очаговый, прерывистый характер у симпатического, а также парасимпатического отдела, но размещены равномерно в соматическом сегменте.
Иные различия вегетативной и соматической систем:
- иннервация гладкой мускулатуры осуществляется непроизвольно;
- в ряде органов наблюдается мощное сокрушение мышечных групп – к примеру, в сфинктерах;
- соматический отдел контролирует мускулатуру скелетного строения – побуждает ее к быстрым, а также сознательным сокращениям;
- вегетативное влияние обеспечивает трофику;
- очаговый выход вегетативных корешков, как от внутричерепных, так и от спинномозговых ядер – принцип сегментарности постганглионарными симпатическими, а также парасимпатическими периферическими волокнами не соблюдается;
- различие присутствует и в строении рефлекторных дуг, к тому же вся деятельность вегетативного отдела основана не только на высших центральных, но и на периферических дугах.
Специалистами было выяснено, что у вегетативных отделов присутствует ряд примитивных черт – диффузность размещения нейронов, однообразие форм, а также размеров нейронов, меньший калибр волокон из-за отсутствия миелиновой оболочки. Поэтому и скорость иннервации существенно ниже. К тому же вегетативный отдел обладает меньшей избирательностью к гормонам и механизму метаболизма.
Признаки расстройства вегетативных структур
Сложность строения и функционирования как парасимпатической, так и симпатической вегетативной системы обусловливает, что сбой в одном их сегменте, будет негативно сказываться на деятельности всего организма.
Заподозрить появление расстройства в иннервируемом органе можно по ряду признаков. К примеру, при частых симптомах сухости во рту, дрожи в кистях рук либо треморе век. Иногда на вегетативные отклонения в системе указывают проблемы со сном – трудности засыпания, прерывистость ночного отдыха, разбитость в утренние часы.
Характерными будут колебания артериального давления и температуры – без предшествующего развития гипертонической болезни либо инфекционного процесса. Человек ощущает приливы жара и зябкости, головные боли и ухудшение зрения – затем самочувствие улучшается.
В стрессовых ситуациях сбои здоровья различимы четче – резкие расстройства сердечнососудистых и пищеварительных функций, сбои в эндокринных либо дыхательных органах. Симптомы выглядят, как нарастание одышки, позывы на тошноту, рвоту, боли в районе сердца, желудка.
На подобные сигналы организма необходимо обращать пристальное внимание. В противном случае вегетативные расстройства переходят в серьезные заболевания внутренних органов, с последующими осложнениями. Вылечить сбои в парасимпатическом либо симпатическом отделе системы намного легче на начальном этапе их появления. На помощь приходят силы природы – народные рецепты отваров и настоев, современные аптечные средства, санаторно-курортное оздоровление, к примеру, гидротерапия, солнечные ванны, ароматерапия.
Контрольная работа №1
1. Раскройте содержание в развернутой письменной форме.
1.1. Место и роль адренорецепторов в эфферентной иннервации. Типы адренорецепторов и их функциональное значение. Классификация лекарственных средств, влияющих на адрен орецепторы.
Эфферентный отдел периферической нервной системы может быть разделен на два основных подотдела: вегетативную, или автономную, и соматическую нервные системы. Вегетативная нервная система преимущественно автономна, т.е. независима от прямого контроля сознания. Она имеет дело преимущественно с висцеральными функциями -сердечная деятельность, кровоснабжение различных органов, пищеварение и т.д., которые необходимы для поддержания нормальной жизнедеятельности организма. Соматическая нервная система преимущественно неавтономна, т.е. контролируется сознанием человека и имеет дело с такими функциями, как движение тела, сохранение позы и дыхание [1].
Нервные пути вегетативной нервной системы состоят из двух отрезков - преганглионарного и постганглионарного, которые соединяются в ганглиях, представляющих собой скопление нервных клеток. Кроме того, вегетативная нервная система состоит из симпатического и парасимпатического отделов. Важным отличием симпатической и парасимпатической нервных систем является то, что медиатором в постганглионарных симпатических волокнах является норадреналин (поэтому они часто называются адренергическими), а медиатором парасимпатической нервной системы является ацетилхолин (поэтому они называются холинергическими) [1].
Симпатическая нервная система является важным регулятором активности сердца и периферических сосудов, в особенности в ответ на стресс. Специфический эффект стимуляции симпатических нервов опосредуется выделением в нервных окончаниях норадреналина, который и возбуждает адренорецепторы на постсинаптической мембране. Кроме того, в ответ на стресс из мозгового слоя надпочечников выбрасывается адреналин, который кровью доставляется в органы-мишени [1].
Адренорецепторы различаются по чувствительности к одним и тем же веществам.
Выделяют α-адренорецепторы и β-адренорецепторы. α-Адренорецепторы подразделяют на α1 -адренорецепторы и α2 -адренорецепторы, а среди β-адренорецепторов различают β1 -, β2 - и β3 -адренорецепторы.
На постсинаптической мембране эффекторных клеток локализованы α1 - и β1 -адренорецепторы (постсинаптические рецепторы). Эти рецепторы стимулируются норадреналином, который высвобождается из окончаний адренергических волокон.
α2 - и β2 -Адренорецепторы могут быть внесинаптическими и пресинаптическими, Внесинаптические α2 - и β2 -адренорецепторы локализованы вне синапсов, на мембране эффекторных клеток, не получающих симпатическую иннервацию (неиннервируемые рецепторы). Они возбуждаются циркулирующим в крови адреналином, который выделяется из хромаффинных клеток мозгового вещества надпочечников, α2 -адренорецепторы, кроме того, могут возбуждаться циркулирующим в крови норадреналином. Находящиеся на пресинаптической мембране (пресинаптические) α2 -адренорецепторы регулируют высвобождение норадреналина по принципу отрицательной обратной связи. Стимуляция этих рецепторов норадреналином или другими веществами с α2 -адреномиметической активностью тормозит высвобождение норадреналина из варикозных утолщений. В отличие от пресинаптических α2 -адренорецепторов стимуляция пресинаптических β2 -адренорецепторов приводит к повышению выделения норадреналина [2].
Основные эффекты, вызываемые стимуляцией адренорецепторов, представлены в табл. 1 [2].
Подтипы адренорецепторов и эффекты, вызываемые их стимуляцией
- силы сердечных сокращений;
- частоты сердечных сокращений;
Расслабление гладких мышц сосудов, бронхов, матки;
расширение кровеносных сосудов;
снижение тонуса и сократительной активности миометрия
1.2. Средства для неингаляционного наркоза: пропанидид, кетамин, пропофол, тиопентал, натрия оксибутират. Особенности неингаляционного наркоза. Комбинированный наркоз.
Современные средства для неингаляционного наркоза имеют латентный период короче, чем ингаляционные общие анестетики. При этом для использования неингаляционных средств не нужна сложная и дорогостоящая аппаратура, нет необходимости очистки воздуха от выдыхаемого ингаляционного анестетика. В отличие от ингаляционного, внутривенный наркоз протекает практически без стадии возбуждения. Высокая липофильность позволяет препаратам этой группы легко проникать в мозг. Необходимо учитывать, что в случае использования средств для внутривенного наркоза управляемость глубиной наркоза низкая.
Современные препараты для внутривенного наркоза по продолжительности действия могут быть разделены на следующие группы [1, 3]:
1) кратковременного действия (продолжительность наркоза при внутривенном введении до 15 мин) ‒ пропанидид, пропофол, кетамин ;
2) средней продолжительности действия (продолжительность наркоза 20-30 мин) ‒ тиопентал-натрий ;
3) длительного действия (продолжительность наркоза 60 мин и более) ‒ натрия оксибутират .
Пропанидид представляет собой маслянистую жидкость, все остальные препараты являются порошкообразными веществами. Применяют средства для неингаляционного наркоза в растворах.
Тиопентал-натрий (пентотал-натрий) при внутривенном введении вызывает наркоз примерно через 1 мин без стадии возбуждения. Продолжительность наркоза 20-30 мин. Кратковременность эффекта связана с перераспределением препарата в организме, в частности с накоплением его в больших количествах в жировой ткани. Инактивация тиопентал-натрия происходит постепенно в печени. При введении препарата могут наблюдаться судорожные подергивания мышц. У некоторых больных возникает ларингоспазм. Тиопентал-натрий следует вводить очень медленно, так как при быстром нарастании концентрации проявляется его угнетающее действие на дыхательный и сосудодвигательный центры, а также на сердце. Быстрое введение препарата может привести к апноэ и коллапсу. Тиопентал-натрию свойственно и некоторое местное раздражающее действие. Применяют его для вводного наркоза или при кратковременных оперативных вмешательствах [3].
Длительное действие оказывает натрия оксибутират . Является синтетическим аналогом естественного метаболита, обнаруженного в ЦНС. Хорошо проникает через гематоэнцефалический барьер. Оказывает седативное, снотворное, наркотическое и антигипоксическое действие. Анальгетический эффект выражен в небольшой степени. При сочетании с другими средствами для наркоза и анальгетиками натрия оксибутират повышает их активность, не влияя на токсичность. Вызывает выраженную релаксацию скелетных мышц. Повышает устойчивость тканей мозга и сердца к гипоксии. Наркотическая активность натрия оксибутирата невелика, поэтому его вводят в больших дозах. Стадия возбуждения обычно не возникает. При быстрой инфузии, однако, возможны возбуждение и судорожные сокращения мышц. Стадия хирургического наркоза наступает через 30-40 мин после внутривенной инъекции (вводят препарат медленно). Длительность наркоза 1,5-3 ч. Натрия оксибутират вводят также внутрь. Он хорошо всасывается из тонкой кишки и через 40-60 мин вызывает наркоз, который продолжается 1,5—2,5 ч. Токсичность натрия оксибутирата низкая. Отрицательного влияния на кровообращение и дыхание в наркотических дозах не оказывает. Возможна рвота. Иногда развивается гипокалиемия. При передозировке наблюдается угнетение центра дыхания.
Применяют препарат главным образом для вводного и базисного наркоза, для обезболивания родов, при гипоксическом отеке мозга, в качестве противошокового средства, с целью получения успокаивающего и снотворного эффектов [3].
Особое место занимает кетамин (кеталар, калипсол) ‒ порошкообразное вещество, применяемое в виде растворов для внутривенного и внутримышечного введения. Кетамин вызывает лишь общее обезболивание и легкий снотворный эффект с частичной утратой сознания (состояние типа нейролептанальгезии). Хирургический наркоз под влиянием кетамина не развивается. При внутривенном введении эффект наступает через 30-60 с и продолжается 5-10 мин, а при внутримышечном ‒ через 2-6 мин и продолжается 15-30 мин. Инактивируется кетамин в печени.
Скелетные мышцы на фоне действия кетамина не расслабляются; могут наблюдаться непроизвольные движения конечностей. Глоточный, гортанный, кашлевой рефлексы сохранены. Артериальное давление повышается, частота пульса увеличивается. Может наблюдаться гиперсаливация. Незначительно повышается внутриглазное давление.
Применяют кетамин для введения в наркоз, а также при проведении кратковременных болезненных манипуляций (например, при обработке ожоговой поверхности и т.п.) [3].
Комбинированный наркоз
В современной анестезиологии крайне редко ограничиваются введением одного средства для наркоза. Обычно сочетают 2-3 препарата. Комбинируют средства для ингаляционного наркоза с ингаляционно или неингаляционно вводимыми препаратами.
Целесообразность таких комбинаций заключается в том, что устраняется стадия возбуждения и осуществляется быстрое введение в наркоз. Так, наркоз часто начинают с внутривенного введения тиопентал-натрия, обеспечивающего быстрое развитие наркоза без стадии возбуждения. Особенно показано сочетание со средствами для неингаляционного наркоза препаратов с выраженной стадией возбуждения (например, эфира).
Преимущество комбинированного наркоза заключается также в том, что концентрации (дозы) компонентов смеси ниже, чем при использовании для наркоза одного средства, поэтому удается уменьшить их токсичность и снизить частоту побочных эффектов.
Одной из часто используемых в настоящее время комбинаций средств для наркоза является следующая: барбитурат или другой быстродействующий препарат для неингаляционного наркоза + фторотан (или энфлуран, изофлуран) + азота закись.
Независимо от характера сочетаний важно, чтобы основные этапы операции проводились на фоне действия хорошо управляемых препаратов (газообразные средства для наркоза, фторотан, энфлуран, изофлуран, десфлуран) [3].
2. Выпишите рецепты (в тех рецептах, где это необходимо, на полях справа приведите расчеты). Письменно дайте информацию к каждому рецепту, ответив на следующие вопросы:
• к какой (или каким) фармакотерапевтической группе относится препарат;
• показания (основные, кратко);
• механизм фармакологического действия (кратко);
• основные побочные эффекты (наиболее типичные);
• синонимы (если имеются);
• если рецепт состоит из нескольких препаратов, обоснуйте целесообразность данной комбинации;
• возможность замены.
2.1. Селективный α 1 -адреноблокатор.
2.2. Никетамид.
2.4. Лития оксибутират.
2.5. Этилморфина гидрохлорид с тетракаином ‒ капли
Rp.: Prazosini 0,001
D.t.d. №30 in tabulettis
S . По 1 таблетке 3 раза в день.
Фармакотерапевтическая группа : α1 -адреноблокатор (селективный).
Механизм фармакологического действия : блокирует сосудосуживающее действие медиатора (норадреналина) без влияния на другие виды его деятельности.
Синонимы : Адверзутен, Минипресс, Ново-Празин, Польпрессин, Празозинбене, Прайтор.
Возможная замена : теразозин, доксазозин, тамсулозин.
Rp.: Nicethamidi 1 ml
D.t.d. №10 in ampullis
S . Вводить подкожно по 1 мл 2 раза в день.
Фармакотерапевтическая группа : аналептическое средство.
Показания : Острый коллапс и асфиксия (в том числе асфиксия новорожденных), шоковые состояния, возникающие во время хирургических вмешательств и в послеоперационном периоде, при понижении сосудистого тонуса и ослабления дыхания у больных с инфекционными заболеваниями и у выздоравливающих; иногда при отравлении снотворными, наркотическими анальгетиками и барбитуратами [4].
Механизм фармакологического действия : возбуждает непосредственно сосудодвигательный центр (особенно при его пониженном тонусе), а также опосредованно дыхательный центр в результате стимуляции хеморецепторов каротидного синуса [4].
Основные побочные эффекты: Рвота, нарушение сердечного ритма, болезненность в месте введения, аллергические реакции.
Возможная замена: бемегрид, сульфокамфокаин.
Rp.: Tabulettam Phenibuti 0,25
S . По 1 таблетке 3 раза в день.
Фармакотерапевтическая группа : ноотропный препарат.
Показания : астенические и тревожно-невротические состояния, беспокойство, тревога, страх, бессонница, премедикация; используют также при болезни Меньера, головокружениях, связанных с дисфункцией вестибулярного аппарата, для профилактики укачивания, купирования абстинентного синдрома; детям назначают при заикании [4].
Механизм фармакологического действия : обладает элементами ноотропной активности – активизирует утилизацию глюкозы мозгом, синтез макроэргических веществ, РНК, белков и фосфолипидов мембран; является синтетическим аналогом ГАМК (гамма-аминомасляной кислоты) – эндогенного тормозного нейромедиатора [4].
Основные побочные эффекты: При первых приемах или при передозировке может наблюдаться сонливость и тошнота.
Возможная замена: гамма-аминомасляная кислота, пикамилон, пантогам.
Rp.: Solutionis Lithii oxybutyratis 20% - 2 ml
D.t.d. №10 in ampullis
S. По 2 мл в/м.
Фармакотерапевтическая группа : нормотимические препараты (препараты лития).
Показания : гипоманиакальные и маниакальные состояния и профилактика приступов аффективных расстройств; также применяют при психопатиях, неврозах, органических и других заболеваниях с рецидивирующими аффективными расстройствами.
Механизм фармакологического действия : ионы лития блокируют транспорт ионов натрия в нервных и мышечных клетках; под влиянием лития усиливается внутриклеточное дезаминирование норадреналина и уменьшается количество свободного норадреналина, действующего на адренорецепторы мозга, возрастает серотонинергическая активность.
Основные побочные эффекты: чаще наблюдаются в начале лечения и выражаются в треморе пальцев, чувстве усталости, сонливости, нарушении координации, повышенной жажде, диспепсических явлениях, диарее и др.
Синонимы : Лития оксибат.
Возможная замена : Лития карбонат.
2.5. Rp.: Aethylmorphini hydrochloridi 0,2
Tetracaini 0,05
Solutionis Natrii chloride isotonicae 10 ml
Misce . Da . Signa . По 1 капле 2 раза в день в правый глаз.
Расчет массы натрия хлорида для изотонирования :
Изотонический коэффициент по натрию хлориду для этилморфина гидрохлорида [5]:
Количество натрия хлорида эквивалентное 0,2 г этилморфина гидрохлорида:
1,0 этилморфина гидрохлорида – 0,15 натрия хлорида
0,2 этилморфина гидрохлорида – 0,03 натрия хлорида
Изотонический коэффициент по натрию хлориду для тетракаина [5]:
Количество натрия хлорида эквивалентное 0,05 г тетракаина:
1,0 тетракаина – 0,18 натрия хлорида
0,05 тетракаина – 0,009 натрия хлорида
На 10 мл раствора необходимо натрия хлорида 0,09 г.
Количество натрия хлорида, необходимое для изотонирования:
0,09 – 0,03 – 0,009 = 0,051 ≈ 0,05 г.
Фармакотерапевтическая группа : наркотический анальгетик + местный анестетик.
Читайте также:


