Велаксин при головной боли
Н. В. Латышева
Е. Г. Филатова, доктор медицинских наук, профессор
ММА им. И. М. Сеченова, Москва
Хроническая ежедневная головная боль (ХЕГБ) беспокоит пациентов более 15 дней в месяц на протяжении более трех месяцев. ХЕГБ не является самостоятельной нозологической формой, а представляет синдром, включающий различные первичные и вторичные головные боли (ГБ). Распространенность ХЕГБ в популяции составляет примерно 3–5%, а в специализированных клиниках доля пациентов с ежедневной или почти ежедневной ГБ достигает 70–80%. Заболевание обуславливает значительное снижение качества жизни, нарушает социальную активность пациентов и их трудоспособность, а также представляет собой сложную проблему с точки зрения терапии.
Самыми частыми формами ХЕГБ являются хроническая мигрень (ХМ), хроническая ГБ напряжения (ХГБН) и абузусная ГБ. ХЕГБ в большинстве случаев является осложнением длительно существующей эпизодической ГБ и лишь у немногих пациентов с момента своего дебюта принимает ежедневный или почти ежедневный характер.
Среди факторов хронизации ГБ описаны ожирение, женский пол, исходно частая ГБ (более 1 раза в неделю), чрезмерное употребление анальгетических препаратов (более 10 дней в месяц) и эмоциональный стресс. У более чем половины пациентов с ХЕГБ выявляются нарушения сна и расстройства настроения депрессивного и тревожного характера.
Патогенез ХЕГБ в настоящее время изучен недостаточно. Предполагаются два основных механизма, которые могут лежать в основе хронизации разных форм ГБ — сенситизация ноцицептивных структур и снижение активности антиноцицептивных отделов центральной нервной системы (ЦНС).
При мигрени периферическая сенситизация происходит в сенсорных нейронах, иннервирующих внутримозговые сосуды и оболочки. Центральная сенситизация (ЦС) описана в спинномозговом ядре тройничного нерва, куда стекаются импульсы от мозговых оболочек и кожи лица. Многие пациенты испытывают неприятные ощущения во время и между приступами мигрени при бритье, расчесывании волос, ношении очков и украшений. Ощущение боли при воздействии неболевого раздражителя обозначается как аллодиния, которая в настоящее время часто коррелирует с центральной сенситизацией. Различают статическую (от давления или укола) и динамическую (от поглаживания) аллодинию. При дальнейшем течении некупированного приступа мигрени включаются более центральные отделы ноцицептивной системы. Уже при активации таламуса аллодиния становится двусторонней, ее зона может с головы и лица переходить на руку. При эпизодической мигрени в течение 72 часов включаются антиноцицептивные системы, которые приводят к купированию мигренозного приступа.
Со временем признаки ЦС исчезают не полностью после окончания приступа, и постепенно формируется стабильная ЦС, которая поддерживает боль в хроническом состоянии. При этом нейроны в ЦНС становятся слабо или совсем нечувствительными к периферическим воздействиям. На этом этапе терапевтические воздействия должны быть направлены на усиление нисходящих антиноцицептивных влияний — on/off-нейроны в околоводопроводном сером веществе (ОСВ), антиноцицептивная функция которых нарушена при ХЕГБ.
В настоящее время для профилактики ГБ активно используются антидепрессанты. Показано, что анальгетическое действие трициклических антидепрессантов (ТЦА) не зависит от их антидепрессивного действия и обусловлено их сочетанным серотонинергическим и норадреналинергическим действием. В то же время более безопасные селективные ингибиторы обратного захвата серотонина (СИОЗС) недостаточно эффективны в лечении мигрени и ХГБН [21].
Венлафаксин, структурно новый антидепрессант, по химической структуре отличен от ТЦА, однако также угнетает обратный захват серотонина (5-HT) и норадреналина. Кроме того, по сравнению с амитриптилином препарат действует более специфично на эти рецепторы. Венлафаксин облегчает головную боль так же эффективно, как и ТЦА, но вызывает гораздо меньше побочных эффектов. В ходе двойного слепого исследования профилактического эффекта СИОЗС и венлафаксина при мигрени было показано, что процент пациентов, у которых было достигнуто значительное улучшение в группе венлафаксина, превысил этот показатель в группе СИОЗС.
Эффективность венлафаксина неоднократно доказана в исследованиях пациентов с различными формами нейропатической боли: при диабетической полинейропатии, нейропатии после химиотерапевтического лечения и др. Проведен также ряд исследований профилактического действия венлафаксина при хронической мигрени и ХГБН.
Целью настоящей работы явилось изучение феномена ЦС при ХЕГБ, ее роли в хронификации ГБ и эффективности венлафаксина для ее урежения.
Материал. В исследовании приняли участие 69 пациентов с ХЕГБ и 30 пациентов с эпизодической мигренью (ЭМ) в соответствии с критериями ICHD-2, а также 15 участников группы контроля с ГБ не чаще 1 дн./мес. Группа ХЕГБ была представлена пациентами с ХМ, ХГБН и пациентами со смешанными формами ГБ.
Методы исследования. Всем пациентам была предложена анкета для изучения демографических данных, анамнеза и клинической картины головной боли. Кроме того, пациенты заполняли анкету для изучения симптомов аллодинии.
Статическая аллодиния (СА) исследовалась при помощи альгометра в 5 парах симметричных точек на голове и шее (лоб, висок, темя, задняя поверхность шеи, плечо/трапециевидная мышца).
Порог боли от давления определяется как сила давления, которая необходима для вызывания субъективно неприятного/болезненного ощущения. Использовался ручной альгометр (Commander Algometer™, JTech). В каждой точке выполнялось два последовательных измерения с интервалом в 20 секунд. Для анализа использовалось среднее значение.
СА также измерялась при помощи уколов механическим стимулято ром (Neuropen®, Owen Mumford) с нанесением силы укола в 40 г в тех же точках. Выраженность боли или неприятного ощущения измеря лась по 100-бальной шкале.
Феномен wind-up (временная суммация боли) исследовался при помощи нанесения серии из 10 уколов на участок кожи площадью 1 см 2 на лбу, виске и шее стимулятором Neuropen®. Участники исследования оценивали силу единичного укола и всей серии.
Мигательный рефлекс (МР) вызывался при помощи электрической стимуляции правого надглазничного нерва, подаваемой через поверхностные электроды диаметром 5 мм. Катод располагался над наглазничным отверстием, а анод приблизительно на 2 см выше на коже лба. Наносились одиночные электрические стимулы прямоугольной формы длительностью 0,2 мс с произвольными интервалами не менее 30 секунд для минимизации габитуации и регистрировались четкие R1-, R2- и R3-компоненты мигательного рефлекса. В работе анализировались пороги возникновения позднего компонента R3, для которого описан полисинаптический путь, проходящий от ствола головного мозга до спинального ядра тройничного нерва и затем в латеральную ретикулярную формацию.
Ноцицептивный флексорный рефлекс (НФР) регистрировался при стимуляции правого икроножного нерва трендами длительностью 20 мс и частотой 300 Гц с произвольными интервалами не менее 15 секунд. Катод располагался в проекции нерва, а анод на 2 см ниже в области латеральной лодыжки. Референтный электрод располагался над сухожилием двуглавой мышцы бедра, а заземляющий — на середине голени. Регистрировался порог возникновения R3-ответа и порог субъективной болевой чувствительности (когда пациент болевое ощущение оценивал на 5 баллов по 10-бальной шкале ВАШ). Также рассчитывалось соотношение порог боли/порог рефлекса. R3-компонент замыкается через ретикулярную формацию ствола мозга.
Результаты анализировались при помощи компьютерного пакета Statistica (U-тест Манна–Уитни для сравнения групп, корреляционный тест Спирмена, точный тест Фишера для сравнения пропорций, например, распространенности аллодинии). Все показатели приведены в формате Х ± SD.
Результаты исследования
1. Клинические и демографические характеристики пациентов
Группа ХЕГБ была представлена 28 пациентами с ХМ, 31 пациентом с ХГБН и 10 пациентами со смешанными формами ГБ (ХМ или ХГБН в сочетании с цервикогенной ГБ) в соответствии с критериями ICHD-2. В группу вошли 57 женщин и 12 мужчин, средний возраст 40 лет. Средняя частота ГБ составила 25 дн./мес, сила боли 7 баллов. При общей длительности ГБ в анамнезе в 19 лет, наши пациенты страдали ХЕГБ в среднем 6 лет. О злоупотреблении анальгетическими препаратами сообщили 33% пациентов (табл. 1).
Таблица 1
Клинические и демографические характеристики пациентов и контроля
| ХЕГБ | ЭМ | Контроль | |
| Число пациентов | 69 | 30 | 15 |
| Пол, ж:м | 57:12 | 28:2 | 10:5 |
| Возраст, лет | 40,1 ± 12,3 | 37,3 ± 10,5 | 43,1 ± 18,1 |
| Частота ГБ, дн./мес | 25,2 ± 6,0 | 4,7 ± 1,3 | |
| Сила боли, ВАШ | 7,1 ± 1,9 | 7,7 ± 1,2 | |
| Длительность ГБ, лет | 18,2 ± 12,7 | 16,3 ± 9,7 | |
| Длительность ХЕГБ, лет | 5,7 ± 7,0 | – | |
| ХМ:ХГБН:Смеш. | 28:31:10 | – | |
| Абузус | 20 (33%) | 1 | |
| Кожная аллодиния (анкета) | 79% | 46% | |
| Сила боли во время исследования, ВАШ | 2,3 ± 1,9 | 0 |
По данным анкеты аллодинии, в группе ХЕГБ распространенность ЦС во время интенсивной ГБ составила 79%.
2. Статическая аллодиния, феномен wind-up и порог R3 МР и НФР у пациентов с ХЕГБ
Чувствительность к боли от давления достоверно выше в группе ХЕГБ во всех точках, кроме висков, к боли от укола и wind-up во всех точках, кроме лба, по сравнению с группой контроля.
Для удобства расчетов использовался индекс альгометрии. Это сумма порогов боли от давления во всех точках. Так как нет данных о том, какой порог боли от давления указывает на аллодинию, мы использовали группу контроля для получения нормативных данных. Об аллодинии свидетельствует индекс, выше которого указали свои пороги 95% участников группы контроля (в нашем исследовании пороговый индекс альгометрии составил 41,9 фунта). Таким образом, распространенность ЦС во время наименьшей боли в группе ХЕГБ составила 70%. Группа ХЕГБ достоверно отличалась от контроля по индексу альгометрии.
Более того, отсутствие различий в болевых порогах справа и слева, независимо от преимущественной стороны боли при ее усилениях, говорит о стабильности ЦС, так как в приступе мигрени аллодиния всегда развивается на стороне боли и переходит на противоположную сторону, шею и плечи только при длительных приступах.
Для определения нормативных данных порога R3 МР это исследование было проведено на 15 участниках группы контроля. По нашим данным, порог R3-компонента составил 9,6 ± 1,5 мА. В группе ХЕГБ выявлено достоверное снижение порога R3 мигательного рефлекса (7,6 ± 2,16 мА). Нормативный порог НФР составил 10,3 ± 1,7 мА, порог боли 9,8 ± 1,8 мА. В группе ХЕГБ выявлено достоверное снижение порога НФР (9,0 ± 2,2 мА) и порога боли (6,2 ± 1, мА).
3. Статическая аллодиния, феномен wind-up в группе сравнения с ЭМ
Для изучения закономерностей развития ЦС и ее влияния на хронизацию ГБ была исследована группа пациентов с ЭМ с частотой ГБ более 2 дн./мес и менее 15 дн./мес. Возраст пациентов, длительность заболевания и сила боли не отличались в группах ЭМ и ХЕГБ. Средняя частота приступов составила 5,2 дн./мес.
У пациентов группы ЭМ выявлены достоверно более высокие пороги боли от давления и укола во всех точках по сравнению с группой ХЕГБ. Пороги боли при ЭМ достоверно не отличались от показателей контрольной группы испытуемых, что свидетельствует об отсутствии СА при эпизодической мигрени в межприступном периоде. Средний индекс wind-up, напротив, достоверно не различался при ЭМ и ХЕГБ.
Таким образом, группа ЭМ отличается от контроля только по индексу wind-up и от ХЕГБ по остальным показателям сенситизации.
Пациентов с ЭМ можно разделить на 2 подгруппы по индексу wind-up: с высоким и низким индексом. Точка раздела была определена аналогично точке раздела для альгометрии и составила 14,1. В подгруппе с более высоким wind-up выявлена более высокая частота приступов (7,5 дн./мес vs. 3,5 дн./мес) и меньшая длительность заболевания (12,1 года vs. 19,1 года). В подгруппе пациентов, указывающих на признаки кожной аллодинии в анамнезе, выявлена большая частота приступов.
4. Терапия венлафаксином
В качестве профилактического лечения головной боли 18 пациентам из вышеописанной группы пациентов с ХЕГБ был назначен прием венлафаксина (Велафакс®) курсом продолжительностью 1,5 месяца. Схема дозирования: 37,5 мг (18,9 мг × 2 раза в сутки) в течение 7 дней с последующим повышением до 75 мг (37,5 мг × 2 раза в сутки).
5 пациентов (28%) закончили исследование преждевременно: 3 пациента (17%) из-за побочных эффектов, развившихся на стадии титрования препарата и помешавших поднять дозу до минимальной терапевтической; 2 пациента (11%) — из-за отсутствия эффекта от лечения. 13 пациентов прошли полный курс лечения и были включены в анализ. Им также было проведено повторное обследование (аналогичное описанному выше) после окончания 6-недельного курса лечения.
По результатам лечения было достигнуто достоверное снижение средней силы боли (с 6,6 до 4 баллов) и ее частоты (с 26 до 12 дн./мес). У 10 пациентов (77%) частота боли снизилась достоверно, а 54% пациентов отметили как минимум 50%-ное урежение ГБ. У 70% пациентов было достигнуто урежение ГБ более чем на 10 дн./мес (табл. 2).
Таблица 2
Результаты лечения венлафаксином
| До лечения | После лечения | р | |
| Сила боли, ВАШ | 6,6 ± 1,1 | 4,0 ± 2,0 | 0,0005* |
| Частота ГБ | 26,0 ± 4,7 | 12,0 ± 10,7 | 0,0001* |
| Количество анальгетиков | 21,8 ± 22,7 | 5,1 ± 9,3 | 0,005* |
| Индекс альгометрии | 40,6 ± 12,8 | 53,8 ± 13,1 | 0,0003* |
| Индекс боли от укола | 48,2 ± 49,8 | 25,3 ± 42,2 | 0,117 |
| Индекс wind-up | |||
| Аллодиния | 3,7 ± 1,6 | 1,1 ± 1,2 | 0,003* |
| МР R3 | 7,3 ± 1,9 | 9,2 ± 3,0 | 0,023* |
| НФР порог боли | 6,6 ± 4,13 | 7,6 ± 2,6 | 0,100 |
| НФР порог рефлекса | |||
| НФР боль/рефлекс | 0,57 ± 0,2 | 0,8 ± 0,2 | 0,002* |
* достоверные различия.
Заметное снижение частоты и интенсивности ГБ позволило пациентам сократить количество принимаемых анальгетиков (с 21,8 до 5,1 таблетки в месяц), что значительно снижает риск развития абузусной ГБ.
Кроме того, в ходе лечения было достигнуто достоверное повышение индекса альгометрии до нормальных значений и уменьшение выраженности и распространенности аллодинии. У 54% пациентов клинические признаки аллодинии исчезли полностью.
По данным нейрофизиологических исследований, порог R3 МР достоверно повысился и достиг нормального диапазона значений (с 7,3 до 9,2 мА). Пороги боли и рефлекса НФР, а также соотношение порог боли/порог рефлекса также имели тенденцию к повышению, но не достигли нормальных значений.
78% пациентов указали на наличие побочных эффектов в ходе лечения. Наиболее частыми среди них были: тошнота, урежение стула, нарушение концентрации внимания, снижение аппетита. У большинства пациентов эти эффекты были легкими и быстро проходящими. Они развивались в большинстве случаев в течение первой недели приема (на субтерапевтической дозе в 37,5 мг) и исчезали в среднем через 5–7 дней, что не препятствовало повышению дозы до терапевтической.
Обсуждение
В группе пациентов с ХЕГБ выявлена сенситизация центральных ноцицетивных структур — статическая аллодиния, которая сохраняется даже в период наименьшей боли или ее отсутствия. В то же время при ЭМ у большинства пациентов в межприступном периоде аллодиния отсутствует. Однако в группе ЭМ выявляются также пациенты с повышенным индексом wind-up, т. е. те, у кого признаки сенситизации проявляются даже в межприступном периоде. У таких пациентов отмечена более высокая частота приступов и меньшая длительность заболевания. Можно сделать вывод о том, что со временем элементы ЦС не полностью исчезают после окончания мигренозного приступа и пациент становится более восприимчивым к следующему приступу, т. е. встает на путь хронизации ГБ. После того как боль приобретает ежедневный или почти ежедневный характер, она существует самостоятельно, независимо от наличия или отсутствия провоцирующих факторов, и поддерживается в результате центральной сенситизации ноцицептивных структур.
Более низкая длительность ЭМ в подгруппе с высоким wind-up говорит о том, что сам фактор длительности заболевания не приводит к хронизации ГБ. Из клинического опыта известно, что некоторые пациенты могут в течение многих лет страдать ЭМ с неизменной частотой приступов. У другой части пациентов частота приступов начинает неуклонно нарастать вскоре после дебюта заболевания. Таким образом, измерение феномена wind-up позволяет выделить пациентов, у которых началась динамика ЭМ в направлении хронизации и трансформации ГБ.
По нашим данным, пациентов с ГБ можно разделить на несколько стадий вне зависимости от диагноза по критериям ICHD-2 (рисунок):
- эпизодическая ГБ с признаками аллодинии только во время приступа;
- эпизодическая ГБ, при которой повышение wind-up сохраняется между приступами;
- ХЕГБ со стабильными признаками ЦС во время усилений боли, фоновой ГБ и безболевом периоде.
Рисунок. Стадии развития ГБ
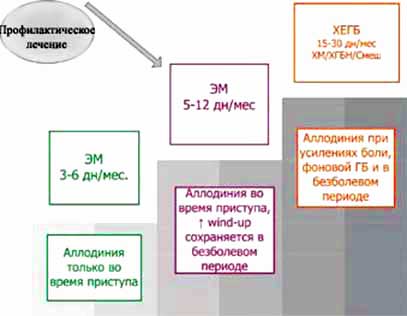
Выявление ЦС с помощью простого метода wind-up у пациентов с эпизодической ГБ в межприступном периоде позволяет выделить группу риска, уже вступившую на путь хронизации ГБ, и является показанием к началу профилактического лечения.
В ходе исследования было показано, что венлафаксин является эффективным и безопасным средством для урежения ГБ. Профилактическое лечение Велафаксом приводит к выраженному клиническому облегчению состояния пациентов, сокращению приема анальгетиков. Позитивный эффект препарата подтверждается уменьшением выраженности аллодинии, а также нормализацией порога болевого R3-компонента мигательного рефлекса, который отражает функциональное состояние стволовых структур и спинномозгового ядра тройничного нерва, участвующих в поддержании ЦС.
По вопросам литературы обращайтесь в редакцию.

Велаксин является антидепрессантом, который относится к группе избирательных блокаторов обратного захвата моноаминов. Молекула его действующего вещества была изобретена в 90-х годах прошлого века. Велаксин — это дженерик с запатентованным названием и улучшенной формулой препарата.

Форма выпуска
Велаксин выпускается в двух формах — в виде капсул и таблеток для приема внутрь. Таблетки и капсулы упакованы в блистеры по 14 штук. Каждая упаковка содержит два блистера.
Дозировка капсул и таблеток различается, и может составлять 37,5, 75 или 150 мг действующего вещества. Точная дозировка указана на упаковке.
Состав
Основное действующее вещество препарата — венлафаксин. Это антидепрессант из группы избирательных ингибиторов обратного захвата серотонина и норадреналина. Венлафаксин — это международное название, которое выпускается разными фирмами под разными торговыми наименованиями, одним из которых является Велаксин. Дозировка препарата рассчитывается по действующему веществу.
Дополнительные вещества необходимы для того, чтобы придать препарату необходимую форму. Велаксин содержит следующие вещества: целлюлозу и ее соединения, тальк, диметикон, соединения натрия, кадмия, калия, кремния и железа. Капсулы, кроме того, содержат желатин и пищевые красители.
Фармакологические свойства
Велаксин и его основное действующее вещество венлафаксин относятся к группе селективных ингибиторов обратного захвата серотонина и норадреналина. Это означает, что препарат препятствует поступлению серотонина и норадреналина внутрь клеток, повышая тем самым их концентрацию в центральной нервной системе. Таким образом возрастает количество двух медиаторов-моноаминов из трех.
Моноамины — это вещества в головном мозге, которые улучшают настроение, уменьшают тревожность, помогают бороться со стрессом. Снижение их концентрации приводит к развитию депрессии и тревожно-фобического расстройства. В большей степени на настроение влияют серотонин и норадреналин. Велаксин помогает бороться с депрессией и тревогой путем повышения количества этих веществ в головном мозге.
Отличительной особенностью данного препарата является отсутствие влияния на обмен дофамина, что снижает риск возникновения многих побочных эффектов. Кроме того, средство в меньшей степени, чем другие антидепрессанты влияет на парасимпатическую вегетативную нервную систему.
Фармакокинетика
Венлафаксин после орального приема практически полностью метаболизируется в печени. 16% переводится в N-дидесметилвенлафаксин (DDV) и 56% метаболизируется до O-десметилвенлаваксин (ODV). Среди всех метаболитов, ODV фармакологически более активен с более высокой концентрацией и более длинным периодом полувыведения, чем исходное соединение (4-9 ч против 11-13 ч) и терапевтически вносит значительный вклад влиянию VEN. Терапевтические уровни концентрации в плазме VEN обычно колеблются от 30 до 200 нг/мл, в то время как уровни ODV находятся в границах 50 до 500 нг/мл.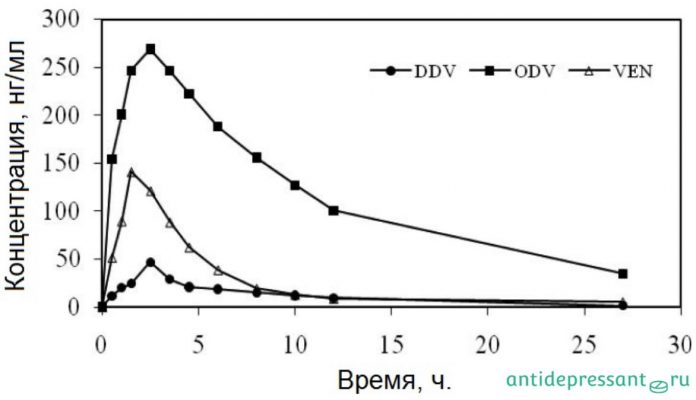
На рисунке изображен профиль концентрации Венлафаксина (VEN), O-десметилвенлаваксина (ODV) и N-дидесметилвенлафаксина (DDV) после однократного приема дозы 75 мг. добровольцем. Спустя полчаса концентрация ODV в плазме значительно превысила концентрацию исходного соединения в плазме. Однако максимальная концентрация зарегистрирована почти через 1 ч в плазме. Таким образом, максимальные концентрации соединений в плазме крови составили 141,2, 268,7 и 47,0 нг/мл, которые наблюдались почти через 1,5, 2,5 и 2,5 ч. после введения VEN, ODV и DDV соответственно. Период полураспада VEN, ODV и DDV был примерно 5.1, 8.2 и 5.4 ч. соответственно.
Показания
Велаксин является сильным антидепрессантом, который входит в топ-12 наиболее эффективных средств этой группы. Его назначение оправдано в следующих случаях:
- Единичный эпизод депрессии тяжелая форма;
- Рекуррентное депрессивное расстройство текущий эпизод депрессии тяжелой степени;
- Рекуррентное депрессивное расстройство ремиссия — с целью профилактики приступов;
- Тревожные расстройства;
- Социальные фобии.
В некоторых случаях велаксин назначают и при других заболеваниях. Например, его используют для профилактики приступов мигрени и лечения некоторых других неврологических заболеваний.
Противопоказания
Перед применением велаксина необходимо убедиться в отсутствии противопоказаний. Они делятся на две группы — абсолютные и относительные. К абсолютным противопоказаниям, при наличии которых велаксин назначать строго запрещено, относятся:
- Гиперчувствительность к компонентам препарата;
- Декомпенсированная печеночная или почечная недостаточность;
- Детский возраст;
- Беременность и кормление грудью;
- Маниакальный синдром;
- Недавний прием антидепрессантов группы ингибиторов моноаминоксидазы;
- Повышение внутриглазного давления;
- Артериальная гипертензия третьей степени.
Относительные противопоказания означают, что прием препарата может навредить здоровью пациента и возможность его назначения должен определить врач. К относительным противопоказаниям относятся заболевания сердца, включая аритмии и нарушения коронарного кровообращения, маниакальный синдром в анамнезе, судорожный синдром в анамнезе, низкая масса тела.
Побочные действия
Велаксин обладает большим количеством побочных эффектов. Часть из них встречается часто, другие же — в единичных случаях. К частым побочным эффектам относится головная боль и тошнота в самом начале приема препарата. Со временем эти симптомы уходят самостоятельно при продолжении приема медикамента. Также часто встречается половая дисфункция, которая может проявляться разными симптомами от снижения либидо до импотенции у мужчин и аноргазмии у женщин.
Реже встречаются нарушения в виде тремора конечностей, головокружения, судорожных проявлений. Также могут быть аллергические реакции и появление сыпи. У предрасположенных к гипертонической болезни пациентов велаксин может вызвать повышение артериального давления вплоть до наступления гипертонического криза.
Достаточно часто встречаются реакции со стороны психического статуса больного. При этом может наблюдаться как возбуждение, так и угнетение центральной нервной системы. Это проявляется либо раздражительностью пациента, либо, наоборот, сонливостью. Возможно нарушение сна с наличием ярких угрожающих сновидений. У пациентов с биполярным аффективным расстройством велика вероятность перехода депрессии в манию или гипоманию.
Возможна повышенная кровоточивость кожных покровов или слизистых, например, носовые кровотечения. Иногда наблюдаются патологические явления со стороны вегетативной нервной системы: запор, нарушения мочеиспускания, нарушение аккомодации.
Постепенный отказ от приема препарата ведет к регрессии побочных эффектов. Резкое прекращение лечение может сопровождаться синдромом отмены, о котором следует узнать дополнительно.
При передозировке препарата существует высокий риск развития серотонинового синдрома. Он сопровождается делириозным состоянием с бредом, галлюцинациями и нарушением сознания. В тяжелых случаях возможно развитие комы.
Инструкция по применению
Велаксин принимают один раз в сутки во время еды. Капсулы необходимо запивать большим количеством воды. Разламывать оболочку капсулы не допускается.
Начинать прием следует со стартовой дозировки 75 мг. Такая доза должна применятся не менее двух недель. Затем можно увеличить ее еще на 75 мг. Повышать дозировку рекомендовано не чаще одного раза в неделю и только при необходимости. Максимальная суточная доза 350 мг.
Заканчивать прием следует также постепенно уменьшая дозировку. Рекомендуемый минимальный курс лечения составляет полгода. Затем можно перейти на минимальную профилактическую дозу.
Аналоги
К полным аналогам препарата велаксин относятся следующие средства:
- Випакс;
- Эффексор;
- Велафакс;
- Венлаксор;
- Эфевелон;
- Ньювелонг.
Все перечисленные медикаменты имеет одинаковое международное название — венлафаксин и, соответственно, одинаковое действующее вещество. Разница в торговом названии зависит от фирмы производителя. Все лекарства из списка относятся к группе дженериков.
Отзывы
Павел М.: “Начал принимать велаксин в связи с выраженным фобическим расстройством. Мне было очень сложно взаимодействовать с людьми, я боялся толпы и остерегался незнакомцев. Принимал препарат около полугода. Тревога ушла, я смог спокойно выходить на улицу и общаться с другими людьми. Действие средства развивалась постепенно. В начале приема была тошнота, но она быстро прошла. Отменять препарат пока боюсь.”
Кристина Н.: “У меня рекуррентное депрессивное расстройство. Последняя госпитализация была год назад. Тогда мне назначили велаксин из-за тяжелого течения заболевания. Лечилась я примерно месяц и заметила значительное улучшение. Оставшееся время пила таблетки для профилактики депрессии и пока они помогают. Единственный минус — у меня отсутствует аппетит. Борюсь с анорексией с помощью приема пищи по будильнику, считаю, что это из-за лекарства.”
Отзыв врача-психиатра: “Велаксин — это антидепрессант нового поколения, который избирательно воздействует на эмоционально-волевую сферу психики пациентов. Это сильное средство, которое мы применяем в тяжелых случаях. Велаксин обладает высокой эффективностью и достаточно хорошо переносится пациентами. Рекомендуем начинать лечение этим препаратом в условиях стационара из-за риска развития побочных реакций.”
Велаксин: инструкция по применению и отзывы
Латинское название: Velaxin
Код ATX: N06AX16
Действующее вещество: венлафаксин (venlafaxine)
Производитель: EGIS Pharmaceuticals PLC (Венгрия)
Актуализация описания и фото: 21.08.2019
Цены в аптеках: от 714 руб.
Велаксин – препарат, применяемый при лечении депрессий.
Форма выпуска и состав
Велаксин выпускают в следующих лекарственных формах:
В состав 1 таблетки входит:
- Активное вещество: венлафаксин (в виде гидрохлорида венлафаксина) – 25, 37,5, 50 или 75 мг;
- Вспомогательные компоненты (по 25/37,5/50/75 мг соответственно): моногидрат лактозы – 56,62/84,93/113,24/169,86 мг, микрокристаллическая целлюлоза – 24/36/48/72 мг, гликолят крахмала натрия (типа А) – 8,4/12,6/16,8/25,2 мг, безводный коллоидный диоксид кремния – 0,9/1,35/1,8/2,7 мг, стеарат магния – 1,8/2,7/3,6/5,4 мг.
В состав 1 капсулы входит:
- Активное вещество: венлафаксин (в виде гидрохлорида) – 75 или 150 мг;
- Вспомогательные компоненты: микрокристаллическая целлюлоза, этилцеллюлоза, хлорид натрия, диметикон, тальк, коповидон, хлорид калия, ксантановая камедь, безводный коллоидный диоксид кремния, оксид железа желтый.
Состав желатиновых капсул: оксид железа желтый и красный, диоксид титана, желатин.
Фармакологические свойства
Активное вещество Велаксина – венлафаксин. Это антидепрессант, который является рацематом двух активных энантиомеров и химически не относится ни к одному классу антидепрессантов (тетрациклическим, трициклическим или прочим).
Механизм антидепрессивного действия венлафаксина основан на его способности потенцировать передачу нервного импульса в центральной нервной системе. Венлафаксин и его главный метаболит О-десметилвенлафаксин (ОДВ) – сильные ингибиторы обратного захвата серотонина и норадреналина (SNRI) и слабые ингибиторы обратного захвата допамина.
Вещество и ОДВ одинаково эффективно влияют на обратный захват нейротрансмиттеров и способствуют снижению бета-адренергической реактивности как после однократного применения, так и при курсовой терапии.
Венлафаксин сродством к холинергическим, мускариновым, α1-адренергическим и гистаминовым (Н1) рецепторам головного мозга не обладает, активность моноаминоксидазы не подавляет. Также вещество не обладает сродством к бензодиазепиновым, опиатным, N-метил-d-аспартатным (NMDA) либо фенциклидиновым рецепторам.
Венлафаксин из желудочно-кишечного тракта хорошо всасывается.
После однократного приема 25–150 мг венлафаксина в форме таблеток Cmax (максимальная концентрация вещества) в плазме крови достигает 33–172 нг/мл примерно за 2,4 часа.
Вещество подвергается интенсивному метаболизму при первом прохождении через печень с образованием ОДВ. Период полувыведения венлафаксина и ОДВ – примерно 5 и 11 часов соответственно. Максимальная концентрация ОДВ в плазме крови составляет 61–325 нг/мл, время ее достижения – приблизительно 4,3 часа.
После приема Велаксина в виде капсул пролонгированного действия пиковые плазменные концентрации венлафаксина и ОДВ в крови достигаются в течение 6 ± 1,5 и 8,8 ± 2,2 часа соответственно. Скорость всасывания вещества из капсул пролонгированного действия ниже скорости его элиминации. В связи с этим период полувыведения венлафаксина после применения препарата в этой лекарственной форме составляет 15 ± 6 часов и представляет собой фактически период всасывания, нежели период распределения (5 ± 2 часа), который отмечается после назначения Велаксина в виде таблеток.
Венлафаксин и ОДВ связываются с белками плазмы крови на уровне 27% и 30% соответственно. Выведение ОДВ и прочих метаболитов, а также неметаболизированного венлафаксина осуществляется почками. Равновесные концентрации венлафаксина и ОДВ после многократного применения достигаются за 3 дня.
В диапазоне доз 75–450 мг в день венлафаксин и ОДВ имеют линейную кинетику. После приема Велаксина во время еды время достижения Cmax в плазме крови возрастает на 20–30 минут, при этом величины абсорбции и максимальной концентрации не изменяются.
При циррозе печени концентрации в плазме крови венлафаксина и ОДВ увеличиваются, а скорость их выведения снижается.
Общий клиренс венлафаксина и ОДВ у пациентов с умеренной/тяжелой почечной недостаточностью снижается, а период полувыведения – возрастает. Снижение общего клиренса наблюдается главным образом при клиренсе креатинина ниже 30 мл/мин.
Влияние пола и возраста на фармакокинетику препарата не зафиксировано.
Показания к применению
Согласно инструкции, Велаксин назначают при депрессиях различной этиологии, включая состояние тревоги (лечение и профилактика).
Противопоказания
- Тяжелые функциональные нарушения почек (при скорости клубочковой фильтрации 30 мл в минуту): коррекция режима дозирования не требуется;
- Средняя степень (при скорости клубочковой фильтрации 10-30 мл в минуту): требуется уменьшение дозы на 25-50%, при этом суточную дозу нужно принимать 1 раз в день;
- Тяжелая степень (при скорости клубочковой фильтрации 1/100 – часто, 1/1000 – нечасто, 1/10 000 – редко,
Читайте также:


