Фенитоин при рассеянном склерозе
– вице-президент Российского комитета исследователей рассеянного склероза и президент, генеральный директор Общероссийской общественной организации инвалидов – больных рассеянным склерозом, доктор медицинских наук профессор Ян Власов;
– президент Российского комитета исследователей рассеянного склероза, профессор кафедры неврологии, нейрохирургии и медицинской генетики лечебного факультета РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук, врач высшей категории Алексей Бойко.

Дебют этой опасной болезни у большинства людей не вызывает настороженности. Ведь её начальные симптомы обычно не внушают тревоги. Повышенную усталость, слабость в руках и ногах, проблемы со зрением сами больные часто списывают на проблемы с позвоночником (дорсопатии), стрессы, недосып. Но ведь именно так может начинаться и рассеянный склероз, который чаще всего выбирает именно молодых (обычно возникает в возрасте 25–40 лет). Это заболевание – вторая по частоте причина инвалидности (после травм) у людей молодого возраста. К сожалению, очень часто об истинном положении вещей пациенты узнают с большим опозданием, так как врачи обычно ставят более распространённые диагнозы.

Всё хуже и хуже
В мире рассеянный склероз диагностирован у 2,3 млн людей. В России, по оценкам специалистов, таких больных не менее 150 тысяч человек. Большая часть из них страдает рецидивирующим рассеянным склерозом (РРС), течение которого проходит с периодами рецидивирующей формы болезни, характеризующейся обострениями, сменяющимися ремиссиями, – то есть спокойными периодами, когда состояние больных улучшается. Но со временем нарушения всё равно накапливаются, и заболевание неуклонно прогрессирует, появляются новые или усугубляются уже имеющиеся симптомы. Тем не менее благодаря своевременной диагностике и правильно назначенному лечению врачам удаётся сдерживать развитие патологии.
Шаг вперёд
Помочь таким пациентам врачи долгое время были не в состоянии – ведь поддерживающее симптоматическое лечение и физическая реабилитация могли лишь немного снизить мышечный тонус, но не замедлить развитие болезни. До сих пор нигде в мире не существовало лекарств с доказанной эффективностью при такой форме болезни. Сегодня благодаря регистрации в России инновационного препарата Окрелизумаб у российских пациентов с таким диагнозом появилась возможность отсрочить развитие инвалидности. По клиническим исследованиям, при приёме этого лекарства скорость прогрессирования болезни снижается на 24%. А по наблюдению врачей, на фоне терапии у трети пациентов вообще отсутствуют какие-либо признаки прогрессирования заболевания, то есть возникает состояние, сравнимое с ремиссией. Кроме того, Окрелизумаб показал более высокую эффективность (на 50% выше, чем у ПИТРС) и в отношении рецидивирующего рассеянного склероза. У 9 из 10 пациентов, проходивших лечение, отсутствовало прогрессирование болезни, что подтверждалось не только клинически, но и на МРТ.

Препарат Окрелизумаб представляет собой моноклональное антитело к особому белку, который связывается с B‑лимфоцитами (клетками иммунной системы) и запускает процесс их уничтожения. Несмотря на то, что лекарство очень дорогое (ожидается, что годовой курс будет стоить более миллиона рублей), есть надежда, что оно войдёт в перечень жизненно необходимых лекарственных средств и каждый больной сможет получить его бесплатно, что даст возможность этим людям воплотить в жизнь задуманное: строить карьеру, создавать семью да и просто нормально жить.
Симптомы рассеянного склероза:
- Повышенная утомляемость. Есть у 90% людей с этим диагнозом.
- Слабость в ногах.
- Онемение конечностей и других участков тела.
- Головная боль.
- Проблемы со зрением (более чем у 25% пациентов).
- Депрессия (в 2 раза чаще, чем у остальных).
- Нарушения работы мочевого пузыря (как минимум у 80% пациентов).
Безусловно, самые дорогие препараты — те, которые создаются для людей с неизлечимыми или смертельными заболеваниями со сложной морфологией. Например, компания Novartis при описании стоимости своих препаратов делает акцент на их клиническом значении, влиянии на пациентов и систему здравоохранения в целом, а также на существенном улучшении качества жизни.
Симптомы рассеянного склероза существенно варьируются. Некоторые люди с тяжелым течением заболевания могут потерять способность ходить и есть, в то время как другие могут испытывать длительные периоды ремиссии без каких-либо новых симптомов.
Ремиттирующий рассеянный склероз — наиболее распространенное течение заболевания. Он характеризуется четко выраженными приступами новых или нарастающих неврологических симптомов. Эти приступы, также называемые рецидивами или обострениями, сопровождаются периодами частичного или полного выздоровления (ремиссиями). Во время ремиссий, все симптомы могут исчезнуть, или некоторые симптомы могут становиться постоянными. Однако явного прогрессирования заболевания в периоды ремиссии не наблюдается. Приблизительно у 85% людей с РС первоначально диагностируется именно РРС.
Большинство людей с диагнозом РРС в срок от 3–5 лет с появления первых симптомов приходят к вторичному прогрессирующему течению болезни, при котором со временем происходит ухудшение неврологических функций и инвалидизация пациента.
В 2010 году FDA одобрило препарат Gilenya, ставший широко применяемым для лечения РС. Месячный курс данного препарата стоит $2500.
Novartis даже подала иск в прошлом году, пытаясь заблокировать продажи непатентованных версий Gilenya после истечения срока действия основного патента на препарат в августе. Однако пока судебная тяжба ни к чему не привела.
В США около миллиона человек живут с РС, в России — порядка 150 тыс. человек с подтвержденным диагнозом РС, а во всем мире этим недугом страдают 2,3 млн человек. Последним методом лечения РС, одобренным FDA, был окрелизумаб в 2017 году. Это анти-CD20 моноклональное антитело, поражающее зрелые B-лимфоциты, являясь иммуносупрессором. Он вышел на рынок с заявленной стоимостью $65 000 за год лечения.
По сравнению с естественным течением болезни, пациенты, которых лечили препаратом, демонстрировали значительные улучшения моторного развития — дети смогли держать головку и самостоятельно сидеть.
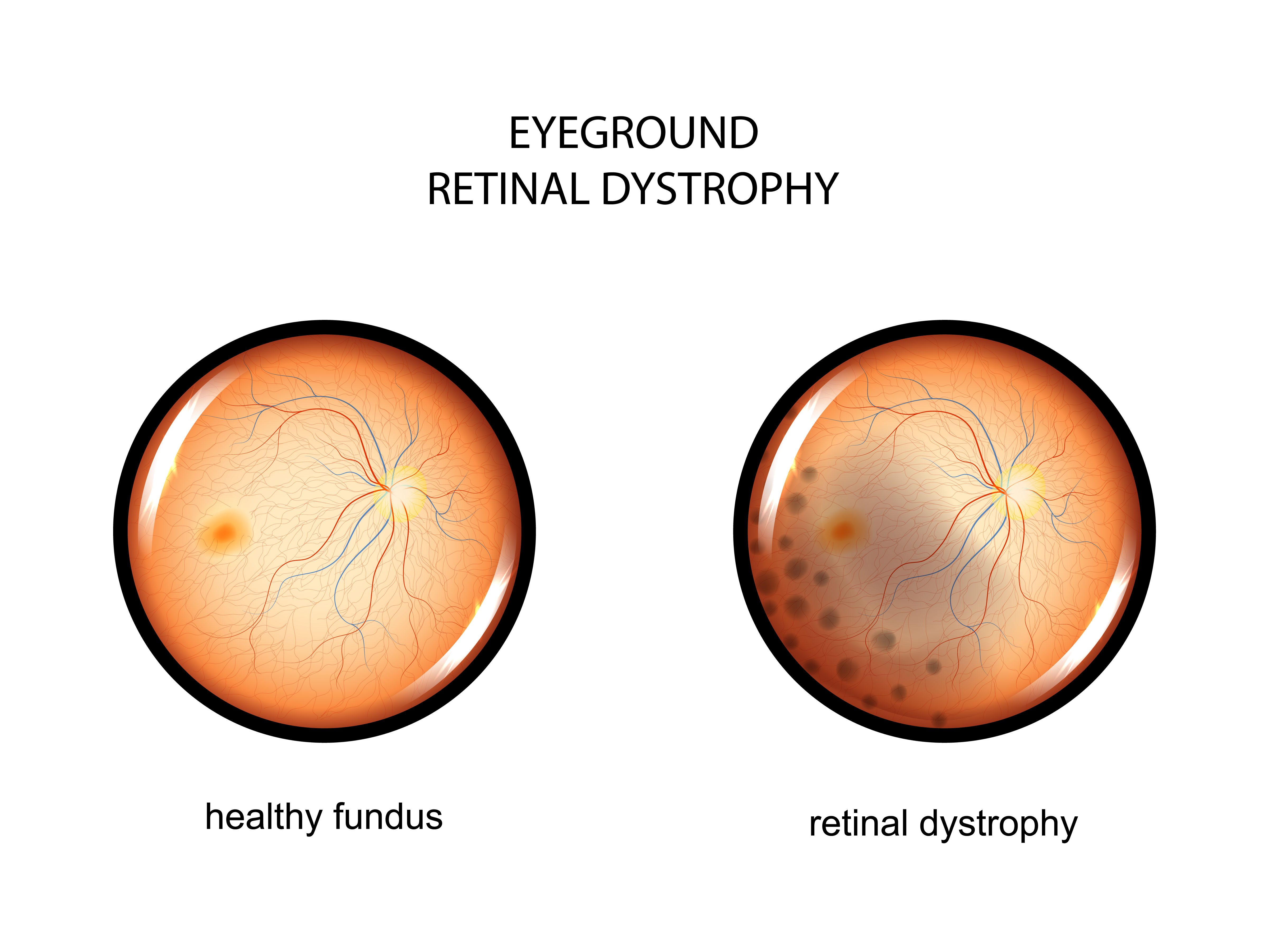
Ген RPE65 кодирует специфичный фермент клеток сетчатки глаза, участвующий в регенерации светочувствительного пигмента, который необходим для палочек и колбочек, чтобы обеспечить человеку нормальное зрение. Мутации в этом гене приводят к снижению или отсутствию уровней активности фермента, блокируя зрительный цикл и приводя к ухудшению зрения. Существует несколько типов наследственных заболеваний сетчатки, связанных с вышеназванным геном. Наиболее распространенными считают врожденный амавроз Лебера и пигментный ретинит. Из-за биаллельных мутаций гена RPE65 (генных мутаций обоих родителей) страдающие этими заболеваниями часто сталкиваются с никталопией (ночной слепотой) из-за снижения светочувствительности в детском или раннем взрослом возрасте и нистагмом (непроизвольными движениями зрачков). По мере прогрессирования заболевания происходят потеря периферического зрения, развитие туннельного зрения и, в конечном итоге, потеря центрального зрения, что означает полную слепоту.
Ретинальная дистрофия или наследственные дегенеративные заболевания сетчатки — это целый ряд болезней, которые отличаются по своей патологии, симптомам, а также последствиями. Очень трудно предсказать, насколько сильно ухудшится зрение, и как быстро будет прогрессировать заболевание, но во многих случаях люди с наследственной дистрофией сетчатки могут полностью потерять свое зрение.
Врожденный амавроз Лебера (ВАЛ) — редкое наследственное заболевание, которое приводит к нарушению деятельности сетчатки глаза и ухудшению зрения в раннем детстве, часто прямо с рождения. Из всех заболеваний, связанных с дегенерацией сетчатки, ВАЛ начинается раньше всего и может иметь наиболее тяжкие последствия. Уровень потери зрения при ВАЛ различается от случая к случаю, но остается стабильным в 75% случаев. У примерно 15% детей отмечается прогрессирующая потеря зрения, а у 10% может отмечаться некоторое незначительное, часто временное, улучшение.
Но FDA уже одобрило его для лечения двух редких заболеваний — хронического гранулематозного заболевания и тяжелого злокачественного остеопороза.
Хроническое гранулематозное заболевание — наследственное заболевание, при котором иммунная система отсутствует или не функционирует должным образом.
Синдром Хантера представляет собой рецессивное наследственное заболевание, вызванное недостаточным уровнем в организме лизосомального фермента. Проще говоря, необходимый для правильного углеводного обмена фермент не вырабатывается в нужных количествах и полисахариды (естественные сахара) неправильно усваиваются. В связи с отсутствием или наличием дефектного фермента у пациентов с синдромом Хантера полисахариды накапливаются в лизосомах клеток, приводя к клеточному перенасыщению, органомегалии, разрушению тканей и нарушению функций внутренних органов. Частота заболевания в мире составляет один человек на 100 тысяч. В России зарегистрировано около 150 пациентов.
Наследственный ангионевротический отек (HAE) — очень редкое и потенциально смертельное заболевание, которое встречается примерно у одного из 10 тыс. человек в мире. Главный симптом HAE — отеки в различных частях тела. У пациентов часто бывают приступы мучительной боли в животе, тошнота и рвота, вызванные отеком кишечной стенки. Отек дыхательных путей особенно опасен и может привести к смерти от удушья.
У пациентов с НАЭ имеется дефект в гене, который контролирует белок крови, называемый ингибитором С1. Генетический дефект приводит к выработке либо неадекватного, либо нефункционального белка C1-Inhibitor. Нормальный C1-Inhibitor помогает регулировать сложные биохимические взаимодействия систем на основе крови, участвующих в борьбе с болезнями, воспалительной реакцией и коагуляцией. Поскольку дефектный C1-Inhibitor не выполняет надлежащим образом свою регуляторную функцию, может возникнуть биохимический дисбаланс и продуцировать нежелательные пептиды. Они побуждают капилляры высвобождать жидкость в окружающую ткань, вызывая тем самым отек.
Стоимость жизненно важных препаратов зависит от множества исходных данных, но и их польза неоспорима. Обеспечить идентичную замену дефектным клеткам или способствовать выработке нужных для больного ферментов, зачастую могут только сложные разработки, в которых задействованы большое количество специалистов. В России, к большому сожалению, еще не все эти лекарства одобрены или выдаются по квоте всем нуждающимся. Но однажды мы к этому придем.
ПИТРС (препараты, изменяющее течение рассеянного склероза) получают все большее распространение и клиническое обоснование при лечении рассеянного склероза. В каждом конкретном случае ПИТРС подбираются индивидуально, с учетом характера течения заболевания, уже имеющейся симптоматики и ранее назначенной терапии. На сегодняшний день врачи выработали алгоритм применения ПИТРС при рассеянном склерозе. Он предусматривает повод для назначения, коррекции и отмены препарата, а также схему перевода пациента на другой препарат этой группы. Как правило, препараты ПИТРС назначаются сразу, как только диагноз установлен, чтобы предельно сдержать развитие рассеянного склероза.
ПИТРС воздействуют на патологический процесс демиелинизации. Применение ПИТРС может позволить снизить частоту или полностью предотвратить возникновение обострений, делая их менее выраженными, а также замедлить нарастание инвалидизации.
Продолжительный период времени лечение рассеянного склероза сводилось к гормонотерапии и сопутствующей терапии, направленными на снижение выраженности симптомов, улучшения обмена веществ нервной ткани, укрепление сосудов и реабилитации. Все эти способы лечения приносили пациенту лишь временное облегчение, подчас очень значимое, но существенно не влияющее на развитие рассеянного склероза.
Применение ПИТРС позволяет пациенту:
- стабилизировать свое состояние;
- не допускать перехода в прогрессирующую форму;
- замедлять развитие неврологического дефицита.
Но клинический эффект ПИТРС при рассеянном склерозе развивается не сразу, пациент может перестать принимать препарат, рассудив, что не испытывает никакого улучшения. Стоит помнить, что прогресс становится заметен лишь в период от 1 до 6 месяцев от начала приема препарата.
Комментарий врача
Комментарий о принципах лечения препаратами, изменяющими течение рассеянного склероза (ПИТРС) и о целях терапии дает ведущий специалист в области рассеянного склероза, доктор медицинских наук, профессор кафедры нервных болезней и нейрохирургии с клиникой Первого Санкт-Петербургского государственного медицинского университета имени академика И.П.Павлова Тотолян Наталья Агафоновна
Различают препараты первой и второй линии.
ПИТРС первой линии назначаются, как только диагноз рассеянный склероз подтвердился. Они замедляют прогрессирование болезни и уменьшают проявления симптомов.
ПИТРС второй линии применяются, когда течение рассеянного склероза становится активным. А препараты первой линии — недостаточно эффективны.
ПИТРС первой линии
ПИТРС второй линии
Основные эффекты ПИТРС:
- замедление развития необратимых нарушений (инвалидности);
- снижение частоты обострений;
- уменьшение воспалительной реакции.
В настоящее время разработаны:
- четкие алгоритмы лечения препаратами ПИТРС;
- способы мониторинга изменений состояния пациентов;
- рекомендации, позволяющие существенно снизить выраженность побочных реакций или полностью убрать их.
Тем не менее, бывают случаи, которые могут потребовать смены препаратов группы ПИТРС .
К ним относятся:
- Тяжелые побочные реакции, не поддающиеся коррекции;
- Беременность (в том числе, планируемая);
- Отсутствие эффективности терапии.
В любом случае, решение о назначении или отмене ПИТРС принимается лечащим врачом и зависит от состояния пациента.
Международным медицинским сообществом принято, что ПИТРС являются первоочередными и наиболее эффективными препаратами для лечения рассеянного склероза.
Комментарий врача Е. В. Поповой о ПИТРС
Екатерина Валерьевна расскажет о том, какие виды ПИТРС существуют, чем отличаются различные ПИТРС и о том, что влияет на выбор врача в назначении того или иного препарата при терапии рассеянного склероза. Рассмотрим показания для назначения ПИТРС при различных видах течения РС
Клинический эффект ПИТРС при рассеянном склерозе развивается, как правило, от 1 месяца до полугода от начала приема. Для оценки эффективности препарата результаты лечения рассматриваются в период от 6 месяцев до 1 года.
Пациенты, которым впервые были назначены ПИТРС часто задают следующие вопросы:
Механизмы действия ПИТРС таковы, что ощутимый эффект от терапии, как правило, наступает в течение 1-6 месяцев. Продолжительность этого периода индивидуальна и зависит от ряда факторов, таких как характер течения болезни, состояние пациента до назначения препаратов, прием сопутствующей терапии, индивидуальные реакции на препарат и т.д. Кроме того, стоит помнить, что эффект от лечения ПИТРС проявляется не какими-либо специфическими ощущениями, а длительным отсутствием обострений.
Бывают случаи, когда диагноз рассеянный склероз ставят пациенту, у которого никогда не было проявлений заболевания. Чаще всего это происходит, когда очаги обнаруживаются по результатам МРТ еще до появления симптоматики. Тогда пациенту ставится диагноз радиологически изолированный синдром (РИС). С другой стороны, у пациента мог произойти лишь один клинический эпизод — клинически изолированный синдром (КИС). И, поскольку симптомы РС неспецифичны и могут проявляться при различных неврологических заболеваниях, пациент может не понять, что у него произошло обострение. И в том и в другом случае, по решению лечащего врача, пациенту может быть назначена терапия ПИТРС. Такой подход обоснован.
Как правило, терапия ПИТРС останавливает развитие обострений РС. Чаще на фоне лечения могут проявиться различные побочные эффекты препарата. Субъективно эти ощущения могут расцениваться пациентом как ухудшение состояния. Со временем эти реакции могут становиться менее выраженными и уже не приносят столь выраженного беспокойства пациенту. В каждом случае необходимо обсуждать возникновение побочных эффектов препарата и варианты их коррекции с лечащим врачом.
Если получен хороший результат на назначенную терапию и обострения не возникают, лечение ПИТРС прекращать не стоит. Некоторые пациенты прекращают лечение ПИТРС самостоятельно, при этом, как правило, у большинства из них симптомы РС возобновляются в течение двух лет после отмены терапии или ранее. Долгосрочное лечение препаратами часто вызывает беспокойство у пациентов. Можно сравнить ПИТРС с препаратами для снижения артериального давления или нормализующими сахар крови, которые также принимаются в течение длительного времени. Расценивать это лечение стоит как помощь организму в том, с чем он не может справиться самостоятельно. В любом случае необходимо проконсультироваться с лечащим врачом.
При длительном приеме назначенных препаратов группы ПИТРС проводится обязательный мониторинг клинических показателей крови, оценивается функция печени, почек и других жизненно важных органов. Если определяются серьезные отклонения в каком-либо из показателей, препарат может быть на время отменен или заменен лечащим врачом. Если при регулярном мониторинге изменения не выявляются, риск для организма отсутствует.
Критериями смены лечения ПИТРС являются:
- планируемая беременность;
- плохая переносимость терапии;
- изменение типа течения рассеянного склероза;
- низкая эффективность терапии.
Перечисленные ситуации достаточно редки, за исключением возможной беременности и побочных реакций. Как правило, нежелательные реакции чаще беспокоят пациента в начале терапии. Со временем они становятся менее выраженными или проходят совсем. В случае, если лечащий врач подтверждает тяжесть побочных явлений, а терапия, назначаемая для снижения их выраженности, не помогает, препарат следует заменить.
При беременности и родах, а также во время грудного вскармливания принимать препараты ПИТРС не рекомендуется. Продолжение терапии обязательно следует обсудить с лечащим врачом, который оценит пользу и возможные риски терапии. После окончания грудного вскармливания пациентка, как правило, возвращается к прежней терапии. Препарат для каждого пациента должен подбираться индивидуально, с учетом формы рассеянного склероза и особенностей течения заболевания. Выбор должен зависеть также от наличия определенных симптомов и переносимости тех или иных лекарств. ПИТРС способны сохранить здоровье больного и продлить период трудоспособности и активности пациентов с рассеянным склерозом

Люди, у которых диагностировали такое хроническое аутоиммунное заболевания, часто задаются вопросом какие пить таблетки от рассеянного склероза.
Но этот подход не совсем верный, поскольку для облегчения состояния при обострениях и для продления периода ремиссии необходима комплексная терапия (прием лекарственных препаратов, отказ от вредных привычек, правильное питание, физиотерапия, плазмаферез и т.д.).
По принципу действия выделяют 3 группы лекарств:
Таблетки, успокаивающие нервную систему при рассеянном склерозе
Противозачаточные таблетки и рассеянный склероз
Концентрация стероидных гормонов, вырабатываемых женскими половыми железами (яичниками), взаимосвязана с течением Р.С. Поэтому, с целью контрацепции, пациенткам часто назначают КОК (комбинированные оральные контрацептивы).
• минимизация дисменореи или полное устранение характерных болей внизу живота;
• профилактика анемии вследствие больших потерь крови (при повышенных менструальных объемах);
• корректировка цикла менструаций;
• снижение риска возникновения болезней воспалительного характера (речь идет об органах малого таза);
• исключение беременности, если рождение ребенка является прямым противопоказанием.
Исследования, проведенные в 2003 году, подтвердили теорию о снижении тяжести течения РС при введении эстрадиола (основной компонент оральных контрацептивов) перорально. Результаты магнитно-резонансной томографии подтвердили количественное уменьшение повреждений нервных тканей головного мозга при приеме эстриола.
Примечание: к исследованиям применен 3-й уровень доказательности.
Гормональные таблетки при рассеянном склерозе
Подобный подход к лечению называют пульс-терапией.
С помощью перечисленных препаратов можно достичь частичного восстановления утерянных функций, а также сократить длительность периода очередного обострения.
Побочные эффекты:
• снижение иммунитета;
• ухудшение зрения, вплоть до катаракты;
• увеличение массы тела;
• нестабильный психоэмоциональный фон.
Примечание: гормоны неэффективны при первично-прогрессирующей форме болезни.
Терифлуномид (международное название) относится к иммуномодулирующим лекарствам. Отличается отличными противовоспалительными свойствами.
Клинически доказанная результативность приема заключается в:
• уменьшении концентрации мочевой к-ты;
• количественном уменьшении активированных лимфоцитов в периферической крови;
• сокращения количества активных очагов (результаты скринограммы МРТ);
• снижении частоты обострений и рецидивов;
• отсрочка момента инвалидизации.
Противопоказания:
1. Есть возрастные ограничения ― не назначают особам младше 18 лет.
2. Беременность.
3. Грудное вскармливание.
4. Синдром приобретенного иммунодефицита.
5. Тяжелая печеночная или почечная недостаточность.
6. Вирусные инфекции в стадии обострения.
7. Нейтропения.
8. Анемия.
9. Тромбоцитопения.
10. Лейкопения.
11. Индивидуальная непереносимость отдельных компонентов.
Противопоказание ― индивидуальная гиперчувствительность.
Суточная доза варьируется в диапазоне от 150 до 60 миллиграмм (разбивается на два-три приема).
ПИТРС при рассеянном склерозе в таблетках
1. Первая линия ― одинарная или двойная доза ГА (глатирамер ацетат), бета-интерферон, терифлуномид, лахинимод.
2. Вторая линия ― митоксантрон, натализумаб.
3. Сильные иммуносупрессоры ― циклоспорин, микофенолат, циклофосфамид.
4. Дополнительные лекарства ― алемтузумаб, диметилфумарат.
Относится к группе антиметаболитов, противоопухолевых лекарств.
Действие нацелено на уменьшение выраженности атрофических процессов, которые происходят в головном мозге.
Клинические исследования подтвердили минимизацию скорости потери объема мозга (измерялось среднегодовое значение) у пациентов с ремиттирующей формой заболевания, а также происходила отсрочка инвалидизации в среднем на два года.
Противопоказания:
• Повышенная чувствительность к отдельным компонентам.
• Хроническая почечная недостаточность.
• Дети (возраст до 16-ти лет).
• Лактация.
• Беременность.
Примечание: терапия данным лекарственным средством должна проходить под тщательным наблюдением лечащего врача.
Никотиновая кислота (таблетки) при рассеянном склерозе
Ниацин используется для:
• лечения сосудистых нарушений (оказывает сосудорасширяющее действие), вызванных прогрессированием РС;
• улучшения микроциркуляции в головном мозге;
• детоксикации;
• нормализации количества липидов, содержащихся в тканях и клетках пациентов;
• устранения перевозбуждения нервной системы.
Схема введения в организм основана на постепенном увеличении дозировки.
Atara Biotherapeutics: T-клеточная терапия против вируса Эпштейна — Барр.
Человеческий разум относится к новой идее так же,
как тело относится к странному белку: он отвергает ее.
Питер Медавар, биолог, нобелевский лауреат
Новая научная истина торжествует не потому,
что ее противники признают свою неправоту,
просто ее оппоненты со временем вымирают,
а подрастающее поколение знакомо с нею с самого начала.
Макс Планк, физик, нобелевский лауреат
Суть проблемы
Прогрессирующий рассеянный склероз (PMS), как тяжелая форма этого демиелинизирующего заболевания, классифицируется на первично-прогрессирующий рассеянный склероз (PPMS) и вторично-прогрессирующий рассеянный склероз (SPMS). Первый справедлив при непрестанном ухудшении течения заболевания к моменту постановки его диагноза (15% случаев). Второй начинается как рецидивирующе-ремиттирующий рассеянный склероз (RRMS), который в конечном итоге превращается в SPMS у 80% пациентов.
Согласно глобальной статистике, мировая популяция пациентов с рассеянным склерозом разбивается следующим образом : на долю RRMS приходится 57% больных, тогда как PMS охватывает 43%, включая 15% пациентов с PPMS и 28% с SPMS.
Медицинская потребность в новых прорывных и, главное, высокоэффективных лекарственных препаратах для терапии прогрессирующего рассеянного склероза по-прежнему остается незакрытой. Сообщество врачей и пациентов мечтает либо об обращении инвалидизации вспять с последующим устойчивым поддержанием достигнутых успехов, либо о хотя бы стабильной остановке прогрессирования рассеянного склероза.
Гипотеза, нашедшая ответ
- У EBV-положительных иммунологически разнообразных и со здоровой иммунной системой доноров (не больных рассеянным склерозом) лейкоферезом собирают мононуклеарные клетки периферической крови (PBMC). Из них выделяют T-клетки и B-клетки, которые затем культивируют и размножают.
- B-клетки трансформируют в антигенпрезентирующие клетки (APC) путем их трансфектирования рекомбинантным аденовирусным вектором AdE1-LMPpoly, который кодирует CD8 + T-клеточные эпитопы, имеющие отношение к антигенам вируса Эпштейна — Барр — ядерному EBV-антигену 1 (EBNA1), латентному мембранному белку 1 (LMP1), латентному мембранному белку 2A (LMP2A).
- T-клетки подвергаются воздействию APC, которые экспрессируют указанные EBV-антигены. Итогом становится стимуляция и размножение EBV-специфических CD8 + T-клеток — таргетированных цитотоксических T-лимфоцитов (CTL).
- При внутривенном введении CTL пациентам с рассеянным склерозом они уничтожают персистирующие в центральной нервной системе EBV-инфицированные B-клетки, которые несут искомые EBV-антигены.
Поскольку ATA188 является HLA-совместимым только частично, создается обширная библиотека криоконсервированных ATA188-препаратов: нужный отбирается для каждого пациента сообразно соответствию хотя бы по двум HLA-аллелям, общим для ATA188 и конкретного больного.
Возможная победа над прогрессирующим рассеянным склерозом
Клинические исследования NCT03283826 фазы I проверяют безопасность и эффективность ATA188, назначаемого монотерапевтически один раз в год (несколькими циклами) на протяжении пяти лет взрослым EBV-положительным пациентам (n=97) с прогрессирующими формами рассеянного склероза — первично-прогрессирующим или вторично-прогрессирующим. Испытания состоят из двух частей. Среди критериев включения: возраст 18–66 и 18–56 лет, балл по расширенной шкале степени инвалидизации (EDSS) 3,0–7,0 и 3,0–6,5 — соответственно для первой и второй частей.
В еще не начатой второй части исследований (рандомизированных, двойных слепых, плацебо-контролируемых) будут определены изменения конечных точек: EDSS, тест на время прохождения 25 футов (T25-FW), тест с девятью отверстиями и стержнями (9-HPT), МРТ-объемы шейного отдела спинного мозга и всего головного мозга, число очагов поражения головного мозга на T1-взвешенных МРТ-изображениях с контрастированием гадолинием и число новых или увеличивающихся очагов на T2-взвешенных МРТ-изображениях.
Заявлено, что с увеличением дозы ATA188 ответ на лечение углублялся. Так, по одному пациенту в когортах 1 и 2 и два пациента в когорте 3 показали SDI за период 6 месяцев, который сохранялся и по истечении 12 месяцев. Два участника в когорте 4 максимальной дозы также продемонстрировали SDI за 6 месяцев, но их 12-месячные данные еще не собраны. Основной вклад в достижение SDI поступил со стороны улучшения балла EDSS.
- шкала тяжести усталости (FSS): минимальное клиническое улучшение составляло −0,7 балла;
- шкала влияния рассеянного склероза (MSIS-29) [домен физических возможностей]: −8 баллов;
- T25-FW: −20%;
- 9-HPT: −20%;
- субъективный опросник способности передвигаться (MSWS-12): −8 баллов;
- EDSS: −1 балл (при исходном EDSS 3–5 баллов) и −0,5 балла (EDSS 5,5–7,0);
- острота зрения (VA) [по шкале LogMAR]: изменение минимум на −0,1 в каждом глазу.
Подтверждено, что длительно сохраняющаяся заявленная терапевтическая эффективность ATA188 напрямую коррелирует с увеличением дозы препарата.
Профиль безопасности ATA188 характеризуется отсутствием дозолимитирующей токсичности и фатальных побочных реакций. Все отрицательные явления, связанные с терапией, носили легко-умеренную степень выраженности. И хотя один пациент столкнулся с тяжелой побочной реакцией, приведшей к выходу из клинических исследований, она проявилась на фоне продолжающихся симптомов инфекции верхних дыхательных путей и возможной стоматологической инфекции. Насморк — единственная побочная реакция, зафиксированная у более чем одного испытуемого.
ATA188 не оказал клинически значимого эффекта на выработку цитокинов, в том числе не привел к синдрому выброса цитокинов.
Более чем надежда
И хотя развитие рассеянного склероза, вероятно, подталкивается не одним причинным фактором, вирус Эпштейна — Барр является единственным известным на сегодняшний день фактором риска, в обязательном порядке необходимым для манифестации заболевания. Доказано, что 100% пациентов с рассеянным склерозом подверглись воздействию EBV. При этом EBV-инфицированные клетки, особенно B-клетки памяти, ставшие ввиду вирусного заражения бессмертными, играют, есть мнение, важнейшую роль в иммунном каскаде, ответственном за рецидивирующие и прогрессирующие формы рассеянного склероза. Успехи существующей фармакотерапии, которая истощает пул всех периферических B-клеток, лишний раз свидетельствует о ключевой позиции этих клеток в патофизиологии рассеянного склероза. Показана оправданность продолжения экспериментов с терапией рассеянного склероза при помощи ATA188 — цитотоксическими T-клетками, селективно таргетированными против EBV-инфицированных B-клеток и плазматических клеток, как циркулирующих в организме, так и персистирующих в центральной нервной системе.
Некоторые наблюдения таковы, что эффективность ATA188 в отношении улучшения статуса инвалидизации зависит, кажется, от исходного балла по шкале EDSS: чем запущеннее заболевание, тем меньше (или медленнее) проявляется целебная сила лечения. И всё же улучшение показателя EDSS даже на один балл — уже примечательно. Ведь если пациент, к примеру, изначально передвигался с тростью, то после терапии ATA188 он обрел способность самостоятельной ходьбы.
Имеющиеся лекарственные препараты способны лишь слегка придержать ухудшение прогрессирующего рассеянного склероза — им не по силам остановить или обратить заболевание вспять. Если ATA188 добьется этого в ходе строго контролируемой части 2 клинических испытаний, нас ждет эволюция в парадигме лечения прогрессирующей и других форм рассеянного склероза.
Рассеянный склероз и вирус Эпштейна — Барр
Считается, что генетические и внешние факторы вносят определенный вклад в риск развития рассеянного склероза — хронического воспалительного демиелинизирующего заболевания центральной нервной системы, вызывающего прогрессирующую инвалидизацию. За последние четыре десятка лет появилось всё больше доказательств , что вирус Эпштейна — Барр (EBV) играет существенную роль в развитии рассеянного склероза. Предположение подкреплено рядом независимых исследований, указывающих на поголовное присутствие инфекции у пациентов и наличие высоких титров сывороточных антител против EBV как в ходе клинического течения рассеянного склероза, так и до его манифестации .
Вирус Эпштейна — Барр, или вирус герпеса человека 4 типа (HHV-4), во многих отношениях является уникальным. Так, в целях колонизации организма он заражает B-лимфоциты, активирует и способствует их клональному размножению, а затем на протяжении всей жизни человека персистирует латентной инфекцией в B-клетках памяти, несущих фенотип покоящихся клеток. Вирус, переключаясь с латентной (спящей) на литическую (репликационную) форму посредством модуляции своих ядерных генов, латентных мембранных белков (LMP) 1, 2A и 2B и вирусного предраннего белка BZLF1 (ZEBRA), реактивируется в плазматических клетках и эпителиальных клетках миндалин, организуя собственную передачу другим организмам через слюну и генитальные выделения. Несмотря на то что этим ДНК-двухцепочечным гамма-герпесвирусом заражено приблизительно 95% взрослого населения планеты, число EBV-инфицированных клеток в организме удерживается под строгим иммунным контролем, в том числе EBV-специфическими цитотоксическими T-лимфоцитами CD8 + , которые уничтожают пролиферирующие и литически инфицированные клетки.
В ряде случаев иммунологический надзор над EBV ослабевает, что отражается развитием различных болезней. Известно, что вирус Эпштейна — Барр является причиной инфекционного мононуклеоза. Он ассоциирован с определенными онкологическими заболеваниями, включая лимфому Ходжкина, лимфому Беркитта, рак желудка, карциному носоглотки. Вирус Эпштейна — Барр связан с детскими расстройствами вроде синдрома Алисы в стране чудес и острой мозжечковой атаксии. Есть мнение, что он усиливает риски развития аутоиммунных патологий, в том числе дерматомиозита, системной красной волчанки, ревматоидного артрита, синдрома Шегрена.
Касательно рассеянного склероза, считается , что у восприимчивых хозяев EBV-инфекция наделяет зараженные аутореактивные B-клетки аномальной способностью к выживаемости и пролиферации. Такие латентно инфицированные клетки аккумулируются в лимфоидных структурах и органах-мишенях, затрагиваемых при этом заболевании. Если речь идет о головном мозге, это приводит к постоянному синтезу аутоантител, которые атакуют и повреждают олигодендроциты, миелин и нейроны.
Что примечательно, 78% хронических областей мозгового поражения при рассеянном склерозе и только 33,3% образцов здорового мозга содержали плазматические клетки CD138 + в паренхиме, где быть их не должно. Не исключено, EBV-инфекция ответственна за экстравазацию последних из сосудистой сети головного мозга, наделяя воспалительный процесс постоянством.
В 46% и 44% тканях соответственно был найден белок BZLF1, притом что в случае биоптатов с рассеянным склерозом он находился преимущественно в связке с областями хронического поражения головного мозга. Считается, что BZLF1 способен подавлять выработку интерлейкина 2 (IL-2) и интерлейкина 6 (IL-6). Помимо участия в B-клеточном созревании IL-6 важен для нейро- и генеза олигодендроглии в нормальных условиях и после повреждения.
Кроме того, в 85% образцах головного мозга пациентов с рассеянным склерозом отмечалось куда более выраженное присутствие иммунных клеток с EBV-кодируемыми малыми РНК-1 (EBER1), нежели в биоптатах здоровых лиц.
Дополнительные свидетельства
Так, ассоциированный с рассеянным склерозом ретровирус (MSRV), относящийся к патогенному W-семейству эндогенных вирусов человека (pHERV-W), может трансактивироваться внешними факторами, например вирусом герпеса человека 6-го типа (HHV-6) или вирусом Эпштейна — Барр. Итогом становится генерация патогенного оболочечного белка MSRV-Env, который, сверхактивируя эндогенный толл-подобный рецептор 4 (TLR4), запускает провоспалительный каскад и подавление ремиелинизации.
Темелимаб (GNbAC1) — рекомбинантное гуманизированное моноклональное антитело, избирательно таргетированное на внеклеточный домен MSRV-Env в целях его нейтрализации.
Читайте также:


