Альфа рецепторы нервной системы
Адренорецепторы - это белки клеточной мембраны, их функция - соединять, а также распознавать адреналин и норадреналин, синтетические аналоги катехоламинов. Белки находятся во всех тканях и клетках. Есть альфа и бета-адренорецепторы, они уже выделены и очищены. Группы адренорецепторов отличаются реакцией к разным продуктам.
Рецепторы бывают: альфа1; альфа2; бета1; бета2; бета3.
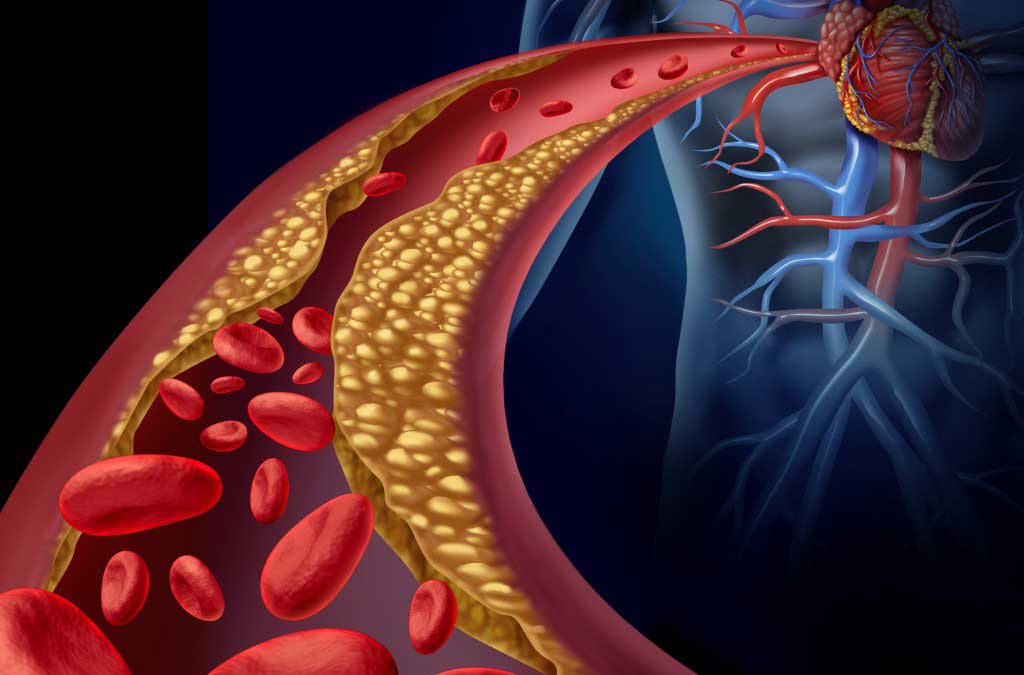
Альфа
Альфа-адренорецепторы - это рецепторы, что проявляют восприимчивость к норадреналину. Когда они находятся в возбужденном состоянии, наблюдается сокращение селезенки, матки, уменьшение сосудов и расширение зрачков.
Бета-адренорецепторы - это рецепторы, что проявляются высокой эмотивностью к изадрину. Когда они возбуждены, сосуды начинают расширяться, бронхи расслабляются, учащаются сокращения сердца, также рецепторы приостанавливают сокращение матки.
Главные свойства рецепторов
Альфа1 и бета1 зачастую размещаются в постсинаптических мембранах, рецепторы проявляют чувствительность на работу норадреналина, он вырабатывается в нервных окончаниях постганлионарных нейронов симпатического отдела.
Рецепторы альфа2 и бета2 относятся к внесинаптическим, у них на мембранах размещены нейроны. Рецепторы группы альфа2 воздействуют, как адреналин и как норадреналин. Бета2 проявляют восприимчивостью к работе адреналина. На пресинаптической мембране норадреналин работает по формуле отрицательной обратной связи (он способен ингибировать собственные выделения). Во время реакции адреналина на адренорецепторы группы бета2 выделение пресинаптической мембраны норадреналина увеличивается. Адреналин формируется мозговым слоем надпочечников под действием норадреналина, образуется петля положительной обратной связи.
Краткая характеристика рецепторов
Основные характеристики следующие:
- Альфа1 размещаются в артериолах, последствия стимуляции – это возникновение спазма в артериолах, в результате этого увеличивается давление, уменьшается сосудистая проницаемость и экссудативное воспаление.
- Альфа2 относятся к пресинаптическими рецепторами, их характеризуют, как петлю обратной отрицательной связи для адренэргической системы, в конечном результате артериальное давление падает благодаря стимуляции.
- Бета1 дислоцированный в сердце, стимуляция производит к увеличению силы и частоты сердечных сокращений. Помимо этого, последствие стимуляция - увеличение потребности миокарда в кислороде и поднятие артериального давления. Бета1 также есть и в почках, это рецепторы юкстагломерулярного аппарата.
- Бета2 есть в бронхиолах, последствием стимуляции является увеличение бронхиол и устранение бронхоспазма. Эта группа рецепторов находится на клетках печени, под влиянием гормона возникает процесс гликогенелиза, вывод глюкозы в кровь.
- Бета3 помещен в жировой ткани. Под действием таких рецепторов увеличивается липолиз, а под их влиянием выделяется энергия, и увеличивается теплопродукция.
Взаимодействие адренорецепторов
Между адренорецепторами и исполнительными системами клетки располагаются белки, их функция связывать гуаниловые нуклеотиды, так называемые G-белки. Они разделяются на типы: стимулирующие и ингибирующие.
Взаимосвязь адренорецепторов с G-белками является главнейших звеном механизма поступления сигналов через клеточную мембрану.
Классификация адренорецепторов была сделана на различиях чувствительности к фармакологическим средствам: адреностимуляторам и адреноблокаторам. Все адренорецепторы группы бета напрямую связаны с белками Gs альфа, они способствуют стимуляции аденилатциклазы, ускоряют поток кальция в клетки.
Передача сигнала от рецепторов альфа1 спровоцированная белком Gg и фосфоинозитидной системой. Альфа2 контактируют с белком Gi, после их активации наступает подавление синтеза цАМФ и поток кальция в клетки. Гены всех подтипов адренорецепторов являются клонами.
Основные физиологические реакции, связанные с адренорецепторами, основаны на их взаимодействии с эндогенными лигандами, катехрламиналами.
Блокаторы адренорецепторов ведут борьбу с катехоламинами за возможность связывания с рецепторами. Взаимодействуя с рецепторами без их активации, адреноблокаторы мешают вступать в связь с катехоламинами рецепторов, отвечающих за образование клеточной реакции. Адреноблокаторы способны оказывать влияние на все адренорецепторы и на подтипы рецепторов по-отдельности.

Медицинское значение
Если брать во внимание большую локализацию адренорецепторов во всем организме, то модуль их движения приводит к различным терапевтическим, либо токсическим последствиям.
Помимо веществ, которые стимулируют адренорецепторы, есть и другие факторы, вызывающие стимуляцию, они это делают с помощью МАО. Такое вещество способное уничтожить адреналин и норадреналин, а его ингибирование производит увеличение концентрации нейромедиаторов, а также увеличение стимуляции рецепторов. Ингибиторы МАО используются в роли антидепрессантов.
Адренорецепторы - это определенные рецепторы, которые применяются вместе с адреномиметрическими средствами, как сосудосуживающие препараты. Эти средства в основном приписывают, чтобы поднять артериальное давление при шоковом состоянии, гипотонической болезни, коллапсе, конъюнктивитах, для уменьшения воспалительных процессов и сужения сосудов, а еще ими обрабатывают места для остановки кровотечения.
Адреномиметические вещества входят в канестезирующие средства, чтобы те могли работать. Для таких целей применяют почти все адреномиметические средства, кроме изадрина, который действует исключительно на бета-адренорецепторы, также исключают и фенамин, так как он провоцирует сильное психическое возбуждение.
Большое количество средств этой группы применяют как бронхорасширяющий препарат для устранения и профилактики приступов бронхиальной астмы, еще они применяются при астмоидных и эмфизематозных бронхитах.
Адреномиметрические средства запрещено употреблять при гипертонических болезнях, атеросклерозе и тиреотоксикозе.

Холинергические механизмы нервной системы - это вещества, которые обеспечивают передачу возбуждения в холинергическом синапсе.
Медиатор ацетилхолин (эфир холина и уксусной кислоты) образуется из аминокислоты холина и ацетил-СоА на пресинаптическом окончании нервноего волокна. Образующийся медиатор поступает в везикулы, а частично может остаться в свободном состоянии. При возбуждении медиатор выделяется из везикул. Процесс выделения медиатора С-зависим. Для нормальной работы синапса необходим запас медиатора, поэтому на пресинаптической мембране идёт ресинтез ацетилхолина. Для этого аминокислота холин выделяется из постсинаптической мембраны, частично из синаптической щели (возврат медиатора). Для образования медиатора необходима энергия метехондрий.
Фермент, способствующий синтезу ацетилхолина - ацетилхолинтрансфераза или холинацетилаза. Этот фермент образуется в теле нейрона и поступает в нервные окончания. Для нормального образования медиатора необходима целостность тела нейрона. Изолированное нервное волокно не может долго выделять медиатор.
Фермент, расщепляющий ацетилхолин - ацетилхолинэстераза. Этот фермент обладает высоким сродстворм к ацетилхолину, который находится в виде комплекса и Х-рецептором. Различают истинную ацетилхолинэстеразу (находится в синапсах и эритроцитах), которая расщепляет ацетилхолин в физиологических концентрациях и ложную ацетилхолинэстеразу (в жидкостях организма - слюне, плазме и т. д.), которая расщепляет ацетилхолин в высоких концентрациях и разрушает еще и различные производные ацетилхолина (курарекодовые препараты). Освобождённый холин с помощью переносчиков поступает на пресимпатическую мембрану, а уксусная кислота и глюкоза поступают в кровь через межтканевую жидкость.
Х-рецепторы - белковые молекулы, обладающие высоким сродством к ацетилхолину.
Существует 2 вида холинорецепторов - М и Н.
М-холинорецепторы - чувствительны к мускалину (яду мухомора) - расположены в основном во внутренних органах, эндокринных железах, сердце, сосудах, дыхательных путях, желудочнокишечном тракте. Они обладают медленным, но продолжительным действием, могут суммировать возбуждение. Существуют 2 вида М-холинорецепторов: одна - во внутренних органах, другая - в эндокринных железах. При возбуждении М-холинорецепторв происходит торможение сердечной деятельности, раширение сосудов, активация деятельности желудочно-кишечного тракта, изменяется секреция некоторых эндокринных желёз.
Н-холинорецепторы - чувствительны к никотину. Располагаются в вегетативных ганглиях, мионевральных синапсах, в хлорофильной ткани надпочечников. Эти рецепторы обладают быстрым, кратковременным действием, не могут суммировать возбуждение. Существует 3 разновидности. За счёт наличия разновидностей рецепторы могут блокироваться различными веществами. В центральной нервной системе больше Н-холинорецепторов. М-холинорецепторы преобладают в области ствола мозга, подкорковых узлах, лимбической системе, ретикулярной формации, гипоталамусе.
Адренергические механизмы нервной системы осуществляются за счет норадреналина - составляет 90 % и других катехоламинов - 10 %.
Предшественник норадреналина - изопропилнораденалин, дофамин. Для синтеза необходимы аминокислоты тиронин, фениламин, которые поступают с постсинапсической мембраны и из тела нейрона. Любые структуры могут образовывать норадреналин, но 95 % его образуется на пресимпатической мембране.
Ферменты синтеза норадреналина - трансаминазы.
Ферменты разрушения ноадреналина - группа катехоламинтрансфераз, часто моноаминоуксусная кислота и моноаминооксидант.
Адренорецепторы - белковые молекулы, обладающие сродством к норадреналину и его производным. Эти рецепторы - наружная субъединица крайней белковой молекулы, внутренняя субъединица может быть ферментом (адемилат- и гуанилатциклазы). При взаимодействии с рецептором изменяется структура молекулы белка и, как следствие, изменяется активность фермента.
Существуют 2 вида адренорецепторов:
Альфа-адренорецепторы - блокируется дегидроэрготамином, обладают повышенной чувствительностью и норадреналину, имеют низкий порог раздражения, при выделении необходимого количества медиатора возбуждаются альфа-рецепторы. Они расположены в некоторых внутренних органах и сосудистой стенке, встречается в центральной нервной системе. Различают альфа 1- и альфа 2-адренорецепторы.
Альфа 1-адренорецепторы - при их возбуждении происходит сужение сосудов, сокращение капсулы селезёнки, матки (особенно беременной), сужение зрачка и т. д. Происходит торможение желудочнокишечного тракта (моторной и секреторной), сокращение сфинктеров.
Альфа 2-адренорецепторы - в основном в центральной нервной системе.
Бетта-адренорецепторы - блокруются бетта-блокаторами (пропранолол). Они обладают высоким порогом раздражения, т. к. имеют меньшее сродство к норадреналину. Чувствительны к различным производным норадреналина (изопротеренолол).
Бетта 1-адренорецепторы - в миокарде; при их возбуждении увеличивается сила сердечных сокращений, ускоряются обменные процессы в миокарде, несколько увеличивается частота сердечных сокращений.
Бетта 2-адренорецепторы - в сосудах, внутренних органах, эндокринных железах. При их возбуждении обеспечивается тормозной эффект, расширение сосудов (коронарных, скелетных мышц), расслабление гладких мышц, дыхательных путей. В сосудах могут встречаться альфа 1- и бетта 2-рецепторы. Альфа 1-рецепторы обеспечивают сужение, а бетта 2 - расширение сосудов. Эффект зависит от: количества медиаторов, количества рецепторов данного вида.
| Предыдущая статья: | Отделы вегетативной нервной системы |
| Следующая статья: | Физиологические механизмы боли |
| Лучшая по просмотрам статья: | Высшая нервная деятельность. Сигнальные системы |
| Последняя статья: | Физиологическая сущность аппетита и жажды. Функциональная система, поддерживающая уровень питательных веществ в крови |
| Другие статьи: | Физиологические механизмы боли Проводящие пути болевой чувствительности Антиноцицептивная система. Формирование функциональных систем с участием боли Учение о медиаторах нервной системы Отделы вегетативной нервной системы Особенности вегетативной нервной системы |
Все размещенные на нашем ресурсе материалы получены из открытых источников сети Интернет и опубликованы исключительно в информационных целях. В случае получения соответствующей просьбы от правообладателей в письменном виде, материалы будут незамедлительно убраны из нашей базы. Все права на материалы принадлежат первоисточникам и/или их авторам.
а) Ганглионарная передача нервных импульсов. Преганглионарные нейроны симпатической и парасимпатической систем — холинергические: при образовании аксодендритических синапсов с ганглионарными клетками из этих нейронов высвобождается ацетилхолин (АХ). Рецепторы на поверхности ганглионарных клеток называют никотиновыми, так как их возбуждение может происходить при местном действии никотина.
б) Передача нервных импульсов в нейроэффекторном синапсе. Постганглионарные нервные волокна симпатической и парасимпатической систем образуют нейроэффекторные соединения (синапсы)с эффекторными тканями (тканями-мишенями). За высвобождение нейромедиаторов отвечают многочисленные пресинаптические утолщения, расположенные по ходу нервных волокон.
Главный нейромедиатор в симпатических нейроэффекторных соединениях — норадреналин (норэпинефрин), который высвобождается из гранулярных везикул. Постганглионарные симпатические волокна — преимущественно адренергические; исключение составляют холинергические волокна, отвечающие за симпатическую иннервацию расположенных по всему телу эккриновых потовых желез. Главный нейромедиатор в парасимпатических нейроэффекторных соединениях — ацетилхолин (АХ). Постганглионарные парасимпатические волокна преимущественно холинергические.
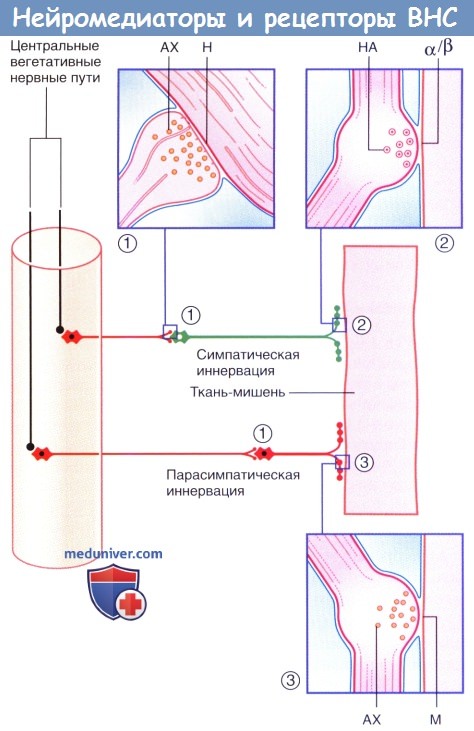
Нейромедиаторы и рецепторы вегетативной нервной системы.
(1) Аксодендритические синапсы с никотиновыми рецепторами.
(2) Нейроэффекторные синапсы с адренергическими рецепторами.
(3) Нейроэффекторные синапсы с мускариновыми рецепторами. Ганглионарные нейроны и постганглионарные волокна выделены красным цветом.
АХ — ацетилхолин; М — мускариновые рецепторы; Н — никотиновые рецепторы; НА — норадреналин.
в) Рецепторы в нейрозффекторном синапсе. Физиологические эффекты вегетативной нервной системы (ВНС) зависят от вида рецепторов на постсинаптической мембране (плазматической мембране эффекторных клеток). На высвобождение нейромедиаторов также влияют рецепторы пресинаптической мембраны (аксолеммы).
- Синаптические рецепторы симпатической системы (адренорецепторы). Для норадреналина существуют два вида а-адренорецепторов и два вида β-адренорецепторов.
1. Постсинаптические α1-адренорецеторы, активация которых вызывает сокращение гладких мышц мелких периферических артерий и крупных артериол, дилататора зрачка, а также мышц семявыносящего протока, сфинктеров ЖКТ и шейки мочевого пузыря.
2. Пресинаптические α2-адренорецеторы локализуются как на симпатических, так и на парасимпатических нервных окончаниях и ингибируют в них высвобождение нейромедиаторов. Пресинаптические α2-адренорецеторы симпатической системы называют ауторецепторами.
3. Постсинаптические адренорецепторы, возбуждение которых приводит к увеличению пейсмекерной активности клеток сердца, а также к повышению силы сердечных (желудочковых) сокращений. При резком падении артериального давления за счет активации симпатических β1-адренорецепторов юкстагломерулярных клеток почек происходит секреция ренина, который, в свою очередь, вызывает секрецию мощного вазоконстриктора ангиотензина II.
4. β2-Адренорецепторы, которые реагируют как на норадреналин, так и на адреналин (эпинефрин).
Активация постсинаптических β2-адренорецепторов вызывает расслабление гладких мышц, наиболее ярко выраженное в трахеобронхиальном дереве и мышцах глаза, участвующих в аккомодации. Часть постсинаптических β2-адренорецепторов располагается на поверхности гепатоцитов. При возрастании энергетических затрат организма их активация вызывает распад гликогена, необходимый для поддержания уровня глюкозы в крови.
Пресинаптические β2-адренорецепторы адренергических нервных окончаний отвечают за высвобождение норадреналина.
В симпатических нервных окончаниях большая часть высвобождаемого норадреналина подвергается обратному захвату моноаминным ферментным насосом. После обратного захвата часть норадреналина разрушается митохондриальным ферментом — моноаминоксидазой (МАО). Влияние лекарственных средств на симпатическую систему подробно рассмотрено в блоке клинической информации ниже.
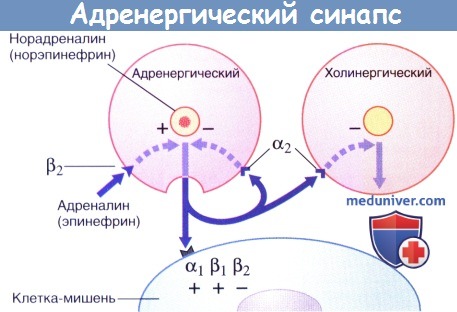
Передача возбуждения в адренергическом нейроэффекторном синапсе.
Секреция норадреналина стимулируется адреналином и ингибируется путем активации пресинаптических α2-рецепторов (данные рецепторы активируются и на пресинаптической мембране близлежащих парасимпатических синапсов, где также ингибируют секрецию).
- Синаптические рецепторы парасимпатической системы. Парасимпатические синаптические рецепторы называют мускариновыми, так как их активацию, помимо АХ, может вызывать другое химическое вещество — мускарин. Стимуляция парасимпатической системы приводит к следующим М-холинергическим эффектам.
• Замедление (в ответ на стимуляцию блуждающего нерва) частоты сердечных сокращений, а также уменьшение силы желудочковых сокращений.
• Сокращение гладких мышц, которое обусловливает такие процессы, как перистальтика кишечника, опустошение мочевого пузыря, а также рефлекс аккомодации при взгляде на близкое расстояние.
• Секреция желез.
Помимо представленных выше эффектов, пресинаптические мускариновые рецепторы симпатических нервных окончаний также отвечают за ингибирование высвобождения норадреналина.
Влияние лекарственных средств на парасимпатическую систему подробно рассмотрено в Блоке клинической информации. Лекарственные средства, обладающие мускариноподобным действием, называют холинергическими (холиномиметическими). Лекарственные средства, блокирующие доступ АХ к постсинаптической мембране, называют антихолинергическими (холинолитическими).
Главный фактор, который необходимо учитывать при назначении препаратов, активирующих или подавляющих деятельность симпатической и парасимпатической систем,— наличие рецепторов к этим лекарственным веществам α-, β- и мускариновых) в ЦНС. Так, в частности, применение данных лекарственных средств в психиатрии обусловлено их действием на центральные, а не на периферические рецепторы.
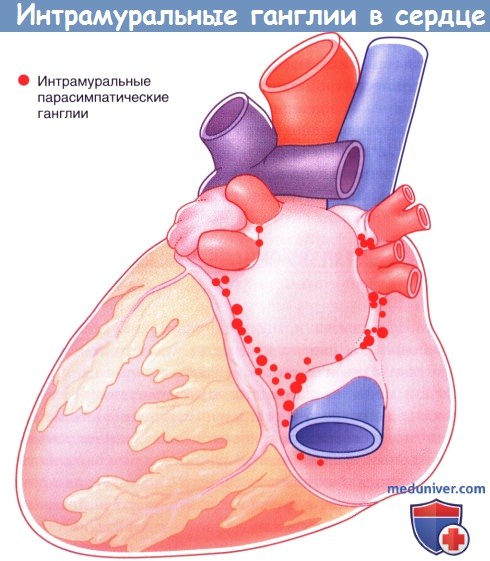
Расположение парасимпатических интрамуральных ганглиев в сердце. 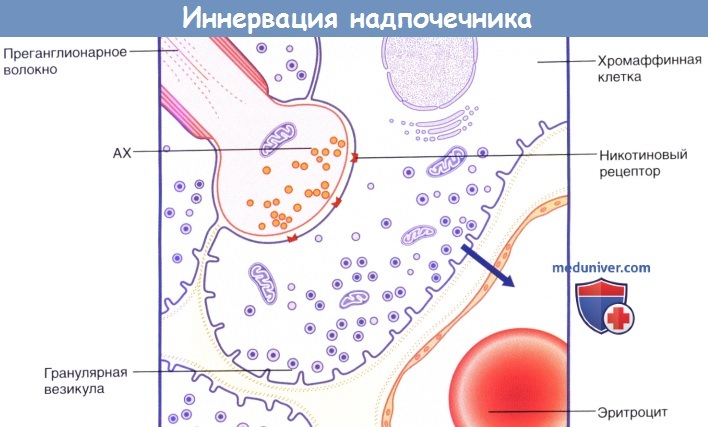
Синаптическое соединение преганглионарного волокна грудного внутренностного нерва и хромаффинной клетки мозгового вещества надпочечников.
Активация никотиновых рецепторов ацетилхолином (АХ).
8% клеток содержат крупные гранулярные везикулы (представлены на рисунке), высвобождающие адреналин; его секрекция в капиллярное русло обозначена стрелкой.
20% клеток содержат маленькие гранулярные везикулы, высвобождающие норадреналин. 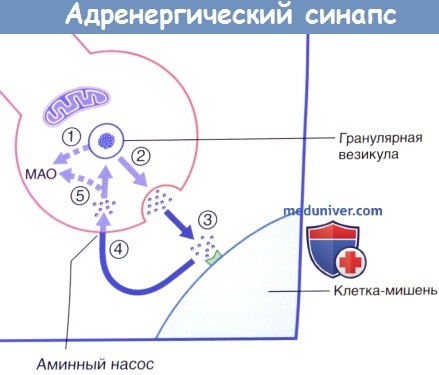
Высвобождение и обратный захват нейромедиатора в адренергическом нервном окончании.
МАО — моноаминоксидаза. 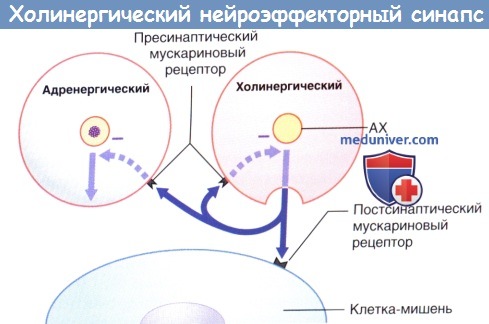
Передача возбуждения в холинергическом нейроэффекторном синапсе.
Избыточная секреция ацетилхолина (АХ) ингибируется путем активации пресинаптических мускариновых рецепторов (данные рецепторы активируются и на пресинаптической мембране близлежащих симпатических синапсов, где также ингибируют секрецию).
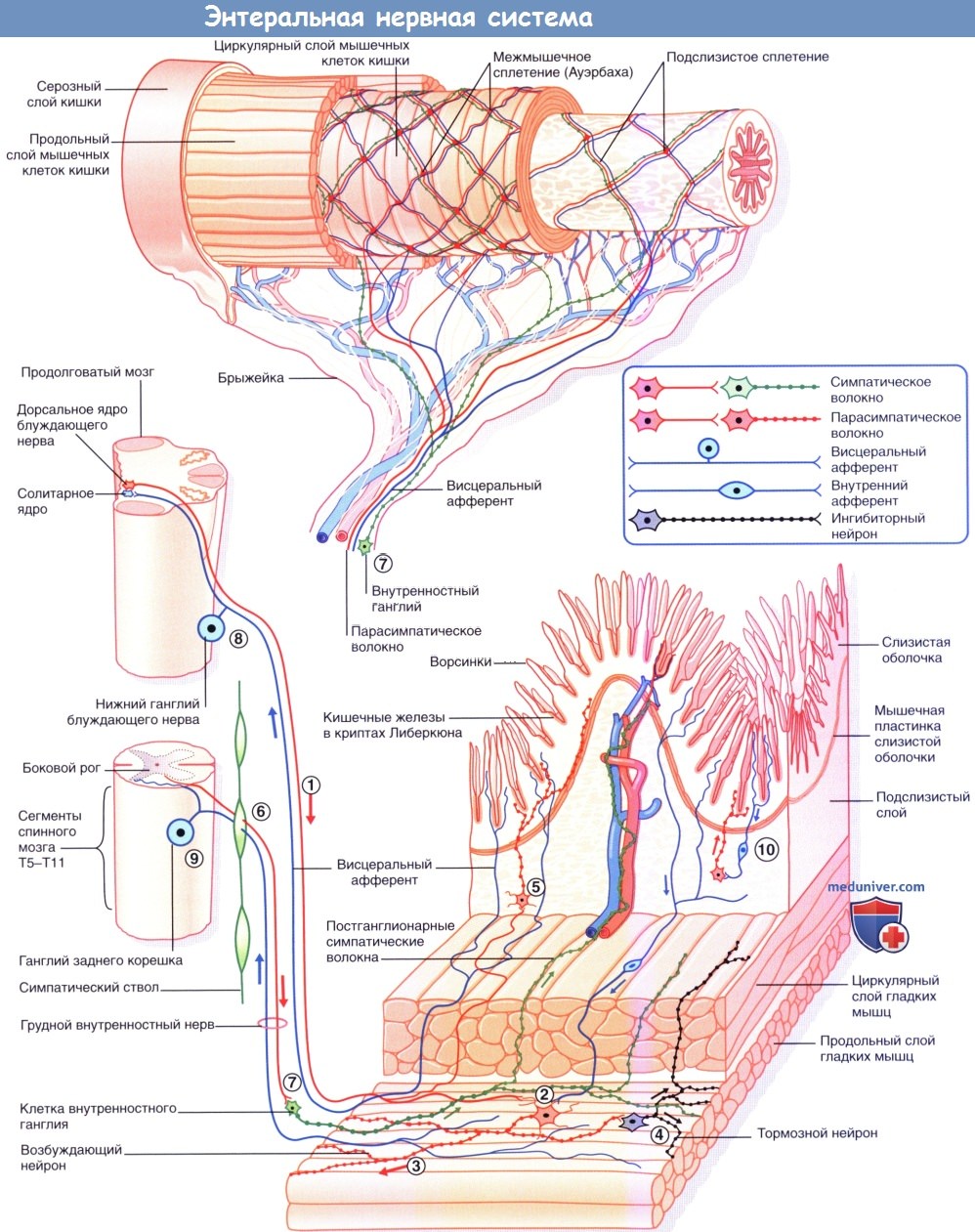
г) Другие типы нейронов. И в симпатическом, и в парасимпатическом отделах ВНС часть нейронов представлена неадренергическими, нехолинергическими нейронами (NANC-нейронами). Находящиеся в симпатических ганглиях небольшие вставочные нейроны отвечают за высвобождение дофамина — предшественника норадреналина. Часть дофамина выделяется в капиллярное русло, другая часть связывается с дофаминовыми рецепторами на основных (адренергических) нейронах, оказывая на них слабое тормозное действие.
Самое большое количество NANC-нейронов находится в области ганглионарных клеток стенки ЖКТ и в тазовых ганглиях. Эти нейроны содержат более 50 разнообразных белковых субстанций, находящихся в несвязанном состоянии или в различных комбинациях. Функция большей части этих веществ — регуляторная: действуя на пресинаптическую или постсинаптическую мембрану, они влияют на продолжительность работы основных нейромедиаторов. Другие белковые субстанции (вещества, выделяющиеся совместно с ацетилхолином (АХ)) представляют собой комедиаторы (сопутствующие медиаторы).
Редактор: Искандер Милевски. Дата публикации: 14.11.2018

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.

Центральная стимуляция деятельности сердечно-сосудистой системы осуществляется посредством симпатической нервной системы через адренергические альфа2- и имидазолиновые рецепторы. Адренергические альфа2-рецепторы локализованы во многих отделах головного мозга, но наибольшее их число находится в ядрах солитарного тракта. Имидазолиновые рецепторы локализованы главным образом в ростральной вентролатеральной части продолговатого мозга, а также в хромаффинных клетках мозгового слоя надпочечников.
Преимущественным стимулирующим действием на а2-адренорецепторы обладают метилдопа и гуанфацин. Моксонидин и рилменидин стимулируют в основном имидазолиновые рецепторы. Среди антигипертензивных ЛС этой группы только клонидин имеет форму для папаэнтерального введения и применяется в анестезиологической практике и в пред-, и в постоперационном периоде. К высокоселективным стимуляторам альфа2-адренорецепторов относится зарубежные агонисты альфа2-адренорецепторов - дексмедетомидин, оказывающее антигипертензивное действие, но применяющееся в основном в качестве седативного средства во время анестезиологического обеспечения (долгое время - лишь в ветеринарии, но не так давно внедрено в клиническую практику у людей).
Агонисты альфа2-адренорецепторов: место в терапии
Клонидин с успехом можно использовать для купирования гипертензионных реакций во время и после оперативного вмешательства, для профилактики гипердинамической реакции организма в ответ на стрессорные воздействия (интубация, пробуждение и экстубация больного).
Для премедикации клонидин назначается внутрь или в/м. При в/в введении клонидина первоначально возникает кратковременный подъем АД, который сменяется более продолжительной гипотензией. Вводить агонисты альфа2-адренорецепторов в/в желательно методом титрования.
Клонидин может использоваться в периоперационном периоде в качестве анальгетического и седативного компонента общей анестезии. При этом уменьшается гемодинамическая реакция на интубацию трахеи. В качестве компонента общей анестезии он позволяет стабилизировать гемодинамику, уменьшить потребности в ингаляционных анестетиках (на 25-50%), гипнотиках (примерно на 30%) и опиоидах (на 40-45%). Послеоперационное введение альфа2-агонистов также снижает потребность в опиоидах, предотвращая развитие к ним толерантности.
Из-за ряда побочных эффектов, малой управляемости, возможности развития выраженной гипотонии во время индукции и поддержания анестезии клонидин не получил широкого распространения. Однако в ряде клинических ситуаций его охотно используют для целей премедикации, а также потенцирования эффектов некоторых средств для анестезии в целях сокращения их дозировок на этапе ее поддержания, а также для купирования трудно поддающихся терапии эпизодов интраоперационной гипертензии. Также его применяют в послеоперационном периоде с целью купирования послеоперационной гипертензии.
Клонидин может использоваться для купирования озноба в послеоперационном периоде.
Угнетение дыхания сопровождается миозом и напоминает действие опиоидов. Лечение острого отравления включает вентиляционную поддержку, введение атропина или симпатомимети-ков для контроля брадикардии и волемическую поддержку. При необходимости назначают допамин или добутамин. Для альфа2-агонистов существует специфический антагонист - атипамезол, введение которого быстро обращает их седативный и симпатолитический эффекты.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11], [12], [13], [14]
Механизм действия и фармакологические эффекты
В результате стимуляции центральных а2-адренорецепторов, вызываемой ЛС этой группы и, в частности, клонидином, происходит угнетение вазомоторного центра, уменьшение симпатической импульсации из ЦНС и подавление активности адренергических систем на периферии. Результирующим эффектом является уменьшение ОПС и в меньшей степени СВ, что проявляется снижением АД. Агонисты альфа2-адренорецепторов урежает ЧСС и уменьшает выраженность барорецепторного рефлекса, направленного на компенсацию снижения АД, что является дополнительным механизмом развития брадикардии. Клонидин уменьшает образование и содержание ренина в плазме крови, что также вносит свой вклад в развитие гипотензивного эффекта при длительном приеме. Несмотря на снижение АД, уровень почечного кровотока не изменяется. При длительном применении клонидин вызывает задержку в организме натрия и воды и увеличение ОЦП, что является одной из причин снижения его эффективности.
В больших дозах агонисты альфа2-адренорецепторов активируют периферические пресинаптические а2-адренорецепторы в окончаниях адренергических нейронов, через которые осуществляется регуляция высвобождения норадреналина на основе отрицательной обратной связи и таким образом вызывает кратковременное повышение АД за счет сужения сосудов. В терапевтических дозах прессорное действие клонидина не выявляется, но при передозировке может развиться выраженная гипертензия.
В отличие от ГГБ и фентоламина клонидин снижает АД, не вызывая выраженной постуральной реакции. Клонидин вызывает также понижение внутриглазного давления за счет уменьшения секреции и улучшения оттока водянистой влаги.
Фармакологические эффекты альфа2-адренергических агонистов не ограничиваются антигипертензивным действием. Клонидин и дексмедетомидин используются также в связи с их отчетливыми седативным, анксиолитическим и анальгетическим свойствами. Седативный эффект связывают с депрессией основного адренергического ядра головного мозга - locus ceruleus в области ромбовидной ямки продолговатого мозга. В результате подавления аденилатциклазного и протеинкиназного механизмов уменьшается нейрональная импульсация и выброс нейротрансмиттеров.
Клонидин оказывает выраженный седативный эффект и подавляет гемодинамическую реакцию организма на стресс (например, гипердинамическую реакцию на интубацию, травматичный этап операции, пробуждение и экстубацию больного). Проявляя седативный эффект и потенцируя действие анестетиков, клонидин не оказывает существенного влияния на картину ЭЭГ (что очень важно во время операций на брахиоцефальных артериях).
Хотя собственная анальгетическая активность клонидина недостаточна для достижения периоперационной аналгезии, ЛС способно потенцировать действие общих анестетиков и наркотических веществ, особенно при интратекальном его введении. Этот положительный эффект позволяет существенно уменьшить используемые во время общей анестезии дозы анестетиков и наркотических ЛС. Важной особенностью клонидина является его способность уменьшать соматовегетативные проявления опиатной и алкогольной абстиненции, что, вероятно, также обусловлено снижением центральной адренергической активности.
Клонидин увеличивает длительность региональной анестезии, а также оказывает прямое влияние на постсинаптические альфа2-рецепторы задних рогов спинного мозга.
Читайте также:


