Аминокислоты медиаторы нервной системы
Глутамат — это единственный медиатор, который оказывает только возбуждение. При избытке глутамата возникает судорожная готовность мозга, которая может перетечь в эпилепсию. Он взаимодействует с NMDA-рецепторами. Он токсичен для гиппокампа, в связи с чем ухудшается память. В этот момент погибает большое количество нейронов, и поэтому нужно действовать ещё и нейропротекторами, а не только снимать судороги. Таких препаратов очень мало.
Глицин — это медиатор, вызывающий только торможение. Глутамат -> ГАМК (возбудитель -> тормозитель). Опять возникает судорожная готовность мозга, которая может привести к эпилепсии. С глицином в клетку входит избыток хлора, из-за чего происходит гиперполяризация. Глицин вызывает торможение в спинном мозге и немного в головном. То есть он в основном действует на мотонейроны и затормаживает их.
При входе хлора возникает гиперполяризация. Мефенезин вводят, из которого образуется мепробат, а из него бензодиазепины (их всегда совершенствуют, увеличивают их свойства. Они им побочный эффект и привыкание. Они оказывают успокаивающее действие (явл транквилизаторами)). На ГАМК-рецепторе есть участок, который продливает действие ГАМК, и на нем находятся БД. Эндозепины вырабатываются в организме и делают нас более спокойными. Оппиатная система мозга, которая препятствует болевой чувствительности. Ноуицептивная система и опиатная система (эндорфины вырабатываются в гипоталамогипофизарной системе и снижают болевую чувствительность, и энкофалины вырабатываются в среднем мозге и также снижают болевую чувствительность). Опиатная система приспособлена к тому, чтобы взаимодействовать с морфием. В мозге вырабатывается морфий, и к нему есть рецепторы. Он нужен для того, чтобы также снижать болевую чувствительность.
Бордопиратами можно снять эпилептический статус, но они приводят к резкому снижению интеллектуальной деятельности.

У нас в организме синтезируется 23 аминокислоты. В мозге также содержатся аминокислоты, первая их функция – они принимают участие в синтезе белка, но аминокислоты, которые содержатся в головном и спинном мозге выполняют медиаторную функцию. И 75% аминокислот в ЦНС приходится на глутомат, глицин, аспаразиновую кислоту (ее в программе нет) и гаммааминомаслянную кислоту.
Что касается глицина, его функцию мы в прошлый раз выяснили – это мощный тормозный медиатор, он обеспечивает как прямое торможение в системе реципропной иннервации мышц антагонистов и в системе возвратного торможения с участием клеток РЕНШОУ. За счет чего возникает торможение с помощью глицина? - На мембране возникает процесс гиперполяризации в результате того, что открывается большее количество каналов (повышается проницаемость мембраны) для ионов калия. Глицин синтезируется из глюкозы и не только в нервных клетках, но и во многих клетках организма, он проходит через гематоэнцефалический барьер (ГЕБ). Рецепторы к глицину есть не только в постсинаптический мембране нервной клетки, но и в других участках мембраны нейрона, и это обеспечивает лечебное действие того глицина, который применяется в фармакологии, т. е. он не включается в синаптическую передачу, а влияет на рецепторы в нервной клетке внесинаптические.
Глутомат – это только возбуждающий медиатор, он синтезируется из глюкозы только в клетках нервной системы. Он напротив вызывает деполяризацию мембраны нейронов, за счет повышения ее проницаемости для ионов натрия. Сконцентрированы нейроны, синтезирующие глутомат в основном в лобной коре. Если 3-4 года назад он рассматривался только как медиатор, то сейчас говорят о том, что он принимает участие в синтезе белка, т.е. он включается в метоболические процессы в нервных клетках.. К нему открыты NMDA – рецепторы. Когда глутомат взаимодействует с ними, происходит деполяризация мембраны, которая приводит к возникновению потенциала действия, а значит возбуждению нервной клетки. После открытия NMDA- рецепторов стало понятно, почему барбитураты оказывают тормозное влияние на эпилептические приступы. Оказалось на рецепторе к глютонату есть участок который взаимодействует с барбитуратами. Если есть вещество, которое садится на этот рецептор, глутомату не с чем взаимодействовать и поэтому возникает торможение. К сожалению глутомат – необходимый медиатор при взаимодействии нервных клеток для формирования памяти, он обязательно включается в механизмы формирования памяти. Особенно опасно применять барбитураты для лечения маленьких детей, у которых страдает память, обучение. Хотя нет еще таких препаратов, которые так быстро снимали эпилептический приступ.
Один фермент, который взаимодействует с глутоматом, одна ступенька от глутомата, и глутомат превращается в ГАМК. Гаммааминомаслянная кислота – это тоже тормозный медиатор, она синтезируется только в мозге, содержится в коре, в мозжечке, в черной субстанции. Это мощная тормозная система головного мозга (глицин – спинной мозг). Повышенная активность глюконатэргической системы, или усиленный выброс глуконата приводит к судорожной готовности мозга, которая может спровоцировать приступ эпилепсии. Недостаток гамкэргической системы приводит к тем же последствиям, к повышенной судорожной готовности мозга. Большая часть препаратов, которыми лечится эпилепсия, направлены на то, чтобы усилить секрецию ГАМК или затормозить разрушение ГАМК.
Рисуем нервную клетку, мембрану, рецептор к ГАМК.
Когда ГАМК взаимодействует с этим рецептором, каков механизм действия ГАМК?
ГАМК повышает проницаемость клеточной мембраны для хлора, хлор входит в клетку и увеличивается на мембране мембранный потенциал, на мембране возникает гиперполяризация в виде ТПСП, а это повышает порог этой клетки, клетка затормаживается к ней сигналы подходят, но она возбудиться не может. Можно менять проницаемость для натрия, для кальция, для хлора, вот ГАМК меняет проницаемость мембраны клетки к хлору. ГАМК – это мощный тормозитель. На основе ГАМК был синтезирован препарат мефенезин его применяли при операции для расслабления мускулатуры. Затем его решили усовершенствовать, задача была та же – повысить расслабление скелетной мускулатуры, и синтезировали мекробамат, когда его стали применять оказалось, что он оказывает к тому же успокаивающее влияние на больного.
Тогда стали работать с этим препаратом, искать различные его формы и разработали – бензодиазепины – транквелизаторы, которые гасят чувство страха, снимают эмоциональное напряжение.
Почему они оказывают свое действие? – значит к этим веществам есть рецепторы. Оказалось что рецепторы к бензодиазепину находятся на рецепторе к ГАМК-у (он взаимодействует с участком рецепторов к ГАМК-у) Явление успокоения возникает в результате того, что бензодиазепин задерживает ГАМК в синаптической щели, т. е. он не разрушается и не захватывается обратно, бензодиазипин удлиняет срок действия Гамк-а в синаптической щели. Природные легамды, вещества которые обладают успокаивающим действием на человека, пока они не найдены. Но зато был найден эндозипин – к нему тоже есть участок на ГАМК – рецепторе, но при этом взаимодействии возникает чувство страха, чувство паники. Все зависит от того что возьмет верх эндозепины или бензодиазепины, которых мы еще не знаем, или те бензодиазепины, которые мы принимаем в виде таблеток, все они борются за рецепторы. Оказалось, что у нас в мозге синтезируется карболины, которые вызывают чувство паники.
Наиболее распространенный возбуждающий медиатор головного и спинного мозга — аминокислота L-глутамат. Значимый пример возбуждающих нейронов, использующих глутамат в качестве медиатора,— все нейроны, идущие от коры полушарий к белому веществу мозга, независимо от их направления в других частях коры полушарий, ствола или спинного мозга. Глутамат синтезируется из α-кетоглутарата, который, кроме того, служит субстратом для образования ГАМК.
ГАМК — самый распространенный в спинном и головном мозге тормозной медиатор, участвующий в работе приблизительно трети всех синапсов нервной системы. Миллионы ГАМКергических нейронов образуют основную часть вещества хвостатого и чечевицеобразного ядер, их также встречают в большом количестве в околоводопроводном сером веществе, гипоталамусе и гиппокампе. Кроме того, ГАМК выполняет функцию медиатора в крупных клетках Пуркинье, которые являются единственными клетками, выходящими из коры мозжечка. Аксоны клеток Пуркинье спускаются к зубчатому и другим ядрам мозжечка. ГАМК синтезируется из глутамата под действием фермента глутаматдекарбоксилазы.
Третий аминокислотный нейромедиатор — глицин. Глицин участвует в синтезе белков всех тканей организма и представляет собой простейшую аминокислоту, синтезируемую из серина в процессе катаболизма глюкозы. Этот нейромедиатор оказывает тормозное действие преимущественно в синапсах ассоциативных нейронов ствола мозга и спинного мозга.
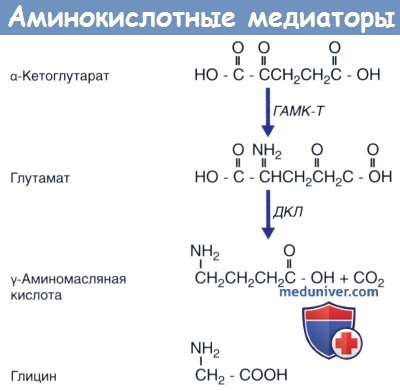
Три аминокислотных медиатора.
Глутамат синтезируется из а-кетоглутарата под действием фермента ГАМК-трансаминазы (ГАМК-Т);
γ-аминомасляная кислота (ГАМК) синтезируется из глутамата под действием декарбоксилазы глутаминовой кислоты (ДГК).
Глицин представляет собой простейшую аминокислоту.
а) Глутамат. Глутамат выполняет функцию нейромедиатора как в ионотропных, так и в метаботропных рецепторах. К ионотропным рецепторам относят АМРА-, каинат- и NMDA-рецепторы, которые получили свои названия благодаря активирующим их синтетическим агонистам: амино-метил-изоксазол-пропионовой кислоте, каинату и N-метил-D-аспартату, соответственно. Каинатные рецепторы редко встречаются изолированно; чаще всего они комбинируются с АМРА-рецепторами и входят в состав АМРА-каинатных (АМРА-К) рецепторов.
Важно отметить, что ионы Са 2+ также проникают внутрь клетки и за счет продолжительного периода деполяризации, длительность которого достигает 500 мс от возникновения единичного потенциала действия, активируют Са 2+ -зависимые ферменты, способные изменять структуру клетки-мишени и даже количество ее синаптических контактов. Феномен синаптической пластичности в ответ на активацию рецепторов можно отчетливо проследить в экспериментальных исследованиях на культивируемых срезах гиппокампа крыс. Этот феномен считают основным механизмом развития кратковременной памяти. Например, анальгетик кетамин, блокирующий NMDA-каналы, помимо своего основного действия препятствует формированию памяти.
Характерная особенность многократно повторяющейся активации NMDA-рецепторов — долговременное потенцирование, проявляющееся возникновением ВПСП со значениями, превышающими нормальные показатели даже несколько дней спустя (см. далее — длительная депрессия).
Роль NMDA-рецепторов в развитии феномена глутаматной эксайтотоксичности подтверждена развитием ишемических инсультов у экспериментальных животных. Предполагают, что причиной гибели большого количества нейронов стало избыточное поступление ионов Са 2+ в клетку в ходе следующих событий: ишемия > избыточное поступление ионов Са 2+ в клетку > активация Са 2+ -зависимых протеаз и липаз > разрушение белков и липидов > гибель клетки. Назначение антагониста NMDA-рецепторов сразу же после первичного инсульта позволяет снизить тяжесть ишемического поражения мозга.
Метаботропные глутаматные рецепторы Выделяют более 100 различных метаботропных глутаматных рецепторов. Все метаботропные рецепторы — это внутренние мембранные белки, большинство которых располагается на постсинаптических мембранах и оказывает возбуждающее действие. Некоторые метаботропные рецепторы локализуются на пресинаптической мембране и являются тормозными ауторецепторами.
б) ГАМК. ГАМК-рецепторы могут быть как ионотропными, так и метаботропными.
1. Ионотропные ГАМК-рецепторы. Рецепторы, называемые ГАМКA, расположены в большом количестве в области лимбической доли головного мозга. Каждый рецептор связан с хлорным каналом. При активации ГАМКA-рецепторов хлорные каналы открываются, и ионы Cl- по градиенту концентрации поступают из синаптической щели в цитозоль. Причиной гиперполяризации, при которой достигаются значения -70 мВ и ниже, служит суммация последовательных ТПСП.
Основной антагонист, занимающий активный центр рецептора, — конвульсант бикукуллин. Другой конвульсант — пикротоксин — связывается с субъединицами белка, в активном состоянии закрывающими ионный канал.
Ответная реакция этого вида рецепторов нейрона-мишени медленнее и слабее по сравнению с ионофорезом ГАМКA, и для их активации необходима стимуляция большей частоты. В связи с этим считают, что ГАМКA-рецепторы расположены не во внешнем слое синаптической щели, а внесинаптически. Это предположение может быть подтверждено наличием еще одного вида расположенных внесинаптически G-направленных каналов. Эти кальциевые каналы также потенциалозависимые и принимают участие в обеспечении клетки количеством ионов Са 2+ , необходимым для перемещения синаптических пузырьков через пресинаптическую мембрану. При активации G-Са 2+ -лигандного участка связывания происходит закрытие кальциевых каналов, что приводит к снижению влияния потенциала действия, а также к торможению исходного нейрона (источника возбуждения) и других прилежащих глутаматергических нейронов.
В некоторых случаях для лечения заболеваний, связанных с чрезмерным рефлекторным тонусом мышц (мышечная спастичность), применяют инъекции миорелаксанта баклофена (агониста ГАМКВ) в окружающее спинной мозг субарахноидальное пространство. Баклофен проникает в спинной мозг и ингибирует высвобождение глутамата из чувствительных нервных окончаний в основном за счет уменьшения поступления большого количества ионов Са 2+ в клетку, возникающего под влиянием потенциалов действия чрезмерной частоты.
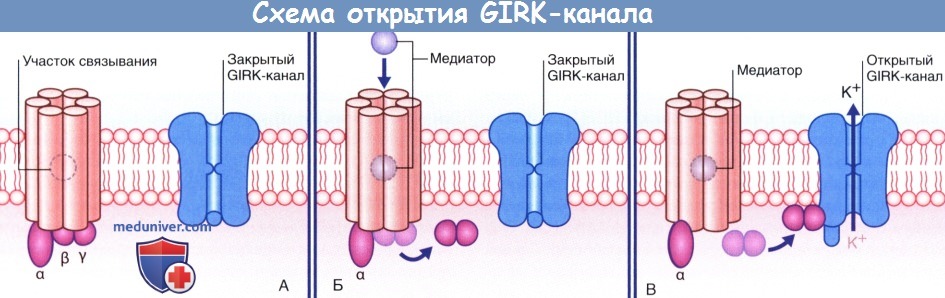
Схема открытия GIRK-канала, расположенного на постсинаптической мембране, G-белком.
(А) Состояние покоя. (Б) ГАМК активирует рецептор, и βγ-субъединица G-белка перемещается по направлению к GIRK-каналу.
(В) βγ-субъединица вызывает высвобождение ионов К + , что приводит к гиперполяризации мембраны. 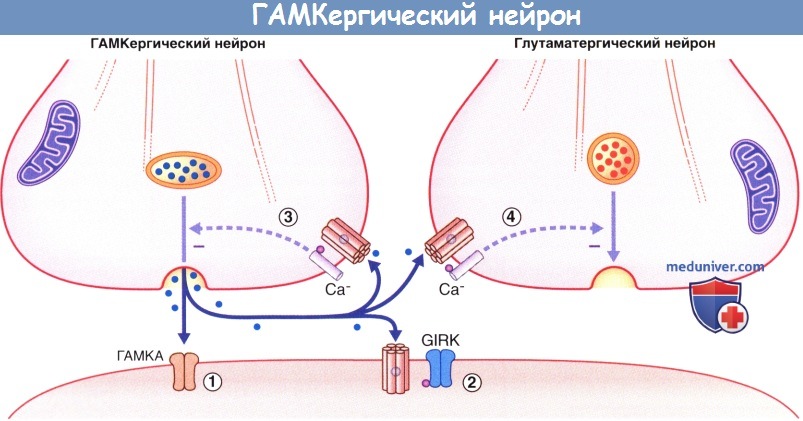
Высвобождение медиатора и дальнейшие процессы, происходящие в ГАМКергическом нейроне.
(1) Связываясь с ГАМКA-рецепторами, медиатор вызывает гиперполяризацию мембраны нейрона-мишени за счет открытия хлорных (Cl - ) каналов.
(2) Аналогичное действие оказывают связывающиеся с GIRK рецепторы ГАМКВ за счет открытия G-белок-связанных калиевых каналов внутреннего выпрямления (GIRKS).
(3) При связывании ГАМКВ-ауторецепторов уменьшается высвобождение медиатора исходным нейроном за счет закрытия лиганд-G-белок-зависимых кальциевых (Са 2+ ) каналов.
(4) Связывание ГАМКВ-рецепторов соседнего глутаматергического нейрона оказывает аналогичное влияние, опосредованное действием ионов Са 2+ .
3. Обратный захват глутамата и ГАМК. Обратный захват глутамата и ГАМК происходит двумя путями. В левой части каждого рисунка показано, что некоторые молекулы медиатора захватываются из синаптической щели транспортными белками мембраны и помещаются обратно в синаптические пузырьки. В правых частях рисунков изображен захват молекул медиаторов прилежащими астроцитами. Находясь в астроците, глутамат под действием глутаминсинтетазы превращается в глутамин. В процессе последующего транспорта к синаптическому уплотнению глутамат достраивается под действием глутаминазы и помещается в синаптический пузырек. ГАМК превращается в глутамат под действием ГАМК-трансаминазы. В процессе транспорта глутамат трансформируется в глутамин под действием глутаминсинтетазы.
Вернувшись в область синаптического уплотнения, глутамин под действием глутаминазы превращается в глутамат, из которого под действием глутаматдекарбоксилазы синтезируется ГАМК, молекулы которой помещаются в синаптические пузырьки.
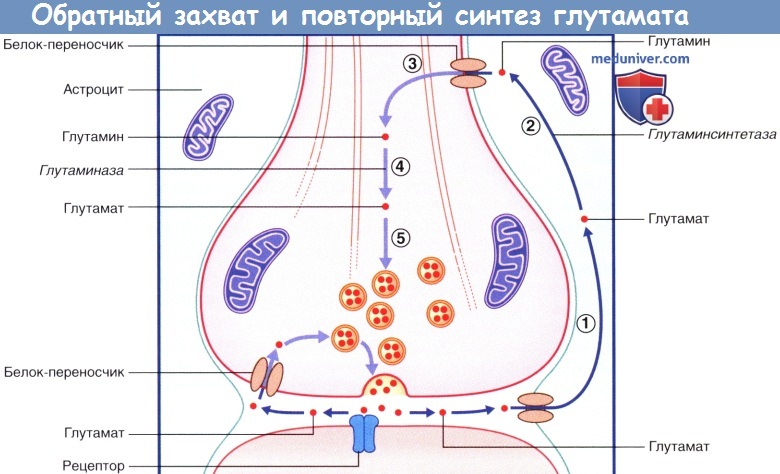
Схема обратного захвата и повторного синтеза глутамата.
В левой части рисунка происходит обратный захват молекулы глутамата в неизменном виде.
В правой части рисунка (1) глутамат захватывается астроцитами, затем (2) под действием глутаминсинтетазы превращается в глутамин.
(3) Глутамин поступает в нервное окончание, (4) где под действием глутаминазы превращается в глутамат, который (5) возвращается в синаптические пузырьки. 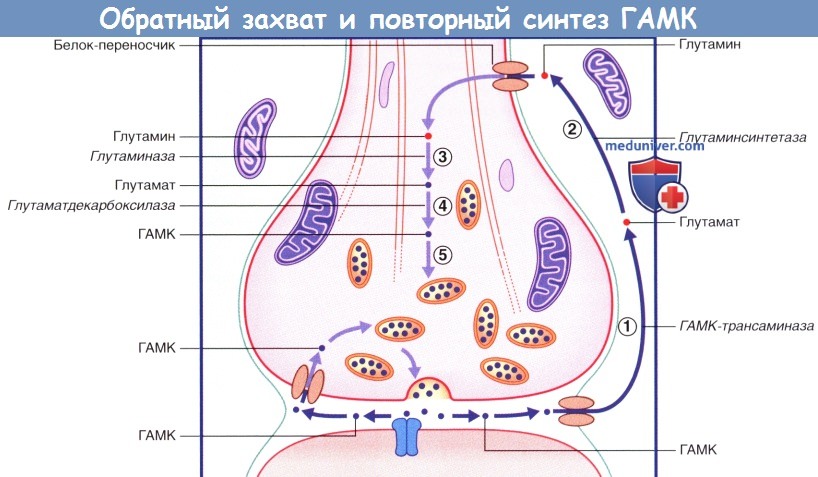
Схема обратного захвата и повторного синтеза ГАМК. В левой части рисунка происходит обратный захват молекулы ГАМК в неизменном виде.
В правой части рисунка ГАМК захватывается астроцитами, затем (1) под действием ГАМК-трансаминазы превращается в глутамат, который (2) под действием глутаминсинтетазы превращается в глутамин.
(3) Глутамин поступает в нервное окончание и под действием глутаминазы образует глутамат.
(4) Глутамат под действием глутаматдекарбоксилазы превращается в ГАМК, которая (5) возвращается в синаптические пузырьки.
г) Глицин. Глицин синтезируется из серина в процессе катаболизма глюкозы. Основная функция этого нейромедиатора — обеспечение отрицательной обратной связи двигательных нейронов ствола мозга и спинного мозга. При инактивации глицина (например, при отравлении стрихнином) возникают мучительные судороги.
Обратный захват. В области синаптического уплотнения при помощи аксональных белков-переносчиков осуществляется быстрый обратный захват глицина с последующим его помещением в синаптические пузырьки.
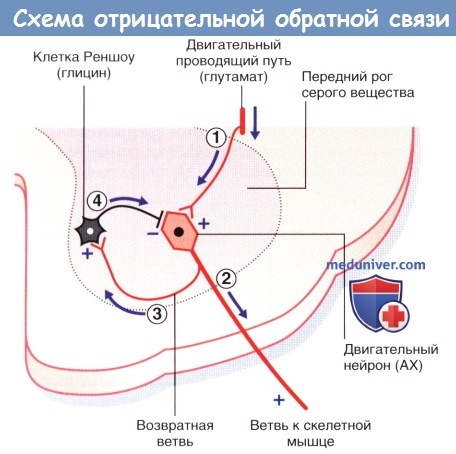
Схема отрицательной обратной связи: клетки Реншоу ингибируют избыточное возбуждение двигательных нейронов. АХ—ацетилхолин.
(1) Нейрон нисходящего двигательного проводящего пути оказывает возбуждающее действие на двигательный нейрон спинного мозга.
(2) Двигательный нейрон вызывает сокращение мускулатуры.
(3) Возвратная ветвь стимулирует клетку Реншоу.
(4) Клетка Реншоу оказывает ингибирующее влияние, достаточное для предупреждения чрезмерной активации двигательного нейрона.
Редактор: Искандер Милевски. Дата публикации: 12.11.2018
Медицинский эксперт статьи


Нейромедиатор (нейротрансмиттер, нейропередатчик) - это вещество, которое синтезируется в нейроне, содержится в пресинаптических окончаниях, высвобождается в синаптическую щель в ответ на нервный импульс и действует на специальные участки постсинаптической клетки, вызывая изменения мембранного потенциала и метаболизма клетки.
До середины прошлого века к медиаторам относили только амины и аминокислоты, однако открытие нейромедиаторных свойств у пуриновых нуклеотидов, производных липидов и нейропептидов значительно расширило группу медиаторов. В конце прошлого века было показано, что некоторые АФК также обладают свойствами, сходными с медиаторами.

[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11]
Химическое строение медиаторов
По химическому строению медиаторы являются неоднородной группой. В нее входят эфир холина (ацетилхолин); группа моноаминов, включающая катехоламины (дофамин, норадреналин и адреналин); индолы (серотонин) и имидазолы (гистамин); кислые (глутамат и аспартат) и основные (ГАМК и глицин) аминокислоты; пурины (аденозин, АТФ) и пептиды (энкефалины, эндорфины, вещество Р). К этой же группе примыкают вещества, которые не могут быть классифицированы как истинные нейромедиаторы - стероиды, эйкозаноиды и ряд АФК, прежде всего N0.
Для решения вопроса о нейромедиаторной природе какого-либо соединения используется ряд критериев. Основные из них изложены ниже.
- Вещество должно накапливаться в пресинаптических окончаниях, высвобождаться в ответ на приходящий импульс. Пресинаптическая область должна содержать систему синтеза этого вещества, а постсинаптическая зона - обнаруживать специфический рецептор для данного соединения.
- При стимуляции пресинаптической области должно происходить Са-зависимое выделение (путем экзоцитоза) этого соединения в межсинаптическую щель, пропорциональное силе стимула.
- Обязательная идентичность эффектов эндогенного нейромедиатора и предполагаемого медиатора при его аппликации на клетку-мишень и возможность фармакологического блокирования эффектов предполагаемого медиатора.
- Наличие системы обратного захвата предполагаемого медиатора в пресинаптические терминали и/или в соседние астроглиальные клетки. Возможны случаи, когда обратному захвату подвергается не сам медиатор, а продукт его расщепления (например, холин после расщепления ацетилхолина ферментом ацетилхолинэстеразой).
Влияние лекарственных препаратов на различные этапы медиаторной функции в синаптической передаче
Добавка предшественника
Блокада обратного захвата
Блокада ферментов синтеза
Торможение захвата в везикулы Торможение связывания в везикулах
Стимуляция тормозных ауторецепторов Блокада ауторецепторов
Нарушение механизмов экзоцитоза
Эффекты агонистов на рецепторы
Блокада постсинаптических рецепторов
Блокада обратного захвата нейронами и/или глией
Торможение разрушения в нейронах
Торможение разрушения в синаптической щели
Применение различных методов тестирования медиаторной функции, в том числе и самых современных (иммуногистохимических, рекомбинантных ДНК и др.), затруднено из-за ограниченной доступности большинства индивидуальных синапсов, а также из-за ограниченности набора средств направленного фармакологического воздействия.
Первоначально считалось, что нервное окончание может содержать только один медиатор. К настоящему времени показана возможность наличия в терминали нескольких медиаторов, высвобождающихся совместно в ответ на импульс и воздействующих на одну клетку-мишень - сопутствующие (сосуществующие) медиаторы (комедиаторы, котрансмиттеры). При этом происходит накопление разных медиаторов в одной пресинаптической области, но в разных везикулах. Примером комедиаторов могут служить классические медиаторы и нейропептиды, которые различаются местом синтеза и, как правило, локализуются в одном окончании. Высвобождение комедиаторов происходит в ответ на серию возбуждающих потенциалов определенной частоты.
В современной нейрохимии кроме нейромедиаторов выделяют вещества, модулирующие их эффекты, - нейромодуляторы. Их действие носит тонический характер и более продолжительно во времени, чем действие медиаторов. Эти вещества могут иметь не только нейрональное (синаптическое), но и глиальное происхождение и не обязательно опосредоваться нервными импульсами. В отличие от нейромедиатора модулятор действует не только на постсинаптическую мембрану, но и на другие части нейрона, в том числе и внутриклеточно.
Вещества, осуществляющие медиаторные функции, различаются не только по химическому строению, но и по тому, в каких компартментах нервной клетки происходит их синтез. Классические низкомолекулярные медиаторы синтезируются в аксонной терминали и включаются в маленькие синаптические пузырьки (50 нм в диаметре) для хранения и высвобождения. N0 также синтезируется в терминали, но, поскольку не может быть упакован в пузыръки, то сразу же диффундирует из нервного окончания и оказывает воздействие на мишени. Пептидные нейромедиаторы синтезируются в центральной части нейрона (перикарионе), упаковываются в большие везикулы с плотным центром (100-200 нм в диаметре) и транспортируются с помощью аксонального тока к нервным окончаниям.

[12], [13], [14], [15], [16], [17], [18], [19], [20], [21]
Важнейшими медиаторами центральной нервной системы являются аминокислоты: глутаминовая килота, γ-аминомасляная кислота и глицин.
Глутаминовая кислота (глутамат)

воздействует на ионотропные рецепторы, связанные с катионными каналами и, по-видимому, является важнейшим возбуждающим препаратом в ЦНС, подобно тому, как в периферической нервной системе эту же роль играет ацетилхолин.
γ-Аминомасляная кислота (ГАМК) H2N-CH2-CH2-CH2-COOH в противоположность глутамату, опосредует быстрое торможение в головном мозге. Ионотропные рецепторы, с которыми взаимодействует этот медиатор, соединены с каналами, которые, открываясь, пропускают небольшие отрицательно заряженные ионы, главным образом Cl-, но не проницаемы для положительных ионов (анионные каналы, см. рис. в след. лекции). Концентрация ионов хлора вне клетки намного больше, чем внутри, а равновесный хлорный потенциал близок к МПП или даже более отрицателен. Если равновесный хлорный потенциал более отрицателен чем МПП, то открытие анионных каналов приведет к вхождению ионов хлора в клетку и вызывает гиперполяризацию клетки. Если же равновесный хлорный потенциал равен МПП, то в покое ток ионов хлора не увеличится, но при деполяризации мембраны поток ионов хлора в клетку сразу увеличится и будет стремиться вернуть мембранный потенциал к исходному значению и тем самым затруднять (тормозить) деполяризацию и препятствовать возникновению ПД.
Сходную функцию выполняет в спинном мозге простейшая аминокислота глицин H2N-CH2-COOH.
Нейропептиды.
Ацетилхолин, моноамины и другие медиаторы, которые рассматривались в предыдущем разделе, - это "классические" низкомолекулярные медиаторы. Однако в нервной системе образуются и выделяются также пептиды, играющие роль медиаторов или синаптичесиких модуляторов (агентов, влияющих на синаптическое проведение). Список этих пептидов постоянно растет, и к началу девяностых годов их было известно более 30. Пока не ясно, сколько из этих нейропептидов играют роль истинных нейромедиаторов, влияющих на постсинаптические клетки, непосредственно примыкающие к тому волокну, которое выделяет нейропептиды. Большинство пептидов первоначально известных как интестинальные (кишечные) гормоны (являются также медиаторами энтеральной нервной системы), такие как секретин, гастрин, брадикинин, соматостатин, вазоактивный интестинальный полипептид и холецистокинин присутствует в головном мозге и могут высвобождаться при определенных воздействиях. Первым намеком на идентичность пептидов центральной и энтеральной нервной системы стал медиатор, известный как субстанция Р. Субстанция Ρ состоит из 11 аминокислотных остатков и является членом небольшого семейства родственных пептидов — тахикининов. Были установлены три рецептора нейрокининов (ΝΚ1, ΝΚ2, ΝΚ3), которые принадлежат к суперсемейству рецепторов, сопряженных с G-белками. Субстанция Ρ выполняет функцию медиатора в окончаниях сенсорных аксонов малого диаметра дорзальных слоев спинного мозга, связанных с восприятием боли (ноцицепцией).
Некоторые из этих веществ, подобно рилизинг-факторам гипоталамуса, более корректно называют нейросекреторными веществами, т.е. веществами, которые выделяются из нервных окончаний в кровоток и поступают к клеткам мишеням с кровью. Есть данные, что одни и те же пептиды могут выделяться в качестве медиаторов одними нейронами, нейросекретов - другими и кроме того выделяться тканями внутренних органов в виде гормонов. Подобная полифункциональность не так уж и удивительна, поскольку давно известно, что биогенный амин норадреналин и близкий к нему адреналин образуются как гормоны в мозговом слое надпочечников, так и высвобождаются некоторыми нервными окончаниями в качестве медиатора. Кроме того, нейропептиды могут выделяться в качестве медиаторов нервными окончаниями, высвобождающими одновременно и какой либо классический медиатор, например ацетилхолин, серотонин или норадреналин. Большой интерес у исследователей вызывают две группы нейропептидов - эндорфины и энкефалины. Эти вещества обладают аналгетическими (уменьшающими боль), а также другими морфиноподобными свойствами, например, вызывают ощущение удовольствия и эйфорию. Содержание этих веществ в головном мозге увеличивается, когда человек ест, слушает приятную музыку или занимается другими видами деятельности вызывающими чувство удовлетворения. В отношении воздействия на нервную систему эндорфины и энкефалины сходны с опиатами (опий и его производные). Поэтому их называют эндогенными опиоидами. До недавнего времени не знали, почему некоторые алкалоиды типа опия, морфина и героина оказывают столь мощное влияние на нервную систему. Теперь же известно, что на плазматических мембранах некоторых нейронов имеются опиоидные рецепторы. В естественных условиях с этими рецепторами связываются эндогенные опиоиды т.е. энкефалины и эндорфины и в следствие этого может возникнуть чувство удовлетворения или развиться анальгетический эффект. И лишь по случайному совпадению к этим рецепторам способны присоединяться наркотические опиаты, выделяемые из растений, вызывая состояние эйфории. Это ощущение душевного комфорта, положительное восприятие окружающей обстановки независимо от реальной действительности, уверенность в себе, возникающая в результате, мощной неестественной стимуляции опиоидных рецепторов, побуждает людей повторно употреблять наркотики. Однако при этом возникают компенсаторные изменения метаболизма нервных клеток, приводящие к развитию наркотической метаболической зависимости. Организм нуждается в постоянном поступлении опиоидов, без введения которых человек испытывает чрезвычайный дискомфорт. Подобная метаболическая зависимость называется пристрастием, а страдающий ей человек - наркоманом.
При изучении опиоидных рецепторов весьма полезным оказалось вещество налоксон - конкурентный блокатор этих рецепторов. Поскольку налоксон припятствует связыванию опиатов или опиоидов с клетками-мишенями, с его помощью можно определить, вызвана ли та или иная реакция возбуждением таких рецепторов. Было обнаружено, например, что налоксон в значительной степени снимает анальгетический эффект плацебо (нейтрального вещества, которое дают больным, уверяя их, что оно снимет у них боль). Очевидно, что вера в лекарство или другое средство лечения, которое должно снять боль, приводит к выбросу опиоидных пептидов; возможно, в этом и состоит физиологический механизм действия плацебо. Налоксон снимает также обезболивающий эффект иглоукалывания. Отсюда был сделан вывод, что при иглоукалывании из ЦНС выбрасываются естественные опиоидные пептиды. Обезболивающий эффект энкефалинов и эндорфинов может быть связан с тем, что эти нейропептиды препятствуют выделению медиаторов (в частности, субстанции Р) из окончаний нервных клеток, участвующих в формировании болевой чувствительности.
Читайте также:


