Биогенные амины в нервной системе
К биогенных аминов относят катехолами ни — адреналин, норадреналин, дофамин — производные тирозина, а также серотонин, который синтезируется из триптофана. Адреналин проявляет в основном гормональную активность, норадреналин — медиатор адренергических синапсов центральной и периферической нервной системы. Роль норадреналина как одного из основных медиаторов нервной системы заключается в поддержании активности нервовопсихичних реакций, формировании когнитивных и адаптивных процессов.
Биосинтез катехоламинов в нервной системе происходит по общему механизму из тирозина.
Ключевой фермент синтеза — тирозингидроксилазы регулирует образование ДОФА, который преобразуется в дофамин под действием пиридоксинзалежнои декарбоксилазы. Гидроксилирования боковой цепи дофамина приводит к синтезу норадреналина. Аналогичная реакция происходит в мозговом слое надпочечников. В реакции метилирования норадреналина при участии SAM образуется адреналин. Катехоламины хранятся в синаптических пузырьках до их выделения под влиянием нервного импульса.

Биогенные амины нервной системы
Существуют α и βадренергични рецепторы для норадреналина. Они отличаются по специфическим реакциями, которые вызывают, а также по специфическим ингибиторами, которые эти реакции блокируют.
В нервной системе адренорецепторы расположены на постсинаптических мембранах и обеспечивают передачу нервного импульса на эффекторную клетку, а также на пресинаптических мембранах, тормозя поступления медиатора в синаптическую щель.
Передача сигнала в адренергических синапсах через α1адренорецепторы происходит путем повышения цитозольной концентрации Са + + за счет поступления его внутрь клетки и высвобождение из внутренних депо. Увеличение концентрации Са + + активирует Сазалежни процессы в клетке.
В отличие от α1адренорецепторив α2адренорецепторы, зьязуючись со специфическими ингибиторной белками, тормозят активность аденилатциклазы.
Дофамин — медиатор центральной и периферической нервной системы. Он регулирует поведение, контролирует произвольные движения тела, деятельность многих систем и органов организма. Нарушение дофаминергической передачи нервных импульсов приводит к развитию паркинсонизма).
После воздействия на клеточные мембраны катехоламины быстро удаляются из синаптической щели. Регуляторный белок пресинаптической мембраны ахромогранин чувствителен к концентрации медиатора в синаптической щели, прекращает его выделения и связывает катехоламин, который уже освободился. С помощью активного транспорта медиатор транслоцируется снова в пресинаптическую мембрану и включается в синаптические визикулы. В пресинаптических нервных окончаниях избыток медиатора инактивируется МАО (МАО), шо регулирует окислительное дезаминирование норадреналина, серотонина, дофамина, адреналина с образованием соответствующих альдегидов. Кроме того, катехоламины, попадающих через общий кровоток в печень, инактивируются катехоламінОметилтрансферазою и экскретируются с мочой в виде ароматических кислот.
Химические соединения, которые изменяют метаболизм катехоламинов, нарушают их синтез, накопление и выделения, способны изменять поведение, настроение, вызвать седативный или антидепрессантный эффект. Алкалоид резерпин специфически тормозит вторичный транспорт катехоламинов в гранулы нейронов, вследствие чего медиатор становится доступным для расщепления МАО. Исчерпание запасов норадреналина вызывает седативный, успокаивающий, гипотензивный эффект. Гипотензивный эффект имеет αметилдофа, который под действием энзимов нервной клетки трансформируется в норадреналинподибну вещество, которое вместе с медиатором секретируется, снижает его концентрацию в синаптической щели и эффективность действия.
Вещества, увеличивающие содержание катехоламинов в синаптической щели, способствуют стимуляции адренорецепторов и вызывают возбуждающий, антидепрессантный эффект. К таким веществам относятся: ингибиторы МАО (блокируют инактивацию медиатора), кокаин (тормозит активный транспорт катехоламинов), амфетамин (способствует выделению норадреналина и одновременно блокирует его поглощения), имипримин (ингибирует вторичный транспорт норадреналина) и другие).
Уменьшение количества серотонина в организме или нарушение функции серотониновых рецепторов вызывает развитие депрессивных состояний, психических заболеваний, нарушения сна, повышение чувствительности к боли, тяги к алкоголю и наркотикам).
Адренергические и холинергические системы мозга взаимодействуют с другими и используют серотонин как медиатор.
Серотонин Катаболизирует преимущественно под действием МАО в 5оксииндолоцтовои кислоты, которая выводится с мочой. Ингибиторы энзима увеличивают количество серотонина в головном мозге.
Образуются при декарбоксилирование аминокислот ферментами декорбаксилазами. К биогенным аминам относят дофамин,норадреналин,адреналин( синтезируются изначально из аминокислоты тирозина), серотонин, мелотанин( синтезируются из триптофана) Многие амины могут выполнять роль гормонов и нейромедиаторов

Амины, образовавшиеся при декарбоксилировании аминокислот, часто являются биологически активными веществами. Они выполняют функцию нейромедиаторов (серотонин, дофамин, ГАМК и др.), гормонов (норадреналин, адреналин), регуляторных факторов местного действия (гистамин, карнозин, спермин и др.). Серотонин может превращаться в гормон мелатонин, регулирующий суточные и сезонные изменения метаболизма организма и участвующий в регуляции репродуктивной функции.
| Амино- кислоты | Серии | Триптофан | Тирозин | Глутами- новая кислота | Гистидин | Орнитин Лизин |
| Продукты декарбокси- лирования | Этаноламин | Триптамин | γ-амино- масляная кислота | Гистамин | Путресцин Кадаверин | |
| Биологичес- ки активные вещества | Ацетилхолин | Серотонин | Дофамин | ГАМК | Гистамин | Спермидин (и спермин) |
| Формулы | 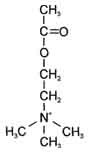 |  |  |  |  | 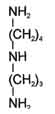 |
| Физиологи- ческая роль | Возбуждаю- щий медиаторвегетативной нервной системы | Возбуждающий медиатор средних отделов мозга | Медиатор среднего отдела мозга | Тормозной медиатор высших отделов мозга | Медиатор воспаления, аллергических реакции, пищеваритель- ный гормон | Изменяют степень агрегации полисом. Регулируют синтез РНК и белка |
В организме биогенные амины подвергаются реакции окислительного дезаминирования с образованием альдегидов и аммиака. Процесс осуществляется при участии моноаминооксидаз.
Схематически механизм трансдезаминирования можно представит так:

24)Образование серотонина и гистамина. Роль аминов
Гистамин образуется путем декарбоксилирования гистидина в тучных клетках соединительной ткани
Гистамин образует комплекс с белками и сохраняется в секреторных гранулах тучных клеток. Секретируется в кровь при повреждении ткани (удар, ожог, воздействие эндо- и экзогенных веществ), развитии иммунных и аллергических реакций. Гистамин выполняет в организме человека следующие функции:
- стимулирует секрецию желудочного сока, слюны (т.е. играет роль пищеварительного гормона);
- повышает проницаемость капилляров, вызывает отёки, снижает АД (но увеличивает внутричерепное давление, вызывает головную боль);
- сокращает гладкую мускулатуру лёгких, вызывает удушье;

Схема А
- участвует в формировании воспалительной реакции - вызывает расширение сосудов, покраснение кожи, отёчность ткани;
- вызывает аллергическую реакцию;
- выполняет роль нейромедиатора;
- является медиатором боли.
Серотонин - нейромедиатор проводящих путей. Образуется в надпочечниках и ЦНС из аминокислоты 5-гидрокситриптофана в результате действия декарбоксилазы ароматических аминокислот. Этот фермент обладает широкой специфичностью и способен также декарбоксилировать триптофан и ДОФА, образующийся из тирозина. 5-Гидрокситриптофан синтезируется из триптофана под действием фенилаланингидроксилазы с коферментом Н4БП (этот фермент обладает специфичностью к ароматическим аминокислотам и гидроксидирует также фенилаланин) (см. схему ниже).
Серотонин может превращаться в гормон мелатонин, регулирующий суточные и сезонные изменения метаболизма организма и участвующий в регуляции репродуктивной функции.
Серотонин- биологически активное вещество широкого спектра действия. Он стимулирует сокращение гладкой мускулатуры, оказывает сосудосуживающий эффект, регулирует АД, температуру тела, дыхание, обладает антидепрессантным действием. По некоторым данным он может принимать участие в аллергических реакциях, поскольку в небольших количествах синтезируется в тучных клетках.
Вопрос № 25
Образование катехоламинов и ГАМК, функции аминов.
В мозговом веществе надпочечников и нервной ткани тирозин является предшественником катехоламинов( дофамина, норадреналина, адреналина).
При образовании катехоламинов и меланина (в меланоцитах) промежуточным продуктом служит диоксифенилаланин (ДОФА). Однако гидроксилирование тирозина в клетках различных типов катализируется различными ферментами:
- Тиразиназа ( Cu-зависимый фермент)
- ДОФА – декарбоксилаза (2)
дофамин и норадреналин служат медиаторами в синаптической передаче нервных импульсов, а адреналин – гормон широкого спектра действия, регулирующий энергетический обмен. Одна из функций катехоламинов – регуляция деятельности ССС.
В нервных клетках декарбоксилирование глутамата (отщепление а-карбоксильной группы) приводит к образованию γ-Аминомасляной кислоты(ГАМК), которая служит основным тормозным медиатором высших отделов мозга. Содержание ГАМК в головном мозге в десятки раз выше других нейромедиаторов. Она увеличивает проницаемость постсинаптическизх мембран для ионов К+, что вызывает торможение нервного импульса, повышает дыхательную активность нервной ткани, улучшает кровоснабжение головного мозга.

Амины, образовавшиеся при декарбоксилировании аминокислот, часто являются биологически активными веществами. Они выполняют функцию нейромедиаторов (серотонин, дофамин, ГАМК и др.), гормонов (норадреналин, адреналин), регуляторных факторов местного действия (гистамин, карнозин, спермин и др.).
Вопрос № 26

Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).

Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ - конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.

Общие условия выбора системы дренажа: Система дренажа выбирается в зависимости от характера защищаемого.

Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Биогенные амины – это амины, образующиеся в организме в результате метаболизма. Распространение в природе. Синтез биогенных аминов. Физические и химические свойства. Основной физиологический эффект мелатонина. Триптамины, метилтриптамины, этилтриптамины.
| Рубрика | Химия |
| Вид | контрольная работа |
| Язык | русский |
| Дата добавления | 11.10.2011 |
биогенный амин метаболизм
Важной группой азотсодержащих природных продуктов являются амины.
Замещение в аммиаке атомов водорода углеводородными остатками приводит к соединения, называемым аминами. Многие из них оказывают заметное биолого-фармакологическое действие и называются биогенными аминами. Биогенные амины - это амины, образующиеся в организме в результате метаболизма.
Алифатические амины были открыты А. Вюрцем в 1849 году в результате случайного воспаления их паров, выделившихся при взаимодействии калиевых солей с серной и циановой кислот.
Группа, характеризующая данный класс называется аминогруппой. Число аминогрупп в молекуле определяет принадлежность соединения к моно-, ди- и полиаминам. Моноамины содержат одну аминогруппу.
Катехоламины -- физиологически активные вещества, выполняющие роль химических посредников (медиаторов и нейрогормонов) в межклеточных взаимодействиях у животных; производные пирокатехина.
Катехоламины эпинефрин, норэпинефрин и дофамин синтезируются мозговом веществе надпочечников, в симпатической нервной системе и в мозге. Так как при различных заболеваниях катехоламины и их метаболиты метанефрин и норметанефрин секретируются в повышенных количествах, их можно использовать в диагностических целях.
К катехоламинам относятся другие нейромедиаторы, такие как мелатонин, адреналин, норадреналин, гистамин, серотонин.
Распространение в природе
Растения, содержащие диметилтриптамин:
Mimosa eregrin, Diplopterys cabrerana (чалипонка), Psychotria viridis (Чакруна), Virola, Anadenanthera eregrine (Йопо).
Адреналин содержится в разных органах и тканях, в значительных количествах образуется в хромаффинной ткани, особенно в мозговом веществе надпочечников.
Холин широко распространён в живых организмах. Особенно высоко содержание его в яичном желтке, мозге, печени, почках и мышце сердца.
Мускарин содержится в мухоморах, содержание не превышает 0,02 %. Мускарин также получают синтетическим путём.
Синтез биогенных аминов
I. Процесс декарбоксилирования ? - аминокислот ведет к образованию биогенных аминов
В организме этот процесс происходит с участием ферментов декарбоксилаз и кофермента пиридоксальфосфата.
II. Из всех нейронов ЦНС только около 7 тысяч вырабатывают дофамин. Известно несколько дофаминовых ядер, расположенных в стволе мозга.
III. В лабораторных условиях эта реакция протекает при нагревании ? - аминокислот в присутствии поглотителей диоксида углерода, например гидроксида бария Ba(OH)2.
IV. Серотонин образуется из аминокислоты триптофана путём её последовательного 5-гидроксилирования ферментом 5-триптофан-гидроксилазой (в результате чего получается 5-гидрокситриптофан, 5-ГТ) и затем декарбоксилирования получившегося 5-гидрокситриптофана ферментом триптофан-декарбоксилазой.
Физические свойства
Метил- и этилаламины являются газообразными веществами, а остальные низшие амины - жидкостями с резким запахом. С увеличением молекулярной массы растворимость в воде понижается.
Рассмотрим физические свойства биогенных аминов на примере:
Холин - бесцветные кристаллы, хорошо растворимые в воде, этиловом спирте, нерастворимые в эфире, бензоле. Холин легко образует соли с сильными кислотами, его водные растворы обладают свойствами сильных щелочей.
Мускарин - при комнатной температуре представляет собой бесцветные кристаллы, хорошо растворимые в воде. Температура плавления 179--180 °С.
Химические свойства
I. Холин легко образует соли с сильными кислотами, его водные растворы обладают свойствами сильных щелочей.
II. Ацетилирование холина с помощью ацетилкофермента А
В результате окисления свободного холина образуется диполярный ион бетаин, который служит источником метильных групп в реакциях трансметилирования:
III. Накопление биогенных аминов может отрицательно сказываться на физиологическом статусе и вызывать ряд существенных нарушений функций в организме. Однако органы и ткани, как и целостный организм, располагают специальными механизмами обезвреживания биогенных аминов, которые в общем виде сводятся к окислительному дезаминированию этих аминов с образованием соответствующих альдегидов и освобождением аммиака:
Ферменты, катализирующие эти реакции, получили название моноамин- и диаминоксидаз. Более подробно изучен механизм окислительного дез-аминирования моноаминов. Этот ферментативный процесс является необратимым и протекает в две стадии:
+ Е-ФАД + 0-> R-CHO + + Е-ФАД- (1)
Первая (1), анаэробная, стадия характеризуется образованием альдегида, аммиака и восстановленного фермента, вторая (2), в аэробной фазе окисляется молекулярным кислородом. Образовавшаяся перекись водорода далее распадается на воду и кислород.
IV. Подобно пирокатехину, катехоламины с раствором хлорида железа (III)
Дают изумрудно - зеленое окрашивание., переходящее в вишнево - красное при добавлении раствора аммиака, что может служит качественной реакцией на эти соединения.
Физиологическая роль
I. Дофамин обладает рядом физиологических свойств, характерных для адренергических веществ.
Дофамин вызывает повышение сопротивления периферических сосудов (менее сильное, чем под влиянием норадреналина). Он повышает систолическое артериальное давление в результате стимуляции ?-адренорецепторов. Также дофамин увеличивает силу сердечных сокращений в результате стимуляции ?-адренорецепторов. Увеличивается сердечный выброс. Частота сердечных сокращений увеличивается, но не так сильно, как под влиянием адреналина.
Потребность миокарда в кислороде под влиянием дофамина повышается, однако в результате увеличения коронарного кровотока обеспечивается повышенная доставка кислорода.
В результате специфического связывания с дофаминовыми рецепторами почек дофамин уменьшает сопротивление почечных сосудов, увеличивает в них кровоток и почечную фильтрацию. Наряду с этим повышается натрийурез. Происходит также расширение мезентериальных сосудов. Этим действием на почечные и мезентериальные сосуды дофамин отличается от других катехоламинов (норадреналина, адреналина и др.). Однако в больших концентрациях дофамин может вызывать сужение почечных сосудов.
Дофамин ингибирует также синтез альдостерона в коре надпочечников, понижает секрецию ренина почками, повышает секрецию простагландинов тканью почек.
II. Основной физиологический эффект мелатонина заключается в торможении секреции гонадотропинов. Кроме того, снижается, но в меньшей степени, секреция других тропных гормонов передней доли гипофиза -- кортикотропина, тиротропина, соматотропина.
Секреция мелатонина подчинена суточному ритму, определяющему, в свою очередь, ритмичность гонадотропных эффектов и половой функции. Синтез и секреция мелатонина зависят от освещённости -- избыток света тормозит его образование, а снижение освещённости повышает синтез и секрецию гормона.
III. Серотонин -- это вещество, являющееся химическим передатчиком импульсов между нервными клетками человеческого мозга и контролирующее аппетит, сон, настроение и эмоции человека.
IV. Катехоламины -- физиологически активные вещества, выполняющие роль химических посредников (медиаторов и нейрогормонов) в межклеточных взаимодействиях у животных.
V. Адреналин оказывает стимулирующее воздействие на ЦНС. Он повышает уровень бодрствования, психическую энергию и активность, вызывает психическую мобилизацию, реакцию ориентировки и ощущение тревоги, беспокойства или напряжения, гегенируется при пограничных ситуациях.
Некоторые представители биогенных аминов
Молярная масса 160.216 г/моль
Триптамин -- моноаминый алкалоид, производное индола. Триптамин обнаруживается в растениях и организмах животных. Химически схож с аминокислотой триптофаном. Предполагается, что триптамин сам играет роль нейромедиатора и нейротрансмитера в головном мозге млекопитающихся, а большинство производных от триптамина веществ обнаруживают психоактивные свойства. Одним из известных производных триптамина является серотонин, важнейший нейромедиатор и гормон.
Молярная масса 174.24 г/моль
?-метил-триптамин - синтетическое вещество семейства триптаминов. В 1960-е годы в Советском Союзе выпускался в качестве антидепрессанта под названием Индопан, в таблетках по 5-10 мг. Подобно другим триптаминам, в увеличенных дозах производит психоделический и галлюциногенный эффект, наступающий в течении 2-3 часов после приема и длящийся 18-24 часа. Также действует как ингибитор моноаминой оксидазы и как стимулянт.
?-этилтриптамин - это психоактивное вещество из группы триптаминов. Использовался в качестве антидепрессанта, но был вскоре запрещен из-за очевидного негативного эффекта - у слишком большого процента пациентов случалась алейкия (отсутствие или уменьшение количества гранулоцитов в крови).
Диизопропилтриптамин
Диизопропилтриптамин - психоделический галлюциногенный наркотик из семейства триптаминов. По своему действию уникален тем, что вызывает слуховые галлюцинации, что отличает его от большинства других галлюциногенов, дающих в основном галлюцинации визуального плана.
Может вызывать расстройство слуха - тиннитус (звон в ушах), который может продолжаться нескольких дней или даже, что случается очень редко, не прекращаться никогда.
Холин (от греч. choly -- жёлчь) -- гидроокись 2-оксиэтилтриметиламмония
Холин обычно относят к витаминам группы В, хотя животные и микроорганизмы способны его синтезировать. Холин входит в состав фосфолипидов (например, лецитина, сфингомиелина), служит источником метильных групп в синтезе метионина. Из холина в организме животных синтезируется ацетилхолин -- один из важнейших химических передатчиков нервных импульсов. Холин является т.н. липотропным веществом -- предотвращает тяжёлые заболевания печени, возникающие при её жировом перерождении.
Холин - в медицине для лечения заболеваний печени применяют хлорид холина. Его вводят также в состав комбикормов сельско-хозяйственным животных. Для аналитических целей используют способность холина давать плохо растворимые соли с фосфорновольфрамовой, платинохлористоводородной и некоторыми др. гетерополикислотами.
Мускарин не нашёл применения в медицинской практике. Он используется только в экспериментальных исследованиях при изучении строения и функции холинорецепторов и холинергических процессов.
На этом применение биогенных аминов не заканчиваются. Есть множество областей медицины, где они продолжают помогать, благодаря своим свойствам.
В заключении хотелось бы сделать вывод всего выщесказанного: амины биогенные, протеиногенные, группа азотсодержащих органических соединений, образующихся в организмах человека, животных, растений и бактерий путём декарбоксилирования аминокислот, т. е. отщепления от них карбоксильной группы - COOH. Многие из биогенных аминов - гистамин, серотонин, норадреналин, адреналин, тирамин - биологически активные вещества, оказывающие воздействие на процессы торможения и возбуждения в коре головного мозга и подкорковых центрах, вызывающие сдвиги кровяного давления расширением или сужением сосудов и др. изменения в организме.
Таким образом, трудно представить наш организм без биогенных аминов, ведь они участники многих жизненно - важных процессов в нашем организме. И я надеюсь, что в будущем на основе этих соединений будут найдены ответы на основные проблемы медицины, искусственной пищи и других вопросов.
1. Балаклеевский А.И., Кораблев М.В. Нейрогормоны-биогенные амины, 1978.
2. Н.А.Тюкавкина,Ю.И.Бауков. Биоорганическая химия. М.: Дрофа, 2004.
Понятие гликозидов, их классификация и разновидности, значение и характер воздействия на организм, распространенность и основные функции. Биогенные амины и алкалоиды как антиалиментарные факторы. Характеристика основных алкалоидов - морфина и кофеина.
контрольная работа [20,8 K], добавлен 19.09.2009
Применение дифениламина. Амины. Ацилирование и алкилирование аминов. Образование производных мочевины. Алкилирование первичных и вторичных аминов. Расщепление и окисление аминов. Синтез на основе анилина и анилиновой соли. Синтез из хлорбензола и анилина.
курсовая работа [471,2 K], добавлен 17.01.2009
Сущность, понятие и характеристика аминов. Их основные свойства и реакции. Характеристика реакций получения аминов, их восстановления и окисления. Методы получения аминов. Аммонолиз гелоленуглеводородов, описание их основных свойств и реакций соединений.
лекция [157,0 K], добавлен 03.02.2009
Методы получения ароматических аминов: первичные, вторичные, третичные. Физические и химические свойства ароматических аминов. Галогенирование анилина свободными галогенами. Гидрирование анилина в присутствии никеля. Отдельные представители аминов.
реферат [278,6 K], добавлен 05.10.2011
Амины как производные аммиака, в молекуле которого один, два или три атома водорода замещены органическими радикалами, их классификация и типы. Принципы и методы получения данных соединений, направления практического применения. Строение аминов.
контрольная работа [416,9 K], добавлен 05.08.2013
Изучение строения и свойств аминов как органических соединений, являющихся производными аммиака. Номенклатура аминов и замена атомов водорода углеводородными радикалами. Синтез, анализ, химические реакции аминов и их взаимодействие с азотистой кислотой.
презентация [1,2 M], добавлен 02.08.2015
Номенклатура аминов, их физические и химические свойства. Промышленные и лабораторные способы получения аминов. Классификация аминокислот и белковых веществ. Строение белковых молекул. Катализ биохимических реакций с участием ферментов (энзимов).
реферат [54,1 K], добавлен 01.05.2011
Понятие аминов, их сущность и особенности, общая формула и основные химические свойства. Классификация аминов на ароматические и алифатические, их отличительные черты. Особенности алифатических аминов, способы их получения и характерные реакции.
реферат [147,0 K], добавлен 21.02.2009
По рациональной номенклатуре амины - это алкил или ариламины. Алкилирование алкилгалогенидами и окисление третичных аминов. Ацилирование и действие сульфонилхлоридов, замещение ароматических аминов в кольцо. Взаимодействие аминов с азотистой кислотой.
реферат [109,5 K], добавлен 03.02.2009
Методы синтеза и химические свойства аминов. Изомерия в ряду алифатических аминов и восстановление нитросоединений. Получение первичных, вторичных ароматических аминов. Получение третичных аминов. Реагенты и оборудование и синтез бензальанилина.
курсовая работа [627,8 K], добавлен 02.11.2008
Эти важные продукты метаболизма аминокислот участвуют в процессах проведения импульсов от одной нервной клетки к другой. После раздражения первой нервной клетки она освобождает химический агент в заполненную жидкостью щель между нею и соседней нервной клеткой. Повышение ионной проницаемости мембраны второй клетки под влиянием этого агента в указанной щели, или синапсе, приводит к быстрой диффузии ионов натрия во вторую клетку. Результатом является деполяризация клеточной мембраны, инициирующая волну электрических разрядов вдоль второго нерва.
Те химические агенты, которые образуются при таком раздражении и обеспечивают передачу нервного импульса через синапс, обычно называют нейромедиаторами. Как было отмечено выше, к числу таких участвующих в проведении нервных импульсов соединений относятся тормозные агенты — ГАМК и глицин. Установлено, что существуют четыре типа возбуждающих нейромедиаторов, распространение которых в нервной системе различно.
К числу таких нейромедиаторов относятся ацетилхолин (в холинэргических окончаниях), норадреналин (в адренэргических окончаниях), серотонин (в серотонинэргических окончаниях) и гистамин (который, как считают, участвует в функционировании ряда сенсорных нервных механизмов).
Рассматривая участие ацетилхолина в процессах нервного возбуждения, различают четыре фазы в судьбе этого важного соединения: биосинтез, депонирование, выделение и распад. Химически ацетилхолин представляет собой простой эфир, образованный ацетатом и аминоспиртом холином. Последний образуется из аминокислоты серина путем декарбоксилирования до этаноламина с последующим присоединением трех метальных групп, источником которых служит S-аденозилметионин. Как было отмечено выше, этим превращениям подвергаются азотистые соединения, образующие комплексы с фосфолипидами. Холин, кроме того, представляет собой важный компонент структуры мембран нервных клеток.
Биосинтез ацетилхолина, катализируемый специфическим ферментом холинацетилтрансферазой, происходит только в нервных волокнах, в частности в тех участках, где их окончания соприкасаются с поверхностями других нервных или мышечных клеток. В таких нервных окончаниях холин, который был доставлен либо с током крови, либо синтезирован в самих нервах, реагирует с ацетил-КоА, образующимся преимущественно при окислении углеводов в нервной системе. Синтезированный таким образом ацетилхолин быстро инкапсулируется, переходя в стойкую резервную форму и хранится в мельчайших образованных мембраной пузырьках.
При раздражении нерва эти пузырьки сливаются с поверхностной мембраной клетки и выделяют свое содержимое, которое представляет собой конгломерат молекул ацетилхолина, в синаптическую щель. Затем нейромедиатор, мигрируя через щель, достигает мембраны соседней нервной клетки и повышает ее проницаемость для натрия. После того как работа завершена, т. е. после индукции изменений электрического потенциала во второй нервной клетке, избыток ацетилхолина должен быть разрушен и удален, т. е. его эффект должен быть кратковременным. Этот процесс осуществляется на поверхности мембраны при участии специфического гидролитического фермента ацетилхолинэстеразы, который расщепляет ацетилхолин вновь до ацетата и холина. Распределение ацетилхолина в нервной системе соответствует распределению ферментов ацетилхолинтрансферазы и эстеразы, достигая наивысших концентраций на месте контакта моторных нервных окончаний со скелетной мышцей, а также в области окончаний парасимпатических нервов, например блуждающего.
Специфические ингибиторы ацетилхолинэстеразы позволяют ацетилхолину накапливаться, поскольку иных путей удаления этого нейромедиатора, кроме медленной диффузии, не существует. Агенты, оказывающие такие воздействия, называют антихолинэстеразами; к их числу относятся вещества, используемые в качестве лекарственных средств для контролируемого локального потенцирования действия ацетилхолина, а также яды. К категории последних относят инсектициды и нервные газы, воздействие которых сопровождается накоплением в нервной системе больших количеств ацетилхолина, что приводит к гибели пораженного организма при развитии судорог и остановке дыхания.
Читайте также:


