Глубокая стимуляция мозга при треморе

Лучшая аналогия DBS – это установка кардиостимулятора. Только кардиостимулятор замещает функцию несостоятельной проводящей системы сердца, а электростимулятор в технологии DBS – функцию стриопаллидарной системы (группы подкорковых ядер в глубине серого вещества полушарий мозга).
Стриопаллидарная система является частью мозга, обеспечивающей нормальную двигательную активность человека. И если в ней развиваются дегенеративные изменения, возникают тяжелые расстройства движений, приводящие в результате к социальной дезадаптации и глубокой инвалидизации. Глубинная стимуляция мозга позволяет эффективно подавлять симптомы расстройств этой системы – тремор, неподатливость мышц и бедность движений.
Метод DBS показан при:
- болезни Паркинсона в качестве дополнения к медикаментозному лечению;
- эссенциальном треморе для устранения дрожи в руках;
- различных формах первичной дистонии, устойчивой к медикаментозной терапии, начиная с 7-летнего возраста.
Пациентам, страдающим паркинсонизмом, метод DBS рекомендуют:
- при стаже болезни более 5 лет;
- если не удается с помощью медикаментов удовлетворительно корректировать двигательные расстройства;
- при резком снижении качества жизни из-за частых и выраженных колебаний (флюктуаций) симптомов гипокинезии (ограничения подвижности), разнообразных расстройств движения (дискинезий) и тремора;
- если при тестировании выявляется высокая эффективность леводопы с уменьшением выраженности всех расстройств более чем наполовину;
- когда на высоте действия подобранной пациенту медикаментозной схемы его двигательная активность остается неудовлетворительной;
- если отсутствуют противопоказания к хирургическим методам лечения;
- когда пациент имеет сохранную психику, у него нет деменции и тяжелой депрессии со склонностью к суициду, так как он должен понимать суть операции, стремиться к положительному результату и находиться в контакте с хирургом во время вмешательства (часть операции проводится под местной анестезией, и пациент находится в сознании).
Отбор пациентов на DBS производится неврологом с дальнейшим участием нейрохирурга, который определяет возможность выполнения операции рекомендованным пациентам. Для этого проводятся многочисленные медикаментозные тесты и нейрофизиологические исследования, позволяющие прогнозировать ожидаемые эффекты и риски вмешательства.
Когда вопрос об операции принципиально решен, приступают к ее подготовке. Эта подготовка направлена на максимальную, вплоть до 1 мм, точность имплантации электродов. Для этого выполняют магнитно-резонансные томограммы, а сама операция проводится с использованием современных стереотаксических аппаратов. Это позволяет найти нужную мишень на мониторе компьютера и сопоставить ее положение со структурами в мозге пациента.
Имплантируемая система для DBS состоит из:
- внедряемых в мозг электродов;
- генератора электрических импульсов, помещаемого под кожей передней поверхности тела;
- проводов, соединяющих электроды с нейростимулятором и также располагающихся подкожно.
Электроды в мозг погружают под местной анестезией. Она необходима только для получения доступа к нему во время манипуляций с мягкими покровами и костями черепа. Ткань мозга безболезненна, поэтому для введения электродов анестезии не требуется. В глубинных структурах мозга их устанавливают под контролем трехмерной компьютерной нейронавигации и дополнительного мониторинга неврологических функций посредством речевого контакта с пациентом. Он выполняет инструкции нейрохирурга, отвечает на вопросы, рассказывает о своих ощущениях.
Второй этап операции (установку нейростимулятора) в некоторых клиниках проводят одномоментно, под общим наркозом. В других центрах предпочитают на несколько недель расположить его снаружи, а имплантировать уже после окончательной регулировки и подбора оптимального режима.
Когда все манипуляции окончены, пациент получает магнитный пульт, с помощью которого может дистанционно регулировать устройство в соответствии со своими потребностями. Без замены источников питания оно работает 6-10 лет.
Электроды для DBS могут быть установлены:
- в таламусе, если патология проявляется только тремором;
- во внутренней части бледного шара – для уменьшения тремора, дискинезий, замедленности движений и ригидности, улучшения координации и устойчивости при ходьбе;
- в субталамических ядрах – дополнительно к эффектам стимуляции бледного шара обеспечивается возможность снижения доз противопаркинсонных препаратов, а значит, снижается риск связанных с их приемом дискинезий.
Преимущества глубинной стимуляции мозга в сравнении с операциями по деструкции нервных образований при паркинсонизме несомненны. Это:
- полная обратимость. При необходимости стимулирующие электроды и генератор электрических импульсов могут быть извлечены из организма без каких-либо негативных последствий;
- возможность регулировать режим импульсов в соответствии с потребностями конкретного пациента;
- возможность двусторонней установки электродов, в отличие от операций деструкции таламуса и бледного шара;
- отсутствие значимых побочных эффектов и их непостоянство;
- возможность сочетать электростимуляцию с медикаментозной терапией, свободно регулируя параметры обоих методов лечения.
Благодаря глубинной стимуляции мозга:
- почти на 7 часов в день увеличивается период нормальной физической активности;
- появляется возможность снизить дозы и количество противопаркинсонных препаратов;
- приобретается механизм эффективного контроля двигательных расстройств;
- качество жизни пациентов улучшается настолько, что работоспособные люди могут вернуться к своей профессии, а пенсионеры – ни от кого не зависеть в быту.
Метод глубинной стимуляции мозга – сложное нейрохирургическое вмешательство, эффективность и безопасность которого зависят от правильного определения показаний, высокой квалификации бригады специалистов и технического оснащения операционной. Крупные нейрохирургические центры мира имеют в выполнении DBS огромный опыт – более 60 тысяч пациентов, вернувшихся благодаря успешной операции к активной жизни.
Похожие темы научных работ по клинической медицине , автор научной работы — Волкман Й.
УДК 616.8-009.3-085.786 Й. Волкман
СТИМУЛЯЦИЯ ГЛУБИННЫХ СТРУКТУР ГОЛОВНОГО МОЗГА ПРИ ЭССЕНЦИАЛЬНОМ ТРЕМОРЕ
Университет К. Альбрехта (г. Киль, Германия)
Ключевые слова: эссенциальный тремор, лечение.
Классическая клиническая картина эссенциального тремора (ЭТ) представлена единственным симптомом — тремором (постуральным и тремором действия), который медленно прогрессирует с течением времени. ЭТ — наиболее частое расстройство экс-трапирамидной системы, его распространенность составляет от 1 до 5%. У 60% пациентов тремор выявляется у одного или более родственников первой или второй степени родства. Отягощенный семейный анамнез, а также высокая конкордантность у однояйцевых близнецов свидетельствуют об ауто-сомно-доминантном типе наследования ЭТ. Тем не менее ген или, скорее всего, несколько отдельных генов, отвечающих за это расстройство, до сих пор не идентифицированы. Еще одна важная особенность ЭТ — уменьшение его выраженности после приема алкоголя. Положительное влияние алкоголя отмечается у 2/3 пациентов [1].
Естественное течение ЭТ
Несмотря на то, что более распространенной формой является постуральный тремор, в половине наблюдений присутствует интенционный тремор и другие неявные признаки мозговой дисфункции, например легкая атаксия при тандемной ходьбе. У большей части кандидатов на лечение методами функциональной нейрохирургии ЭТ характеризуется выраженным ин-тенционным компонентом.
Медикаментозное лечение ЭТ
При лечении ЭТ препаратами первого ряда являются пропранолол и примидон. Примерно на 2/3 пациентов один из препаратов оказывает лечебное действие. Однако результаты длительной медикаментозной терапии не такие благоприятные. Примерно половина больных из-за нестабильного эффекта прекращает прием пропранолола в течение первого года. Только в 25% случаев хороший лечебный эффект препаратов сохраняется в течение двух лет и более. Главный недостаток примидона заключается в его плохой переносимости. Более того, его седативный эффект может ограничить прием даже при медленном наращивании дозы.
Препараты второго ряда менее эффективны для лечения ЭТ. К ним относятся габапентин, топирамат и клоназепам (при ЭТ с интенционным тремором). В нескольких небольших исследованиях была показана хорошая эффективность клозапима. По-видимому, клиническое улучшение в ответ на небольшую дозу этого препарата (12,5—25 мг) является показателем хорошей эффективности при длительном лечении. Основные побочные эффекты клозапина — седативное действие и лейкопения, которая в некоторых случаях может привести к тяжелым последствиям вплоть до летального исхода. Местные инъекции ботулоток-сина рекомендуют применять при ЭТ головы. Однако результаты лечения тремора рук таким методом менее благоприятны: инъекции приводят к возникновению инвалидизирующего пареза. Даже несмотря на оптимальную медикаментозную терапию (табл. 1),
Алгоритм лечения эссенциального тремора
Алгоритм Препарат Дозировка Замечания
Первая линия Пропранолол 30—320 мг, 2—3 приема (стандартные или ретардные формы) Противопоказания: брадиаритмии, астма, гипотония, обструктивные заболевания легких, диабет и т.д.
Примидон 62,5—500 мг, 1 раз на ночь Предпочтительно у пациентов старше 60 лет
Комбинация: пропра-нолол и примидон Максимальная доза каждого препарата Попробовать перед переходом к лекарствам второй линии
Габапентин 1 800—2 400 мг в день
Вторая линия Клоназепам 0,75—6 мг Нет
Топирамат 50—300 мг
Третья линия Клозапин Тест — 12,5 мг, 30—50 мг в день Риск агранулоцитоза, обязательный регулярный контроль белого кровяного ростка
Четвертая линия Стереотаксическая хирургия
Критерии отбора на DBS при ЭТ
Включения Значительное нарушение жизненной активности, связанное с ЭТ: • нарушение ежедневной активности; • ограничение профессиональной деятельности; • социальная неполноценность.
Медикаментозная терапия неэффективна или вызывает непереносимые побочные эффекты
Исключения Плохое общее состояние
Выраженные сопутствующие психические заболевания: •тяжелая депрессия; • психоз; • алкогольная или наркотическая зависимость; • тяжелые личностные расстройства, приводящие к неадекватности пациента
Значительные нейрохирургические факторы риска: • атрофия мозга; • иммуносупрессия; • лечение антикоагулянтами
тремор может сохраняться и ограничивать ежедневную активность пациента. В таком случае следует рассмотреть возможность хирургического лечения.
Хирургическое лечение ЭТ
На протяжении прошедших 40—50 лет стереотакси-ческая таламотомия оставалась единственным методом нейрохирургического лечения тяжелого ЭТ. Ее эффективность, а также побочные эффекты отмечены во многих научных работах [1, 3]. Данный метод подразумевает ограниченную деструкцию вентрола-теральной части таламуса и (или) субталамического белого вещества. Воздействие деструктивного метода, включая нежелательные побочные эффекты, необратимо.
Высокочастотная стимуляция глубинных структур головного мозга (Deep Brain Stimulation — DBS) путем имплантации постоянных электродов в вентральное промежуточное ядро таламуса была предложена в качестве альтернативного метода лечения в 1987 г. В последние годы благодаря своим очевидным достоинствам DBS постепенно вытеснила деструктивные стереотаксические операции. К преимуществам DBS относится:
• возможность коррекции лечебного эффекта в соответствии с ходом заболевания:
• отсутствие серьезных побочных эффектов и их преходящий характер.
С помощью DBS удается достигнуть значительного уменьшения выраженности постурального тремора (на два пункта по шкале оценки тремора) почти у 90% лиц с ЭТ. Эффективность метода в отношении тремора движения менее выражена. При лечении методом DBS полное или почти полное исчезновение контрлатерального тремора (0 или 1 балл) отмечается почти у 70% пациентов. По данным европейского многоцентрового исследования,
эффективность терапии сохраняется в течение 6 и более лет [3, 4].
Недавно было завершено проспективное рандомизированное клиническое исследование, в котором оценивались безопасность и эффективность таламотомии и DBS [2]. По данным этой работы, эффективность обоих методов в отношении симптомов болезни примерно одинаковая, однако при DBS частота необратимых побочных эффектов значительно ниже, а функциональный эффект существенно лучше. В большинстве исследований DBS частота стойких осложнений, включая внутримозговые кровоизлияния и инфекционные осложнения, составила менее 1%. Проведение билатеральных деструктивных операций часто приводит к формированию дизартрии. При двухсторонней имплантации электродов для DBS дизартрия встречается значительно реже. Это преимущество имеет огромное значение для пациентов с двухсторонним выраженным тремором. Кроме того, билатеральная имплантация показана при треморе головы, а также при вовлечении в процесс аксиальной мускулатуры.
По нашим данным, примерно 10% пациентов с ЭТ, несмотря на оптимальную медикаментозную терапию, ограничены в повседневной активности [1]. У этих людей тремор оказывает выраженное влияние на ежедневную активность (прием пищи и письмо) или является причиной неприемлемых социальных стигм (например, в случае выраженного тремора головы или голоса). Таких больных следует проинформировать о возможности хирургического лечения методом DBS. Если явных противопоказаний к оперативному вмешательству нет, а пациент согласен на хирургическое лечение, следует направить его на консультацию к нейрохирургу. Специалисты, занимающиеся хирургическим лечением двигательных расстройств, оценят соотношение риска оперативного вмешательства и потенциального лечебного эффекта DBS в каждом конкретном случае (табл. 2).
Наиболее важный фактор отбора кандидатов для хирургического лечения эссенциального тремора — то, как они видят свою болезнь. Ограничения жизнедеятельности, обусловленные двигательным дефектом, в большой степени зависят от индивидуальных особенностей человека, таких как профессия, социальное положение и приспосабливаемость к заболеванию. Некоторые пациенты при сильном функциональном ограничении организуют жизнь вокруг своего болезненного состояния и не нуждаются в инвазивном лечении. Другие больные при относительно небольшом двигательном дефекте, наоборот, активно стремятся к хирургическому лечению, так как боятся потерять работоспособность или оказаться неспособными исполнять свои социальные функции. Врач должен выяснить ожидания пациента от лечения и оценить возможность их реализации. Затем потенциальная польза вмешательства должна быть соотнесена с индивидуальным риском осложнений.
УДК 616.342-002.44-005.1-072.1-089 С.В. Юдин1, С.П. Тихомиров1, О.В. Кизим2
ЭНДОСКОПИЧЕСКАЯ ДИАГНОСТИКА И ЛЕЧЕНИЕ ОСТРЫХ ДУОДЕНАЛЬНЫХ КРОВОТЕЧЕНИЙ
1 Городская клиническая больница № 2 (г. Владивосток),
2 Владивостокский государственный медицинский университет
Ключевые слова: язва 12-перстной кишки, кровотечение, эндоскопия.
На протяжении последних лет отмечается стабильная тенденция как к росту заболеваемости язвенной болезнью 12-перстной кишки, так и к увеличению удельного веса осложненных кровотечением луковичных язв. При этом консервативная терапия требует длительных усилий, а осложнения отмечаются у 10—30% пациентов [1, 2, 6]. Число больных, подвергшихся открытым операциям по поводу кровоточащих язв луковицы 12-перстной кишки между и вмешательствам с использованием ургентной эндоскопии, существенно различается в различных клиниках [3—5]. Иллюстрацией значения кровоточащих луковичных язв в клинической практике может служить общая структура желудочно-кишечных кровотечений у пациентов, доставляемых каретой скорой помощи в приемное отделение ГКБ № 2 Владивостока. Так, наиболее частой причиной кровотечения здесь в 2005—2007 гг. явилась язвенная болезнь 12-перстной кишки (табл. 1).
Целью настоящего исследования явилась сравнительная оценка эффективности операций эндоскопического гемостаза в комплексном лечении кровото-
1. Deuschl G., Volkmann J. // Parkinson’s Disease and movement disoders / Jankovic J. and Tolosa E., ed. -Baltimore :Lippincott W&W, 2002. - P. 270—290.
2. Limousin P., Speelman J.D., Gielen F., Janssens M. // J. Neurol. Neurosurg. Psychiatry. - 1999. - Vol. 66. - P. 289—296.
3. Rehncrona S., Johnels B., Widner H. et al. // Mov. Disord. - 2003. - Vol. 18. - P. 163-170.
4. Schuurman P.R., Bosch D.A., Bossuyt P.M. et al. // N. Engl. J. Med. - 2000. - Vol. 342. - P. 461-468.
Поступила в редакцию 5.03.2008. THE STIMULATION OF THE DEEP BRAIN STRUCTURES AT ESSENTIAL TREMOR J. Volkmann
Kristian Albreht University (Kiel, Germany)
Summary — Indications and contra-indications to medical and surgical treatment of the essential tremor are considered. Among surgical methods the basic attention is given to the stereotaxic thalamotomia and Deep Brain Stimulation. The advantages of last method are shown, as well as the criteria of selection of patients for Deep Brain Stimulation.
Pacific Medical Journal, 2008, No. 1, p. 64-66.
чащих дуоденальных язв. Причиной тому послужили высокая частота неинформативных эндоскопий при кровотечениях из верхних отделов желудочно-кишечного тракта, а также необходимость своевременного прогноза возможного рецидива кровотечения. В наших исследованиях у 107 больных с кровоточащими дуоденальными язвами (в т.ч. 4 больных с профузным кровотечением) независимо от степени кровопотери или активности кровотечения использовался эндоскопический метод диагностики.
Стойкая гипотония как проявление геморрагического шока не являлась препятствием к выполнению фиброгастродуоденоскопии, но требовала предварительной катетеризации центральной вены. Эндоскопию выполняли на фоне инфузионной терапии в отделении реанимации, в палате интенсивной терапии или кабинете гастроскопии. Исследование проводили в положении пациента на левом боку, преимущественно под местным обезболиванием. Частота визуальной диагностики язв луковицы 12-перстной кишки
Общая структура желудочно-кишечных кровотечений, диагностированных в ГКБ № 2
Хроническая глубокая стимуляция мозга (ХГСМ) стала методом выбора в хирургии двигательных расстройств, заняв место таких процедур, как таламотомия и паллидотомия, которые широко используются для лечения пациентов с болезнью Паркинсона (БП), тремором или дистонией. По сравнению с абляционной хирургией, ХГСМ предлагает неповреждающую модуляцию базальных ганглиев; ее последствия являются принципиально обратимыми кроме того, ее можно адаптировать в зависимости от течения заболевания и индивидуальных потребностей пациента.
Основное преимущество, однако, в том, что двусторонняя операция может быть выполнена в один оперативный прием без повышенного риска побочных эффектов. Возрождается интерес к хирургическому лечению БП, а также интерес к функциональной стереотаксической хирургии для других двигательных расстройств, таких как дистония. В крупных рандомизированных исследованиях ХГСМ было показано, что она обеспечивает существенную выгоду при БП и треморе, а также при дистонии.
Механизмы хронической глубокой стимуляции мозга (ХГСМ) являются предметом интенсивных исследований, и они все еще полностью не изучены. Судя по данным анализа записей микроэлектродов и локальных потенциалов от базальных ганглиев. Хроническая глубокая стимуляция мозга (ХГСМ), вероятно, инактивирует патологические импульсы от базальных ганглиев.
В будущем хроническая глубокая стимуляция мозга (ХГСМ) может быть использована в сочетании с другими новыми методами лечения, технологиями, и перспективными направлениями, такими как вирусные векторы, генная терапия, терапия стволовыми клетками и введение нейротрофических факторов.
В настоящее время хроническая глубокая стимуляция мозга (ХГСМ) утвердилась в качестве мощной нейрохирургической процедуры для лечения различных двигательных расстройств. Помимо основных показаний для ХГСМ, улучшение было также доказано для таких редких заболеваний как гемихорея/гемибаллизм, синдрома Мейгса и нейродегенерации, связанной с пантотенаткиназой (PKAN). Этот раздел дает краткий обзор принципов хирургии ХГСМ и основных показаний и клинических результатов ХГСМ для двигательных расстройств.
а) Принципы хирургии хронической глубокой стимуляции мозга (ХГСМ) двигательных расстройств:
1. Анатомия и цели. Общие цели при БП, треморе и дистонии показаны на рисунке и таблице ниже.
Другие цели — педункулопонтинные ядра и интраламинарные ядра таламуса. Самой выгодной мишенью для лечения тремора является вентроинтермедиальное ядро таламуса или задние вентролатеральные ядра. Дорсолатеральная часть субталамического ядра и заднебоковые сегменты бледного шара являются общими анатомическими целями ХГСМ при лечении болезни Паркинсона (БП). Заднебоковые сегменты бледного шара были установлены также в качестве целевого выбора при тяжелой дистонии. Для лечения вторичной дистонии при ХГСМ было предложено воздействие на таламус.

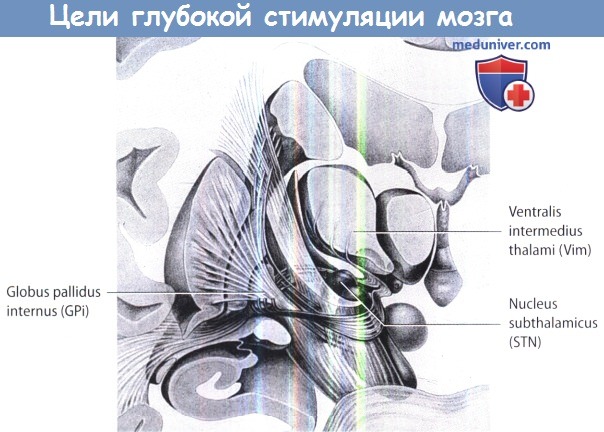
Общие анатомические цели для глубокой стимуляции мозга. 
Анатомические цели для глубокой стимуляции мозга при лечении двигательных расстройств.
2. Оборудование. Система ХГСМ состоит из трех основных компонентов:
1. Имплантируемый генератор импульсов (ИГИ).
2. Удлинительный кабель подключения электродов и ХГСМ ИГИ.
3. Четырехполюсные (четыре контакта) ХГСМ-электроды (две модели с различными зазорами между контактами: 3387, 1,5-мм интервалы и 3389 0,5-мм интревалы; Medtronic)
На протяжении многих лет два разных ИГИ были доступны для ХГСМ: одноканальные системы (например, Soletra, Medtronic) или двухканальные системы (например, Kinetra, Medtronic,).
С 2009 г. в комплект входят также перезаряжаемые аккумуляторные батареи ИГИ. Два электрода могут быть подключены к двухканальному ИГИ. Устройство для внешнего программирования используется для изменения регулируемых переменных, в том числе выбора стимулирующих контактов, длительности импульса, амплитуды и частоты. ИГИ можно выключить или изменить его параметры в заданных пределах с помощью ручного программатора.
3. Оперативная техника. Стереотаксическая хирургия позволяет достичь определенной целевой области в любой точке мозга с трехмерной точностью наведения системы координат. Стереотаксическая система состоит из прямоугольной или круглой рамы, которая крепится к голове пациента с помощью штифтов под местной анестезией. Каждое место в мозге может быть определено в прямоугольной системе координат (X/Y/Z) или в полярной системе координат относительно рамки. Для расчета целевых координат, выполняют стереотаксическое КТ и/или стереотаксическое МРТ сканирование.
Как правило, операция проводится под местной анестезией, чтобы пользоваться контактом с пациентом, в частности, для тестирования порогов эффективности подавления симптомов и побочных эффектов от макростимуляции. При тяжелой дистонии или у детей оперируют под общим наркозом. Для дальнейшего уточнения цели используются несколько нейрофизиологических методов. Самым простым является запись с микроэлектрода. После имплантации электродов ХГСМ макростимуляция осуществляется через различные контакты.
Для тестирования клинической эффективности или для записи местных потенциалов электрод может располагаться снаружи. При второй процедуре он подключается через удлинитель к ИГИ, размещаемому подкожно в подключичной области под общей анестезией. Риск операции сравнительно невелик. В недавнем исследовании (n=319) зафиксированы серьезные осложнения, включая судороги у четырех пациентов (1,2%), внутримозговые кровоизлияния у двух пациентов (0,6%), внутрижелудочковое кровоизлияние у двух пациентов (0,6%) и субдуральную гематому у одного пациента (0,3%).
4. Неполадки оборудования. Технические проблемы, связанные с оборудованием, могут включать дислокацию электродов из-за недостаточной фиксации на фрезевом отверстии, кабельные разъединения (кабель-удлинитель) и инфекции системы (кабеля или ИГИ). Общий уровень инфекции описывается в диапазоне от 2 до 10%. В серии из 119 пациентов в 15% случаев было 23 аппаратных осложнения, которые включали восемь поломок электродов, четыре миграции электрода, две миграции стимулятора, три эрозии, две эрозии и инфекции, два случая инфекции и два случая неисправности ИГИ. Большинство из этих осложнений произошло в первые четыре года после операции. В случае инфекции в первую очередь следует назначать антибиотики; если это не удается, всю систему иногда приходится удалять.
Полный разряд батареи в ИГИ требует дополнительной операции. Время до разряда батареи отличается в зависимости от выбранных параметров стимуляции (амплитуды, длительности импульса и выбора контактов). Необходимость смены ИГИ батареи чаще у пациентов с дистонией (1-3 года) в связи с более высокой энергией стимуляции, чем при болезни Паркинсона (БП) или у пациентов с тремором (3-6 лет).
в) Отбор пациентов для глубокой стимуляции мозга. Для рассмотрения возможности ХГСМ необходимо соответствующее диагностическое исследование и медикаментозное лечение. Заметьте, что ХГСМ является комплесным подходом, включающим междисциплинарный отбор и наблюдение за пациентами. Противопоказаниями являются слабоумие, психопатологические изменения и тяжелая депрессия. Кроме того, ограничивающим фактором может быть преклонный возраст.
1. Хроническая глубокая стимуляция мозга при треморе. Тремор определяется как непроизвольные ритмические колебания одной или нескольких частей тела. Типы тремора классифицируются по режиму активации (отдых, действия или кинестезии), частоте, наследственности и сопутствующей симптоматике, которая может прояснить этиологию тремора (симптомы других нарушений движения, полинейропатии и др.). Распространенность тремора составляет до 400/100000 в нормальной популяции и до 4,8% у пациентов старше 65 лет.
Тремор может быть не просто помехой, но привести к инвалидности и к серьезным социальным осложнениям. Консервативное лечение тремора включает в себя применение пропранолола, примидона или топирамата. Медикаментозная терапия первой линии для лечения тремора при болезни Паркинсона во многих случаях не дает существенного улучшения. Фармакологическая терапия, с другой стороны, часто неэффективна при треморе. Это должно быть учтено, однако атаксия, сопровождающаяся тремором, плохо контролируется ГСМ. Было отмечено, что у пациентов с БП дополнительные симптомы, такие как постуральная нестабильность, акинезия или ригидность, которые могут возникнуть при развитии болезни, не зависят от ГСМ таламуса.
Таким образом, вряд ли таламус является целью при ХГСМ у молодого пациента с тремором. ГСМ субталамического ядра подавляет тремор в одинаковой степени при БП. ГСМ таламуса можно использовать, но вероятно, только у пожилых пациентов с БП, страдающих моносимптомным тремором в течение многих лет.
2. Хроническая глубокая стимуляция мозга при болезни Паркинсона (БП). БП—результат дегенерации нескольких конкретных областей, и, в частности, дисфункции нигростриарных путей в связи с потерей дофаминергических нейронов в черной субстанции. Основные двигательные симптомы — акинезия, ригидность, тремор и постуральная неустойчивость — сопровождаются сенсорным, вегетативным, психологическим и когнитивным дефицитом. Распространенность среди населения в возрасте старше 55 лет была оценена как 1,5-2,0%. ХГСМ—вариант лечения для пациентов с болезнью Паркинсона.
Лучший кандидат для хирургического лечения — пациент, хорошо реагирующий на дофаминергическую терапию, но имеющий двигательные осложнения, которые развиваются через 5-7 лет дофаминергической терапии. Снижается выраженность тяжелых флюктуаций и дискинезии, также улучшаются основные двигательные симптомы БП (тремор, ригидность, акинезия, и постуральная неустойчивость).
После стимуляции доза дофаминергических препаратов может быть уменьшена. Депрессия или тревожность могут также зависеть от ХГСМ. Должны быть учтены возраст пациента и стадия заболевания. В целом возраст не должен превышать 70 лет, а стадия заболевания не должна быть терминальной. Степень послеоперационного улучшения может быть предсказана предоперационным ответом на прием леводопы, что имеет первостепенное значение для выявления пациентов с другими паркинсонизмами, такими как множественная системная атрофия, прогрессивный супрануклеарный паралич и кортикобазальноядерная дегенерация.
В этих случаях результаты от ХГСМ обычно отсутствуют. У пациентов с моносимптомным тремором при БП ХГСМ таламуса может быть альтернативой в пожилом возрасте, так как в меньшей степени вызывает психосоциальные или когнитивные проблемы.
3. Хроническая глубокая стимуляция мозга при дистонии. Дистония характеризуется устойчивым сокращением мышц, часто вызывая скручивание и повторяющиеся движения или ненормальные позы. Дистонию можно классифицировать по трем различным направлениям: возраст начала заболевания, анатомическое распределение (очаговая, сегментарная, общая, гемидистония) и этиологии (первичная или вторичная). Спастическая кривошея или цервикальная дистония (ЦД) является наиболее распространенной формой координационной дистонии. ЦД встречается у 0,39% жителей США.
Фокусная дистония может успешно лечиться инъекциями ботулинического токсина. При гемидистонии, сегментарной или общей дистонии, часто необходим хирургический подход в связи с распространенным вовлечением нескольких групп мышц. В то же время пациенты с первичной (генетической или спорадической) генерализованной и сегментарной дистонией и пациенты со сложными ЦД считаются лучшими кандидатами для паллидумальной ХГСМ. В целом, пациенты с первичными дистониями, по всей видимости, хорошо реагируют на лечение, а пациенты с вторичными дистониями отвечают на лечение хуже.
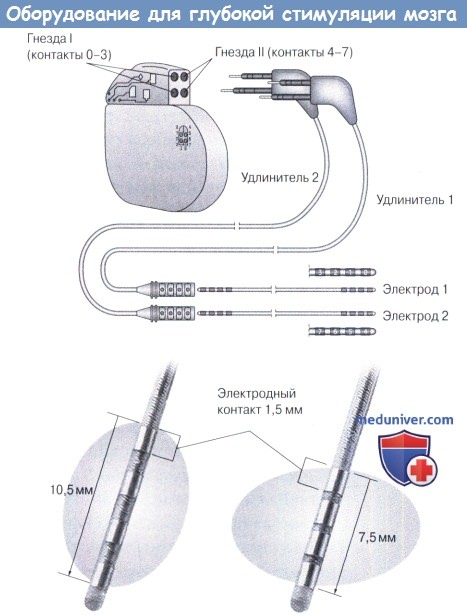
Оборудование для глубокой стимуляции мозга. Четырехполюсные электроды и имплантированный генератор импульсов (ИГИ) соединены кабелями. 
А-Г. Стереотаксические рамки. CRW рамка (А), рама Leksell (Б), рама Riechert-Mundiger (В), рама Riechert-Mundiger с аркой Zamorano-Dujovny (Г). 
Программер для включения, выключения либо смены частоты ИГИ. 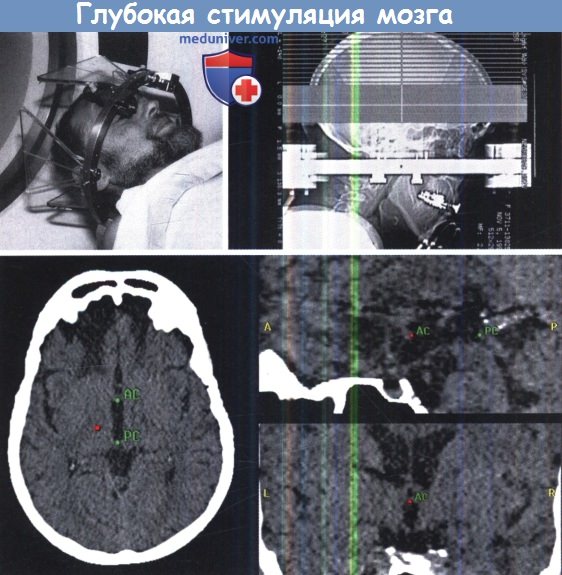
Стереотаксическая рамка (рама Riechert-Mundiger), установленная на голове пациента и полученные стереотаксические изображения (верхний ряд).
Идентификация передней и задней комиссур на КТ с одновременным улучшением визуализации в аксиальной, сагиттальной и коронарной проекциях (нижний ряд). 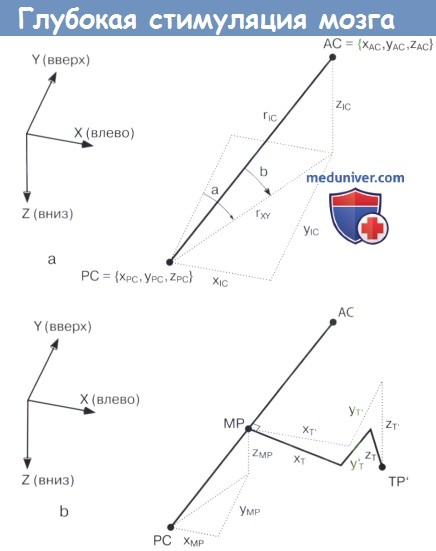
Возможен наклон линии АС-3С относительно стереотаксической рамки во всех трех плоскостях.
Эти отклонения должны быть скорректированы с использованием специальных измерительных алгоритмов.
Читайте также:


