Паркинсонизм и черная субстанция
Из разнообразных нейронных проекций в системе базальных ганглиев наиболее изучены так называемые нигро-стриарные связи, простирающиеся от черной субстанции до хвостатого ядра. В 1965 г. было окончательно доказано, что в указанной системе связей дофамин выполняет медиаторную функцию.
В периферической нервной системе дофамин является предшественником норадреналина — основного медиатора в симпатической нервной системе. В центральной нервной системе млекопитающих и человека дофамин выполняет уже самостоятельную и очень важную медиаторную функцию.
Дофаминергические нейроны расположены не только в черной субстанции, но и в структурах среднего мозга (например, в nucleus accumbens, поражение которого, кстати, наблюдается и при паркинсонизме) и в некоторых важнейших образованиях лимбико-ретикулярного комплекса: в лимбической и префронтальной коре, в ядрах миндалевидного комплекса, а также в тубероинфундибулярной системе, связывающей гипоталамус с гипофизом.
Уже простого перечисления этих структур, по-видимому, достаточно для того, чтобы получить представление о функциональном значении дофамина, принимающего участие в контролировании психических, двигательных и эндокринных функций организма.
Знание топографии дофаминергических систем мозга необходимо в силу ряда важных для невролога обстоятельств. Во-первых, высказано предположение, что паркинсонизм представляет собой системное заболевание дофаминергических нейронов мозга и, следовательно, не ограничивается поражением только нигростриарных дофаминергических путей.
Во-вторых, лечебное воздействие на дофаминергические системы с помощью средств, блокирующих или стимулирующих эти системы, часто приводит к нежелательным побочным эффектам, характер которых зависит от того, на какие дофаминергические системы мозга оказывает свое преимущественное влияние тот или иной препарат.
Дело в том, что в настоящее время предполагается существование специфических типов дофаминергических рецепторов в разных частях мозга. Поэтому изучение различных дофаминергических систем мозга является необходимым условием для разработки более целенаправленных средств лечебного воздействия, а также для прогнозирования и профилактики побочных эффектов при лечении самых разнообразных неврологических заболеваний, в том числе и паркинсонизма.
Изложение современных представлений о моноаминергических системах мозга, разумеется, не входит в задачи этой книги. Мы остановимся лишь на некоторых механизмах функционирования дофаминергического нейрона, необходимых для понимания патогенеза паркинсонизма и основных принципов и перспектив его лечения.
Наиболее полная сводка работ, посвященных моноаминергическим, в том числе дофаминергическим, системам мозга, представлена в монографиях Кална, А. Ю. Буданцева, в обобщающих статьях С. Л. Левина, Фьюкса и других авторов.
В черной субстанции расположены тела нейронов, аксоны которых, составляющие нигро-стриарный путь, проходят через ножки мозга, внутреннюю капсулу и оканчиваются в неостриа-туме в виде широкого сплетения терминальных микровезикул с высоким содержанием дофамина. Именно этот путь является тем местом в мозге, поражение которого приводит к формированию синдрома паркинсонизма.
При болезни Паркинсона поражаются нейроны головного мозга
Болезнь Паркинсона является самым распространенным в мире заболеванием, протекающим с двигательными нарушениями.
Болезнь Паркинсона встречается среди представителей всех рас, мужчины несколько более предрасположены к развитию заболевания, чем женщины.
Болезнь Паркинсона считается заболеванием людей пожилого возраста. Средний возраст начала заболевания составляет 60–65 лет. (Хотя при раннем развитии болезни Паркинсона первые симптомы могут появиться в возрасте от 21 до 40 лет. Среди всех пациентов с болезнью Паркинсона раннее развитие заболевания наблюдается в 5–10% случаев).
Чёрная субстанция имеет сложную структуру и обильное кровоснабжение, что говорит о высокой роли её компонентов в системе координации жизнедеятельности.
Благодаря чёрной субстанции осуществляются функции: движения глаз, она регулирует и координирует мелкие и точные движения, в частности, пальцев; координирует процессы жевания и глотания. Имеются данные о роли чёрной субстанции в регуляции многих вегетативных функций: дыхания, сердечной деятельности, тонуса кровеносных сосудов.
Чёрная субстанция имеет решающее значение в развитии многих заболеваний, включая болезнь Паркинсона. Повреждение чёрной субстанции человека, приводит к произвольным движениям головы и рук, когда больной сидит спокойно (болезнь Паркинсона). Нередко, возникает т. н. экстрапирамидный синдром в виде:
- мышечной гипертонии, при этом некоторые гиперкинезы (хореические) связаны с мышечной гипотонией;
- гипокинезии (Олигокинезии), то есть уменьшением двигательной инициативы и затруднениями при переходе из состояния покоя в состояние движения и наоборот;
- брадикинезии, замедлением движений и уменьшением их амплитуды;
- преобладания сгибательной позы (согнутая спина, наклонённая к груди голова, согнутые в локтях и лучезапястных руки и в коленях - ноги);
- гипомимии, снижение или отсутствие мимики;
- монотонной, тихой и глухой речи;
- отсутствия содружественных движений;
- гиперкинезами (Тремор, торсионный спазм, атетоз, хорея, миоклонии, локализованный спазм).
Возможности инструментальной диагностики болезни Паркинсона остаются крайне ограниченными. Сравнительно недавно было показано, что с помощью транскраниальной сонографии возможна визуализация структур головного мозга и выявление определенных изменений, характерных для различных экстрапирамидных заболеваний.
Основными преимуществами транскраниальной сонографии по сравнению с другими методами исследования являются относительно не высокая стоимость исследования, неинвазивность, короткое время проведения исследования и возможность многократного обследования без риска для здоровья пациента.
Единственным ограничением применения транскраниальной сонографии является отсутствие височного окна, что имеет место приблизительно в 10% случаев, главным образом, у женщин пожилого возраста.
Значение слова Гипер. по Ефремовой:
Гипер. - Начальная часть сложных слов, вносящая значение: превышающий какую-л. норму (гиперзаряд, гиперзвуковой, гиперпространство, гиперреализм, гиперсекреция, гипертония, гипертрофия и т.п.).
Эхогенность, эхоплотность – ультразвуковая яркость
Характеристики эхогенность и эхоструктура являются основными в ультразвуковой диагностике, они используются совместно для описания любых визуальных объектов.
Дофамин. Нервные клетки, которые передают импульсы с помощью дофамина, сосредоточены преимущественно в трёх областях: в гипоталамусе, в чёрной субстанции и в вентральной покрышке. Нейромедиатором он работает только тут.
Итак, гипоталамус. Те нервные клетки, которые пользуются дофамином, чтобы общаться между собой, в этой области довольно замкнуты друг на друга: далеко свои аксоны не тянут, предпочитают свой тесный внутренний круг. Но при этом рулят довольно важными системными функциями: могут отдать команду на выработку ряда гормонов или тормознуть её, могут также, к примеру, понизить мотивацию на предмет чего-нибудь пожрать, могут усилить агрессивность или повысить либидо. Раз — и вектор человеческого поведения заметно поменялся.
Ну с гипоталамусом учёным ещё долго разбираться, там уж очень тесно и сложно намешано нервного и гормонального, а вот в чёрном веществе и в вентральной покрышке дофаминовые нервные клетки изучены подробнее. Не в последнюю очередь из-за паркинсонизма, шизофрении и наркотиков.
Если дофамина в чёрном веществе дофига, и чёрная субстанция активна, то такие люди — как правило, живчики. То есть, с удовольствием двигаются, танцуют, занимаются спортом и вообще получают кайф от движения. Те, кто победнее дофамином в своей чёрной субстанции — внешне кажутся более ленивыми, зато умеют получать удовольствие от чего-то иного: еды, например, новизны как таковой, созерцания.
Отростки нервных клеток из этой чёрной субстанции не только между собой соединены: в отличие от тех, что в гипоталамуса, у них более длинные лапки. И много таких отростков идут вверх, к большим полушариям головного мозга. И в частности — к скоплениям нервных клеток, которые названы базальными ганглиями. 80% этих ганглиев отвечают за движения.
На оставшиеся 20% идут отростки от другого образования —вентральной покрышки - на них-то как раз во многом завязана система, которая отвечает за формирование потребностей и мотиваций, которая тесно связана с эмоциями.
Соответственно, и нарушение работы в этой связке тоже не проходит для человека бесследно. Если в силу ряда (в том числе генетических) причин покрышка работает слабо — человек недополучает положительные эмоции от новизны. И в ряде случаев это оказывается стержнем будущей депрессии. Если дофамина в покрышке слишком много — получите скачку идей и неспособность долго сосредоточиться на одной мысли, как при выраженной мании. В отдельных же случаях система срабатывает вхолостую: вроде бы и нет входящего стимула, а отклик в покрышке почему-то возник.
Среди тех базальных ганглиев, к которым идут отростки от покрышки, есть такое образование — прилежащее ядро, или nucleus accumbens - центр, генерирующий положительные эмоции.
Именно на связь покрышки с прилежащим ядром и действуют наркотики амфетамин и кокаин, разгоняя, усиливая действие дофамина в ней. Именно это действие и даёт тот фейерверк положительных эмоций, тот прилив бодрости и сил, а также ощущение предельной собранности и кристальной ясности мышления вкупе с его быстротой.
![]()
Уж если в заголовок вынес болезнь Паркинсона, то как-то надо поподробнее про неё. И не понятно за каким ты в конце наркоту приплел ко всему. Начал за здравие, а кончил за упокой
Наркота, типа феназепама, вызывает синдром паркинсонизма
Внутри шизофрении. Часть 1.
Заболевание, которое можно счесть за шизофрению, было известно с древних времен, возможно, даже доисторических. Отчетливые упоминания есть в Библии (помните, как царь Навухудоносор кушал траву с луга?), ими сквозит Античность и так далее. Однако утверждать на 100% ничего невозможно: существуют психозы и помимо шизофрении, а также есть, например, паразиты, поражающие нервную систему и способные вызвать галлюцинации. К тому же, не надо забывать о сифилисе, который с человеком живет уж точно не меньше, чем шизофрения.

В историю шизофрении я не собираюсь сильно вдаваться, поскольку об этом много сказано. Все написанное выше я упоминаю только с одной целью: чтобы показать, насколько сложный и ускользающий смысл вкладывается в этот термин.
Здесь нужно сделать небольшую оговорку: нам с вами, с раннего детства давящимися плодами науки, которые созревали в течение столетий, люди прошлого могут казаться очень недалекими. Ну как тут было не отличить, скажем, расстройства настроения и психозы? Ну вот больного глючит, как скотину, а вот он просто грустный сидит. Очевидно же, что это разные заболевания! На самом деле, нет. Главная боль всей медицины состоит в том, что одна болезнь в большинстве случаев не мешает развиваться другой. И расстройства настроения (аффективные расстройства) не только не мешают психозам, а зачастую сочетаются.
(Вот и сам Крепелин):

Надо сказать, что в те годы содержимое черепа было настоящим черным ящиком для науки. Оно и сейчас в значительной мере остается черным ящиком, но тогда мы даже представить не могли, КАКАЯ херня там творится. Все эти нервные связи, нейромедиаторы, нейронные сети, колонки, контуры… Едва ли хоть кто-то догадывался, что все может быть устроено так странно. Сама идея о том, что электрическая активность мозга большей частью опосредуется химическими веществами – дикость какая-то. Поэтому все, что оставалось психиатрам тех лет – наблюдать и накапливать знания, надеясь на психиатров будущего.
Для того, чтобы хоть немного приоткрыть завесу тайны над заболеванием, нужны были очень крупные открытия в нейробиологии и нейрофизиологии, которые в те времена были невозможны просто технологически. Первый толчкок, который помог предположить истинные причины шизофрении, был со стороны фармакологии. Это открытие аминазина. Цитата с одного ресурса:
В 1950 году французский нейрохирург Генри Лабори предположил, что чрезмерные переживания его пациентов перед операцией вызывают выброс избыточного количества гистамина. Гистамин — небольшая молекула, которая регулирует сотни процессов в организме: от выделения желудочного сока до температуры. Лабори считал, что именно чрезмерный выброс гистамина из-за тревоги пациентов может вызывать осложнения анестезии и даже внезапную смерть.
Лабори методом проб и ошибок пытался подобрать подходящий антигистаминный препарат. Совершенно случайно он обнаружил, что не самое популярное лекарство — хлорпромазин — действительно успокаивает пациентов. Более того, хлорпромазин усиливал действие анестезии.
Предположение довольно типичное для тех времен, хотя и неверное. Тем не менее, ошибочное предположение привело к великому открытию – открытию первого на свете нейролептика. А сочетание нейролептиков с анестетиками используется до сих пор (нейролептанальгезия). Нейролептики (они же антипсихотики) – препараты, (относительно) избирательно действующие на симптомы психоза – бред и галлюцинации. Это открытие, в конечном счете, и помогло составить современные представления о причинах и патогенезе (т.е развитии болезни) шизофрении. Последовавшие исследования позволили открыть различные рецепторы в головном мозге, в том числе рецептора домафина. Именно тогда и оказалось, что основным эффектом нейролептиков является блокада эффектов дофамина, а дальше все заверте…
Вот мы и подошли к тому, чтобы описать сегодняшние представления о патогенезе шизофрении. Только представьте, какую дикую работу пришлось проделать, чтобы подойти к примерному представлению о том, как развивается эта психическая болезнь. Я буду идти в своем рассказе по такому принципу: от самых элементарных представлений на уровне молекул и клеток до нарушений в работе мозга в целом, а затем до нарушений психики.

Возможно, у вас уже возник вопрос: а почему тогда не использовать методы типа позитронно-эмисионной томографии или ф-МРТ и не выявить, какие отделы мозга работают неправильно? Да, заманчивая идея, и это, конечно же, пытались сделать, и даже есть результаты. Однако результаты эти породили больше вопросов, чем ответов. Действительно, удалось найти нарушения в работе мозга при шизофрении на ПЭТ и ф-МРТ, и касаются они преимущественно работы височных и лобных долей мозга, а также лимбической системы и их взаимодействия. Однако они встречаются не только при шизофрении, и не у всех шизофреников идентичны, чтобы можно было вбить в программу шаблон, который бы автоматически определял подобные изменения. Идея не нова, и в свое время изучали шизофрению с помощью рентгена, эхоэнцефалографии/скопии и других методик, однако результат всегда был похожим: да, что-то есть, но данных, однозначно указывающих на шизофрению, нет.
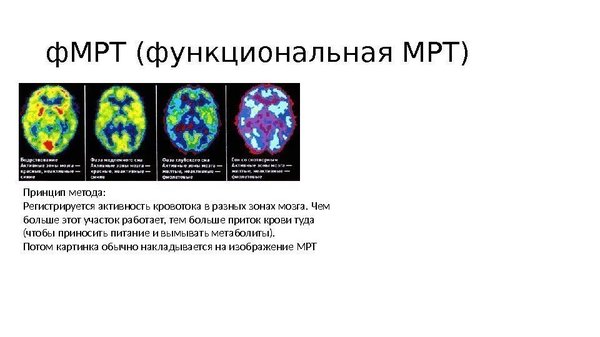
Как видно, даже здесь шизофрения дает прикурить. Очень мозаичное и скользкое заболевание, не дающее нам никакой нити, за которую можно было бы уцепиться и распустить весь клубок. Таким же оно предстает перед психиатрами – королева масок.
Как нетрудно догадаться, эти анатомические изменения порождают нейрохимические изменения, и тут, боюсь, придется вкратце напомнить основы нейрохимии мозга.
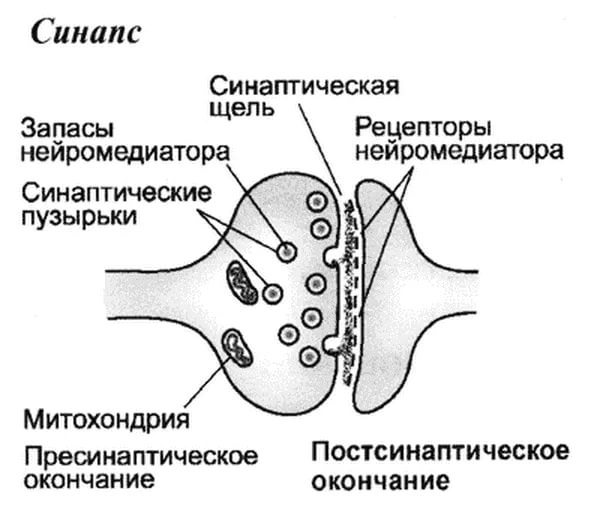
В нашем мозге постоянно осуществляется напряженная работа, которая проявляется в передаче электрических импульсов между нейронами. Соединение между двумя нейронами осуществляется с помощью специальной структуры – синапса. Примерно так он выглядит:
"Мой супруг — офицер, человек очень уравновешенный. Он всю жизнь работал, ни на что не жаловался, я никогда не слышала от него про усталость. Но приблизительно шесть лет назад он стал слишком тихим, мало разговаривал — просто сидел и смотрел в одну точку. Мне даже в голову не пришло, что он болен. Наоборот, ругала, что раньше времени постарел. Примерно тогда же к нам приехала двоюродная сестра из Англии — она работает в больнице — и сразу сказала, что у Рафика все очень плохо, нужно завтра же вести его к врачу. Так мы узнали о болезни Паркинсона", — вспоминает Седа из Еревана.
Что такое болезнь Паркинсона
Паркинсон — одна из самых страшных фамилий, что можно услышать в кабинете у невролога. Ее носил английский врач, который в 1817 году подробно описал шесть случаев загадочной болезни. День рождения Джеймса Паркинсона, 11 апреля, и выбран памятной датой Всемирной организацией здравоохранения. Из-за основных симптомов Паркинсон называл недуг дрожательным параличом: движения больных замедляются, становятся скованными, мышцы сильно напрягаются, а руки, ноги, подбородок или все тело бесконтрольно трясутся. Впрочем, в четверти случаев дрожания — самого известного признака болезни — нет.
Все это напоминает обыкновенную старость. Двигательные симптомы — собирательно их называют паркинсонизмом — встречаются у многих здоровых стариков. Но болезнь Паркинсона этим не исчерпывается. На поздних стадиях человек легко теряет равновесие, то и дело застывает на месте во время ходьбы, ему трудно говорить, глотать, спать, появляются тревога, депрессия и апатия, мучают запоры, падает кровяное давление, слабеет память, а под конец часто развивается слабоумие. Самое печальное — вылечить болезнь Паркинсона пока невозможно.
В начале XX века российский невропатолог Константин Третьяков выяснил, что при болезни Паркинсона гибнут клетки черной субстанции, области мозга, которая частично отвечает за движения, мотивацию, обучение. Что вызывает смерть нейронов, неизвестно. Возможно, дело в сбоях внутри клеток, но еще замечено, что внутри них скапливается вредный белок. Оба процесса наверняка как-то связаны, но ученые не знают, как именно.
В 2013 году физиолог Сьюзан Гринфилд из Оксфордского университета представила новую модель развития нейродегенеративных заболеваний, в том числе болезней Паркинсона и Альцгеймера. Гринфилд предположила, что при повреждении мозга, например, от сильного удара выделяется особое вещество. У маленьких детей из-за него растут новые клетки, а на взрослых оно, судя всему, действует противоположным образом, дальше повреждая клетки. После этого следует еще больший выброс вещества, и цепная реакция постепенно разрушает мозг. По злой иронии взрослые впадают в младенчество из-за фермента, необходимого младенцам.

Впрочем, догадка Гринфилд объясняет не все. Болезнь Паркинсона связана с наследственностью: близкий родственник с таким же диагнозом или тремором другой природы — главный фактор риска. На втором месте — запоры: иногда их вызывают изменения в мозге, когда еще не появились двигательные симптомы. Также риск растет, если человек никогда не курил, живет за городом, пьет колодезную воду, но при этом сталкивался с пестицидами, а снижается — у любителей кофе, алкоголя и гипертоников. В чем тут секрет, непонятно, как непонятно, почему болезнь Паркинсона обычно начинается в старости: если на пятом десятке лет болеет примерно один из 2500 человек, то на девятом — уже один из 53.
Новую зацепку дала свежая работа ученых из Университета Томаса Джефферсона: возможно, болезнь Паркинсона связана с иммунной системой. Исследователи взяли мышей с мутантным геном, который часто встречается у больных, и ввели им безвредные остатки бактерий. Из-за этого у зверьков началось воспаление, затронувшее и мозг, причем иммунных клеток было в 3–5 раз больше, чем у обычных мышей. Из-за этого в мозге мутантов начались процессы, губительные для нейронов черной субстанции. Как и в модели Гринфилд, процессы эти оказались циклическими: воспаление в мозге может остаться даже после того, как тело справилось с инфекцией. Впрочем, сами авторы исследования признаются, что в этом механизме еще многое не ясно.
Каково живется больным и их близким
В России болезнь Паркинсона есть примерно у 210–220 тыс. человек. Но эти данные рассчитаны по косвенным показателям, а единого реестра не существует. Анастасия Обухова, кандидат медицинских наук с кафедры нервных болезней Сеченовского университета и специалист по болезни Паркинсона, считает эту статистику заниженной. "Многие больные впервые приходят уже на развернутых стадиях болезни. При расспросе удается выяснить, что признаки появились еще несколько лет назад. У большинства наших людей действует принцип "Пока гром не грянет, мужик не перекрестится": они читают в интернете, спрашивают соседок, а к врачу не обращаются. Это в Москве, а в маленьких городках и поселках к врачу идут только если совсем помирают", — объясняет Обухова.
Вдобавок попасть на прием не так-то просто. Для этого сначала нужно сходить к терапевту, чтобы тот направил к неврологу. Но и тогда нет гарантии, что человеку поставят правильный диагноз и назначат нужное лечение. "Врач в поликлинике не может разбираться во всем, поэтому должен послать больного к узкому специалисту. А окружных паркинсонологов, по-моему, убрали. Во всяком случае, пациенты на это жаловались", — рассказывает Обухова. Правда, если больной все-таки попал к нужному доктору, лечить его будут на мировом уровне. Оттого в Россию с болезнью Паркинсона прилетают даже из других стран.
Одиссею по кабинетам приходится часто повторять, потому что болезнь прогрессирует — терапию нужно подстраивать. Лечение обходится дорого: месячный запас некоторых лекарств стоит по 3–5 тыс. рублей, а на поздних стадиях назначают сразу несколько препаратов. "В районных поликлиниках лекарства иногда дают бесплатно, но только дешевые дженерики. Комментировать их качество не буду. Иногда нужных лекарств нет. Тогда их заменяют чем-то другим. Пациентам от этого плохо", — объясняет Обухова.

Дофаминергические нейроны, полученные из iPSC, в культуре. Credit: Dr. Regis Grailhe, Nasia Antoniou, Dr. Rebecca Matsas
Болезнь Паркинсона – это нейродегенеративное заболевание, которое характеризуется постепенным отмиранием дофаминергических нейронов в черной субстанции, находящейся в среднем мозге. Из-за этого нарушается мышечный тонус – движения становятся скованными, неловкими, медленными, появляется тремор, возникают когнитивные расстройства. Эффективное лечение болезни на данный момент не найдено, а для коррекции состояния используются предшественник дофамина леводопа и ее аналоги, а также глубокая стимуляция мозга. Подробнее об этом вы можете узнать в нашей статье.
Первым пациентом стал 50-летний мужчина, страдающий болезнью Паркинсона более семи лет. Длилась операция, точнее, процедура около трех часов, провели ее в октябре, и уже месяц за пациентом внимательно наблюдают. Пока его состояние не вызывает никаких опасений, побочные действия также не дали о себе знать. Если через шесть месяцев никаких осложнений не возникнет, ученые планируют пересадить ему еще 2,4 миллиона клеток.
Технология по клеточному репрограммированию, которую разработал Синъя Яманака в 2006 году на базе Университета Киото, привела своего создателя к Нобелевской премии в 2012 году. В 2014 же году iPS клетки впервые были одобрены для клинического применения в качестве лечения заболеваний сетчатки. Причем создала эту методику жена Джуна Такахаши, офтальмолог Масайо Такахаши (Masayo Takahashi).
Текст: Анна Хоружая

Как известно, симптомы болезни Паркинсона вызваны гибелью дофаминергических нейронов в черном веществе головного мозга и ослаблением связей между ними: известно, что патологические процессы начинаются ещё…
Учёные из Имперского колледжа Лондона выяснили, что белок альфа-синуклеин, который до этого считался ранним маркёром болезни Паркинсона, оказывается, важен для нормальной работы мозга. Мобилизуя нужное…
Новый метод прижизненной идентификации активности нейронов, чем-то напоминающий светофор, создали нейробиологи из Национального института наук о связи здоровья и окружающей среды, входящего в Национальные институты…

Исследователи из Научного центра неврологии и Института молекулярной генетики РАН изучили, насколько эффективной оказалась пересадка индуцированных плюрипотентных стволовых клеток (iPSC) при нейродегенеративных заболеваниях. Создав животные…
Исследования показывают, что анализ слёз может помочь докторам диагностировать болезнь Паркинсона. В слезах людей с этим заболеванием повышен уровень особого белка, олигомерного альфа-синуклеина.Такие выводы были…

Перед вами — дофаминергические нейроны. Но не простые, а выращенные из стволовых клеток человека, которые, в свою очередь, были получены из клеток кожи пациента с болезнью…

Исследователи выяснили, что люди с ранней стадией болезни Альцгеймера (в возрасте до 65 лет) не получают улучшений от глубокой стимуляции мозга – терапии, которая показала…


Перед вами — дофаминовые нейроны чёрной субстанции, которые гибнут при болезни Паркинсона. Исследователи, кажется, сумели выяснить, как именно погибают эти нейроны. Проследив все биохимические каскады, в…

Доктор биологических наук, профессор кафедры физиологии человека и животных биологического факультета МГУ, Вячеслав Дубынин рассказывает о болезни Паркинсона, связи дофамина с шизофренией и истории нейролептиков.
Одним из важнейших медиаторов центральной нервной системы является вещество, называющееся дофамин. Дофамин известен достаточно давно, где-то с середины XX века. Это соединение, специфично связанное с мозгом, прежде всего с головным, в отличие, например, от ацетилхолина, норадреналина, которые активны в периферической нервной системе.
Дофамин образуется в наших нейронах в результате довольно несложной цепочки химических реакций. Начинается она с аминокислоты, которая называется тирозин, и дальше тирозин превращается в молекулу, называемую L-ДОФА, а уже L-ДОФА становится дофамином. То есть получается цепочка из двух реакций, причем L-ДОФА в данной цепочке является предшественником дофамина, что дальше определяет использование молекулы L-ДОФА как лекарственного препарата, но об этом чуть позже.
Дофамин действительно очень важен для центральной нервной системы, и если мы начинаем анализировать строение мозга, то обнаруживаем дофаминовые нейроны в основном в трех зонах: это гипоталамус и две области среднего мозга, одна называется черная субстанция, а вторая — вентральная покрышка. Если мы смотрим на гипоталамус, то видим, что у дофаминовых нейронов гипоталамуса довольно короткие отростки-аксоны. Они в основном занимаются внутригипоталамическими проблемами и воздействуют на выброс некоторых гормонов или на центры некоторых потребностей, немного участвуют в вегетативной регуляции, но в общем это довольно локальные функции, хотя, конечно, важные. Например, в гипоталамусе дофамин может понижать пищевую мотивацию, повышать агрессивность или усиливать либидо, то есть это локальные, но важные моменты.
Наиболее известны те дофаминовые нейроны, которые находятся как раз в черной субстанции и вентральной покрышке. Черная субстанция потому так и названа, что эта зона мозга имеет темную окраску: нейроны там содержат некоторое количество меланина — темного пигмента. Аксоны этих клеток идут вверх, в большие полушария, и в основном они заканчиваются в базальных ганглиях. Данный блок дофаминовой системы связан с регуляцией двигательной активности: от того, насколько много дофамина выделяет черная субстанция, во многом зависит, насколько человек физически активен, моторен, любит двигаться, охотно двигается. Люди с активной черной субстанцией с удовольствием занимаются спортом, танцуют и вообще перемещаются в пространстве. Люди, у которых черная субстанция не очень активна (а это в основном зависит от генов), соответственно, двигательно более ленивы и не получают столько удовольствия от физических упражнений, но они получают удовольствие от чего-то другого: от еды или новизны — во всяком случае, окружающие их порой воспринимают как лентяев.
Если мы смотрим, куда конкретно приходят аксоны черной субстанции в больших полушариях, то это зона, называемая базальные ганглии. Это очень непростая область, находящаяся в глубине больших полушарий. Когда мы говорим о больших полушариях, мы прежде всего вспоминаем кору, зону, которая находится на поверхности полушарий и содержит огромное количество нервных клеток с самыми разными функциями. Но в глубине больших полушарий есть крупные скопления нейронов, которые в свое время и были названы базальными ганглиями. И там расположена масса анатомических структур: полосатое тело, бледный шар, скорлупа, ограда. У всех них сложные латинские названия, но если в целом смотреть на базальные ганглии, то видно, что где-то 80% нейронов в этой группе структур занимаются движениями. Именно на активность этих нейронов и влияет черная субстанция. Остальные 20% базальных ганглий входят в другую систему, связанную с потребностями, мотивациями, эмоциями, и об этом блоке я еще скажу.
Вторая область — вентральная покрышка. Аксоны этой зоны идут в кору больших полушарий и в ту часть базальных ганглий, которая занимается как раз потребностями, мотивациями и эмоциями. Дофамин, вырабатывающийся нейронами вентральной покрышки, в коре больших полушарий, во многом определяет скорость обработки информации и, если угодно, скорость нашего мышления. Если много дофамина в этой системе и вентральная покрышка будет достаточно активна, то мы видим, что информационные процессы идут быстро, у человека быстрый мозг. Такие люди могут очень успешно заниматься математикой, программированием и вообще профессиями, связанными с абстрактным мышлением.
Кроме того, этот же блок дает нам положительные эмоции, связанные с новизной. Это очень важная составляющая нашей психической жизни, потому что наш мозг очень любопытен и получение новой информации биологически очень важно: мы должны знать, что меняется в окружающем мире, оперативно эти изменения детектировать и анализировать. Кроме того, нас это радует, и для человека, занимающегося наукой или искусством, это важнейшая составляющая психической жизни, потому что что-то сочинить или открыть — это просто замечательно. Получается, что дофамин связан с положительными эмоциями, которые коррелируют с новизной, творчеством, юмором, потому что шутка — это тоже некая рассказанная ситуация, в которой был банальный выход, а вам предложили что-то необычное, какую-то небанальную соль анекдота, и вы смеетесь — это тоже выделение дофамина.
К сожалению, эта система тоже может работать не очень правильно. Если она работает слабо по каким-то причинам (в основном генетическим), то человек недобирает положительных эмоций, связанных с новизной, и это может быть одним из компонентов депрессии. Если эта система работает слишком сильно, то мышление может стать избыточно быстрым, дерганным, человек не может сосредоточиться и долго думать одну и ту же мысль. Порой сенсорные системы начинают генерировать сигналы в тот момент, когда нет никаких реальных раздражителей. В пределе это выливается в симптоматику, которая называется шизофренией. К сожалению, шизофрения является весьма распространенным заболеванием: от 0,5 до 1% населения страдают этим заболеванием. В этом случае нужны препараты, ослабляющие активность дофаминовой системы. Такие препараты существуют, они относятся к группе нейролептиков и являются блокаторами дофаминовых рецепторов.
Рекомендуем по этой теме:
Молекулярные системы действия психотропных средств
У дофамина довольно много рецепторов, выделено пять основных типов. Если смотреть на разные отделы мозга, мы прежде всего обнаруживаем рецепторы D-2, тормозящие различные нервные процессы. И довольно много рецепторов D-1, то есть дофаминовых рецепторов первого типа, которые активируют различные нервные процессы. В некоторых нейросетях рецепторы D-1 и D-2 вставлены как конкурирующие блоки, рецепторы D-2 ограничивают активность D-1. Это очень хорошо наблюдается в базальных ганглиях. Если мы начинаем использовать антагонистов дофаминовых рецепторов, то степень выраженности их эффектов зависит от того, на какие рецепторы мы попадаем.
История нейролептиков начинается с вещества, которое называется аминазин. Аминазин — грубый нейролептик, воздействующий не только на все типы дофаминовых рецепторов, но и на рецепторы норадреналина. Тем не менее аминазин в истории психиатрии стал важнейшим препаратом, с помощью которого впервые удалось на фармакологическом уровне купировать и тяжелую шизофрению, и тяжелые маниакальные расстройства. В 1960-е годы стали создавать более избирательно действующие препараты, в основном блокирующие активность рецепторов D-2. Современные нейролептики являются именно блокаторами рецепторов D-2 разной степени эффективности, потому что более востребованы препараты более мягкого действия. К счастью, легкая шизофрения встречается чаще, чем тяжелая, даже с точки зрения фармакологического рынка гораздо важнее производить легкие нейролептики: они имеют гораздо более широкую сферу распространения.
Основной мишенью действия нейролептических препаратов оказывается кора больших полушарий и та часть базальных ганглиев, которая связана с эмоциями, потребностями, мотивацией. В базальных ганглиях есть две структуры: одна называется миндалина (она находится в глубине височных долей), а вторая структура — nucleus accumbens (переводится как ‘прилежащее ядро прозрачной перегородки’). Эти две структуры являются важнейшими мишенями для нейролептиков, а nucleus accumbens очень активно изучается как ключевой центр, связанный с генерацией положительных эмоций. У нас большинство информационных потоков, связанных с тем, что наш организм успешно выполнил какую-то деятельность: поел или избежал опасности, узнал что-то новое или успешно размножился, — идут через nucleus accumbens, и дальше сигналы от этой структуры, поднимаясь в кору больших полушарий, определяют процессы обучения и формирования памяти. Поэтому эта зона очень активно изучается, и дофамин там важнейший медиатор.
Если используются агонисты дофаминовых рецепторов, то можно получить активацию и процессов мышления, и центров положительных эмоций, в том числе nucleus accumbens. Известны подобного рода препараты, они относятся к группе психомоторных стимуляторов. Классическим психомоторным стимулятором является амфетамин — вещество, открытое еще в начале XX века, прошедшее сложную историю. Его пытались использовать как препарат, вызывающий похудание, и как психомоторный стимулятор, и как спортивный допинг. В настоящее время он является запрещенным наркотиком и одновременно иногда используется в клинике при тяжелых депрессиях. К этой же категории относится очень мощный и опасный наркотический препарат, который называется кокаин. Он тоже очень сильно увеличивает активность дофаминовой системы и очень быстро вызывает формирование привыкания и зависимости, серьезно меняя состояние нейронных сетей и особенно центров положительных эмоций, например nucleus accumbens.
Читайте также:


