Пнп с тремором что это
Тремор (дрожание) - непроизвольные насильственные ритмичные колебательные движения части тела вокруг фиксированной точки в пространстве, которые вызываются сокращениями групп мышц-антагонистов. Тремор преобладает в структуре непроизвольных движений человека и по локализации относится к гиперкинезам преимущественно стволового уровня. Тремор является полиэтиологическим синдромом и встречается в клинической практике врачей многих специальностей (неврологов, эндокринологов, психиатров и т.д.). Тремор имеет две основные характеристики: частота колебаний и их амплитуда, определяемая величиной смещения части тела вокруг фиксированной точки.
По частоте колебаний дрожание может быть условно разделено на 3 группы:
- низкочастотное (3-5 Гц),
- среднечастотное (5-8 Гц),
- высокочастотное (9-12 Гц).
По амплитуде дрожание делится на:
- низкоамплитудное,
- среднеамплитудное,
- высокоамплитудное.
Выделяют фокальный либо генерализованный тремор, при котором одновременно поражаются конечности, голова, нижняя челюсть, голосовые связки, язык. Подобные нарушения существенно ухудшают качество жизни и адаптацию этих пациентов в обществе.
В клинической работе невролога практическое значение имеет выделение следующих видов тремора: покоя, постурального и кинетического. Тремор покоя (статический тремор) имеет частоту 3-6 Гц и наиболее характерен для болезни Паркинсона или дегенеративных заболеваний ЦНС. Постуральный (антигравитационный) тремор характеризуется частотой 5-9 Гц, выявляется в положении с вытянутыми вперед руками и имеет место при синдроме отмены алкоголя, некоторых лекарственных препаратов, при обменных нарушениях, а также может быть психогенным или физиологическим. Кинетический тремор имеет частотную характеристику 3-10 Гц, подразделяется на тремор сокращения, проявляющийся при изометрическом напряжении мышц (при сжатии кисти в кулак) и интенционный тремор, возникающий при целенаправленном движении конечности (например, при выполнении пальценосовой пробы). Этот тип характерен для тремора Минора, поражения ствола мозга или мозжечка различного генеза (рассеянный склероз, опухоль, гематома). Вариантом кинетического тремора является task-specific tremor (тремор при выполнении определенного действия), появляющийся при выполнении точных мелких движений, таких как застегивание украшений, работа с маленькими деталями и т.п.
Клинические проявления тремора
Клинические проявления тремора полиморфны и встречаются при широком круге неврологических заболеваний. По этиологическому принципу виды тремора подразделяются на:
Физиологические: нормальный и усиленный тремор.
Патологические виды тремора:
- эссенциальный (наследственный и спорадический);
- паркинсонический;
- дистонический;
- мозжечковый (интенционное дрожание);
- тремор Холмса (среднего мозга или рубральный);
- невропатический;
- психогенный.
Физиологический тремор (асимптомное дрожание) встречается у любого здорового человека при волнении, характеризуется частотой 8-12 Гц в руках и менее чем 6,5 Гц в других частях тела. Усиленный физиологический тремор отличается от физиологического большей амплитудой и чаще встречается при гиперадренергических состояниях (эмоциональный стресс, эндокринные нарушения), во время приема ряда лекарственных препаратов или алкоголя. Особенностью данного вида тремора является его значительное уменьшение или полное исчезновение при назначении β-блокаторов.
Патологический тремор. Наиболее распространенной причиной патологического тремора является эссенциальный тремор Минора, частота и степень выраженности которого увеличивается с возрастом. Этот вид может быть как наследственным (аутосомно-доминантный тип наследования с вариабельной пенетрантностью) и, соответственно, проявляться в нескольких поколениях одной семьи, так и манифестироваться спорадически у членов одной семьи. Частота эссенциального тремора составляет 4-11 Гц и зависит от того, какой сегмент тела поражен. Проксимальные сегменты характеризуются низкими частотами, дистальные - более высокими. Наиболее часто поражается голова и/или кисти рук. Для данного вида тремора характерен постуральный и кинетический компонент. Тремор Минора может представлять самостоятельную нозологическую форму, реже - сопровождать различные нарушения движений, например паркинсонизм или фокальную дистонию.
Ортостатический тремор является редким расстройством движения. Характеризуется дрожанием ног в положении стоя и исчезает при ходьбе, сидении или в положении лежа. Отличительной особенностью данного вида тремора является его высокая частота: 14-16 Гц. В положении стоя у пациента может определяться подергивание четырехглавой мышцы бедра.
Дистонический тремор представляет собой дрожание части тела, в которой локализован дистонический синдром. Для данного вида тремора характерна нерегулярная амплитуда и вариабельная частота, часто - подверженность модулирующему влиянию позы.
При треморе Холмса (рубральном треморе) представлены все 3 основных типа дрожания, которые отличаются степенью выраженности. Данный тип возникает при повреждениях среднего мозга (инсульт, ЧМТ, опухоль или рассеянный склероз). Его частота составляет 2-5 Гц.
Мозжечковый (интенционный) тремор является кинетическим и проявляется при выполнении произвольного акта. Его развитие связано с нарушением корригирующего влияния мозжечковых систем на двигательный акт вследствие повреждений, локализующихся в латеральных мозжечковых ядрах или в верхней ножке мозжечка, либо в местах их соединений. При поражении срединных структур мозжечка развивается тремор в руках, голове и туловище. При клиническом осмотре выраженность тремора различается от небольших толчкообразных движений, до крупных, переходящих в мозжечковую хорею или асинергию.
Невропатический тремор имеет место при врожденных или приобретенных невропатиях и клинически напоминает эссенциальный тремор. Причиной дрожания является нарушение проприоцептивной чувствительности. Характерной чертой невропатического тремора является его усиление при выполнении задания (пальценосовой пробы и др.) с закрытыми глазами.
Психогенный тремор - наиболее сложный вид дрожания, поскольку требует исключения его органической природы. Данный вид может быть постуральным, а может проявляться в покое или при движении. Клинически психогенный тремор характеризуется внезапным началом, спонтанной ремиссией, стационарным течением и неклассифицируемыми видами тремора.
Диагностика тремора
Диагностика тремора основана на объективных тестах и инструментальных методах исследования. К широко известным объективным тестам относятся: рисование спирали, наливание воды из чаши, шкалы оценки тремора, тест лабиринта Гибсона. Инструментальные методы исследования включают позитронно-эмиссионную томографию, поверхностную электромиографию (ЭМГ), оптические методики и акселерометрию. Позитронно-эмиссионная томография позволяет с помощью меченых изотопов (F 18 , O 15 ) проследить за изменением уровня регионарного кровотока и оценить локализацию вовлечения нейронов. Поверхностная суммарная ЭМГ регистрирует запись залпов определенной частоты и амплитуды, которые чередуются с участками изолинии. Оптические методики основаны на использовании источника света и регистрирующего устройства.
Современным методом регистрации тремора является акселерометрия. Методика основана на использовании специальных датчиков - акселерометров, измеряющих линейное ускорение, характерное для всех движений (кроме случаев с постоянной скоростью). Получаемые сигналы с помощью аналогово-цифрового устройства преобразуются в цифровые и поступают в компьютер. Специальными программами производится их обработка, что позволяет построить графическую зависимость перемещения датчиков во времени, уточнить частотную и амплитудную характеристику движения.
Лечение тремора
Выделяют этиотропное, патогенетическое и симптоматическое лечение тремора. В современной клинической практике наиболее распространена симптоматическая терапия дрожания, выбор которой зависит от типа тремора.
Препаратами выбора коррекции кинетического тремора являются β-блокаторы, бензодиазепины или вальпроаты. Механизм воздействия β-блокаторов (анаприлин, пропранолол) на дрожание окончательно не изучен. Препарат назначают в начальной дозе 10 мг 3 раза в день, с постепенным повышением до максимальной дозы 240 мг/сут. По данным Koller W. C., пропранолол в дозе 160 мг/сут уменьшает амплитуду тремора на 50-70%. Среди недостатков лечения β-блокаторами - относительно высокая частота отмены лечения (в основном из-за возникновения повышенной утомляемости и брадикардии) и невозможность резкого прекращения их приема. Бензодиазепины (диазепам, клоназепам) воздействуют на тремор за счет своего противосудорожного и миорелаксирующего эффектов. Дозировка подбирается индивидуально и обычно составляет 4-6 мг/сут. Побочными эффектами бензодиазепинов являются головокружение, сонливость, возможное привыкание. Соли вальпроевой кислоты (производные натриевой и кальциевой соли) оказывают влияние на тремор посредством воздействия на обмен гамма-аминомасляной кислоты. Их суточная доза составляет 300-600 мг/сут. Побочные эффекты этих медикаментов - тошнота и диарея.
С целью влияния на тремор покоя применяют антихолинергические препараты, агонисты дофаминовых рецепторов, L-допа-содержащие препараты, амантадины. Антихолинергические препараты (тригексифенидил, бипериден) обладают центральным и периферическим холинолитическим эффектом, могут назначаться в дозировке 1-2 мг 3 раза в сутки. Применяются, прежде всего, у пациентов молодого и среднего возраста. В настоящее время циклодол редко используют в связи с его частыми побочными эффектами (сухость во рту, запоры, задержка мочеиспускания, психотические нарушения). Агонисты дофаминовых рецепторов (мирапекс, проноран, апоморфин) воздействуют на тремор путем прямой стимуляции специфических Д1, Д2, Д3 рецепторов, обеспечивают равномерный синтез и высвобождение дофамина, не индуцируют антиоксидантный стресс. Лечение начинают с малых доз с постепенным наращиванием дозы до 150 мг/сут. В последние годы начал применяться метод введения апоморфина с помощью особой помпы, эффективность которого сопоставима с нейрохирургическим вмешательством. L-допа-содержащие препараты (наком, мадопар, синдопа, синемет) представляют собой метаболические предшественники дофамина. Эффективность их воздействия на дрожание существенно меньше, чем на ригидность и акинезию. Средняя терапевтическая доза составляет 500-750 мг/сут. Увеличение дозы приводит к моторным флюктуациям и дискинезиям. Амантадины (ПК-Мерц, мидантан) с успехом применяются для лечения акинезии и ригидности у пациентов с болезнью Паркинсона и симптоматическим паркинсонизмом. Нам не встретилось работ о влиянии амантадинов на паркинсонический тремор. Поэтому в июне - ноябре 2006 г. на базе 2-го неврологического отделения 5-й городской клинической больницы г. Минска нами проведено клиническое исследование по оценке эффективности инфузионной формы ПК-Мерца на дрожание в комплексном лечении болезни Паркинсона.
На фоне проводимой терапии наряду с регрессом экстрапирамидной ригидности и гипокинезии у 3 пациентов (10%) достигнуто полное исчезновение постурального тремора и тремора покоя. Еще у 6 пациентов (20%) было отмечено исчезновение постурального дрожания и уменьшение тремора покоя. В 16 случаях (53,3%) - одновременное значительное уменьшение тремора покоя и постурального тремора (амплитуда дрожания уменьшилась более чем на 50% согласно данным акселерометрии). Влияния препарата на частоту паркинсонического дрожания во время лечения зафиксировано не было.
Результаты влияния препарата на амплитуду дрожания приведены на рисунке: до лечения амплитуда тремора покоя в исследуемой группе составила: медиана - 272 ед.; 25-й перцентиль - 112 ед.; 75-й перцентиль - 611 ед.; среднее отклонение - 641. После лечения амплитуда тремора достоверно уменьшилась: медиана - 73 ед.; 25-й перцентиль - 29 ед.; 75-й перцентиль - 149 ед.; среднее отклонение - 134 (p
Отсутствие эффекта от всех видов консервативного лечения во всем мире является показанием для нейрохирургического вмешательства. Паллидарная стимуляция и стимуляция субталямического ядра являются в настоящее время наиболее современными хирургическим вмешательствами для уменьшения тремора.
Таким образом, тремор является наиболее частым проявлением гиперкинетического синдрома, обладает существенным клиническим полиморфизмом, затрудняющим его диагностику. Существенную пользу в распознавании тремора приносят инструментальные методы. Одним из современных методов регистрации дрожания является акселерометрия. Подход медика к лечению тремора должен быть дифференцированным, индивидуальным и ступенчатым. В терапии паркинсонического дрожания показано применение инфузионной формы препарата ПК-Мерц. При отсутствии эффекта прибегают к политерапии или нейрохирургическому вмешательству.

Тремор представляет собой дрожание того или иного участка тела. В основе этого состояния находится сокращение и расслабление мышц, которое сменяет друг друга.
Дрожание конечностей может встречаться в любом возрасте, но чаще всего это происходит у пожилых пациентов.
При этом наблюдается определенная закономерность – чем старше пациент, тем быстрее прогрессирует заболевание и тем сильнее становится дрожание.
Основные виды тремора
Тремор может наблюдаться у человека и в норме. Однако он практически не заметен окружающим в отличие от патологического дрожания.
Таким образом, тремор может быть разделен на патологический и физиологический.
Другими классификационными подходами в отношении тремора являются следующие:
- По быстроте и ритмичности мышечных сокращений. Быстрое дрожание происходит с частотой от 6 до 12 Герц. При медленном треморе колебания происходят с частотой от 3 до 5 Герц.
- По локализации в той или иной мышечной группе – может быть тремор мышц лица, тремор конечностей и т.д.
- По степени тяжести. Легкое дрожание не нарушает привычный образ жизни человека, при среднетяжелом наблюдается некоторое ограничение в самообслуживании, а при тяжелом – человек не может обойтись без посторонней помощи.
Также врачам очень важно различать активный и пассивный тремор. Активный возникает в тот момент, когда мышца находится в сокращенном состоянии.
О пассивном дрожании говорят, если сокращение и расслабление мышцы происходит на фоне ее полного покоя. Интенционный тремор может быть как пассивным, так и активным.
Особенности интенционного дрожания
Особенностью тремора является возникновение его в момент целенаправленного движения руки к тому или иному 
предмету. Обычно он является признаком поражения мозжечка или нервных путей, имеющих к нему связь.
Такая ситуация наблюдается при рассеянном склерозе.
Другими причинами интеционного тремора могут быть:
- алкоголизм;
- инсульт в мозжечок или преходящие нарушения кровообращения в этом отделе мозга;
- отравление организма различными токсичными веществами, в том числе и наркотиками.
Интересен факт о влиянии алкоголя на выраженность тремора.
В начальном периоде употребления алкоголя дрожание становится менее выраженным, и пациенты начинают тяготеть к спиртному. Со временем это приводит к усилению тремора и развитию алкогольной зависимости.
На этом фоне наблюдается быстрое прогрессирование болезни.

Чем характерна джексоновская эпилепсия — что отличает этот вид эпилепсии от других видов заболевания узнайте в нашей статье.
Своевременно оказанная первая помощь при приступе эпилепсии может спасти человеку жизнь. Как нужно вести себя в такой ситуации?
Обойма осложнений — обычное дело
Со временем интенционный тремор может привести к развитию целого ряда осложнений.
Наиболее часто встречаются такие, как:
- Нарушенная адаптация в социуме, связанная с комплексами о собственной неполноценности.
- Невозможность выполнять определенную работу, что накладывает ограничения в профессиональной деятельности. Например, пациенты, страдающие тремором, не могут быть ювелирами, хирургами.
- Нарушения речи из-за трудностей, связанных с поражением лицевых мышц и языкодвигательных.
- Проблема в психоэмоциональной сфере, связанные с нарушением способности выполнять привычные действия, например, бритье, чистка зубов, причесывание, еда ложкой или вилкой и т.д.
Симптомы и диагностика синдрома
Клиническими признаками интенционного тремора являются:
- появление дрожания в покое;
![]()
- усиление дрожания наблюдается на фоне какой-либо активности (например, движение руки к предмету);
- появление дрожи при желании охранить ту или иную позу тела;
- движения конечностей грубые и широкие;
- в сравнении с эссенциальным тремором движения более медленные;
- может наблюдаться дрожание только туловища, при этом голова и/или конечности не дрожат;
- у некоторых пациентов тремор может усиливаться в вертикальном положении тела, а прекращаться при занятии горизонтального положения.
Уточнить диагноз помогают специальные методы исследования. Они направлены на выявление причины этого патологического состояния.
Поэтому врач рекомендует следующие диагностические тесты:
- электроэнцефалография;
- компьютерная томография головного мозга;
- исследование уровня гормонов щитовидной железы (повышенный уровень часто наблюдается при эссенциальном треморе);
- определение уровня серотонина в крови, который изменяется при болезни Паркинсона.
В процессе диагностики врач также выясняет, не было ли расстройств у ближайших родственников.
Интенционное дрожание может иметь генетическую природу, в основе своего развития. Поэтому у таких пациентов обязательно определяют, нет ли у них отягощенной наследственности.
Что нужно знать о лечении расстройства

Если интенционный тремор не доставляет человеку дискомфорта и в мозжечке не выявлена какая-либо патология, то лечение можно и не приводить.
Некоторым пациентам требуется проведение симптоматической терапии, которая позволяет уменьшить выраженность дрожания.
Полностью избавиться от этого неприятного симптома невозможно, проводя консервативную терапию. Для улучшения качества жизни пациента назначаются препараты из группы бета-блокаторов.
Хирургическое лечение показано, когда в мозжечке диагностируется опухоль или киста, нарушающая его функционирование. В этом случае после проведенной операции дрожания не наблюдается.
Вместо вывода
Можно сделать следующие выводы:
- интенционный тремор является признаком поражения мозжечка тем или иным патологическим процессом;
- дрожание начинается в покое, а усиливается при движении руки к той или иной цели;
- движения размашистые, которые хорошо заметны;
- диагностический поиск в обязательном порядке должен исключить опухолевое образование, локализующееся в мозжечке;
- консервативное лечение назначает только врач и для этой цели использует бета-блокаторы, хирургическое вмешательство проводится только при опухолях.
*Импакт фактор за 2018 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.
Читайте в новом номере
ММА имени И.М. Сеченова
Клиническая картина

Болезнь Паркинсона. На рисунке А показан участок мозга здорового человека с хорошо пигментированным черным веществом. На рисунке В - участок мозга пациента, страдающего болезнью Паркинсона. Заметно отсутствие пигментации черного вещества.
П – это синдром, который может встречаться в рамках разных заболеваний. Наиболее часто причиной П является идиопатический паркинсонизм, или болезнь Паркинсона (БП). П часто наблюдается в рамках других идиопатических дегенеративных заболеваний нервной системы. Последние часто называют паркинсонизмом–плюс. К этой группе относятся мультисистемная атрофия, прогрессирующий надъядерный паралич, болезнь диффузных телец Леви, кортико-базальная дегенерация. Нередко встречается симптоматический П (не связанный с первичным дегенеративным заболеванием нервной системы). К нему относят лекарственный, сосудистый, посттравматический, постэнцефалитический, токсический П, П при опухолях головного мозга и гидроцефалии. П характеризует также клиническую картину некоторых наследственных дегенеративных заболеваний ЦНС. К их числу относятся гепатолентикулярная дегенерация (болезнь Вильсона-Коновалова), спиноцеребеллярные атаксии, семейная кальцификация базальных ганглиев, болезнь Гентингтона и др. Таким образом, синдром П не является синонимом БП.
Диагноз и дифференциальный диагноз
Эссенциальный тремор
На первом этапе диагностической работы необходимо убедиться, что у больного действительно имеется синдром П. Наиболее часто за истинный П ошибочно принимают эссенциальный тремор (ЭТ) и своеобразные изменения походки, связанные с сосудистой патологией головного мозга. Таким пациентам очень часто неправильно ставят диагноз БП.
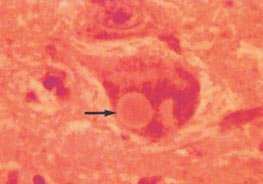
Тельца Леви при болезни Паркинсона. В цитоплазме нейрона определяется эозинофильное ядро окруженное неокрашенной зоной.
Последние, как правило, выявляют множественные мелкие очаги сосудистого происхождения (лакуны) в области базальных ганглиев и/или изменения белого вещества полушарий головного мозга (лейкоареоз). Следует иметь в виду, что схожая клиническая картина может возникать иногда при нормотензивной гидроцефалии и реже – при опухолевом поражении головного мозга. При нормотензивной гидроцефалии наряду с нарушением ходьбы по типу описанного выше имеют место деменция и расстройство функции тазовых органов (эту триаду симптомов называют триадой Хакима–Адамса). МРТ головы, как правило, обнаруживает резко расширенные боковые желудочки.
Болезнь Паркинсона
Диагноз БП – это клинический диагноз. Параклинические методы исследования обычно выявляют неспецифические изменения. Нередко у больных с классической БП в головном мозге имеются сосудистые изменения. Это, однако, ни в коем случае не является свидетельством сосудистого генеза болезни. Просто у большинства пожилых людей, в том числе практически здоровых, подобные изменения могут иметь место. Тем не менее, в некоторых случаях на БП наслаивается атеросклеротический псевдопаркинсонизм, что может быть причиной необычной для БП походки и ранних постуральных нарушений.
Лекарственный паркинсонизм
Лекарственный П может быть обусловлен препаратами, которые воздействуют на пресинаптические дофаминовые нейроны черной субстанции, истощая запасы дофамина в них (например, резерпин) или, наиболее часто, нейролептиками, которые блокируют постсинаптические дофаминовые рецепторы, такими как производные фенотиазина (хлорпромазин), бутирофеноны (галоперидол), тиоксантины (флупентиксол) и бензамиды (сульпирид). Эти препараты часто применяются при психических заболеваниях. Также П может быть вызван прохлорперазином (используется при рвоте, головокружении и неустойчивости), метоклопрамидом (применяется при заболеваниях желудочно-кишечного тракта, для купирования тошноты и рвоты). П может быть обусловлен также циннаризином, который является атипичным блокатором кальциевых каналов (применяется при вестибулярных расстройствах). Комбинация нейролептиков и антидепрессантов также может быть причиной П.
В психиатрических лечебницах лекарственный П встречается часто. Гипомимия и ахейрокинез – настолько обычное явление среди этого контингента больных, что психиатры часто даже не обращают на них внимание. Тремор встречается менее часто, но может иметь вид классического паркинсонического дрожания. Более того, лекарственный П может быть асимметричным, подобно БП, и нередко совершенно не отличим от БП. Одним из признаков, по которому следует заподозрить лекарственный П, является наличие наряду с акинетико-ригидным синдромом насильственных движений в виде, например, оро-мандибулярной дискинезии (непроизвольные жевательные и/или сосательные движения) или дистонических явлений (спастической кривошеи, окулогирных кризов), стереотипий, акатизии (неусидчивость). Нередко тяжелый лекарственный П сопровождается выраженной дизартрией и дисфагией. Индивидуальная чувствительность к дофаминблокирующим препаратам очень разнообразна. Некоторые пациенты без каких-либо проблем переносят длительное лечение большими дозами этих веществ, тогда как у других побочные явления развиваются уже на малых дозах. Чаще, однако, признаки лекарственного П возникают при приеме больших доз нейролептиков. Лекарственный П обычно развивается постепенно в течение дней или недель. У большинства больных первые признаки появляются через 3 нед после начала лечения. Наиболее часто встречающиеся дебютные признаки – гипомимия и недостаточное раскачивание рук во время ходьбы.
Течение лекарственного П может быть различным. В большинстве случаев он постепенно, в течение нескольких недель, а иногда и дней, проходит после прекращения приема вызвавшего его препарата. Тем не менее нередки случаи, когда П длится в течение месяцев, иногда почти год. Такая ситуация наблюдается при применении нейролептических препаратов, способных к депонированию. В редких случаях лекарственный П не проходит и продолжает прогрессировать, несмотря на прекращение приема вызвавшего его агента. Подобные случаи чаще встречаются среди пожилых людей. Считается, что в таких случаях прогрессирует не сам по себе лекарственный П, а начинает развиваться БП.
Мультисистемная атрофия
Мультисистемная атрофия (МСА) – это спорадическое заболевание, возникающее у взрослых лиц, при котором в отличие от БП дегенерации подвергается не только нигро-стриарная система, но также множество других образований ЦНС, включая мозжечок и его связи, пирамидные пути и образования вегетативной нервной системы (отсюда и происходит название болезни). Соответственно клинически МСА характеризуется сочетанием П, мозжечковых нарушений, пирамидных расстройств и прогрессирующей вегетативной недостаточности (ПВН). П при МСА обусловлен не только поражением клеток черной субстанции, что вызывает дефицит дофамина, но также дегенерацией тех постсинаптических рецепторов, с которыми должен взаимодействовать дофамин.
В клинической картине МСА может преобладать та или иная симптоматика. Те случаи, при которых на первый план выступает П, обозначают термином нигро-стриальная дегенерация (СНД); если в клинической картине ведущим является мозжечковый синдром, это состояние называют оливо-понто-церебеллярной атрофией (ОПЦА); случаи, когда ядром клинической картины является ПВН, обозначают эпонимическим названием – синдром Шая–Дрейджера (СШД).
Несмотря на все различия, нередки ситуации, когда МСА невозможно отличить от БП. В таких случаях следует в основном ориентироваться на эффект препаратов леводопы. При БП эти препараты оказывают драматический положительный эффект, тогда как при МСА этот эффект не столь выражен, кратковременен, а нередко отсутствует совсем. Это обусловлено поражением постсинаптических рецепторов, с которыми должна взаимодействовать леводопа.
Признаки, при наличии которых у больных с П следует подумать об МСА, следующие: быстрое прогрессирование симптоматики; рано развившиеся нарушения равновесия и падения; отсутствие улучшения при лечении препаратами леводопы или недостаточный эффект этих препаратов; ПВН; пирамидные и/или мозжечковые знаки; похолодание, зябкость конечностей; контрактуры; диспропорциональный антеколлис; выраженная дисфония, дисфагия или дизартрия; респираторный стридор; нерегулярный тремор или миоклонии.
Прогрессирующий надъядерный паралич
Болезнь диффузных телец Леви
В последнее время стали выделять новую нозологическую форму, протекающую с синдромом П – болезнь диффузных телец Леви (БДТЛ). Тельца Леви – это внутриклеточные эозинофильные цитоплазматические включения, которые обнаруживаются в клетках черного вещества при БП и считаются маркером этой болезни. При БДТЛ они встречаются не только в черном веществе, но в большом количестве широко диссеминированы по всему головному мозгу. Диагноз БДТЛ – патоморфологический диагноз. Клинически это заболевание характеризуется П, который обычно хорошо лечится препаратами леводопы, наряду с деменцией с выраженными зрительными галлюцинациями. Типичным является также флуктуация выраженности расстройств высших психических функций – в основном за счет изменения способности концентрации внимания.
Гепатолентикулярная дегенерация (болезнь Вильсона-Коновалова) и другие заболевания
Существует несколько более редких причин истинного или псевдопаркинсонизма. Одна из них, о которой следует всегда вспомнить при наличии П у людей моложе 45 лет (в том числе у детей), это гепатолентикулярная дегенерация, или болезнь Вильсона-Коновалова. Это наследственное заболевание, при котором отмечается нарушение метаболизма меди в организме из-за недостаточности фермента церулоплазмина. В результате медь в избыточном количестве откладывается в печени, базальных ганглиях и вокруг радужной оболочки глаза. Болезнь Вильсона-Коновалова следует подозревать не только при наличии П у молодых людей, но и при возникновении у них других признаков поражения экстрапирамидной системы (например, дистонии) или психических расстройств. Диагностика основана на обнаружении с помощью щелевой лампы отложения меди вокруг радужки – кольцо Кайзера–Флейшера. Последнее на стадии неврологических проявлений имеет место у 98% больных. Диагностическое значение имеет также исследование экскреции меди с мочой и концентрации церулоплазмина в крови. Последнее, однако, в отсутствие кольца Кайзера–Флейшера и нормальной экскреции меди не имеет диагностической значимости. Если ситуация продолжает оставаться неясной, проводится биопсия печени или генетическое тестирование. Болезнь Вильсона-Коновалова довольно успешно лечится с помощью D-пеницилламина и препаратов цинка в сочетании с диетой.
Токсический П может иметь место при интоксикации марганцем. Нередко встречается П, вызванный токсином МФТП (1-метил-4-фенил- 1, 2, 3, 6-тетрагидропиридин), так как оно избирательно поражает черную субстанцию, вызывая гибель дофаминовых нейронов. Схожий с этим веществом токсин вырабатывается при кустарном приготовлении некоторых наркотических веществ, поэтому П нередко наблюдается среди молодых людей, страдающих наркоманией. Наряду с П при этом могут отмечаться пирамидные и псевдобульбарные симптомы.
П встречается при энцефалопатии боксеров. Считается, что в таком случае этиологическую роль играют регулярно получаемые множественные черепно-мозговые травмы. Следует помнить, что энцефалопатия боксеров – практически единственная ситуация, когда черепно-мозговые травмы играют роль в развитии П. В целом у людей, не занимающихся боксом, наличию черепно-мозговой трамы в анамнезе (одной или нескольких) не придается этиологическое значение.
П иногда может иметь место при хорее Гентингтона, которое обычно протекает с выраженными гиперкинезами. Это наследственное заболевание обычно дебютирует на четвертом десятилетии жизни, однако встречаются случаи и более раннего начала. Обычно с акинетико-ригидным синдромом протекает так называемая ювенильная форма хореи Гентингтона (форма Вестфаля). Встречаются также семейные случаи П, в том числе ювенильного. Поэтому у всех больных, имеющих синдром П, сбор наследственного анамнеза имеет большое значение.
Акинезия и ригидность могут иногда наблюдаться при болезни Альцгеймера, Пика, при которых ядром клинической картины является прогрессирующая деменция. При болезни Альцгеймера в первую очередь страдает память, а при болезни Пика на первый план выступает распад личности. При этих заболеваниях П чаще проявляется умеренной акинезией, ригидность выражена меньше, а паркинсонический тремор практически никогда не наблюдается.
Постэнцефалитический П в наше время практически не встречается. Много случаев наблюдалось после пандемии летаргического энцефалита в начале XX столетия. С тех пор в литературе описано только несколько случаев.
Особая эндемическая форма П наблюдается на острове Гуам и в некоторых других местах восточной части Тихого океана. В этих местах отмечается много случаев П в сочетании с амиотрофиями и деменцией (гуамский комплекс паркинсонизм – деменция). Патоморфологически мозг этих больных выглядит, как мозг больных ПНП. Одинаковыми являются также гистологические маркеры.
Читайте также:



