Поражения нервной системы при внутриутробных инфекций
Клинические проявления внутриутробных инфекций полиморфны и зависят не столько от этиологии/сколько от локализации и тяжести процесса. Наиболее типичны задержка внутриутробного развития, гепатомегалия, спленомегалия, желтуха, сыпь, синдром дыхательных расстройств, сердечнососудистая недостаточность и неврологические нарушения. Тяжесть клинических проявлений в большей мере зависит от того, на каких сроках гестации произошло инфицирование.
При развитии инфекции во второй половине беременности заболевание у новорожденного клинически манифестирует как генерализованная инфекция или как поражение отдельных органов. У всех наблюдавшихся больных, госпитализированных в Центр детской гепатогии с перинатальной патологией гепато-билиарной системы, были выражены и поражения центральной нервной системы, по поводу которых они получали специальное обследование и лечение невропатолога.
Последствия перинатальных инфекционных заболеваний ЦНС в плане этиологии и патогенетической основы рассматриваются как:
1) поражения вследствие перенесенного (врожденного) энцефалита, менингита, менингоэнцефалита (TORCH-синдром — цитомегаловирусная инфекция, герпетическая инфекция, токсоплазмоз, врожденная краснуха, ECHO — вирусы и другие, сифилис);
2) поражения ЦНС вследствие перенесенного неонатального сепсиса (менингит, менингоэнцефалит, вентрикулит, энцефалит).
Варианты клинических форм в первой группе — перинатальное постинфекционное (врожденное) органическое поражение мозга с различными клиническими синдромами, исходы которых могут варьировать от легких до тяжелых форм умственной отсталости, ДЦП, симптоматических резистентных эпилепсии. Варианты клинических форм во второй группе — постинфекционная
3) энцефалопатия или постинфекционное поражение ЦНС, проявляющиеся клиническими синдромами гидроцефалии, гиперактивного поведения, нарушений (задержки) моторного развития, очаговых нарушений (парезы и параличи), тяжелых нарушений моторного развития (формирующиеся и сформированные ДЦП) и другими. Исходы поражений ЦНС зависят от ранней диагностики и определяются своевременностью адекватной терапии, могут варьировать от легких функциональных до тяжелых психоневрологигеских нарушений.
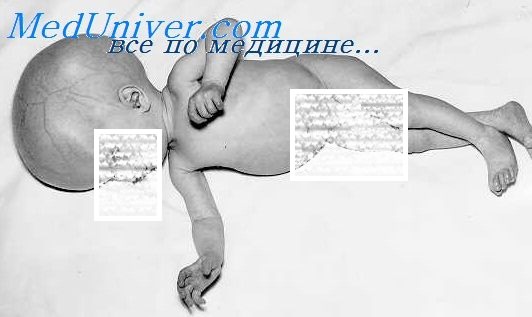
Новорожденный с врожденным токсоплазмозом
Целью исследований К. Е. Скляр с соавторами было выявление клинико-патогенетических закономерностей формирования врожденных пороков развития при внутриутробной инфекции у новорожденных. Проведено обследование 86 новорожденных с врожденными пороками развития различной локализации (у 50 % — врожденные пороки сердца) и клиническими признаками внутриутробной инфекции. Положительные результаты ПЦР получены у 43 (53 %) детей, в том числе РНК краснухи — у 36, ДНК токсоплазмоза — у 2, ДНК хламидий и вируса простого герпеса — в двух случаях, смешанная инфекция — у трех.
Анализ анамнестических данных и клинического течения заболевания не позволил авторам выделить каких-либо симптомов, соответствующих этиологии инфекции. У 30 (34,9%) оперативное лечение проведено в периоде новорожденности, из них — у 8 (9,3 %) в первые сутки после рождения. При морфологическом исследовании интраоперационно полученных биоптатов выявлены нарушения гистоархитектоники, склеротические и дистрофические явления, признаки нарушения локального кровообращения. Развитие указанных процессов в органах, по всей видимости, отражает исход инфекционного процесса.
По мнению авторов, именно склеротические процессы в аномальных тканях могут оказывать влияние на дальнейшее развитие детей и проявляться в различных формах хронических состояний, в том числе хронического гепатита и атрезии желчевыводящих путей при поражении пегени.
Желтуха и поражение печени наряду с поражением центральной нервной системы — ведущие клинические признаки большинства перинатальных инфекций.
В подтверждении диагноза и выяснении этиологии поражения пегени у новорожденных велика ответственность спектра, кагества проведения и клинического толкования результатов лабораторных исследований. Характеристика диагностических методов внутриутробной инфекции, применяемых в повседневной практике, предполагает определение титра специфических антител IgG в динамике (если он не снижается в возрасте от 6 до 12 недель, диагностируется врожденная инфекция). В 6 месяцев титр пассивно приобретенных от матери антител должен быть не выше 1:8.
Однако диагностика иммунохимическими методами у беременных и новорожденных может быть затруднена из-за недостаточной выработки специфических маркеров острой инфекции — антител класса IgM, трансплацентарной передачи антител класса IgG, низкого уровня продукции антигенов. В связи с этим клиническую значимость приобретает метод полимеразной цепной реакции.
Диагностика предполагает использование методов этиологической расшифровки с помощью генодиагностики. В то же время выявление ДНК вируса и тем более микоплазм и хламидий не может служить основанием для верификации этиологии инфекции и назначения лечения. Е. М. Малковой с соавторами из 117 новорожденных с признаками ВУИ у 112 обнаружены ДНК 26 возбудителей. Отмечено значительное количество вирусно-вирусных, микоплазменно-вирусных, вирусно-вирусно-микоплазменных, вирусно-хламидийных и прочих ассоциаций, составивших 22,1% среди положительных результатов исследований.
Клиническая картина не имела специфических признаков, была выраженной дыхательная недостаточность с развитием пневмонии, раннее и затяжное тегение желтухи, неврологические нарушения. Развитие фетального гепатита преобладало при сочетанных инфекциях. Наиболее тяжелое состояние отмечалось у детей при положительных результатах ПЦР сразу в нескольких биоматериалах. Необходимость терапии латентных форм заболеваний у новорожденных при детекции ДНК возбудителей определяется способностью многих из них длительно сохраняться в условиях иммунокомпетентного организма (персистировать с сохранением патогенных свойств).
При изменении иммунного статуса происходит быстрое восстановление вирулентности, которое становится основой рецидивирующего характера хронических инфекций и возможной инвалидизации ребенка. Однако, по данным авторов, результаты ПЦР-иследований у беременных женщин и их детей совпали только в 33,3 % слугаев, поэтому их трактовка, с нашей тогки зрения, должна быть осторожной.

Внутриутробные инфекции – группа заболеваний плода и новорожденного, развивающихся вследствие заражения в дородовом периоде или в родах. Внутриутробные инфекции могут приводить к гибели плода, самопроизвольному аборту, задержке внутриутробного развития, преждевременным родам, формированию врожденных пороков, поражению внутренних органов и ЦНС. Методы диагностики внутриутробных инфекций включают микроскопические, культуральные, иммуноферментные, молекулярно-биологические исследования. Лечение внутриутробных инфекций проводится с использованием иммуноглобулинов, иммуномодуляторов, противовирусных, антибактериальных препаратов.

- Причины внутриутробных инфекций
- Классификация
- Симптомы внутриутробных инфекций
- Врождённый токсоплазмоз
- Врождённая краснуха
- Врождённая цитомегалия
- Врождённая герпетическая инфекция
- Диагностика
- Лечение внутриутробных инфекций
- Прогноз и профилактика
- Цены на лечение
Общие сведения
Внутриутробные инфекции – патологические процессы и заболевания, обусловленные антенатальным и интранатальным инфицированием плода. Истинная распространенность внутриутробных инфекций не установлена, однако, согласно обобщенным данным, с врожденными инфекциями рождается не менее 10% новорожденных. Актуальность проблемы внутриутробных инфекций в педиатрии обусловлена высокими репродуктивными потерями, ранней неонатальной заболеваемостью, приводящей к инвалидизации и постнатальной гибели детей. Вопросы профилактики внутриутробных инфекций лежат в плоскости рассмотрения акушерства и гинекологии, неонатологии, педиатрии.

Причины внутриутробных инфекций
Внутриутробные инфекции развиваются в результате инфицирования плода в дородовом периоде или непосредственно во время родов. Обычно источником внутриутробной инфекции для ребенка выступает мать, т. е. имеет место вертикальный механизм передачи, который в антенатальном периоде реализуется трансплацентарным или восходящим (через инфицированные околоплодные воды) путями, а в интранатальном - аспирационным или контактным путями.
Реже происходит ятрогенное инфицирование плода в период беременности при проведении женщине инвазивной пренатальной диагностики (амниоцентеза, кордоцентеза, биопсии ворсин хориона), введении плоду препаратов крови через сосуды пуповины (плазмы, эритроцитарной массы, иммуноглобулинов) и т. д.
В антенатальном периоде инфицирование плода обычно связано с вирусными агентами (вирусами краснухи, герпеса, цитомегалии, гепатита В и С, Коксаки, ВИЧ) и внутриклеточными возбудителями (токсоплазмоза, микоплазмоза).
В интранатальном периоде чаще происходит микробная контаминация, характер и степень которой зависит от микробного пейзажа родовых путей матери. Среди бактериальных агентов наиболее распространены энтеробактерии, стрептококки группы В, гонококки, синегнойная палочки, протей, клебсиелла и др. Плацентарный барьер непроницаем для большинства бактерий и простейших, однако при повреждении плаценты и развитии фетоплацентарной недостаточности, может произойти антенатальное микробное инфицирование (например, возбудителем сифилиса). Кроме этого, не исключается и интранатальное вирусное заражение.
Факторами возникновения внутриутробных инфекций служат отягощенный акушерско-гинекологический анамнез матери (неспецифические кольпиты, эндоцервициты, ЗППП, сальпингофориты), неблагополучное течение беременности (угроза прерывания, гестозы, преждевременная отслойка плаценты) и инфекционная заболеваемость беременной. Риск развития манифестной формы внутриутробной инфекции существенно выше у недоношенных детей и в том случае, когда женщина инфицируется первично во время беременности.
На тяжесть клинических проявлений внутриутробной инфекции влияют сроки инфицирования и вид возбудителя. Так, если инфицирование происходит в первые 8-10 недель эмбриогенеза, беременность обычно заканчивается самопроизвольным выкидышем. Внутриутробные инфекции, возникшие в раннем фетальном периоде (до 12 недели гестации), могут приводить к мертворождению или формированию грубых пороков развития. Внутриутробное инфицирование плода во II и III триместре беременности проявляется поражением отдельных органов (миокардитом, гепатитом, менингитом, менингоэнцефалитом) либо генерализованной инфекцией.
Известно, что тяжесть проявлений инфекционного процесса у беременной и у плода может не совпадать. Бессимптомное или малосимптомное течение инфекции и у матери может вызвать тяжелые поражения плода, вплоть до его гибели. Это связано с повышенным тропизмом вирусных и микробных возбудителей к эмбриональным тканям, преимущественно ЦНС, сердца, органа зрения.
Классификация
Этиологическая структура внутриутробных инфекций предполагает их деление на:
- вирусные (вирусный гепатит, герпес, краснуха, ОРВИ, цитомегалия, эпидемический паротит, энтеровирусная инфекция)
- бактериальные (туберкулез, сифилис, листериоз, сепсис)
- паразитарные и грибковые (микоплазмоз, токсоплазмоз, хламидиоз, кандидоз и др.)
Для обозначения группы наиболее распространенных внутриутробных инфекций используется аббревиатура TORCH-синдром, объединяющий токсоплазмоз (toxoplasmosis), краснуху (rubella), цитомегалию (cytomegalovirus), герпес (herpes simplex). Буквой О (other) обозначаются другие инфекции, в числе которых - вирусные гепатиты, ВИЧ-инфекция, ветряная оспа, листериоз, микоплазмоз, сифилис, хламидиоз и др.).
Симптомы внутриутробных инфекций
Наличие внутриутробной инфекции у новорожденного может быть заподозрено уже во время родов. В пользу внутриутробного инфицирования может свидетельствовать излитие мутных околоплодных вод, загрязненных меконием и имеющих неприятный запах, состояние плаценты (полнокровие, микротробозы, микронекрозы). Дети с внутриутробной инфекцией часто рождаются в состоянии асфиксии, с пренатальной гипотрофией, увеличенной печенью, пороками развития или стигмами дисэмбриогенеза, микроцефалией, гидроцефалией. С первых дней жизни у них отмечается желтуха, элементы пиодермии, розеолезных или везикулезных высыпаний на коже, лихорадка, судорожный синдром, респиратрные и кардиоваскулярные расстройства.
Ранний неонатальный период при внутриутробных инфекциях нередко отягощается интерстициальной пневмонией, омфалитом, миокардитом или кардитом, анемией, кератоконъюнктивитом, хориоретинитом, геморрагическим синдромом и др. При инструментальном обследовании у новорожденных могут обнаруживаться врожденная катаракта, глаукома, врожденные пороки сердца, кисты и кальцификаты мозга.
В перинатальном периоде у ребенка отмечаются частые и обильные срыгивания, мышечная гипотония, синдром угнетения ЦНС, серый цвет кожных покровов. В поздние сроки при длительном инкубационном периоде внутриутробной инфекции возможно развитие поздних менингитов, энцефалитов, остеомиелита.
Рассмотрим проявления основных внутриутробных инфекций, составляющих TORCH-синдром.
Внутриутробное инфицирование одноклеточным протозойным паразитом Toxoplasma Gondii приводит к тяжелым поражениям плода – задержке развития, врожденным порокам развития мозга, глаз, сердца, скелета.
После рождения в остром периоде внутриутробная инфекция проявляется лихорадкой, желтухой, отечным синдромом, экзантемой, геморрагиями, диареей, судорогами, гепатоспленомегалией, миокардитом, нефритом, пневмонией. При подостром течении доминирую признаки менингита или энцефалита. При хронической персистенции развивается гидроцефалия с микроцефалией, иридоциклит, косоглазие, атрофия зрительных нервов. Иногда встречаются моносимптомные и латентные формы внутриутробной инфекции.
К числу поздних осложнений врожденного токсоплазмоза относятся олигофрения, эпилепсия, слепота.
Внутриутробная инфекция возникает из-за заболевания краснухой при беременности. Вероятность и последствия инфицирования плода зависят от гестационного срока: в первые 8 недель риск достигает 80%; последствиями внутриутробной инфекции могут служить самопроизвольное прерывание беременности, эмбрио- и фетопатии. Во II триместре риск внутриутробного инфицирования составляет 10-20%, в III – 3-8%.
Дети с внутриутробной инфекцией обычно рождаются недоношенными или с низкой массой тела. Для периода новорожденности характерна геморрагическая сыпь, длительная желтуха.
Классические проявления врожденной краснухи представлены триадой Грега: поражением глаз (микрофтальмией, катарактой, глаукомой, хориоретинитом), ВПС (открытым артериальным протоком, ДМПП, ДМЖП, стенозом легочной артерии), поражением слухового нерва (сенсоневральной глухотой). В случае развития внутриутробной инфекции во второй половине беременности у ребенка обычно имеется ретинопатия и глухота.
Кроме основных проявлений врожденной краснухи, у ребенка могут выявляться и другие аномалии: микроцефалия, гидроцефалия, расщелины нёба, гепатит, гепатоспленомегалия, пороки развития мочеполовой системы и скелета. В дальнейшем внутриутробная инфекция напоминает о себе отставанием ребенка в физическом развитии, ЗПР или умственной отсталостью.
Внутриутробное заражение цитомегаловирусной инфекцией может приводить к локальному или генерализованному поражению многих органов, иммунодефициту, гнойно-септическим осложнениям. Врожденные дефекты развития обычно включают микроцефалию, микрогирию, микрофтальмию, ретинопатию, катаракту, ВПС и др. Неонатальный период врожденной цитомегалии осложняется желтухой, геморрагическим синдромом, двусторонней пневмонией, интерстициальным нефритом, анемией.
К отдаленным последствиям внутриутробной инфекции относятся слепота, нейросенсорная глухота, энцефалопатия, цирроз печени, пневмосклероз.
Внутриутробная герпес-инфекция может протекать в генерализованной (50%), неврологической (20%), слизисто-кожной форме (20%).
Генерализованная внутриутробная врожденная герпетическая инфекция протекает с выраженным токсикозом, респираторным дистресс-синдромом, гепатомегалией, желтухой, пневмонией, тромбоцитопенией, геморрагическим синдромом. Неврологическая форма врожденного герпеса клинически проявляется энцефалитом и менингоэнцефалитом. Внутриутробная герпес-инфекция с развитием кожного синдрома сопровождается появлением везикулярной сыпи на кожных покровах и слизистых оболочках, в т. ч. внутренних органов. При наслоении бактериальной инфекции развивается сепсис новорожденных.
Внутриутробная герпес-инфекция у ребенка может приводить к формированию пороков развития - микроцефалии, ретинопатии, гипоплазии конечностей (кортикальной карликовости). В числе поздних осложнений врожденного герпеса - энцефалопатия, глухота, слепота, задержка психомоторного развития.
Диагностика
В настоящее время актуальной задачей является пренатальная диагностика внутриутробных инфекций. С этой целью на ранних сроках беременности проводится микроскопия мазка, бактериологический посев из влагалища на флору, ПЦР-исследование соскоба, обследование на TORCH-комплекс. Беременным из группы высокого риска по развитию внутриутробной инфекции показана инвазивная пренатальная диагностика (аспирация ворсин хориона, амниоцентез с исследованием амниотической жидкости, кордоцентез с исследованием пуповинной крови).
Возможно выявление эхографических маркеров внутриутробных инфекций с помощью акушерского УЗИ. К косвенным эхографическим признакам внутриутробного инфицирования относятся маловодие или многоводие; наличие гиперэхогенной взвеси в околоплодных водах или амниотических тяжей; гипоплазия ворсин хориона, плацентит; преждевременное старение плаценты; отечный синдром плода (асцит, перикардит, плеврит), гепатоспленомегалия, кальцификаты и пороки развития внутренних органов и др. В процессе допплерографического исследования кровотока выявляются нарушения плодово-плацентарного кровотока. Кардиотокография обнаруживает признаки гипоксии плода.
После рождения ребенка с целью достоверной верификации этиологии внутриутробной инфекции используются микробиологические (вирусологические, бактериологические), молекулярно-биологические (ДНК-гибридизация, ПЦР), серологические (ИФА) методики обследования. Важное диагностическое значение имеет гистологическое исследование плаценты.
По показаниям новорожденные с внутриутробными инфекциями в первые сутки жизни должны быть осмотрены детским неврологом, детским кардиологом, детским офтальмологом и др. специалистами. Целесообразно провести ЭхоКГ, нейросонографию, офтальмоскопию, исследование слуха методом вызванной отоакустической эмиссии.
Лечение внутриутробных инфекций
Общие принципы лечения внутриутробных инфекций предполагают проведение иммунотерапии, противовирусной, антибактериальной и посиндромной терапии.
Иммунотерапия включает применение поливалентных и специфических иммуноглобулинов, иммуномодуляторов (интерферонов). Противовирусная терапия направленного действия осуществляется, главным образом, ацикловиром. Для противомикробной терапии бактериальных внутриутробных инфекций используются антибиотики широкого спектра действия (цефалоспорины, аминогликозиды, карбапенемы), при микоплазменной и хламидийной инфекциях – макролиды.
Посиндромная терапия внутриутробных инфекций направлена на купирование отдельных проявлений перинатального поражения ЦНС, геморрагического синдрома, гепатита, миокардита, пневмонии и т. д.
Прогноз и профилактика
При генерализованных формах внутриутробных инфекций летальность в неонатальном периоде достигает 80%. При локальных формах возникают серьезные поражения внутренних органов (кардиомиопатии, ХОБЛ, интерстициальный нефрит, хронический гепатит, цирроз и т. д.). Практически во всех случаях внутриутробные инфекции приводят к поражению ЦНС.
Профилактика внутриутробных инфекций заключается в проведении предгравидарной подготовки, лечении ЗППП до наступления беременности, исключении контактов беременной с инфекционными больными, коррекции программы ведения беременности у женщин групп риска. Женщины, ранее не болевшие краснухой и не получавшие прививки против краснухи, должны быть вакцинированы не позднее, чем за 3 месяца до предполагаемой беременности. В ряде случаев внутриутробные инфекции могут являться основанием для искусственного прерывания беременности.
Инфекции ЦНС у новорождённых относятся к одним из наиболее тяжёлых и неблагоприятных заболеваний, характеризуются воспалительными изменениями в виде менингита, менингоэнцефалита, энцефалита, вентрикулита. Инфицирование происходит внутриутробно, интранатально или постнатально и может быть изолированным, проявлением неонатального сепсиса или генерализованных TORCH-инфекций.
Р35-Р37. Поражение ЦНС при внутриутробных инфекциях (TORCH-синдром)
Врожденные нейроинфекции могут быть представлены энцефалитом, менингитом, вентрикулитом или их комбинациями.
| Пренатальная инфекция плода наступает только при первичном инфицировании беременной женщины. |
Врожденный токсоплазмоз.
Врожденный токсоплазмоз с явной и характерной клинической картиной встречается в периоде новорожденности крайне редко (от 1:3000 до 1:10000 живорожденных).
Фактор риска: первичное заболевание токсоплазмозом беременной женщины (протекает без каких-либо специфических симптомов, напоминает простудное заболевание).
Критерии диагноза:
Клинические,чаще наличие общих симптомов:
· Мышечная гипотония или адинамия
· Синдром внутричерепной гипертензии
· Желтуха с прямой гипербилирубинемией;
· Высокая концентрация белка
· Плеоцитоз, часто мононуклеарный
Реже встречается классическая триада, проявляющаяся позднее:гидроцефалия, хориоретинит, внутримозговые кальцинаты.
ИФА, РСК– специфическиеантитела из класса IgM в крови новорожденного.
Лечение.
При подтвержденном врожденном токсоплазмозе наиболее эффективны препараты пириметамина (тиндурин, дараприм, хлоридин) в комбинации с сульфаниламидами.
Схема 1: пириметамин 1 мг/кг - 5 дней, сульфаниламиды (сульфадиазин, сульфадимезин, сульфадиметоксин) 0,1 мг/кг – 7 дней, провести 3 цикла с перерывами между ними в 7-14 дней. Побочные действия перечисленных препаратов на метаболизм фолиевой кислоты устраняются назначением фолиевой кислоты 1 мг/сутки.
Схема 2: имеются комбинированные препараты: фансидар,метакельфин, содержащие сульфадоксин и пириметамин, расчет дозы по пириметамину 1 мг/кг.
Схема 3: на втором месте по эффективности стоят макролиды: спирамицин 150 - 300 тыс.ед./кг/сут, 10 дней; рокситромицин (рулид) 5-8 мг/кг/сутки; азитромицин (сумамед) 5 мг/кг/сутки, 7-10 дней.
Герпетический менингоэнцефалит.
Изолированное поражение ЦНС у новорожденных вызывает вирус простого герпеса 1-го и 2-го типа. Внутриутробная герпес-вирусная инфекция – это осложнение генитального герпеса (ВПГ 2) при интранатальном пути инфицирования. Возможно и трансплацентарное проникновение ВПГ в организм плода.
Критерии диагноза:
· синдромом повышенной нервно-рефлекторной возбудимости,
· судороги, купируемые с трудом,
· важный симптом заболевания - типичные везикулёзные элементы на коже и слизистых ротовой полости.
СМЖ – высокая концентрация белка, лимфоцитарный плеоцитоз
· специфические антитела из класса IgM в крови новорожденного
· специфические антитела IgM в ликворе
· определение специфических антител (IgG и IgМ)в парных сыворотках
ПЦР – выявление антигена ВПГ в крови и ликворе
НСГ – изменения не специфичны
Лечение.
- Специфическая противовирусная терапия – ацикловир60 мг/кг/сутки в течение 21 дня.
- Поддержание жизненно важных функций организма ребенка проводится в соответствии с общими принципами интенсивной терапии.
Бактериальные менингиты.
Р 36. Бактериальный менингит при неонатальном сепсисе.
Патогенные (вызывающие болезнь) факторы могут приводить к поражению нервной системы плода. К этим факторам относятся инфекции, физические и психические травмы и различные болезни беременных женщин (болезни сердца, легких, эндокринных желез, половой сферы), физические (радиоактивное и рентгеновское облучение) и химические факторы, а также токсикозы беременности и интоксикации (алкогольная, никотиновая. лекарственная и др.). Между временем воздействия патогенных факторов на развивающийся плод и клиническими проявлениями патологии мозга существует отчетливая связь: чем раньше в эмбриогенезе повреждается мозг, тем тяжелее последствия этих влияний. Вместе с тем различные факторы, действующие в одно и то жевремя, вызывают сходные патологические состояния. В связи с этимтрудно разграничить влияние отдельных патогенных факторов, определить удельный вес тех или иных воздействий в возникновении врожденных поражений мозга. Наиболее полно изучены инфекционные поражения плода, являющиеся одной из частых причин неврологических нарушений в детском возрасте. Возбудителями внутриутробной инфекции могут быть вирусы краснухи, гриппа, кори, паротита (свинка), цитомегалии, токсоплазмы, бледная трепонема (возбудитель сифилиса), туберкулезная палочка.
Инфицирование плода происходит во время беременности. Источником инфекции является больная мать. Наиболее тяжелые поражения нервной системы отмечаются при врожденной краснухе, цитомегалии, токсоплазмозе, сифилисе. Возбудитель из организма матери проникает к плоду через плаценту. Факторами, способствующими развитию внутриутробных инфекций, являются токсикоз беременных и другие заболевания, ослабляющие организм матери и повышающие проницаемость маточно-плацентарного барьера для проникновения различных возбудителей. Другой путь заражения — инфицирование околоплодных вод при преждевременном вскрытии плодного пузыря и длительных родах.
Частота гибели плодов от внутриутробных инфекций составляет 17 — 34% по отношению к общему показателю ранней детской смертности (смертность до 7-го дня жизни).
Механизмы развития нарушений нервной системы различны: прямое разрушающее действие возбудителя на нервную клетку, избирательное подавление роста и дифференциации нейронов, кислородное голодание тканей плода вследствие поражения сосудов плаценты, воспалительные изменения мозговых оболочек и вещества мозга, в тяжелых случаях приводящие к деструктивным изменениям.
Менингоэнцефалиты развиваются, как правило, в достаточно дифференцированных тканях мозга, способных давать ответную реакцию на инфицирование в виде воспалительного процесса. При менингоэнцефалитах выявляют отек и набухание вещества мозга, повышенное кровенаполнение сосудов, мелкоточечные кровоизлияния, расширение полостей желудочков мозга, тромбозы мелких и средних сосудов, участки разрушения нервной ткани с последующим образованием полостей и кист, разрастание элементов соединительной ткани.
Последствия, к которым приводит инфицирование плода, зависят не столько от типа возбудителя, сколько от того, на каком месяце внутриутробного развития произошло инфицирование.
При воздействии возбудителя на плод в период плацентация (3 —4-й мес) и органогенеза нарушается нормальный процент закладки и дифференцировки органов и систем. В больинство случаев это приводит к несовместимым с жизнью нарушения самопроизвольному аборту или рождению мертвого ребенка При более позднем воздействии патогенных факторов могут иметь место врожденные пороки развития, внутриутробная гибель плода. задержка внутриутробного развития с поражением различных тканей и органов.
Симптомы поражения нервной системы, как правило, возникают уже в периоде новорожденности. Они могут быть различной степени выраженности. Тяжелые нарушения представлены такими пороками развития нервной системы, как микроцефалия, гидроцефалия, спинно-мозговые и черепно-мозговые грыжи различных размеров и локализации.
При инфицировании плода в последние 3 мес беременности ребенок может родиться вполне здоровом. Однако уже в период новорожденное™ или спустя некоторое время отмечаются общемозговые и очаговые симптомы поражения нервной системы. Дети становятся беспокойными, плохо спят, отказываются от еды. Появляются рвота и повышенная чувствительность к прикосновению, звукам, свету. Нередко температура тела держится в пределах 37,5 — 38 ° С. Масса тела снижается. Большой родничок напряжен, тонус мышц часто повышен, нередки судороги. Дети малоэмоциональны, капризны, не интересуются игрушками, не узнают близких.
Очаговые симптомы поражения нервной системы могут быть выражены в виде грубого сходящегося или расходящегося косоглазия, нистагма, асимметрии лица, расстройств фонации и глотания, парезов и др. В этих случаях симптомы поражения нервной системы обусловлены текущими бактериальными или вирусными менингоэнцефалитами.
Кроме нарушений функций нервной системы при внутриутробных инфекциях отмечаются симптомы поражения других органов. Так, при врожденной краснухе определяются разнообразные поражения глаз. Наиболее часто встречается помутнение хрусталика (катаракта). Могут иметь место пороки развития сердца, почек, надпочечников, кишечника, аномалии скелета. Перенесшие краснуху во внутриутробный период новорожденные имеют маленькие массу тела и рост. В дальнейшем эти показатели отстают от нормы.
При инфекциях, вызванных вирусом простого герпеса, кроме признаков поражения нервной системы могут наблюдаться сердечно-сосудистые нарушения, обусловленные изменениями сердечной мышцы, звездчатая сыпь на коже вследствие тромбоза мелких сосудов, язвы на коже, слизистой оболочке полости рта и роговице.
Специфическими признаками внутриутробного токсоплазмоза кроме нарушений нервной системы являются недоразвитие глаз (микрофтальмия), атрофия зрительных нервов, катаракта, воспаление сосудистой оболочки глаз. Все эти болезни глаз приводят к полной слепоте. Часто отмечают также глухоту или снижение слуха, нарушение процессов окостенения, эндокринные расстройства.
Для раннего врожденного сифилиса характерны высыпания на кожеи слизистых оболочках, увеличение печени и селезенки, болезненность костей и частые переломы их, воспаление сосудистой оболочки глаза. Поздний врожденный сифилис характеризуется триадой симптомов (триада Хатчинсона). Она включает изменение зубов, помутнение роговицы, глухоту. Могут быть также различные деформации костей; выбухание лобных бугров — “олимпийский” лоб, западение корня носа, искривление длинных трубчатых костей.
У большинства больных, перенесших внутриутробные инфекции, можно выявить отчетливые признаки дизэмбриогенеза в виде аномалий лицевого скелета, нарушений прикуса, деформаций ушных раковин, высокого нёба и др. (рис. 83).

Рис. 83. Пороки развития черепа: - оксицефалия; б — гидроцефалия; в — акроцефалия; г — микроцефалия
Диагностика внутриутробных инфекций представляет определенные трудности. Она основывается на данных клинического и лабораторных методов исследования. Наиболее достоверны — специфические иммунологические реакции и внутрикожные пробы, подтверждающие характер возбудителя. Имеют значение исследование жидкости, глазного дна и рентгенография черепа. Необходимо также обследовать родителей ребенка и лиц, находящихся с ним в контакте. Важное значение придают акушерскому анамнезу матери, при исследовании которого могут быть отмечены инфекционные заболевания во время беременности, выкидыши и мертворождения.
К последствиям внутриутробных инфекций нервной системы относят микроцефалию, гидроцефалию, глухоту, слепоту, спастические параличи и парезы, судороги, непроизвольные движения (гиперкинезы), нарушения психического развития (от легких задержек темпа развития до тяжелых форм олигофрении).
Лечение заключается в проведении различных для каждого за болевания курсов противовоспалительной терапии. Большое зна чение придают профилактике внутриутробных инфекций. В связь с этим проводят лабораторные исследования беременных с отягощенным акушерским анамнезом или бывших в контакте с инфекционными больными.
Лечение последствий внутриутробных инфекций симптоматическое. Широко используют препараты, улучшающие обменные процессы в ткани мозга, снижающие тонус мышц, уменьшающие судороги и т.д.
С целью социальной адаптации больных с нарушениями зрения, слуха, речи, отставанием в психическом развитии показано проведение комплекса медицинских и педагогических воздействий В процессе обучения и воспитания максимально используются сохранные функции.
ХРОМОСОМНЫЕ БОЛЕЗНИ
Хромосомные болезни обусловлены изменением числа или структуры хромосом. Такие нарушения могут возникать либо в половых клетках родителей, либо в процессе деления оплодотворенной яйцеклетки (зигота) под действием биологически активных физических, химических, вирусологических, бактериологических и других факторов. Частота хромосомных болезней среди новорожденных детей составляет около 1 %. Грубые аномалии хромосом несовместимы с жизнью и часто являются причиной самопроизвольных выкидышей и мертворождений.
Различают хромосомные синдромы, обусловленные изменением половых хромосом, и синдромы, вызванные аномалиями аутосом (любой из 22 пар неполовых хромосом). Среди аномалий половых хромосом наиболее часты синдром Шерешевского — Тернера, при котором в хромосомном наборе отсутствует одна половая хромосома, и синдром Клайнфелтера, при котором имеется одна или несколько добавочных половых хромосом.
Наиболее распространенным синдромом, обусловленным аномалией аутосом, является болезнь Дауна. В хромосомном наборе больных присутствует лишняя 21-я хромосома. Клиническая картина хромосомных синдромов складывается из сочетания врожденных пороков, дизэмбриогенетических стигм (знак, признак), отставания в физическом и нервно-психическом развитии. В структуре заболеваний, протекающих со слабоумием, хромосомные синдромы составляют 2,5 — 4%.
Последнее изменение этой страницы: 2016-04-25; Нарушение авторского права страницы
Читайте также:


