Признаки демиелинизации при энмг
Демиелинизация – патологический процесс, при котором разрушается миелиновая оболочка нервных волокон. Миелиновая оболочка выполняет изолирующую функцию: она обеспечивает распространение электрического импульса по волокну без энергетических потерь. Демиелинизация становится причиной нарушения функциональной активности структур, вовлеченных в патологический процесс.
Причины
К наиболее частым причинам демиелинизации относятся:
- генетически обусловленная несостоятельность миелиновой оболочки;
- повреждение белковых молекул миелина аутоиммунными комплексами;
- обменные нарушения в клетках нервной системы;
- вирусные агенты, клетками-мишенями которых становятся глиальные клетки (клетки, формирующие миелиновую оболочку);
- неопластические процессы в нервной ткани (первичные опухоли нервной системы и метастатические образования в данной области);
- тяжелая интоксикация.
Различают 2 типа демиелинизации:
- Миелинокластия – разрушение миелина в результате генетического дефекта.
- Миелинопатия – нарушение целостности миелиновой оболочки под влиянием внешних или внутренних факторов, не связанных с миелином.
В зависимости от локализации патологического процесса выделяют:
- демиелинизацию структур центральной нервной системы;
- демиелинизацию анатомических образований периферической нервной системы.
Последствием демиелинизации могут стать различные по локализации и выраженности нарушения функций нервной системы.
- изолированную демиелинизацию;
- генерализованную демиелинизацию.
Признаки
Клиническая картина при демиелинизации зависит от следующих факторов:
- локализация патологического процесса;
- его выраженность;
- компенсаторные возможности организма, то есть скорость естественной ремиелинизации (восстановления целостности миелиновой оболочки).
Изолированная демиелинизация двигательных нервов характеризуется двигательными нарушениями (парезами разной степени выраженности и параличами).
При изолированной демиелинизации чувствительных нервных волокон в клинической картине превалируют симптомы нарушенной чувствительности в области, за которую отвечает пораженный нерв (парестезии, гиперестезии, диссоциации, гипестезии, анестезии, дизестезии).
Генерализованная демиелинизация характеризуется следующими симптомами:
- хроническая усталость, повышенная утомляемость;
- упорные головные боли;
- головокружения;
- нарушения интеллектуальной деятельности;
- снижение остроты зрения;
- затруднения глотания (дисфагия);
- смазанная речь;
- неустойчивость, шаткость походки;
- тремор конечностей;
- необычные ощущения в разных частях тела.
Диагностика
С целью локализации патологического процесса проводится тщательный неврологический осмотр.
Для диагностики периферической демиелинизации используется электромиография (исследование биопотенциалов скелетных мышц).
Наиболее информативный метод – магнитно-резонансная томография, посредством которой удается визуализировать патологические очаги диаметров более 3 мм.
Лечение
Целями терапии являются ремиелинизация, то есть восстановление целостности миелиновой оболочки нервного волокна, и нормализация функций участка нервной системы, вовлеченного в патологический процесс.
Изолированная демиелинизация двигательных нервов характеризуется двигательными нарушениями (парезами разной степени выраженности и параличами).
Для стимулирования ремиелинизации назначаются следующие группы препаратов:
- противовоспалительные средства;
- нейропротекторы;
- средства, улучшающие трофику нервной ткани, в том числе витамины.
Профилактика
Своевременное выявление наследственной предрасположенности к развитию демиелинизирующих заболеваний исходя из изучения семейного анамнеза и проведения генетического типирования, а также мероприятия, направленные на предупреждение развития аутоиммунных заболеваний и нейроинфекций, позволяют существенно снизить риск демиелинизации нервных волокон.
Последствия и осложнения
Последствием демиелинизации могут стать различные по локализации и выраженности нарушения функций нервной системы.
Информация является обобщенной и предоставляется в ознакомительных целях. При первых признаках болезни обратитесь к врачу. Самолечение опасно для здоровья!
Желудок человека неплохо справляется с посторонними предметами и без врачебного вмешательства. Известно, что желудочный сок способен растворять даже монеты.
Согласно исследованиям ВОЗ ежедневный получасовой разговор по мобильному телефону увеличивает вероятность развития опухоли мозга на 40%.
Согласно исследованиям, женщины, выпивающие несколько стаканов пива или вина в неделю, имеют повышенный риск заболеть раком груди.
В течение жизни среднестатистический человек вырабатывает ни много ни мало два больших бассейна слюны.
В четырех дольках темного шоколада содержится порядка двухсот калорий. Так что если не хотите поправиться, лучше не есть больше двух долек в сутки.
Упав с осла, вы с большей вероятностью свернете себе шею, чем упав с лошади. Только не пытайтесь опровергнуть это утверждение.
Вес человеческого мозга составляет около 2% от всей массы тела, однако потребляет он около 20% кислорода, поступающего в кровь. Этот факт делает человеческий мозг чрезвычайно восприимчивым к повреждениям, вызванным нехваткой кислорода.
Работа, которая человеку не по душе, гораздо вреднее для его психики, чем отсутствие работы вообще.
У 5% пациентов антидепрессант Кломипрамин вызывает оргазм.
Для того чтобы сказать даже самые короткие и простые слова, мы задействуем 72 мышцы.
На лекарства от аллергии только в США тратится более 500 млн долларов в год. Вы все еще верите в то, что способ окончательно победить аллергию будет найден?
Самая высокая температура тела была зафиксирована у Уилли Джонса (США), который поступил в больницу с температурой 46,5°C.
Самое редкое заболевание – болезнь Куру. Болеют ей только представители племени фор в Новой Гвинее. Больной умирает от смеха. Считается, что причиной возникновения болезни является поедание человеческого мозга.
Американские ученые провели опыты на мышах и пришли к выводу, что арбузный сок предотвращает развитие атеросклероза сосудов. Одна группа мышей пила обычную воду, а вторая – арбузный сок. В результате сосуды второй группы были свободны от холестериновых бляшек.
Кариес – это самое распространенное инфекционное заболевание в мире, соперничать с которым не может даже грипп.
Каждый человек может столкнуться с ситуацией, когда он теряет зуб. Это может быть плановая процедура, проведенная стоматологам, или следствие травмы. В каждом и.
Электрофизиологические исследования (ЭМГ и исследование нервной проводимости) используются для выявления, локализации, характеристики и прогнозирования нарушений, влияющих на моторную единицу.
Аномальные нейрогенные результаты ЭМГ не являются специфичными для конкретного заболевания, но полезны в диагностическом процессе. При электрофизиологическом обследовании определяются клинические показания для нейровизуализации.
Электрофизиологическое исследование предоставляет информацию о локализации поражения в моторной единице (нижний мотонейрон, нервно-мышечное соединение или мышечные волокна). Также устанавливается тип повреждения, либо демиелинизирующее или аксональное, либо оба.
а) Поражения нижнего мотонейрона. Острое очаговое поражение нижнего мотонейрона (включая передние рога, нервные корешки, нервные сплетения и периферические нервы) вызывает изменения при ЭМГ и при исследовании нервной проводимости и зависит от механизма (компрессия, растяжение, разрыв или ишемия).
Распределение электрофизиологических изменений зависит от места поражения, а также от того, какие мышцы и нервы были выбраны для исследования, что в свою очередь зависит от симптомов у пациента.
Поражение клеток передних рогов, нарушение непрерывности аксонов и демиелинизация (нейроапраксия) немедленно отражаются на ЭМГ и в исследовании нервной проводимости. Эти изменения являются неспецифическими, и их может быть трудно отличить, например, от поражения верхних мотонейронов или субмаксимальной контрактуры мышц.
При ЭМГ частота оставшихся моторных единиц увеличивается для получения исходной силы сокращения мышц с меньшим количеством моторных единиц, а картина интерференции максимального сокращения мышц может быть уменьшена при достаточно низком количестве выживших моторных единиц. В течение второй недели происходит увеличение спонтанной активности (потенциал фибрилляции, положительные острые волны и фасцикуляции), но она не присутствует в большинстве пораженных мышц до следующих 3-5 недель.
При проведении исследования при остром очаговом поражении периферических нервов появляются различные нарушения, если природа нарушений демиелинизирующая или связана с потерей аксонов.
При фокальной демиелинизации миелиновая оболочка нарушается и затруднено распространение нервных потенциалов действия на месте поражения. Соответственно выявляется электрофизиологическое снижение скорости проводимости или проводниковая анестезия. Проводниковая анестезия может быть полной или частичной.
В случае замедления проводимости амплитуда потенциалов действия мышцы нормальная после стимуляции и проксимального и дистального концов. Проведение полностью блокируется, если распространение потенциалов действия двигательных нервов не представляется возможным по всему периметру демиелинизации. При полном моторном блоке нормальные потенциалы действия мышц вызываются дистальнее места поражения но отсутствуют при стимуляции проксимальнее места поражения. При частичном блоке распространение потенциалов действия проходит только по аксонам.
Таким образом, амплитуда потенциала действия, записанная после стимуляции проксимально от поражения, снижается по сравнению с дистальной стимуляцией.
После острого аксонального повреждения часть аксона дистальнее поражения подвергается валлеровский дегенерации. Скорость проведения может быть несколько снижена в связи с потерей самых быстропроводящих нервных волокон.
Так как валлеровская дегенерация начинается только через два дня после прекращения аксонального проведения, часть аксонов дистальнее места повреждения остается возбудимой до полной дегенерации. Валлеровская дегенерация завершается к 10 дню после аксонального поражения. Чтобы записать или классифицировать поражение как демиелинизируещее или аксональное, электрофизиологическое исследование должно быть отложено, по крайней мере на 11 дней после поражения. После полной валлеровской дегенерации ЭМГ обследование позволяет локализовать поражение, так как нейрогенные нарушения выявляются только в мышцах с иннервацией ветвями, возникающими дистальнее места поражения.
ЭМГ также может быть использована для оценки прогресса реиннервации.
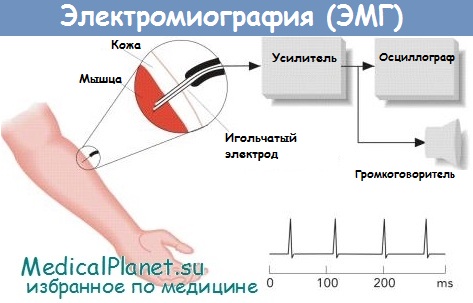
б) Поражения периферических нервов. Исследования нервной проводимости и ЭМГ играют важную роль в дифференциальной диагностике нервных нарушений.
Во время исследования нервной проводимости выявляются нормальные результаты при клинической картине ущемления нерва, вызванной наличием болезненных точек или других болезненных состояний опорно-двигательного аппарата. Это можно наблюдать, например, при болезненной точке подостной мышцы, когда часто возникает парестезия локтевой части кисти и предплечья или при латеральном эпикондилите, когда можно выявить парез мышц разгибателей запястья и кисти.
Электромиография при повреждении сплетений и корешков покажет нейропатические результаты вне зоны поражения. Например, при поражении нижнего ствола плечевого сплетения помимо нарушений в мышцах, иннервируемых локтевым нервом (ущемление нерва позади медиального надмыщелка), нарушения будут присутствовать в мышце, отводящей мизинец (иннервируется срединным нервом), в соответствии с ходом нервных волокон из корешков С8 и Т1 через нижний ствол срединного нерва.
в) Плексопатии. Плечевое и пояснично-крестцовое нервные сплетения являются сложными структурами. Для локализации повреждения необходимы детальные знания об их анатомии. Дифференциальная диагностика между поражениями корешка и повреждением сплетения важна после тракционной травмы. Исследование СВП показывает нормальное проведение потенциалов действия и скорость проведения в случае травмы корешка (см. ниже), в то время как потенциалы действия снижают амплитуду или отсутствуют при поражении сплетения при исследовании пациента после полной валлеровской дегенерации (более чем через 10 дней после травмы).
Выявление нейрогенного нарушения в мышцах, иннервируемых двумя или более периферическими нервами с общим ходом через сплетение, подтверждает диагноз поражения сплетения.
г) Радикулопатия. Поражения нервных корешков вызывают валлеровскую дегенерацию мотонейронов в периферических нервах, а затем нейрогенные нарушения обнаруживаются в мышцах, иннервируемых этими нервными волокнами. Напротив, сенсорные нервные волокна в периферических нервах не перерождаются, потому что их трофические центры находятся в задних корешках. Таким образом, при поражении корешков будут диагностироваться нормальные сенсорные потенциалы действия вместе с нейрогенными нарушениями в распределении сегментарных миотомов при ЭМГ.
При радикулопатиях (и поражениях, связанных с передними рогами), в отличие от более периферических поражений, страдают параспинальные мышцы и мышцы, иннервируемые ветвями, отходящими в непосредственной близости от межпозвонкового отверстия (например, зубчатая мышца), и при ЭМГ можно зарегистрировать нейрогенные нарушения в этих мышцах.
д) Поражение спинного мозга. Поражения, связанные с мотонейронами в передних рогах спинного мозга, дают такие же изменения на ЭМГ и нарушения моторной проводимости, как при радикулопатиях. Распределение патологических изменений и дополнительные находки предполагают повреждение верхнего мотонейрона, что подтверждает диагноз повреждения спинного мозга.
е) Поражение верхнего мотонейрона. При поражения спинного мозга ниже места поражения не выявляется никаких отклонений в сенсорном или моторном проведении нервов. При ЭМГ спонтанная активность не определяется, а МВП имеют нормальную конфигурацию. Единственным электрофизиологическим нарушением является снижение интерференционного паттерна при максимальном сокращении и снижении частоты моторной единицы. Эти нарушения также могут быть найдены при истерических парезах.
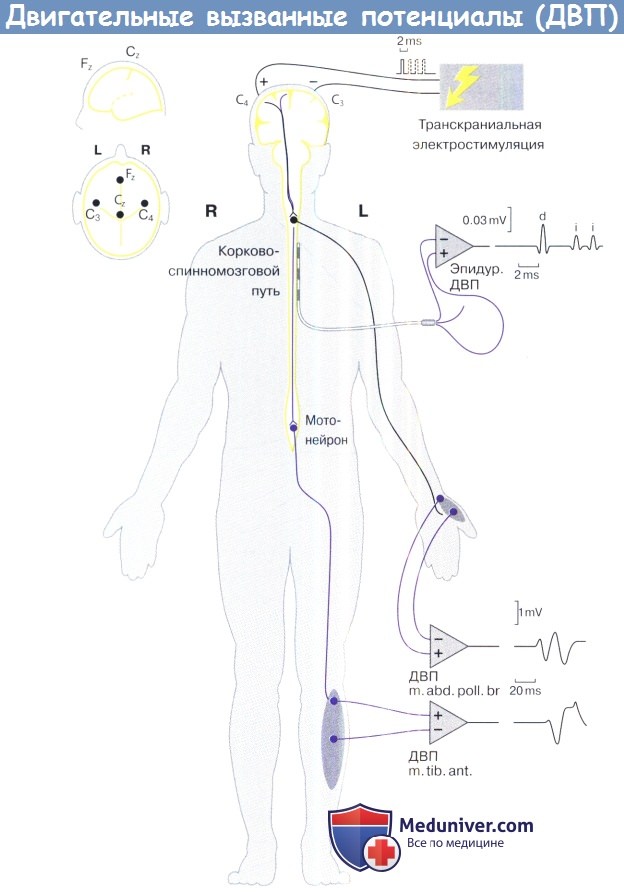
Настройка мониторинга двигательных вызванных потенциалов.
Транскраниальная электростимуляция (ТЭС) через кожу/игольчатые электроды в области С3 и С4, анод (+) является стимулом для аксонов кортикоспинального тракта.
Стимул должен состоять из последовательных 4-7 импульсов, с коротким межимпульсным интервалом.
Стимуляция в основном осуществляется с частотой 1-0,5 Гц, особенно в критические периоды операции.
Общие характеристики приведены в таблице ниже. Запись осуществляется с помощью иглы или поверхностных электродов в/на мышцах рук (например, m. abductor pollicis brevis, m.abd. poll.br) и ног (m. tibialis anterior, m.tib.ant.).
Во время открытой операции на позвоночнике могут быть размещены эпидуральные электроды ниже (и выше) зоны риска, например, в случае интрамедуллярных опухолей.
На рисунке показано, что в случае записи с мышц участвуют два синапса: один на двигательном нейроне, и один на мышце.
При эпидуральной записи (D-волны) синапсы не вовлечены, что делает контроль в такой ситуации нечувствительным к анестезии или релаксации.
Эпидуральная запись также показывает позднюю реакцию, называемую I-волной, которая является результатом стимуляции ассоциативных волокон в коре головного мозга, вместо аксонов кортикоспинального тракта.
В возрасте от 40 до 60 лет часто возникает демиелинизирующая полинейропатия. Она относится к группе болезней – нервно-мышечные патологии.

Поражает женщин в два раза реже, чем мужчин. Характеризуется уменьшением двигательной активности рук и ног вплоть до паралича, снижением чувствительности. При своевременной диагностике, рано начатом и регулярном лечении прогноз для жизни достаточно благоприятный.
Демиелинизирующая полинейропатия
Постепенное разрушение миелиновой оболочки, обусловленное аутоиммунными факторами, носит название демиелинизирующей полинейропатии. Заболевание носит рецидивирующий характер. Средний возраст его обнаружения – 47 лет. Однако описаны случаи и раннего возникновения. Наиболее тяжелое течение характерно для людей старше 50 лет. Они также хуже воспринимают лекарственную терапию.
Патология ведет к поражению некоторого количества периферических нервов, передающих сигналы, связанные с двигательной активностью и чувственными восприятиями. Спинной и головной мозг остаются сохранными.
Характер течения позволяет говорить о трех формах заболевания – острой, подострой и хронической. Первую характеризует быстрое, даже стремительное развитие патологии. До четырех недель требуется для того, чтобы симптомы проявились в полную силу.
Подострая прогрессирует медленнее, признаки проявляются и нарастают в течение полугода. За несколько лет развивается хроническая демиелинизирующая полинейропатия. Ее течение скрытое, почти незаметное.
Характер развития полинейропатии зависит от того, в каком типе нерва произошло воспаление. При поражении нервных волокон, отвечающих за восприятие и передачу ощущений, говорят о чувствительной полинейропатии. В случае повреждения двигательного волокна – о моторной. Сочетанное поражение свидетельствует о том, что развивается сенсорно-моторная патология. Выделяют также вегетативную форму.
Преимущественное повреждение тела длинного отростка нейрона позволяет говорить об аксональной форме. Разрушение миелина – о демиелинизирующей. В некоторых ситуациях выделяют смешанную, аксоно-демиелинизирующую патологию.
Течение болезни может проходить в атипичной и классической форме.
При классической поражение ведет к нарастанию слабости всех отделов конечностей и снижению их чувствительности. Нарастание симптоматики происходит ступенчато.

Атипичная характеризуется ассиметричным поражением мышц стоп, голени, предплечий, кистей. Иногда отмечаются локальные нарушения отдельных участков конечностей, например, плеча или поясницы. К этой форме относятся расстройства только чувствительных или только моторных нервов.
Механизм развития
В основе развития хронической воспалительной демиелинизирующей полинейропатии лежит сочетание нескольких факторов:
- Тяжелые ситуации, травмы, болезни (рак, сахарный диабет), изматывающие человека психически и эмоционально и ведущие к истощению.
- Попадание в организм инфекции, в составе которой есть белок, сходный по строению с белками человека.
- Генетическая предрасположенность.
Вследствие сочетанного воздействия факторов происходит разрушение нервных отростков, их миелиновой оболочки или нарушение выработки миелина. Какой из этих процессов является первичным у пациента, зависит от различных причин и не всегда очевиден. К примеру, у больного алкоголизмом при дефиците фолиевой кислоты и некоторых витаминов первично нарушение выработки миелина.
Считается, что под воздействием некоторых факторов начинается выработка антигенов миелина. Вероятно, это происходит под влиянием попадания в организм инфекции со сходным белком или определенного внутреннего нарушения. В результате миелиновый белок начинает считываться организмом как патогенный. В области нерва скапливаются клетки типа Th1, проникающие через гематоневрологический барьер. Развивается воспаление, приводящее к разрушению миелина и нарушению его выработки.

Причины
Не всегда очевидно, что вызвало демиелинизирующую полинейропатию, часто важную роль играет несколько факторов. Среди ключевых причин выделяют инфекционные заболевания: грипп, ВИЧ, герпес.
Часто заболевание развивается на фоне сахарного диабета и болезней, связанных с нарушениями обменных процессов.
Под воздействием алкоголя, некоторых лекарственных средств, солей тяжелых металлов, ртути развивается токсическая нейропатия.
ХВДП проявляется также вследствие воздействия травмирующих факторов. Их влияние прослеживается двояким образом: прямым разрушением нервных волокон из-за повреждения, а также проникновением в рану инфекции.
Полинейропатия аллергического генеза развивается преимущественно после вакцинации при повышенной чувствительности организма к вводимому препарату.
Провоцируют появление патологии генетические факторы, ситуации, связанные с сильными эмоциональными и психическими, тяжелыми физическими нагрузками. Риск развития повышается на фоне гормональных нарушений.
Симптомы
Вряд ли какой-то человек вспомнит тот момент, когда у него начали проявляться признаки полинейропатии. Обращать внимание на проблемы он начинает, когда из-за слабости не сможет подняться по лестнице, потеряет способность писать, брать небольшие предметы.
Симптомы ХВДП зависят от того, какой нерв поражен. При патологии двигательных волокон появляется слабость мышц. Человек теряет способность самостоятельно двигаться, садиться. Часто появляются болевые ощущения. Наблюдается снижение рефлексов. Отмечается дрожание при попытке удержать руку или ногу в определенном положении. Возникает нарушение речи, расстройства зрения.

Поражение чувствительных нервов сопровождается во многих случаях онемением, чувством жжения кистей, стоп, голеней, ощущением бегающих мурашек.
Заподозрить воспалительные процессы в вегетативной нервной системе можно по мраморности кожи, отекам, белому цвету пальцев.
Диагностика
Определение диагноза и причин заболевания осуществляется на основе анализа симптомов и применения различных способов исследования. В рамках диагностики уточняют причину демиелизирующей полинейропатии, определяют степень поражения:
- Электрофизиологические методы. Уточняются нейрофизиологические симптомы, в том числе уменьшение скорости проводимости, прерывание, блокада проведения импульсов.
- Анализ спинномозговой жидкости. При проведении этого исследования обнаруживается присутствие в ликворе признаков ХВДП: повышение содержания белков, антигенов, лейкоцитов, остатков клеточных структур. Данный метод не всегда считается информативным по отношению к полинейропатии.
- Биопсия. Во время исследования берут пробу волокна. Обнаруживаются признаки поражения аксонов или миелиновой оболочки. Наиболее выраженными оказываются изменения в глубоких отделах нервов, однако они из-за своего положения не всегда доступны для анализа. Биопсия проводится, если в результате электрофизиологического исследования отмечается расстройство в двух нервах.
- Магнитно-резонансная томография. На получаемых снимках наблюдается удлинение корешков нервов, исходящих из спинного мозга, увеличение некоторых участков нервных волокон, отеки, признаки воспалений.
Несмотря на наличие разных методов исследования, в настоящее время быстро определить правильный диагноз получается не всегда. Усложняется диагностика наличием атипичных форм.
Лечение
Ключевым фактором улучшения прогноза полинейропатии является своевременно начатое лечение. Оно направлено на прекращение демиелинизации, разрушения аксонов.

Проводится гормональная терапия, плазмаферез, применяется иммуноглобулин G. В некоторых случаях показана монотерапия, в других рекомендуется сочетанное применение трех методов.
Преимущественное применение глюкокортикостероидов обусловлено улучшением состояния больных через 1,5-2 месяца лечения. Симптомы исчезают или значительно уменьшаются при лечении, проводимом до полутора лет. На фоне отмены возможны рецидивы. Проведение гормональной терапии показано при постоянном контроле давления, плотности ткани костей, формулы крови. Проблема данного метода заключается в большом количестве противопоказаний и побочных эффектов.
Плазмаферез позволяет провести очищение крови от антигенов, токсинов. Считается эффективным методом, однако действие его продолжается в течение короткого промежутка времени, поэтому рекомендуется повторное проведение. На начальных этапах исследования процедура осуществляется дважды в неделю, после уменьшения симптоматики – ежемесячно. Плазмаферез рекомендуется проводить сразу после определения диагноза.
У около 60% пациентов эффективным оказалось введение иммуноглобулинов G. Преимущество этого метода в малом количестве побочных действий. Детям часто проводят иммуносупрессорную терапию.
При симптоматическом лечении применяют лекарства, уменьшающие боли в мышцах. Показаны антихолинэстеразные препараты (Нейромидин, Аксамон). Они направлены на возбуждение ЦНС и повышение тонуса мышц.
Уменьшению болезненности, разогреву мышц способствуют некоторые мази. Назначают, в частности, Капсикам. Использование дополнительных препаратов обусловлено основной причиной, которая вызвала заболевание. Показан прием витаминов, антиоксидантов, лекарств, улучшающих обмен веществ.
Для стимуляции передачи нервных импульсов используется электрофорез. Мягкое воздействие усиливает приток крови с кислородом и питательными веществами к пораженным частям тела.
Магнитотерапия воздействует локально, она улучшает обмен веществ и проведение нервных импульсов. Для восстановления мышечных тканей после атрофии показан массаж, особенно если нет возможности заниматься физкультурой.
Улучшить кровоснабжение, нормализовать мышечную силу и начать снова ходить поможет лечебная физкультура.
Профилактика
Чтобы уменьшить риск развития демиелинизирующей полинейропатии, осуществляют следующие мероприятия:
- для работы, связанной с токсическими веществами, используют защитную одежду;
- не употребляют алкоголь;
- принимают лекарственные средства только по назначению врача;
- ведут активный образ жизни;
- в меню включают овощи и фрукты;
- не допускают переход острых болезней в хроническую форму;
- контролируют состояние здоровья.
Прогноз
Патология носит хронический характер, периодичность возникновения рецидивов зависит от характера течения. Отмечается, что уже в первый год у половины больных возникают повторные проявления болезни. Чаще происходит это при отмене терапии.
Прогноз благоприятнее в тех случаях, когда симптомы нарастали медленно, а борьба с заболеванием началась на ранних этапах и не прекращается. Важно обращать внимание на появление первых же признаков, свидетельствующих о расстройствах неврологического характера.
Лучше перспективы у молодых людей, у них наблюдается длительная ремиссия. В случае развития у пожилых, воспалительная полинейропатия, сопровождаемая необратимыми неврологическими нарушениями, приводит к инвалидизации и в некоторых случаях к смерти.
Развитие демиелинизирующей полинейропатии связано с воспалительными процессами, от которых страдает периферическая система. Слабеют мышцы, развиваются парезы. В результате человек теряет способность самостоятельно передвигаться, вставать, сидеть. Избавиться от болезни удается далеко не всегда, однако использование назначенных врачом лекарственных препаратов позволяет добиться ремиссии и уменьшения рецидивов.
Для подготовки статьи использовались следующие источники:
Жирнова И. Г., Комелькова Л. В., Павлов Э. В., Авдюнина И. А., Попов А. А., Пирогов В. Н., Ганнушкина И. В., Пирадов М. А. Иммунологические особенности тяжелых форм демиелинизирующих и смешанных полинейропатий // Журнал Альманах клинической медицины — 2005.
Турсынов Н. И., Григолашвили М. А., Илюшина Н. Ю., Сопбекова С. У., Мухаметкалиева А. Д., Утегенов А. У. Современные аспекты диагностики и лечения хронических демиелинизирующих полинейропатий // Журнал Нейрохирургия и неврология Казахстана — 2016.
Демиелинизирующее заболевание представляет собой патологический процесс разрушения миелиновой оболочки, при котором поражаются нейроны головного и спинного мозга. При этом ухудшается проводимость импульсов в нервной системе. Болезнь характеризуется уничтожением миелина мозга. Это опасное состояние влияет на функционирование всего организма. Заболевание встречается с одинаковой частотой как у взрослых, так и детей. Современная медицина не обладает средствами для полного излечения от этого заболевания. Его можно лишь ослабить и замедлить течение.
Демиелинизация
Демиелинизирующее заболевание головного мозга по МКБ-10 имеет коды G35, G36 и G77. Процесс, вызванный поражением нервной ткани, негативно сказывается на функционировании всего организма в целом. Определенные нервные окончания покрыты миелиновой оболочкой, которая выполняет в организме важные функции. Например, миелин обеспечивает быструю передачу электрических импульсов и соответственно при нарушении этого процесса страдает вся система. Миелин состоит из липидов и белковых соединений в пропорции 70/30.

Врач-невролог
Наиболее распространенное демиелинизирующее заболевание головного мозга – рассеянный склероз. Симптомы его очень разнообразны, поэтому пациент редко сразу приходит к неврологу. Снижение зрения, онемение конечностей, проблемы с моторикой – разные врачи дают разные рекомендации, хотя достаточно просто отправить пациента на МРТ и лабораторные исследования, которые подтвердят опасения или исключат заболевания мозга.
Благодаря современным методам терапии и исследований доброкачественное течение наблюдается примерно в половине случаев — больные полностью сохраняют трудоспособность, заводят семьи, рожают детей. Есть некоторые ограничения, например, запрещено посещение бань и саун, длительное нахождение на солнце, но в остальном образ жизни сохраняется, никаких специальных диет не нужно.
Нервная система состоит из центрального и периферического отделов. Механизм регуляции между ними работает следующим образом: импульсы от рецепторов периферической системы передаются в нервные центры спинного мозга, а оттуда в головной мозг. Расстройство этого сложного механизма становится причиной демиелинизации.
Нервные волокна покрыты миелиновой оболочкой. В результате рассматриваемого патологического процесса эта оболочка разрушается и на ее месте формируется фиброзная ткань. Она в свою очередь не может проводить нервные импульсы. В условии отсутствия нервных импульсов нарушается работа всех органов, поскольку мозг не может отдавать команды.
Причины
Демиелинизирующие заболевания головного мозга характеризуются поражением периферической и центральной нервной системы. Они чаще всего возникают на фоне генетической предрасположенности. Случается и так, что сочетание определенных генов провоцирует нарушения в функционировании иммунной системы. Выделяются и иные причины возникновения демиелинизирующих заболеваний:
- состояние хронической или острой интоксикации;
- солнечная радиация;
- ионизирующее облучение;
- аутоиммунные процессы в организме и генетические патологии;
- осложнение бактериальной и вирусной инфекции;
- неправильное питание.
Наиболее подверженной этой патологии считается европеоидная раса, особенно те ее представители, которые проживают в северных географических широтах. Такой тип заболевания может провоцироваться травмой головы или позвоночника, депрессией, вредными привычками. Некоторые типы вакцин также могут стать пусковым механизмом для начала развития таких патологий. Это относятся к прививкам против кори, оспы, дифтерии, гриппа, коклюша, гепатита В.
Классификация
Демиелинизирующее заболевание нервной системы классифицируется на различные типы, в основе которых лежит разрушение миелиновой оболочки. В связи с этим рассматриваемая патология подразделяется соответствующим образом на рассеянный склероз, болезнь Марбурга, болезнь Девика, прогрессирующую мультифокальную лейкоэнцефалопатию и синдром Гийена-Барре.
Рассеянный склероз характеризуется как тяжелое хроническое и дезиммуно- нейродегенеративное заболевание ЦНС, склонное к прогрессированию. В большинстве случаев заболевание встречается в молодом возрасте и почти всегда приводит к инвалидности. Этому демиелинизирующему заболеванию ЦНС по МКБ-10 присвоен код G35.
В настоящее время причины развития рассеянного склероза до конца не изучены. Большинство ученых склоняются к мультифакторной теории развития этого заболевания, когда сочетается генетическая предрасположенность и внешние факторы. К числу последних относятся:
- инфекционные заболевания;
- состояние хронической интоксикации;
- прием некоторых лекарственных средств;
- смена места жительства с резкой сменой климата;
- недостаток клетчатки и высококалорийная диета.
Не всегда прослеживается взаимосвязь симптоматики рассеянного склероза со стадией заболевания. Патология может иметь волнообразное течение. Обострения и ремиссии могут повторяться с различным интервалом. Особенностью рассеянного склероза является то, что каждое новое обострение имеет более тяжелое течение по сравнению с предыдущим.
Прогрессирование рассеянного склероза характеризуется развитием следующей симптоматики:
- нарушения чувствительности (мурашки по коже, онемение, покалывание, жжение, зуд);
- расстройство зрения (нарушение цветопередачи, снижение остроты зрения, размытость картинки);
- дрожание конечностей или туловища;
- головные боли;
- нарушения речи и затруднение глотания;
- мышечные спазмы;
- изменения походки;
- когнитивные нарушения;
- непереносимость тепла;
- головокружение;
- хроническая усталость;
- нарушение либидо;
- тревожность и депрессия;
- нестабильность стула;
- бессонница;
- вегетативные расстройства.
Выделяют также вторичные симптомы рассеянного склероза. Они подразумевают осложнения болезни. Очаги демиелинизации в головном мозге определяются с помощью магнитно-резонансной томографии, в том числе с введением контрастного вещества.
Лечение рассеянного склероза осуществляется с помощью таких методов, как:
- плазмаферез;
- прием цитостатиков;
- назначение иммуносупрессоров;
- применение иммуномодуляторов;
- прием бета интерферонов;
- гормональная терапия.
- симптоматическая терапия с назначением антиоксидантов, ноотропных препаратов и витаминов.
В период ремиссии пациентам показано санаторно-курортное лечение, массаж, лечебная физкультура. При этом должны быть исключены все тепловые процедуры. Для облегчения симптомов заболевания назначаются препараты: снижающие мышечный тонус, устраняющие тремор, нормализующие мочеиспускание, стабилизирующие эмоциональный фон, противосудорожные средства.
Рассеянный склероз относится к категории неизлечимых заболеваний. Поэтому указанные методы лечения направлены на уменьшение проявлений и улучшение качества жизни больного. Длительность жизни больных с таким заболеванием зависит от характера течения патологии.
Болезнь Марбурга
Геморрагическая лихорадка или болезнь Марбурга представляет собой острую инфекционную патологию, вызванную марбургским вирусом. Он проникает в организм через поврежденную кожу и слизистую оболочку глаз и полости рта.
Инфицирование происходит воздушно-капельным и половым путем. Кроме того, заразиться можно через кровь и другие выделения больного. После того как человек переболеет этим заболеванием, у него формируется стойкий и длительный иммунитет. Повторное заражение в практике не встречалось. У переболевшего геморрагической лихорадкой Марбурга наблюдается образование некрозов и очагов кровоизлияний в печени, миокарде, легких, надпочечниках, почках, селезенке и других органах.
Симптоматика заболевания зависит от стадии патологического процесса. Инкубационный период длится от 2 до 16 дней. Болезнь имеет острое начало и характеризуется повышением температуры тела до высоких показателей. Наряду с температурой может появиться озноб. Нарастают признаки интоксикации, такие как разбитость, головная боль, боль в мышцах и суставах, интоксикация и обезвоживание. Через 2-3 дня после этого присоединяются расстройство функционирования ЖКТ и геморрагический синдром. В области груди появляется колющая боль, которая усиливается во время дыхания. Кроме того, у больного может появиться сухой кашель и загрудинные колющие боли. Боль может перейти на область горла. Слизистая оболочка глотки сильно краснеет. Почти у всех больных наблюдался понос, который длился почти 7 дней. Характерным признаком этого заболевания является появление сыпи на туловище по подобию кори.
Все симптомы усиливаются к концу первой недели. Также могут наблюдаться кровотечения, из носа, желудочно-кишечного тракта, половых путей. К началу 2 недели все признаки интоксикации достигает своего максимума. При этом возможны судороги и потеря сознания. По анализу крови происходят специфические изменения: тромбоцитопения, пойкилоцитоз, анизоцитоз, зернистость эритроцитов.
При подозрении у человека болезни Марбурга он экстренно госпитализируется в инфекционное отделение и должен находиться в изолированном боксе. Период выздоровления может затянуться до 21-28 дней.
Болезнь Девика
Оптикомиелит или болезнь Девика по хронической картине похож на рассеянный склероз. Это аутоиммунное заболевание, причины возникновения которого до сих пор не выяснены. В качестве одной из причин его развития отмечается увеличение проницаемости барьера между мозговой оболочкой и сосудом.
Некоторые аутоиммунные заболевания способны спровоцировать прогресс болезни Девика:
- ревматоидный артрит;
- системная красная волчанка;
- синдром Шегрена;
- дерматомиозит;
- тромбоцитопеническая пурпура.
Болезнь имеет специфическую симптоматику. Клинические проявления обусловлены нарушением проводящих импульсов. Кроме того, поражается зрительный нерв и ткань спинного мозга. В большинстве случаев болезнь заявляет о себе нарушением зрения:
- пелена перед глазами;
- боль в глазницах;
- размытость зрения.
При прогрессировании заболевания и отсутствии адекватного лечения больной рискует полностью потерять зрение. В некоторых случаях возможен регресс симптоматики с частичным восстановлением функций глаз. Иногда случается так, что миелит предшествует невриту.
Оптиконевромиелит имеет два варианта течения: поступательное нарастание симптоматики с одновременным поражением ЦНС. В редких случаях встречается монофазное течение болезни. Оно характеризуется устойчивым прогрессом и усугублением симптоматики. В этом случае повышен риск летального исхода. При правильно подобранном лечении патологический процесс замедляется, но при этом полное выздоровление не гарантируется.
Для выявления болезни Девика проводится комплекс мероприятий. Помимо стандартных диагностических процедур проводится люмбальная пункция с анализом ликвора, офтальмоскопия и МРТ позвоночника и головного мозга.
Лечение болезни Девика длительное и непростое. Главной задачей становится замедление прогрессирования заболевания и улучшение качества жизни больного. В рамках медикаментозной терапии применяются глюкокортикостероиды миорелаксанты, антидепрессанты, обезболивающие средства центрального действия. При тяжелом течении болезни пациент может столкнуться с такими осложнениями, как паралич ног, слепота или стойкое нарушение функций органов таза. При своевременном и правильном лечении гарантируется полное выздоровление.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Люди с иммунным дефицитом могут столкнуться с прогрессирующей многоочаговой мультифокальной лейкоэнцефалопатией. Это инфекционное заболевание, спровоцированное проникновением в организм вируса JC, относящегося к семейству Полиомавирусов. Особенностью патологии является то, что происходит несимметричное и многоочаговое поражение головного мозга. Вирусом поражаются оболочки нервных окончаний, состоящие из миелина. Поэтому данное заболевание принадлежит к группе демиелинизирующих патологий.
Почти 85% пациентов с таким диагнозом являются больными СПИДом или ВИЧ инфицированными. В группу риска входят пациенты со злокачественными опухолями.
Основные симптомы заболевания:
- перепады настроения;
- зрительные нарушения;
- парестезия и паралич;
- нарушение памяти.
Синдром Гийена-Барре
Все пациенты с таким диагнозом должны госпитализироваться в отделение интенсивной терапии. Поскольку существует риск развития дыхательной недостаточности и может потребоваться подключение к ИВЛ, в отделении должна быть реанимация. Также пациентам необходим должный уход с профилактикой пролежней и тромбоэмболии. Также необходимо купировать аутоиммунный процесс. С этой целью применяется плазмаферез и пульс-терапия иммуноглобулинами. Полное восстановление пациентов с таким диагнозом следует ожидать в течение 6-12 месяцев. Летальные исходы происходят из-за пневмонии, дыхательной недостаточности и тромбоэмболии легочной артерии.
Симптомы
Демиелинизация всегда проявляется неврологическим дефицитом. Этот признак свидетельствует о начале процесса разрушения миелина. В него вовлекается и иммунная система. Атрофируются ткани мозга — спинного и головного, а также наблюдается расширение желудочков.
Проявления демиелинизации находятся в зависимости от вида заболевания, причинных факторов и локализации очага. Симптоматика может отсутствовать, когда поражение мозгового вещества незначительное, до 20%. Это обусловлено компенсаторной функцией: здоровые ткани мозга выполняют задачи пораженных очагов. Неврологическая симптоматика проявляется редко — только при повреждении более 50% нервной ткани.
В качестве общих признаков демиелинизирующих заболеваний головного мозга отмечаются следующие:
- параличи;
- ограниченная подвижность мышц;
- тонические спазмы конечностей;
- нарушение функционирования кишечника и мочевого пузыря;
- псевдобульбарный синдром (нарушение произношения звуков, затруднение глотания, изменение голоса);
- нарушение мелкой моторики рук;
- онемение кожи и покалывание;
- зрительная дисфункция (снижение остроты зрения, размытость картинки, колебания глазных яблок, искажения цвета).
Нейропсихологические нарушения, характерные для рассматриваемой патологии, вызваны ухудшением памяти и снижением мыслительной деятельности, а также изменениями поведения и личностных качеств. Это проявляется развитием неврозов, депрессии, слабоумием органического генеза, эмоциональными перепадами, выраженной слабостью и снижением работоспособности.
Диагностика
Ранняя стадия течения патологии с отсутствием характерной симптоматики случайно обнаруживается во время диагностического обследования по другому поводу. Для подтверждения диагноза проводится нейровизуализация, а также невролог определяет степень нарушения проводящей функции мозга. Основным методом диагностики является магнитно-резонансная томография. На снимках можно отчетливо увидеть участки пораженной ткани. Если сделать ангиографию, то можно определить степень повреждения сосудов.
Лечение
Демиелинизирующее заболевание ЦНС относится к категории неизлечимых. Терапевтические меры направлены на улучшение качества жизни пациента и устранение симптоматики. Для проведения симптоматической терапии назначают:
- анальгетики;
- седативные средства;
- ноотропы;
- миорелаксанты;
- противовоспалительные препараты;
- нейропротекторные препараты.
Прогноз
Прогноз относительно жизни больного напрямую зависит от характера течения заболевания, вида патологии и объема пораженной мозговой ткани. Если заболевание было диагностировано на ранней стадии и начато адекватное лечение, то прогноз относительно жизни благоприятный. Тем не менее невозможно полностью излечить болезнь. Она может привести к инвалидности или окончиться летальным исходом.
Читайте также:


