Строения синапса схема передачи нервного импульса в холинергических синапсах
Холинергические синапсы представляют собой место, в котором происходит контакт двух нейронов или нейрона и эффекторной клетки, получающей сигнал. Синапс состоит из двух мембран – пресинаптической и постсинаптической, а также из синаптической щели. Передача нервного импульса осуществляется посредством медиатора, то есть вещества-передатчика. Происходит это в результате взаимодействия рецептора и медиатора на постсинаптической мембране. В этом заключаются основные функции холинергического синапса.
Медиатор и рецепторы
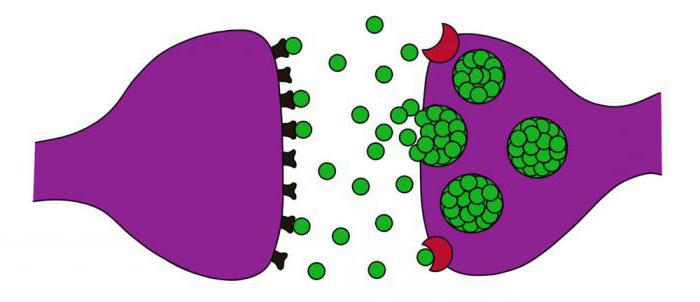
В парасимпатической НС медиатором является ацетилхолин, рецепторами – холинорецепторы двух типов: Н (никотин) и М (мускарин). М-холиномиметики, обладающие прямым типом действия, могут стимулировать рецепторы на мембране постсинаптического типа.
Синтез ацетилхолина осуществляется в цитоплазме нейронных холинергических окончаний. Он образуется из холина, а также ацетилкоэнзима-А, который имеет митохондриальное происхождение. Синтез происходит под действием цитоплазматического энзима холинацетилазы. В синаптических пузырьках происходит депонирование ацетилхолина. В каждом из таких пузырьков может находиться до нескольких тысяч ацетилхолиновых молекул. Нервный импульс провоцирует высвобождение молекул ацетилхолина в синаптическую щель. После этого он вступает во взаимодействие с холинорецепторами. Строение холинергического синапса уникально.
Строение
По данным, которые имеются у биохимиков, холинорецептор нервно-мышечного синапса может включать 5 белковых субъединиц, которые окружают ионный канал и проходят сквозь всю толщу мембраны, состоящей из липидов. Пара молекул ацетилхолина вступает во взаимодействие с парой α-субъединиц. Это приводит к тому, что открывается ионный канал и постсинаптическая мембрана деполяризуется.
Виды холинергических синапсов
Холинорецепторы по-разному локализованы и так же по-разному чувствительны к воздействию фармакологических веществ. В соответствии с этим различают:
- Маскариночувствительные холинорецепторы – так называемые М-холинорецепторы. Мускарин представляет собой алкалоид, присущий ряду ядовитых грибов, к примеру мухоморам.
- Никотиночувствительные холинорецепторы – так называемые Н-холинорецепторы. Никотин представляет собой алкалоид, содержащийся в листьях табака.
Их расположение
Первые располагаются в постсинаптической мембране клеток в составе эффекторных органов. Расположены они у окончаний постганглионарных парасимпатических волокон. Помимо этого они также есть в нейронных клетках вегетативных ганглиев и в коре головного мозга. Установлено, что М-холинорецепторы различной локализации гетерогенны, что обуславливает различную чувствительность холинергических синапсов к веществам фармакологической природы.

Виды в зависимости от расположения
Биохимики различают несколько видов М-холинорецепторов:
- Расположенные в вегетативных ганглиях и в ЦНС. Особенностью первых является то, что они локализованы вне синапсов – М1-холинорецепторы.
- Расположенные в сердце. Некоторые из них способствуют снижению высвобождения ацетилхолина – М2-холинорецепторы.
- Расположенные в гладких мышцах и в большей части эндокринных желез – М3-холинорецепторы.
- Расположенные в сердце, в стенках легочных альвеол, в ЦНС – М4-холинорецепторы.
- Расположенные в ЦНС, в радужной оболочке глаза, в слюнных железах, в мононуклеарных кровяных клетках – М5-холинорецепторы.
Воздействие на холинорецепторы
Большая часть эффектов, оказываемых известными фармакологическими веществами, влияющими на М-холинорецепторы, связана с взаимодействием этих веществ и постсинаптических М2- и М3-холинорецепторов.
Рассмотрим классификацию средств, стимулирующих холинергические синапсы, ниже.
Н-холинорецепторы располагаются в постсинаптической мембране нейронов ганглиев у окончаний каждого из преганглионарных волокон (в парасимпатических и симпатических ганглиях), в синокаротидной зоне, в мозговом слое надпочечников, в нейрогипофизе, в клетках Реншоу, в скелетных мышцах. Чувствительность различных Н-холинорецепторов неодинакова к веществам. Например, Н-холинорецепторы в структуре вегетативных ганглиев (рецепторы нейтрального типа) имеют значительные отличия от Н-холинорецепторов в скелетных мышцах (рецепторы мышечного типа). Именно такая их особенность позволяет избирательно блокировать ганглии специальными веществами. Например, курареподные вещества способны блокировать нервно-мышечную передачу.
Пресинаптические холинорецепторы и адренорецепторы участвуют в регуляции процесса высвобождения ацетилхолина в синапсах нейроэффекторной природы. Возбуждение этих рецепторов будет угнетать высвобождение ацетилхолина.
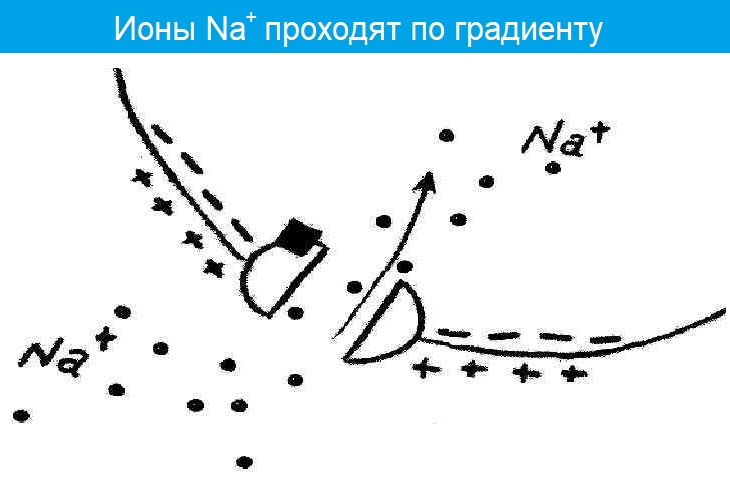
Ацетилхолин взаимодействует с Н-холинорецепторами и изменяет их конформацию, повышает уровень проницаемости постсинаптической мембраны. Ацетилхолин оказывает возбуждающий эффект на ионы натрия, которые проникают затем внутрь клетки, а это приводит к тому, что постсинаптическая мембрана деполяризуется. Изначально возникает локальный синаптический потенциал, который достигает определенной величины и начинает процесс генерации потенциала действия. После этого местное возбуждение, которое ограничено синаптической областью, начинает распространяться по всей клеточной мембране. Если происходит стимуляция М-холинорецептора, то при передаче сигнала значительную роль играют вторичные мессенджеры и G-белки.
Ацетилхолин действует в течение весьма короткого времени. Это обусловлено тем, что он стремительно гидролизуется под действием фермента ацетилхолинэстеразы. Холин, который образуется в процессе гидролиза ацетилхолина, в половине объема будет захвачен пресинаптическими окончаниями и транспортирован в цитоплазму клетки для последующего биосинтеза ацетилхолина.
Вещества, которые воздействуют на холинергические синапсы
Фармакологические и разнообразные химические вещества способны воздействовать на множество процессов, которые связаны с синаптической передачей:
- Процесс синтеза ацетилхолина.
- Процесс высвобождения медиатора. К примеру, карбахолин способен усиливать процесс выделения ацетилхолина, а ботулиновый токсин может препятствовать процессу высвобождения медиатора.
- Процесс взаимодействия между ацетилхолином и холинорецептором.
- Гидролиз ацетилхолина энзиматической природы.
- Процесс захвата холина, образованного в результате гидролиза ацетилхолина, пресинаптическими окончаниями. К примеру, гемихолиний способен угнетать нейроновый захват и транспортировку холина в цитоплазму клетки.
Классификация
Средства, стимулирующие холинергические синапсы, способны оказывать не только этот эффект, но и холиноблокирующий (угнетающий) эффект. В качестве основы для классификации подобных веществ биохимики используют направленность действия этих веществ на различные холинорецепторы. Если придерживаться такого принципа, то вещества, оказывающие влияние на холинорецепторы, можно классифицировать следующим образом:
- Вещества, которые оказывают влияние на М-холинорецепторы и Н-холинорецепторы: к холиномиметикам относятся ацетилхолин и карбахолин, а к холиноблокаторам – циклодол.
- Средства антихолинэстеразного характера. К ним относятся салицилат физостигмина, прозерин, гидробромид галантамина, армин.
- Вещества, которые влияют на холинергические синапсы. К холиномиметикам относятся гидрохлорид пилокарпина и ацеклидин, к холиноблокаторам – сульфат атропина, матацин, гидротартрат платифиллина, бромид ипратропия, гидробромид скопаламина.
Мы подробно рассмотрели средства, влияющие на холинергические синапсы.
Синапсы( и соответственно нервные волокна), в которых передача импульсов осуществляется с помощью ацетилхолина, получили название холинергических.
Холинергический синапс состоит из:
пресинаптического окончания - синаптической бляшки, в везикулах которой содержится ацетилхолин
синаптической щели, которая содержит фермент - ацетилхолинэстреразу
постсинаптической мембраны, на которой расположены м- или н- холинорецепторы -
Состояние постсинаптической мембраны меняется следующим образом:
1 стадия- поляризации, когда мембрана полупроницаема и готова воспринимать возбуждение
2 стадия- деполяризации, когда мембрана перезаряжается и органы возбуждаются
3 стадия - реполяризации, когда уменьшается количество ацетилхолина за счет его разрушения ацетилхолинэстреразой и мембрана вновь становится непроницаемой для ионов.
Этапы медиации.
1. Синтез и депонирование медиатора. Ацетилхолин синтезируется в пресинаптических окончаниях из ацетил-КоА и холина. В цитоплазме пресинаптического окончания содержится большое количество митохондрий, здесь путем окислительного декарбоксилирования a-кетокислот синтезируется ацетил-КоА. Холин поступает в клетку извне благодаря специальному трансмембранному переносчику. Транспорт холина в нейрон сопряжен с переносом ионов натрия и может быть блокирован гемихолином.
Таблица 2. Сравнительная характеристика холинорецепторов клетки.
| Тип | Агонист | Антагонист | Локализация | Функция | Механизм |
| НМ | PTMA Никотин | d-тубокурарин a-бунгаротоксин | Скелетные мышцы | Деполяризация концевой пластинки, сокращение мышцы | Открытие Na + -канала |
| НН | DMPP Эпибатидин Никотин | Триметафан | Вегетативные ганглии Мозговое вещество надпочечников Каротидные клубочки ЦНС | Деполяризация и возбуждение постганглионарного нейрона Секреция адреналина и норадреналина Рефлекторная стимуляция дыхательного центра Контроль психических и моторных функций, когнитивные процессы. | Открытие Na + , K + и Са 2+ -каналов |
| М1 | Мускарин Оксотреморин | Атропин Пирензепин | Вегетативные ганглии (пресинаптически) ЦНС | Деполяризация, усиление секреции медиатора (поздний постсинаптический потенциал) Контроль психических и моторных функций, когнитивные процессы. | Активация фосфолипазы С через Gq белок и синтез IP3 (выход Са 2+ из депо), DAG (активация Са 2+ -каналов, протеинкиназы С). |
| М2 | Мускарин Метахолин | Атропин Метоктрамин Трипитрамин | Миокард | САУ: снижение автоматизма; АВУ: снижение проводимости; Рабочий миокард: незначительное снижение сократимости. | Через a-единицу Gi-белка торможение аденилатциклазы (”цАМФ). Через bg-единицы Gi-белка активация К + -каналов и блокада L-типа Са 2+ -каналов. |
| М3 | Бетанехол | Атропин Дарифенацин HHSDP | Гладкие мышцы Железы Эндотелий сосудов (внесинаптически) | Сокращение, “ тонуса Повышение секреции Секреция NO и дилятация сосуда | Подобен М1 |
| М4 | ? | ? | Сердце Альвеолы ЦНС | ? | Подобен М2 |
| М5 | ? | ? | Слюнные железы Радужка глаза Моноциты ЦНС | ? | Подобен М1 |
Примечание: a-бунгаротоксин – яд тайваньской гадюки (Bungaris multicintus) и кобры (Naja naja).
АВУ – атриовентрикулярный узел
САУ – синоаурикулярный узел
Синтез ацетилхолина проводит особый фермент холинацетилтрансфераза, путем ацетилирования холина. Образовавшийся ацетилхолин поступает в везикулы при помощи антипортера переносчика в обмен на протон. Работа этого переносчика может быть заблокирована векзамиколом. Обычно в каждой везикуле содержится от 1.000 до 50.000 молеукл ацетилхолина, а общее число везикул в пресинаптическом окончании достигает 300.000.
2. Выделение медиатора. Во время фазы покоя, через пресинаптическую мембрану выделяются единичные кванты медиатора (изливается содержимое 1 везикулы). Одна молекула ацетилхолина способна вызвать изменение потенциала мембраны всего на 0,0003 мВ, а то количество, которое содержится в 1 везикуле – на 0,3-3,0 мВ. Такие миниатюрные сдвиги не вызывают развития биологического ответа, но поддерживают физиологическую реактивность, тонус ткани-мишени.

Схема 4. Передача сигнала в холинергическом синапсе. ХАТ – холинацетилтрансфераза, В1 – тиамин, Ach – ацетилхолин, М1-Хр – М1-холинорецепторы, АХЭ – ацетилхолинэстераза, ФлС – фосфолипаза С, PIP2 – фосфатидилинозитол бифосфат, IP3 – инозитол трифосфат, DAG – диацилглицерол, PkC – протеинкиназа С, Б – белок-фермент, Б-РО4 – фосфорилированная форма белка-фермента.
3. Развитие биологического ответа. В синаптической щели путем диффузии ацетилхолин поступает к постсинаптической мембране, где активирует холинорецепторы. При взаимодействии с Н-холинорецепторами происходит открытие натриевых каналов и на постсинаптической мембране генерируется потенциал действия.
В том случае, если ацетилхолин активирует М-холинорецепторы, сигнал передается через систему G-белков на фосфолипазу С, ионные каналы К+ и Са2+ и все это приводит в конечном итоге к изменению поляризации мембраны, процессов фосфорилирования внутриклеточных белков.
Помимо постсинаптической мембраны ацетилхолин может воздействовать на холинорецепторы пресинаптической мембраны (М1 и М2). При активации ацетилхолином М1-пресинаптического рецептора выделение медиатора усиливается (положительная обратная связь). Роль М2-холинорецепторов на пресинапетической мембране недостаточно ясна, полагают, что они могут тормозить секрецию медиатора.
Развитие биологического ответа можно вызвать при введении лекарственных веществ, которые стимулируют холинорецепторы или предотвратить, если ввести средства, блокирующие эти рецептры. Повлиять на развитие эффекта можно и не затрагивая рецепторы, а воздействуя лишь на пострецепторные механизмы:
· Токсин коклюшной палочки может активировать Gi-белок и снижать активность аденилатциклазы на затрагивая М-холинорецептор;
· Токсин холерного вибриона может активировать Gs-белок и повышать активность аденилатциклазы;
· Дитерпен форсколин из растения Coleus forskohlii способен непосредственно активировать аденилатциклазу в обход рецепторов и G-белков.
4. Окончание действия медиатора. Время существования ацетилхолина в синаптической щели составляет всего 1 мС, после чего он подвергается гидролизу до холина и остатка уксусной кислоты. Уксусная кислота быстро утилизируется в цикле Кребса. Холин в 1.000-10.000 раз менее активен, чем ацетилхолин, 50% его молекул подвергаются обратному захвату в аксон для ресинтеза ацетилхолина, остальная часть молекул включается в состав фосфолипидов.
Гидролиз ацетилхолина осуществляет особый фермент – холинэстераза. В настоящее время известно 2 его изоформы:
· Ацетилхолинэстераза (AChE) или истинная холинэстераза – осуществляет высокоспецифичный гидролиз ацетилхолина и локализуется на постсинаптической мембране холинергических синапсов.
· Бутирилхолинэстераза (ButChE) или псевдохолинэстераза – осуществляет низкоспецифичный гидролиз эфиров. Локализуется в плазме крови и перисинаптическом пространстве.
Типы холинорецепторов.
Холинорецепторы разной локализации обладают неодинаковой чувствительностью к фармакологическим веществам. На этом основано выделение так называемых мускариночувствительных и никотиночувствительных холинорецепторов1 (соответственно м-
холинорецепторы и н-холинорецепторы). М-холинорецепторы расположены в постсинаптической мембране клеток эффекторных органов у окончаний постганглионарных холинергических (парасимпатических) волокон . Выделяют м1- холинорецепторы (в вегетативных ганглиях и в ЦНС), м2-холинорецепторы (основной подтип м- холинорецепторов в сердце)3 и м3-холинорецепторы (в гладких мышцах, большинстве экзокринных желез). Н-холинорецепторы находятся в постсинаптической мембране ганглионарных нейронов у окончаний всех преганглионарных волокон (в симпатических и парасимпатических ганглиях), мозговом слое надпочечников, синокаротидной зоне, концевых пластинках скелетных мышц и
ЦНС (в нейрогипофизе, клетках Реншоу и др.).
Механическое удерживание земляных масс: Механическое удерживание земляных масс на склоне обеспечивают контрфорсными сооружениями различных конструкций.


Папиллярные узоры пальцев рук - маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Поперечные профили набережных и береговой полосы: На городских территориях берегоукрепление проектируют с учетом технических и экономических требований, но особое значение придают эстетическим.
Механизм химической передачи нервных импульсов через синапс сводится к тому, что содержимое синаптических пузырьков (медиатор) поступает в виде небольших порций (квантов) в синаптическую щель и взаимодействует затем с рецепторными белками постсинаптической мембраны. Это вызывает деполяризацию мембраны и возбуждение следующего нейрона. Ультраструктурные особенности синапса и механизм передачи импульсов определяют строгую однонаправленность передачи импульсов, что лежит в основе проведения импульсов по рефлекторным дугам.
В зависимости от того, какое вещество выполняет роль нейромедиатора, синапсы подразделяются на холинергические (медиатор — ацетилхолин), адренергические (адреналин и норадреналин), дофаминергические (дофамин), серотонинергические (серотонин), пептидергические (медиаторы — пептиды и аминокислоты, например, мет-энкефалин, гамма-аминомасляная кислота, глицин и др.).
Нейрохимические синапсы подразделяются в функциональном отношении на две противоположные по своему значению группы — возбуждающие и тормозные. Свойства этих синапсов зависят как от медиаторов, так и от ультраструктурных особенностей синапсов. Так, некоторые медиаторы (например, глутамат) характерны для возбуждающих синапсов, а в тормозных синапсах медиатором является гамма-аминомасляная кислота. Предполагают, что в возбуждающих синапсах к постсинаптической мембране прилежит электронно-плотное вещество, в связи с чем синапс приобретает асимметричное строение.
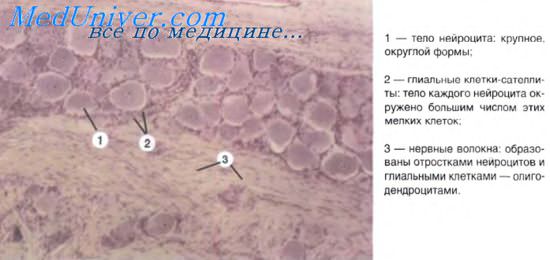
В пресинаптических частях таких соединений содержатся круглые синаптические пузырьки. Тормозные синапсы имеют симметричное строение. Синаптическая щель у них сужена и в пресинаптической части содержатся уплощенные синаптические пузырьки.
Кроме нейрохимических синапсов между нервными клетками (преимущественно между дендритами или телами нейронов) возникают электротонические синапсы. Последние у млекопитающих встречаются редко и по строению соответствуют щелевым контактам. Они проводят возбуждение благодаря формированию трансмембранных каналов — коннексонов.
Каждый нейрон на своей поверхности имеет огромное количество (до 10000) синапсов. Интеграция импульсов в пределах отдельного нейрона происходит так: от синапсов, расположенных на дендритах и теле, по его плазмолемме передается импульс к аксонному холмику (генераторному пункту нейрона), где путем суммирования всех возбуждающих и тормозных импульсов возникает результирующий потенциал действия.
Синаптические структуры обладают высокой чувствительностью к действию токсических факторов, в том числе психотропных отравляющих веществ. Их изменения играют важную роль в механизмах реактивности нервных тканей.
Рецепторные нервные окончания подразделяются на две группы: экстерорецепторы, воспринимающие раздражения из внешней среды, и интерорецепторы, служащие для восприятия раздражений из внутренней среды организма. В зависимости от специфичности раздражения, воспринимаемого рецептором, различают следующие чувствительные нервные окончания: механорецепторы, барорецепторы, хеморецепторы, терморецепторы, болевые рецепторы (ноцицепторы). Все рецепторы по особенностям их строения подразделяют на свободные и несвободные нервные окончания.
Первые из них состоят только из конечных разветвлений периферического отростка чувствительного нейрона; вторые — имеют в составе рецептора кроме нервного отростка глиальный компонент, а нередко и соединительнотканную капсулу. В последнем случае несвободные рецепторные окончания называют инкапсулированными. К числу таких рецепторов относятся пластинчатые, осязательные тельца, концевые колбы, мышечные веретена и др.
Эффекторные нервные окончания подразделяются на двигательные и секреторные. Двигательный, или моторный, эффектор передает нервные импульсы на рабочие органы и ткани. В скелетных мышцах они называются нервно-мышечными (аксомышечными) окончаниями. Терминальное разветвление аксона двигательного нейрона заканчивается булавовидным расширением. Оно соответствует пресинаптической части нервно-мышечного синапса, содержит скопление синаптических пузырьков и митохондрий, ограничено пресинаптической мембраной характерного строения.
Плазмолемма мышечного волокна в этой области образует многочисленные складки и углубления. В постсинаптической части волокна находится зернистая саркоплазма с большим количеством митохондрий и овальных ядер. Синаптическая щель имеет ширину 50-100 нм. У человека медиатором в нервно-мышечных синапсах является ацетилхолин. Моторные окончания в гладкой мышечной ткани, а также секреторные эффекторы имеют вид тонких пучков аксонов или их одиночных терминалей, прилежащих к клеткам иннервируемых тканей.
Возрастные изменения нервных тканей связаны с постепенным уменьшением запаса нервных клеток, особенно — чувствительных нейронов, а также снижением уровня метаболических процессов, что выражается в закономерном накоплении включений липофусцина ("пигмент изнашивания") в нейроплазме.
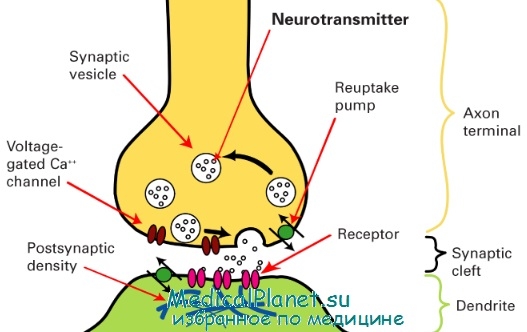
Схема строения синапса
1. Процесс синтеза и депонирования медиатора.
2. Высвобождение медиатора.
3. Передача возбуждения на постсинаптическую мембрану.
4. Трансформация влияния медиатора в эффект.
5. Утилизация медиатора.
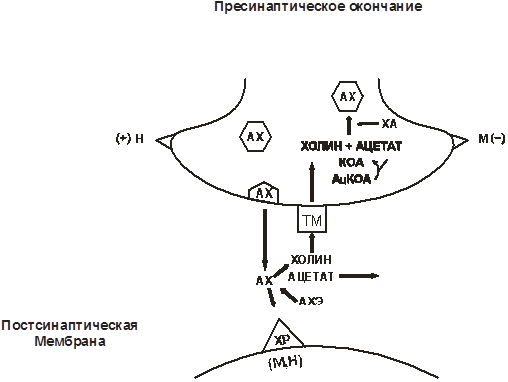
Рис. 11. Процессы, происходящие в холинергическом нервном синапсе
АХ — ацетилхолин, ХР — холинорецептор, М — М-холинорецептор, Н — Н-холинорецептор, АХЭ — ацетилхолинэстераза, Ац-КоА — ацетилкоэнзим А (митохондрий), КоА — коэнзим А (митохондрий), ХА — холинацетилаза (холинацетилтрансфераза), ТМ — транспортный механизм, (+) — активация, (-) — торможение.
Синтез. АХ образуется в цитоплазме холинергических нейронов из холина и ацетилкоэнзима А под влиянием ацетилхолинтрансферазы. Накапливается в везикулах пресинаптическпх окончаний, после чего выделяется в синаптическую щель под действием нервного импульса. Медиатор связывается с рецепторами на постсинаптической мембране и это связывание индуцирует цепь изменений, приводящих к изменению функций клетки (рис. 11).
Судьба медиатора. Присутствующий в синапсе фермент холинэстераза катализирует расщепление АХ на холин и уксусную кислоту. Холин транспортируется в нервное окончание, где используется для синтеза медиатора. Уксусная кислота метаболизируется в тканях.
Описанные выше механизмы в синапсе протекают очень быстро. Регулирование высвобождения АХ из пресинапса в синаптическую щель осуществляется по механизму отрицательной обратной связи путем стимулирования М-ХР пресинаптической мембраны. Экзоцитоз ацетилхолина при этом уменьшается.
Механизмы холинергической передачи нервного импульса:
¾ нервный импульс вызывает деполяризацию пресинаптической мембраны, что увеличивает ее проницаемость для Са ++ ;
¾ ионы Са ++ входят внутрь пресинаптического окончания и активируют механизмы высвобождения АХ в синаптическую щель;
Молекулярные механизмы трансформации влияния АХ в эффект разнообразны.
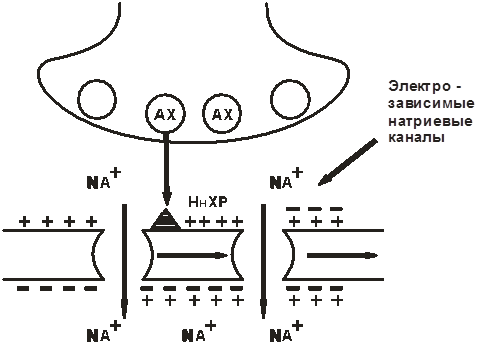
Рис. 12. Нн-холинорецептор нервного типа
Нн-холинорецептор нервного типа (ЦНС, вегетативные ганглии, синокаротидная зона, хромаффинная ткань надпочечников). После связывания АХ с Нн-холинорецепторами, открываются Na + -каналы и Na устремляется внутрь клетки, неся положительный заряд. Постсинаптическая мембрана деполяризуется. Возникает потенциал действия, который смещается по мембране нейрона, открывая электрозависимые Na + -каналы. Возникает нервный импульс в постганглионарном волокне (рис. 12).
Нм-холинорецептор мышечного типа (мембраны клеток скелетной мускулатуры). Начальные процессы схожи, но открываются электрозависимые Са ++ -каналы. Внутрь мышечного волокна поступают ионы Са ++ , происходит высвобождения Са ++ из саркоплазматического ретикулума. Уровень Са ++ повышается, что индуцирует сокращение мышц (рис. 13).
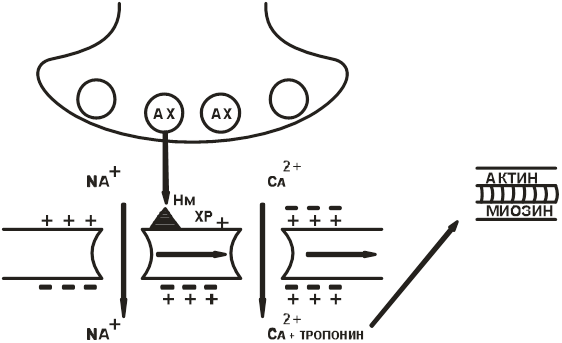
Рис. 13. Нмхолинорецептор мышечного типа
М2-холинорецептор (постсинаптическая мембрана клеток сердца). Ацетилхолин, возбуждая М2-ХР, связанный с двумя G-белками, вызывает следующие эффекты (рис. 14):
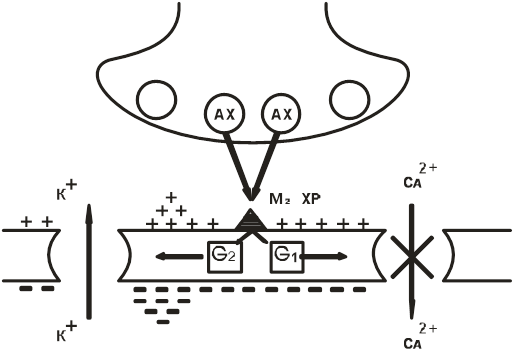
Рис. 14. М2-холинорецептор
¾ снижение транспорта Са ++ внутрь миокардиоцитов, что приводит к снижению сократимости миокарда;
¾ усиливает выход ионов К + из миокардиоцитов, что приводит к гиперполяризации мембран и в результате снижается ЧСС.
М3-холинорецептор (мембраны ГМК и клетки экзокринных желез). Ацетилхолин стимулирует М3-ХР, связанные с G-белком. Активируется фосфолипаза-С, что катализирует расщепление ФИДФ (фосфатидилинозитолдифосфата) на ИТФ (инозитолтрифосфат) и ДАГ (диацилглицерол). ИТФ, поступая в цитоплазму ГМК, высвобождает Са ++ из кавелл.
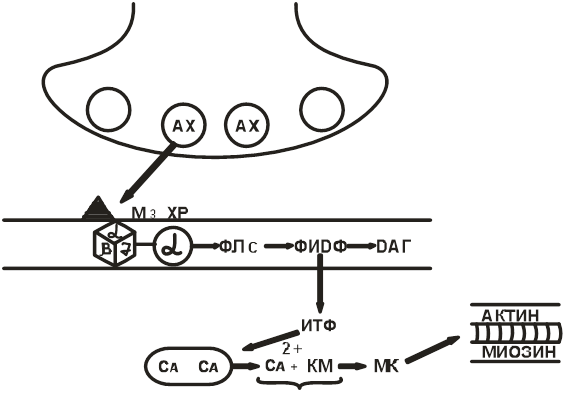
Рис. 15. М3-холинорецептор
Са ++ связывается с кальмодулином, активирует миозинкиназу (МК), катализирующую фосфорилирование легких цепей миозина, что приводит к сокращению клетки (рис. 15). Аналогичным образом передается импульс в синапсах секреторных желез.
Классификация лекарственных средств, влияющих
на холинергическую иннервацию:
I. Холинергические агонисты (холиномиметики):
Теория по нормальной физиологии на тему: Синапс. Физиология мышечных волокон. В данной статье рассматривается механизм синаптической передачи, НМС…
При создании данной страницы использовалась лекция по соответствующей теме, составленная Кафедрой Нормальной физиологии БашГМУ
Синапс — это специфическое место контакта двух возбудимых систем (клеток) для передачи возбуждения.
По способу передачи сигналов:
- механические,
- химические,
- электрические.
По виду медиатора: холинэргические и др.
Нервно-мышечный синапс (НМС) — химический, передача с помощью медиатора ацетилхолина.
Синонимы к слову НМС:
- Нервно-мышечное соединение;
- Моторная концевая пластинка.

Аксоны нервных клеток на своих окончаниях теряют миелиновую оболочку , ветвятся, и концевые веточки аксона утолщаются. Это пресинаптическая терминаль или бляшка или пуговка , которая погружается в углубление на поверхности мышечного волокна.
Покрывающая концевую веточку аксона поверхностная мембрана называется пресинаптической мембраной , т.е. это мембрана, покрывающая поверхность синаптической бляшки (терминали аксона).
Мембрана, покрывающая мышечное волокно в области синапса, называется постсинаптической мембраной , или концевой пластинкой. Она имеет извитую структуру, образуя многочисленные складки, уходящие вглубь мышечного волокна, за счет чего увеличивается площадь контакта.
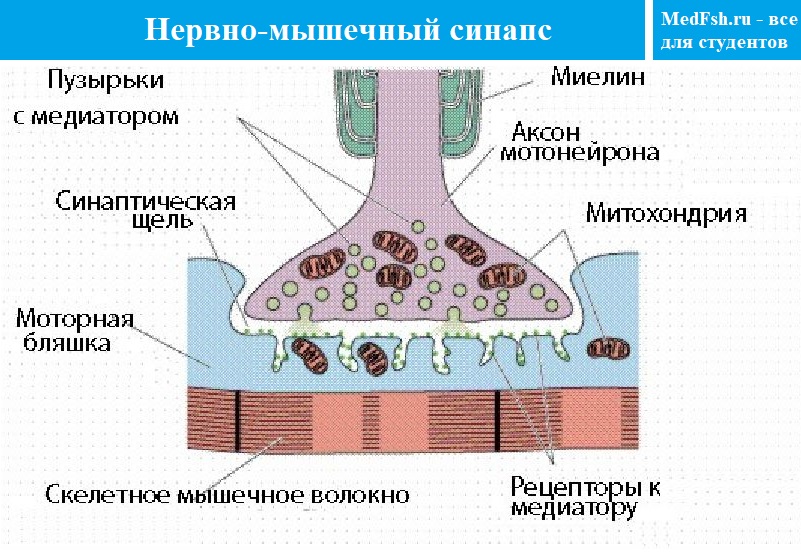
На постсинаптической мембране находятся белковые структуры — рецепторы , способные связывать медиатор . В одном синапсе количество рецепторов достигает 10-20 млн.
Между пре- и постсинаптическими мембранами находится синаптическая щель , размеры ее в среднем 50 нм, она открывается в межклеточное пространство и заполнена межклеточной жидкостью .
В синаптической щели находится мукополисахаридное плотное вещество в виде полосок, мостиков и содержится фермент ацетилхолинэстераза .
В пресинаптической терминали находится большое количество пузырьков или везикул , заполненных медиатором — химическим веществом посредником, осуществляющим передачу возбуждения.
В нервно-мышечном синапсе медиатор — ацетилхолин (АХ).
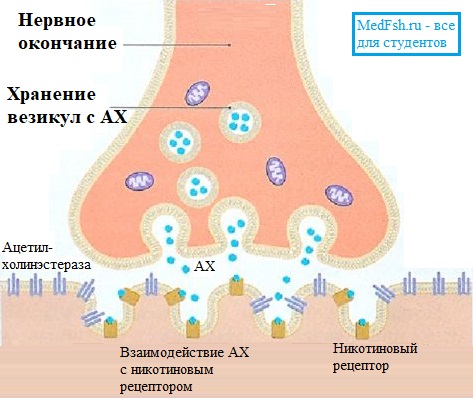
АХ синтезируется из холина и уксусной кислоты (ацетил-коэнзима А) с помощью фермента холинэстеразы. Эти вещества перемещаются из тела нейрона по аксону к пресинаптической мембране. Здесь в пузырьках происходит окончательное образование АХ.
3 фракции медиатора:
- Первая фракция — доступная — располагается рядом с пресинаптической мембраной.
- Вторая фракция — депонированная — располагается над первой фракцией.
- Третья фракция — диффузно рассеянная — наиболее удаленная от пресинаптической мембраны.
Механизм синаптической передачи

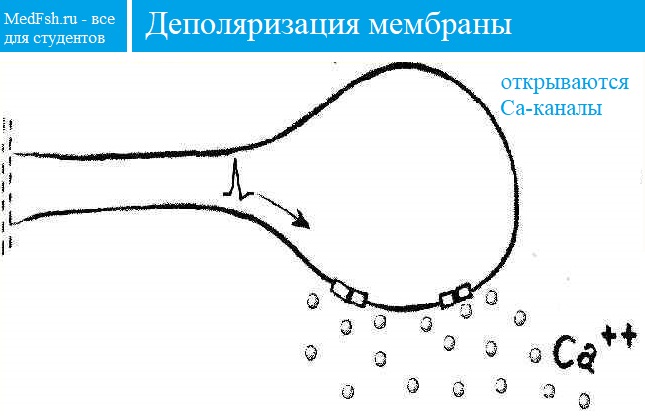
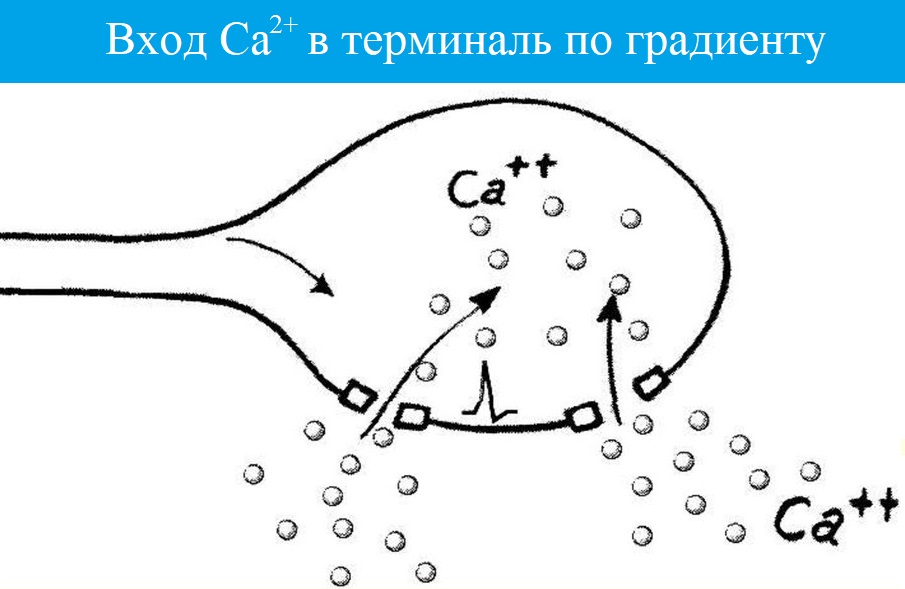
Ионы Ca вызывают образование специального белкового комплекса , который включает в себя везикулу и структуры, расположенные непосредственно около пресинаптической мембраны.
Они связаны между собой так называемыми белками экзоцитоза.
Часть белков расположена на везикулах (синапсин, синаптотагмин, синаптобревин), а часть — на пресинаптической мембране (синтаксин, синапсо-ассоциированный белок). Данный комплекс получил название секретосома .
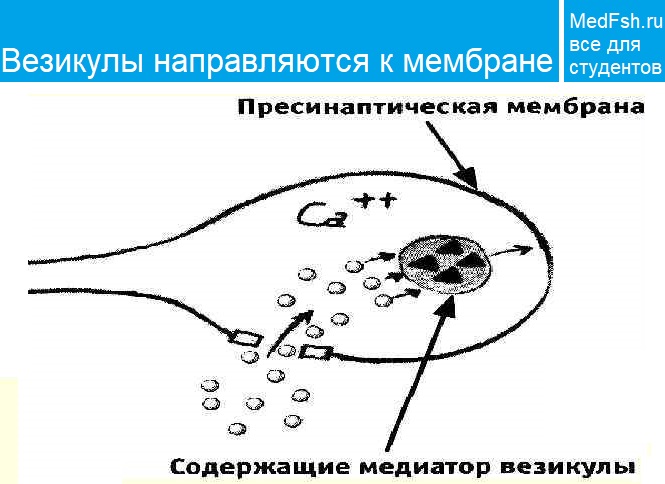
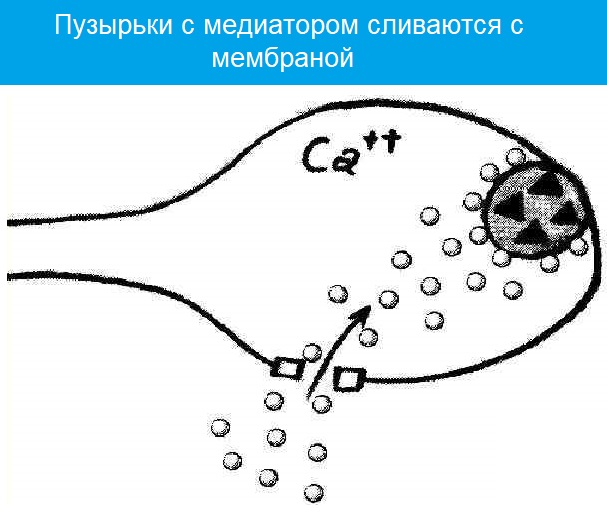
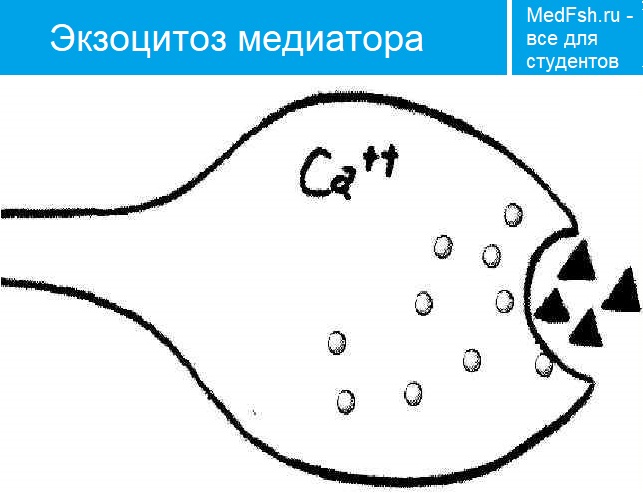
Излитию содержимого пузырька в щель способствует белок синаптопорин , формирующий канал, по которому идет выброс медиатора.
Квант медиатора — количество молекул, содержащихся в одной везикуле.
На 1 ПД выбрасывается 100 квантов АХ.
На постсинаптической мембране возникает потенциал концевой пластинки (ПКП). Он является аналогом локального ответа (ЛО).
Потенциал действия на постсинаптической мембране не возникает ! Он формируется на соседней мембране мышечного волокна.
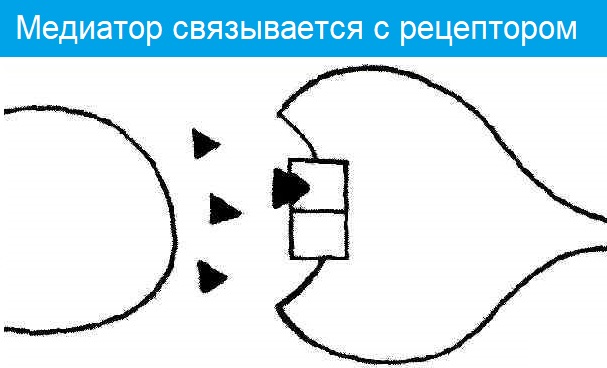
- связывание с рецептором,
- разрушение ферментов (ацетилхолинэстеразой),
- обратное поглощение в пресинаптическую мембрану,
- вымывание из щели и фагоцитоз.
События в синапсе :
- ПД приходит к терминали аксона;
- Он деполяризует пресинаптическую мембрану;
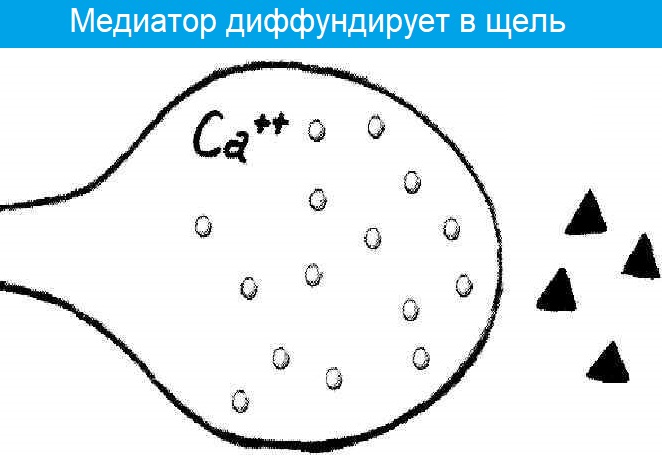
- Ca2+ входит в терминаль, что приводит к выделению АХ;
- В синаптическую щель выделяется медиатор АХ;
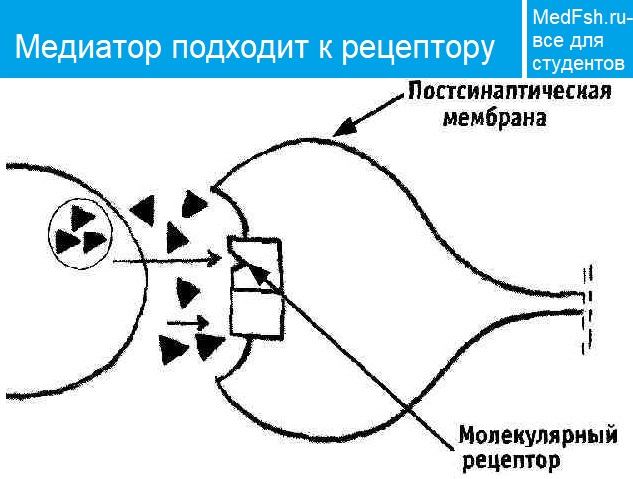
- Он диффундирует в щель и связывается с рецепторами постсинаптической мембраны;
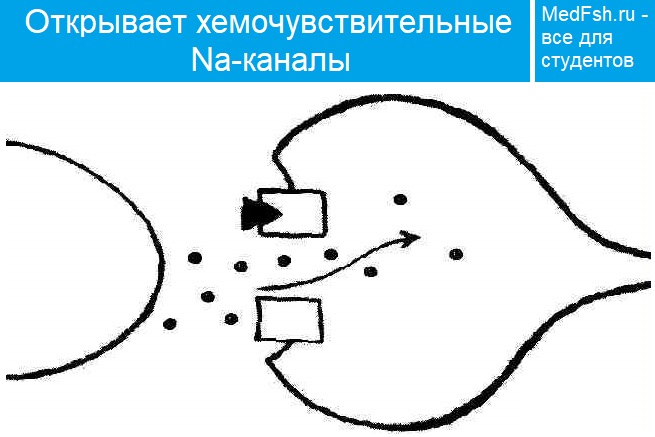
- Меняется проницаемость постсинаптической мембраны для ионов Na+;
- Ионы Na+ проникают в постсинаптическую мембрану и уменьшают ее заряд — возникает потенциал концевой пластинки (ПКП) .
На самой постсинаптической мембране ПД возникнуть не может, так как здесь отсутствуют потенциалзависимые каналы, они являются хемозависимыми!
- ПКП суммируются и достигают КУД на соседнем участке мышечного волокна, что приводит к возникновению ПД и его распространению по мышечному волокну (около 5 м/с).
Достигнув пороговой величины, то есть КУД, ПКП возбуждает соседнюю (внесинаптическую) мембрану мышечного волокна за счет местных круговых токов.

Особенности проведения возбуждения в нервно-мышечном синапсе
Одностороннее проведение возбуждения — только в направлении от пресинаптического окончания к постсинаптической мембране.
Суммация возбуждения соседних постсинаптических мембран.
Синаптическая задержка — замедление в проведении импульса от нейрона к мышце составляет 0,5-1 мс. Это время затрачивается на секрецию медиатора, его диффузию к постсинаптической мембране, взаимодействие с рецептором, формирование ПКП, их суммацию.
Низкая лабильность — она составляет 100-150 имп/с для сигнала, что в 5-6 раз ниже лабильности нервного волокна.
Чувствительность к действию лекарственных веществ, ядов, БАВ, выполняющих роль медиатора.
Утомляемость химических синапсов — выражается в ухудшении проводимости вплоть до блокады в синапсе при длительном функционировании синапса. Главная причина утомляемости — исчерпание запасов медиатора в пресинаптическом окончании.
Законы проведения возбуждения по нервам:
- Закон функциональной целостности нерва.
- Закон изолированного проведения возбуждения.
- Закон двустороннего проведения возбуждения.
В зависимости от скорости проведения возбуждения нервные волокна подразделяются на 3 группы: A, B, C. В группе A выделяют 4 подгруппы: альфа, бетта, гамма и сигма.
Физиология мышечных волокон
- скелетная (40-50% массы тела),
- сердечная (менее 1%),
- гладкая (8-9%).
Физиологические свойства скелетных мышц:
- Возбудимость — способность отвечать на действие раздражителя возбуждением.
- Проводимость — способность проводить возбуждение из места его возникновения к другим участкам мышцы.
- Лабильность — способность мышцы сокращаться в соответствии с частотой действия раздражителя (200-300 Гц для скелетной мышцы).
- Сократимость — для мышцы является специфическим свойством — это способность мышцы изменять длину или напряжение в ответ на действие раздражителя.
Физические свойства скелетных мышц:
- Растяжимость — способность мышцы изменять длину под действием растягивающей силы.
- Эластичность — способность мышцы восстанавливать первоначальную длину или форму после прекращения действия растягивающей силы.
- Силы мышц — способность мышцы поднять максимальный груз.
- Способность мышцы совершать работу.
Режимы сокращения:
- Изотонический,
- Изометрический,
- Ауксотонический.
Изотонический режим — сокращение мышцы происходит с изменением ее длины без изменения напряжения (тонуса) (напр.: сокращение мышц языка).
Изометрический режим — длина постоянная, увеличивается степень мышечного напряжения (тонуса) (напр.: при поднятии непосильного груза).
Ауксотонический режим — одновременно изменяется длина и напряжение мышцы (характерен для обычных двигательных актов).
Механизм сокращения поперечно-полосатых мышц
Любая скелетная мышца состоит из мышечных волокон, которые, в свою очередь, состоят из множества тонких нитей — миофибрилл , расположенных продольно. Каждая миофибрилла состоит из протофибрилл — нитей сократительных белков: миозина (миозиновая протофибрилла), актина (актиновая протофибрилла).
Кроме сократительных белков в миофибрилле имеются два регуляторных белка: тропомиозин и тропонин .
Миозиновые волокна соединены в толстый пучок, от которого в торону актиновых нитей отходят поперечные мостики. У каждого мостика выделяют шейку и головку.
Нить актина располагается в виде 2 скрученных ниток бус. На ней имеются актиновые центры.
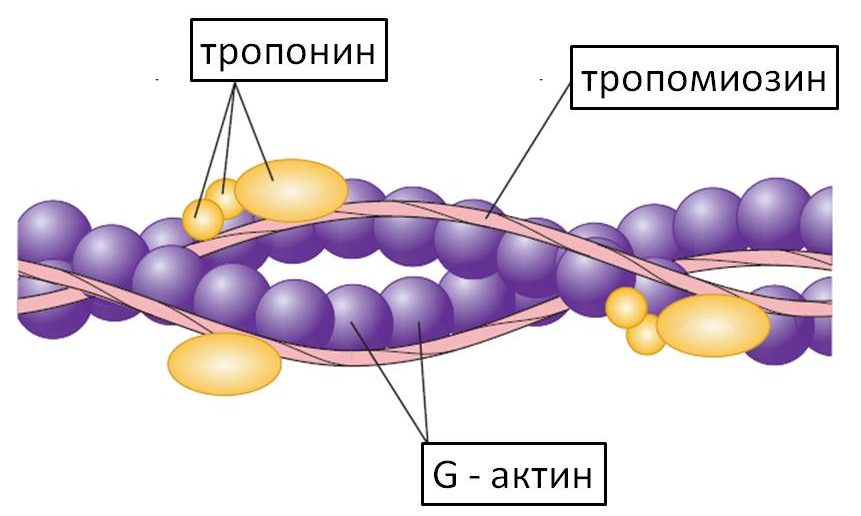
Тропомиозин в виде спиралей оплетает поверхность актина, закрывая в покое ее центры. Одна молекула тропомиозина контактирует с 7 молекулами актина.
Тропонин образует утолщение на конце каждой нити тропомиозина.
Под влиянием возникшего в мышечном волокне ПД из саркоплазматического ретикулума (СПР — депо Ca2+) высвобождаются ионы Ca. Кальций связывается с тропонином, который смещает тропомиозиновый стержень, что приводит к открытию актиновых центров.
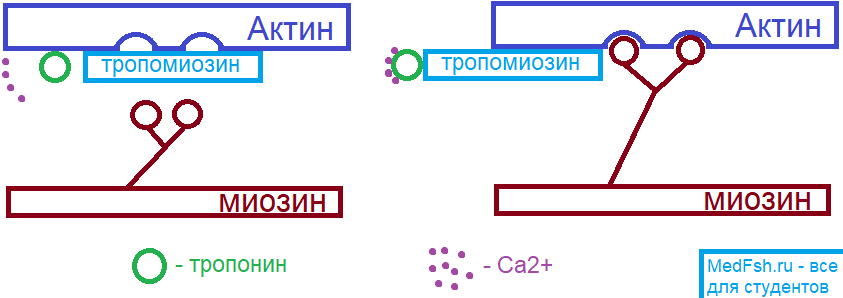
В результате, к актиновым центрам присоединяются головки поперечных миозиновых мостиков.
Процесс расслабления происходит в обратной последовательности с использованием энергии АТФ за счет функционирования кальциевого насоса.
При отсутствии повторного импульса ионы Ca не поступают из СПР. В результате отсутствия Ca-тропонинового комплекса, тропомиозин возвращается на свое прежнее место, блокируя актиновые центры актина. Актиновые протофибриллы легко скользят в обратном направлении благодаря эластичности мышцы, и мышца удлиняется (расслабляется).
Гладкие мышцы
Гладкие мышцы — это мышцы, формирующие слой стенок полых внутренних органов. Они построены из веретенообразных одноядерных мышечных клеток без поперечной исчерченности за счет хаотичного расположения миофибрилл.
Особенности гладких мышц:
- Иннервируются волокнами вегетативной нервной системы (ВНС);
- Обладают низкой возбудимостью:
- Обладают низкой величиной МП (мембранного потенциала) — -50 — -60 мВ из-за более высокой проницаемости для ионов Na+
- ПД (потенциал действия) отличается меньшей амплитудой и большей длительностью. Он формируется в основном за счет ионов Ca2+
- Медленная проводимость:
Клетки в гладких мышцах функционально связаны между собой посредством щелевидных контактов — нексусов, которые имеют низкое электрическое сопротивление. За счет этих контактов ПД распространяется с одного мышечного волокна на другое, охватывая большие мышечные пласты, и в реакцию вовлекается вся мышца.
Гладкие мышцы способны осуществлять относительно медленные ритмические и длительные тонические сокращения.
Медленные ритмические сокращения обеспечивают перемещение содержимого органа из одной области в другую.
Длительные тонические сокращения, особенно сфинктеров полых органов, препятствуют выходу из них содержимого.
Это способность сохранять приданную им при растяжении или деформации форму. Благодаря пластичности гладкая мышца может быть полностью расслаблена как в укороченном, так и в растянутом состоянии.
Особенность гладких мышц, отличающая их от скелетных. Благодаря автоматии гладкие мышцы могут сокращаться в условиях отсутствия иннервации . Важную роль в этом играет растяжение.
Растяжение является адекватным раздражителем для гладкой мускулатуры. Сильное и резкое растяжение гладких мышц вызывает их сокращение.
Сравнительная характеристика скелетных и гладких мышц:
Читайте также:


