Восстановление спинного мозга стволовыми нервными клетками

Препарат на основе двух генов поможет восстановить двигательную активность пациента после травмы спинного мозга. Революционная разработка российских ученых защищает нейроны от гибели, стимулирует рост кровеносных сосудов и новых нервных волокон. Эффективность препарата показали проведенные на крысах эксперименты — спустя несколько месяцев после начала лечения животные смогли ходить на прежде парализованных конечностях. Для того чтобы начать доклинические испытания, исследователям осталось решить проблемы с финансированием.
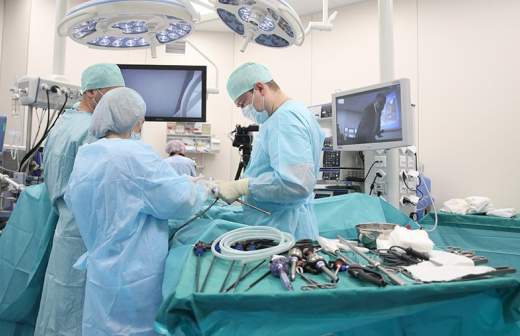
Травма спинного мозга, возникшая в результате аварии, несчастного случая или падения с высоты, нередко приводит к потере чувствительности и способности двигать частями тела ниже места поражения. Сейчас помочь мышцам усилить сигнал может только экзоскелет и нейропротезы, и то при условии, что не полностью утрачена связь между спинным и головным мозгом. Исследователи из Казанского федерального университета (КФУ) создали препарат, который позволяет успешно бороться с травмами спинного мозга, несмотря на наличие осложняющих выздоровление факторов.
Дело в том, что при повреждении спинного мозга организм постепенно наращивает в месте травмы рубец, состоящий из соединительной ткани. Он необходим для своеобразной фиксации места повреждения, но в дальнейшем препятствует росту аксонов, отростков нервных клеток, с помощью которых осуществляется связь с другими клетками.
Перед исследователями стояла задача создать такой препарат, который снижал бы скорость образования рубца и восстанавливал нервную ткань.
Исследователи из института фундаментальной медицины и биологии КФУ создали такой препарат, взяв за его основу два гена (VEGF и FGF2). Первый ген нормализует кровоснабжение при нейротравме, поддерживает выживаемость нейронов, стимулирует нейрогенез, рост новых сосудов и аксонов. Второй ген представляет собой фактор роста, обладает выраженным нейротрофическим действием — поддерживает выживаемость клеток в области повреждения, способствует развитию нервных волокон. Получившийся препарат содержит и регуляторные элементы, которые контролируют работу этих генов.
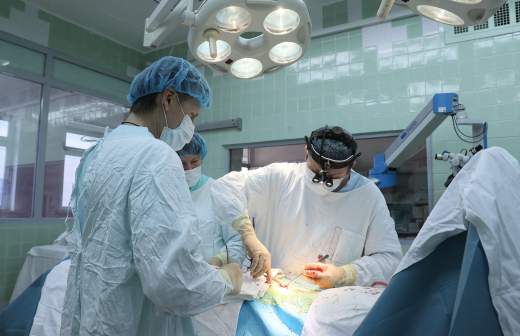
Испытания препарата на животных проходили следующим образом. Чтобы смоделировать повреждение спинного мозга, у подопытных вскрывали позвоночник и по нему с помощью специального молоточка наносили удар строго определенной силы. После операции животные теряли чувствительность задних конечностей и способность ими двигать. Во время всего эксперимента за животными тщательно ухаживали, помогая справляться с гигиеной и приемом пищи.
После нанесения травмы ученые переходили к лечению. Опытной группе животных вводили генный препарат, а контрольной позволяли восстанавливаться без стороннего вмешательства.
У крыс контрольной группы через два месяца после травмы наблюдалось частичное восстановление двигательных функций — животные сгибали лапы в одном или двух суставах. Однако полноценно передвигаться, удерживать вес тела и координировать движения грызуны не могли. Крысы в опытной группе в этот же период стали уверенно вставать на лапы, ходить, контролируя движения передних и задних конечностей.
— Помимо применения генного препарата мы проводим исследования эффективности лечения травм спинного мозга с помощью мезенхимных стволовых клеток, — рассказал старший научный сотрудник лаборатории генных и клеточных технологий института фундаментальной медицины и биологии КФУ Яна Мухамедшина. — Результаты обеих работ обнадеживают и показывают, что мы можем эффективно восстанавливать травмированный спинной мозг и его функции у крупных животных, в частности свиней, а в дальнейшем и у человека.
В перспективе ученые планируют сочетать эти методики для лечения травм головного мозга и терапии нейродегенеративных заболеваний.
Несмотря на то что гены в составе препарата и так присутствуют в человеческом организме, некий элемент риска всё равно есть и его невозможно предсказать, считает директор Института молекулярной медицины Научно-технологического парка биомедицины Сеченовского университета Андрей Замятнин.
— В составе генетической конструкции, которая используется, есть части (регуляторные элементы), которые в человеческом организме отсутствуют, — пояснил он. — Их влияние на организм абсолютно непредсказуемо. Поэтому для доказательства безопасности препарата необходимо провести клинические испытания.
Ученые готовы начать доклинические испытания в течение года, если решат вопрос финансирования.
В течение ближайшего десятилетия ожидается прорыв, который облегчит положение людей с ограниченными возможностями, а может даже полностью решит проблему восстановления нервных связей и возвращения подвижности парализованным конечностям.
Проблема этих, казалось бы очень успешных, экспериментов в том, что в них позвоночник травмируется сверхострыми лезвиями, что радикально ускоряет процесс сращивания аксонов, особенно в присутствии PEG или стволовых клеток. В реальности травмы мозга обычно связанны с обширным повреждением нервной ткани позвоночника, с гибелью участков протяженностью в 0,5-1 см. Полностью соединить такой разрыв нервных путей ученые до сих пор не могут.
В ноябре 2012 года команда ученых из Кембриджа и Центра регенеративной медицины Университета Эдинбурга опубликовала результаты эксперимента по исцелению подопытных собак с тяжелым повреждением спинного мозга.
Ученые проводили опыты на 34 собаках, в основном на таксах. Уникальность этих экспериментов в том, что они были максимально приближены к тем условиям, что могут возникнуть в реальных случаях травм у людей. Другими словами, были взяты обычные домашние собаки, которые в различное время получили травмы позвоночника, связанные с разрывом нервных путей и потерей части нервных клеток. После травм собаки в течение 12 месяцев и более не могли использовать свои задние ноги и потеряли чувствительность задней части туловища. Надо отметить, что у такс часто возникают такие же повреждения спинного мозга, как и у людей: связанные со смещением позвонков относительно друг друга.
Для лечения собак применили перспективную технологию имплантации обкладочных нейроэпителиальных клеток (OEC). Эти клетки находятся в носу и обладают свойствами нейральных стволовых клеток, то есть могут превращаться в нейроны. Впервые нейральные стволовые клетки из слизистой оболочки носа взрослого человека выделили в 2001 году, что стало важнейшим достижением, поскольку из носа добывать нейральные стволовые клетки относительно просто.
Собак разделили на две группы: одной ввели стволовые клетки непосредственно в место травмы позвоночника, а вторая группа была контрольной и получила плацебо. Через месяц собак в специальном поддерживающем корсете отправили на беговую дорожку для проверки функций конечностей.

Собаки, которым трансплантировали собственные нейральные стволовые клетки из слизистой оболочки носа, вновь смогли управлять задними конечностями
Пока идет работа над полным излечением травм спинного мозга, ученые из Case Western Reserve University и клиники Кливленда пытаются хотя бы частично улучшить состояния людей с очень серьезными повреждениями нервной ткани. В случае с обширной потерей нейронов пока почти нет надежды на полное исцеление, но для пациентов было бы большим облегчением восстановить хотя бы частичную функциональность парализованной части туловища.
Успехи в этой области уже есть, и они весьма существенные. Американским ученым удалось восстановить у подопытных крыс контроль над мочевым пузырем, причем потеря контроля произошла в результате серьезной травмы позвоночника: полного перерезания позвоночного столба с массивной потерей нейронов.
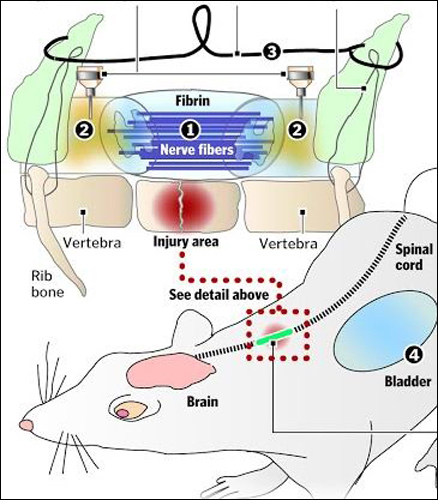
С помощью двух десятков нервных волокон ученые соединили разорванный спинной мозг. На рисунке видны нервные волокна и тонкий металлический проводок, защищающий новое нервное соединение от обрыва
Ученые не ставили перед собой задачу полностью вернуть подопытным мышам подвижность – это было невозможно при такой серьезной травме. Вместо этого была проделана кропотливая работа по пересадке нервной ткани из груди крыс в место повреждения в позвоночнике. Спустя много месяцев нейроны, подпитанные специальными химическими веществами и факторами роста, смогли прорасти навстречу разорванным участкам спинного мозга и соединить его через огромный по медицинским меркам разрыв шириной более 5 мм. В итоге получилось тонкое, всего в примерно 20 нервных волокон, соединение, которое, конечно, не могло полностью восстановить функциональность спинного мозга.
Тем не менее, впоследствии, мыши восстановили некоторый контроль над потерянными функциями организма, в частности смогли контролировать мочевой пузырь. Потенциально, данная методика может помочь восстановить множество других функций, в частности 2 года назад с ее помощью у крыс с менее тяжелыми повреждениями мозга восстановили контроль над дыхательными мышцами. Возможно, в перспективе с помощью подобной технологии все же можно будет ремонтировать обширные повреждения спинного мозга и полностью восстанавливать его функциональность.
Победа над природой
Не всегда врачи могут сразу определить, приходится ли им иметь дело с полным либо с частичным повреждением. При частичном повреждении спинной мозг может передавать некоторые сигналы в головной мозг и наоборот, поэтому такие пациенты обладают некоторой чувствительностью и даже некоторыми моторными функциями ниже пораженной области.
Полное повреждение спинного мозга сопровождается полной или почти полной потерей моторной функции и чувствительности ниже области поражения. И хотя даже при тяжелой травме спинной мозг почти никогда не является полностью перерезанным, обширность повреждения приводит к тому, что восстановление пациента становится делом практически безнадежным. Во всяком случае, так считалось до сравнительно недавнего времени.
Несколько фактов

Больница Крейга в штате Колорадо, США, специализирующаяся на лечении и реабилитации пациентов с параличом, предлагает на своем сайте несколько фактов, позволяющих больным и их близким сориентироваться в новой для них реальности.
– Почти всегда остается надежда на восстановление по крайней мере некоторых из утраченных функций.
– При неполном параличе шансы восстановления выше. Анализ медицинской статистики штата Колорадо показал, что только 1 из 7 полностью парализованных после травмы пациентов смог добиться значительной степени восстановления движения. Для тех, кто сразу после травмы сохранил хотя бы слабую способность к движению конечностей, эта пропорция значительно выше: 3 из 4 таких пациентов добиваются существенных улучшений.
– При полном параличе неплохой шанс есть у того, кто сохранил чувствительность в нижней части туловища сразу после травмы. Примерно 2/3 пациентов с повреждением спинного мозга в шейном отделе после длительной реабилитации смогли нарастить достаточную силу мышц в ногах для того, чтобы ходить, при условии, что сразу после травмы они ощущали укол ноги иголкой. Что касается тех, кто ощущал только легкое прикосновение, ходить сможет примерно 1 из 8 таких пострадавших.
– Чем скорее после травмы начнут работать мышцы, тем выше шанс на прогресс, тем реальнее перспектива встать и пойти. Как правило, если мышцы становятся способны функционировать лишь через несколько недель, это с большей вероятностью будут мышцы рук, а не ног.
Сколько длится тот период, в который можно надеяться на существенное улучшение, будь то пациент с неполным или полным повреждением спинного мозга? Как долго можно жить надеждой? На этот вопрос нет однозначного ответа. Понятно, что после двух или трех лет паралича, шансы на то, что мышцы заработают без посторонней помощи, практически ничтожны.
Что же касается месяца, двух, полугода после травмы – прогноз сделать сложнее, однако есть два правила, которые помогут сориентироваться:
– Если есть постоянные улучшения, если все новые мышцы постепенно восстанавливают функцию, значит, высок шанс дальнейшего значительного прогресса.
– Чем дольше период без улучшений, тем ниже шанс на восстановление.
Что ж, эти факты внушают умеренный оптимизм даже тем, кто пострадал от обширного поражения спинного мозга. Еще больший оптимизм внушают научные разработки, которые в перспективе могут сделать паралич излечимым или, по крайней мере, создать условия для значительной адаптации пострадавших от травм спинного мозга к нормальной жизни.
Почва для оптимизма

Роб Саммерс в свои 20 лет был полон надежд: он должен был начать обучение в Университете штата Орегон, активно занимался бейсболом. Все изменилось 12 июля 2006 года: его сбила машина, после чего он оказался полностью обездвижен. И хотя у него сохранялась некоторая чувствительность в нижней части туловища, прогноз был неутешительным. Врачи сказали, что ходить Роб никогда не сможет.
В конце XX века история на этом бы и закончилась, но в наше время медицина все быстрее переходит от научной теории к практике. Робу Саммерсу и еще трем молодым людям с повреждениями спинного мозга предложили инновационную терапию – эпидуральные стимуляторы, имплантируемые в спинной мозг. Все четыре пациента, парализованные, по крайней мере, от груди и до кончиков ног, теперь в состоянии двигать ногами.
Роб Саммерс первым получил экспериментальное лечение, разработанное доктором Регги Эдгертоном из Калифорнийского университета (Лос-Анджелес) и доктором Сьюзан Харкема из Университета Луисвиля (Кентукки) при участии наших соотечественников из Института физиологии имени Павлова (Санкт-Петербург). Они опубликовали свою историю успеха в 2011 году в журнале Lancet.
В чем суть терапии?
Стимулятор подает непрерывный электрический импульс на разных частотах и разной интенсивности нижнему спинному мозгу, то есть в пояснично-крестцовую зону, и тем самым имитирует мозговые сигналы, которые инициируют движения.
Все четыре пациента приобрели способность двигать ногами сразу же после имплантации и активации стимулятора, при этом движения были произвольными. Исследователи пришли к выводу, что некоторые сигнальные пути могли остаться неповрежденными после травмы, и именно они облегчают совершение произвольных движений. Мозг воспринимает сигнал стимулятора как свой собственный, и мгновенно начинает контролировать и направлять движения мышц.
Экзоскелеты, стволовые клетки и даже носовые нейроны!
Две недели назад в журнале Scientific Reports была опубликована статья международного коллектива бразильских, американских и немецких ученых, добившихся восстановления некоторых двигательных функций у пациентов, которые в результате тяжелых травм спинного мозга были полностью парализованы в течение очень длительных сроков – от 3 до 15 лет.
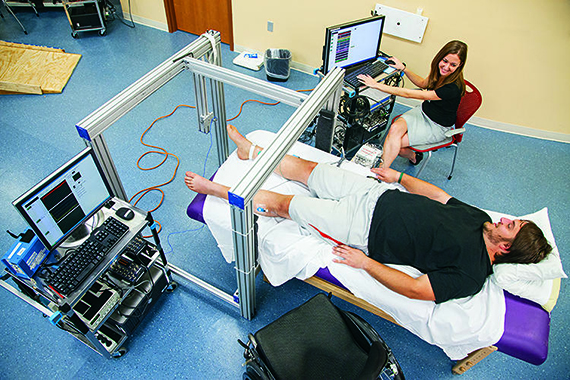
Метод реабилитации включал 3 компонента: виртуальную реальность, нейроинтерфейс и роботизированный экзоскелет.
Нейроинтерфейс представляет собой электроэнцелограф, регистрирующий активность мозга и передающий данные в компьютер для анализа. Когда пациент представлял себе, что он ходит, сигналы мозга, обрабатываемые компьютерной программой, приводили к тому, что аватар на экране двигался. Когда этот этап был пройден, пациенты перешли к занятиям с экзоскелетом, также управляемым нейроинтерфейсом.
Летом 2014 года член научной команды, нейробилог Мигель Николелис, представил на чемпионате мира по футболу одного из своих парализованных подопечных в экзоскелете, и тот на глазах у изумленной публики ударил по мячу.
Научное сообщество отнеслось к этой демонстрации весьма скептически: глядя со стороны, трудно было понять, действительно ли человек в экзоскелете самостоятельно контролировал свое футуристического вида оснащение.

Эти результаты кому-то могут показаться скромными, но ведь речь идет о пациентах, у которых чувствительность и минимальные моторные функции отсутствовали годами, а, как мы знаем, даже небольшой прогресс вселяет надежду на прогресс дальнейший.
Важно заметить также, что экзоскелеты с нейроинтерфейсом и ранее использовались в экспериментах по реабилитации парализованных людей, но подобный результат был достигнут впервые благодаря тому, что начинался эксперимент с обучения действиям в виртуальной реальности.
Было бы нелогично, если паралич не попробовали бы лечить стволовыми клетками. На сегодняшний день в арсенале ученых-медиков немало экспериментов, проведенных на животных.


Ученые считают, что новая методика поможет и парализованным людям, потерявшим подвижность после травм. Впрочем, пока о клинических испытаниях терапии на людях говорить преждевременно. В ближайшее время авторы протестируют разработанную ими технологию на более крупных животных.
Чуть раньше были опубликованы результаты исследований австралийских ученых из Университета Нового Южного Уэльса. Им удалось перепрограммировать клетки костной и жировой тканей в индуцированные мультипотентные стволовые клетки, способные участвовать в регенерации любых тканей.
Команда ученых уже успешно испытала полученные стволовые клетки на мышах. Теперь ученые считают, что в 2017 году они смогут протестировать клетки на людях. С помощью новых клеток авторы планируют лечить паралич и справиться с другими заболеваниями, например, с хроническими болями в спине или последствиями травм.
В октябре 2014 года в журнале Cell Transplantation был опубликован отчет о еще одной инновационной медицинской технологии, разработанной группой польских и английских медиков во главе с нейрохирургом Павлом Табаковым.
Сорокалетний Дерек Фидика в 2010 году после удара ножом в спину оказался парализован от груди и ниже. После двух лет безуспешной терапии медики решились на экспериментальный вид лечения.
Врачи провели операцию по извлечению обонятельной луковицы пациента, затем в специальных условиях были выращены особые клетки обонятельной выстилки носа, известные своей способностью проводить нервные импульсы. После этого были сделаны микро-инъекции клеток в область повреждения спинного мозга. Наконец, в ту же область были имплантированы четыре полоски нервной ткани.
По словам врачей, пересаженные клетки, прижившись в спинном мозге, стали выполнять функцию по проведению нервных импульсов между клетками самого мозга, таким образом способствуя их регенерации и восстановлению активности.
Уже спустя три месяца после вмешательства пациент почувствовал первые изменения, ощутив мышцы собственной ноги. Спустя еще полгода он смог сделать первые шаги при поддержке специального устройства и при помощи врача.
Важное преимущество метода заключается в том, что пациенту пересаживаются клетки из его собственной обонятельной луковицы, а значит, не произойдет реакции отторжения, как это бывает с донорскими органами и клетками.
Трудно сказать, какая из описанных терапий наиболее перспективна. Важно, что их несколько, что они развиваются, и каждая дает основания для надежды на то, что в будущем паралич станет полностью излечимым заболеванием.
Уйти от врача на своих ногах - обычное вообще-то дело, но, когда дело касается парализованных инсультников или спинальников, иначе как чудом его не назовешь.
В России на вечную неподвижность из-за травмы спинного мозга обречены 500 тысяч "колясочников", еще около 350 тысяч инвалидов каждый год появляется среди тех, кто перенес инсульт. Собственный организм парализованного человека содержит резерв для возвращения к полноценной жизни, но использовать его на благо пациента только-только научились. Рассказывает директор клиники восстановительной интервенционной неврологии и терапии "НейроВита" при РОНЦ им. Н. Н. Блохина РАМН, доктор медицинских наук, профессор Андрей Степанович БРЮХОВЕЦКИЙ.
- Я БОЛЬШЕ двенадцати лет занимаюсь стволовыми клетками, еще с тех пор, когда о них мало кто слышал. В 33 года я защитил докторскую диссертацию и понял, что нужно сделать что-то важное. Захотелось сделать нечто, что реально помогало бы неврологическим больным. В то время я уже думал о клеточных технологиях. Будучи главным неврологом ВМФ, я получил полную поддержку руководства, и мне дали возможность организовать работу. Доказав на животных возможность регенерации поврежденного мозга, мы провели ограниченные клинические испытания на больных с тяжелыми нервными болезнями, в лечении которых все традиционные методы были неэффективны. Долгое время мы работали по личной инициативе, доказывая, что стволовые клетки могут восстанавливать поврежденный головной и спинной мозг. Применение нашей технологии тканевой инженерии мозга во вторую чеченскую войну позволило снизить среди военнослужащих смертность на 5%, а инвалидность - на 18%.
В вечной изоляции
В НОРМЕ стволовые клетки никогда не попадают в мозг - им мешает гематоэнцефалический барьер: клетки крови функционируют по сосудам, но они никогда не связываются непосредственно с нейронами. Если, не дай бог, происходит кровоизлияние и клетки крови попадают непосредственно в мозг, нейроны погибают. Если бы гематоэнцефалического барьера не было, то мозг мог бы сам себя постоянно восстанавливать и связи, наработанные им в течение жизни, пропадали бы.
Пересадить человеку мозг невозможно, во-первых, технически. Во-вторых, что бы мы получили, если бы это стало возможно? Чтобы решить кардинальную проблему пересадки мозга, ученые стали смотреть, можно ли его хотя бы реконструировать и дать возможность жить. Так родилась идея применения клеточной и тканевой инженерии. Мы действовали на уровне клеток и доказали, что их можно использовать. Чтобы вылечить человека, необходимо дать ему ресурс, который его организм сам использует. При повреждении других органов можно ввести стволовые клетки, они сами придут и все сделают. Мы предложили принципиально иную идею терапии. Существует информационная матрица, по которой выстраивается все в организме.
Если мы хотим реконструировать мозг, то к нему нужно подходить не как к суперсложной системе, а разложить на простые элементы: нейроны, олигодидроциты, астроциты, микроглию. Проблема не в устройстве мозга (сегодня мы знаем его до миллиметра), а в его системной организации, поэтому мы не пытаемся переделать структуру, а пытаемся создать новый участок мозга на месте поврежденного. Глупо подсаживать клетки в место, где свои собственные погибли, - они точно так же погибнут, поэтому сначала нужно создать условия для приживления клеток ("хоуминг").
Выяснить, сколько примерно клеток погибло, имея современные методы исследования (лучевую диагностику, компьютерный томограф), не составляет труда. По плотности мозгового вещества можно рассчитать процент поврежденного мозга, и тогда понятно, какое количество клеток нужно подсадить.
Чтобы они не попали в "мертвую зону", мы реконструируем сосудистое русло, потому что без нормального питания поврежденная зона работать не может. Восстановить его можно несколькими способами. Например, взять сосуд из височной артерии, проделать в мозге дырочку, завести его туда и пришить непосредственно к сосудам полушария головного мозга. От своей сонной артерии поврежденная зона уже не может кровоснабжаться, а мы это исправляем, организуя новый приток кровоснабжения. В некоторых случаях это давало потрясающий результат абсолютно самостоятельно. У кого-то мы применяли рентгенохирургию.
Научи свой мозг
СЛЕДУЮЩИЙ этап технологии - применение стволовых клеток в зоне повреждения. Когда мозг погибает, иммунная система умершие клетки утилизирует, и на месте повреждения возникает дырка. Наша задача - максимально сохранить оставшиеся нервные клетки. Традиционно при сотрясении мозга больного укладывают и прописывают полный покой. Но неправильно ждать, пока погибнут все пострадавшие нейроны, и вводить препараты, улучшающие сохранившиеся, - результатом будут микродырочки в мозге. Функционально они ничего не значат, просто образуются кисты, заполненные жидкостью. Наша идеология была другой - не надо ждать, пока мозг погибнет, надо улучшить его кровоснабжение и дать ресурс клеток. Количество вводимых клеток зависит от места повреждения, иногда - больше того количества, которое погибло, в ряде случаев - равное. А путей введения несколько:
рентгенохирургический - клетки подводятся в зону повреждения через сосуды головного мозга. Катетером подошли к сосуду, встали в сосуд и в зону повреждения четко ввели клетки;
стереотаксический - вскрыли твердую мозговую оболочку и в мягкую - специальным шприцем или аппаратом (стереотаксисом) - в необходимый отдел мозга длинной иглой ввели стволовые клетки;
трансфузия клеток - входим в желудочковую систему мозга и вставляем туда трубочки, которые стоят под кожей, или в желудочковую систему мозга вводим клетки во время операции;
самонаведение клеток - механизм срабатывает, если основные двигательные пути сохранены: клетки сами придут в зону повреждения и восстановят ее. Если дефект огромен (полный перерыв спинного мозга), то, пока мы не восстановим анатомическую целостность, мы ничего не сможем добиться.
Набор клеток только тогда становится тканью, когда получает иннервацию, то, есть "загружается работой", поэтому следующий этап - восстановить вегетативное обеспечение. Мы пытаемся встроить то, что сделали из нового кровеносного русла и набора клеток, в огромную систему мозга.
Самое главное - не построить новый мозг, а научить его новым функциям. Это не реабилитация в привычном смысле, когда человек восстанавливается. В нашем случае восстанавливать нечего, мы должны научить заново. Например, мы подвешиваем больного на бегущую дорожку и вырабатываем у него автоматизм ходьбы. Американцы доказали потрясающую вещь: реконструкция мозга приводит к дальнейшим переподключениям, формируется новая система связей между нейронами. 10 лет назад мы назвали это "биоинженерный метод восстановления функции мозга". Сегодня и американская, и российская наука называет это тканевой инженерией.
Во всем мире больные с полным перерывом спинного мозга считаются обреченными. Мы разработали биополимерную матрицу - специальный гель на основе коллагена птицы и человека, который фаршируется стволовыми клетками и имплантируется в мозг, в зону повреждения. У пятнадцатилетней девочки, которая в результате автомобильной аварии получила перерыв спинного мозга 4 см, через три месяца, после того как мы смоделировали ей искусственную нервную ткань, заработал пальчик на ноге.
Сегодня нам не нужны чужие, донорские клетки, мы научились выращивать собственные клетки пациента. Нейроны мы берем из выстилки носа по технологии английского ученого Джеффри Райтмана, который получил разрешение на работы на людях позже нас. А если ввести специальный фактор нейпоген, в кровь выходят стволовые клетки костного мозга.
Липовый бум
СЕЙЧАС возник бум стволовых клеток, поскольку их начали применять в косметологии для омоложения. Они действительно помогают. Это мы отметили еще 10 лет назад как побочный эффект клеточной трансплантации.
Но мода на омоложение стволовыми клетками дискредитирует клеточную технологию. Их используют сейчас все кому не лень, а серьезные исследования из-за этого страдают, хотя положительные результаты есть. Ученые Кельнского университета уже используют стволовые клетки при опухолях сердца. Они доказали, что если ввести стволовые клетки в опухоль сердца, то она сморщивается, поскольку стволовые клетки ее поедают. Академик Бокерия показал, как при тяжелом повреждении сердца - при инфаркте миокарда - стволовые клетки встраиваются в сердечную мышцу и восстанавливают ее.
Стволовые клетки могут и будут работать. Технология прошла очень тяжелый путь - вплоть до полного отрицания. А сейчас на этой теме "сидит" целая толпа, но тех, кто занят настоящим делом, можно перечесть по пальцам. Стандартизированную культуру стволовых клеток могут вырастить в Институте им. Сербского, РГМУ, Центре акушерства, гинекологии и перинатологии и РОНЦ. Все! Остальные лаборатории пока произвести хорошие стволовые клетки не могут.
Мы работаем только с собственными стволовыми клетками человека. Оказалось, что их эффективность выше, чем эмбриональных. Мы лечим травмы головного и спинного мозга, болезнь Паркинсона, последствия инсультов и рассеянный склероз. Когда понятна причина болезни и мы лечим последствия повреждения мозга, эффективность гораздо лучше. У больных, перенесших инсульт, которым не помогает ничто, мы добиваемся результатов в половине случаев: у пациентов восстанавливаются речь, двигательная функция. При травме спинного мозга видим улучшения у 70% больных: у одного заработал палец, у другого - нога, у третьего восстановилась функция тазовых органов и нормализовалась чувствительность, кто-то стал ходить.
Все работы идут в рамках научного исследования. Отраслевую программу утвердила РАМН, но государство ее не финансирует. Англичанину Джеффри Райтману на аналогичную работу выделили 300 млн. фунтов стерлингов. В среднем курс лечения стоит 10-15 тысяч долларов, если это трансфузия - значительно меньше. Для сравнения: в Великобритании ту же операцию будут проводить за 350 тысяч фунтов стерлингов (500 тысяч долларов), а в Швеции трансплантация эмбриональных стволовых клеток в мозг стоит 100 тысяч долларов. Первые шесть больных, которым провели реконструкцию спинного мозга, были прооперированы бесплатно. Они очень бедные люди и попали в программу благодаря спонсору, которая сейчас лежит здесь. У Олеси частичное повреждение спинного мозга. Она профинансировала работы на животных, моделирование гелей и оплатила лечение шестерых больных. Сегодня она приехала, чтобы лечь на реконструкцию спинного мозга. Олеся - фантастическая женщина! Она сумела с травмой спинного мозга выйти замуж, родить ребенка, научилась бороться и поддерживать всех моих парализованных больных. Без нее все это просто не состоялось бы, потому что она своим оптимизмом зажгла огромное число людей.
Читайте также:


