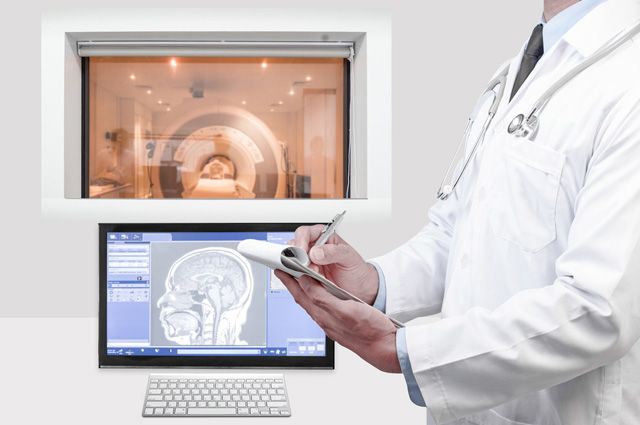
Флуорозамин при рассеянном склерозе
Нейробиологи из Университета Калгари нашли вещество, которое может помочь больным рассеянным склерозом справиться с болезнью. Им оказался N-ацетилглюкозамин (флуорозамин), который пока еще не одобрен для использования людьми, однако демонстрирует эффективность при экспериментах на мышах. Результаты исследования опубликованы в Nature Communications.
Рассеянный склероз — хроническое заболевание, вызванное атакой иммунной системы на здоровые клетки самого организма. В результате происходит разрушение электроизолирующих миелиновых оболочек, которые окружают нервные волокна центральной нервной системы. У больного образуются множественные очаги аутоимунного воспаления, где нормальная нервная ткань заменяется на соединительную. Миелиновая оболочка образуется из глиальных клеток, к которым относятся олигодендроциты. Определенные вещества, например, хондроитин сульфат протеингликаны, играют роль молекулярных сигналов, регулирующих регенерацию миелина на участках повреждения нервных волокон. Они способствуют подавлению развития и функций олигодендроцитов. Ученые испытали 245 препаратов, чтобы найти те соединения, что позволяют олигодендроцитам расти и работать в присутствие протеингликанов. Они обнаружили, что N-ацетилглюкозамин в клетках подопытных мышей уменьшает синтез протеингликанов и восстанавливает функции глиальных клеток. Исследователи продемонстрировали, что введение препарата способствует регенерации миелиновых оболочек и уменьшения пареза конечностей у грызунов, страдающих рассеянным склерозом.
В экспериментах нейробиологи использовали две группы животных по семь-восемь особей в каждом. Ученые подчеркивают, что это предварительные исследования, и необходимы дальнейшие клинические испытания препарата, чтобы подтвердить безопасность и эффективность потенциального метода лечения, прежде чем проверять его действие на людях. Нейробиологи из Университета Калгари нашли вещество, которое может помочь больным рассеянным склерозом справиться с болезнью. Им оказался N-ацетилглюкозамин (флуорозамин), который пока еще не одобрен для использования людьми, однако демонстрирует эффективность при экспериментах на мышах. Результаты исследования опубликованы в Nature Communications.
Рассеянный склероз — хроническое заболевание, вызванное атакой иммунной системы на здоровые клетки самого организма. В результате происходит разрушение электроизолирующих миелиновых оболочек, которые окружают нервные волокна центральной нервной системы. У больного образуются множественные очаги аутоимунного воспаления, где нормальная нервная ткань заменяется на соединительную.
Миелиновая оболочка образуется из глиальных клеток, к которым относятся олигодендроциты. Определенные вещества, например, хондроитин сульфат протеингликаны, играют роль молекулярных сигналов, регулирующих регенерацию миелина на участках повреждения нервных волокон. Они способствуют подавлению развития и функций олигодендроцитов. Ученые испытали 245 препаратов, чтобы найти те соединения, что позволяют олигодендроцитам расти и работать в присутствие протеингликанов. Они обнаружили, что N-ацетилглюкозамин в клетках подопытных мышей уменьшает синтез протеингликанов и восстанавливает функции глиальных клеток. Исследователи продемонстрировали, что введение препарата способствует регенерации миелиновых оболочек и уменьшения пареза конечностей у грызунов, страдающих рассеянным склерозом. В экспериментах нейробиологи использовали две группы животных по семь-восемь особей в каждом. Ученые подчеркивают, что это предварительные исследования, и необходимы дальнейшие клинические испытания препарата, чтобы подтвердить безопасность и эффективность потенциального метода лечения, прежде чем проверять его действие на людях.
Результат, оптогенетического эксперимента с обезьянами, кистевой экзоскелет оснастили вторым большим пальцем, систма поиска оператора на основе полета дрона, нейроны в полупроводнике, следующее поколение миниатюрной электроники

Признаки COVID-19 в речи, восприятие речи во время сна, передача данных через чип, с помощью света, робот проводит химические экспиременты, разработка биоморфного нейропроцессора в России

NEUROTECH CUP 2020 - международный конкурс проектов молодых исследователей и инженеров в области нейротехнологий и искуственного интеллекта

Было подано 463 заявки на участие, 145 человек в настоящее время проходят программу обучения
VR-очки с голографическим экраном, жидкий протез сетчатки, кристаооы для сверхбыстрой магнитно-оптической памяти, обман рецепторов, с помощью VR
Рассеянный склероз — хроническое заболевание, вызванное атакой иммунной системы на здоровые клетки самого организма. В результате происходит разрушение электроизолирующих миелиновых оболочек, которые окружают нервные волокна центральной нервной системы. У больного образуются множественные очаги аутоимунного воспаления, где нормальная нервная ткань заменяется на соединительную. Миелиновая оболочка образуется из глиальных клеток, к которым относятся олигодендроциты. Определенные вещества, например, хондроитин сульфат протеингликаны, играют роль молекулярных сигналов, регулирующих регенерацию миелина на участках повреждения нервных волокон. Они способствуют подавлению развития и функций олигодендроцитов. Ученые испытали 245 препаратов, чтобы найти те соединения, что позволяют олигодендроцитам расти и работать в присутствие протеингликанов. Они обнаружили, что N-ацетилглюкозамин в клетках подопытных мышей уменьшает синтез протеингликанов и восстанавливает функции глиальных клеток. Исследователи продемонстрировали, что введение препарата способствует регенерации миелиновых оболочек и уменьшения пареза конечностей у грызунов, страдающих рассеянным склерозом.
В экспериментах нейробиологи использовали две группы животных по семь-восемь особей в каждом. Ученые подчеркивают, что это предварительные исследования, и необходимы дальнейшие клинические испытания препарата, чтобы подтвердить безопасность и эффективность потенциального метода лечения, прежде чем проверять его действие на людях. Нейробиологи из Университета Калгари нашли вещество, которое может помочь больным рассеянным склерозом справиться с болезнью. Им оказался N-ацетилглюкозамин (флуорозамин), который пока еще не одобрен для использования людьми, однако демонстрирует эффективность при экспериментах на мышах. Результаты исследования опубликованы в Nature Communications.
Рассеянный склероз — хроническое заболевание, вызванное атакой иммунной системы на здоровые клетки самого организма. В результате происходит разрушение электроизолирующих миелиновых оболочек, которые окружают нервные волокна центральной нервной системы. У больного образуются множественные очаги аутоимунного воспаления, где нормальная нервная ткань заменяется на соединительную.
Миелиновая оболочка образуется из глиальных клеток, к которым относятся олигодендроциты. Определенные вещества, например, хондроитин сульфат протеингликаны, играют роль молекулярных сигналов, регулирующих регенерацию миелина на участках повреждения нервных волокон. Они способствуют подавлению развития и функций олигодендроцитов. Ученые испытали 245 препаратов, чтобы найти те соединения, что позволяют олигодендроцитам расти и работать в присутствие протеингликанов. Они обнаружили, что N-ацетилглюкозамин в клетках подопытных мышей уменьшает синтез протеингликанов и восстанавливает функции глиальных клеток. Исследователи продемонстрировали, что введение препарата способствует регенерации миелиновых оболочек и уменьшения пареза конечностей у грызунов, страдающих рассеянным склерозом. В экспериментах нейробиологи использовали две группы животных по семь-восемь особей в каждом. Ученые подчеркивают, что это предварительные исследования, и необходимы дальнейшие клинические испытания препарата, чтобы подтвердить безопасность и эффективность потенциального метода лечения, прежде чем проверять его действие на людях

Глюкозамин-как добавка подавляет множественные атаки рассеянного склероза
N-ацетилглюкозамина (GlcNAc), который подобен , но более эффективным , чем широко доступного глюкозамина, ингибирует рост и функцию аномальных Т-клеток
"Этот сахар на основе дополнения исправляет генетический дефект, который заставляет клетки атаковать Миелина при рс," сказал Деметриу, доцент кафедры неврологии и микробиологии и молекулярной генетики ", что делает метаболической терапии рациональный подход, который существенно отличается от имеющихся в настоящее время лечения."
Практически все белки на поверхности клеток, в том числе иммунные клетки, такие как Т-клетки, которые модифицированы путем сложных сахарных молекул различных размеров и состава. Недавние исследования связывают изменения этих сахаров в Т-клеточной гиперактивности и аутоиммунных заболеваний.
В мышиных моделях рс-как аутоиммунное заболевание, Деметриу и его команда обнаружили, что GlcNAc в пероральной форме тем мышам, со слабостью ног подавлена Т-клеточный гиперактивность и аутоиммунную реакцию путем увеличения модификации сахара в Т-клеточных белков, тем самым удалось обратить вспять прогрессирование паралича у мышей.
Исследование продолжается на людях показывающих потенциал GlcNAc в организме человека. Восемь из 12 детей с резистентным к лечению аутоиммунного воспалительного заболевания кишечника значительно улучшилось после двух лет GlcNAc терапии. Не было отмечено каких-либо серьезных неблагоприятных побочных эффектов

НА ОСНОВЕ НАГ был создан препарат fluorosamine который стимулирует регенирацию аксонов и ремиелинизацию .
peracetylated 4-F-GlcNAc (4, далее именуемые fluorosamine для краткости)
------------------------------------------------------------------------------------------------------------------------------------------—
Вещество под названием fluorosamine было создано, чтобы повысить ремиелинизацию у мышей, предотвращая синтез хондроитинсульфат протеогликанов и путем содействия функции олигодендроцитов. Полученные данные показали, что целевые молекулы, которые блокируют ремиелинизацию может быть перспективным терапевтическим подходом при рассеянном склерозе (MS).
Положительная регуляция хондроитинсульфат протеогликанов - крупных молекул, состоящих из позвоночника белка, украшенной сахара - являются частью процесса рубцевания после возникновения демиелинизирующих поражения. Высокая производительность этих молекул астроцитарных глиальные клетки, также были связаны с недостаточностью к ремиелинизации.
Исследователи из Университета Калгари, Канада, ранее показали, что протеогликаны (CSPGs) блокируют созревание олигодендроцитов клеток, которые отвечают за производство миелина, предотвращая ремиелинизацию на животных моделях.
Путем скрининга скрининга библиотеки лекарств из 245 анализируемых веществ не было найдено
вещество способное блокировать CSPGs.
Команда вместо этого сосредоточила свое внимание на лекарстве, которые могли бы уменьшить синтез протеогликанов, и обнаружили, что fluorosamine вещество действительно может снизить такого синтеза. Исследователи также установили, что активность fluorosamine будет улучшена, если структуру несколько модифицировать что и было сделано.
Принимая перорально fluorosamine на животных моделях, команда затем показала, что fluorosamine существенно замедляет процесс демиелинизации и способствовал ремиелинизацию. Так же было замечены частично свойства иммуномодулирующих препарата с противовоспалительными свойствами. В животной модели РС, известный как экспериментальный аутоиммунный энцефаломиелит (EAE), лечение fluorosamine улучшили симптомы как на ранних и более поздних стадиях заболевания.

В связи с последней статьей у меня появились опасения касательно N-A-G
Определенные вещества входящие в состав НАГ (хондроитинсульфат) способны увеличить CSPGs в мозге.
(CSPGs это те вещества которые делают рубцы)

в калгаре разработали новый припарат флоурозамин который как я понял и блокирует CSPGs. наг наоборот увеличивает их количество но на самом деле как мне ответили увеличить он не может так как не попадает в мозг.
А воще сильно мои выводы не надо читать я не врачь и во всех этих жспжс не разбираясь. есть ориг статьи их надо самим изучать а не читать выводы непонятно кого. тоже самое не искать в гугле каких то периписак этих статей. изучать надо только оригеналы.
особено с калгари так в гугле деза на русском языке там пишется что наг и флоурозамин это одно и тоже на самом деле это новый препарат с модиф формулой. они взяли и модиф наг и создали что то новое.
Про наг лучше читать первую статью 2011 года исследований где именно наг изучался на мышах с рс. и как выяснилось он способен подавлять т хелперные клетки к том-же он благоприятно действовал на мышей и не давал параличам развиваться. но все таки две мыши скопытились от приема наг в начале лечения. этот ньюанс тоже был. а вообще пиречитуйте сами. вопросы лучше задавать автором статей. и не забывать публиковать ответы тут

Действительно, GlcNAc добавки в лабораторных условиях и / или в естественных условиях подавляет рост Т - клеток путем ограничения передачи сигналов TCR и повышение CTLA-4 удержания поверхности, ингибирует Th1 и Th17 реакции и подавляет EAE, а также аутоиммунный диабет (41 , 47 ). К тому же , Марч и др обнаружено , что оральное GlcNAc терапия ингибирует клиническое заболевание у 8 из 12 детей с резистентным к лечению воспалительного заболевания кишечника ( 55 ). Таким образом, обмен веществ регулирует N-гликанов разветвление и тем самым влияет на восприимчивость к Т-клеточного аутоиммунитета у мышей.
Витамин D 3 синтезируется из 7-дегидрохолестерола в коже при ультрафиолетовом воздействии солнца и его дефицит сильно ассоциируется с МС ( 8 , 58 , 59 ). 1α, 25-дигидрокси D 3 (1,25 (OH) 2 D 3), активная форма витамина D 3ингибирует активацию Т - клеток, дифференцировки Th1 и подавляет ЕАЕ у мышей, воздействуя на Т - клетки ( 60 - 62 ), тем не менее молекулярные механизмы были неясны.
D 3 увеличивается N-гликанов разветвление в активированныхисключая виво Т - клеток , подавлять их рост ( 44 ). Сокращение диетического питания витамина D 3 у мышей уменьшилась N-гликана разветвление в Т - клетках, тогда как внутрибрюшинную инъекцию 1,25 (OH) 2 D 3 увеличилась N-гликана разветвление. Основной белок миелина (ОБМ) индуцированный ЕАЕ ингибируется интраперитонеально 1,25 (OH) 2 D 3 в отсутствии , но не наличие swainsonine, ингибитор N-гликанов разветвленности. В совокупности эти данные свидетельствуют о том, что витамин D 3 подавляет рост Т - клеток и EAE за счет повышения N-гликана ветвление в Т - клетках.
Таким образом, два независимых экологических факторов, а именно обмен / снабжение питательными веществами и солнце / витамин D 3 Влияние Т - клеток опосредованной аутоиммунные путем регулирования N-гликана ветвление ( рис 1). Метаболический гомеостаз состоит из нескольких механизмов обратной связи, но небольшие изменения в гомеостатических заданных точках с возрастом и сигналами окружающей среды могут быть клинически значимыми в сложных признака заболеваний, таких как MS. Терапевтическое вмешательство с устным GlcNAc и / или витамина D 3 может обеспечить простое лечение для повышения N-гликана ветвление и подавлять MS.
Терапевтическое добавок Гольджи увеличить N-гликана биосинтез может предоставить такую терапию. Оба витамина D 3 и GlcNAc , активны при пероральном введении, обратный дефициты в N-гликанов разветвлений у мышей и людей, а также ингибируют EAE и спонтанным аутоиммунным диабетом у мышей ( 41 , 61 , 73 ). Более поздние данные из нашей лаборатории показали , что пероральное GlcNAc также ингибирует Th1 и Th17 реакции и прогрессирование заболевания в EAE при введении после начала заболевания ( 47 ) Пилотное исследование полости рта GlcNAc в педиатрической резистентных к лечению воспалительных заболеваний кишечника сообщили , что 8 из 12 дети с тяжелой болезнью ушел в клинической ремиссии с признаками гистологического улучшения ( 55 ). Три из реагирующих с рецидивами в течение
Atara Biotherapeutics: T-клеточная терапия против вируса Эпштейна — Барр.
Человеческий разум относится к новой идее так же,
как тело относится к странному белку: он отвергает ее.
Питер Медавар, биолог, нобелевский лауреат
Новая научная истина торжествует не потому,
что ее противники признают свою неправоту,
просто ее оппоненты со временем вымирают,
а подрастающее поколение знакомо с нею с самого начала.
Макс Планк, физик, нобелевский лауреат
Суть проблемы
Прогрессирующий рассеянный склероз (PMS), как тяжелая форма этого демиелинизирующего заболевания, классифицируется на первично-прогрессирующий рассеянный склероз (PPMS) и вторично-прогрессирующий рассеянный склероз (SPMS). Первый справедлив при непрестанном ухудшении течения заболевания к моменту постановки его диагноза (15% случаев). Второй начинается как рецидивирующе-ремиттирующий рассеянный склероз (RRMS), который в конечном итоге превращается в SPMS у 80% пациентов.
Согласно глобальной статистике, мировая популяция пациентов с рассеянным склерозом разбивается следующим образом : на долю RRMS приходится 57% больных, тогда как PMS охватывает 43%, включая 15% пациентов с PPMS и 28% с SPMS.
Медицинская потребность в новых прорывных и, главное, высокоэффективных лекарственных препаратах для терапии прогрессирующего рассеянного склероза по-прежнему остается незакрытой. Сообщество врачей и пациентов мечтает либо об обращении инвалидизации вспять с последующим устойчивым поддержанием достигнутых успехов, либо о хотя бы стабильной остановке прогрессирования рассеянного склероза.
Гипотеза, нашедшая ответ
- У EBV-положительных иммунологически разнообразных и со здоровой иммунной системой доноров (не больных рассеянным склерозом) лейкоферезом собирают мононуклеарные клетки периферической крови (PBMC). Из них выделяют T-клетки и B-клетки, которые затем культивируют и размножают.
- B-клетки трансформируют в антигенпрезентирующие клетки (APC) путем их трансфектирования рекомбинантным аденовирусным вектором AdE1-LMPpoly, который кодирует CD8 + T-клеточные эпитопы, имеющие отношение к антигенам вируса Эпштейна — Барр — ядерному EBV-антигену 1 (EBNA1), латентному мембранному белку 1 (LMP1), латентному мембранному белку 2A (LMP2A).
- T-клетки подвергаются воздействию APC, которые экспрессируют указанные EBV-антигены. Итогом становится стимуляция и размножение EBV-специфических CD8 + T-клеток — таргетированных цитотоксических T-лимфоцитов (CTL).
- При внутривенном введении CTL пациентам с рассеянным склерозом они уничтожают персистирующие в центральной нервной системе EBV-инфицированные B-клетки, которые несут искомые EBV-антигены.
Поскольку ATA188 является HLA-совместимым только частично, создается обширная библиотека криоконсервированных ATA188-препаратов: нужный отбирается для каждого пациента сообразно соответствию хотя бы по двум HLA-аллелям, общим для ATA188 и конкретного больного.
Возможная победа над прогрессирующим рассеянным склерозом
Клинические исследования NCT03283826 фазы I проверяют безопасность и эффективность ATA188, назначаемого монотерапевтически один раз в год (несколькими циклами) на протяжении пяти лет взрослым EBV-положительным пациентам (n=97) с прогрессирующими формами рассеянного склероза — первично-прогрессирующим или вторично-прогрессирующим. Испытания состоят из двух частей. Среди критериев включения: возраст 18–66 и 18–56 лет, балл по расширенной шкале степени инвалидизации (EDSS) 3,0–7,0 и 3,0–6,5 — соответственно для первой и второй частей.
В еще не начатой второй части исследований (рандомизированных, двойных слепых, плацебо-контролируемых) будут определены изменения конечных точек: EDSS, тест на время прохождения 25 футов (T25-FW), тест с девятью отверстиями и стержнями (9-HPT), МРТ-объемы шейного отдела спинного мозга и всего головного мозга, число очагов поражения головного мозга на T1-взвешенных МРТ-изображениях с контрастированием гадолинием и число новых или увеличивающихся очагов на T2-взвешенных МРТ-изображениях.
Заявлено, что с увеличением дозы ATA188 ответ на лечение углублялся. Так, по одному пациенту в когортах 1 и 2 и два пациента в когорте 3 показали SDI за период 6 месяцев, который сохранялся и по истечении 12 месяцев. Два участника в когорте 4 максимальной дозы также продемонстрировали SDI за 6 месяцев, но их 12-месячные данные еще не собраны. Основной вклад в достижение SDI поступил со стороны улучшения балла EDSS.
- шкала тяжести усталости (FSS): минимальное клиническое улучшение составляло −0,7 балла;
- шкала влияния рассеянного склероза (MSIS-29) [домен физических возможностей]: −8 баллов;
- T25-FW: −20%;
- 9-HPT: −20%;
- субъективный опросник способности передвигаться (MSWS-12): −8 баллов;
- EDSS: −1 балл (при исходном EDSS 3–5 баллов) и −0,5 балла (EDSS 5,5–7,0);
- острота зрения (VA) [по шкале LogMAR]: изменение минимум на −0,1 в каждом глазу.
Подтверждено, что длительно сохраняющаяся заявленная терапевтическая эффективность ATA188 напрямую коррелирует с увеличением дозы препарата.
Профиль безопасности ATA188 характеризуется отсутствием дозолимитирующей токсичности и фатальных побочных реакций. Все отрицательные явления, связанные с терапией, носили легко-умеренную степень выраженности. И хотя один пациент столкнулся с тяжелой побочной реакцией, приведшей к выходу из клинических исследований, она проявилась на фоне продолжающихся симптомов инфекции верхних дыхательных путей и возможной стоматологической инфекции. Насморк — единственная побочная реакция, зафиксированная у более чем одного испытуемого.
ATA188 не оказал клинически значимого эффекта на выработку цитокинов, в том числе не привел к синдрому выброса цитокинов.
Более чем надежда
И хотя развитие рассеянного склероза, вероятно, подталкивается не одним причинным фактором, вирус Эпштейна — Барр является единственным известным на сегодняшний день фактором риска, в обязательном порядке необходимым для манифестации заболевания. Доказано, что 100% пациентов с рассеянным склерозом подверглись воздействию EBV. При этом EBV-инфицированные клетки, особенно B-клетки памяти, ставшие ввиду вирусного заражения бессмертными, играют, есть мнение, важнейшую роль в иммунном каскаде, ответственном за рецидивирующие и прогрессирующие формы рассеянного склероза. Успехи существующей фармакотерапии, которая истощает пул всех периферических B-клеток, лишний раз свидетельствует о ключевой позиции этих клеток в патофизиологии рассеянного склероза. Показана оправданность продолжения экспериментов с терапией рассеянного склероза при помощи ATA188 — цитотоксическими T-клетками, селективно таргетированными против EBV-инфицированных B-клеток и плазматических клеток, как циркулирующих в организме, так и персистирующих в центральной нервной системе.
Некоторые наблюдения таковы, что эффективность ATA188 в отношении улучшения статуса инвалидизации зависит, кажется, от исходного балла по шкале EDSS: чем запущеннее заболевание, тем меньше (или медленнее) проявляется целебная сила лечения. И всё же улучшение показателя EDSS даже на один балл — уже примечательно. Ведь если пациент, к примеру, изначально передвигался с тростью, то после терапии ATA188 он обрел способность самостоятельной ходьбы.
Имеющиеся лекарственные препараты способны лишь слегка придержать ухудшение прогрессирующего рассеянного склероза — им не по силам остановить или обратить заболевание вспять. Если ATA188 добьется этого в ходе строго контролируемой части 2 клинических испытаний, нас ждет эволюция в парадигме лечения прогрессирующей и других форм рассеянного склероза.
Рассеянный склероз и вирус Эпштейна — Барр
Считается, что генетические и внешние факторы вносят определенный вклад в риск развития рассеянного склероза — хронического воспалительного демиелинизирующего заболевания центральной нервной системы, вызывающего прогрессирующую инвалидизацию. За последние четыре десятка лет появилось всё больше доказательств , что вирус Эпштейна — Барр (EBV) играет существенную роль в развитии рассеянного склероза. Предположение подкреплено рядом независимых исследований, указывающих на поголовное присутствие инфекции у пациентов и наличие высоких титров сывороточных антител против EBV как в ходе клинического течения рассеянного склероза, так и до его манифестации .
Вирус Эпштейна — Барр, или вирус герпеса человека 4 типа (HHV-4), во многих отношениях является уникальным. Так, в целях колонизации организма он заражает B-лимфоциты, активирует и способствует их клональному размножению, а затем на протяжении всей жизни человека персистирует латентной инфекцией в B-клетках памяти, несущих фенотип покоящихся клеток. Вирус, переключаясь с латентной (спящей) на литическую (репликационную) форму посредством модуляции своих ядерных генов, латентных мембранных белков (LMP) 1, 2A и 2B и вирусного предраннего белка BZLF1 (ZEBRA), реактивируется в плазматических клетках и эпителиальных клетках миндалин, организуя собственную передачу другим организмам через слюну и генитальные выделения. Несмотря на то что этим ДНК-двухцепочечным гамма-герпесвирусом заражено приблизительно 95% взрослого населения планеты, число EBV-инфицированных клеток в организме удерживается под строгим иммунным контролем, в том числе EBV-специфическими цитотоксическими T-лимфоцитами CD8 + , которые уничтожают пролиферирующие и литически инфицированные клетки.
В ряде случаев иммунологический надзор над EBV ослабевает, что отражается развитием различных болезней. Известно, что вирус Эпштейна — Барр является причиной инфекционного мононуклеоза. Он ассоциирован с определенными онкологическими заболеваниями, включая лимфому Ходжкина, лимфому Беркитта, рак желудка, карциному носоглотки. Вирус Эпштейна — Барр связан с детскими расстройствами вроде синдрома Алисы в стране чудес и острой мозжечковой атаксии. Есть мнение, что он усиливает риски развития аутоиммунных патологий, в том числе дерматомиозита, системной красной волчанки, ревматоидного артрита, синдрома Шегрена.
Касательно рассеянного склероза, считается , что у восприимчивых хозяев EBV-инфекция наделяет зараженные аутореактивные B-клетки аномальной способностью к выживаемости и пролиферации. Такие латентно инфицированные клетки аккумулируются в лимфоидных структурах и органах-мишенях, затрагиваемых при этом заболевании. Если речь идет о головном мозге, это приводит к постоянному синтезу аутоантител, которые атакуют и повреждают олигодендроциты, миелин и нейроны.
Что примечательно, 78% хронических областей мозгового поражения при рассеянном склерозе и только 33,3% образцов здорового мозга содержали плазматические клетки CD138 + в паренхиме, где быть их не должно. Не исключено, EBV-инфекция ответственна за экстравазацию последних из сосудистой сети головного мозга, наделяя воспалительный процесс постоянством.
В 46% и 44% тканях соответственно был найден белок BZLF1, притом что в случае биоптатов с рассеянным склерозом он находился преимущественно в связке с областями хронического поражения головного мозга. Считается, что BZLF1 способен подавлять выработку интерлейкина 2 (IL-2) и интерлейкина 6 (IL-6). Помимо участия в B-клеточном созревании IL-6 важен для нейро- и генеза олигодендроглии в нормальных условиях и после повреждения.
Кроме того, в 85% образцах головного мозга пациентов с рассеянным склерозом отмечалось куда более выраженное присутствие иммунных клеток с EBV-кодируемыми малыми РНК-1 (EBER1), нежели в биоптатах здоровых лиц.
Дополнительные свидетельства
Так, ассоциированный с рассеянным склерозом ретровирус (MSRV), относящийся к патогенному W-семейству эндогенных вирусов человека (pHERV-W), может трансактивироваться внешними факторами, например вирусом герпеса человека 6-го типа (HHV-6) или вирусом Эпштейна — Барр. Итогом становится генерация патогенного оболочечного белка MSRV-Env, который, сверхактивируя эндогенный толл-подобный рецептор 4 (TLR4), запускает провоспалительный каскад и подавление ремиелинизации.
Темелимаб (GNbAC1) — рекомбинантное гуманизированное моноклональное антитело, избирательно таргетированное на внеклеточный домен MSRV-Env в целях его нейтрализации.
– вице-президент Российского комитета исследователей рассеянного склероза и президент, генеральный директор Общероссийской общественной организации инвалидов – больных рассеянным склерозом, доктор медицинских наук профессор Ян Власов;
– президент Российского комитета исследователей рассеянного склероза, профессор кафедры неврологии, нейрохирургии и медицинской генетики лечебного факультета РНИМУ им. Н. И. Пирогова Минздрава России, доктор медицинских наук, врач высшей категории Алексей Бойко.

Дебют этой опасной болезни у большинства людей не вызывает настороженности. Ведь её начальные симптомы обычно не внушают тревоги. Повышенную усталость, слабость в руках и ногах, проблемы со зрением сами больные часто списывают на проблемы с позвоночником (дорсопатии), стрессы, недосып. Но ведь именно так может начинаться и рассеянный склероз, который чаще всего выбирает именно молодых (обычно возникает в возрасте 25–40 лет). Это заболевание – вторая по частоте причина инвалидности (после травм) у людей молодого возраста. К сожалению, очень часто об истинном положении вещей пациенты узнают с большим опозданием, так как врачи обычно ставят более распространённые диагнозы.

Всё хуже и хуже
В мире рассеянный склероз диагностирован у 2,3 млн людей. В России, по оценкам специалистов, таких больных не менее 150 тысяч человек. Большая часть из них страдает рецидивирующим рассеянным склерозом (РРС), течение которого проходит с периодами рецидивирующей формы болезни, характеризующейся обострениями, сменяющимися ремиссиями, – то есть спокойными периодами, когда состояние больных улучшается. Но со временем нарушения всё равно накапливаются, и заболевание неуклонно прогрессирует, появляются новые или усугубляются уже имеющиеся симптомы. Тем не менее благодаря своевременной диагностике и правильно назначенному лечению врачам удаётся сдерживать развитие патологии.
Шаг вперёд
Помочь таким пациентам врачи долгое время были не в состоянии – ведь поддерживающее симптоматическое лечение и физическая реабилитация могли лишь немного снизить мышечный тонус, но не замедлить развитие болезни. До сих пор нигде в мире не существовало лекарств с доказанной эффективностью при такой форме болезни. Сегодня благодаря регистрации в России инновационного препарата Окрелизумаб у российских пациентов с таким диагнозом появилась возможность отсрочить развитие инвалидности. По клиническим исследованиям, при приёме этого лекарства скорость прогрессирования болезни снижается на 24%. А по наблюдению врачей, на фоне терапии у трети пациентов вообще отсутствуют какие-либо признаки прогрессирования заболевания, то есть возникает состояние, сравнимое с ремиссией. Кроме того, Окрелизумаб показал более высокую эффективность (на 50% выше, чем у ПИТРС) и в отношении рецидивирующего рассеянного склероза. У 9 из 10 пациентов, проходивших лечение, отсутствовало прогрессирование болезни, что подтверждалось не только клинически, но и на МРТ.

Препарат Окрелизумаб представляет собой моноклональное антитело к особому белку, который связывается с B‑лимфоцитами (клетками иммунной системы) и запускает процесс их уничтожения. Несмотря на то, что лекарство очень дорогое (ожидается, что годовой курс будет стоить более миллиона рублей), есть надежда, что оно войдёт в перечень жизненно необходимых лекарственных средств и каждый больной сможет получить его бесплатно, что даст возможность этим людям воплотить в жизнь задуманное: строить карьеру, создавать семью да и просто нормально жить.
Симптомы рассеянного склероза:
- Повышенная утомляемость. Есть у 90% людей с этим диагнозом.
- Слабость в ногах.
- Онемение конечностей и других участков тела.
- Головная боль.
- Проблемы со зрением (более чем у 25% пациентов).
- Депрессия (в 2 раза чаще, чем у остальных).
- Нарушения работы мочевого пузыря (как минимум у 80% пациентов).
Читайте также:


