Медиаторы высшая нервная деятельность
В настоящее время при классификации медиаторных веществ принято выделять: первичные медиаторы, сопутствующие медиаторы, медиаторы-модуляторы и аллостерические медиаторы. Первичными медиаторами считают те, которые действуют непосредственно на рецепторы постсинаптической мембраны. Сопутствующие медиаторы и медиаторы-модуляторы могут запускать каскад ферментативных реакций, которые, например, фосфорилируют рецептор для первичного медиатора. Аллостерические медиаторы могут участвовать в кооперативных процессах взаимодействия с рецепторами первичного медиатора.
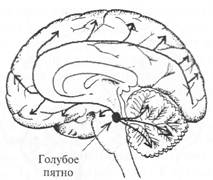
Рис. 2.14. Схема норадренергических путей в головном мозге.
Основным источником норадренергических аксонов являются нейроны голубого пятна — nucl. cereleus (указано стрелкой) и прилежащих участков среднего мозга. Аксоны этих нейронов широко распространяются в стволе мозга, мозжечке, конечном мозге, а также в спинном мозге (на схеме не показано).
обеспечивается не точным анатомическим контактом, а наличием соответствующего рецептора на клетке-мишени. Собственно этот принцип был давно известен в эндокринологии, а исследования последних лет нашли ему более широкое применение.
Одними из самых распространенных являются медиаторы, принадлежащие к группе биогенных аминов. Эта группа медиаторов достаточно надежно идентифицируется микрогистологическими методами. Известны две группы биогенных аминов: катехоламины (дофамин, норадреналин и адреналин) и индоламин (серотонин). Функции биогенных аминов в организме весьма многообразны: медиаторная, гормональная, регуляция эмбриогенеза.
Основным источником норадренергических аксонов являются нейроны голубого пятна и прилежащих участков среднего мозга (рис. 2.14). Аксоны этих нейронов широко распространяются в мозговом
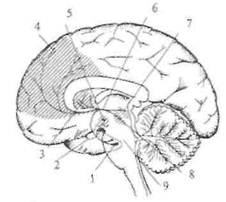
Рис. 2.15. Дофаминергические системы головного мозга.
1 — энторинальная кора; 2 — гипофиз; 3 — хвостатое ядро; 4 — фронтальная кора; 5 — гипоталамус; 6 — медиальный пучок переднего мозга; 7 — черная субстанция; 8 — средний мозг (покрышка); 9 — мозговой ствол.
стволе, мозжечке, в больших полушариях. В продолговатом мозге крупное скопление норадренергических нейронов находится в вентролатеральном ядре ретикулярной формации. В промежуточном мозге (гипоталамусе) норадренергические нейроны наряду с дофаминергическими нейронами входят в состав гипоталамо-гипофизарной системы. Норадренергические нейроны в большом количестве содержатся в периферической нервной системе. Их тела лежат в симпатической цепочке и в некоторых интрамуральных ганглиях.
Дофаминергические нейроны у млекопитающих находятся преимущественно в среднем мозге (так называемая нигро-неостриарная система), а также в гипоталамической области. Дофаминовые цепи мозга млекопитающих хорошо изучены. Известны три главные цепи, все они состоят из однонейронной цепочки. Тела нейронов находятся в мозговом стволе и отсылают аксоны в другие области головного мозга (рис. 2.15).
Одна цепь очень проста. Тело нейрона находится в области гипоталамуса и отсылает короткий аксон в гипофиз. Этот путь входит в состав гипоталамо-гипофизарной системы и контролирует систему эндокринных желез.
Вторая дофаминовая система также хорошо изучена. Это черная субстанция, многие клетки которой содержат дофамин. Аксоны этих нейронов проецируются в полосатые тела. Эта система содержит примерно 3 /4 дофамина головного мозга. Она имеет решающее значение в регулировании тонических движений, Дефицит дофамина в этой системе приводит к болезни Паркинсона. Известно, что при этом заболевании происходит гибель нейронов черной субстанции. Введение L-DOPA (предшественника дофамина) облегчает у больных некоторые симптомы заболевания.
Третья дофаминергическая система участвует в проявлении шизофрении и некоторых других психических заболеваний. Функции этой системы пока изучены недостаточно, хотя сами пути хорошо известны. Тела нейронов лежат в среднем мозге рядом с черной субстанцией. Они проецируют аксоны в вышележащие структуры мозга, мозговую кору и лимбическую систему, особенно к фронтальной коре, к септальной области и энторинальной коре. Энторинальная кора, в свою очередь, является главным источником проекций к гиппокампу.
Согласно дофаминовой гипотезе шизофрении, третья дофаминергическая система при этом заболевании сверхактивна. Эти представления возникли после открытия веществ, снимающих некоторые симптомы заболевания. Например, хлорпромазин и галоперидол имеют разную химическую природу, но они одинаково подавляют активность дофаминергической системы мозга и проявление некоторые симптомов шизофрении, У больных шизофренией, в течение года получавших эти препараты, появляются двигательные нарушения, получившие название tardive dyskinesia (повторяющиеся причудливые движения лицевой мускулатуры, включая мускулатуру рта, которые больной не может контролировать).
Серотонин почти одновременно открыли в качестве сывороточного сосудосуживающего фактора (1948) и энтерамина, секретируемого энтерохромаффиновыми клетками слизистой оболочки кишечника. В 1951 г. было расшифровано химическое строение серотонина и он получил новое название — 5-гидрокситриптамин. В организме млекопитающих он образуется гидроксилированием аминокислоты триптофана с последующим декарбоксилированием. 90% серотонина образуется в организме энтерохромаффиновыми клетками слизистой оболочки всего пищеварительного тракта. Внутриклеточный серотонин инактивируется моноаминоксидазой, содержащейся в митохондриях. Серотонин внеклеточного пространства окисляется перулоплазмином. Большая часть вырабатываемого серотонина связывается с кровяными пластинками и по кровяному руслу разносится по организму. Другая часть действует в качестве
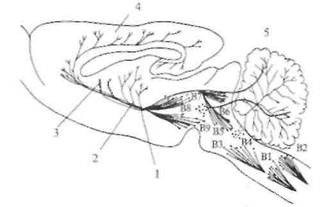
Рис. 2.16. Серотонинергичсские пути в головном мозге крысы (схема).
В1-В9 — группы серотонинергических нейронов в области шва, аксоны которых проецируются в кору больших полушарий, гипоталамус и другие структуры; 1 — медиальный пучок переднего мозга; 2 — гипоталамус; 3 — хвостатое ядро; 4 — кора; 5 — мозжечок.
местного гормона, способствуя авторегулированию кишечной перистальтики, а также модулируя эпителиальную секрецию и всасывание в кишечном тракте.
Серотонинергические нейроны широко распространены в центральной нервной системе (рис. 2.16). Они обнаруживаются в составе дорсального и медиального ядер шва продолговатого мозга, а также в среднем мозге и варолиевом мосту. Серотонинергические нейроны иннервируют обширные области мозга, включающие кору больших полушарий, гиппокамп, бледный шар, миндалину, область гипоталамуса. Интерес к серотонину был привлечен в связи с проблемой сна. При разрушении ядер шва животные страдали бессонницей. Сходный эффект оказывали вещества, истощающие хранилище серотонина в мозге.
Самая высокая концентрация серотонина обнаружена в эпифизе (pineal gland). Серотонин в эпифизе превращается в мелатонин, который участвует в пигментации кожи, а также влияет у многих животных на активность женских гонад. Содержание как серотонина, так и мелатонина в эпифизе контролируется циклом свет—темнота через симпатическую нервную систему.
Другую группу медиаторов ЦНС составляют аминокислоты. Уже давно известно, что нервная ткань с ее высоким уровнем метаболизма содержит значительные концентрации целого набора аминокислот (перечислены в порядке убывания): глутаминовой кислоты, глутамина, аспарагиновой кислоты, гамма-аминомасляной кислоты (ГАМК).
Глутамат в нервной ткани образуется преимущественно из глюкозы. У млекопитающих больше всего глутамата содержится в конечном мозге и мозжечке, где его концентрация примерно в 2 раза выше, чем в стволе мозга и спинном мозге. В спинном мозге глутамат распределен неравномерно: в задних рогах он находится в большей концентрации, чем в передних. Глутамат является одним из самых распространенных медиаторов в ЦНС.
Посте инаптические рецепторы к глутамату классифицируются в соответствии с аффинностью (сродством) к трем экзогенным агонистам — квисгулату, каинату и N-метил-D-аспартату (NMDA). Ионные каналы, активируемые квисгулатом и каина-том, подобны каналам, которые управляются никотиновыми рецепторами — они пропускают смесь катионов (Na + и К + ). Стимуляция NMDA-рецепторов имеет сложный характер активации: ионный ток, который переносится не только Na + и К + , но также Са ++ при открывании ионного канала рецептора, зависит от потенциала мембраны. Вольтзависимая природа этого канала определяется разной степенью его блокирования ионами Mg ++ с учетом уровня мембранного потенциала. При потенциале покоя порядка —75 мВ ионы Mg ++ , которые преимущественно находятся в межклеточной среде, конкурируют с ионами Са ++ и Na + за соответствующие каналы мембраны (рис. 2.17). Вследствие того что ион Mg ++ не может пройти через пору, канал блокируется всякий раз, как попадает туда ион Mg ++ . Это приводит к уменьшению времени открытого канала и проводимости мембраны. Если мембрану нейрона деполяризовать, то количество ионов Mg ++ , которые закрывают ионный канал, снижается и через канал беспрепятственно могут проходить ионы Са ++ , Na + и К + . При редких стимуляциях (потенциал покоя изменяется мало) глутаматергического рецептора ВПСП возникает преимущественно за счет активации квисгулатных и каинатных рецепторов; вклад NMDA-рецепторов незначителен. При длительной деполяризации мембраны (ритмическая стимуляция) магниевый блок удаляется и NMDA-каналы начинают проводить ионы Са ++ , Na + и К + . Ионы Са +4 через вторичные посредники могут потенцировать (усиливать) минПСП, что может привести, например, к длительному увеличению синаптической проводимости, сохраняющейся часами и даже сутками.
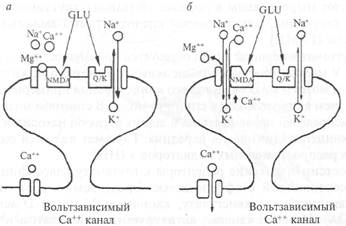
Рис. 2.17. Ответ постсинаптической мембраны на активацию ее глута-матом (схема).
а — при небольшой и 6 — при высокой частоте синаптической активации. В случае а глутамат (GLU) активирует как NMDA, так и квисгулатные/каинатные (Q/K) рецепторы, открываются каналы, пропускающие ионы Na + и К + . NMDA-каналы заблокированы Mg ++ . В случае б имеет место устойчивая деполяризация постсинаптической мембраны, ионы Mg ++ покидают NMDA-каналы и они начинают пропускать ионы Ca ++ , Na + и К + . Деполяризация может также активировать вольтзависимые кальциевые каналы.
Из тормозных медиаторов ГАМК является самой распространенной в ЦНС. Она синтезируется из L-глутаминовой кислоты в одну стадию ферментом декарбоксилазой, наличие которой является лимитирующим фактором этого медиатора. Известно два типа ГАМК-рецепторов на постсинаптической мембране: ГАМКА (открывает каналы для ионов хлора) и ГАМКБ (открывает в зависимости от типа клетки каналы для К + или Са ++ ). На рис. 2.18 показана схема ГАМК-рецептора. Интересно, что в его состав входит бензодиазипиновый рецептор, наличием которого объясняют действие так называемых малых (дневных) транквилизаторов (седуксена, тазепама и др.). Прекращение действия медиатора в ГАМК-синапсах происходит по принципу обратного всасывания (молекулы медиатора специальным механизмом поглощаются из синаптической щели в цитоплазму нейрона). Из антагонистов ГАМК хорошо известен бикукулин. Он хорошо проходит через гематоэнцефалический барьер, оказывает сильное воздействие на организм даже в
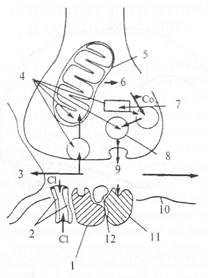
Рис. 2.18. Схема рецептора постсинаптической мембраны к ГАМК вместе с бензодиазипиновым рецептором. Активация бензодиази-пинового рецептора открывает хлорный канал.
1 — бензодиазипиновый рецептор; 2 — хлорный канал; 3 — глиальная клетка; 4, 9 — ГАМК; 5 — митохондрия; 6 — глютаминовая кислота; 7 — глютаматдекарбоксилаза; 8 — синаптический пузырек; 10 — субсинаптическая мембрана; 11 — ГАМК-рецептор; 12 — ГАМК-модулин.
малых дозах, вызывая конвульсии и смерть. ГАМК обнаруживается в ряде нейронов мозжечка (в клетках Пуркинье, клетках Гольджи, корзинчатых клетках), гиппокампа (в корзинчатых клетках), в обонятельной луковице и черной субстанции.
Идентификация ГАМК-цепей мозга трудна, так как ГАМК — обычный участник метаболизма в ряде тканей организма. Метаболическая ГАМК не используется как медиатор, хотя в химическом отношении их молекулы одинаковы. ГАМК определяется по ферменту декарбоксилазе. Метод основан на получении у животных антител к декарбоксилазе (антитела экстрагируют, метят и вводят в мозг, где они связываются с декарбоксилазой).
Другим известным тормозным медиатором является глицин. Глицинергические нейроны находятся главным образом в спинном и продолговатом мозге. Считают, что эти клетки выполняют роль тормозных интернейронов.
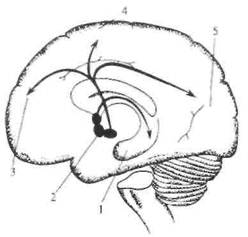
Рис. 2.19. Ацетилхолинергические пути в головном мозге (схема).
1 — гиппокамп; 2 — базальное ядро; 3 — фронтальная кора; 4 — теменная кора; 5 — затылочная кора.
Ацетилхолин — один из первых изученных медиаторов. Он чрезвычайно широко распространен в периферической нервной системе. Примером могут служить мотонейроны спинного мозга и нейроны ядер черепных нервов. Как правило, холинергические цепи в мозге определяют по присутствию фермента холинэстеразы. В головном мозге тела холинергических нейронов находятся в ядре перегородки, ядре диагонального пучка (Брока) и базальных ядрах. Нейроанатомы считают, что эти группы нейронов формируют фактически одну популяцию холинергических нейронов: ядро переднего мозга, nucleus basalis (оно расположено в базальной части переднего мозга) (рис. 2.19). Аксоны соответствующих нейронов проецируются к структурам переднего мозга, особенно в новую кору и гиппокамп. Здесь встречаются оба типа ацетилхолиновых рецепторов (мускариновые и никотиновые), хотя считается, что мускариновые рецепторы доминируют в более рострально расположенных мозговых структурах. По данным последних лет складывается впечатление, что ацетилхолиновая система играет большую роль в процессах, связанных с высшими интегративными функциями, которые требуют участия памяти. Например, показано, что в мозге больных, умерших от болезни Альцгеймера, наблюдается массивная утрата холинергических нейронов в nucleus basalis.
Медиаторы - довольно разнородная группа веществ. В настоящее время идентифицировано около 100 веществ, которые выполняют роль медиатора: моноамины, аминокислоты, нейропептиды (вещество Р, метэнкефалин, лейэнкефалин, эндорфин, нейротензин, АКТГ, ангиотензин, окситоцин, вазопрессин, вазоактивный кишечный пептид, соматостатин, тиролиберин, бомбезин, холецистокининоподобный пептид, карнозин).
Низкомолекулярные медиаторы синтезируются в пресинаптических нейронах и накапливаются в их везикулах. Синтез медиаторов происходит из соответствующих предшественников и требует энергии. Он протекает в соме нейрона, откуда везикулы перемещаются к нервным окончаниям.
Благодаря исследованиям последних десятилетий довольно простая схема химической синаптической передачи значительно усложнилась. Появление иммунохимических методов позволило показать, что в одном синапсе могут сосуществовать несколько групп медиаторов, а не один, как это предполагали раньше. Например, в одном синаптическом окончании одновременно могут находиться синаптические пузырьки, содержащие ацетилхолин и норадреналин, которые довольно легко идентифицируются на электронных фотографиях (ацетилхолин содержится в прозрачных пузырьках диаметром около 50 нм, а норадреналин -- в электронно-плотных пузырьках диаметром до 200 нм). Кроме классических медиаторов, в синаптическом окончании могут находиться один или несколько нейропептидов. Количество веществ, содержащихся в синапсе, может доходить до 5-6 (своеобразный коктейль). Более того, медиаторная специфичность синапса может меняться в онтогенезе. Например, нейроны симпатических ганглиев, иннервирующие потовые железы у млекопитающих, исходно норадренергичны, но у взрослых животных становятся холинергичными.
В настоящее время при классификации медиаторных веществ принято выделять: первичные медиаторы, сопутствующие медиаторы, медиаторы-модуляторы и аллостерические медиаторы. Первичными медиаторами считают те, которые действуют непосредственно на рецепторы постсинаптической мембраны. Сопутствующие медиаторы и медиаторы-модуляторы могут запускать каскад ферментативных реакций, которые, например, изменяют чувствительность рецептора к первичному медиатору. Аллостерические медиаторы могут участвовать в кооперативных процессах взаимодействия с рецепторами первичного медиатора.
Одними из самых распространенных являются медиаторы, принадлежащие к группе биогенных аминов. Эта группа медиаторов достаточно надежно идентифицируется микрогистологическими методами. Известны две группы биогенных аминов: катехоламины (дофамин, норадреналин и адреналин) и индоламин (серотонин). Функции биогенных аминов в организме весьма многообразны: медиаторная, гормональная, регуляция эмбриогенеза.
Основным источником норадренергических аксонов являются нейроны голубого пятна и прилежащих участков среднего мозга. Аксоны этих нейронов широко распространяются в мозговом стволе, мозжечке, в больших полушариях. В продолговатом мозге крупное скопление норадренергических нейронов находится в вентролатеральном ядре ретикулярной формации. В промежуточном мозге (гипоталамусе) норадренергические нейроны наряду с дофаминергическими нейронами входят в состав гипоталамо-гипофизарной системы. Норадренергические нейроны в большом количестве содержатся в периферической нервной системе. Их тела лежат в симпатической цепочке и в некоторых интрамуральных ганглиях.
ДОФАМИН - присутствует в "центрах удовольствия" лимбической системы и некоторых ядрах ретикулярной формации, где он участвует в процессах избирательного внимания. Много дофаминергических нейронов у млекопитающих находится в среднем мозге (так называемая нигро-неостриарная система), а также в гипоталамической области. Дофаминовые цепи мозга млекопитающих хорошо изучены. Известны три главные цепи, все они состоят из однонейронной цепочки. Тела нейронов находятся в мозговом стволе и отсылают аксоны в другие области головного мозга.
Одна цепь очень проста. Тело нейрона находится в области гипоталамуса и отсылает короткий аксон в гипофиз. Этот путь входит в состав гипоталамо-гипофизарной системы и контролирует систему эндокринных желез.
Вторая дофаминовая система также хорошо изучена. Это черная субстанция, многие клетки которой содержат дофамин. Аксоны этих нейронов проецируются в полосатые тела. Эта система содержит примерно 3/4 дофамина головного мозга. Она имеет решающее значение в регулировании тонических движений. Дефицит дофамина в этой системе приводит к болезни Паркинсона. Известно, что при этом заболевании происходит гибель нейронов черной субстанции. Введение L-DОРА (предшественника дофамина) облегчает у больных некоторые симптомы заболевания.
Третья дофаминергическая система участвует в проявлении шизофрении и некоторых других психических заболеваний. Функции этой системы пока изучены недостаточно, хотя сами пути хорошо известны. Тела нейронов лежат в среднем мозге рядом с черной субстанцией. Они проецируют аксоны в вышележащие структуры мозга, мозговую кору и лимбическую систему, особенно к фронтальной коре, к септальной области и энторинальной коре. Энторинальная кора, в свою очередь, является главным источником проекций к гиппокампу.
Согласно дофаминовой гипотезе шизофрении, третья дофаминергическая система при этом заболевании сверхактивна. Эти представления возникли после открытия веществ, снимающих некоторые симптомы заболевания. Например, хлорпромазин и галоперидол имеют разную химическую природу, но они одинаково подавляют активность дофаминергической системы мозга и проявление некоторые симптомов шизофрении. У больных шизофренией, в течение года получавших эти препараты, появляются двигательные нарушения, получившие название tardive dyskinesia (повторяющиеся причудливые движения лицевой мускулатуры, включая мускулатуру рта, которые больной не может контролировать).
Серотонин - в стволе мозга регулирует сон и определяет объем информации в сенсорных путях, идущих к коре мозга (ограничивает ее). Оказывает контролирующее влияние на активность спинного мозга. В гипоталамусе контролирует температуру тела.
Серотонин почти одновременно открыли в качестве сывороточного сосудосуживающего фактора (1948) и энтерамина, секретируемого клетками слизистой оболочки кишечника. В 1951 г. было расшифровано химическое строение серотонина и он получил новое название -- 5-гидрокситриптамин. В организме млекопитающих он образуется гидроксилированием аминокислоты триптофана с последующим декарбоксилированием. 90% серотонина образуется в организме энтерохромаффиновыми клетками слизистой оболочки всего пищеварительного тракта. Внутриклеточный серотонин инактивируется моноаминоксидазой, содержащейся в митохондриях.
Серотонинергические нейроны широко распространены в центральной нервной системе . Они обнаруживаются в составе дорсального и медиального ядер шва продолговатого мозга, а также в среднем мозге и варолиевом мосту. Серотонинергические нейроны иннервируют обширные области мозга, включающие кору больших полушарий, гиппокамп, бледный шар, миндалину, область гипоталамуса. Интерес к серотонину был привлечен в связи с проблемой сна. При разрушении ядер шва животные страдали бессонницей. Сходный эффект оказывали вещества, истощающие хранилище серотонина в мозге.
Самая высокая концентрация серотонина обнаружена в эпифизе. Серотонин в эпифизе превращается в мелатонин, который участвует в пигментации кожи, а также влияет у многих животных на активность женских гонад. Содержание как серотонина, так и мелатонина в эпифизе контролируется циклом свет--темнота через симпатическую нервную систему.
Другую группу медиаторов ЦНС составляют аминокислоты. Уже давно известно, что нервная ткань с ее высоким уровнем метаболизма содержит значительные концентрации целого набора аминокислот (перечислены в порядке убывания): глутаминовой кислоты, глутамина, аспарагиновой кислоты, гамма-аминомасляной кислоты (ГАМК). Глутамат в нервной ткани образуется преимущественно из глюкозы. У млекопитающих больше всего глутамата содержится в конечном мозге и мозжечке, где его концентрация примерно в 2 раза выше, чем в стволе мозга и спинном мозге. В спинном мозге глутамат распределен неравномерно: в задних рогах он находится в большей концентрации, чем в передних. Глутамат является одним из самых распространенных медиаторов в ЦНС.
Из тормозных медиаторов ГАМК является самой распространенной в ЦНС. Она синтезируется из L-глутаминовой кислоты. Известно два типа ГАМК-рецепторов на постсинаптической мембране: ГАМК-А (открывает каналы для ионов хлора) и ГАМК-Б (открывает в зависимости от типа клетки каналы для К или Са). Интересно, что в их состав входит бензодиазипиновый рецептор, наличием которого объясняют действие так называемых малых (дневных) транквилизаторов (седуксена, тазепама и др.). Прекращение действия медиатора в ГАМК-синапсах происходит по принципу обратного всасывания (молекулы медиатора специальным механизмом поглощаются из синаптической щели в цитоплазму нейрона). Из антагонистов ГАМК хорошо известен бикукулин. Он хорошо проходит через гематоэнцефалический барьер, оказывает сильное воздействие на организм даже в малых дозах, вызывая конвульсии и смерть. ГАМК обнаруживается в ряде нейронов мозжечка (в клетках Пуркинье, клетках Гольджи, корзинчатых клетках), нейронах гиппокампа (в корзинчатых клетках), в обонятельной луковице и черной субстанции.
Идентификация ГАМК-цепей мозга трудна, так как ГАМК -- обычный участник метаболизма в ряде тканей организма. Метаболическая ГАМК не используется как медиатор, хотя в химическом отношении их молекулы одинаковы. ГАМК определяется по фериенту декарбоксилазе. Метод основан на получении у животных антител к декарбоксилазе (антитела экстрагируют, метят и вводят в мозг, где они связываются с декарбоксилазой).
Другим известным тормозным медиатором является глицин. Глицинергические нейроны находятся главным образом в спинном и продолговатом мозге. Считают, что эти клетки выполняют роль тормозных интернейронов.
Ацетилхолин -- один из первых изученных медиаторов. Он чрезвычайно широко распространен в периферической нервной системе. Примером могут служить мотонейроны спинного мозга и нейроны ядер черепных нервов. Как правило, холинергические цепи в мозге определяют по присутствию фермента холинэстеразы. В головном мозге тела холинергических нейронов находятся в ядре перегородки, ядре диагонального пучка (Брока) и базальных ядрах. Нейроанатомы считают, что эти группы нейронов формируют фактически одну популяцию холинергических нейронов: ядро переднего мозга, базальное ядро (оно расположено в базальной части переднего мозга). Аксоны соответствующих нейронов проецируются к структурам переднего мозга, особенно в новую кору и гиппокамп. Здесь встречаются оба типа ацетилхолиновых рецепторов (мускариновые и никотиновые), хотя считается, что мускариновые рецепторы доминируют в более рострально расположенных мозговых структурах. По данным последних лет складывается впечатление, что ацетилхолиновая система играет большую роль в процессах, связанных с высшими интегративными функциями, которые требуют участия памяти. Например, показано, что в мозге больных, умерших от болезни Альцгеймера, наблюдается массивная утрата холинергических нейронов в базальных ядрах.
Доброго времени суток. На просторах всемирной сети вы найдете огромное количество научно-популярной информации о том, что такое нейромедиаторы и почему их влияние столь колоссально, если мы говорим о поведенческих аспектах человеческой жизни.
Однако среди большого количества статей вы найдете большое количество ненужной информации которая никак не пригодиться вам. Я беру на себя непростую задачу и попытаюсь вам на пальцах объяснить что к чему (для тех, кто не в теме) и упорядочить знания тех, кто с физиологией немного знаком.
Нейромедиаторы-биологически активные субстанции, с помощью которых нервные клетки взаимодействуют между собой. На каждый нейромедиатор приходится свой уникальный рецептор (их как правило несколько) с которым тот взаимодействует. В зависимости от типа медиатора, действие на ЦНС может сильно отличаться. Для вашего удобства, я разделю эти молекулы на 2 большие группы: медиаторы тормозные и активирующие. К тормозным относится бОльшая часть: ГАМК, ацетилхолин, эндорфины, анандамиды и др.
Возбуждающих медиаторов не так много. К ним относится в первую очередь глутамат, адреналин и норадреналин.
В рунете и в частности на пикабу вы можете натолкнутся на статьи, которые будут вас убеждать в том, что серотонин-медиатор счастья, дофамин-медиатор мотивации и др. Однако такое упрощение сильно искажает реальную картину. На самом деле, один медиатор может выполнять разнообразные функции, которые варьируются от типа рецептора на который с которым он контактирует. Так, дофамин в черной субстанции (зона головного мозга) отвечает за двигательную активность и у людей страдающих Паркинсоном нейроны в этой области погибают, в следствии чего у них наблюдается тремор конечностей. Заметьте, дофаминовые нейроны черной субстанции уничтожены, а проблема заключается исключительно в неспособности совершать некоторые двигательные акты. Человек с данный синдромом может вообще не испытывать каких-либо проблем с мотивацией, что подтверждает разнообразность функций, выполняемых одним нейромедиатором.
Итак, забудьте про серотониновое счастье, дофаминовую мотивацию и другие некорректные высказывания. Я попытаюсь объяснить, почему данные медиаторы второстепенны и расскажу, что на самом деле оказывает колоссальное влияние на поведение и самочувствие.
Вы знакомы с состоянием, когда вы проснулись, не успели сделать ничего толкового и уже заебались? Наверняка. Чувство усталости без повода и прокрастинация присуще всем индивидам. Сейчас, я выскажу суждение, которое дальше буду раскрывать: "Когда вы ничего не делаете, вы тратите энергии больше, чем при выполнении различных действий и вдобавок получаете крайне неприятное чувство усталости и апатии".
Как это происходит: Вся информация, которая поступает к вам в мозг привязана к сенсорным системам организма, и будучи ими обработана она преобразуется в электрический импульс, с помощью нейротрансмиттеров. Любого рода раздражители (свет, звук, прикосновение и т.д) заставляют организм вырабатывать адреналин и норадреналин, оказывая возбуждающее действие. Следом за этим возбуждением всегда должна идти седатация, которую в первую очередь выполняют молекулы ГАМК и эндорфины. А теперь к сути. Хорошее настроение-это не дофамин и серотонин, а скорость седатации, с помощью которой организм нивелирует влияние стрессовых гормонов. Внимательно вчитайтесь в эти слова. Скорость седатации-основное на чем стоит заострить свой взор. Почему? На самом деле все предельно просто. Когда происходит секреция стрессовых медиаторов и гормонов, они довольно быстро расходуют молекулы АТФ (Главный источник энергии). АТФ преобразуется в АДФ и так до АМФ, а вот АМФ будет стимулировать аденозиновые рецепторы, которые и отвечают за "неприятную усталость". Чтобы этого избежать, вы должны максимально быстро сбрасывать напряжение, которое возникает в том или ином центре головного мозга и только в таком случае вы получите хорошее настроение и отсутствие симптома, описанного выше.
Смоделируем ситуацию: Вы в течении дня занимались определенной деятельностью и все вроде бы шло по плану, однако придя домой, вы взяли смартфон и начали листать ленту. Что в это время происходит в ЦНС? Возбуждение, поступающее из вне находится в зрительной зоне головного мозга. Работает только 1 зона мозга, в то время как другие работают совсем незначительно. Адреналин с норадреналином быстро реализуют свое действие и вы чувствуете, как нормальное настроение сменяется апатией и ленью, хотя вы вроде бы "отдыхаете". Это происходит за счет того, что другие зоны мозга не получают стимуляцию. Как следствие, организм секретирует меньшее количество тормозных медиаторов, что приводит к изменению сознания.
А теперь самое интересное. Что же все таки нужно делать, чтобы почти всегда испытывать нормальное или по настоящему хорошее настроение? Нужно делать то, что активирует большОе количество нейронных сетей. Сразу пример:
Вы выходите на пробежку и начинаете бег (работает двигательный центр), в это же время ваша барабанная перепонка воспринимает любимую музыку с наушников (слуховой центр) и ваши глаза воспринимают информацию о местности вокруг (зрительный центр). Уже на полпути до окончания сеанса пробежки вы начинаете испытывать чувство удовлетворения от своей деятельности и происходит это не от вашего любимого дофамина/серотонина, а от эндорфинов и ГАМК, которые гасят волну возбуждения возникшей в нескольких центрах.
Важно: Чем больше зон мозга вы задействуете в единый момент времени, тем быстрее будет седатация и тем большее удовлетворение вы получите.
Пример номер 2. Вы собираетесь посмотреть с друзьями фильм. Разместившись в кинотеатре еще до начала фильма вы активно потребляете попкорн запивая кока-колой (сразу идет информация о поступлении пищи в организм и задействуется область нейронов ответственная за процесс пищеварения), вы начинаете смотреть фильм и ваши зрительные, слуховые и ассоциативные центры начинают работать интенсивнее. Далее вы получаете заслуженную седатацию и хорошее настроение.
Важно: Чем сильнее скорость и степень возбуждения, тем сильнее и быстрее происходит седатация и как следствие пряник, подаренной самой эволюцией в виде эндогенных опиатов (эндорфинов).
Друзья, нет адреналинового кайфа. Когда парашутист совершает прыжок с парашюта в первые секунды надпочечники секретируют огромное количество адреналина. И организм, что бы адаптироваться к такому стрессу начинает выработку эндорфинов и ГАМК. Понимание работы этих молекул координально изменит ваше поведение и степень удовлетворения жизнью.
Теперь перейдем к веществам, поскольку в данной статье грех не затронуть такую тему. Как известно, самую сильную аддикцию и кайф вызывают вещества относящиеся к группе опиатов. Не стимуляторы, действующие на ваши дофамины. Не эмпатогены, взаимодействующие с серотониновыми рецепторами, а именно опиаты. Я думаю, после прочтения того, что я изложил выше у вас не должны возникать вопросы, почему это так. Все предельно понятно.
Помимо опиатов, существует другая группа веществ называемых миорелаксантами. Большинство подростков активно злоупотребляют Лирикой, Габапентином и другими сильнодействующими соединениями для получения кайфа. ВЫ МОЖЕТЕ ПОЛУЧИТЬ ЭТОТ КАЙФ САМИ. Забудьте про психоактивные вещества, и перечитайте примеры, которые изложены выше. Вам требуется лишь активация нескольких зон головного мозга и вы получите мощный выброс ГАМК и эндорфинов, и не получите тяжелую зависимость и синдром отмены, который возникает при приеме экзогенных веществ.
Друзья, тема довольно обширна и сложна в понимании. Я постарался изложить то, что знаю. Если у вас возникли вопросы и нужно что-либо пояснить я постараюсь ответить вам в комментариях.
Удачи и хорошего настроения
![]()
Определить дефицит того или иного медиатора или нарушение чувствительности рецептора к ним можно основываясь на симптомы. Анализы здесь бесполезны. Низкая эмоциональность может быть нормой, если у вас это было всегда. Если же нет, можете обратиться к специалисту
Про медитацию у меня есть статься, можешь ознакомиться. По всей видимости, механизм "кайфа" в медитации тоже заключен в скорости падения сигнала. Сначала ты концентрируешься на объекте медитации (рост возбуждения, возможен хаотичный поток мыслей), а далее происходит довольно сильная седатация (отсутствие мыслей, спокойно-бдительное состояние) . Но с первого раза это мало у кого выйдет. Тренировать концентрацию-задача требующая времени
А как название на латыни препаратов ГАМК, ну, чтоб таблетки посмотреть?
Не понял суть вопроса. Введите в поисковике миорелаксанты и/или транквилизаторы и получите список.
Спасибо, поизучаем. Я имел в виду названия лекарств, чтобы поискать в европах. В Эстонии, к примеру, препаратов с ГАМК в аптеках нет.
У вас наверняка есть ГАМКи в чистом виде. Такие как Фенибут или Аминалон. Однако про их эффективность ничего сказать не могу. Многие считают, что работают они как плацебо и не более. Однако агонисты ГАМК рецепторов (диазепам, алпразолам) должны продаваться в ваших аптеках (но строго по рецепту психотерапевта)
Спасибо, информация - та, что надо мне сейчас.
Практикуйте и убеждайтесь в прочитанном :)
Что скажете про Тофизопам, в лечении депрессии, когда нет ни энергии, ни желания ничего делать?
Бензодиазепины не используют при лечении депрессии. В первую очередь их юзают как противотревожные и снотворные. При депрессиях на данный момент выбор психотерапевта падает на селективные ингибиторы обратного захвата серотонина (СИОЗС), поскольку данный класс довольно эффективен и обладает минимумом побочных эффектов. В случае, если ответа на СИОЗС или СИОЗСН нет, могут назначить трициклические антидепрессанты. Очень редко-ингибиторы моноаминоксидазы (ИМАО)
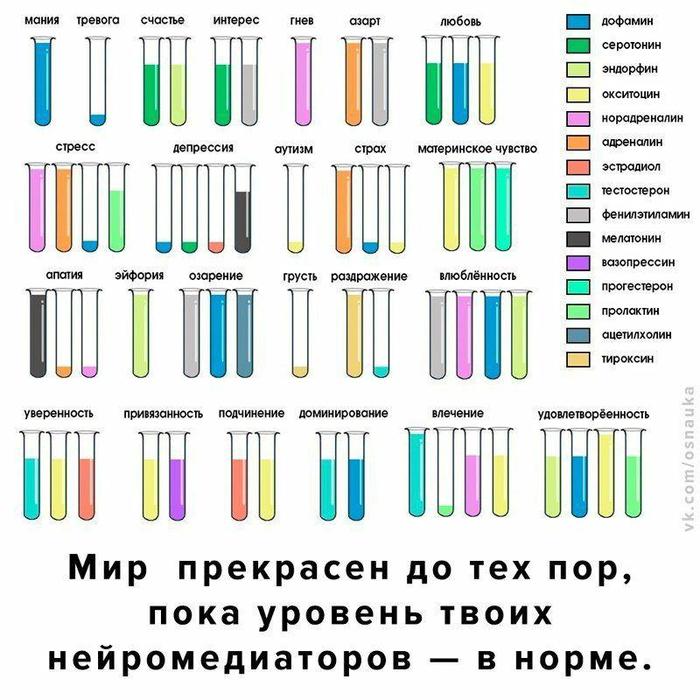
Какой твой уровень нейромедиаторов?
![]()
Внутри шизофрении. Часть 1.
Заболевание, которое можно счесть за шизофрению, было известно с древних времен, возможно, даже доисторических. Отчетливые упоминания есть в Библии (помните, как царь Навухудоносор кушал траву с луга?), ими сквозит Античность и так далее. Однако утверждать на 100% ничего невозможно: существуют психозы и помимо шизофрении, а также есть, например, паразиты, поражающие нервную систему и способные вызвать галлюцинации. К тому же, не надо забывать о сифилисе, который с человеком живет уж точно не меньше, чем шизофрения.

В историю шизофрении я не собираюсь сильно вдаваться, поскольку об этом много сказано. Все написанное выше я упоминаю только с одной целью: чтобы показать, насколько сложный и ускользающий смысл вкладывается в этот термин.
Здесь нужно сделать небольшую оговорку: нам с вами, с раннего детства давящимися плодами науки, которые созревали в течение столетий, люди прошлого могут казаться очень недалекими. Ну как тут было не отличить, скажем, расстройства настроения и психозы? Ну вот больного глючит, как скотину, а вот он просто грустный сидит. Очевидно же, что это разные заболевания! На самом деле, нет. Главная боль всей медицины состоит в том, что одна болезнь в большинстве случаев не мешает развиваться другой. И расстройства настроения (аффективные расстройства) не только не мешают психозам, а зачастую сочетаются.
(Вот и сам Крепелин):

Надо сказать, что в те годы содержимое черепа было настоящим черным ящиком для науки. Оно и сейчас в значительной мере остается черным ящиком, но тогда мы даже представить не могли, КАКАЯ херня там творится. Все эти нервные связи, нейромедиаторы, нейронные сети, колонки, контуры… Едва ли хоть кто-то догадывался, что все может быть устроено так странно. Сама идея о том, что электрическая активность мозга большей частью опосредуется химическими веществами – дикость какая-то. Поэтому все, что оставалось психиатрам тех лет – наблюдать и накапливать знания, надеясь на психиатров будущего.
Для того, чтобы хоть немного приоткрыть завесу тайны над заболеванием, нужны были очень крупные открытия в нейробиологии и нейрофизиологии, которые в те времена были невозможны просто технологически. Первый толчкок, который помог предположить истинные причины шизофрении, был со стороны фармакологии. Это открытие аминазина. Цитата с одного ресурса:
В 1950 году французский нейрохирург Генри Лабори предположил, что чрезмерные переживания его пациентов перед операцией вызывают выброс избыточного количества гистамина. Гистамин — небольшая молекула, которая регулирует сотни процессов в организме: от выделения желудочного сока до температуры. Лабори считал, что именно чрезмерный выброс гистамина из-за тревоги пациентов может вызывать осложнения анестезии и даже внезапную смерть.
Лабори методом проб и ошибок пытался подобрать подходящий антигистаминный препарат. Совершенно случайно он обнаружил, что не самое популярное лекарство — хлорпромазин — действительно успокаивает пациентов. Более того, хлорпромазин усиливал действие анестезии.
Предположение довольно типичное для тех времен, хотя и неверное. Тем не менее, ошибочное предположение привело к великому открытию – открытию первого на свете нейролептика. А сочетание нейролептиков с анестетиками используется до сих пор (нейролептанальгезия). Нейролептики (они же антипсихотики) – препараты, (относительно) избирательно действующие на симптомы психоза – бред и галлюцинации. Это открытие, в конечном счете, и помогло составить современные представления о причинах и патогенезе (т.е развитии болезни) шизофрении. Последовавшие исследования позволили открыть различные рецепторы в головном мозге, в том числе рецептора домафина. Именно тогда и оказалось, что основным эффектом нейролептиков является блокада эффектов дофамина, а дальше все заверте…
Вот мы и подошли к тому, чтобы описать сегодняшние представления о патогенезе шизофрении. Только представьте, какую дикую работу пришлось проделать, чтобы подойти к примерному представлению о том, как развивается эта психическая болезнь. Я буду идти в своем рассказе по такому принципу: от самых элементарных представлений на уровне молекул и клеток до нарушений в работе мозга в целом, а затем до нарушений психики.

Возможно, у вас уже возник вопрос: а почему тогда не использовать методы типа позитронно-эмисионной томографии или ф-МРТ и не выявить, какие отделы мозга работают неправильно? Да, заманчивая идея, и это, конечно же, пытались сделать, и даже есть результаты. Однако результаты эти породили больше вопросов, чем ответов. Действительно, удалось найти нарушения в работе мозга при шизофрении на ПЭТ и ф-МРТ, и касаются они преимущественно работы височных и лобных долей мозга, а также лимбической системы и их взаимодействия. Однако они встречаются не только при шизофрении, и не у всех шизофреников идентичны, чтобы можно было вбить в программу шаблон, который бы автоматически определял подобные изменения. Идея не нова, и в свое время изучали шизофрению с помощью рентгена, эхоэнцефалографии/скопии и других методик, однако результат всегда был похожим: да, что-то есть, но данных, однозначно указывающих на шизофрению, нет.
Как видно, даже здесь шизофрения дает прикурить. Очень мозаичное и скользкое заболевание, не дающее нам никакой нити, за которую можно было бы уцепиться и распустить весь клубок. Таким же оно предстает перед психиатрами – королева масок.
Как нетрудно догадаться, эти анатомические изменения порождают нейрохимические изменения, и тут, боюсь, придется вкратце напомнить основы нейрохимии мозга.
В нашем мозге постоянно осуществляется напряженная работа, которая проявляется в передаче электрических импульсов между нейронами. Соединение между двумя нейронами осуществляется с помощью специальной структуры – синапса. Примерно так он выглядит:
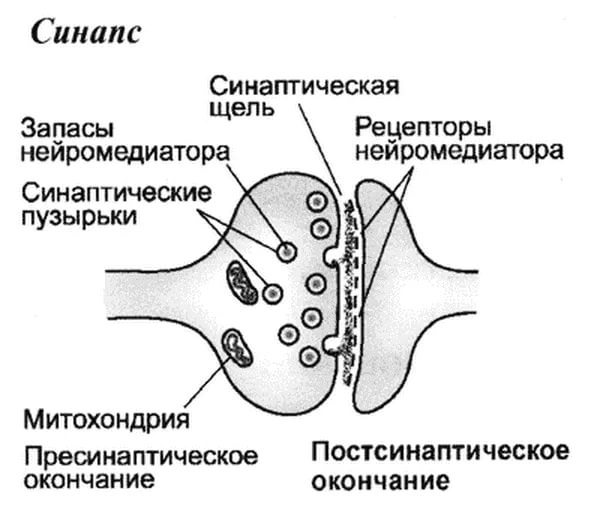
Читайте также:


