Тригеминальная невротизация лицевого нерва
Общие сведения
Нейропатия лицевого нерва (синоним — неврит лицевого нерва, паралич Белла) представляет собой паралич/парез лицевого нерва, сопровождающийся чувствительными, двигательными и вегетативными нарушениями в зоне иннервации мимических мышц и асимметрией лица. Нейропатия лицевого нерва (НЛН) является одной из распространенных и актуальных проблем неврологии.
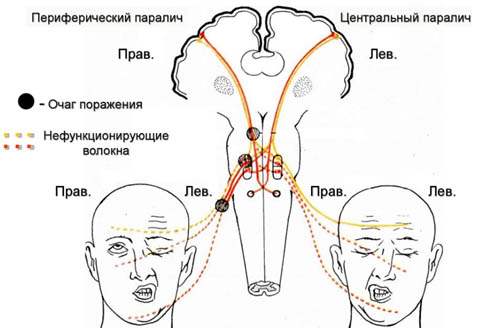
В первую очередь необходимо отметить, что НЛН развивается всегда лишь при поражении нервного волокна от двигательного ядра лицевого нерва до его выхода из шилососцевидного отверстия (периферический парез) и всегда на одноименной стороне в отличии от центрального пареза, который возникает преимущественно при инсульте и зачастую сочетается с парезом конечностей, развивающихся на противоположной очагу стороне (рис. ниже).
Лицевой нерв (ЛН) относится к преимущественно двигательным нервам, которые обеспечивают мимику, процессы моргания, жевания, глотания, нахмуривания. Однако в составе ствола лицевого нерва также проходят составные части промежуточного нерва — парасимпатические (секреторные) и чувствительные (вкусовые) волокна, иннервирующих слюнные железы, а также вкусовую чувствительность языка.
Относительно высокая частота поражения лицевого нерва во много обусловлена присущими ему анатомо-топографическими особенностями — нерв имеет сложный и длительный ход в узком костном канале височной кости. Наиболее уязвимым отрезком ЛН (в котором происходит его ущемление/сдавливание) является отрезок, расположенный в узком извитом канале где в случаях развития отека, обусловленного различными причинами (например, воспалением) и происходит его сдавление.
Среди разных локализаций поражения периферического отдела ЛН паралич Белла относится к наиболее часто встречаемой патологии (16-25 случаев /100 000 населения) и обусловлен развитием отека и последующей его компрессии в костном канале (туннельный синдром). Высокая ранимость ЛН в фаллопиевом канале объясняется превалированием его в поперечном сечении канала, где он занимает 40%-70% всей площади. При этом несмотря на то, что канал в отдельных местах сужается, толщина самого нервного ствола остается неизменной.
В подавляющем большинстве случаев периферический парез лицевого нерва проявляется односторонним поражением лицевого нерва. Правая/левая лицевая сторона поражаются с одинаковой частотой. На долю двусторонней невропатии ЛН приходится всего 6,2% всех его поражений. Средний возраст начала заболевания около 40 лет, но может встречаться в любом возрасте. Наименьший показатель заболеваемости отмечается у детей в возрасте до 10 лет, повышается у лиц возрастной группы 10–29 лет, стабильные показатели характерны для лиц 30–69 лет и максимальных показателей достигает в популяции больных после 70 лет.
Для заболевания характерна высокая частота осложнений (7–18% случаев), в 24,5% отмечаются рецидивирующие невропатии ЛН. Повторные невропатии по сравнению с первичными протекают более тяжело, труднее лечатся и крайне редко завершаются полным восстановлением. Нейропатия лицевого нерва, как пишут многие пациенты, посещающие специальный форум, является чрезвычайно психотравмирующей ситуацией для больных и крайне негативно отражается на психоэмоциональной сфере и физическом состоянии пациентов вплоть до развития невроза. Паралич ЛН является частой причиной длительного нарушения трудоспособности и существенно снижает качество жизни.
Патогенез
Пусковым фактором НЛН является раздражение сосудов черепно-цервикального отдела, что способствует развитию ангиоспазма позвоночной и ветвей наружной сонной артерии, что приводит к первичной ишемии корешка ЛН. Нарастающие нарушения микроциркуляции в структурах ЛН приводят к аноксическому отеку нерва. Это в сою очередь приводит к компрессии (сдавливанию) нервной ткани в лицевом (фаллопиевом) канале височной кости, нарушению нервно-мышечной проводимости, обусловленного блокадой процесса высвобождения из окончаний двигательных аксонов ацетилхолина и расстройством взаимодействия ацетилхолина с рецепторами, расположенными на постсинаптической мембране. По мере нарастания расстройств в нервной ткани развивается вторичная ишемия ЛН.
Классификация
Выделяют первичное поражение ЛН, вызванное переохлаждением и вторичное, как осложнение других заболеваний.
По этиологическому признаку выделяют:
- Паралич Белла (идиопатическая невропатия).
- Отогенные невриты (при воспалении среднего уха/сосцевидного отростка височной кости).
- Инфекционные невриты (при гриппе, герпесе, паротите, полиомиелите и др.).
- Травматические невриты (повреждение лицевого нерва).
- Ишемические (в случаях нарушении кровоснабжения нерва).
Причины неврита лицевого нерва
При периферическом характере поражения ЛН установить причины возникновения заболевания в большинстве случаев достаточно сложно. Принято считать, что причины невропатии ЛН полиэтиологичны (ишемические, отогенные, идиопатические, травматические, инфекционные и другого генеза). Как уже указывалось, паралич Белла развивается вследствие сдавления нерва в узком извитом канале височной кости, происходящего по различным причинам (воспаление, наследственная предрасположенность в виде врожденной узости канала лицевого нерва).
К провоцирующим факторам невропатии ЛН относятся переохлаждение, инфекции, сдавление нерва опухолью (невринома), травматизация костей основания черепа/лица с механическим повреждением/разрывом нервных волокон, отравления. Также невропатия может развиваться как осложнение отита, паротита, мезотимпанита, нейротропной вирусной инфекции (полиомиелита, герпеса), воспалительных процессов в головном мозге.
Симптомы
Симптомы неврита лицевого нерва определяются уровнем его поражения. Рассмотрим лишь симптоматику компрессионно-ишемического поражения ЛН (паралич Белла). Наиболее часто компрессионно-ишемическая невропатия проявляется остро развившимся парезом/параличом мимической мускулатуры в виде:
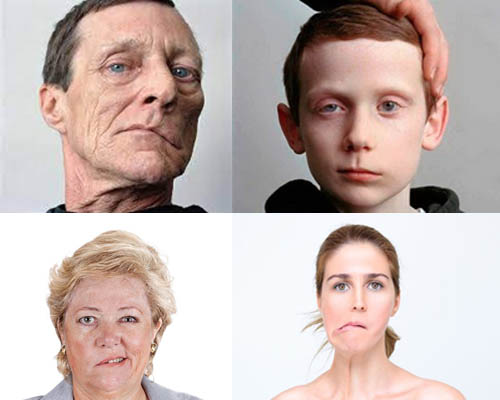
Паралич лицевого нерва начинается преимущественно внезапно. В начале заболевания у некоторых пациентов за 1-2 дня до появления двигательных расстройств или одновременно появляются умеренные/легкие боли и парестезии в области сосцевидного отростка/уха.
Анализы и диагностика
Диагноз устанавливается на основании клинической симптоматики и жалоб пациента. С целью исключения вторичной природы заболевания назначаются дополнительные инструментальные обследования (МРТ/КТ головного мозга). Для уточнения локализации поражения ЛН, степени его поражения могут назначаться электромиография и электронейрография.
Лечение неврита лицевого нерва
Вылечить парез лицевого нерва можно лишь используя комплексное лечение, включающее медикаментозную терапию, массаж, физиопроцедуры, ЛФК и специальные упражнения. Лечебные мероприятия направлены на улучшение крово/лимфообращения в области лица, нормализацию проводимости лицевого нерва, предупреждение появления мышечной контрактуры и восстановление функции мимических мышц. Лечение, в зависимости от тяжести заболевания может проводится амбулаторно или стационарно в неврологическом отделении.
Основным принципом медикаментозного лечения невропатии является снятие отека и скорейшее восстановление микроциркуляции. В остром периоде заболевания достаточно высокую эффективность имеют системные глюкокортикостероиды препараты. С этой целью проводится пульс-терапия: Метипред внутривенно капельно в течение 3 дней и далее назначается ГКС перорально в течение 5 дней, а затем доза постепенно снижает ежедневно на 5 мг. Или же назначается Преднизолон в течении 7 дней по 60-80 м/сутки с постепенной отменой за 5-6 суток. Некоторые авторы считают, что при параличе Белла более целесообразным является периневральное введение гормонов (Гидрокортизон с новокаином), что способствует более быстрой декомпрессии лицевого нерва. Параллельно назначаются диуретики — Фуросемид, Диакарб, Триамтерен.
Для снижения болевого синдрома и противовоспалительной терапии назначаются НПВС – Ксефокам, Диклофенак, Ибупрофен, Кеторолак, Зорника. Эффективны сосудорасширяющие препараты (Скополамин, Никотиновая кислота, Ксантинола никотинат). Показано назначение витаминов группы В, которые оказывают нейротропное действие, улучшают регенерацию и трофические процессы в нервной ткани, уменьшают боль (Нейромультивит, Мильгамма, Нейробион и др.).
Назначаются препараты альфа-липоевой кислоты (Тиоктацид, Берлитион, Тиогамма), способствующие восстановлению структуры нерва и купированию процессов демиелинизации.
Вне острого периода (на 7-10 сутки) для нормализации проводимости лицевого нерва проводится стимулирующая терапия — назначаются антихолинэстеразные препараты (Галантамин, Нейромидин, Ипидакрин, Аксамон). Лицевой неврит с затяжным течением требует назначения антидепрессантов — Имипрамин, Амитриптилин, Дулоксетин, Венлафаксин. В качестве дополнительного средства рекомендуется назначение оксидантов — Тиоктацид, Берлитион. Для местного обезболивания можно использовать Анестезиновую/Лидокаиновую мазь, которая наносится на болевые зоны. Если на протяжении первых 2-3- месяцев восстановление лицевого нерва в полном объеме не произошло, назначают Лидазу и препараты-биостимуляторы (ФИБС, Алоэ). При развитии контрактур показаны Мидокалм, Тегретол.
Диагноз тригеминальная невралгия означает хронические боли в области лица, имеющие приступообразный характер. Причиной, по которой воспалилися тройничный нерв, могут стать как поражения самого нерва, так и вторичные факторы: стоматологические воспалительные заболевания, синуситы, опухоли мягких тканей или костей.

Воспаленный тройничный нерв лечат соответствующее, комплекс включает прием противосудорожных, противовоспалительных или обезболивающих препаратов, проведение блокад, хирургические операции.
Анатомия и функции
Что такое и где находится тройничный нерв у человека? Речь идет о самой крупной, пятой из 12 пар черепных нервов. Каждый из них, правый и левый, отходит от ствола у основания мозга (в зоне варолиева моста) и иннервирует соответствующую половину лица. На верхушке пирамиды височной кости имеется утолщение – тройничный или Гассеров узел, где происходит разделение на три ветви:
- глазничную – проходит в области лба, спинки носа и верхнего века;
- верхнечелюстную – локализуется в зоне крыльев носа, верхней челюсти, щеки и нижнего века, иннервирует также верхнюю губу;
- нижнечелюстную – отвечает за иннервацию тканей нижней челюсти.
Тройничный или лицевой нерв является смешанным, то есть обеспечивает чувствительность лица, глазных яблок и ротовой полости, а также двигательную активность жевательных мышц.
Причины и виды невралгии
Бывает центральная и периферическая тригеминальная невралгия. В первом случае поражается Гассеров ганглий с его нервными волокнами, почему болит одна из сторон лица. Заболевание диагностируется преимущественно у лиц в возрасте от 40 до 60 лет. Патология данного типа является следствием различных нарушений кровообращения, перенесенных воспалений и травм ЦНС, инфекций, интоксикаций. Причиной может стать также климакс, ревматизм.

Периферической называется невралгия, при которой повреждаются уже ветви нерва. Среди провоцирующих факторов выделяют преимущественно стоматологические заболевания воспалительного характера (пульпит, периодонтит), некачественно выполненное протезирование и лечение зубов. Часто боли возникают из-за опухолей, развивающихся в костях лицевого черепа или мышцах, слизистой, вируса герпеса, хронических инфекционно-воспалительных процессов в придаточных пазухах (гайморовых верхнечелюстного отдела), ротоглотке, носовой или ротовой полостях.
Существует также подразделение патологии на идиопатическую и симптоматическую. Идиопатическая или первичная тригеминальная невралгия – результат сдавливания корешка кровеносным сосудом в месте выхода из ствола мозга. Компрессия является причиной болезни в большинстве случаев, но достоверно ее выявить можно только в ходе нейрохирургической операции. Поэтому диагноз ставится по умолчанию, если не обнаружено признаков вторичного или симптоматического нарушения.
Невралгия также классифицируется согласно локализации поражения относительно ветвей тройничного нерва. Выделяют достаточно редкие назолициарную и супраорбитальную невралгии, а также более распространенные инфраорбитальную, щечную, язычную и другие. Чаще всего поражаются 2-я и 3-я ветви, патология первой встречается гораздо реже. Отдельно диагностируется постгерпетический тип заболевания, развивающийся вследствие поражения нервных волокон герпесвирусом Herpes zoster.
Симптомы
Вне зависимости от типа лицевой невралгии, имеются общие, характерные для всех разновидностей симптомы поражения тройничного нерва. К ним относятся:
- неизменная локализация боли на протяжении многих лет;
- продолжительность приступов не более 2 минут, в среднем – 10-15 секунд;
- наличие промежутков между ними (рефрактерный период);
- жесткий, стреляющий характер боли, напоминающей электрический разряд;
- поведение во время приступа – неподвижность, отсутствие криков или плача с одновременным подергиванием мимических или жевательных мускулов;
- наличие зон, называемых триггерными, раздражение которых провоцирует боль (определенные участки ротовой полости или лица);
- триггерные факторы, вызывающие приступ, – разговор, жевание или умывание.
Неврит лицевого нерва — наиболее часто вызывается разнообразными инфекционными агентами на фоне охлаждения, гипертонической болезни, травм, атеросклероза мозговых сосудов и др. В случае нарушения кровообращения в позвоночной артерии наблюдается изолированное поражение лицевого нерва. Неврит может быть осложнением таких заболеваний, как отит, паротит, патологические процессы основания мозга, в частности наличие очага воспаления. Существует возможность внезапного развития паралича лицевого нерва при анестезии нижнего альвеолярного нерва.
КЛИНИЧЕСКАЯ КАРТИНА
Обычно неврит лицевого нерва возникает остро с появления паралича или пареза мимических мышц. Чаще поражается лишь одна сторона, только в 2 % случаев заболевания отмечается двусторонняя симптоматика. Первоначально возможно появление слабой болезненности и парестезии в области сосцевидного отростка и ушной раковины. Они предшествуют развитию двигательных расстройств на 1–2 дня, либо возникают одновременно с ними. Поражение узла коленца лицевого нерва вызывает появление наиболее интенсивных болей. Другие клинические проявления неврита находятся в зависимости от уровня поражения лицевого нерва. Поражение ядра провоцирует возникновение изолированного паралича (пареза) мимических мышц. Сочетание с симптомами поражения преддверно-улиткового нерва говорит о повреждении корешка лицевого нерва в месте выхода из ствола мозга. Встречается поражение нерва внутри пирамиды височной кости до места отхождения большого каменистого нерва. В этом случае к параличу мимических мышц присоединятся ксерофтальмия (сухость глаза), нарушение слюноотделения, вкуса, гиперакузия. В случае поражения лицевого нерва ниже места отхождения большого каменистого нерва, но выше отхождения стремянного нерва вместо ксерофтальмии наблюдается слезотечение. Отсутствие гиперакузии свидетельствует о поражении нерва после отхождения стремянного нерва. Наличие двигательных расстройств наблюдается при повреждении в месте выхода из шилососцевидного отверстия.
СИМПТОМЫ
В случае повреждения двигательных волокон развивается прозоплегия, т.е. паралич мышц лица периферического характера. Для данной патологии характерна асимметрия лица: половина лица на стороне поражения нерва становится неподвижной, маскообразной, лобные и носогубная складки сглажены, глаз на пораженной стороне не закрывается, расширяется глазная щель, угол рта опущен вниз. Характерно наличие феномена Белла–поворот глазного яблока кверху при попытке закрытия глаза на стороне поражения. Наблюдается паралитическое слезотечение, связанное с постоянно происходящим раздражением пылью и другими частицами слизистой оболочки глаза вследствие отсутствия мигания. Раздражение слизистой провоцирует развитие воспалительных процессов в виде конъюнктивита и кератита.
Помимо отсутствия мигания слезотечение провоцирует нарушение оттока слезной жидкости по слезному каналу, что связано с параличом круговой мышцы глаза и недостаточным прилеганием к глазному яблоку нижнего века.
Уровень поражения лицевого нерва определяет клиническую картину. Изолированный паралич мимической мускулатуры лица характерен для повреждения двигательного ядра лицевого нерва. В случае присоединения поражения корешковых волокон к клинической симптоматике добавляется синдром Мийяра-Гюблера (центральный паралич конечностей на стороне, противоположной поражению).
При поражении лицевого нерва в мостомозжечковом углу помимо паралича мимической мускулатуры наблюдается снижение слуха или глухота, отсутствие корнеального рефлекса, что свидетельствует об одновременном поражении слухового и тройничного нервов. Данная патология имеет место при воспалении области мостомозжечкового угла (арахноидит), невриноме слухового нерва. Присоединение гиперакузии и нарушение вкуса говорит о повреждении нерва до отхождения от него большого каменистого нерва в лицевом канале пирамиды височной кости.
ЛЕЧЕНИЕ
Лечение должно производиться исключительно врачом-неврологом. Самолечение недопустимо. Первоначально необходимо выяснить причину возникновения заболевания и устранить ее при помощи проведения комплекса лечебных мероприятий, оказывающих влияние не только на сам этиологический фактор, но и на все звенья патогенеза болезни. Необходимо назначение противовоспалительных препаратов, спазмолитиков, вазодилататоров. В случае выраженного болевого синдрома применяются анальгетики. В качестве дополнительных методов лечения используются физиотерапевтические методики, такие, как УВЧ-терапия, ультразвук с гидрокортизоном пораженной половины лица и сосцевидного отростка, грязевые маски на обе половины лица.
Тригеминальная невралгия (ТН) (синонимы: tic douloureux, или болезнь Фотергилла) является одной из самых распространенных лицевых болей (прозопалгий) и относится к числу наиболее устойчивых болевых синдромов в клинической неврологии [1].
Тригеминальная невралгия (ТН) (синонимы: tic douloureux, или болезнь Фотергилла) является одной из самых распространенных лицевых болей (прозопалгий) и относится к числу наиболее устойчивых болевых синдромов в клинической неврологии [1]. ТН является типичным примером нейропатической боли (НБ) пароксизмального характера и считается самым мучительным видом прозопалгии. ТН чаще всего имеет хроническое или рецидивирующее течение, сопровождается большим количеством коморбидных расстройств, гораздо труднее поддается лечению, чем многие другие типы хронической боли и приводит к временной или постоянной нетрудоспособности, что делает ее большой экономической и социальной проблемой [2]. Хроническая НБ оказывает значительное отрицательное воздействие на качество жизни пациентов, вызывая нарушения сна, усиление тревоги, депрессии, снижение повседневной активности [3]. Высокая интенсивность и стойкость ТН, ее особый, часто мучительный характер, резистентность к традиционным методам обезболивания придают этой проблеме исключительную актуальность. Тригеминальная невралгия — заболевание, характеризующееся возникновением приступообразной, обычно односторонней, кратковременной, острой, резкой, интенсивной, напоминающей удар электрическим током, боли в области иннервации одной или нескольких ветвей тройничного нерва [4, 5]. Чаще всего поражение возникает в зоне II и/или III ветви и крайне редко — I ветви n. trigeminus [6].
По данным ВОЗ распространенность ТН составляет до 30–50 больных на 100 000 населения, а заболеваемость — 2–4 человека на 100 000 населения. ТН чаще встречается у женщин, чем у мужчин, дебютирует на пятом десятилетии жизни и в 60% случаев имеет правостороннюю локализацию [7, 8].
Согласно Международной классификации головных болей (2-е издание), предложенной Международным обществом головной боли (2003), ТН подразделяется на классическую, вызванную компрессией тригеминального корешка извилистыми или патологически измененными сосудами, без признаков явного неврологического дефицита, и симптоматическую, вызванную доказанным структурным повреждением тройничного нерва, отличным от сосудистой компрессии [9].
На экстракраниальном уровне основными факторами, приводящими к возникновению ТН, являются: туннельный синдром — компрессия в костном канале, по которому проходит нерв (чаще в подглазничном отверстии и нижней челюсти), связанная с его врожденной узостью, присоединением сосудистых заболеваний в пожилом возрасте, а также в результате хронического воспалительного процесса в смежных зонах (кариес, синуситы); местный одонтогенный или риногенный воспалительные процессы. Развитие ТН может провоцироваться инфекционными процессами, нейроэндокринными и аллергическими заболеваниями, демиелинизацией корешка тройничного нерва при рассеянном склерозе [7, 12].
В зависимости от воздействия патологического процесса на соответствующий отдел тригеминальной системы выделяют ТН преимущественно центрального и периферического генеза. В возникновении ТН центрального генеза большую роль играют нейроэндокринные, иммунологические и сосудистые факторы, которые приводят к нарушению реактивности корково-подкорковых структур и формированию очага патологической активности в ЦНС. В патогенезе ТН периферического уровня большую роль играют компрессионный фактор, инфекции, травмы, аллергические реакции, одонтогенные процессы [7, 8, 12].
Несмотря на появившееся в последние годы большое количество обзоров литературы и метаанализов, посвященных проблеме лечения НБ [13], к которой относится и ТН, среди исследователей не существует единого мнения относительно основных принципов медикаментозной терапии этого заболевания [14]. Лечение нейропатической боли все еще остается недостаточно эффективным: менее чем у половины пациентов отмечается значительное улучшение в результате проведенного фармакологического лечения [15, 16].
Проблема терапии тригеминальной невралгии на сегодняшний день остается не до конца решенной, что связано с неоднородностью данного заболевания в отношении этиологии, патогенетических механизмов и симптоматики, а также с малой эффективностью обычных анальгетических средств и развитием фармакорезистентных форм ТН, требующих проведения хирургического лечения. В современных условиях лечебная тактика при данном заболевании включает в себя медикаментозные и хирургические методы.
Основными направлениями медикаментозной терапии являются: устранение причины ТН, если она известна (лечение больных зубов, воспалительных процессов смежных зон и др.), и проведение симптоматического лечения (купирование болевого синдрома).
Патогенетическое лечение больных с ТН включает применение препаратов нейрометаболического, нейротрофического, антиоксидантного, антигипоксантного действия. В последние годы обнаружена высокая эффективность использования метаболических препаратов в комплексном лечении НБ [8, 17]. При лечении пациентов с ТН показана высокая эффективность препарата метаболического действия Актовегина — депротеинизированного деривата из крови молодых телят. Основное действие этого препарата заключается в стабилизации энергетического потенциала клеток за счет повышения внутриклеточного транспорта и утилизации глюкозы и кислорода. Актовегин обладает также антигипоксическим эффектом, являясь непрямым антиоксидантом. Кроме того, действие Актовегина проявляется непрямым вазоактивным и реологическим эффектами за счет повышения капиллярного кровотока, снижения периферического сосудистого сопротивления и улучшения перфузии органов и тканей [17]. Такой широкий спектр фармакологического действия Актовегина позволяет использовать его в терапии ТН. В период приступа целесообразно применение Актовегина внутривенно медленно струйно или капельно в течение 10 дней в дозе 400–600 мг/сутки. В межприступном периоде препарат назначается внутрь в дозе 200 мг 3 раза в сутки на протяжении 1–3 месяцев [8]. К патогенетическому лечению больных с ТН можно отнести применение высоких доз витаминов группы B в составе поликомпонентных препаратов, что обусловлено их полимодальным нейротропным действием (влиянием на обмен веществ, метаболизм медиаторов, передачу возбуждения в нервной системе), а также способностью существенно улучшать регенерацию нервов. Кроме того, витамины группы B обладают анальгезирующей активностью. К таким препаратам, в частности, относятся Мильгамма, Нейромультивит, Нейробион, содержащие сбалансированную комбинацию тиамина (B1), пиридоксина (B6), цианокобаламина (B12). Витамин B1 устраняет ацидоз, снижающий порог болевой чувствительности; активирует ионные каналы в мембранах нейронов, улучшает эндоневральный кровоток, повышает энергообеспечение нейронов и поддерживает аксоплазматический транспорт белков. Эти эффекты тиамина способствуют регенерации нервных волокон [18–20]. Витамин B6, активируя синтез миелиновой оболочки нервного волокна и транспортных белков в аксонах, ускоряет процесс регенерации периферических нервов, проявляя тем самым нейротропный эффект. Восстановление синтеза ряда медиаторов (серотонина, норадреналина, дофамина, гамма-аминомасляной кислоты (ГАМК) и активация нисходящих тормозных серотонинергических путей, входящих в антиноцицептивную систему, приводит к снижению болевой чувствительности (антиноцицептивное действие пиридоксина) [18, 21]. Витамин B12 участвует в процессах регенерации нервной ткани, активируя синтез липопротеинов, необходимых для построения клеточных мембран и миелиновой оболочки; уменьшает высвобождение возбуждающих нейротрансмиттеров (глутамата); обладает противоанемическим, гемопоэтическим и метаболическим эффектом [18, 22]. Для быстрого купирования боли и патогенетического нейротропного воздействия при ТН целесообразно использование парентеральной формы препарата Нейробион — комбинированного препарата витаминов группы B, содержащего оптимальное количество витамина B12 как в ампулированной, так и в таблетированной форме. Нейробион применяется в дозе 3 мл в сутки внутримышечно 2–3 раза в неделю — 10 инъекций (при выраженном болевом синдроме можно применять ежедневно в той же дозировке в течение 10–15 дней). Затем для усиления, пролонгирования терапевтического эффекта и профилактики рецидива заболевания назначается Нейробион в таблетированной форме в дозировке по 1 таблетке внутрь 3 раза в день в течение 1–2 месяцев [8].
Также препаратами выбора для лечения ТН являются антиконвульсанты, а карбамазепин стал одним из первых препаратов, официально зарегистрированных для лечения этого состояния [24].
В начале 90-х годов прошлого столетия появилась новая генерация противоэпилептических препаратов, и теперь антиконвульсанты обычно делят на препараты первого и второго поколения.
К антиконвульсантам первого поколения относятся фенитоин, фенобарбитал, примидон, этосуксимид, карбамазепин, вальпроевая кислота, диазепам, лоразепам, клоназепам. Препараты первого поколения практически не рассматриваются в качестве первой линии терапии НБ (за исключением карбамазепина при ТН) из-за недостаточного уровня обезболивающего эффекта и высокого риска возникновения нежелательных реакций. К наиболее частым побочным эффектам антиконвульсантов первого поколения относятся: реакции со стороны ЦНС (сонливость, головокружение, атаксия, седативный эффект или повышенная возбудимость, диплопия, дизартрия, когнитивные расстройства, ухудшение памяти и настроения), гематологические нарушения (агранулоцитоз, апластическая анемия, тромбоцитопения, лейкопения), гепатотоксичность, снижение минеральной плотности кости, кожные высыпания, гиперплазия десен, симптомы со стороны желудочно-кишечного тракта (рвота, анорексия). К антиконвульсантам второго поколения относятся прегабалин (Лирика), габапентин (Нейронтин, Габагамма, Тебантин), ламотриджин (Ламиктал), окскарбазепин (Трилептал), топирамат (Топамакс), леветирацетам (Кеппра), тиагабин (Габитрил), зонисамид (Зонегран), вигабатрин (Сабрил), фелбамат (Талокса). Эти препараты имеют более благоприятные фармакокинетические характеристики и профили безопасности, а также низкий риск лекарственных взаимодействий по сравнению с антиконвульсантами первого поколения [24, 25].
Основные механизмы действия антиконвульсантов 1-го и 2-го поколения представлены в таблице [26].
Первым антиконвульсантом, успешно используемым для лечения ТН, был фенитоин (Дифенин) [27]. Дифенин, производное гидантоина, близкого по химической структуре к барбитуровой кислоте, противопоказан при тяжелых заболеваниях почек, печени, сердечной недостаточности.
Согласно рекомендациям Европейской федерации неврологических сообществ (2009) фармакотерапия ТН основана, прежде всего, на использовании предложенного С. Блюмом в 1962 году карбамазепина (Финлепсина, Тегретола) (200–1200 мг/сутки), который является препаратом первого выбора (уровень доказательности A) [27, 28]. Противоболевое действие этого препарата обусловлено, главным образом, его способностью уменьшать проницаемость для натрия мембран нейронов, участвующих в ноцицептивных реакциях. Обычно назначается следующая схема лечения карбамазепином. В первые два дня суточная доза составляет 200 мг (по 1/2 таблетки утром и вечером), затем в течение двух дней суточная доза увеличивается до 400 мг (утром и вечером), а после этого — до 600 мг (по 1 таблетке утром, в обед и вечером). Если эффект недостаточный, то общее количество препарата в сутки может быть доведено до 800–1000 мг. У части больных ТН (около 15% в популяции) карбамазепин не оказывает анальгезирующего воздействия, поэтому в таких случаях применяется другой антиконвульсант — фенитоин.
Проведенные около 40 лет назад три плацебо-контролируемые исследования, которые включали в себя в общей сложности 150 пациентов с ТН, показали эффективность карбамазепина в отношении как частоты, так и интенсивности пароксизмов [24]. Рядом авторов было показано, что карбамазепин может уменьшить болевую симптоматику приблизительно в 70% случаев. [29]. Однако применение карбамазепина ограничено фармакокинетическими факторами и возникающими в ряде случаев тяжелыми побочными эффектами (например, синдром Стивенса–Джонсона), особенно у пожилых пациентов.
Окскарбазепин (Трилептал) имеет структурное сходство с карбамазепином, но гораздо лучше переносится пациентами и имеет гораздо меньше побочных эффектов. Обычно окскарбазепин используется в начале лечения ТН в дозе 600–1800 мг/сутки (уровень доказательности B) [30].
В качестве дополнительной терапии ТН показана эффективность ламотриджина (Ламиктала) в дозе 400 мг/сутки [31] и баклофена в дозе 40–80 мг/сутки [32], которые относятся к препаратам второй линии (уровень доказательности C). Малые открытые исследования (класс IV) свидетельствуют об эффективности применения клоназепама, вальпроата, фенитоина [33, 34]. Указанная терапия наиболее эффективна при классической форме ТН. При ТН периферического генеза в схемы лечения предпочтительно включать ненаркотические анальгетики, а в случае развития хронического болевого синдрома (более трех месяцев) показано назначение антидепрессантов (амитриптилин) [7, 12].
Габапентин (Нейронтин) — первый в мире препарат, который был зарегистрирован для лечения всех видов нейропатической боли. Во многих исследованиях была показана эффективность габапентина у больных с ТН, не отвечающих на лечение другими средствами (карбамазепин, фенитоин, вальпроаты, амитриптилин); при этом в большинстве случаев наблюдалось полное купирование болевого синдрома [35]. Терапевтическая доза составляет от 1800 до 3600 мг/сутки. Препарат принимают 3 раза в сутки по следующей схеме: 1-я неделя — 900 мг/сутки, 2-я неделя — 1800 мг/сутки, 3-я неделя — 2400 мг/сутки, 4-я неделя — 3600 мг/сутки.
Недавно были опубликованы результаты открытого проспективного 12-месячного исследования 53 пациентов с ТН, в котором оценивалась эффективность прегабалина (Лирики) в дозе 150–600 мг/сутки. Лечение прегабалином привело к обезболиванию или, по крайней мере, к 50%-му снижению интенсивности боли у 25% и 49% пациентов соответственно [36]. В другом мультицентровом проспективном 12-недельном исследовании 65 больных, резистентных к предшествующей анальгетической терапии, лечение прегабалином в средней дозе 196 мг/сутки (в подгруппе монотерапии) и 234 мг/день (в подгруппе политерапии) приводило к уменьшению интенсивности боли ≥ 50% в среднем у 60% больных, а также уменьшало степень выраженности тревоги, депрессии и нарушений сна [37]. При лечении ТН начальная доза прегабалина может составлять 150 мг/сутки в 2 приема. В зависимости от эффекта и переносимости дозу можно увеличить до 300 мг/сутки через 3–7 дней. При необходимости можно увеличить дозу до максимальной (600 мг/сутки) через 7-дневный интервал.
Впервые об использовании леветирацетама (Кеппра) при лечении ТН сообщили в 2004 году K. R. Edwards et al. [38]. Механизм действия леветирацетама неизвестен; имеются данные, полученные в экспериментах на животных, что он является селективным блокатором N-типа кальциевых каналов [39]. Свойства этого препарата особенно подходят для лечения пациентов с ТН с тяжелой болью, нуждающихся в быстром ответе на терапию. Фармакокинетика леветирацетама линейна и предсказуема; концентрация в плазме крови увеличивается пропорционально дозе в пределах клинически обоснованного диапазона от 500 до 5000 мг [40]. В отличие от других антиконвульсантов, особенно карбамазепина, в метаболизм леветирацетама не вовлечена система печеночного цитохрома Р450 и препарат экскретируется через почки [41]. Кроме того, данный препарат характеризуется благоприятным терапевтическим индексом и имеет незначительное число неблагоприятных побочных эффектов (что является основной проблемой при использовании препаратов для лечения ТН) [42]. Побочными эффектами леветирацетама, о которых обычно сообщают, являются: астения, головокружение, сонливость, головная боль и депрессия. В 10-недельном проспективном открытом исследовании показано, что для лечения ТН по сравнению с терапией эпилепсии были необходимы более высокие дозы леветирацетама, составляющих 3000–5000 мг/день (50–60 мг/кг/день), которые, тем не менее, не вызвали значительных побочных эффектов. Это обстоятельство свидетельствует о перспективе использования этого лекарственного средства для лечения ТН [43].
В одном отечественном исследовании отмечены положительные результаты при комбинации карбамазепина и габапентина [44].
С 1970-х годов прошлого столетия для лечения ТН стали использовать антидепрессанты [45]. В настоящее время доказана эффективность использования трициклических антидепрессантов (ТЦА) при лечении ТН [46].
Пациентам, длительно страдающим от непереносимой боли, и при неэффективности консервативной терапии в случае классической ТН рекомендуется хирургическое лечение. В настоящее время используются следующие подходы:
1) хирургическая микроваскулярная декомпрессия [48];
2) стереотаксическая лучевая терапия, гамма-нож [49];
3) чрескожная баллонная микрокомпрессия [50];
4) чрескожный глицериновый ризолизис [51];
5) чрескожное радиочастотное лечение Гассерова узла [52].
Наиболее эффективным методом хирургического лечения ТН является метод P. Janetta, заключающийся в размещении специальной прокладки между тройничным нервом и раздражающим сосудом; в отдаленном периоде эффективность лечения составляет 80% [53–55].
В заключение заметим, что лечение ТН должно носить мультидисциплинарный характер, при этом c пациентом должны быть обсуждены выбор различных методов лечения и риски возможных осложнений.
Литература
*Первый МГМУ им. И. М. Сеченова, **МОНИКИ им. М. Ф. Владимирского, Москва
Читайте также:


