Угнетение нервно мышечной передачи
Описание
Передача возбуждения с соматических нервов на скелетную мускулатуру осуществляется с помощью ацетилхолина. Он выделяется пресинаптической мембраной и связывается н-холинорецепторами; активация последних инициирует комплекс изменений, приводящий к сокращению мышцы. Усиление сократительной деятельности можно получить агонистами ацетилхолина или препаратами, вызывающими накопление медиатора в синаптической щели — антихолинэстеразными средствами (см. Холиномиметические средства).
Противоположное действие оказывают миорелаксанты (см. н-Холинолитики (миорелаксанты)). В группу миорелаксантов объединяют лекарственные средства, расслабляющие скелетную мускулатуру.
Кураре и курареподобные препараты применяют в медицине для расслабления скелетной мускулатуры, главным образом, при хирургических операциях. Действие этих препаратов связано с экранирующим влиянием на н-холинорецепторы постсинаптической мембраны поперечно-полосатых мышц.
Кураре представляет собой смесь сгущенных экстрактов из южноамериканских растений видов Strychnos (S. toxifera и др.) и Chondodendron (Ch. Tomentosum, Ch. Platyphyllum и др.); он с давних пор использовался аборигенами в качестве яда для стрел (вызывает обездвиживание или смерть животного в результате асфиксии, обусловленной прекращением сокращений дыхательной мускулатуры). Еще в прошлом столетии было установлено, что вызываемое при помощи кураре обездвиживание зависит от прекращения передачи возбуждения с двигательных нервов на мышцы (Клод Бернар, Е.В. Пеликан).
Оказалось, что сходными свойствами обладают синтетические курареподобные соединения, некоторые алкалоиды и их производные.
Антидеполяризующие или недеполяризующие миорелаксанты (пахикураре) парализуют нервно-мышечную передачу, уменьшая чувствительность н-холинорецепторов синаптической области к ацетилхолину, исключая возможность деполяризации концевой пластинки и возбуждения мышечного волокна. К ним относятся d-тубокурарин, диплацина дихлорид, пипекурония бромид, атракурия безилат и др. Соединения этой группы являются истинными курареподобными веществами. Их антагонисты — антихолинэстеразные вещества: ингибирование холинэстеразы приводит к накоплению в области синапсов ацетилхолина, который при повышенной концентрации вытесняет курареподобные вещества с н-холинорецепторов и восстанавливает нервно-мышечную проводимость.
Деполяризаторы (лептокураре) расслабляют мускулатуру, вызывая, напротив, стойкую деполяризацию концевой пластинки, делая ее (подобно избыточным количествам ацетилхолина) невосприимчивой к новым импульсам и в конечном итоге также нарушая проведение возбуждения с нерва на мышцу. Препараты этой группы относительно быстро гидролизуются холинэстеразой и при однократном введении дают кратковременный эффект; разумеется, антихолинэстеразные средства усиливают их действие. Основным представителем этой группы является суксаметония йодид.
Отдельные миорелаксанты могут оказывать смешанное действие — антидеполяризующее и деполяризующее.
Ряд препаратов расслабляет соматическую мускулатуру по центральным механизмам. Миорелаксацию могут вызывать анксиолитики (см. Анксиолитики). В последние годы найдены соединения (толперизон, баклофен, тизанидин и др.), миорелаксантный эффект которых связан со специфическим влиянием на ретикулярную формацию мозга, спинальные моно- и полисинаптические рефлексы. Они устраняют повышенный тонус произвольных мышц без существенного нарушения двигательных функций. Их используют при спастических состояниях, поясничном радикулите, ревматических и других заболеваниях, сопровождающихся спазмом скелетных мышц. В механизме действия этих препаратов важную роль играет модуляция ГАМКергических процессов мозга.
Нервно-мышечные соединения являются одним из самых уязвимых структур периферического нейромоторного аппарата. Синаптический аппарат мышцы служит местом приложения всех миорелаксантов, применяемых в анестезиологической практике.
Поражение нервно-мышечной передачи служит причиной тяжелых мышечных расстройств при воздействии ядов различных насекомых и змей, интоксикации различными медикаментами, в частности антибиотиками.
Блокада выделения передатчика возбуждения с нерва на мышцу является причиной тяжелых двигательных нарушений при ботулинической интоксикации, некоторых формах карциноматозных нейромиопатий. Патология синаптического аппарата мышц является причиной развития тяжелого нервно-мышечного страдания — миастении.
В течение последних лет изучению физиологии и патофизиологии нервно-мышечной передачи посвящено огромное количество исследований.
Подробно изучены механизмы образования, хранения, выделения передатчика возбуждения — ацетилхолина (АХ). Тончайшими исследованиями установлена природа рецептора ацетилхолина (холинорецептора) постсинаптической мембраны мышц. Уделено большое внимание изучению механизмов патологии нервно-мышечной передачи при различных заболеваниях человека.
Велико также число исследований, посвященных изучению клинической картины нервно-мышечных заболеваний, связанных с нарушениями функционирования нервно-мышечной передачи. Результаты этих исследований приводятся в соответствующих разделах данной главы. Здесь же нам хотелось подчеркнуть, что ни в одной области клинической неврологии внедрение электрофизиологических методов не принесло столь очевидного успеха, как в изучении синаптических болезней мышц.
Благодаря разработке и широкому внедрению новых методов изучения нервно-мышечной передачи удалось выделить, а затем и клинически дифференцировать различные формы заболеваний, ранее относимых к миастении. В настоящее время клиническая диагностика миастении и ряда миастенических синдромов стала рутинным делом, не требующим особой квалификации. Вместе с тем до настоящего времени остается неясным вопрос о нозологическом единстве различных клинических форм миастении.
Есть основание полагать, что миастения — не единая клиническая форма, а группа заболеваний с различным патогенезом. Кроме того, продолжает выделяться все большее число миастенических синдромов, обусловленных нарушениями нервно-мышечной передачи, отягощающих или сопровождающих поражения других уровней нейромоторного аппарата, а иногда сочетающихся с поражениями мозжечковых и пирамидных систем.
Интерес к проблеме синаптических болезней обусловлен и другим обстоятельством: значительная роль в механизме их формирования принадлежит механизму нарушения иммунитета — аутоиммунным и иммуно-аллергическим расстройствам.
Это делает миастению и ряд миастенических синдромов удобной моделью для изучения иммунодефицитных состояний у человека. Кроме того, изучение этого механизма миастении открывает новые успешные пути терапии миастенической болезни и миастенических синдромов с помощью кортикостероидных препаратов и иммунодепрессантов.

Особой формой миастенических расстройств, обусловленных поражением терминальных ветвлений двигательных нервов и грубыми расстройствами нервно-мышечной передачи, является описанная нами в 1979 г. терминальная полиневропатия с миастеническим синдромом. К настоящему времени мы наблюдаем в течение 12 лет 13 больных с этим симптомокомплексом (12 мужчин и 1 женщина). У 2 больных заболевание началось в возрасте старше 30 лет,…
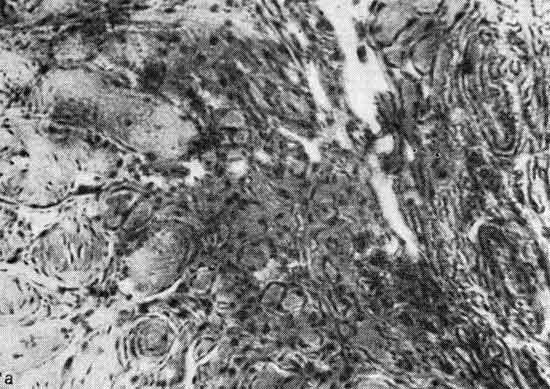
Прежде всего при данном заболевании наблюдаются типичные ЭМГ-ские изменения, свидетельствующие о грубых изменениях нервно-мышечной передачи, снижение амплитуды вызванного ПД мышцы, грубый блок нервно-мышечной передачи при стимуляции редкими частотами (1 и 3 имп/с) и тетанизации мышцы (частотой 50 имп/с). Во всех случаях отмечено изменение резидуальной латенции, свидетельствующее о замедлении скорости проведения возбуждения по самым дистальным претерминальным…

Патологическая утомляемость мышц является нередким симптомом всех форм полимиозита, однако у ряда больных наблюдали сочетание выраженных мышечных расстройств полимиозитического характера с несомненными клиническими и электрофизиологическими признаками, свидетельствующими о вовлечении в процесс синаптических структур, по характеру близкому патологическому процессу, наблюдаемому при миастении. Уже в конце XIX века Е. Wagner (1863, 1887) описал сочетание клиники полимиозита и…
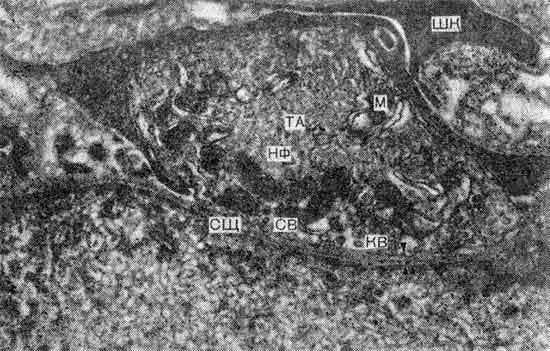
Частично результаты обследования больных данной группы опубликованы в 1974 г. К настоящему времени под нашим наблюдением находятся 12 больных с этим клиническим синдромом. Все больные — девочки. Начало заболевания отмечается в возрасте от 10 до 15 лет. При обследовании больных обращают на себя внимание выраженная мышечная гипотония, снижение, а иногда и выпадение сухожильных рефлексов. Лишь…

В связи с неоднородностью механизмов развития нарушений нервно-мышечной передачи единого лечения миастенических синдромов нет. Воздействия на состояние нервно-мышечной передачи. При большинстве форм миастенических синдромов в определенной степени оказываются эффективными антихолинэстеразные препараты — прозерин, оксазил, калимин и их аналоги (смотрите Лечение миастении). Принципиально иной механизм действия другого препарата — гуанидина хлорида, способствующего выделению ацетилхолина из терминалей…

При обсуждении миастенического синдрома типа Ламберта — Итона следует отметить условность его названия, так как тщательное изучение клиники и механизмов развития данного заболевания позволило считать его неоднородным клиническим синдромом, обусловленным не только, как это предполагалось ранее, специфическим влиянием ракового процесса на нервно-мышечную передачу, но и типом реагирования нервно-мышечного синапса на целый ряд вредностей. Первыми миастенический…

Парестезии рук и ног наблюдаются у 50% больных. Все мужчины с синдромом Ламберта — Итона страдали импотенцией. Иллюстрациями к клинике миастенического синдрома Ламберта — Итона, связанного с бронхогенной мелкоклеточной карциномой, служат следующие наблюдения. Больной С., 43 лет, поступил в октябре 1975 г. с жалобами на слабость и утомляемость в мышцах ног и рук, мышцах туловища,…
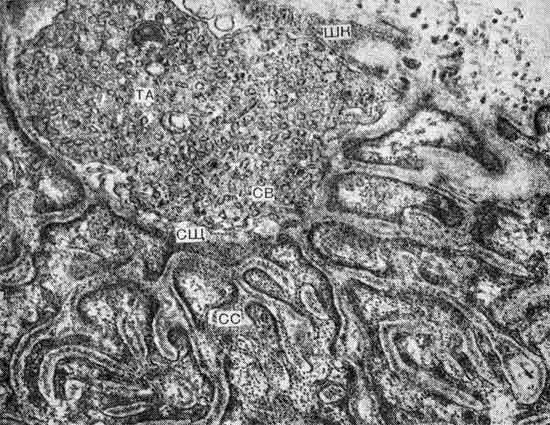
При анализе патогенеза данного клинического синдрома обращает внимание относительная ясность механизмов, обусловливающих двигательные расстройства на синаптическом уровне, и полное отсутствие представления о причинах формирования синаптического дефекта. Существенное место в раскрытии механизмов синаптических нарушений принадлежит изложенным выше результатам ЭМГ-ского исследования и результатам изучения ультраструктуры нервно-мышечных соединений. Электрофизиологическое изучение больных с миастеническим синдромом типа Ламберта — Итона…

Потенциалы действия двигательных единиц и спонтанная активность мышечных волокон. Исследование ПД ДЕ с помощью концентрических игольчатых электродов выявляет снижение их длительности и амплитуды и увеличение числа полифазных потенциалов. Аналогичные данные получены и другими исследователями [Oh S., 1972]. Уменьшение длительности ПД ДЕ отмечено также Е. Lambert и D. Elmqvist (1972), W. Brown и R. Johns (1974).…

Патологическая утомляемость миастенического типа нечасто встречается при полиневропатиях, однако подобные наблюдения описаны в литературе. Большинство из них выявлены при ЭМГ-ском обследовании больных, но в ряде случаев патологическая утомляемость выявлялась и при клиническом обследовании (Гехт Б. М., 1964; Смирнов Ю. К., 1969; Ashby D., Bulmer Е., 1950; Simpson J., Lenman J., 1959). Динамический миастенический компонент заболевания…

Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Нарушение нервно-мышечной передачи происходит вследствие дефектов постсинаптических рецепторов (например, при миастении) или пресинаптического высвобождения ацетилхолина (например, ботулизм), а также распада ацетилхолина в синаптической щели (действие лекарственных или нейротоксических препаратов). Типичны флюктуации степени мышечной слабости и утомляемости.
Код по МКБ-10
Болезни, при которых происходит нарушение нервно-мышечной передачи
Синдром Итона-Ламберта развивается при нарушении высвобождения ацетилхолина из пресинаптических нервных окончаний.
Ботулизм - последствие нарушения высвобождения ацетилхолина пресинаптической терминалью из-за необратимого связывания с нею токсина Clostridium botulinum. Среди симптомов выраженная слабость вплоть до нарушений дыхания и признаки увеличения симпатического тонуса из-за блокирования парасимпатической активности: мидриаз, сухость во рту, запор, задержка мочи, тахикардия, чего не бывает при миастении. На ЭМГ умеренное снижение ответа на низкочастотное (2-3 в 1 секунду) раздражение нерва и рост ответа при увеличении частоты раздражения (50 имп/с) или после кратковременной (10 с) мышечной работы.
Лекарства или токсические вещества могут нарушать функцию нервно-мышечного синапса. Холинергические препараты, фосфорорганические инсектициды и большинство нервнопаралитических газов блокируют нервно-мышечную передачу, деполяризуя постсинаптическую мембрану из-за избыточного действия ацетилхолина на ее рецепторы. Результат: миоз, бронхорея, миастеноподобная слабость. Аминогликозиды и полипептидные антибиотики уменьшают пресинаптическое высвобождение ацетилхолина и чувствительность к нему постсинаптической мембраны. На фоне латентной миастении высокие концентрации этих антибиотиков в сыворотке усугубляют нервно-мышечный блок.
Продолжительное лечение пеницилламином может сопровождаться обратимым синдромом, который клинически и по ЭМГ напоминает миастению. Избыток магния (уровень в крови 8-9 мг/дл) чреват развитием выраженной слабости, что также напоминает миастенический синдром. Лечение включает устранение токсического воздействия, интенсивное наблюдение и при необходимости ИВЛ. Для уменьшения избыточной бронхиальной секреции назначают атропин 0,4-0,6 мг внутрь 3 раза/ день. При отравлении фосфорорганическими инсектицидами или нервно-паралитическим газом могут потребоваться более высокие дозы (2-4 мг в/в за 5 мин).
Синдром ригидного человека - это внезапное появление прогрессирующей ригидности мышц туловища и живота, в меньшей степени - конечностей. Других отклонений, в том числе и на ЭМГ, нет. Этот аутоиммунный синдром развивается как паранеопластический (чаще при раке груди, легких, прямой кишки и при болезни Ходжкина). Аутоантитела против нескольких белков, связанных с ГАМК глициновыми синапсами, воздействуют преимущественно на ингибиторные нейроны передних рогов спинного мозга. Лечение симптоматическое. Диазепам существенно уменьшает мышечную ригидность. Результаты плазмафереза противоречивы.
Синдром Исаакса (синонимы: нейромиотония, синдром броненосца) проявляется, главным образом, жалобами на работу конечностей. Появляются миокимии - мышечные фасцикуляции, выглядящие как конгломерат шевелящихся под кожей червей. Другие жалобы: карпопедальные спазмы, интермиттирующие крампи, повышенное потоотделение и псевдомиотония (нарушение расслабления после сильного мышечного сокращения, но без типичного для истинной миотонии нарастания - убывания на ЭМГ). Первоначально поражает периферический нерв, поскольку кураре снимает жалобы, а под общим наркозом симптомы сохраняются. Причина неизвестна. Карбамазепин или фенитоин уменьшают жалобы.
На примере работы нервно-мышечного синапса можно рассматривать функционирование любого химического синапса. Также на этом примере можно рассмотреть механизмы подавления (угнетения) передачи сигнала в химическом синапсе. Так, например, существует несколько способов блокады нервно-мышечной передачи.
1. Блокада проведения возбуждения по нервам. Так действуют местные анестетики (новокаин, лидокаин) (рис. 5.4).

Рис. 5.4. Действие местных анестетиков на передачу сигнала по аксону 1
- 2. Блокада высвобождения медиатора — ботулинический токсин, недостаток кальция или замена его на магний.
- 3. Блокада синтеза медиатора — гемихолиний (угнетает обратный захват холина иресинаптическим окончанием).
- 4. Блокада рецепторов ацетилхолина — необратимое связывание (альфа-бунгаротоксин), обратимое конкурентное связывание — яд кураре (rf-тубокурарин). Ядом кураре пользовались еще индейцы Южной Америки для охоты на животных. Это смесь экстрактов некоторых южноамериканских растений. Кураре, попадая в кровь, вызывает обездвиживание животного, и оно погибает фактически от удушья, но сердце этот [1]
яд не останавливает. Активным соединением, вызывающим эти реакции, является б/-ту6окурарин. При попадании в кровь он блокирует передачу нервных импульсов с двигательных нервов на скелетную мускулатуру, вызывая паралич скелетных мышц.
5. Блокада работы фермента ацетилхолинэстеразы — фосфорорганиче- ские соединения (инсектициды, нервно-паралитические газы).
Исследования показали, что существуют два типа рецепторов ацетилхо- лина — Н (никотиновые) и М (мускариновые) холинорецепторы. Первые хорошо связываются с никотиновой кислотой, а вторые — с мускарином — веществом, выделенным из грибов. Эти типы рецепторов по-разному распространены в организме. Так, на мышечных клетках располагаются Н-холинорецепторы, а на сердечной мышце и в нейронах головного мозга — М-холинорецепторы. Вещество, блокирующее один тип рецепторов, не влияет на работу рецепторов другого типа, поэтому кураре, блокирующее действие ацетилхолина на скелетные мышцы, не затрагивает работы сердечной мышцы и нервных клеток.
В настоящее время в медицине широко применяются синтетические аналоги яда кураре для обездвиживания больных во время сложных операций на внутренних органах.
Известно заболевание, связанное с хроническим нарушением нервно- мышечной передачи: Myasthenia gravis (миастения). Эта болезнь характеризуется слабостью и патологической утомляемостью скелетных мышц. Такие симптомы связаны с уменьшением числа постсинаптических рецепторов к ацетилхолину. Поэтому даже если высвобождается достаточное количество медиатора, амплитуда ПКП оказывается недостаточной для генерации ПД в мышце и ее сокращения. Недостаток рецепторов связан с аутоиммунной реакцией, специфично направленной именно против молекул рецептора ацетилхолина. У больных вырабатываются антитела против холинорецепторов, которые либо повышают скорость разрушения рецепторов, либо блокируют сами рецепторы. Лечение осуществляется при помощи ингибиторов холинэстеразы, которые увеличивают длительность действия ацетилхолина на рецепторы [2] .
- [1] Рисунок В. А. Дубинина (2013), печатается с разрешения автора.
- [2] 2 Физиология человека / под ред. Р. Шмидта, Г. Тевса.
Трофическая функция двигательных нервных волокон и их окончаний
Наряду с функцией передачи импульсов, вызывающих мышечные сокращения, нервные волокна и их окончания оказывают также трофическое воздействие на мышцу, т. е. участвуют в регуляции ее обмена веществ. Хорошо известно, что денервация мышцы, развивающаяся при дегенерации двигательного нерва, приводит к атрофии мышечных волокон, которая проявляется в том, что вначале уменьшается количество саркоплазмы, а затем и диаметр мышечных волокон; позднее происходит разрушение миофибрилл. Специальные исследования показали, что эта атрофия не является результатом лишь бездеятельности мышцы, потерявшей двигательную активность. Бездеятельность мышцы может быть вызвана и путем тендотомии, т. е. перерезки сухожилия. Однако, если сравнить мышцу после тендотомии и после денервации, можно убедиться, что в последнем случае в мышце развиваются качественно иные изменения ее свойств, не обнаруживающиеся при тендотомии. Наиболее ярко это проявляется в изменениях чувствительности мышцы к ацетилхолину. В нормальной и тендотомированной мышце к ацетилхолину чувствительна только постсинаптическая мембрана, в которой сосредоточены хемовозбудимые ионные каналы, снабженные холинорецепторами. Денервация приводит к тому, что такие же каналы появляются и во внесинаптических областях мышечного волокна. В результате чувствительность денервированной мышцы к ацетилхолину резко возрастает. Указанная гиперчувствительность к ацетилхолину не формируется, если при помощи определенных химических реагентов затормозить белковый синтез в мышечных волокнах. Реиннервация мышцы вследствие регенерации нервных волокон приводит к исчезновению холинорецептивных каналов области внепостсинаптической мембраны. Эти данные свидетельствуют о том, что нервные волокна регулируют синтез белков, образующих хемовозбудимые холинорецепторные каналы.
В денервированной мышце резко падает также активность ряда ферментов, в частности АТФ-азы, играющей важную роль в процессе освобождения энергии, заключенной в фосфатных связях АТФ. В то же время при денервации значительно усилены процессы распада белков. Это приводит к характерному для атрофии постепенному уменьшению массы мышечной ткани.
Важную роль в осуществлении трофических влияний нерва играет ацетилхолин, секретируемый нервными окончаниями как в покое, так особенно при возбуждении. Имеются основания считать, что ацетилхолин и продукты его расщепления холинэстеразой — холин и уксусная кислота — участвуют в обмене веществ мышцы, оказывая активирующее влияние на определенные ферментные системы. Так, при введении ацетилхолина в денервированную мышцу кролика резко увеличивается распад аденозинтрифосфата, креатинфосфата и гликогена во время тетануса, вызванного прямым электрическим раздражением этой мышцы.
Из нервных окончаний выделяются вещества, которые оказывают специфическое влияние на синтез белков мышечного волокна. Об этом свидетельствуют опыты с перекрестным сшиванием двигательных нервов, иннервирующих быстрые и медленные скелетные мышцы. При таком сшивании периферические отрезки нервов и их окончания в мышце дегенерируют, а по их путям в мышцу прорастают новые волокна из центральных отрезков нервов. Вскоре после того, как эти волокна образуют двигательные окончания, происходит отчетливая перестройка функциональных свойств мышц. Мышцы, которые ранее были быстрыми, теперь становятся медленными, а те, которые были медленными, становятся быстрыми. При такой перестройке изменяется активность АТФ-азы их сократительного белка миозина: в бывших быстрых мышцах она резко падает, а в медленных возрастает. Соответственно в первых скорость распада АТФ увеличивается, а во вторых — уменьшается. Изменяются также свойства ионных каналов клеточной мембраны.
Трофическое влияние на скелетную мышцу оказывают и волокна симпатической нервной системы, окончания которых высвобождают норадреналин.
1. Пресинаптические нарушения. Рассматриваются только избранные расстройства. Миастенический синдром Итона-Ламберта (Eaton-Lambert), имеющий более скрытые проявления, в настоящем разделе не обсуждается.
Ботулизм вызывается токсином, продуцируемым Clostridium botulinum. Это заболевание часто проявляется слабостью глазных мышц с последующей дизартрией, слабостью дыхательных мышц и мышц конечностей. Этот диагноз может быть подтвержден сведениями о приеме инфицированных пищевых продуктов. Нарастание ответов наблюдается при ритмической стимуляции нервов высокой частотой. Проводимость нервов обычно не изменена. Интоксикация чаще всего развивается у тех младенцев и маленьких детей, чей желудочно-кишечный тракт мог быть колонизирован С. botulinum,
Клещевой паралич является редким заболеванием, вызываемым Dermacentor andersonL Неврологические расстройства начинаются с затруднений ходьбы и нарушений равновесия, затем обнаруживаются восходящий вялый паралич и арефлексия. Могут быть заинтересованы глазные и бульбарные мышцы. ЭМГ выявляет снижение амплитуды мышечных потенциалов действия и нарастание ответов на стимуляцию высокой частоты, особенно в острой стадии. Может наблюдаться некоторое замедление проведения импульсов по двигательным и сенсорным нервам. Рекомендуется тщательный осмотр волосистой части головы и лобковой области для обнаружения возбудителя.

Отравление органическими фосфатами вызывает слабость преимущественно проксимальных отделов мускулатуры ног. Может наблюдаться быстрая утомляемость и слабость экстраокулярных и бульбарных мышц. Часто присутствуют мускари-новые симптомы (миоз, усиление саливации, генерализованные фасцикуляции). ЭМГ обычно нормальная. Ритмическая стимуляция нервов может выявить увеличение ответов при высокой частоте стимуляции.
Медикаментозная миастения. Некоторые медикаменты оказывают побочное действие на нервно-мышечную передачу. Слабость обычно возникает в мускулатуре проксимальных отделов конечностей в большей степени, чем в окулярных или бульбарных мышцах. Медикаментозно-обусловленная миастения может возникать при приеме канамицина, гентамицина, прокаинамида, примидона, гидантоинов.
2. Постсинаптические нарушения: миастения. У взрослых людей миастения с аутоиммунными нарушениями обычно начинается с непостоянной и асимметричной слабости экстраокулярных мышц и мышц век, а затем проявляется слабостью бульбарных мышц и мышц конечностей. Обычно клинические проявления одно- или двусторонние и включают птоз, дизартрию, дисфагию, слабость проксимальных отделов мускулатуры, дисфункцию дыхательных мышц. При повторении движений также наблюдается утомляемость мышц. Мышечный тонус, объем мышц, рефлексы, чувствительная сфера без отклонений. Диагноз основывается на результатах клинического обследования, результатах теста с эдрофонием (тензилоном), ЭМГ одиночных волокон, ритмической стимуляции и определения антител к рецепторам сывороточного ацетилхолина.
1. Полимиозит/дерматомиозит (ПМ/ДМ). Острые воспалительные миопатии обычно начинаются с симметричной слабости в проксимальной мускулатуре, включая мышцы плечевого и бедренного поясов. Тонус и объем мышц, рефлексы мышечного натяжения в норме. Чувствительные расстройства отсутствуют. Полимиозит обычно протекает без болей. Если типичные кожные поражения (эритематозная сыпь в периорбитальных областях, области лба или грудной клетки и особенно эритематозная сыпь над суставами и на разгибательных поверхностях) наблюдаются в сочетании со слабостью, следует рассматривать возможность развития дерматомиозита. Сывороточная креатинкиназа, альдолаза, лактатдегидрогеназа и аспартатаминотрансфераза часто повышены. СОЭ обычно высокая. СПНВ и амплитуды потенциалов нормальные. Игольчатая ЭМГ обнаруживает увеличение количества спонтанных потенциалов, таких как фибрилляции, положительные острые волны, высокочастотные разряды, малые полифазные непродолжительные низкоамплитудные потенциалы моторных единиц. Мышечная биопсия выявляет воспалительные изменения, распространяющиеся на перимизиум и эндомизиум, сочетающиеся с некрозом мышечных волокон и регенерацией мышечных волокон различной степени.
2. Острый инфекционный миозит. Вирусный миозит часто сопровождается миалгией и слабостью. В тяжелых случаях, как правило, наблюдается генерализованная слабость. Паразитарные инвазии и ВИЧ-инфекция могут сопровождаться слабостью проксимальной мускулатуры.
3. Острая токсическая миопатия. Острая алкогольная миопатия проявляется генерализованной симметричной слабостью. Гипермагниемия также вызывает острую генерализованную слабость, особенно у пациентов, страдающих алкоголизмом и получающих избыток магния с пищей. Амиодарон и L-триптофан могут вызывать острую миопатию. L-триптофан может быть причиной миалгии, слабости и эозинофилии.
4. Острый периодический паралич — это группа первичных мышечных заболеваний, которые связаны с нормальным (нормокалиемический вариант), повышенным (гиперкалиемический вариант) или низким уровнем калия (гипокалиемический вариант). Гиперкалиемический периодический паралич часто возникает на фоне напряжения или богатого углеводами питания после интенсивных нагрузок. Гиперкалиемический периодический паралич проявляется генерализованной слабостью при сохранности функций черепных нервов и дыхательных мышц. Во время приступов рефлексы мышечного натяжения отсутствуют. Диагноз можно заподозрить при наличии указаний на перемежающуюся слабость, вызываемую нагрузкой или богатой углеводами диетой, семейный анамнез, и отклонения содержания сывороточного калия в момент приступа. ЭМГ во время приступа нарушений может не выявить. Мышечная биопсия обнаруживает вакуолярную миопатию, особенно при получении препаратов в момент приступа. При подозрительных случаях с нормальным уровнем калия провокационные тесты могут вызывать развитие приступа.
5. Острая стероидная тетраплегическая миопатия часто наблюдается у пациентов, которым при астматическом статусе назначают высокие дозы стероидов и препараты, блокирующие нервно-мышечную передачу. После купирования астматического статуса пациенты испытывают слабость и нуждаются в механической вентиляции легких. ЭМГ обнаруживает признаки нейрогенных и миопатических нарушений. Проведение импульсов по нервным волокнам не страдает. Мышечная биопсия с электронной микроскопией обычно обнаруживает утрату миозиновых филаментов.
Диагноз строится на выявлении мышечной слабости и определении вовлечения верхнего или нижнего мотонейронов. После исключения поражения верхнего мотонейрона необходимо определение уровня поражения нижнего мотонейрона в соответствии с алгоритмом, представленным на рисунке. Часто требуются лабораторные исследования. Наиболее информативным тестом является ЭМГ. Для подтверждения/исключения ПМ/ДМ рекомендуется биопсия мышц. При невропатиях на фоне васкулита показана биопсия нервов.
Пациенты с острой слабостью нервно-мышечного типа нуждаются в госпитализации, особенно при острых параличах и подозрении на синдром Гийена-Барре. При вовлечении бульбарных и дыхательных мышц пациенты нуждаются в переводе в палату интенсивной терапии. Пациенты с другими нервно-мышечными заболеваниями могут обследоваться и лечиться в амбулаторных условиях. В большинстве случаев помощь может быть оказана врачом общей практики, однако для уточнения диагноза требуется консультация невролога.
Читайте также:


